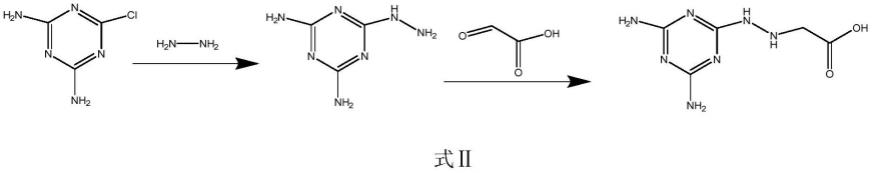
1.本发明涉及医药技术领域,尤其涉及前胡内酯酯类衍生物的制备方法及抑制乙酰胆碱酯酶活性应用。
背景技术:
2.香豆素类化合物是一种具有苯并α-吡喃酮母核的杂环化合物,广泛存在与多种药用植物中,具有抗癌、抗菌、抗病毒、抗炎、抗氧化等生物活性,受到药物研发人员的广泛关注。
3.前胡内脂,又称欧前胡素、白芷乙素,属于线型呋喃香豆素类化合物,其结构特点是具有一个呋喃环、六元内酯环及支链醚结构。前胡内酯主要存在于前胡、白芷、当归、蛇床、独活等药用植物中,具有多种生物活性,具有潜在的药用价值。
技术实现要素:
4.本发明提供了前胡内酯酯类衍生物的制备方法及抑制乙酰胆碱酯酶活性应用,以解决现有技术的上述问题。
5.本发明的方案是:
6.一种前胡内酯酯类衍生物的制备方法,包括下列步骤:
7.1)前胡内酯用1,4-二氧六环溶解,升温至60℃,在不断搅拌的情况下加入二氧化硒,升温至80℃继续反应,tlc跟踪监测,反应结束后过滤,除去反应液中的沉淀;
8.2)沉淀用二氯甲烷洗涤,合并有机溶剂后用无水硫酸钠干燥,用旋转蒸发器浓缩,薄层硅胶层析分离得前胡内酯醛;
9.3)称取前胡内酯醛加入圆底烧瓶中,用无水乙醇溶解,冰浴冷却至0℃,加入硼氢化钠,搅拌反应,待反应结束后加入稀盐酸终止反应,乙酸乙酯萃取,浓缩,柱层析分离的化合物;
10.4)称取步骤3)的化合物加入圆底烧瓶中,加入无水二氯甲烷溶解,然后加入称取的取代酸、dcc与dmap,tlc检测反应是否反应完全;然后过滤,浓缩,薄层硅胶层析分离得到前胡内酯酯类衍生物3a、3b、3c、3d、3e、3f、3g、3h、3i、3j、3k、3l、3m、3n与3o。
11.作为优选的技术方案,所述步骤1)中称取1mmol前胡内酯;加入1.2mmol的二氧化硒。
12.作为优选的技术方案,所述步骤3)中称取1mmol前胡内酯醛加入圆底烧瓶中;加入2mmol硼氢化钠。
13.作为优选的技术方案,所述步骤4)中称取步骤3)的1mmolde化合物加入圆底烧瓶中。
14.本发明还公布了一种前胡内酯酯类衍生物抑制乙酰胆碱酯酶活性应用。
15.本发明还公布了一种前胡内酯酯类衍生物对体外乙酰胆碱酯酶活性检测方法,包
括下列步骤:
16.1)取前胡内酯酯类衍生物样品加适量二甲亚砜溶解,然后加ph 7.4的0.1mol/l磷酸缓冲液溶液,配制成1mg/ml的待测溶液;
17.2)阳性对照采用他克林,空白对照采用磷酸缓冲液溶液;
18.3)测定中首先在96孔板上加入待测溶液样品10μl,再依次加入40μl的pb、20μl 2.5mmol/l的5,5-二流双硝基苯甲酸、10μl的电鳗乙酰胆碱酯酶,振荡混匀,37℃预孵10分钟,然后加入20μl 10mmol/l的碘化硫代乙酰胆碱,37℃反应10分钟,加入30ul1%的sds终止反应,酶标仪测定405nm吸收值并计算样品对乙酰胆碱酯酶的抑制活性。
19.作为优选的技术方案,所述步骤3)中计算所用公式如下:
20.抑制率=[(od空白对照-od反应本底)-(od待测样品-od反应本底)]/(od空白对照-od反应本底)
×
100%。
[0021]
本发明公开了一种前胡内酯酯类衍生物的制备方法,包括下列步骤:
[0022]
1)前胡内酯用1,4-二氧六环溶解,升温至60℃,在不断搅拌的情况下加入二氧化硒,升温至80℃继续反应,tlc跟踪监测,反应结束后过滤,除去反应液中的沉淀;2)沉淀用二氯甲烷洗涤,合并有机溶剂后用无水硫酸钠干燥,用旋转蒸发器浓缩,薄层硅胶层析分离得前胡内酯醛;3)称取前胡内酯醛加入圆底烧瓶中,用无水乙醇溶解,冰浴冷却至0℃,加入硼氢化钠,搅拌反应,待反应结束后加入稀盐酸终止反应,乙酸乙酯萃取,浓缩,柱层析分离的化合物;4)称取步骤3)的化合物加入圆底烧瓶中,加入无水二氯甲烷溶解,然后加入称取的取代酸、dcc与dmap,tlc检测反应是否反应完全;然后过滤,浓缩,薄层硅胶层析分离得到前胡内酯酯类衍生物3a、3b、3c、3d、3e、3f、3g、3h、3i、3j、3k、3l、3m、3n与3o。
[0023]
本发明的优点:
[0024]
本发明的产品对乙酰胆碱酯酶具有抑制作用,表现出对乙酰胆碱酯酶的抑制活性。
[0025]
具有多种生物活性,抗肿瘤、抗炎、抗菌、镇痛、抗乙酰胆碱酯酶活性等,具有潜在的药用价值。
附图说明
[0026]
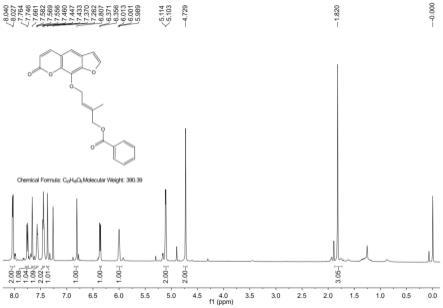
图1为本发明实施例1中前胡内酯酯类衍生物3a的氢谱图;
[0027]
图2为本发明实施例1中前胡内酯酯类衍生物3b的氢谱图;
[0028]
图3为本发明实施例1中前胡内酯酯类衍生物3c的氢谱图。
具体实施方式
[0029]
为了弥补以上不足,本发明提供了前胡内酯酯类衍生物的制备及抑制乙酰胆碱酯酶活性应用以解决上述背景技术中的问题。
[0030]
一种前胡内酯酯类衍生物的制备方法,包括下列步骤:
[0031]
1)前胡内酯用1,4-二氧六环溶解,升温至60℃,在不断搅拌的情况下加入二氧化硒,升温至80℃继续反应,tlc跟踪监测,反应结束后过滤,除去反应液中的沉淀;
[0032]
2)沉淀用二氯甲烷洗涤,合并有机溶剂后用无水硫酸钠干燥,用旋转蒸发器浓缩,薄层硅胶层析分离得前胡内酯醛;
[0033]
3)称取前胡内酯醛加入圆底烧瓶中,用无水乙醇溶解,冰浴冷却至0℃,加入硼氢化钠,搅拌反应,待反应结束后加入稀盐酸终止反应,乙酸乙酯萃取,浓缩,柱层析分离的化合物;
[0034]
4)称取步骤3)的化合物加入圆底烧瓶中,加入无水二氯甲烷溶解,然后加入称取的取代酸、dcc与dmap,tlc检测反应是否反应完全;然后过滤,浓缩,薄层硅胶层析分离得到前胡内酯酯类衍生物3a、3b、3c、3d、3e、3f、3g、3h、3i、3j、3k、3l、3m、3n与3o。
[0035]
所述步骤1)中称取1mmol前胡内酯;加入1.2mmol的二氧化硒。
[0036]
所述步骤3)中称取1mmol前胡内酯醛加入圆底烧瓶中;加入2mmol硼氢化钠。
[0037]
所述步骤4)中称取步骤3)的1mmolde化合物加入圆底烧瓶中。
[0038]
本发明还公布了一种前胡内酯酯类衍生物抑制乙酰胆碱酯酶活性应用。
[0039]
本发明还公布了一种前胡内酯酯类衍生物对体外乙酰胆碱酯酶活性检测方法,包括下列步骤:
[0040]
1)取前胡内酯酯类衍生物样品加适量二甲亚砜溶解,然后加ph 7.4的0.1mol/l磷酸缓冲液溶液,配制成1mg/ml的待测溶液;
[0041]
2)阳性对照采用他克林,空白对照采用磷酸缓冲液溶液;
[0042]
3)测定中首先在96孔板上加入待测溶液样品10μl,再依次加入40μl的pb、20μl 2.5mmol/l的5,5-二流双硝基苯甲酸、10μl的电鳗乙酰胆碱酯酶,振荡混匀,37℃预孵10分钟,然后加入20μl 10mmol/l的碘化硫代乙酰胆碱,37℃反应10分钟,加入30ul1%的sds终止反应,酶标仪测定405nm吸收值并计算样品对乙酰胆碱酯酶的抑制活性。
[0043]
所述步骤3)中计算所用公式如下:
[0044]
抑制率=[(od空白对照-od反应本底)-(od待测样品-od反应本底)]/(od空白对照-od反应本底)
×
100%。
[0045]
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例,进一步阐述本发明。
[0046]
实施例1
[0047]
一、产品:前胡内酯酯类衍生物,各衍生物理化性质详见以下内容;
[0048]
二、制备方法:
[0049]
以下为化合物2的化学合成路线:
[0050][0051]
将称好的1mmol前胡内酯用1,4-二氧六环溶解,升温至60℃,在不断搅拌的情况下加入1.2mmol二氧化硒,在升温至80℃继续反应,tlc跟踪监测,反应结束后过滤,除去反应液中的沉淀。沉淀用二氯甲烷洗涤。合并有机溶剂后用无水硫酸钠干燥,用旋转蒸发器浓缩,薄层硅胶层析分离得前胡内酯醛。将称好的前胡内酯醛(1mmol)加入圆底烧瓶中,用无水乙醇溶解,冰浴冷却至0℃,加入2mmol硼氢化钠,搅拌反应,待反应结束后加入稀盐酸终
止反应,乙酸乙酯萃取,浓缩,柱层析分离的化合物2。产率
[0052]
化合物2的理花化性质如下:
[0053]
1)、产率=69%,白色固体,熔点130-132℃;
[0054]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.76(d,j=9.6hz,1h,h-5),7.69(d,j=2.4hz,1h,h-2),7.37(s,1h,h-4),6.82(d,j=2.4hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),5.89(t,j=6.6hz,1h,h-2’),5.06(d,j=7.2hz,2h,h-1’),4.04(s,2h,h-4’),1.75(s,3h,h-5’),1.69(s,1h,oh);
[0055]
3)该化合物的esi-trap源质谱图ms m/z:309.2([m na]
,100)。
[0056]
以下为前胡内酯酯类衍生物3a~3o的合成路线:
[0057][0058]
将称好的化合物2(1mmol)加入圆底烧瓶中,加入无水二氯甲烷溶解,直接加入称好的取代酸、dcc(二环己基碳二亚胺)、dmap(4-二甲氨基吡啶),tlc检测反应是否反应完全。然后过滤,浓缩,薄层硅胶层析分离得前胡内酯酯类衍生物3a~3o。
[0059]
前胡内酯酯类衍生物3a的理化性质如下:
[0060]
1)、产率=58%,白色固体,熔点114-116℃;
[0061]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:8.02(d,j=7.8hz,2h,h-ar),7.74(d,j=10.8hz,1h,h-5),7.66(d,j=3.6hz,1h,h-2),7.55(t,j=7.8hz,1h,h-ar),7.43(t,j=7.8hz,2h,h-ar),7.37(s,1h,h-4),6.80(d,j=3.0hz,1h,h-3),6.35(d,j=9.0hz,1h,h-6),5.98(t,j=7.2hz,1h,h-2’),5.10(d,j=6.6hz,2h,h-1’),4.72(s,2h,h-4’),1.82(s,3h,h-5’);
[0062]
3)、该化合物的esi-trap源质谱图ms m/z:413.1([m na]
,100)。
[0063]
前胡内酯酯类衍生物3b的理化性质如下:
[0064]
1)、产率=64%,白色固体,熔点46-48℃;
[0065]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.77(d,j=9.6hz,1h,h-5),7.69(d,j=2.4hz,1h,h-2),7.37(s,1h,h-4),6.82(d,j=2.4hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),5.87(td,j=6.6,1.2hz,1h,h-2’),5.07(d,j=7.2hz,2h,h-1’),4.48(s,2h,h-4’),2.29(t,j=7.2hz,2h,ch2ch2ch3),1.73(s,3h,h-5’),1.61-1.68(m,2h,ch2ch2ch3),0.93(t,j=7.2hz,3h,ch2ch2ch3);
[0066]
3)、该化合物的esi-trap源质谱图ms m/z:379.2([m na]
,100)。
[0067]
前胡内酯酯类衍生物3c的理化性质如下:
[0068]
1)、产率=69%,白色固体,熔点83-85℃;
[0069]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.76(d,j=9.6hz,1h,h-5),7.69(d,j=2.4hz,1h,h-2),7.38(s,1h,h-4),6.82(d,j=2.4hz,1h,h-3),6.36(d,j=9.0hz,1h,h-6),5.88(td,j=6.6,1.2hz,1h,h-2’),5.06(d,j=7.8hz,2h,h-1’),4.48(s,2h,h-4’),2.33(q,j=7.8hz,2h,ch2ch3),1.73(s,3h,h-5’),1.12(t,j=7.8hz,3h,ch2ch3);
[0070]
3)、该化合物的esi-trap源质谱图ms m/z:365.1([m na]
,100)。
[0071]
前胡内酯酯类衍生物3d的理化性质如下:
[0072]
1)、产率=89%,白色固体,熔点88-90℃;
[0073]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:8.78(d,j=6.0hz,2h,h-ar),8.69(d,j=6.0hz,2h,h-ar),7.75(d,j=9.6hz,1h,h-5),7.67(d,j=2.4hz,1h,h-2),7.38(s,1h,h-4),6.81(d,j=2.4hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),5.99(td,j=6.6,1.2hz,1h,h-2’),5.10(d,j=6.6hz,2h,h-1’),4.76(s,2h,h-4’),1.83(s,3h,h-5’);
[0074]
3)、该化合物的esi-trap源质谱图ms m/z:414.2([m na]
,100)。
[0075]
前胡内酯酯类衍生物3e的理化性质如下:
[0076]
1)、产率=51%,白色固体,熔点126-128℃;
[0077]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:8.29(d,j=8.4hz,2h,h-ar),8.21(d,j=8.4hz,2h,h-ar),7.76(d,j=9.6hz,1h,h-5),7.68(s,1h,h-2),7.38(s,1h,h-4),6.82(s,1h,h-3),6.36(dd,j=9.6,2.4hz,1h,h-6),6.01(t,j=6.6hz,1h,h-2’),5.10(d,j=7.2hz,2h,h-1’),4.78(s,2h,h-4’),1.84(s,3h,h-5’);
[0078]
3)、该化合物的esi-trap源质谱图ms m/z:458.1([m na]
,100)。
[0079]
前胡内酯酯类衍生物3f的理化性质如下:
[0080]
1)、产率=53%,白色固体,熔点110-112℃;
[0081]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.98(d,j=8.0hz,2h,h-ar),7.74(d,j=9.6hz,1h,h-5),7.66(s,1h,h-2),7.37(s,1h,h-4),6.91(d,j=8.4hz,2h,h-ar),6.80(s,1h,h-3),6.35(d,j=9.6hz,1h,h-6),5.97(t,j=6.6hz,1h,h-2’),5.09(d,j=6.6hz,2h,h-1’),4.69(s,2h,h-4’),3.86(s,3h,och3),1.80(s,3h,h-5’);
[0082]
3)、该化合物的esi-trap源质谱图ms m/z:443.2([m na]
,100)。
[0083]
前胡内酯酯类衍生物3g的理化性质如下:
[0084]
1)、产率=52%,白色固体,熔点109-111℃;
[0085]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.96(d,j=8.4hz,2h,h-ar),7.76
(d,j=9.6hz,1h,h-5),7.66(d,j=2.4hz,1h,h-2),7.41(d,j=8.4hz,2h,h-ar),7.37(s,1h,h-4),6.81(d,j=1.8hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),5.97(td,j=7.2,1.8hz,1h,h-2),5.09(d,j=6.6hz,2h,h-1’),4.72(s,2h,h-4’),1.81(d,j=1.2hz,3h,h-5’);
[0086]
3)、该化合物的esi-trap源质谱图ms m/z:447.1([m na]
,100)。
[0087]
前胡内酯酯类衍生物3h的理化性质如下:
[0088]
1)、产率=60%,白色固体,熔点76-78℃;
[0089]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:8.04-8.06(m,2h,h-ar),7.75(d,j=9.6hz,1h,h-5),7.66(d,j=1.8hz,1h,h-2),7.37(s,1h,h-4),7.10(t,j=9.0hz,2h,h-ar),6.81(d,j=1.8hz,1h,h-3),6.36(d,j=9.0hz,1h,h-6),5.98(td,j=6.6,1.2hz,1h,h-2’),5.09(d,j=6.6hz,2h,h-1’),4.71(s,2h,h-4’),1.81(s,3h,h-5’);
[0090]
3)、该化合物的esi-trap源质谱图ms m/z:431.1([m na]
,100)。
[0091]
前胡内酯酯类衍生物3i的理化性质如下:
[0092]
1)、产率=58%,白色固体,熔点116-118℃;
[0093]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.76(d,j=9.6hz,1h,h-5),7.68(d,j=2.4hz,1h,h-2),7.43(d,j=8.4hz,2h,h-ar),7.38(s,1h,h-4),7.14(d,j=8.4hz,2h,h-ar),6.82(d,j=2.4hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),5.85(td,j=6.6,1.8hz,1h,h-2’),5.04(d,j=6.6hz,2h,h-1’),4.49(s,2h,h-4’),3.59(s,2h,ch2),1.69(s,3h,h-5’);
[0094]
3)、该化合物的esi-trap源质谱图ms m/z:405.1([m na]
,75),507.1([m na]
,100)。
[0095]
前胡内酯酯类衍生物3j的理化性质如下:
[0096]
1)、产率=86%,白色固体,熔点96-98℃;
[0097]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.98(d,j=8.4hz,1h,h-ar),7.84(d,j=8.4hz,1h,h-ar),7.77(dd,j=7.2,1.8hz,1h,h-ar),7.73(d,j=9.6hz,1h,h-5),7.65(d,j=1.8hz,1h,h-2),7.51-7.54(m,1h,h-ar),7.46-7.49(m,1h,h-ar),7.40-7.40(m,2h,h-ar),7.35(s,1h,h-4),6.80(d,j=1.8hz,1h,h-3),6.35(d,j=9.6hz,1h,h-6),5.82(td,j=6.6,1.2hz,1h,h-2’),5.00(d,j=7.2hz,2h,h-1’),4.48(s,2h,h-4’),4.09(s,2h,ch2),1.60(s,3h,h-5’);
[0098]
3)、该化合物的esi-trap源质谱图ms m/z:477.2([m na]
,100)。
[0099]
前胡内酯酯类衍生物3k的理化性质如下:
[0100]
1)、产率=58%,白色固体,熔点116-118℃;
[0101]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:9.20(s,1h,h-ar),8.78(dd,j=4.8,1.8hz,1h,h-ar),8.29(dt,j=7.8,1.8hz,1h,h-ar),7.75(d,j=9.6hz,1h,h-5),7.67(d,j=2.4hz,1h,h-2),7.40-7.42(m,1h,h-ar),7.38(s,1h,h-4),6.81(d,j=2.4hz,1h,h-3),6.35(d,j=9.6hz,1h,h-6),5.99(td,j=6.6,1.8hz,1h,h-2’),5.10(d,j=6.6hz,2h,h-1’),4.76(s,2h,h-4’),1.82(s,3h,h-5’);
[0102]
3)、该化合物的esi-trap源质谱图ms m/z:414.1([m na]
,100)。
[0103]
前胡内酯酯类衍生物3l的理化性质如下:
[0104]
1)、产率=76%,白色固体,熔点113-115℃;
[0105]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.76(d,j=9.6hz,1h,h-5),7.68(d,j=2.4hz,1h,h-2),7.38(s,1h,h-4),7.13(s,1h,h-ar),6.81(s,1h,h-3),6.46(s,1h,h-ar),6.36(d,j=9.6hz,1h,h-6),5.94(t,j=7.2hz,1h,h-2’),5.08(d,j=6.6hz,2h,h-1’),4.69(s,2h,h-4’),1.78(s,3h,h-5’);
[0106]
3)、该化合物的esi-trap源质谱图ms m/z:481.0([m na]
,100),483.0([m na]
,80)。
[0107]
前胡内酯酯类衍生物3m的理化性质如下:
[0108]
1)、产率=84%,白色固体,熔点88-90℃;
[0109]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:8.02(s,1h,h-ar),7.77(d,j=9.6hz,1h,h-5),7.68(d,j=2.2hz,1h,h-2),7.43(t,j=1.8hz,1h,h-ar),7.38(s,1h,h-4),6.82(d,j=2.2hz,1h,h-3),6.74(d,j=1.8hz,1h,h-ar),6.37(d,j=9.6hz,1h,h-6),5.95(td,j=6.8,1.4hz,1h,h-2’),5.09(d,j=6.8hz,2h,h-1’),4.66(s,2h,h-4’),1.78(d,j=1.3hz,3h,h-5’);
[0110]
3)、该化合物的esi-trap源质谱图ms m/z:403.3([m na]
,100)。
[0111]
前胡内酯酯类衍生物3n的理化性质如下:
[0112]
1)、产率=64%,白色固体,熔点109-111℃;
[0113]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:7.80(d,j=3.6hz,1h,h-ar),7.76(d,j=9.3hz,1h,h-5),7.67(s,1h,h-2),7.56(d,j=5.0hz,1h,h-ar),7.37(s,1h,h-4),7.11(t,j=4.4hz,1h,h-ar),6.81(s,1h,h-3),6.37(d,j=9.5hz,1h,h-6),5.98(t,j=7.2hz,1h,h-2’),5.10(d,j=6.8hz,2h,h-1’),4.70(s,2h,h-4’),1.80(s,3h,h-5’);
[0114]
3)、该化合物的esi-trap源质谱图ms m/z:419.2([m na]
,100)。
[0115]
前胡内酯酯类衍生物3o的理化性质如下:
[0116]
1)、产率=57%,白色固体,熔点65-67℃;
[0117]
2)、氢核磁共振图特征1h nmr(600mhz,cdcl3)δ:9.11(s,1h,nh),7.75(d,j=9.5hz,1h,h-5),7.70(d,j=8.1hz,1h,h-indole),7.66(d,j=2.1hz,1h,h-2),7.48(d,j=8.4hz,1h,h-indole),7.37(s,1h,h-4),7.34(t,j=7.8hz,1h,h-indole),7.25(s,1h,h-indole),7.16(t,j=7.5hz,1h,h-indole),6.80(d,j=2.2hz,1h,h-3),6.36(d,j=9.6hz,1h,h-6),6.03(t,j=7.1hz,1h,h-2’),5.09(d,j=7.0hz,2h,h-1’),4.74(s,2h,h-4’),1.80(s,3h,h-5’);
[0118]
3)、该化合物的esi-trap源质谱图ms m/z:452.1([m na]
,100)。
[0119]
实施例2、
[0120]
活性测定
[0121]
采用ellman法对ache体外抑制活性进行测试。将称好的样品加适量二甲亚砜溶解后加ph 7.4的0.1mol/l磷酸缓冲液(pbs)溶液,配制成1mg/ml的待测溶液。阳性对照采用他克林,空白对照采用磷酸缓冲液(pbs)溶液。测定时首先在96孔板上加入用待测样品10μl,再依次加入40μlpb、20μl 2.5mmol/l的5,5-二流双硝基苯甲酸(dtnb)、10μl的电鳗乙酰胆碱酯酶,振荡混匀,37℃预孵10分钟,然后加入20μl 10mmol/l的碘化硫代乙酰胆碱,37℃反应10分钟,加入30ul1%的sds终止反应,酶标仪测定405nm吸收值并计算样品对乙酰胆碱酯酶的抑制活性,计算公式如下:
[0122]
抑制率=[(od空白对照-od反应本底)-(od待测样品-od反应本底)]/(od空白对照-od反应本底)
×
100%。
[0123]
活性结果
[0124]
表1目标化合物对乙酰胆碱酯酶的抑制活性(1μmolm/l)
[0125][0126]a本测试平行3次,重复2次。
[0127]
以上显示和描述了本发明的基本原理、主要特征及本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。