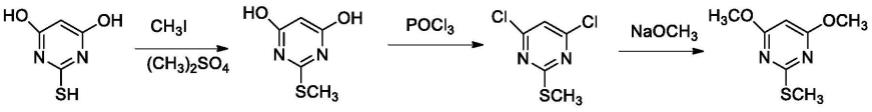
1.本发明涉及一种化合物、合成方法及用途,具体为一种基于胆固醇逆转运途径的调 血脂化合物、合成方法及用途。
背景技术:
2.动脉粥样硬化(atherosclerosis,as)导致的心脑血管疾病严重危害人类健康和生命, 死亡率超过其他大多数疾病。而血脂异常是诱发心血管疾病(cardiovascular diseases, cvd)的主要因素之一。现有的调血脂药主要针对降低低密度脂蛋白胆固醇(low densitylipid cholesterol,ldl-c)水平,其中他汀类药物使用最为广泛。药物治疗能减少发生心 血管事件的危险性,但仍有残留的心血管风险存在,并且调血脂药物存在的不同副作用 也不容忽视。因此,开发疗效显著、安全可靠的调血脂药物是药学工作者面临的重大挑 战。
3.胆固醇逆转运(reverse cholesterol transport,rct)是机体排出多余胆固醇的主要途 径,影响着as的发生发展。研究发现肝x受体α(liver x receptor α,lxrα)在胆固醇 从巨噬细胞流出过程中起关键作用。过氧化物酶体增殖物激活受体α(peroxisomeproliferator activated receptor α,pparα)在肝脏的脂质代谢中发挥重要作用,能够有效缓 解肝脏内脂质蓄积。针对rct信号通路上的pparα和lxrα设计双靶点激动活性的化合 物,从理论上推测,不仅能促进巨噬细胞内的胆固醇逆转运过程,还能有效缓解脂质在 肝脏内的蓄积,达到理想的降脂效果。在对脂肪酸和胆固醇代谢调节过程中,pparα和 lxrα这两个主要的核受体之间存在着密切联系,而且起着协同促进作用。因此,开发 pparα和lxrα双靶点激动剂,能起到促进多余胆固醇的排泄,降低肝脏内脂质的沉积, 发挥预防心血管疾病作用的同时,降低毒副作用。
4.现有的调血脂药主要针对降低低密度脂蛋白胆固醇(low density lipid cholesterol, ldl-c)水平,其中他汀类药物使用最为广泛。药物治疗能减少发生心血管事件的危险 性,但仍有残留的心血管风险存在,并且调血脂药物存在的不同副作用也不容忽视。因 此,开发疗效显著、安全可靠的调血脂药物是药学工作者面临的重大挑战。
技术实现要素:
5.发明目的:本发明的目的在于提供一种基于胆固醇逆转运途径的调血脂化合物,其 可同时靶向pparα与lxrα,发挥激动pparα与lxrα的双重作用。
6.技术方案:本发明所述的具有通式(i)的化合物或其可药用的盐:
[0007][0008]
其中,
[0009]
为碳数2~3的烷基链;
[0010]
为碳数1~2的烷基链,
[0011]
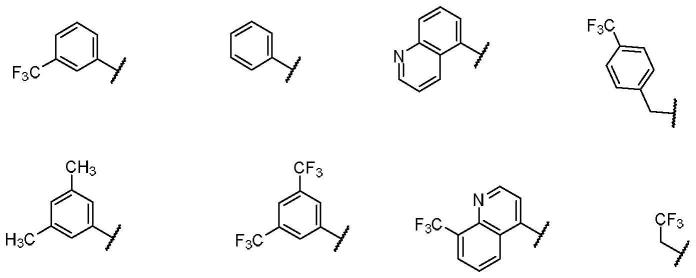
r1选自以下结构;
[0012][0013]
r2为-ch3、-ch3或-ch3;
[0014]
r3为-o(ch2)zch3、卤素、-h中的任一种,其中z为数字0~3中的任一个;
[0015]
r4为-ch2ch3或-h。
[0016]
m,p是指苯环上两个取代基是间位或对位。
[0017]
所述的化合物或其可药用的盐,所述卤素选自f、cl、br、i中的任一种。
[0018]
所述的化合物或其可药用的盐,所述化合物选自如下:
[0019]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a1)
[0020]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-甲苯基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a2)
[0021]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(苯基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a3)
[0022]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a4)
[0023]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a5)
[0024]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(4-(8-三氟甲基喹啉))氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a6)
[0025]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(2-三氟乙基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a7)
[0026]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(4-三氟甲基苯甲基)氨基]乙基]苯氧基]-2-甲基丙酸乙酯(a8)
[0027]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)-5-喹啉氨基]乙基]苯氧基]-2-甲基丙酸(a9)
[0028]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a10)
[0029]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-甲苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a11)
[0030]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a12)
[0031]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a13)
[0032]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a14)
[0033]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(2-三氟乙基)氨基]乙基]苯氧基]-2-甲基丙酸(a15)
[0034]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(4-三氟甲基苯甲基)氨基]乙基]苯氧基]-2-甲基丙酸(a16)
[0035]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸(b1)
[0036]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-丙酸(b2)
[0037]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]乙基]苯氧基]-丁酸(b3)
[0038]
2-[4-[1-[(2-(4-甲氧基苯氧基)乙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-2-甲基丙酸(b4)
[0039]
2-[4-[1-[(3-(4-氟苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-2-甲基丙酸(b5)
[0040]
2-[4-[1-[(3-苯氧基丙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-2-甲基丙酸(b6)
[0041]
2-[4-[1-[(3-(4-甲氧基苯氧基)丙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-2-甲基丙酸(b7)。
[0042][0043]
所述的化合物或其可药用的盐的合成方法,包括以下步骤:
[0044]
(1)化合物1与2在碱性条件下制得化合物3;
[0045]
(2)化合物3在酸性条件下脱去boc得到化合物4;
[0046]
(3)化合物4与5在酰胺缩合剂hatu的催化下生成酰胺缩合产物6;
[0047]
(4)化合物6在lialh4的催化下还原羰基生成仲胺化合物7;
[0048]
(5)化合物7与8在碱性条件下发生亲核取代反应生成化合物11;
[0049]
(6)化合物9与8在碱性条件下发生亲核取代反应生成化合物10;
[0050]
(7)化合物4与10在三乙酰氧基硼氢化钠作用下得到化合物11;
[0051]
(8)化合物11与12经过亲核取代或者碳氮偶联反应(buchwald-hartwig反应) 生成化合物13;
[0052]
(7)化合物13在在碱性条件下水解得到化合物14,反应式如下所示:
[0053][0054]
所述的化合物或其可药用的盐的合成方法,反应条件分别是:(a)nah,dmf,室温; (b)hcl,ch2cl2,室温;(c)4-hydroxyphenylacetic acid,dipea,hatu,dmf;(d)lialh4, ch2cl2或thf;(e)cs2co3,dmf或mecn;(f)sodium triacetoxyborohydride,thf,室 温;(g)chlorinated or brominated substratesubstrate,cs2co3,pd2(dba)3,x-phos, toluene,110℃;(h)koh,thf和h2o。
[0055]
药物组合物,所述的化合物或其可药用的盐、及药学上可接受的载体。
[0056]
所述的化合物或其可药用的盐或所述药物组合物在制备pparα与lxrα激动剂中 的用途。
[0057]
所述的化合物或其可药用的盐或所述药物组合物在制备胆固醇逆转运药物中的用 途。
[0058]
所述的化合物或其可药用的盐或所述药物组合物在制备调血脂药物中的用途。
[0059]
所述的化合物或其可药用的盐或所述药物组合物在制备治疗肝脏脂质蓄积药物中 的用途。
[0060]
所述的化合物或其可药用的盐或所述药物组合物在制备治疗脂肪肝药物中的用途。
[0061]
本发明的技术关键点在于:合成一类药物组合物,其含有治疗有效量的一种或多种 所述的具有通式(i)的调血脂化合物或其可药用的盐,及药学上可接受的载体。
[0062]
有益效果:本发明与现有技术相比,具有如下优点:本发明化合物在hepg2细胞及 raw264.7细胞中有一定的脂质蓄积抑制作用。本发明化合物b4在20μm的浓度下能够 有效的降低hepg2细胞raw264.7细胞中的总胆固醇水平,进一步说明化合物对肝脏中 的脂质蓄积有一定的缓解作用。
附图说明
[0063]
图1为化合物在成脂肪细胞中的脂质蓄积抑制能力测试;
[0064]
图2为hepg2细胞油红染色半定量测试;
[0065]
图3为hepg2细胞油红o染色成像(
×
20);(a)control组;(b)oa酯化模 型组;(c)b4给药组;(d)t0901317给药组;(e)fenofibrate acid给药组;
[0066]
图4为raw264.7细胞油红染色半定量测试;
[0067]
图5为raw264.7细胞油红o染色成像(
×
20);(a)control组;(b)oa酯化 模型组;(c)t0901317给药组;(d)b4给药组;(e)fenofibrate acid给药组;
[0068]
图6为细胞内总胆固醇测定,其中(a)为hepg2细胞内总胆固醇(tc)测定; (b)为raw264.7细胞内总胆固醇(tc)测定。
具体实施方式
[0069]
实施例1
[0070]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸 乙酯(a1)的合成
[0071]
合成路线:
316.1[m h]
.
[0079]
步骤4:
[0080]
将lialh4(1.68g,44.27mmol)加入dcm(5ml)中,0℃下缓慢将化合物18(3.36g,11.16mmol)的dcm(10ml)溶液。滴加完毕后反应液于38℃回流反应,tlc检测直至反应完成。后处理:用冰水在0℃下淬灭反应,过滤除去不溶物,用dcm(5ml
×
2)洗涤滤饼,滤液用dcm(30ml
×
3)萃取,合并有机相,无水na2so4干燥后减压浓缩,经柱层析后得化合物19(1.44g,产率43%)。1hnmr(300mhz,dmso-d6)δ9.36(s,1h),7.04(d,j=8.0hz,2h),6.86(s,4h),6.72(d,j=8.0hz,2h),3.98(t,j=6.1hz,2h),3.69(s,3h),3.02(p,j=5.0,4.2hz,4h),2.83(dd,j=10.3,6.0hz,2h),2.11-1.95(m,2h).msesim/z302.2[m h]
.
[0081]
步骤5:
[0082]
将化合物19(0.34g,1.13mmol)、2-溴-2-甲基丙酸乙酯(0.28g,1.44mmol)、cs2co3(0.74g,2.27mmol)加入无水dmf(5ml)中,室温下反应搅拌过夜。后处理:用水淬灭反应,dcm(10ml
×
3)萃取,合并有机相,无水na2so4干燥后减压浓缩,经柱层析后得化合物20(0.27g,产率57%)。1hnmr(300mhz,methanol-d4)δ7.15(d,j=8.5hz,2h),6.81(s,4h),6.78(d,j=8.5hz,2h),4.18(q,j=7.1hz,2h),3.99(t,j=5.8hz,2h),3.71(s,3h),3.14-3.06(m,4h),2.89(t,j=6hz,2h),2.08(p,j=6.1hz,2h),1.52(s,6h),1.21(t,j=7.1hz,3h).msesim/z416.2[m h]
.
[0083]
步骤6:
[0084]
将化合物20(1g,2.41mmol)、3-碘三氟甲苯(1.32g,4.85mmol)加入甲苯(6ml)中,随后加入cs2co3(1.56g,4.79mmol)、x-phos(58mg,0.12mmol)、pd2(dba)3(110mg,0.12μmol),n2置换。反应液110℃反应过夜。后处理:加水淬灭反应,ea(5ml
×
3)萃取,无水na2so4干燥后减压浓缩,经柱层析后得橙黄色油状化合物a1(0.44g,产率33%)。1hnmr(300mhz,chloroform-d)δ7.30(t,j=8.0hz,1h),7.06(d,j=8.5hz,2h),6.96-6.87(m,3h),6.85(s,4h),6.81(d,j=8.4hz,2h),4.25(q,j=7.1hz,2h),3.92(t,j=5.7hz,2h),3.78(s,3h),3.55(t,j=7.5hz,2h),3.46(t,j=7.0hz,2h),2.81(t,j=7.5hz,2h),1.98(p,j=6.2hz,2h),1.60(s,6h),1.27(t,j=7.1hz,3h).
13
cnmr(101mhz,methanol-d4)δ175.70,155.37,155.28,154.31,149.33,134.79,132.46(q,j=31.3hz,1c),130.91,130.61,126.09(q,j=272.7hz,1c),120.82,116.43,116.27,115.68,112.74(q,j=4.0hz,1c),108.93(q,j=4.0hz,1c),80.36,66.58,62.50,56.08,53.92,48.76,33.38,28.05,25.71,14.37.hrms(esi)m/zcalcdforc
31h36
f3no5[m h]
560.2618,found560.2615.
[0085]
实施例2
[0086]
2-[4-[2-[(3-(4-甲氧基苯氧基)丙基)(3-三氟甲基苯基)氨基]乙基]苯氧基]-2-甲基丙酸(a10)的合成
[0087][0088]
步骤1:
[0089]
将化合物a1(0.28g,0.5mmol)溶于3mlthf以及3ml水的混合溶液中,加入koh(0.14g,2.5mmol)至反应液中,室温反应,tlc监测至反应结束。后处理:加入稀盐酸调ph至中性,减压浓缩至无旋出液,剩余溶液用ea(6ml
×
3)萃取,合并有机相,无水na2so4干燥后减压浓缩,柱层析后得化合物a10(0.13g,产率48%)。化合物a10为淡黄色油状物。1hnmr(300mhz,methanol-d4)δ7.15(t,j=7.9hz,1h),6.91(d,j=8.1hz,2h),6.78(d,j=11.8hz,2h),6.71(d,j=9.6hz,7h),3.72(t,j=5.6hz,2h),3.58(s,3h),3.38(t,j=7.4hz,2h),3.28(t,j=7.1hz,2h),2.63(t,j=7.3hz,2h),1.79-1.66(m,2h),1.40(s,6h).
13
cnmr(101mhz,methanol-d4)δ177.89,155.36,155.27,154.30,149.33,134.77,132.46(q,j=31.3hz,1c),130.90,130.56,126.08(q,j=272.7hz,1c),121.09,116.44,116.27,115.68,112.76(q,j=4.0hz,1c),108.94(q,j=4.0hz,1c),80.24,66.59,56.08,53.94,33.38,28.06,25.71.hrms(esi)m/zcalcdforc
29h32
f3no5[m h]
532.2305,found532.2303.
[0090]
实施例3
[0091]
a2的合成
[0092][0093]
参照实施例1的合成方法,将3-碘三氟甲苯替换成间溴甲苯,其他条件不变。1hnmr(300mhz,methanol-d4)δ7.05-6.97(m,3h),6.81(s,4h),6.76-6.70(m,2h),6.52(d,j=6.5hz,2h),6.41(d,j=7.4hz,1h),4.18(q,j=7.1hz,2h),3.85(t,j=5.7hz,2h),3.71(s,3h),3.45(t,j=7.4hz,2h),3.34(t,j=6.9hz,2h),2.74(t,j=7.3hz,2h),2.19(s,3h),1.86(p,j=6.1hz,2h),1.50(s,6h),1.21(t,j=7.1hz,3h).
[0094]
实施例4
[0095]
a3的合成
[0096]
[0097]
参照实施例1的合成方法,将3-碘三氟甲苯替换成溴苯,其他条件不变。1h nmr (300mhz,methanol-d4)δ7.17-7.07(m,2h),7.05-6.97(m,2h),6.80(s,4h),6.76-6.67 (m,4h),6.58(t,j=7.2hz,1h),4.17(q,j=7.1hz,2h),3.85(t,j=5.7hz,2h),3.70(s, 3h),3.45(t,j=7.4hz,2h),3.35(t,j=7.0hz,2h),2.74(t,j=7.4hz,2h),1.87(p,j=6.1 hz,2h),1.50(s,6h),1.20(t,j=7.1hz,3h).
[0098]
实施例5
[0099]
a4的合成
[0100][0101]
参照实施例1的合成方法,将3-碘三氟甲苯替换成3,5-二甲基溴苯,其他条件不变。 1
h nmr(300mhz,chloroform-d)δ7.07(d,j=8.5hz,2h),6.85(s,4h),6.81(d,j=8.5 hz,2h),6.39(d,j=7.3hz,3h),4.26(q,j=7.1hz,2h),3.94(t,j=5.7hz,2h),3.79(s, 3h),3.50(dd,j=8.9,6.5hz,2h),3.43(t,j=6.9hz,2h),2.86-2.76(m,2h),2.27(s,6h), 1.99(p,j=6.2hz,2h),1.60(s,6h),1.27(d,j=7.1hz,3h).
[0102]
实施例6
[0103]
a5的合成
[0104][0105]
参照实施例1的合成方法,将3-碘三氟甲苯替换成3,5-双三氟甲基溴苯,其他条件 不变。1h nmr(400mhz,dmso-d6)δ7.11(d,j=8.5hz,4h),7.06(s,1h),6.85(s,4h), 6.73-6.68(m,2h),4.14(q,j=7.1hz,2h),3.92(t,j=5.7hz,2h),3.68(s,3h),3.62(t,j =7.4hz,2h),3.50(t,j=7.1hz,2h),2.75(t,j=7.3hz,2h),1.89(t,j=6.9hz,2h),1.46 (s,6h),1.15(t,j=7.1hz,3h).
[0106]
实施例7
[0107]
a6的合成
[0108][0109]
参照实施例1的合成方法,将3-碘三氟甲苯替换成4-溴-8-三氟甲基喹啉,其他条 件不变。1h nmr(300mhz,methanol-d4)δ8.56(d,j=5.3hz,1h),7.99(dd,j=22.1,7.9 hz,2h),7.37(t,j=7.8hz,1h),7.04(d,j=5.1hz,1h),6.90(d,j=8.1hz,2h),6.70(m, 2h),
3.83(t,j=6.1hz,2h),3.63(s,3h),3.35(t,j=6.9hz,2h),3.30-3.22(m,2h),2.72
‑ꢀ
2.63(m,2h),1.82(p,j=6.5hz,2h),1.43(s,6h),1.10(t,j=7.1hz,3h).
[0122]
实施例11
[0123]
a11的合成
[0124][0125]
参照实施例2的合成方法,由a3水解得到。1h nmr(300mhz,chloroform-d)δ7.16
ꢀ‑
7.10(m,1h),7.10-7.05(m,2h),6.91-6.85(m,2h),6.84(s,4h),6.56(q,j=7.5,6.7hz, 3h),3.92(t,j=5.7hz,2h),3.78(s,3h),3.49(t,j=7.7hz,2h),3.43(t,j=7.0hz,2h), 2.84-2.77(m,2h),2.30(s,3h),2.02-1.91(m,2h),1.59(s,6h).
[0126]
实施例12
[0127]
a12的合成
[0128][0129]
参照实施例2的合成方法,由a4水解得到。1h nmr(300mhz,methanol-d4)δ6.99 (dd,j=8.5,7.0hz,2h),6.83(d,j=8.3hz,2h),6.67(d,j=8.5hz,2h),6.62(s,4h),6.56 (d,j=8.3hz,2h),6.45(t,j=7.2hz,1h),3.63(t,j=5.7hz,2h),3.51(s,3h),3.25(t,j= 7.5hz,2h),3.17(t,j=7.0hz,2h),2.54(t,j=7.4hz,2h),1.67(p,j=6.2hz,2h),1.35(s, 6h).
[0130]
实施例13
[0131]
a13的合成
[0132][0133]
参照实施例2的合成方法,由a5水解得到。1h nmr(300mhz,methanol-d4)δ6.86 (d,j=8.6hz,2h),6.69(d,j=8.5hz,2h),6.65(s,4h),6.26(s,2h),6.18(s,1h),3.65(t,j =5.7hz,2h),3.54(s,3h),3.27(t,j=7.5hz,2h),3.24-3.16(m,2h),2.56(t,j=7.4hz, 2h),2.04(s,6h),1.69(p,j=6.1hz,2h),1.39(s,6h).
[0134]
实施例14
[0135]
a14的合成1h nmr(400mhz,methanol-d4)δ7.06(t,j=7.8hz,1h),6.99(s,2h),6.94(s,1h),6.76
‑ꢀ
6.69(m,5h),6.64(d,j=8.0hz,2h),3.78(t,j=5.4hz,2h),3.61(s,3h),3.53(t,j=7.0 hz,2h),3.38(t,j=7.1hz,2h),2.71(t,j=6.9hz,2h),1.81(p,j=5.9hz,2h),1.37(s, 6h).
[0150]
实施例18
[0151]
b2的合成
[0152][0153]
参照实施例14的合成方法,将2-溴-2-甲基丙酸乙酯替换成2-溴丙酸乙酯,其他条 件不变。1h nmr(400mhz,dmso-d6)δ7.14(d,j=5.4hz,3h),7.10(d,j=11.2hz,2h),6.86(s,4h),6.79(d,j=8.1hz,2h),4.71(q,j=6.7hz,1h),3.92(t,j=5.7hz,2h),3.69 (s,3h),3.60(t,j=7.5hz,2h),3.53(t,j=7.3hz,2h),2.74(t,j=7.5hz,2h),1.90(t,j= 6.7hz,2h),1.46(d,j=6.7hz,3h).
[0154]
实施例19
[0155]
b3的合成
[0156][0157]
参照实施例1的合成方法,将2-溴-2-甲基丙酸乙酯替换成2-溴丁酸乙酯,其他条 件不变。1h nmr(400mhz,methanol-d4)δ7.10(d,j=1.4hz,2h),7.08-7.04(m,2h), 7.03(s,1h),6.85-6.78(m,6h),4.49(dd,j=7.1,5.0hz,1h),3.88(t,j=5.5hz,2h),3.71 (s,3h),3.59(t,j=7.2hz,2h),3.49(t,j=7.1hz,2h),2.78(t,j=7.2hz,2h),2.00-1.84 (m,4h),1.05(t,j=7.4hz,3h).
[0158]
实施例20
[0159]
2-[4-[2-[(2-(4-甲氧基苯氧基)乙基)(3,5-二三氟甲基苯基)氨基]甲基]苯氧基]-2-甲基 丙酸(b4)的合成
[0160]
合成路线:
干燥,减压浓缩,纯化后得化合物26(0.64g,产率39%)。1hnmr(300mhz,methanol-d4)δ7.30-7.23(m,2h),6.88-6.81(m,6h),4.23(q,j=7.1hz,2h),4.04(t,j=5.4hz,2h),3.78(s,2h),3.76(s,3h),2.93(t,j=5.4hz,2h),1.58(s,6h),1.26(t,j=7.1hz,3h).
[0170]
步骤5
[0171]
将化合物26(0.33g,0.79mmol)、3,5-二三氟甲基溴苯(0.46g,1.59mmol)、cs2co3(0.52g,1.59mmol)、x-phos(19mg,0.04mmol)、pd2(dba)3(36mg,0.04mmol)加入3ml甲苯中,110℃反应过夜。后处理:加3ml水后用ea(5ml
×
3)萃取,合并有机相,无水na2so4干燥,减压浓缩,柱层析纯化,得化合物27(0.13g,产率27%)。1hnmr(300mhz,methanol-d4)δ7.89-7.82(m,1h),7.18-7.08(m,3h),6.98-6.93(m,1h),6.82(d,j=2.1hz,4h),6.81-6.77(m,2h),4.74(s,2h),4.28-4.21(m,2h),4.19-4.14(m,2h),3.98(t,j=5.1hz,2h),3.75(s,3h),1.55(s,6h),1.23(t,j=7.1hz,3h).msesim/z622.20[m na]
.
[0172]
步骤6:
[0173]
将化合物27(0.15g,0.24mmol)溶于3mlthf以及3ml水的混合溶液中,加入koh(0.13g,2.4mmol)至反应液中,室温反应,tlc监测至反应结束。后处理:加入稀盐酸调ph至中性,减压浓缩至无旋出液,剩余溶液用ea(6ml
×
3)萃取,合并有机相,无水na2so4干燥后减压浓缩,化合物b4为淡黄色油状物。1hnmr(400mhz,methanol-d4)δ7.22(d,j=1.4hz,2h),7.12-7.06(m,3h),6.85(d,j=8.6hz,2h),6.82-6.76(m,4h),4.69(s,2h),4.15(t,j=5.1hz,2h),3.92(t,j=5.1hz,2h),3.71(s,3h),1.49(s,6h).
13
cnmr(101mhz,methanol-d4)δ179.92,156.22,155.55,154.04,150.93,133.11(q,j=32.3hz,2c),131.81,128.27,125.20(q,j=272.7hz,2c),121.02,116.30,115.68,113.24,109.47(m,1c),80.85,67.87,56.03,55.07,52.15,25.86.hrms(esi)m/zcalcdforc
28h27
f6no5[m na]
594.1686,found594.1691.
[0174]
实施例21
[0175]
b5的合成
[0176][0177]
参照实施例20的合成方法,将对羟基苯甲醚替换成4-氟苯酚,将n-boc-2-氨基乙基溴替换成3-(boc-氨基)丙基溴,其他条件不变。1hnmr(400mhz,methanol-d4)δ7.07(d,j=1.4hz,2h),7.02(d,j=8.6hz,2h),6.97(s,1h),6.91-6.85(m,2h),6.81-6.76(m,4h),4.51(s,2h),3.90(t,j=5.6hz,2h),3.65(t,j=7.1hz,2h),2.00(dt,j=12.7,5.7hz,2h),1.44(s,6h).
[0178]
实施例22
[0179]
b6的合成
[0180][0181]
参照实施例20的合成方法,将对羟基苯甲醚替换成苯酚,将n-boc-2-氨基乙基溴 替换成3-(boc-氨基)丙基溴,其他条件不变。1h nmr(400mhz,methanol-d4)δ7.22
‑ꢀ
7.16(m,2h),7.10(d,j=1.5hz,2h),7.05(d,j=8.6hz,2h),6.99(s,1h),6.87-6.83(m, 3h),6.83-6.79(m,2h),4.55(s,2h),3.97(t,j=5.6hz,2h),3.70(t,j=7.2hz,2h),2.04 (dt,j=12.2,5.7hz,2h),1.47(s,6h).
[0182]
实施例23
[0183]
b7的合成
[0184][0185]
参照实施例20的合成方法,将n-boc-2-氨基乙基溴替换成3-(boc-氨基)丙基溴,其 他条件不变。1h nmr(400mhz,methanol-d4)δ7.15(s,2h),7.10(d,j=8.6hz,2h),7.05 (s,1h),6.87(dd,j=8.4,1.5hz,2h),6.82(d,j=2.0hz,4h),4.60(s,2h),3.97(d,j=5.1 hz,2h),3.76-3.69(m,5h),2.06(p,j=6.2hz,2h),1.52(s,6h).
[0186]
实施例24
[0187]
活性测试
[0188]
以下活性测试所用到的仪器来源。
[0189]
表1仪器来源
[0190]
仪器名称生产厂家仪器名称生产厂家万分之一天平上海上平仪器有限公司震荡仪常州国华电器有限公司co2培养箱esco离心机湖南湘仪实验室仪器开发有安全柜苏州净化设备有限公司脱色摇床servicebio倒置显微镜尼康公司电泳仪北京六一仪器厂酶标仪北京普朗新技术有限公暗匣广东粤华医疗器械厂有限公高压蒸汽灭菌锅上海博讯实业有限公司扫描仪epson涡旋机上海沪西分析仪器厂有
ꢀꢀ
[0191]
(一)成脂肪细胞油红染色实验
[0192]
1、实验方法
[0193]
(1)油红染色步骤
[0194]
培养好的细胞吸弃原有培养基,用pbs清洗一遍(5min),加入4%甲醛固定细胞 20-30min,pbs清洗两次,每次5min。油红染色工作液孵育样本30min,pbs清洗2 次,每次
5min。每孔加入150μl异丙醇溶液,置于振荡器上低速振荡20min后,于 492nm测定吸光值。阳性药t0901317、fenofibrate acid作为对照。脂质蓄积抑制率(%) 按下式计算:
[0195][0196]
(2)细胞成像
[0197]
油红染色工作液染色经pbs清洗后,加入甘油:pbs=1:1溶液,封片保存,镜下 观察。
[0198]
(3)实验结果
[0199]
成脂肪细胞株油红染色实验结果见图1。研究结果表明,本发明化合物b4在成脂 肪细胞中脂质抑制活性最好,对其做进一步研究。
[0200]
(二)hepg2以及raw264.7细胞株油红染色实验
[0201]
1、实验方法
[0202]
(1)hepg2细胞酯化模型的建立
[0203]
选择处于对数生长期的hepg2细胞,接种于96孔细胞培养板中,细胞密度为8000 个/孔。5%co2、37℃培养24h后,弃去原细胞培养液,换成dmem完全培养基和终 浓度为0.5mm油酸(oa),在5%co2、37℃培养箱中共同孵育24h,使脂质在hepg2 细胞中沉积。
[0204]
(2)raw264.7细胞酯化模型的建立
[0205]
选择处于对数生长期的raw264.7细胞,接种于96孔细胞培养板中,细胞密度为 5000个/孔。5%co2、37℃培养24h后,弃去原细胞培养液,换成dmem完全培养基 和终浓度为100μg/ml氧化型低密度脂蛋白(ox-ldl),在5%co2,37℃培养箱中共同孵 育24h,使脂质在raw264.7细胞中沉积。
[0206]
(3)实验分组
[0207]
实验共分为3组(每组设6个复孔),分别为
①
空白对照组:不做其他处理,将 hepg2细胞用dmem完全培养基培养24h后换新dmem完全培养基继续培养24h;
ꢀ②
细胞酯化模型组:在细胞液中加入终浓度为0.5mm的oa或者100μg/ml ox-ldl, 共同孵育24h后更换不含酯化试剂的培养基继续培养24h;
③
给药组:细胞制成酯化 模型后,加入含不同药物的培养基继续孵育24h。
[0208]
(4)油红染色步骤
[0209]
培养好的细胞吸弃原有培养基,用pbs清洗一遍(5min),加入4%甲醛固定细胞 20-30min,pbs清洗两次,每次5min。油红染色工作液孵育样本30min,pbs清洗2 次,每次5min。每孔加入150μl异丙醇溶液,置于振荡器上低速振荡20min后,于492 nm测定吸光值。脂质蓄积抑制率(%)按下式计算:
[0210][0211]
(5)细胞成像
[0212]
油红染色工作液染色经pbs清洗后,加入甘油:pbs=1:1溶液,封片保存,镜下 观察。
[0213]
2、实验结果
[0214]
hepg2以及raw264.7细胞株油红染色实验结果见图2-5。研究结果表明,本发明 化
合物b4在hepg2细胞及raw264.7细胞中有一定的脂质蓄积抑制作用。
[0215]
(三)、细胞内总胆固醇(tc)测定
[0216]
1、实验方法
[0217]
将对数生长期的细胞制备为细胞悬液(细胞悬液浓度约为1
×
105个细胞/ml)接种 于25mm直径培养皿中。在5%co2、37℃的细胞培养箱培养12h后给药,实验分组
ꢀ①
空白对照组:不做其他处理,将细胞用dmem完全培养基培养24h后换新dmem 完全培养基继续培养,间隔24h后更换新的dmem完全培养基;
②
细胞酯化模型组: 在细胞液中加入终浓度为0.5mm的oa(hepg2细胞)或100μg/ml ox-ldl(raw264.7 细胞),共同孵育24h后更换不含酯化试剂的培养基继续培养24h;
③
给药组:细胞 制成酯化模型后,加入含药物的培养基继续孵育24h。吸弃原培养基并用pbs清洗2 遍,而后用细胞刮将细胞刮下,收集至离心管中,离心后弃去上清液并用玻璃匀浆管将 细胞破碎3-4min,用bca法进行蛋白定量后,使用总胆固醇检测试剂盒对细胞内的总 胆固醇进行定量检测。
[0218]
2、实验结果
[0219]
结果如图6所示,b4在20μm的浓度下能够有效的降低hepg2细胞、raw264.7 细胞中的总胆固醇水平,进一步说明化合物对肝脏中的脂质蓄积有一定的缓解作用,对 脂肪肝的治疗有良好的应用前景。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。