hoxa5的fish检测探针及其试剂盒和应用
技术领域
1.本发明属于生物分子技术领域,涉及hoxa5的fish检测探针及其试剂盒和应用。
背景技术:
2.胶质母细胞瘤是中枢神经系统最常见的肿瘤,其发展迅速,预后较差。而高通量分析技术加深了我们对胶质母细胞瘤遗传和表观遗传学特征的理解,其中7号染色体的扩增是一部分胶质母细胞瘤的早期事件,导致肿瘤的快速进展和患者较差的预后。然而,部分7号染色体扩增患者的预后也存在较大差异,提示7号染色体上不同基因扩增差异可能导致患者的不同预后。hoxa5基因位于7号染色体上,作为一种转录因子,在胚胎发生过程中在肺和脊髓中表达,缺乏hoxa5表达的小鼠表现出严重的肺形态学缺陷。近年来的研究发现hoxa5在肿瘤侵袭、增殖、诱导凋亡、干性调控中发挥重要作用。然而,hoxa5基因本身的扩增情况及其临床病理学意义目前尚不清楚。
技术实现要素:
3.有鉴于此,本发明的目的在于提供一种hoxa5的fish检测探针及其试剂盒和应用。
4.为达到上述目的,本发明提供如下技术方案:
5.1.检测hoxa5的试剂在制备胶质母细胞瘤诊断和/或预后的试剂和/试剂盒中的应用。
6.2.hoxa5的fish检测探针用于制备胶质母细胞瘤诊断和/或预后的试剂和/试剂盒中的应用。
7.进一步,fish检测探针的序列如seq id no.1所示。
8.4.一种胶质母细胞瘤诊断和/或预后的试剂盒,所述试剂盒包括检测hoxa5与7号染色体的荧光探针。
9.进一步,所述试剂盒的使用方法为,分别检测hoxa5和7号染色体探针信号,再计算hoxa5和7号染色体探针信号比例。
10.本发明的有益效果在于:本发明通过荧光原位杂交方法对胶质母细胞瘤样本中hoxa5基因扩增情况进行了检测,并制定了hoxa5基因扩增的评判标准及流程,通过考察hoxa5与7号染色体探针信号比例的不同情况,显示hoxa5扩增具有异质性,本发明提供的fish探针序列特异性好,信号强、背景低。在hoxa5基因荧光原位杂交结果显示hoxa5基因扩增与胶质瘤级别可能有相关性的基础上,进一步通过不同胶质瘤数据库对hoxa5基因扩增情况进行了验证,充分证明hoxa5基因扩增导致胶质瘤患者生存期缩短。所以本发明提供的hoxa5基因的fish探针为临床检测hoxa5基因扩增有很好的应用性,可用于胶质母细胞瘤的临床诊断和预后判断。进一步通过预后给出适合延长患者生存期的方法,提高患者的生存质量。
附图说明
11.为了使本发明的目的、技术方案和有益效果更加清楚,本发明提供如下附图进行说明:
12.图1为荧光原位杂交及二代测序检测胶质瘤样本中hoxa5基因扩增结果;
13.图2为数据库验证hoxa5基因扩增与胶质瘤分级分型的关系。
14.图3为胶质瘤样本分析及数据库验证hoxa5基因扩增与患者预后的关系的实验结果。
15.图4为研究hoxa5基因扩增与表达的关系的实验结果。
16.图5为验证hoxa5表达与胶质瘤级别及患者预后的关系。
17.图6为本发明fish探针实验得到的荧光图。
具体实施方式
18.下面将结合附图,对本发明的优选实施例进行详细的描述。实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。
19.实施例1探针设计
20.根据hoxa5的基因序列进行fish探针的设计筛选,本发明所设计的核酸探针的特异性好,能够保证原位杂交的准确性。
21.hoxa5位于7号染色体7p15.2;hoxa5在染色体位置:27,141,052
‑
27,143,681;hoxa5探针dna位置:27,108,196
‑
27,262,321。
22.本发明在hoxa5探针标记的是红色荧光,7号染色体标记的是绿色荧光,原位杂交荧光染示意图结果如图6所示。
23.fish探针是通过荧光标记核苷酸(荧光du)置换探针dna核苷酸(t),nick缺口平移标记法标记。
24.(1)荧光原位杂交相关试剂及溶液
[0025]1×
edta修复液:将50
×
edta修复液与双蒸水按照1:49的比例配置,充分溶解混匀后分装置于4℃冰箱短期保存备用。
[0026]
(1)荧光原位杂交实验
[0027]
1)使用组织切片仪进行切片2张,厚度3
‑
5μm,将切片附于防脱载玻片上,放入65℃恒温箱中烤干至少2小时。将其中一张切片进行he染色,染色完成后镜下标记出组织内的肿瘤区域。
[0028]
2)样本脱蜡:
[0029]
1.从恒温箱中取出玻片,将其放入室温二甲苯中10分钟;
[0030]
2.取出玻片,再将其放入另一缸室温二甲苯中10分钟;
[0031]
3.取出玻片,再将其放入室温无水乙醇中5分钟;
[0032]
3)切片前处理:
[0033]
1.设置tbe参数:
[0034][0035]
2.根据切片数量,配制好足量的所需试剂并将试剂倒入tbe对应的试剂瓶里:1号瓶为去离子水dh2o;2号瓶为75%酒精;3号瓶为85%酒精;4号瓶为100%乙醇;5号瓶为修复液(1
×
edta);8号瓶为洗涤液ⅰ(2
×
ssc);10号瓶为洗涤液ⅱ((0.1%np
‑
40/2
×
ssc),所需试剂量最低量可以由tbe软件计算出。
[0036]
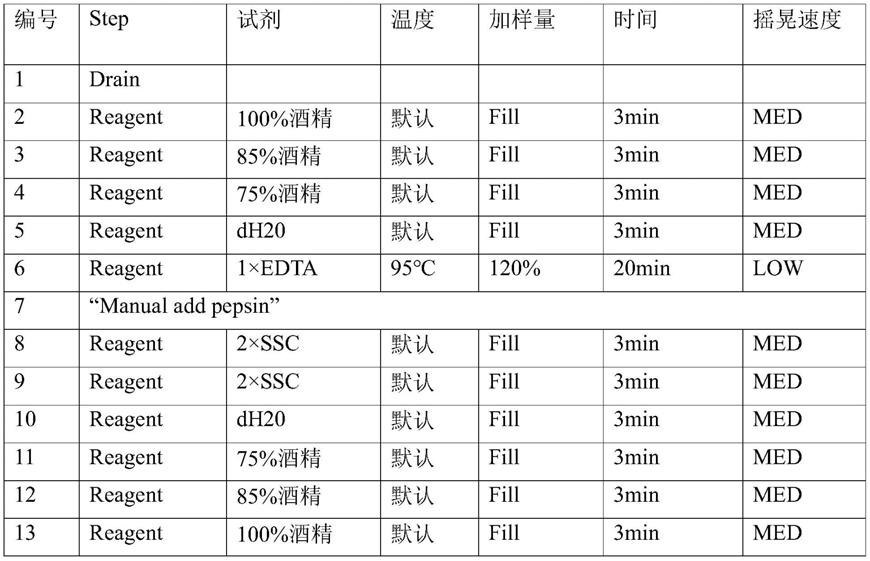
3.将切片放入tbe切片槽,运行设置好的前处理协议。
[0037]
4.当前处理协议运行到步骤7“manual add pepsin”时,机器自动暂停运行,打开tbe盖子,取出切片自然晾干。
[0038]
5.待晾干后,对照he切片上标记的肿瘤区域,刮除非肿瘤区域。
[0039]
6.将切片组织面朝上平置入湿盒内,滴加适量的胃蛋白酶对组织进行消化,消化条件设置:37℃恒温,15
‑
20分钟。
[0040]
7.将多余消化液甩去,将片子放回tbe切片槽中,点击“继续”进行后续的处理。
[0041]
8.待预处理协议结束后,取出玻片,室温条件下晾干。
[0042]
4)检测探针变性杂交(避光操作):
[0043]
1.将探针从
‑
20℃冰箱中取出,在室温下复温,震荡混匀后,使用掌上离心机瞬时离心。
[0044]
2.滴加5μl探针到切片的组织区域后使用18
×
18mm盖玻片将该区域覆盖,轻压使探针均匀分布,注意避免产生气泡。
[0045]
3.设置tbe的变性杂交参数:
[0046]
编号step试剂温度加样量时间摇晃速度1drain
ꢀꢀꢀꢀꢀ
2reagentdh2o80℃50%7minlow3reagentdh2o37℃50%15hlow
[0047]
4.用封片胶沿盖玻片边缘封片,使盖玻片和载玻片接触部位完全封闭。
[0048]
5.封片完成后将玻片放入tbe切片槽,运行设置好的参数,进行过夜杂交。
[0049]
5)切片后处理(避光操作):
[0050]
1.待变性杂交结束后,取出玻片,揭开封片胶。
[0051]
2.设置tbe的后处理参数:
[0052]
编号step试剂温度加样量时间摇晃速度1drain
ꢀꢀꢀꢀꢀ
2reagent2xssc42℃120%3minlow3reagent2xssc42℃120%3minlow4reagent0.1%np
‑
40/2
×
ssc42℃120%4minlow5reagent75%酒精默认120%3minmed6reagent85%酒精默认120%3minmed7reagent100%酒精默认120%3minmed
[0053]
3.轻柔的移去盖玻片,注意不要刮花组织,然后迅速放回全tbe切片槽中,运行后处理协议。
[0054]
4.待后处理协议结束后,取出切片,黑暗处自然晾干。
[0055]
5.滴加10μl dapi复染液到杂交区域,使用20
×
20mm盖玻片迅速覆盖,轻压玻片使杂染液分布均匀,注意避免产生气泡,在暗处存放待观察。
[0056]
实施例2
[0057]
通过实施例1的荧光原位杂交方法对27例胶质母细胞瘤样本中hoxa5基因扩增情况进行了检测,图1为荧光原位杂交及二代测序检测胶质瘤样本中hoxa5基因扩增结果。图1中a为参照who2019版her
‑
2基因扩增制定了hoxa5基因扩增的评判标准及流程。图1中b为荧光原位杂交结果,显示胶质母细胞瘤样本中hoxa5(红色)和7号染色体着丝粒(绿色)探针信号表达(标尺5μm),根据hoxa5与7号染色体探针信号比例主要分为5种情况,显示hoxa5扩增具有异质性。进一步统计分析结果显示:14/27例样本平均拷贝数大于等于6,为hoxa5基因扩增(图1中c);5例样本平均拷贝数介于4
‑
6,进一步免疫组化分析结果发现其中4例hoxa5蛋白呈现强阳性表达(图1中d),显示该4/5例样本为hoxa5基因扩增。图1中e综合荧光原位杂交及免疫组化结果显示18/27例(66.7%)胶质母细胞瘤患者标本为hoxa5基因扩增,配对的正常组织则均显示为未扩增状态。图1中f为进一步通过二代测序方法验证了荧光原位杂交实验的结果,显示44例胶质母细胞瘤样本及配对正常组织中hoxa5基因扩增比例。图1中g二代测序结果7号染色体扩增(20例)与非扩增样本(24例)中hoxa5基因扩增比例,在24例hoxa5基因扩增病例中,4例(16.7%)样本不存在7号染色体扩增,提示存在不依赖于7号染色体扩增的hoxa5基因扩增现象。
[0058]
实施例3
[0059]
hoxa5基因荧光原位杂交结果显示hoxa5基因扩增与胶质瘤级别可能有相关性,我们进一步通过不同胶质瘤数据库对hoxa5基因扩增情况进行了验证。tcga和rembrandt数据库查询结果均显示hoxa5扩增病例比例随着胶质瘤级别的增加而逐渐升高,胶质母细胞瘤明显高于ⅱ级和ⅲ级胶质瘤(图2中a、b)。此外,在胶质母细胞瘤与ⅲ级胶质瘤中,hoxa5基因在idh1野生型中比idh1突变型扩增比例更高,而这种差异在低级别ⅱ级胶质瘤中并不显著(图2中c)。同时,与星形胶质细胞瘤、少突胶质细胞瘤及混合型胶质细胞瘤相比,胶质母
细胞瘤中hoxa5扩增比例更高(图2中d、e)。在tcga数据库中查询四种分子亚型的胶质母细胞瘤发现hoxa5在间充质亚型中扩增比例最高,在前神经亚型中扩增比例最低(图2中f),与胶质瘤干细胞的分布规律较为一致,提示hoxa5扩增与胶质瘤干细胞的潜在联系。
[0060]
最后,我们通过预后分析发现与hoxa5基因非扩增病例相比,hoxa5基因扩增病例预后明显较差(图3中a)。在tcga(图3中b)和rembrandt(图3中c)数据库中也得到了验证,充分证明hoxa5基因扩增导致胶质瘤患者生存期缩短。所以本发明提供的hoxa5基因的fish探针为临床检测hoxa5基因扩增有很好的应用性,可用于胶质母细胞瘤的临床诊断和预后判断。进一步通过预后给出适合延长患者生存期的方法,提高患者的生存质量。
[0061]
实施例4
[0062]
我们对hoxa5基因扩增状态的病例使用相同组织蜡块的连续切片进行hoxa5蛋白的免疫组织化学染色。结果显示hoxa5平均拷贝数与hoxa5蛋白表达呈显著正相关,显示hoxa5基因扩增导致其表达的增加(图4中a、b)。同时,在对胶质瘤细胞系和原代胶质瘤细胞进行检测后也发现,hoxa5基因拷贝数与hoxa5蛋白表达也呈正相关(图4中c、d)。最后,我们通过对胶质瘤tcga数据库中hoxa5基因扩增、表达以及相关临床病理学参数进行了分析,发现hoxa5基因扩增病例其表达也明显较高,同时基因扩增病例富集区域表现为胶质母细胞瘤、idh野生型、间充质亚型等特点,提示hoxa5基因扩增并由此导致的表达增加与胶质瘤恶性生物学行为相关(图4中e)。
[0063]
为了进一步明确hoxa5表达与胶质瘤级别的关系,继续用胶质瘤tcga(图5中a)和gravendeel(图5中b)数据库的数据进行验证,验证结果显示hoxa5在高级别胶质瘤中显著高表达。同时,根据idh突变状态进行进一步分组时也发现无论在idh野生型还是突变型中,高级别胶质瘤组表现出更高的hoxa5基因表达(图5中c、d)。而在tcga数据库中根据7号染色体是否扩增进行分组时发现扩增组中hoxa5基因表达也是显著高于未扩增组(图5中e)。通过将胶质母细胞瘤样本与配对的正常脑组织进行对比发现肿瘤标本中hoxa5表达明显高于正常组织(图5中f)。
[0064]
这一研究发现更加确立了本发明提供的hoxa5基因fish探针检测hoxa5基因扩增在制备胶质母细胞瘤诊断和/或预后的试剂和/试剂盒中的应用价值。也有助于对治疗后的研究和评估。
[0065]
最后说明的是,以上优选实施例仅用以说明本发明的技术方案而非限制,尽管通过上述优选实施例已经对本发明进行了详细的描述,但本领域技术人员应当理解,可以在形式上和细节上对其作出各种各样的改变,而不偏离本发明权利要求书所限定的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。