1.本发明涉及稳定同位素丰度检测技术领域,尤其是涉及一种尿素中同位素丰度的检测方法。
背景技术:
2.尿素-13
c是尿素[
13
c]呼气试验诊断试剂的有效成份,被广泛应用于临床诊断幽门螺杆菌(hp)感染,因具有特异性高、无损伤、无放射性、快速等优势被公认为胃部感染hp诊断的金标准。呼气试验诊断试剂及原料药尿素-13
c中同位素丰度的准确测定直接影响到临床检测结果,因此准确测定尿素-13
c的同位素丰度显得尤为重要。
[0003]
现有尿素-13
c同位素丰度检测方法主要采用行标法《hg/t 4138—2010稳定性同位素
13
c-尿素》,行标法的原理是利用亚硝酸具有强氧化性(杜晓宁,宋明鸣,赵诚,徐建飞.
13
c-尿素同位素丰度的检测方法[j].同位素,2010,23(1):39-43),将尿素-13
c氧化生成
13
c标记二氧化碳,但在反应过程中亚硝酸易分解生成no2等杂质气体。
[0004]
发明专利cn 110793826 a公开了一种用于测定碳13同位素丰度的样品制备方法,包括装样,将
13
c标记的待制备样品与氧化剂的水溶液装入双球反应管的第一球泡中,将酸性物质装入双球反应管的第二球泡中;制备
13
co2气体,保持真空度,同时将第二球泡中的酸性物质加入第一球泡中,生成
13
co2;检测,待真空旋塞阀与气体同位素质谱仪间管路的真空度降至2
×
10-5
pa以下时,打开真空旋塞阀,将第一球泡中的
13
co2引入到气体同位素质谱仪中;设定气体同位素质谱仪的检测参数,检测质量数为44和45的相对强度,计算
13
c同位素丰度。该方法属于氧化法,氧化剂与碳元素反应生成
13
co2,测试的是碳元素的整体同位素丰度。对尿素-13
c单体测试,需要尿素-13
c的纯度非常高,杂质中碳元素也同氧化剂一起反应,杂质的存在会导致
13
c同位素丰度稀释。
[0005]
尿素-15
n2作为农业的示踪剂,可以为量化氮转化过程速率、氮的来源和去向及其发生机制提供解释,从而能够加深对于生态系统尺度上氮循环的认识和提升氮管理能力。
[0006]
现有的尿素-15
n2同位素丰度国标检测方法(gb/t 20622-2006稳定性同位素
15
n无机标记化合物)(杜晓宁;宋明鸣;赵诚.质谱检测用同位素
15
n标记样品的处理方法[j].原子能科学技术,2009,43(增刊):59-63),主要采用浓硫酸将尿素-15
n2消解,后经过加碱蒸馏得到
15
n标记铵盐,最后
15
n标记铵盐与次溴酸钠反应生成
15
n标记氮气,整个过程中消解和蒸馏步骤需要耗时(3~5)h,且过程繁琐。
技术实现要素:
[0007]
本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种尿素中同位素丰度的检测方法,利用脲酶的专一性将
13
c或
15
n标记尿素催化转化生成
13
c或
15
n标记碳酸铵,后续针对
13
c或
15
n不同的同位素丰度测试,采用不同的反应装置。其具有反应时间短(≤30min),反应温度低于50℃、可用于
13
c或
15
n标记尿素同位素丰度测定。
[0008]
本发明的目的可以通过以下技术方案来实现:
[0009]
本发明的目的是提供一种尿素中同位素丰度的检测方法,所述检测方法包括以下过程中的一种或者两种,以此对应检测
13
c、
15
n的单元素标记或双元素标记:
[0010]
过程(1),尿素中
13
c同位素丰度检测时,利用酶的专一性,第一步将
13
c标记尿素在脲酶的水溶液存在下,反应生成碳酸铵-13
c,第二步将碳酸铵-13
c与酸反应分解产生
13
co2,将
13
co2气体引入气体同位素质谱仪中测定
13
c同位素丰度;
[0011]
过程(2),尿素中
15
n同位素丰度检测时,利用酶的专一性,第一步将
15
n标记尿素在脲酶的水溶液存在下,反应生成碳酸铵-15
n,第二步将碳酸铵-15
n与氢氧化钠反应分解释放
15
n标记氨氮,用硫酸吸收得到
15
n标记硫酸铵,第三步将
15
n标记硫酸铵与次溴酸钠反应生成
15
n标记氮气,将
15
n标记氮气引入气体同位素质谱仪中测定
15
n同位素丰度。
[0012]
本发明主要是利用脲酶的专一性,只与尿素-13
c/
15
n单体进行酶催化反应,不受基质和杂质的影响,专一性非常强,对尿素-13
c/
15
n的纯度没有要求。
[0013]
进一步地,过程(1)中,第一步的反应条件包括:ph为7,且在(25~45)℃温度下,反应(3~10)min。
[0014]
进一步地,过程(2)中,ph为7,且在(25~45)℃温度下,反应(3~10)min,第二步的反应条件包括:(25~45)℃温度下,反应(3~10)min。
[0015]
进一步地,过程(1)中,抽真空需要在第一步反应前完成;
[0016]
过程(2)中,抽真空需要在第三步反应前完成。
[0017]
进一步地,过程(1)中,采用三球反应管和进样连接器实现尿素中
13
c同位素丰度检测样品气的制备。
[0018]
进一步地,过程(1)中,包括样品气的制备装置的搭建,具体包括:
[0019]
取尿素-13
c、脲酶加入三球反应管中的b球泡位置,取蒸馏水放入三球反应管中的a球泡位置,取硫酸溶液放入三球反应管中的c球泡位置,且使得进样连接器的一端与三球反应管连接,进样连接器的另一端与真空系统连接,以此完成样品气的制备装置的搭建。
[0020]
进一步地,过程(1)中,包括测定
13
c同位素丰度的样品气的制备过程,具体包括:
[0021]
打开进样连接器的旋塞阀,抽真空,待液体中无气泡,此时将进样连接器的旋塞阀关闭,将进样连接器从真空系统上取下,先将三球反应管a球泡位置中的蒸馏水倒入b球泡位置中,之后再将位置c球泡位置中的硫酸溶液倒入位置b球泡位置中混合后生成
13
c标记二氧化碳气体,即可作为测定
13
c同位素丰度的样品气。
[0022]
进一步地,过程(2)中,包括样品前处理过程,具体包括:
[0023]
取尿素-15
n2、脲酶加入氨氮接收装置e中,取硫酸溶液加入氨氮接收装置d中,将氨氮接收装置d放入氨氮接收装置e中,密封盖盖在氨氮接收装置e上,反应后向氨氮接收装置e中加入氢氧化钠溶液,反应,完成样品前处理过程,所述氨氮接收装置e、氨氮接收装置d均为敞口容器。
[0024]
进一步地,过程(2)中,包括测定
15
n2同位素丰度的样品气的制备过程,具体包括:
[0025]
取氨氮接收装置d中的反应液放入两球反应管h球泡位置中,之后取次溴酸钠溶液放入两球反应管g球泡位置中,且使得两球反应管与进样连接器的一端连接,进样连接器的另一端与真空系统连接;
[0026]
打开进样连接器上的旋塞阀,抽真空,之后将进样连接器中的旋塞阀关闭,将进样连接器从真空系统中取下,生成
15
n标记氮气气体即可作为测定
15
n同位素丰度的样品气。
[0027]
进一步地,测定
13
c的单元素标记过程中:
[0028]
将三球反应管内的
13
co2引入气体同位素质谱仪中,检测质量数为44和45的离子流强度,通过公式计算
13
c同位素丰度;
[0029]
测定
15
n的单元素标记过程中:
[0030]
将两球反应管内的
15
n2引入气体同位素质谱仪中,检测质量数为29和30的离子流强度,通过公式计算
15
n同位素丰度。
[0031]
与现有技术相比,本发明具有以下技术优势:
[0032]
本技术方案利用脲酶的专一性将
13
c或
15
n标记尿素催化转化生成
13
c或
15
n标记碳酸铵,后续针对
13
c或
15
n不同的同位素丰度测试,采用不同的反应装置,整体方案具有反应时间短(≤30min),反应温度低于50℃、可用于
13
c或
15
n标记尿素同位素丰度测定,测试数据准确度和精密度高等优点。
附图说明
[0033]
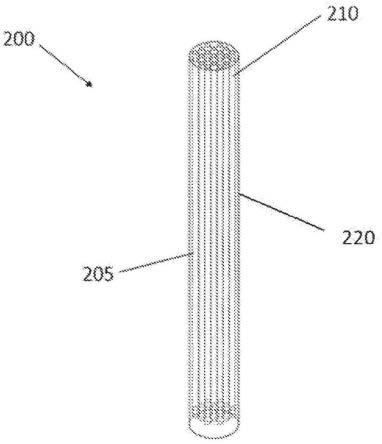
图1为本发明所用的进样连接器的示意图;
[0034]
图2为本发明所用的三球反应管示意图;
[0035]
图3为本发明所用到的氨氮接收装置的示意图;
[0036]
图4为本发明所用到的两球反应管的示意图。
[0037]
图中标记说明:
[0038]
1、4、5、6为标准磨口位置;2、3为旋塞阀。a、b、c、g、h为反应管的球泡位置2,d、e为取氨氮接收装置(具体分别为小敞口容器和大敞口容器),f-密封盖。
具体实施方式
[0039]
下面结合附图和具体实施例对本发明进行详细说明。本技术方案中如未明确说明的制备手段、材料、结构或组成配比等特征,均视为现有技术中公开的常见技术特征。
[0040]
实施例1
[0041]
尿素-13
c同位素丰度测定,包括以下步骤:
[0042]
本实施例采用的反应装置为如图1所示进样连接器、如图2所示的三球反应管。
[0043]
(1)制备
13
co2[0044]
取3mg尿素-13
c、30mg脲酶加入三球反应管中的“b”位置,取1ml蒸馏水放入三球反应管中的“a”位置,取0.5ml 4mol/l硫酸溶液放入三球反应管中的“c”位置,进样连接器“4”与三球反应管“5”连接,进样连接器“1”与真空系统连接,打开旋塞阀“2”和“3”,抽真空。
[0045]
待液体中无气泡,此时可将进样连接器中的旋塞阀“2”和“3”关闭,将三球反应管和进样连接器从真空系统中取下,先将“a”中的蒸馏水倒入“b”球泡中,5min后再将“c”中的硫酸溶液倒入“b”球泡中混合后生成
13
c标记二氧化碳气体即可作为测定
13
c同位素丰度的样品气。
[0046]
(2)仪器参数设置
[0047]
采用电子轰击离子源(ei);离子源温度为110℃;分子量扫描范围为40~50m/z;阱
电压为105v;电子轰击能量为100ev;高压为10kv,检测器为法拉第筒。
[0048]
(3)
13
c同位素丰度的计算
[0049]
进样连接器“1”接入气体同位素质谱仪,将三球反应管的球泡浸入酒精液氮调制的冷冻液中数分钟,利用气体同位素质谱仪的进样系统抽真空,待真空度低于50pa后,打开旋塞阀“2”和“3”,将三球反应管内的
13
co2引入气体同位素质谱仪中,检测质量数为44和45的离子流强度,通过公式计算
13
c同位素丰度。分别为99.252atom%
13
c、99.261atom%
13
c,平均值99.26atom%
13
c。
[0050]
同时,采用行标法《hg/t 4138—2010稳定性同位素
13
c-尿素》测试结果为99.25atom%
13
c,两种方法的测定结果基本相当,可见,本发明的同位素丰度测定方法也具有非常高的测量准确度。
[0051]
实施例2
[0052]
尿素-15
n2同位素丰度测定,包括以下步骤:
[0053]
本实施例采用的反应装置为如图1所示进样连接器、如图3所示的氨氮接收装置、如图4所示的两球反应管。
[0054]
(1)样品前处理
[0055]
取5mg尿素-15
n2、50mg脲酶加入氨氮接收装置“e”中,取2ml 1mol/l硫酸溶液加入氨氮接收装置“d”中,将氨氮接收装置“d”放入氨氮接收装置“e”中,密封盖“f”盖在氨氮接收装置“e”上,反应8min后向氨氮接收装置“e”中加入2ml 1mol/l氢氧化钠溶液,反应5min。
[0056]
(2)制备
15
n2[0057]
取1ml氨氮接收装置“d”中的反应液放入两球反应管“h”球泡中,取1ml1mol/l次溴酸钠溶液放入两球反应管“g”球泡中,两球反应管“6”与进样连接器“4”相连接,进样连接器“1”与真空系统连接,打开旋塞阀“2”和“3”,抽真空。将进样连接器中的旋塞阀“2”和“3”关闭,将两球反应管和进样连接器从真空系统中取下。生成
15
n标记氮气气体即可作为测定
15
n同位素丰度的样品气。
[0058]
(3)仪器参数设置
[0059]
采用电子轰击离子源(ei);离子源温度为99℃;分子量扫描范围为28~44m/z;阱电压为121v;电子轰击能量为100ev;高压为10kv,检测器为法拉第筒。
[0060]
(4)
15
n同位素丰度的计算
[0061]
进样连接器“1”接入气体同位素质谱仪,将双球反应管的球泡浸入液氮中数分钟,利用气体同位素质谱仪的进样系统抽真空,待真空度低于50pa后,打开旋塞阀“2”和“3”,将两球反应管内的
15
n2引入气体同位素质谱仪中,检测质量数为29和30的离子流强度,通过公式计算
15
n同位素丰度。分别为99.341atom%
15
n、99.347atom%
15
n,平均值99.34atom%
15
n。
[0062]
同时,采用国标法《gb/t 20622-2006稳定性同位素
15
n无机标记化合物》测试结果为99.38atom%
13
c,两种方法的测定结果基本相当,可见,本发明的同位素丰度测定方法也具有非常高的测量准确度,同时,本发明实验过程从4h缩短到0.5h。
[0063]
实施例3
[0064]
双标记尿素-13
c,
15
n2同位素丰度测定,包括以下步骤:
[0065]
(1)
13
c同位素丰度测定步骤参考“实施例1”,
13
c同位素丰度分别为99.125atom%
13
c、99.198atom%
13
c,平均值99.16atom%
13
c。
[0066]
(2)
15
n同位素丰度测定步骤参考“实施例2”,
15
n同位素丰度分别为99.230atom%
15
n、99.157atom%
15
n,平均值99.19atom%
15
n。
[0067]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。