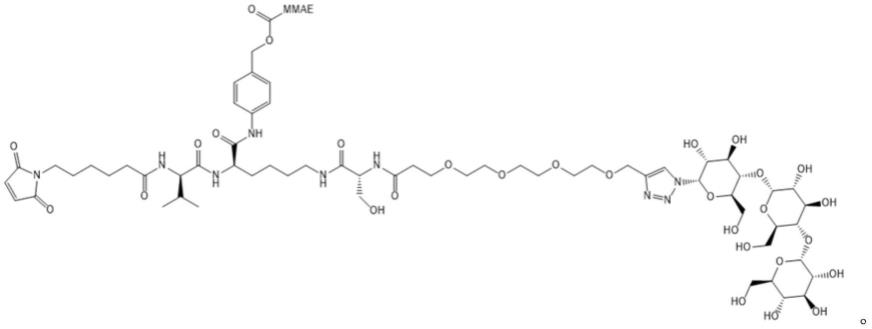
1.本发明属于生物医药领域,涉及新型亲水性糖基化连接子及其合成和应用,具体涉及新型亲水性糖基化连接子的合成和在trop2抗体偶联药物中的应用。
背景技术:
2.抗体偶联药物(antibody-drug conjugates,adcs)由抗体通过化学连接子偶联细胞毒素组成得一种新型的抗体药物,可以将细胞毒性药物靶向递送到特定肿瘤细胞。提高抗肿瘤药物的靶向性并减少毒副作用,扩展药物的治疗窗口,是肿瘤治疗领域发展速度最快的药物之一。
3.人滋养层表面细胞抗原(trophoblast cell-surface antigen 2,trop2),是由 tacstd2基因编码表达的i型单次跨膜糖蛋白,在多种上皮源性的实体瘤(如乳腺癌、宫颈癌、结直肠癌、肾癌、肝癌、肺癌、胰腺癌和前列腺癌等)中过量表达,尤其是三阴性乳腺癌和非小细胞肺癌。trop2还与细胞中多种信号转导途径相关,研究表明trop2可以动员细胞中的ca
2
,转导细胞内钙信号,可以激活下游的有丝分裂原活化蛋白激酶(mitogen-activated protein kinase,mapk)信号通路,促进癌细胞的生长、增殖和侵袭。同时trop2具有干细胞样的特性,调节细胞的生长、转化、再生和增殖,这可能是trop2过表达会导致肿瘤进展,患者生存期降低,预后不良的原因。同时当抗体与trop2结合后,trop2可以有效的介导内吞,所以trop2是一个非常理想的adc靶点。靶向trop2的 adc分子sacituzumab govitecan(immu132)在治疗难治性转移三阴性乳腺癌展现出了优异的药效和安全性,于2020年4月被美国fda批准上市。
4.增加药物抗体比率(drug to antibody ratio,dar)尽管从理论上讲可以提高adc的活性,但高dar值的adc通常热稳定性差、容易聚集、体内清除速率加快,导致药效降低和毒性增加。研究表明,药物-连接子系统的强疏水性可能是导致这一现象的主要原因。为了使adc同时具有理想活性和良好的药代动力学特性,我们希望设计一种亲水性的药物-连接子系统来使高dar值adc 在体内具有良好的抗肿瘤活性、安全性及药代动力学特性。并用以trop2作为靶点进行概念验证,致力于开发新型高效的靶向trop2得抗体偶联药物。
技术实现要素:
5.本发明的目的在于开发一种新型的亲水性连接子-药物系统,有助于提高 adc水溶性和稳定性,克服了高药物抗体比率(dar)的adc分子疏水性强、稳定性差的问题。将其应用在靶向trop2的抗体偶联药物中,得到了一种新型高效的抗体偶联药物分子。
6.本发明采用如下技术方案:
7.本发明的第一方面,设计并合成了3种新型的亲水性糖基化连接子-药物系统,用于高药物抗体比率(dar)高活性抗体偶联药物的制备;
8.优选的,所述的细胞毒性药物选自但不限于单甲基澳瑞他汀 e(monomethyl auristatin,mmae);
9.在一优选例中,连接子含有葡萄糖(glc),所述的连接子-药物为 mc-gly-(glc)val-cit-pabc-mmae(简称mc-g(glc)vc-mmae),结构式如下所示:
10.在另一优选例中,连接子含有葡萄糖(glc)和聚乙二醇(peg),所述的连接子-药物为mc-val-lys(peg4-glc)-pabc-mmae(简称 mc-vk(peg4-glc)-mmae),结构式如下所示:
11.在另一优选例中,连接子含有麦芽三糖(mal)和聚乙二醇(peg),所述的连接子-药物为mc-val-lys(peg4-mal)-pabc-mmae(简称 mc-vk(peg4-mal)-mmae),结构式如下所示:
12.本发明的第二方面,提供3种新型的靶向trop2的抗体偶联药物。
13.抗体偶联药物简称为ab-(l-d)n;
7.其中ab表示抗体(antibody),优选地,所述抗体选自但不限于靶向trop2 的hrs7;
14.d为具有细胞毒性药物(drug),优选地,所述细胞毒性药物选自但不限于单甲基澳瑞他汀e(monomethyl auristatin,mmae);
15.l为连接抗体和小分子的连接子(linker);
16.n为抗体偶联小分子数目,也称为药物抗体比率(dar),n为大于等于1 小于等于8的整数或非整数,下文中n为8。
17.“‑”
为化学键。
18.经典案例中,l为mc-vc-pabc,d为mmae,所述的抗体偶联药物为 hrs7-[mc-vc-pabc-mmae]8(简称hrs7-vc-mmae),结构式如下下所示:
[0019]
hrs7-vc-mmae
[0020]
在一优选例中,l中包含葡萄糖(glc),所述的抗体偶联药物为 hrs7-[mc-g(glc)vc-pabc-mmae]8(简称hrs7-g(glc)vc-mmae),结构式如下所示:
15.hrs7-g(glc)vc-mmae
[0021]
在另一优选例中,l中包含葡萄糖(glc)和聚乙二醇peg4,所述的抗体偶联药物为hrs7-[mc-vk(peg4-glc)-pabc-mmae]8(简称 hrs7-vk(peg4-glc)-mmae),结构式如下所示:
[0022]
hrs7-vk(peg4-glc)-mmae
[0023]
在另一优选例中,l中包含麦芽三糖(mal)和聚乙二醇peg4,所述的抗体偶联药物为hrs7-[mc-vk(peg4-mal)-pabc-mmae]8(简称 hrs7-vk(peg4-mal)-mmae),结构式如下所示:
[0024]
hrs7-vk(peg4-mal)-mmae
[0025]
本发明第三方面,提供了一种制备均一dar8抗体偶联药物(adc)的方法,包括:
[0026]
优选地,抗体溶解到含有2mm edta的pbs中,ph调整到8,加入8 倍当量的tcep,37℃还原2h;
[0027]
优选地,连接子-药物用dmso溶解,将还原后的抗体放在室温冷却至室温后加入12倍当量的连接子药物,室温搅拌反应20min。
[0028]
本发明第四方面,提供了本发明所述的药物组合物的用途,用于制备抗肿瘤药物;所述肿瘤包括胰腺癌、乳腺癌、结肠癌和肺癌等。
[0029]
本发明第五方面,提供一种治疗肿瘤的方法,包括将前述肿瘤治疗药物试用于患者。
[0030]
与现有技术相比,本发明具有如下有益效果:
[0031]
本发明设计并合成的亲水性糖基化连接子有效提升了抗体偶联药物的水溶性和稳定性,有望克服高dar值adc分子因为疏水性强成药性差的问题,可以得到更高活性高dar值adc分子,使细胞毒性分子有效富集到肿瘤部位,减少药物使用剂量,拥有更大的治疗窗口,为那些难治复发性的癌症类型带来新的治疗方法。
附图说明
[0032]
图1:mc-g(glc)vc-mmae的合成路径;
[0033]
图2:mc-vk(peg4-glc)-mmae的合成路径;
[0034]
图3:mc-vk(peg4-mal)-mmae的合成路径;
[0035]
图4:hic-hplc鉴定抗体偶联药物的dar值和疏水性;
[0036]
图5:sec-hplc鉴定抗体偶联药物的稳定性;
[0037]
图6:elisa检测hrs7-vk(peg4-mal)-mmae与trop2亲和力;
[0038]
图7:流式检测hrs7-vk(peg4-mal)-mmae内吞;
[0039]
图8:流式检测肿瘤细胞trop2表达水平;hrs7-vk(peg4-mal)-mmae 抑制肿瘤细胞生长;
[0040]
图9:hrs7-vk(peg4-mal)-mmae在bxpc-3肿瘤模型中的药效。
具体实施方式
[0041]
本发明人通过广泛而深入的研究,选择以糖基化修饰来增加抗体偶联药物中连接子的亲水性,并以trop2为靶点构建dar8的抗体偶联药物的进行概念验证,实验结果表明,与传统连接子药物vc-mmae,修饰后的连接子制备得到的抗体偶联药物的水溶性稳定性得
到显著改善,选择表现最优的 hrs7-vk(peg4-mal)-mmae)分子进行体内实验,结果表明其在单剂量1mg/kg 就有显著的抗肿瘤活性,药效远强于阳性已上市分子immu132,具有治疗 trop2阳性肿瘤的巨大潜力。
[0042]
一、mc-g(glc)vc-pabc-mmae、mc-vk(peg4-glc)-mmae和 mc-vk(peg4-mal)-mmae
[0043]
mc指马来酰亚胺(maleimidomethyl),g指甘氨酸(glycine),v指缬氨酸(valine),glc指葡萄糖(glucose),pabc指对氨基苄基氨基甲酰基 (p-aminobenzyl carbamoyl),peg4指4个聚乙二醇组成的链,mal指麦芽三糖 (maltotriose)
[0044]
二、hrs7-vk(peg4-mal)-mmae
[0045]
本发明的hrs7-vk(peg4-mal)-mmae属于抗体偶联药物,所述细胞毒性药物选自但不限于单甲基澳瑞他汀e(monomethyl auristatin,mmae),所述抗体选自但不限于靶向人滋养层表面细胞抗原(trophoblast cell-surface antigen 2, trop2)的抗体hrs7。
[0046]
每个hrs7分子携带8个单甲基澳瑞他汀e(monomethyl auristatin, mmae)分子。
[0047]
一实施例中,mc-vk(peg4-mal)-mmae通过抗体还原后释放的半胱氨酸游离巯基偶联。
[0048]
三、hrs7-vk(peg4-mal)-mmae制备方法:
[0049]
抗体还原:抗体溶解到含有2mm edta的pbs中,ph调整到8,加入 8倍当量的tcep,37℃还原2h;抗体偶联:连接子-药物用dmso溶解,将还原后的抗体放在室温冷却至室温后加入12倍当量的连接子药物,室温搅拌反应 20min。
[0050]
四、优选分子hrs7-vk(peg4-mal)-mmae的用途
[0051]
本发明hrs7-vk(peg4-mal)-mmae可用于制备肿瘤的治疗药物。
[0052]
一实例中,本发明的hrs7-vk(peg4-mal)-mmae可用于胰腺癌的治疗,能有效抑制肿瘤组织的生长。
[0053]
因此,可采用本发明的mc-vk(peg4-mal)-mmae来制备肿瘤治疗药物,用于肿瘤疾病的治疗。
[0054]
五、肿瘤治疗药物组合物
[0055]
发明的肿瘤治疗药物组合物的有效成分中含有前述抗体-药物偶联物,例如hrs7-vk(peg4-mal)-mmae,所述药物组合物中,hrs7-vk(peg4-mal)
ꢀ‑
mmae为该药物组合物的有效成分之一或唯一有效成分。
[0056]
六、治疗肿瘤的方法
[0057]
将前述肿瘤治疗药物试用于患者,可用来治疗肿瘤。
[0058]
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围。下列实施例中未注明具体条件的试验方法,通常按照常规条件,或者按照各制造商所建议的条件。
[0059]
当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实
现本发明。
[0060]
除非另外说明,本发明中所公开的实验方法、检测方法、制备方法均采用本技术领域常规的分子生物学、生物化学、染色质结构和分析、分析化学、细胞培养、重组dna技术及相关领域的常规技术。这些技术在现有文献中已有完善说明,具体可参见molecular cloning:a laboratory manual,fourth edition,2012, michael r.green and joseph sambrook、culture of animal cells:a manual of basictechnique and specialized applications,7th edition,2016,r.ian freshney。
[0061]
实施例1 mc-gly-(glc)val-cit-pabc-mmae的合成(图1)
[0062]
fmoc-gly(glc)-oh(1)的合成步骤一:在650μl的d2o中加入d-葡萄糖(45mg,0.25mmol),三乙胺(350μl, 2.5mmol)和nan3(152.5mg,2.5mmol),混匀后加入dmc(127.0mg,0.75mmol),冰上搅拌反应1h。lc-ms监测产物生成ms:[m na]
=228.45da,准确分子量205.07da。催化剂:7.5μl 200mm cuso4(0.0015mmol)加入45μl 200mm bttaa(0.009mmol) 混匀后加入20μl 1m vc-na(0.02mmol)步骤二:取fmoc-propargyl-gly-oh(33.5mg,0.1mmol)加入步骤一的溶液中,加入催化剂后室温反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末状的fmoc-gly(glc)-oh(1)(38mg),ms:[m h] =541.29da,准确分子量540.19da。
[0063]
fmoc-gly(glc)-val-cit-pabc-mmae(2)的合成在200μl dmf中加入化合物1(5.4mg,0.01mmol)和hatu(7.6mg,0.02mmol),混匀后加入h2n-val-cit-pabc-mmae(11.2mg,0.01mmol)和dipea(5μl,0.03mmol),室温搅拌反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末fmoc-gly(glc)-val-cit-pabc-mmae(13.6mg)(2)。ms:[m/2 h]
= 823.47da,准确分子量1644.88da。
[0064]
h2n-gly(glc)-val-cit-pabc-mmae(3)的合成化合物2用400μl dmf溶解,加入100μl哌啶(20%),室温反应30min。反相 hplc纯化,冻干后得到白色粉末h2n-gly(glc)-val-cit-pabc-mmae(9.8mg)(化合物3)。ms:[m/2 h]
=712.73da,准确分子量1422.81da。
[0065]
mc-gly(glc)-val-cit-pabc-mmae(linker1)的合成在200μl dmf中加入5-马来酰亚胺戊酸(1.4mg,0.007mmol)和hatu(5.3mg, 0.014mmol)混匀后加入化合物3(9.8mg,0.0069mmol)和dipea(3.5μl, 0.021mmol),室温反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末mc-gly(glc)-val-cit-pabc-mmae(9.3mg,linker1) ms:[m/2 h]
=801.92da,准确分子量1601.87da。
[0066]
实施例2 mc-val-lys(peg4-mal)-pabc-mmae的合成(图2)
[0067]
glc-peg4 ser obzl(4)的合成步骤一:在650μl的d2o中加入d-葡萄糖(45mg,0.25mmol),三乙胺(350μl, 2.5mmol)和nan3(152.5mg,2.5mmol),混匀后加入dmc(127.0mg,0.75mmol),冰上搅拌反应1h。lc-ms监测产物生成ms:[m na]
=228.45da,准确分子量 205.07da。步骤二:在100μl dmf中加入l-ser-obzl.hcl(23.1mg,0.1mmol)和dipea(17μl, 0.1mmol)混匀后加入propargyl-peg4-nhs eater(40mg,0.11mmol)室温反应0.5h。 lc-ms监测产物生成。ms:[m h]
=438.45da
催化剂:7.5μl 200mm cuso4(0.0015mmol)加入45μl 200mm bttaa(0.009mmol) 混匀后加入20μl 1m vc-na(0.02mmol)步骤三:将步骤一和步骤二的反应液混合,加入催化剂后室温反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末glc-peg4 ser obzl (4)(38mg),ms:[m h]
=643.61da,准确分子量642.27da。
[0068]
glc-peg4 ser cooh(5)的合成将化合物4和用5ml(超纯水:甲醇=5:95)的溶液溶解,加入30mg 10%pd/c氢气搅拌催化3h,脱去羧基的保护基obzl。反应液过滤,加压蒸馏后即可获得透明油状产物。glc-peg4 ser cooh(5)(30mg),ms:[m h]
=553.53da,准确分子量555.23da。
[0069]
mc-vk(peg4-glc)-pabc-mmae(linker2)的合成在200μl dmf中加入化合物6(5.5mg,0.01mmol)和hatu(7.6mg,0.02mmol),混匀后加入mc-vk-pabc-mmae(12.9mg,0.01mmol)和dipea(5μl,0.03mmol),室温搅拌反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末mc-vk(peg4-glc)-pabc-mmae(15mg)。ms:[m/2 h]
=913.01da,准确分子量1821.01da。
[0070]
实施例3 mc-vk(peg4-mal)-pabc-mmae的合成(图3)
[0071]
maltotriose-peg4 ser obzl的合成步骤一:在4ml d2o中加入d-麦芽三糖(100mg,0.2mmol),dipea(520μl,3mmol) 和nan3(650mg,10mmol)混匀后加入dmc(169mg,1mmol),室温搅拌反应 1h。lc-ms监测产物生成ms:[m na]
=552.16da,准确分子量529.18da。步骤二:在100μl dmf中加入l-ser-obzl.hcl(23.1mg,0.1mmol)和dipea(17μl, 0.1mmol)混匀后加入propargyl-peg4-nhs eater(40mg,0.11mmol)室温反应0.5h。 lc-ms监测产物生成。ms:[m h]
=438.45da,准确分子量437.20da。催化剂:7.5μl 200mm cuso4(0.0015mmol)加入45μl 200mm bttaa(0.009mmol) 混匀后加入20μl 1m vc-na(0.02mmol)步骤三:将步骤一和步骤二的反应液混合,加入催化剂后室温反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末maltotriose-peg4 ser obzl(6)(48mg),ms:[m h]
=967.38da。准确分子量966.38da。
[0072]
maltotriose-peg4 ser cooh(7)的合成化合物5用5ml(超纯水:甲醇=5:95)的溶液溶解,加入30mg 10%pd/c氢气搅拌催化3h,脱去羧基的保护基obzl。反应液过滤,加压蒸馏后即可获得透明油状产物。maltotriose-peg4 ser cooh(48mg)(7),ms:[m h] =878.38da,准确分子量876.33da。
[0073]
mc-vk(peg4-mal)-pabc-mmae(linker3)的合成在200ul dmf中加入化合物7(8.8mg,0.01mmol)和hatu(7.6mg,0.02mmol),混匀后加入mc-vk-pabc-mmae(12.9mg,0.01mmol)和dipea(5μl,0.03mmol),室温搅拌反应1h。反相半制备hplc纯化,含产物的洗脱液汇总,冻干后得到白色粉末mc-vk(peg4-mal)-pabc-mmae(18mg),ms:[m/2 h]
=1074.57da,准确分子量2145.11da。
[0074]
实施例4hplc分析抗体偶联药物:
[0075]
hic-hplc:疏水柱为赛默飞公司mabpac hic-butyl,5μm,4.6x100mm,流动相a为25mm khpo4,1.5mm(nh4)2so
4 ph=7,流动相b为25mm khpo4, ph=7。流速1ml/min,上样浓
度5mg/ml,上样体积:5μl,柱温25℃,时间程序:0-1min0%b;1-15min0%-100%b;15-20min100%b。
[0076]
sec-hplc:安捷伦1260hplc,sec柱为赛默飞公司mabpacsec-1,5μm,7.8x300mm,流动相a为pbs。流速1ml/min,上样浓度:1mg/ml,上样体积:10μl,室温,时间程序:0-25min100%a。稳定性实验的样品在60℃处理1h后上样。抗体或抗体偶联药物在4℃或60℃处理1h后上样。
[0077]
hic实验结果如图4所示,表明抗体偶联药物的dar值越为8,且使用糖基化修饰连接子-药物的抗体偶联药物的出峰时间相比hrs7-vc-mmae更早,疏水性有了明显改善,其中hrs7-vk(peg4-mal)-mmae水溶性最好;
[0078]
sec实验结果如图5所示,经过60℃加热处理1h的加速聚集实验,使用糖基化修饰连接子-药物的抗体偶联药物的疏水性相比hrs7-vc-mmae聚集明显减少,稳定性得到显著改善,其中hrs7-vk(peg4-mal)-mmae稳定性最好,与水溶性结果一致
[0079]
根据hic和sec的结果,选用表现最好的hrs7-vk(peg4-mal)-mmae作为候选分子进行进一步研究。
[0080]
实施例5酶联吸附免疫实验(elisa)
[0081]
包被:高亲和力的96孔板,每孔加入50μl2μg/ml的trop2,贴上封板膜4℃冰箱过夜;封闭:每孔加入50μl1%的casein,室温封闭1h,0.1%pbst洗3次;一抗孵育:加入合适浓度的抗体或者adc,1:3梯度稀释,每孔加入50μl,室温孵育1h,0.1%pbst洗3次;二抗孵育:每孔加入50μl1:2000稀释的goatanti-human-igg-hrp,室温孵育1h,0.1%pbst洗3次;显色:tmb溶液和h2o2按1:1的比例混合,每孔加入50μl,避光显色10min左右,加入50μl2mh2so4终止;读数:spectramaxm5e全自动酶标仪读取每孔的od
450
,数据用prism处理,得到ec
50
[0082]
elisa的结果表明,hrs7和hrs7-vk(peg4-mal)-mmae与人trop2结合的ec
50
值分别为0.34nm和0.88nm,两者亲和力相当;
[0083]
实施例6流式检测hrs7-vk(peg4-mal)-mmae内吞实验
[0084]
肿瘤细胞同5μg/ml的hrs7/hrs7-vk(peg4-mal)-mmae/isotypeigg1冰上孵育30min,pbs洗三次,分两组,一组37℃、5%co2恒温培养箱培养2.5h,一组冰上放置2.5h,然后5μg/mlpe-goat-anti-humanfc孵育半小时,pbs洗三次,流式细胞仪检测细胞表面荧光强度。
[0085]
内吞比率=(mfi
4s-mfi
37s
)/(mfi
4s-mfi
nc
)x100%
[0086]
其中mfi
4s
指4℃样品平均荧光强度;mfi
37s
指37℃样品平均荧光强度;mfi
nc
指阴性对照样品平均荧光强度
[0087]
实验结果如图7所示,显示hrs7-vk(peg4-mal)-mmae具有良好的内吞性能;
[0088]
流式检测多种肿瘤细胞trop2的表达
[0089]
肿瘤细胞同5μg/ml的hrs7/isotypeigg1冰上孵育30min,pbs洗三次,5μg/mlpe-goat-anti-humanfc孵育半小时,pbs洗三次,流式细胞仪检测细胞表面荧光强度。
[0090]
用相对平均荧光强度(relativemeanfluorescenceintensity,rmfi)表示细胞trop2表达水平:rmfi=(mfiofanti-trop2ab-pe)/(mfiofisotypecontrol-pe)x100%
[0091]
实验结果如图8所示,胰腺癌细胞系bxpc-3的rmfi为60.4,结直肠癌细胞系colo205的rmfi为9.9,小细胞肺癌细胞系nci-h1688的rmfi为1.0。
[0092]
实施例7细胞毒性实验,
[0093]
在96孔的细胞培养板中每孔加入5000-10000个细胞/100μl,37℃,5% co2培养箱中过夜生长,加入hrs7和hrs7-vk(peg4-mal)-mmae,1:3梯度稀释,3复孔,并设计空白对照,继续培养96小时以后,每孔加入100μl含有 10%cck-8的细胞培养液,37℃培养箱孵育2h,用spectramax m5e全自动酶标仪在450nm波长处,读取样品孔的吸光值,并计算细胞生存率;细胞生存率计算方法:
[0094]
存活率=(od
450sam-od450
bc
)/(od450
ab-od450
bc
)x100%
[0095]
其中od
450sam
实验组在450nm波长下的吸光值;od450
bc
空白对照在 450nm波长下的吸光值;od450
ab
单抗在450nm波长下的吸光值。
[0096]
实验结果如图8所示,hrs7-vk(peg4-mal)-mmae对3种细胞具有高活性,并且表现出了trop2表达依赖的杀伤能力,具有良好的活性和选择性。
[0097]
实例8 hrs7-vk(peg4-mal)-mmae裸鼠疗效实验
[0098]
首先建立了bxpc-3胰腺癌裸鼠肿瘤模型,在6-8周龄balb/c裸鼠右侧腋下接种5x106个细胞,等到肿瘤体积达到100-200mm3左右时进行随机分组,分为4组,包括3mg/kg hrs7阴性对照组,1mg/kg hrs7-vk(peg4-mal)-mmae 和3mg/kg hrs7-vk(peg4-mal)-mmae及17.5mg/kg的imm132阳性对照组。以后每隔3天左右用游标卡尺测量肿瘤的尺寸同时记录小鼠重量。肿瘤体积=lx ω2/2。l为最长的直径,ω是最短的直径。当肿瘤体积超过1000mm3时,结束实验。
[0099]
实验结果如图9所示,单剂量1mg/kg hrs7-vk(peg4-mal)-mmae就表现出来卓越的抗肿瘤效果,强于双剂量17.5mg/kg的阳性抗体imm132。进一步证明hrs7-vk(peg4-mal)-mmae巨大的临床潜力。
[0100]
以上所述,仅为本发明的较佳实施例,并非对本发明任何形式上和实质上的限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。凡熟悉本专业的技术人员,在不脱离本发明的精神和范围的情况下,当可利用以上所揭示的技术内容而做出的些许更动、修饰与演变的等同变化,均为本发明的等效实施例;同时,凡依据本发明的实质技术对上述实施例所作的任何等同变化的更动、修饰与演变,均仍属于本发明的技术方案的范围内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
