1.本发明涉及一种肟醚类1,3-环己二酮化合物及其合成方法和应用。具体地,涉及肟醚类1,3-环己二酮化合物,其用于防治植物中不希望杂草的用途,以及该类化合物的制备方法。
背景技术:
2.环己二酮类化合物是一大类具有除草、杀菌、杀虫等广泛生物活性的物质,其中除草活性最受人们关注。环己二酮类除草剂主要分为两类,其一为2-酰基-1,3-环己二酮类化合物,为hppd抑制剂,具有广谱的除草活性;其二为肟醚类1,3-环己二酮化合物,为accase抑制剂,用于防除一年生或多年生禾本科杂草。
3.已知包含环己二酮结构的化合物有烯草酮、烯禾啶、禾草灭、噻草酮、丁氧环酮、三甲苯草酮、吡喃草酮和环苯草酮。但是由于长期使用,在很多杂草上都产生了抗性。本领域剂技术人员一直在寻找合适的替代农药除草剂。
4.现有专利文献1(cn105884665b)公开了一种环己烯酮类化合物及其制备方法与应用,其中公开的化合物结构如下:发现该化合物对稗草和千金子具有较好的防治效果,同时对水稻具有较高的安全性。
5.申请人公开的专利(cn1120528a)中公开了一类环己烷-1,3-二酮类化合物及其合成方法和应用,其中化合物的结构如下:其中公开的化合物e1:表现出具有较好的除草效果和对作物的安全性。
6.申请人公开的专利(cn114105842a)公开了一类环己二烯肟醚类化合物及其应用,其中化合物5表现出较为优异的除草效果。化合物5的结构如下:
7.8.此外,国内公司推出的苯丙草酮,
9.其对抗性稗草的防除效果不佳。
10.目前,这些已知化合物对于有害植物的除草性能,特别是抗性杂草的除草性能并不完全令人满意,同时,对作物的安全性也有待提高。
11.因此,本发明的目的是提供具有改进除草作用的肟醚类1,3-环己二酮化合物。尤其是要提供具有高除草活性,特别是在低施用率下也具有高除草活性,对抗性杂草除草效果也十分优异,并且对农作物具有高度安全性的肟醚类1,3-环己二酮化合物。
技术实现要素:
12.本发明的目的是提供一类新的肟醚类1,3-环己二酮化合物,其相对于现有已知的研发化合物在小剂量施用时即具有较高的除草活性,同时,对植物作物有高度的选择性和相容性,体现出较好的安全性,对已有肟醚类1,3-环己二酮化合物类除草剂,例如,苯丙草酮、烯草酮等产抗性的杂草具有较好的防除效果。可以广泛应用于农业、林业及果园的杂草防治。
13.本发明提供一种式i所示的肟醚类1,3-环己二酮化合物,
[0014][0015]
其中:
[0016]
r1为h、任选取代的c
1-c6烷基、任选取代的c
1-c6烷氧基、任选取代的c
1-c6硫基、任选取代的c
1-c6烷氧基-c
1-c6烷基、任选取代的c
1-c6烷硫基-c
1-c6烷基、任选取代的c
3-c6环烷基、任选取代的c
3-c6环烷基氧基-c
1-c6烷基、任选取代的c
3-c6环烷基硫基-c
1-c6烷基、任选取代的杂环基;
[0017]
r2为任选取代的c
1-c6烷基、任选取代的c
3-c6环烷基;
[0018]
r3为任选取代的c
1-c6烷基、任选取代的c
2-c6烯基、任选取代的c
3-c6环烷基;
[0019]
r4为h、任选取代的苯基,任选取代的杂环基、任选取代的c
2-c6烯基;
[0020]
也包括式i化合物的非对映异构体、对映异构体和旋转异构体和其可农用的盐。
[0021]
本发明还提供了一种式i化合物的制备方法。
[0022]
本发明还提供了一种除草组合物,包含式i化合物。
[0023]
本发明还提供了式i化合物作为除草剂,防治不希望的植物的用途。
[0024]
此外,本发明还提供一种防治不希望的植物生长的方法,其中使除草有效量的至少一种式i的化合物作用于植物,其种子和/或其生长地。施用可以在不希望的植物出苗之前、之中和/或之后进行。
[0025]
此外,本发明涉及制备式i的方法和中间体。
乙基丁基、1,1,2-三甲基丙基、1,2,2-三甲基丙基、1-乙基-1-甲基丙基或1-乙基-2-甲基丙基。
[0042]
术语“任选取代”指相关基团可以被取代基取代,也可不被取代。
[0043]
当相关基团(如烷基)被取代基取代时,所述的取代基可以包括羟基、氰基、硝基、卤素和烷基。烷基被卤素取代时,形成卤代烷基。
[0044]
本发明术语“环”或“环烷基”在每种情况下表示通常具有3~6个碳原子(“c3~c6环烷基”)的单环或双环脂环族基团。具有3~6个碳原子的单环基团示例包括环丙基、环丁基、环戊基和环己基。
[0045]c2-c6烯基,例如,乙烯基、1-丙烯基、2-丙烯基、1-甲基乙烯基、1-丁烯基、2-丁烯基、3-丁烯基、1-甲基-1-丙烯基、2-甲基-1-丙烯基、1-甲基-2-丙烯基、2-甲基-2-丙烯基、1-戊烯基、2-戊烯基、3-戊烯基、4-戊烯基、1-甲基-1-丁烯基、2-甲基-1-丁烯基、3-甲基-1-丁烯基、1-甲基-2-丁烯基、2-甲基-2-丁烯基、3-甲基-2-丁烯基、1-甲基-3-丁烯基、2-甲基-3-丁烯基、3-甲基-3-丁烯基、1,1-二甲基-2-丙烯基、1,2-二甲基-1-丙烯基、1,2-二甲基-2-丙烯基、1-乙基-1-丙烯基、1-乙基-2-丙烯基、1-己烯基、2-己烯基、3-己烯基、4-己烯基、5-己烯基、1-甲基-1-戊烯基、2-甲基-1-戊烯基、3-甲基-1-戊烯基、4-甲基-1-戊烯基、1-甲基-2-戊烯基、2-甲基-2-戊烯基、3-甲基-2-戊烯基、4-甲基-2-戊烯基、1-甲基-3-戊烯基、2-甲基-3-戊烯基、3-甲基-3-戊烯基、4-甲基-3-戊烯基、1-甲基-4-戊烯基、2-甲基-4-戊烯基、3-甲基-4-戊烯基、4-甲基-4-戊烯基、1,1-二甲基-2-丁烯基、1,1-二甲基-3-丁烯基、1,2-二甲基-1-丁烯基、1,2-二甲基-2-丁烯基、1,2-二甲基-3-丁烯基、1,3-二甲基-1-丁烯基、1,3-二甲基-2-丁烯基、1,3-二甲基-3-丁烯基、2,2-二甲基-3-丁烯基、2,3-二甲基-1-丁烯基、2,3-二甲基-2-丁烯基、2,3-二甲基-3-丁烯基、3,3-二甲基-1-丁烯基、3,3-二甲基-2-丁烯基、1-乙基-1-丁烯基、1-乙基-2-丁烯基、1-乙基-3-丁烯基、2-乙基-1-丁烯基、2-乙基-2-丁烯基、2-乙基-3-丁烯基、1,1,2-三甲基-2-丙烯基、1-乙基-1-甲基-2-丙烯基、1-乙基-2-甲基-1-丙烯基和1-乙基-2-甲基-2-丙烯基。
[0046]c3-c6卤代链烯基:部分或全部被氟、氯、溴和/或碘取代的如上所述的c
3-c6链烯基,例如2-氯丙-2-烯-1-基、3-氯丙-2-烯-1-基、3-氯丙-1-烯基、2,3-二氯丙-2-烯-1-基、3,3-二氯丙-2-烯-1-基、2,3,3-三氯丙-2-烯-1-基、2,3-二氯丁-2-烯-1-基、2-溴丙-2-烯-1-基、3-溴丙-2-烯-1-基、2,3-二溴丙-2-烯-1-基、3,3-二溴丙-2-烯-1-基、2,3,3-三溴丙-2-烯-1-基或2,3-二溴丁-2-烯-1-基。
[0047]c1-c6烷氧基-c
1-c6烷基、c
1-c6烷硫基-c
1-c6烷基的c
1-c6烷基结构部分:例如甲基、乙基、正丙基、异丙基、正丁基、1-甲基丙基(仲丁基)、2-甲基丙基(异丁基)、1,1-二甲基乙基(叔丁基)、正戊基、1-甲基丁基、2-甲基丁基、3-甲基丁基、2,2-二甲基丙基、1-乙基丙基、1,1-二甲基丙基、1,2-二甲基丙基、己基、1-甲基戊基、2-甲基戊基、3-甲基戊基、4-甲基戊基、1,1-二甲基丁基、1,2-二甲基丁基、1,3-二甲基丁基、2,2-二甲基丁基、2,3-二甲基丁基、3,3-二甲基丁基、1-乙基丁基、2-乙基丁基、1,1,2-三甲基丙基、1,2,2-三甲基丙基、1-乙基-1-甲基丙基或1-乙基-2-甲基丙基。
[0048]
杂环基:具有3个或更多个,例如3-10个环原子单环或双环饱和、部分不饱和或芳族杂环,例如,含有1-4个选自氧、硫和氮的相同或不同杂原子的3、4、5、6、7元杂环,例如:
[0049]
其中p选自h、-ch3、-c2h5、-c3h7、-cl、-f、-br、-i、-cn、-no2或-cf3,x为氧、硫和氮,y为c
1-c3烷基,n为0-3的整数。
[0050]
下面关于式(i)化合物的变量的及变量的优选实施方案、本发明的用途和方法的特征以及本发明组合物的特征所作描述无论是其自身还是优选相互组合都是有效的。
[0051]
本发明总的方面提供一种式i所示的肟醚类1,3-环己二酮化合物,
[0052][0053]
其中:
[0054]
r1为h、任选取代的c
1-c6烷基、任选取代的c
1-c6烷氧基、任选取代的c
1-c6硫基、任选取代的c
1-c6烷氧基-c
1-c6烷基、任选取代的c
1-c6烷硫基-c
1-c6烷基、任选取代的c
3-c6环烷基、任选取代的c
3-c6环烷基氧基-c
1-c6烷基、任选取代的c
3-c6环烷基硫基-c
1-c6烷基、任选取代的杂环基;
[0055]
r2为任选取代的c
1-c6烷基、任选取代的c
3-c6环烷基;
[0056]
r3为任选取代的c
1-c6烷基、任选取代的c
2-c6烯基、任选c
3-c6环烷基;
[0057]
r4为h、任选取代的c
2-c6烯基、任选取代的苯基,任选取代的杂环基;
[0058]
也包括式i化合物的非对映异构体、对映异构体和旋转异构体和其可农用的盐。
[0059]
根据本发明的一个实施方案,式i化合物中的r1为-h、-ch3、-c2h5、-c3h7、-c4h9、-c5h
11
、-c6h
13
、-q-ch3、-q-c2h5、-ch
2-q-ch3、-q-c3h7、-c2h
4-q-ch3、-ch
2-q-c2h5、-q-c4h9、-ch
2-q-c3h7、-c2h
4-q-c2h5、-c3h
6-q-ch3、-q-c5h
11
、-ch
2-q-c4h9、-ch
2-q-c4h9、-c2h
4-q-c3h7、-c3h
6-q-c2h5、-c4h
8-q-ch3、-q-c6h
13
、-ch
2-q-c5h
11
、-c2h
4-q-c4h9、-c3h
6-q-c3h7、-c4h
8-q-c2h5、-c5h
10-q-ch3、其中x为c、o或者s;q为o或者s。
[0060]
根据本发明的一个实施方案,式i化合物中的r1为-ch3、-ch2ch2ch3、-ch2ch2ch2ch3、-ch
2-o-ch2ch3、-ch2ch
2-s-ch3、-ch
2-o-ch(ch3)2、-ch2ch(ch3)sch2ch3、
[0061]
根据本发明的一个实施方案,式i化合物中的r2为-ch3、-c2h5、-c3h7、-c4h9、-c5h
11
、-c6h
13
、其中n选自0-3的整数,y为c
1-c3的烷基。
[0062]
根据本发明的一个实施方案,式i化合物中的r2为-ch3、-ch2ch3、-ch2ch2ch3、-ch
(ch3)ch2ch3、-ch(ch3)2、-ch(ch3)ch(ch3)ch3、-ch2ch2ch(ch3)2。
[0063]
根据本发明的一个实施方案,式(i)化合物中r3选自-ch3、-c2h5、-c3h7、-c4h9、-c5h
11
、-c6h
13
、-ch=chch3、-ch2ch=ch2、-ch2ch=chz、-ch=chch2z、其中z选自f、cl、br、i,n选自0-3的整数,y为c
1-c3的烷基。
[0064]
根据本发明的一个实施方案,式i化合物中的r3选自-ch2ch=ch2、-ch2ch=chcl、-ch3、-ch2ch3、-ch2ch2ch3、-ch(ch3)2、-ch=chch3、-ch=chch2cl、-ch2ch2ch2ch3。
[0065]
根据本发明的一个实施方案,式i化合物中的r4选自-h、-ch2ch=ch2、-ch2ch=chz、
[0066]
其中,p选自h、-ch3、-c2h5、-c3h7、-cl、-f、-br、-i、-cn、-no2或-cf3,n=0-3,z为f、cl、br、i。
[0067]
本发明特别优选的化合物如下:
[0068]
[0069][0070]
本发明另一方面还提供一种式i化合物的制备方法,包括如下步骤:式ii和式iii化合物在酸性条件下制备得到式i化合物,化合物在酸性条件下制备得到式i化合物,其中r2、r3、r4如上定义;
[0071]
优选的上述反应在有机溶剂中进行,所述的有机溶剂选自二氯甲烷、二氯乙烷、丙酮、甲苯、dmf、石油醚和甲醇中一种,所述的酸选自有机酸,优选甲酸和乙酸。上述反应的反应温度在0~100℃范围内,反应时间为1-10h范围内,优选1~3h;
[0072]
进一步的,上述式iii化合物通过式iv化合物和水合肼反应得到,反应在有机溶剂中进行,所述的有机溶剂选自二氯甲烷、二氯乙烷中一种,反应在0~80℃下反应1~3h,反应结束后加水萃取,取有机层浓缩得到化合物ⅲ;
[0073][0074]
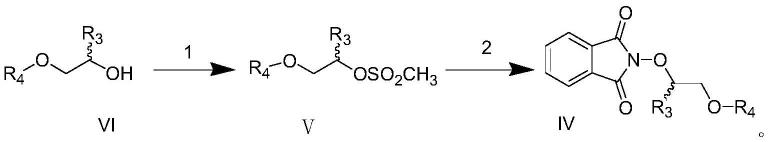
进一步的,上述式iv化合物合成包括如下步骤:
[0075]
步骤1:式vi化合物制备得到式v化合物;
[0076]
步骤2:式v化合物制备得到式iv化合物,其反应路线如下:
[0077][0078]
其中步骤1包括,将vi化合物和碱加入到有机溶剂中,在-20-40℃下滴加甲基磺酰氯制备化合物
ⅴ
。其中所述的有机溶剂选自二氯甲烷、二氯乙烷、石油醚、乙酸乙酯、丙酮、甲苯中一种,所述的碱选自碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、三乙胺、氢氧化钠、氢氧化钾中一种。
[0079]
步骤2包括,将化合物v和n-羟基邻苯二甲酰亚胺加入有机溶剂中,溶解后加入碱,在40-100℃反应制备化合物ⅳ。所述的有机溶剂选自dmf、乙腈、1,4-二氧六环、n-甲基吡咯
烷酮、n、n-二甲基乙酰胺中一种,所述的碱选自碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、氢氧化钠、氢氧化钾中一种。
[0080]
由于本发明通式i化合物具有优异的除草活性和作物的安全性,本发明的式i化合物适用于农业、林业、园艺业的植物保护和不希望植物的防治。本发明化合物对其有防效功效的有害生物包括,例如,有害螨虫以及线虫。有害的生物的具体示例有如下害虫(所列对象仅用于说明本发明,但没有限定本发明的保护范围)。
[0081]
本发明式i化合物可以通过防杂草有效量的活性化合物防治杂草。
[0082]
本发明的除草组合物通常含0.1~95wt%,优选0.5~90wt%的式(i)化合物。当将含本发明的化合物的试剂用于防除不希望的植物和杂草时,按照本发明式i化合物计的施用量通常选择每公顷0.01~1000g,优选有效量为每公顷0.01~500g。本发明式i优选化合物,例如,化合物1-12在0.5g/亩的剂量下就可以具有较好的对杂草杀死效果,特别优选的化合物在0.01g/亩的剂量下就有较好的对杂草杀死效果。当将含式i化合物的农药组合物用于防除杂草的剂型为乳油剂、可湿性粉剂或微乳剂等时,通常通过将含有本发明式i化合物的制剂用水稀释成活性成分的浓度在0.01至5000ppm的范围内来施用。颗粒剂或粉剂等可以不经稀释进行施用。研究结果表明,本发明的式(i)化合物在浓度0.01至100ppm(0.01mg/l至100mg/l)的范围内对某些杂草和抗性杂草具有至少90%的杀死效果。优选的化合物在0.1ppm至100ppm的范围内对某些杂草和抗性具有至少90%的杀死效果。
[0083]
可以将式(i)化合物通过常规的配制方法制成常规的制剂,例如乳油剂、油溶液剂、粉剂、颗粒剂、可湿性粉剂、流动剂、微胶囊、气雾剂、发烟剂、毒饵等等。使用形式取决于特定的使用目的。
[0084]
配制制剂使用常规的已知方式进行制备,例如通过将活性化合物与溶剂和/或载体混合而制备,如果需要可以加入适宜的乳化剂和分散剂或其它常用的助剂。
[0085]
本发明的用于防除有害植物的试剂包含本发明化合物和惰性载体。本文使用的惰性载体表示增量剂、稀释剂和在农业领域中使用的制剂。通常通过将本发明化合物与惰性载体如固体载体、液体载体或气体载体混合,以制备本发明的用于防治有害植物的试剂,并且如果需要,加入表面活性剂和其他制剂用辅助剂,以制成为乳油剂、油溶液剂、粉剂、颗粒剂、可湿性粉剂、流动剂、微胶囊、气雾剂、发烟剂、毒饵等等。
[0086]
农药组合物支撑制剂中所用的固体载体的实例包括:粘土的细粉或颗粒(例如高岭土粘土、硅藻土、膨润土)、合成含水氧化硅、滑石、陶瓷、其他无机材料(例如石英、硫、活性碳、碳酸钙或水合二氧化硅)、化学肥料(例如硫酸铵、磷酸铵、硝酸铵、脲或氯化铵)以及合成树脂(例如聚酯树脂如聚丙烯、聚丙烯腈、聚甲基丙烯酸甲酯和聚对苯二甲酸乙二醇酯、尼龙树脂、聚酰胺树脂、聚氯乙烯、聚偏二氯乙烯、氯乙烯-丙烯共聚物)等等。
[0087]
上述液体载体的实例包括:水、醇(例如甲醇、乙醇、异丙醇、丁醇、己醇、苄醇、乙二醇、丙二醇或苯氧基乙醇)、酮(例如丙酮、甲基乙基酮或环己酮)、芳族烃(例如甲苯、二甲苯、乙苯、十二烷基苯、苯基二甲苯基乙烷或甲基萘);脂族烃(例如己烷、环己烷、煤油或轻油)、酯(例如乙酸乙酯、乙酸丁酯、肉豆蔻酸异丙酯、油酸乙酯、己二酸二异丙酯、己二酸二异丁酯或丙二醇单甲醚乙酸酯、碳酸丙二酯)、腈(例如乙腈或异丁腈)、醚(例如二异丙醚、1,4-二烷、乙二醇二甲醚、二甘醇二甲醚、二甘醇单甲醚、丙二醇单甲醚、二丙二醇单甲醚或3-甲氧基-3-甲基-1-丁醇)、酰胺(例如n,n-二甲基甲酰胺或n,n-二甲基乙酰胺)、卤代烃
15℃下滴加8.3g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤,取滤液用盐酸水溶液萃取,取有机层浓缩得到15.9g目标产物;
[0099]
1.2合成o-[1-(4-甲基-苯氧甲基)-丁-3-烯基]-羟胺
[0100]
向dmf中加入15.9g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入7.6g碳酸钠,在40℃反应2h,然后向体系中加入二氯甲烷,滴加10.8g 50%的水合肼,滴加完毕后在5℃下反应3h,反应结束后加水萃取,取有机层浓缩得到11.2g目标产物;
[0101]
1.3合成2-{1-[1-(4-甲基-苯氧甲基)-丁-3-烯氧基亚氨基]-乙基}-3-羟基-5-甲基-环己-2-烯酮
[0102]
用二氯甲烷溶解11.2g上步产物和9.3g 2-乙酰-3-羟基-5-甲基-环己-2-烯酮,加入5.4g乙酸催化,35℃反应2h,反应结束后除去溶剂得到18.6g目标产物,总收率87%。
[0103]
1h nmr(300mhz,cdcl3):δ14.68(br,1h),δ6.95-7.10(d,2h),δ6.68-6.74(d,2h),δ5.06-5.54(m,3h),δ4.51-4.58(m,1h),δ4.01-4.06(d,2h),δ2.39-2.96(m,4h),δ2.17-2.35(m,6h),δ1.81-1.92(s,3h),δ0.98-1.02(d,3h)
[0104]
实施例2化合物2(z)-2-{1-[4-氯-1-(3-氯-5-氟-苯氧基甲基)-丁-3-烯氧基亚氨基]-丙基}-3-羟基-5-丙基-环己-2-烯酮
[0105][0106]
2.1合成甲基磺酸(z)-4-氯-1-(3-氯-5-氟-苯氧基甲基)-丁-3-烯基酯
[0107]
向二氯乙烷中加入15.9g(z)-5-氯-1-(3-氯-5-氟-苯氧基)-戊-4-烯-2-醇和16.6g碳酸钾,在10℃下滴加7.6g甲基磺酰氯,滴加完毕后反应2h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到19.9g目标产物;
[0108]
2.2合成(z)-o-[4-氯-1-(3-氯-5-氟-苯氧甲基)-丁-3-烯基]-羟胺
[0109]
向乙腈中加入19.9g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入8.3g碳酸钾,在60℃反应3h,降至室温后,向反应体系中加入二氯乙烷,然后滴加7.5g 80%的水合肼,滴加完毕后在20℃下反应3h,反应结束后加水萃取,取有机层浓缩得到15.1g目标产物;
[0110]
2.3合成(z)-2-{1-[4-氯-1-(3-氯-5-氟-苯氧基甲基)-丁-3-烯氧基亚氨基]-丙基}-3-羟基-5-丙基-环己-2-烯酮
[0111]
用二氯乙烷溶解15.1g上步产物和12.6g 3-羟基-2-丙酰基-5-丙基-环己-2-烯酮,加入2.8g甲酸催化,70℃反应2h,反应结束后除去溶剂得到23.6g目标产物,总收率83%。
[0112]
1h nmr(300mhz,cdcl3):δ14.81(br,1h),δ6.46-7.79(m,3h),δ5.84-6.14(m,2h),δ4.48-4.51(m,1h),δ3.96-4.15(d,2h),δ2.64-2.99(m,4h),δ2.12-2.41(m,3h),δ1.21-1.71(m,6h),δ0.94-1.06(m,6h)
[0113]
实施例3化合物3(r)-4-{2-[1-(4-丁基-2-羟基-6-氧代-环己-1-烯基)-丁酰氨基氧基]-丙氧基}-苯甲腈
[0114][0115]
3.1合成(r)-甲基磺酸2-(4-氰基苯氧基)-1-甲基乙酯
[0116]
向石油醚中加入10.6g(r)-4-(2-羟基丙氧基)-苯甲腈和15.1g碳酸氢钠,在35℃下滴加6.9g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用硫酸水溶液萃取,取有机层浓缩得到15.0g目标产物;
[0117]
3.2合成(r)-4-(2-氨基氧基-丙氧基)-苯甲腈
[0118]
向1,4-二氧六环中加入15.0g上步产物、11.7gn-羟基邻苯二甲酰亚胺,溶解后加入14.1g碳酸氢钠,在95℃反应2h,反应结束后降至室温,向反应体系中加入二氯乙烷,然后滴加12.5g 60%的水合肼,滴加完毕后在80℃下反应1h,反应结束后加水萃取,取有机层浓缩得到10.6g目标产物;
[0119]
3.3合成(r)-4-{2-[1-(4-丁基-2-羟基-6-氧代-环己-1-烯基)-丁酰氨基氧基]-丙氧基}-苯甲腈
[0120]
用甲苯溶解10.6g上步产物和15.7g 5-丁基-2-丁基-3-羟基-环己-2-烯酮,加入4.3g乙酸催化,90℃反应1h,反应结束后除去溶剂得到22.3g目标产物,总收率90%。
[0121]
1h nmr(300mhz,cdcl3):δ14.67(br,1h),δ7.45-7.52(d,2h),δ6.88-6.94(d,2h),δ4.45-4.52(m,1h),δ3.90-4.07(d,2h),δ2.58-2.97(m,4h),δ2.20-2.39(m,1h),δ1.23-1.62(m,13h),δ0.98-1.02(m,6h)
[0122]
实施例4化合物4(s)-5-乙氧基甲基-3-羟基-2-{2-甲基-1-[1-(3-三氟甲基-苯氧基甲基)-丙氧基亚氨基]-丁基}-环己-2-烯酮
[0123][0124]
4.1合成(s)-甲基磺酸1-(3-三氟甲基-苯氧甲基)-丙酯
[0125]
向乙酸乙酯中加入14.1g(s)-1-(3-三氟甲基-苯氧基)-丁醇和7.2g碳酸氢钾,在15℃下滴加6.9g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到18.4g目标产物;
[0126]
4.2合成(s)-o-[1-(3-三氟甲基-苯氧甲基)-丙基]-羟胺
[0127]
向n-甲基吡咯烷酮中加入18.4g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入6.6g碳酸氢钾,在50℃反应5h,反应结束后降至室温,向反应体系中加入溶剂二氯乙烷,然后滴加5.7g 85%的水合肼,滴加完毕后60℃下反应3h,反应结束后加水萃取,取有机层浓缩得到13.5g目标产物;
[0128]
4.3合成(s)-5-乙氧基甲基-3-羟基-2-{2-甲基-1-[1-(3-三氟甲基-苯氧基甲基)-丙氧基亚氨基]-丁基}-环己-2-烯酮
[0129]
用丙酮溶解13.5g上步产物和15.2g 5-乙氧基甲基-3-羟基-2-(2-甲基-丁基)-环
己-2-烯酮,加入3.6g乙酸催化,50℃反应3h,反应结束后除去溶剂得到24.7g目标产物,总收率85%。
[0130]
1h nmr(300mhz,cdcl3):δ14.53(br,1h),δ6.77-7.12(m,4h),δ4.42-4.49(m,1h),δ3.93-4.01(d,2h),δ3.31-3.50(m,4h),δ2.54-2.93(m,4h),δ2.11-2.19(m,1h),δ1.11-1.71(m,11h),δ0.96-1.04(m,6h)
[0131]
实施例5化合物52-{[1-(4-氯-吡啶-2-氧基甲基)-丁氧基亚氨基]-环丙基甲基}-3-羟基-5-(2-甲基磺胺基乙基)-环己-2-烯酮
[0132][0133]
5.1合成甲基磺酸1-(4-氯-吡啶-2-氧甲基)丁酯
[0134]
向丙酮中加入12.9g 1-(4-氯-吡啶-2-氧基)-戊烷-2-醇和6.7g三乙胺,在0℃下滴加7.8g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到17.3g目标产物;
[0135]
5.2合成o-[1-(4-氯-吡啶-2-氧基甲基)-丁基]-羟胺
[0136]
向n,n-二甲基乙酰胺中加入17.3g上步产物、11.7gn-羟基邻苯二甲酰亚胺,溶解后加入3.1g氢氧化钠,在40℃反应3h,反应结束后,向反应体系中加入二氯乙烷,然后滴加9.4g 80%水合肼,滴加完毕后在60℃下反应2.5h,反应结束后加水萃取,取有机层浓缩得到13.0g目标产物;
[0137]
5.3合成2-{[1-(4-氯-吡啶-2-氧基甲基)-丁氧基亚氨基]-环丙基甲基}-3-羟基-5-(2-甲基磺胺基乙基)-环己-2-烯酮
[0138]
用溶剂dmf溶解13.0g上步产物和19.5g 2-环丙烷羰基-3-羟基-5-(2-甲基硫基乙基)-环己-2-烯酮,加入5.4g乙酸催化,70℃反应2h,反应结束后除去溶剂得到25.7g目标产物,总收率92%。
[0139]
1h nmr(300mhz,cdcl3):δ14.59(br,1h),δ8.21-8.24(d,1h),δ6.90-6.94(m,2h),δ3.76-4.25(m,3h),δ2.44-2.84(m,6h),δ2.09-2.13(m,1h),δ1.33-1.89(m,9h),δ0.88-1.01(m,8h)
[0140]
实施例6化合物62-[(1-烯丙基氧基甲基-2-甲基丙氧基亚氨基)-(2-甲基环丙基)-甲基]-3-羟基-5-异丙氧基甲基-环己-2-烯酮
[0141][0142]
6.1合成基磺酸1-烯丙基氧基甲基-2-甲基丙基酯
[0143]
向甲苯中加入8.7g 1-烯丙基氧基-3-甲基-丁烷-2-醇和7.3g三乙胺,在-10℃下滴加8.4g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到12.7g目标产物;
[0144]
6.2合成o-(1-烯丙基氧基甲基-2-甲基丙基)-羟胺
[0145]
向溶剂n,n-二甲基乙酰胺中加入12.7g上步产物、9.8gn-羟基邻苯二甲酰亚胺,溶解后加入4.0g氢氧化钾,在50℃反应1h,反应结束后,降至室温向反应体系中加入二氯甲烷,然后滴加9.8g 40%水合肼,滴加完毕后在30℃下反应1.5h,反应结束后加水萃取,取有机层浓缩得到7.8g目标产物。
[0146]
6.3合成2-[(1-烯丙基氧基甲基-2-甲基丙氧基亚氨基)-(2-甲基环丙基)-甲基]-3-羟基-5-异丙氧基甲基-环己-2-烯酮
[0147]
用石油醚溶解7.8g上步产物和13.1g 3-羟基-5-异丙氧基甲基-2-(2-甲基-环丙基甲基)-环己-2-烯酮,加2.8g甲酸催化,60℃反应1.5h,反应结束后除去溶剂得到19.1g目标产物,总收率78%。
[0148]
1h nmr(300mhz,cdcl3):δ14.43(br,1h),δ5.23-5.69(m,3h),δ4.21-4.28(m,3h),δ3.98-4.04(d,2h),δ3.33(d,2h),δ2.35-2.96(m,5h),δ2.05-2.18(m,1h),δ1.01-1.78(m,16h),δ0.84-0.99(m,4h)
[0149]
实施例7化合物72-{1-[2-(4-氯-苯氧基)-1-甲基-乙氧基亚氨基]-丙基}-5-(2-乙基硫基-丙基)-3-羟基-环己-2-烯酮
[0150][0151]
7.1合成甲基磺酸2-(4-氯-苯氧基)-1-甲基乙酯
[0152]
向丙酮中加入22.4g 1-(4-氯-苯氧基)-丙烷-2-醇和18.2g三乙胺,在15℃下滴加15.3g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到31.1g目标产物;
[0153]
7.2合成o-[2-(4-氯-苯氧基)-1-甲基乙基]-羟胺
[0154]
向溶剂dmf中加入31.1g上步产物、21.5gn-羟基邻苯二甲酰亚胺,溶解后加入14.4g氢氧化钠,在60℃反应1h,反应结束后,降至室温,向反应体系中加入二氯乙烷,然后滴加15.4g 70%水合肼,滴加完毕后在50℃下反应2h,反应结束后加水萃取,取有机层浓缩得到21.9g目标产物;
[0155]
7.3合成2-{1-[2-(4-氯-苯氧基)-1-甲基-乙氧基亚氨基]-丙基}-5-(2-乙基硫基-丙基)-3-羟基-环己-2-烯酮
[0156]
用二氯乙烷溶解11.0g上步产物和17.8g 5-(2-乙基硫基-丙基)-3-羟基-2-丙酰基-环己-2-烯酮,加入7.2g乙酸催化,80℃反应2h,反应结束后除去溶剂得到24.2g目标产物,总收率89%。
[0157]
1h nmr(300mhz,cdcl3):δ14.52(br,1h),δ7.28-7.32(d,2h),δ6.88-6.91(d,2h),δ4.51-4.58(m,1h),δ3.99-4.06(d,2h),δ2.38-2.89(m,7h),δ2.07-2.15(m,1h),δ1.20-1.58(m,13h),δ0.99-1.04(t,3h)
[0158]
实施例8化合物82-{1-[2-(4-氯-苯氧基)-1-甲基-乙氧基亚氨基]-丁基}-5-(2-乙基硫基-丙基)-3-羟基-环己-2-烯酮
[0159][0160]
8.1合成2-{1-[2-(4-氯-苯氧基)-1-甲基-乙氧基亚氨基]-丁基}-5-(2-乙基硫基-丙基)-3-羟基-环己-2-烯酮
[0161]
用石油醚溶解10.9g o-[2-(4-氯-苯氧基)-1-甲基乙基]-羟胺和17.6g 2-丁基-5-(2-乙基硫基-丙基)-3-羟基-环己-2-烯酮,加入4g乙酸催化,80℃反应3h,反应结束后除去溶剂得到24.8g目标产物,收率98%。
[0162]
1h nmr(300mhz,cdcl3):δ14.51(br,1h),δ7.22-7.26(d,2h),δ6.85-6.87(d,2h),δ4.49-4.54(m,1h),δ3.98-4.03(d,2h),δ2.33-2.86(m,7h),δ2.07-2.15(m,1h),δ1.23-1.59(m,15h),δ0.91-0.96(t,3h)
[0163]
实施例9化合物94-{2-[1-(2-羟基-4-环氧乙烷基-6-氧代-环己-1-烯基)-丁酰氨基氧基]-戊-3-烯氧基}-苯甲腈
[0164][0165]
9.1合成甲基磺酸1-(4-氰基-苯氧基甲基)-丁-2-烯基酯
[0166]
向溶剂二氯乙烷中加入12.2g 4-(2-羟基-戊-3-烯氧基)-苯甲腈和5.4g氢氧化钾,在35℃下滴加7.6g甲基磺酰氯,滴加完毕后反应1.5h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到16.0g目标产物;
[0167]
9.2合成4-(2-氨基氧基-戊-3-烯氧基)-苯甲腈
[0168]
向dmf中加入16.0g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入4.0g氢氧化钾,在45℃反应3h,反应结束后向反应体系中加入二氯乙烷,然后滴加9.0g 50%的水合肼,滴加完毕后在50℃下反应2h,反应结束后加水萃取,取有机层浓缩得到11.1g目标产物;
[0169]
9.3合成4-{2-[1-(2-羟基-4-环氧乙烷基-6-氧代-环己-1-烯基)-丁酰氨基氧基]-戊-3-烯氧基}-苯甲腈
[0170]
用甲醇溶解11.1g上步产物和13.4g 2-丁基-3-羟基-5-环氧乙烷基-环己-2-烯酮,加入3.9g乙酸催化,60℃反应1.5h,反应结束后除去溶剂得到20.6g目标产物,总收率81%。
[0171]
1h nmr(300mhz,cdcl3):δ14.66(br,1h),δ7.42-7.56(d,2h),δ6.95-7.02(d,2h),δ5.52-5.69(m,2h),δ4.75-4.89(m,1h),δ4.02-4.13(d,2h),δ2.53-2.96(m,8h),δ1.47-1.72(m,7h),δ0.99(t,3h)
[0172]
实施10化合物102-{1-[4-氯-1-(4-硝基-苯氧基甲基)-丁-2-烯氧基亚氨基]-2-甲基丙基}-3-羟基-5-(2-甲基-环丙基磺胺甲基)-环己-2-烯酮
[0173][0174]
10.1合成甲基磺酸4-氯-1-(4-硝基苯氧基甲基)-丁-2-烯基酯
[0175]
向二氯甲烷中加入15.5g 5-氯-1-(4-硝基苯氧基)-戊-3-烯-2-醇和7.2g碳酸氢钾,在-5℃下滴加7.6g甲基磺酰氯,滴加完毕后反应2h,反应结束后抽滤取滤液,用硫酸水溶液萃取,取有机层浓缩得到19.7g目标产物;
[0176]
10.2合成o-[4-氯-1-(4-硝基-苯氧甲基)-丁-2-烯基]-羟胺
[0177]
向1,4-二氧六环中加入19.7g上步产物、10.8gn-羟基邻苯二甲酰亚胺,溶解后加入10.2g碳酸钠,在60℃反应4h,反应结束后降至室温,向反应体系中加入二氯乙烷,然后滴加6.5g 60%水合肼,滴加完毕后在70℃下反应3h,反应结束后加水萃取,取有机层浓缩得到14.8g目标产物;
[0178]
10.3合成2-{1-[4-氯-1-(4-硝基-苯氧基甲基)-丁-2-烯氧基亚氨基]-2-甲基丙基}-3-羟基-5-(2-甲基-环丙基磺胺甲基)-环己-2-烯酮
[0179]
用石油醚溶解14.8g上步产物和17.0g 3-羟基-2-异丁基-5-(2-甲基-环丙基硫基甲基)-环己-2-烯酮,加入7.2g乙酸催化,70℃反应2h,反应结束后除去溶剂得到28.5g目标产物,总收率88%。
[0180]
1h nmr(300mhz,cdcl3):δ14.49(br,1h),δ8.02-8.13(d,2h),δ7.11-7.24(d,2h),δ5.84-5.96(m,2h),δ4.65-4.93(m,3h),δ4.09-4.15(d,2h),δ2.63-2.87(m,7h),δ1.26-1.42(m,2h),δ1.02-1.09(m,9h),δ0.87-0.92(m,3h)
[0181]
实施例11化合物112-{1-[1-(呋喃-2-氧甲基)-戊氧基亚氨基]-2,3-二甲基丁基}-3-羟基-5-(四氢硫吡喃-3-基)-环己-2-烯酮
[0182][0183]
11.1合成甲基磺酸1-(呋喃-2-氧甲基)-戊基酯
[0184]
向二氯甲烷中加入11.1g1-(呋喃-2-氧基)-己烷-2-醇和8.1g碳酸氢钠,在0℃下滴加7.6g甲基磺酰氯,滴加完毕后反应3h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到14.8g目标产物;
[0185]
11.2合成2-[1-(呋喃-2-氧甲基)-戊氧基]-异吲哚-1,3-二酮
[0186]
向乙腈中加入14.8g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入10.8g碳酸钾,在60℃反应2h,反应结束后加入大量水和甲苯萃取,收集有机层除去溶剂得到18.5g目标产物;
[0187]
11.3合成o-[1-(呋喃-2-氧甲基)-戊基]-羟胺
[0188]
向二氯甲烷中加入18.5g上步产物,然后滴加4.2g 85%水合肼,滴加完毕后在20℃下反应3h,反应结束后加水萃取,取有机层浓缩得到11.0g目标产物;
[0189]
11.4合成2-{1-[1-(呋喃-2-氧甲基)-戊氧基亚氨基]-2,3-二甲基丁基}-3-羟基-5-(四氢硫吡喃-3-基)-环己-2-烯酮
[0190]
用二氯乙烷溶解11.0g上步产物和17.4g 2-(2,3-二甲基-丁基)-3-羟基-5-(四氢-硫吡喃-3-基)-环己-2-烯酮,加入4.8g甲酸催化,80℃反应3h,反应结束后除去溶剂得到23.8g目标产物,总收率80%。
[0191]
1h nmr(300mhz,cdcl3):δ14.71(br,1h),δ6.04-6.73(m,3h),δ4.24-4.36(m,1h),δ4.01-4.06(d,2h),δ2.07-2.85(m,9h),δ1.31-1.79(m,11h),δ1.03-1.21(m,14h)
[0192]
实施例12化合物125-(2-乙基硫基丙基)-3-羟基-2-{4-甲基-1-[1-(4-甲基-1h-吡咯-2-氧基甲基)-丙氧基亚胺]-戊基}-环己-2-烯酮
[0193][0194]
12.1合成甲基磺酸1-(4-甲基-1h-吡咯-2-丙氧基甲基)-丙酯
[0195]
向甲苯中加入10.2g 1-(4-甲基-1h-吡咯-2-丙氧基)-丁醇和7.3g三乙胺,在10℃下滴加8.3g甲基磺酰氯,滴加完毕后反应2h,反应结束后抽滤取滤液,用盐酸水溶液萃取,取有机层浓缩得到13.9g目标产物;
[0196]
12.2合成o-[1-(4-甲基-1h-吡咯-2-氧基甲基)-丙基]-羟胺
[0197]
向dmf中加入13.9g上步产物、9.8g n-羟基邻苯二甲酰亚胺,溶解后加入3.4g氢氧化钾,在30℃反应6h,反应结束后向反应体系中加入二氯乙烷,然后滴加7.4g 65%水合肼,滴加完毕后在60℃下反应3h,反应结束后加水萃取,取有机层浓缩得到9.3g目标产物;
[0198]
12.3合成5-(2-乙基硫基丙基)-3-羟基-2-{4-甲基-1-[1-(4-甲基-1h-吡咯-2-氧基甲基)-丙氧基亚胺]-戊基}-环己-2-烯酮
[0199]
用二氯乙烷溶解9.3g上步产物和18.8g 5-(2-乙基硫基丙基)-3-羟基-2-(4-甲基戊基)-环己-2-烯酮,加入7.2g乙酸催化,80℃反应2h,反应结束后除去溶剂得到23.6g目标产物,总收率82%。
[0200]
1h nmr(300mhz,cdcl3):δ14.58(br,1h),δ5.96-6.34(m,2h),δ4.31-4.39(m,1h),δ4.06-4.11(d,2h),δ2.37-2.89(m,7h),δ1.98-2.19(m,2h),δ1.25-1.62(m,17h),δ0.91-1.02(m,9h)
[0201]
生物活性测定
[0202]
分别利用实施例1至12中提供的12种肟醚类1,3-环己二酮化合物进行灭草实验。
[0203]
具体实验条件如下:
[0204]
温室中播种杂草种子,生长条件为:土壤ph≈6.8,土壤有机质含量≈30%,温度22~25℃,光照为14h光周期;适时的补充水分和营养,杂草生长至3~4叶期,按照450l/ha兑水稀释后喷施到杂草上,10天后观察并计算株防效。
[0205]
杂草种类:稗草、马唐、牛筋草、千金子、抗性稗草
[0206]
株防效计算公式:株防效=(处理前株数-处理后株树)/处理前株树*100。
[0207]
药剂:实施例1至12提供的12种肟醚类1,3-环己二酮化合物制备成5重量%乳油使
用,具体成分为:5%化合物(1至12) 6%农乳0204 4%乙醇 85%石脑油。
[0208]
对照样品1:5重量%化合物e1(cn11205208a) 6%农乳0204 4%乙醇 85%石脑油
[0209]
对照样品2:5重量%化合物5(专利cn114105842a) 6%农乳0204 4%乙醇 85%石脑油
[0210]
对照样品3:30%二氯喹啉酸悬浮剂,购自德州绿霸精细化工有限公司,用药量45-85ml/亩。
[0211]
对照样品4:25克/升五氟磺草胺可分散油悬浮剂,购自科迪华农业科技有限责任公司,用药量40-80ml/亩。
[0212]
对照样品5:15%双草醚悬浮剂,购自安徽尚禾沃达生物科技有限公司,用药量10-18毫升/亩。
[0213]
对照样品6:5重量%苯丙草酮 6%农乳0204 4%乙醇 85%石脑油,自合成苯丙草酮,合成方法参照cn11205208a。
[0214]
对照样品7:24%烯草酮乳油,购自山东省济南科海有限公司,用药量15-20毫升/亩。
[0215]
[0216][0217]
表2肟醚类1,3-环己二酮化合物对抗性稗草的防除效果
[0218]
[0219][0220]
化合物安全性测试
[0221]
将作物种子播种于温室中培养(土壤ph≈6.8,土壤有机质含量≈30%,温度22~25℃,光照为14h光周期;适时的补充水分和营养),长至2-3叶期时施加上述活性成分有效质量为5%的乳油,5~7天后评价植物损害情况。其中,植物损害情况的评价标准如下:
[0222]
5,损害100%;
[0223]
4,损害80%以上;
[0224]
3,损害50%以上;
[0225]
2,损害20%以上;
[0226]
1,损害0-20%;
[0227]
0,对植物没有损害;无效果。
[0228]
[0229][0230]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于此。在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,包括各个技术特征以任何其它的合适方式进行组合以及包括组合先后顺序,这些简单变型和组合同样应当视为本发明所公开的内容,均属于本发明的保护范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。