1.本发明涉及高分子纳米粒子制备领域,具体涉及一种制备高分子纳米粒子的普适性方法。
背景技术:
2.高分子纳米粒子主要由合成高分子以及天然高分子通过各种合成方法制备而成,其具有可调的大小、形貌、表面化学以及软硬等物理化学性质,同时具有良好的生物相容性,对酶催化、药物的递送、靶向成像以及能量转换等方面都具有一定的应用价值。
3.模板法是制备高分子纳米粒子最常用的方法,其中层层自组装技术应用广泛,该方法就是通过沉浸、喷涂或者旋涂的方式,利用静电力、主客体相互作用、特异性生物反应、氢键、共价键等相互作用,将各种目标高分子涂覆在模板上形成功能性涂层的方法。该方法制备得到的各种高分子纳米粒子已经被广泛应用于生物化学、药物缓释等方面。然而,层层自组装技术存在制备过程复杂、耗时耗力等缺点。
4.介孔二氧化硅模板法制备高分子纳米粒子可以避免层层自组装技术中涂覆层数多的缺点,并且以介孔二氧化硅为模板制备高分子纳米粒子能够很好的调控纳米粒子的物理化学性质。但是,该方法对参与反应的高分子的种类有一定的要求,并且去除介孔二氧化硅模板需要氢氟酸等苛刻的条件,这都对高分子纳米粒子的合成及应用产生了不利的影响。因此,开发一种新型制备高分子纳米粒子的普适性方法,既能够实现对纳米粒子的各种物理化学性质按需调控,又能够实现模板的简便去除,具有重要理论和实际意义。
5.沸石咪唑酯骨架材料(zif-8)是由锌离子和二甲基咪唑通过配位作用形成的金属有机框架材料,在以聚乙二醇(peg)为矿化剂时能够封装各种合成高分子和蛋白质等生物大分子,并且在酸性条件下会发生降解实现对封装物质的可控释放;同时,通过控制反应温度就可以调控zif-8纳米粒子的尺寸。因此,zif-8是一种理想的封装高分子的模板。
技术实现要素:
6.针对现有制备高分子纳米粒子的方法复杂且不具有普适性等缺点,本发明提供一种制备高分子纳米粒子的普适性方法。
7.本发明第一方面提供一种通过不同化学交联反应来制备高分子纳米粒子的普适性方法以及通过上述方法得到的高分子纳米粒子。包括步骤如下:
8.将矿化剂和高分子前体溶于2-甲基咪唑水溶液中,然后将上述溶液与硝酸锌水溶液共混,反应后离心除去上清液,然后将产物重新分散于水中并离心洗涤产物三次,得到封装高分子前体的zif-8纳米粒子。随后将zif-8纳米粒子分散于溶有高分子交联剂的酸性缓冲溶液中,将反应液倒入透析袋,然后置于酸性缓冲溶液中进行zif-8的降解和高分子前体与高分子交联剂之间的交联反应,反应完成后将透析袋中的反应液取出并离心,用水洗涤产物三次,得到高分子纳米粒子。
9.本发明第二方面分别以多糖、多肽和蛋白质为例,提供一种适用于各类高分子的
制备纳米粒子的普适性方法以及该方法制备得到的纳米粒子。包括步骤如下:
10.将矿化剂和高分子前体一起溶于2-甲基咪唑水溶液中,然后将上述溶液与硝酸锌水溶液共混,反应后离心除去上清液,然后将产物重新分散于水中并离心洗涤产物三次,得到封装了高分子前体的zif-8纳米粒子。随后将zif-8纳米粒子分散于溶有高分子交联剂的酸性缓冲溶液中,将反应液倒入透析袋,然后置于酸性缓冲溶液中进行zif-8的降解和高分子前体与高分子交联剂之间的交联反应,反应完成后将透析袋中的反应液取出并离心,用水洗涤产物三次,得到高分子纳米粒子。
11.本发明第三方面提供一种上述方法制备得到的高分子纳米粒子在生物医学中的应用(例如酶催化、药物和疫苗递送等)。
12.本发明的一个或多个实施方式至少具有以下有益效果:
13.该方法适用于多糖、多肽、蛋白质以及合成高分子等各类高分子制备高分子纳米粒子,也就是说该方法具有普适性。
14.本发明以zif-8作为自牺牲模板由外向内制备得到高分子纳米粒子,在zif-8降解的同时实现高分子前体与高分子交联剂之间的交联,不需要额外的步骤对模板进行去除,制备方法简便快速,可操作性强并且可以大量制备。
15.在本发明中,通过调控高分子前体的反应浓度可以调整zif-8纳米粒子的尺寸,从而控制以zif-8为模板合成的高分子纳米粒子的尺寸;此外,通过调控高分子交联剂的反应浓度,高分子纳米粒子的硬度也能够得到调控。
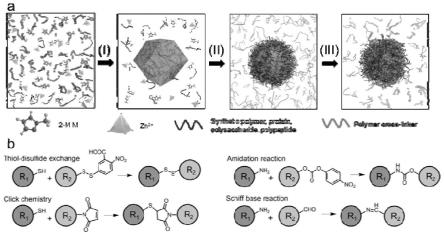
16.本发明中高分子纳米粒子的合成分别由四种不同的交联反应(巯基-双硫键交换反应、席夫碱反应、酰胺化反应和点击化学反应)完成,形成了不同的化学键,从而赋予高分子纳米粒子不同的响应性降解的能力,为高分子纳米粒子的各种应用提供条件。
附图说明
17.图1a为以zif-8纳米粒子为模板,制备高分子纳米粒子的过程示意图;图1b为高分子纳米粒子合成过程中涉及到的四种交联反应。
18.图2a-c分别为8-arm-peg-mal、8-arm-peg-ndec和8-arm-peg-nh2的结构示意图;图2d-f分别为8-arm-peg-mal@zif-8、8-arm-peg-ndec@zif-8和8-arm-peg-nh2@zif-8的tem图片;图2g-i为对应图2d-f中的zif-8为模板制备得到的peg纳米粒子。图中的标尺为1μm。
19.图3a-d分别为ha-sh、pll-sh、ova-sh和lyz的结构示意图;图2e-h分别为ha-sh@zif-8、pll-sh@zif-8、ova-sh@zif-8和lyz@zif-8的tem图片;图2i-l为对应图2e-h中的zif-8为模板制备得到的ha纳米粒子、pll纳米粒子、ova纳米粒子和lyz纳米粒子。图中的标尺为1μm。
20.图4a-d分别为ha-sh的质量为1mg、4mg、10mg和16mg时制备得到的ha-sh@zif-8纳米粒子;图4e-h为对应图4a-d中的ha-sh@zif-8纳米粒子以8-arm-peg-tnb为交联剂制备得到的ha纳米粒子。图中的标尺为500nm。
21.图5为由不同交联剂浓度制备得到的ha纳米粒子的杨氏模量统计数据图。
22.图6为由巯基-双硫键交换反应制备得到的ha纳米粒子和由席夫碱反应制备得到的peg纳米粒子在不同介质中的稳定性数据图。
23.图7a为高分子粒子形成过程示意图;图7b、图7c、图7d、图7e分别为ha粒子在形成过程中10分钟、20分钟、30分钟和60分钟时的共聚焦荧光成像图片。图中的标尺为2μm。
24.图8为ova纳米粒子在gsh(10mm)溶液中ova的释放曲线。
25.图9为不同浓度的自由ova和ova纳米粒子与raw 264.7细胞共孵育6小时后的细胞相互作用实验结果。
26.图10为bmdc细胞成熟实验的统计数据。
27.图11为bmdc细胞中抗原递呈实验的统计数据。
具体实施方式
28.应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
29.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
30.正如背景技术所介绍的,现有制备高分子纳米粒子的方法还具有复杂且不具有普适性等问题。因此,开发一种普适性的方法来制备高分子纳米粒子,对高分子纳米粒子在各个领域的应用具有非常重要的意义。
31.为了解决如上的技术问题,本发明第一方面提供一种通过不同化学交联反应来制备高分子纳米粒子的普适性方法:将矿化剂和高分子前体溶于2-甲基咪唑水溶液中,然后将上述溶液与硝酸锌水溶液共混进行反应,反应后离心除去上清液,然后将产物重新分散于水中并离心洗涤产物,得到封装高分子的zif-8纳米粒子。随后将zif-8纳米粒子分散于溶有高分子交联剂的酸性缓冲溶液中,将反应液倒入透析袋,然后置于酸性缓冲溶液中进行zif-8的降解和高分子前体与高分子交联剂之间的的交联反应,反应完成后将透析袋中的反应液取出并离心,用水洗涤产物三次,得到高分子纳米粒子。
32.所述矿化剂为peg。
33.所述的高分子前体为各类高分子。
34.进一步的,制备的高分子纳米粒子为peg纳米粒子时,peg即是矿化剂,也是高分子前体。
35.进一步的,peg为8-arm-peg-maleimide(8-arm-peg-mal)、8-arm-peg-4-nitrophenyl-2-(2-pyridyldithio)ethyl carbonate(8-arm-peg-ndec)或8-arm-peg-nh2,其分子量为10kda、20kda或40kda,进一步优选的,8-arm-peg-mal的分子量为20kda,8-arm-peg-ndec的分子量为40kda,8-arm-peg-nh2的分子量为20kda。
36.8-arm-peg-ndec的合成路线如路线1所示:
[0037][0038]
路线1
[0039]
所述的peg在2-甲基咪唑水溶液中的浓度为2.5-100mg ml-1
。
[0040]
所述2-甲基咪唑水溶液中,2-甲基咪唑的浓度为120-200mm。
[0041]
所述硝酸锌水溶液中,硝酸锌的浓度为30-70mm。
[0042]
2-甲基咪唑水溶液与硝酸锌水溶液混合的体积比为(1-2):(1-2)。进一步优选的,2-甲基咪唑水溶液与硝酸锌水溶液混合的体积比为1:1。
[0043]
制备封装高分子的zif-8纳米粒子的反应时间为20-40分钟。
[0044]
zif-8的降解和peg分子的交联反应的时间为1-8个小时。
[0045]
zif-8纳米粒子进行离心采用的离心速度为1000-10000rcf。
[0046]
对应zif-8中封装的8-arm-peg-mal、8-arm-peg-ndec或8-arm-peg-nh2,所述的peg交联剂为8-arm-peg-sh、8-arm-peg-nh2或8-arm-peg-cho,分子量为10kda、20kda和40kda。发生的交联反应分别为点击化学反应、酰胺化反应和席夫碱反应。
[0047]
进一步地,8-arm-peg-sh的分子量为20kda,8-arm-peg-nh2的分子量为10kda,8-arm-peg-cho的分子量为10kda;酸性缓冲溶液中peg交联剂的浓度为0.2~15mg ml-1
。
[0048]
所述的酸性缓冲溶液为醋酸钠缓冲溶液,浓度为50mm,酸性缓冲溶液的ph为5.5-6.0。
[0049]
在酸性缓冲溶液中进行透析时使用透析袋的截留分子量为1~7kda,进一步优选的,透析袋的截留分子量为3.5kda。
[0050]
本发明第二方面分别以多糖、多肽和蛋白质为例,提供一种适用于各类高分子的制备纳米粒子的普适性方法。包括步骤如下:
[0051]
将矿化剂和高分子前体一起溶于2-甲基咪唑水溶液中,然后将上述溶液与硝酸锌水溶液共混,反应30分钟后离心除去上清液,然后将产物重新分散于水中并离心洗涤产物,得到封装了高分子前体的zif-8纳米粒子。随后将zif-8纳米粒子分散于溶有高分子交联剂的酸性缓冲溶液中,将反应液倒入透析袋,然后置于酸性缓冲溶液中进行zif-8的降解和高分子前体与高分子交联剂之间的交联反应,1-8小时后将透析袋中的反应液取出并离心,用
水洗涤产物三次,得到高分子纳米粒子。
[0052]
所述的矿化剂为8-arm-peg-oh,8-arm-peg-oh在2-甲基咪唑水溶液中的浓度为2.5~100mg ml-1
,进一步优选的,8-arm-peg-oh在2-甲基咪唑水溶液中的浓度为5mg ml-1
。
[0053]
所述的高分子前体包括巯基化的透明质酸(ha-sh)、巯基化的聚赖氨酸(pll-sh)、巯基化的卵清蛋白(ova-sh)或溶菌酶(lyz)等。
[0054]
所述的高分子交联剂为8-arm-peg-2-nitro-5-thiobenzoate(8-arm-peg-tnb),酸性缓冲溶液中8-arm-peg-tnb的浓度为0.2~15mg ml-1
,发生的交联反应为巯基-双硫键交换反应。
[0055]
所述的高分子纳米粒子分别为ha纳米粒子、pll纳米粒子、ova纳米粒子和lyz纳米粒子。
[0056]
上述制备方法可对高分子物理化学性质进行有效调控,具体可进行调控的物理化学性质包括:尺寸、硬度和响应降解性。
[0057]
本发明第三方面提供一种上述方法制备得到的高分子纳米粒子的应用。具体应用方式为:以8-arm-peg-ndec作为ova的交联剂制备得到ova纳米粒子,然后研究了ova纳米粒子在免疫抗原递送中的应用。
[0058]
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
[0059]
实施例1
[0060]
以peg纳米粒子的合成为例,一种通过不同化学交联反应来制备高分子纳米粒子的普适性方法步骤如下:
[0061]
将8-arm-peg-mal(20kda,20mg)、8-arm-peg-ndec(40kda,20mg)或8-arm-peg-nh2(20kda,20mg)溶于2-甲基咪唑水溶液中,2-甲基咪唑的浓度为160mm;
[0062]
然后加入硝酸锌水溶液中,硝酸锌水溶液的浓度为40mm;
[0063]
混匀反应30分钟后取出反应液,离心并用水洗涤三次,分别得到封装了8-arm-peg-mal、8-arm-peg-ndec或8-arm-peg-nh2的zif-8纳米粒子(8-arm-peg-mal@zif-8、8-arm-peg-ndec@zif-8或8-arm-peg-nh2@zif-8),相关tem表征数据如图2d-f所示;
[0064]
将产物分散于300μl水中后加到溶有peg交联剂的醋酸钠缓冲溶液(50mm,ph5.5)中,将反应液转移至截留分子量为3.5kda的透析袋中,透析袋置于醋酸钠缓冲溶液中透析4小时后取出,离心并用水洗涤三次得到最终产物。对应8-arm-peg-mal@zif-8、8-arm-peg-ndec@zif-8或8-arm-peg-nh2@zif-8的peg交联剂分别为8-arm-peg-sh(20kda,5mg/ml)、8-arm-peg-nh2(20kda,5mg/ml)或8-arm-peg-cho(20kda,5mg/ml),分别通过席夫碱反应、酰胺化反应和点击化学反应制备得到四种peg纳米粒子,tem表征如图2g-i所示。
[0065]
实施例2
[0066]
以多糖、多肽和蛋白质为例,证明该方法是一种适用于各类高分子的制备纳米粒子的普适性方法。步骤如下:
[0067]
将8-arm-peg-oh(40kda,10mg)与ha-sh、pll-sh、ova-sh或lyz一起溶于2-甲基咪唑水溶液(160mm,2ml)中,然后倒入硝酸锌水溶液(40mm,2ml)中;
[0068]
旋转混匀反应半小时后形成ha-sh@zif-8、pll-sh@zif-8、ova-sh@zif-8或lyz@zif-8纳米粒子(tem图像如图3e-h所示),将其离心并用水洗涤,最终分散于300μl水中;
[0069]
将上述产物倒入溶有交联剂8-arm-peg-tnb(10kda,5mg/ml)的醋酸钠缓冲溶液(50mm,ph5.5)中,然后转移至截留分子量为3.5kda的透析袋中,透析袋置于醋酸钠缓冲溶液(50mm,ph5.5)中透析4小时后取出,得到ha、pll、ova或lyz纳米粒子(tem图像如图3i-l所示),将其离心并用水洗涤三次得到最终产物。
[0070]
实施例3
[0071]
通过改变高分子前体的反应浓度调控高分子纳米粒子的尺寸,以ha纳米粒子的制备为例,步骤如下:
[0072]
将8-arm-peg-oh(40kda,10mg)和不同质量的ha-sh(1mg、4mg、10mg或16mg)溶于2-甲基咪唑水溶液(160mm,2ml)中,然后倒入硝酸锌水溶液(40mm,2ml)中;
[0073]
混匀反应30min后取出反应液,离心并用水洗涤三次得到不同尺寸的ha-sh@zif-8(图4a-d),最终分散于300μl水中;
[0074]
将上述产物倒入溶有交联剂8-arm-peg-tnb(10kda,5mg/ml)的醋酸钠缓冲溶液(50mm,ph5.5)中,然后转移至截留分子量为3.5kda的透析袋中,透析袋置于醋酸钠缓冲溶液(50mm,ph5.5)中透析4小时后取出,离心并用水洗涤三次得到最终产物。得到的四种ha纳米粒子的尺寸分别为200nm、500nm、750nm和1200nm(图4e-h)。因此,通过改变高分子的浓度可以调控zif-8纳米粒子的尺寸,进而可以调控高分子纳米粒子的尺寸。
[0075]
实施例4
[0076]
通过改变高分子交联剂的反应浓度调控高分子纳米粒子的硬度,以制备ha纳米粒子为例,步骤如下:
[0077]
将8-arm-peg-oh(40kda,10mg)和ha-sh(10mg)溶于2-甲基咪唑水溶液(160mm,2ml)中,然后加入到硝酸锌水溶液(40mm,2ml)中;
[0078]
混匀30分钟后取出反应液,离心并用水洗涤三次,最终分散于300μl水中;
[0079]
将上述产物加入到溶有不同浓度交联剂8-arm-peg-tnb(0.25mg/ml、1mg/ml、2.5mg/ml或4mg/ml)的醋酸钠缓冲溶液(50mm,ph5.5)中,然后转移至截留分子量为3.5kda的透析袋中,透析袋置于醋酸钠缓冲溶液(50mm,ph5.5)中透析4小时后取出,离心并用水洗涤三次得到最终产物。对得到的四种ha纳米粒子进行afm的表征,并测得了各自的杨氏模量,其统计结果如图5所示。实验结果表明,改变交联剂的浓度可以有效调控高分子纳米粒子的硬度。
[0080]
实施例5
[0081]
通过采用不同的交联策略使高分子纳米粒子具有不同的响应降解性,步骤如下:
[0082]
以8-arm-peg-nh2@zif-8为模板,以8-arm-peg-cho为交联剂通过席夫碱反应制备得到具有ph响应性peg纳米粒子;
[0083]
以ha-sh@zif-8为模板,以8-arm-peg-tnb为交联剂通过巯基-双硫键交换反应制备得到具有还原响应性的ha纳米粒子。
[0084]
将上述peg纳米粒子和ha纳米粒子进行荧光标记后,分别置于pbs,醋酸钠缓冲溶液(ph 5.0)或还原性谷胱甘肽溶液(gsh,10mm)中,在设定的不同时间点取出50μl混合液,使用流式细胞仪对混合液中的纳米粒子个数进行检测。实验结果如图6所示,上述peg纳米粒子和ha纳米粒子在pbs中均具有非常好的稳定性,peg纳米粒子在酸性缓冲溶液中逐渐降解,ha纳米粒子在还原性条件下也逐渐发生降解,由此证明,通过选用不同的交联策略可以
赋予纳米粒子不同的响应降解性,从而能够实现内部封装物质的响应性释放。
[0085]
实施例6
[0086]
以ha纳米粒子的合成为例,通过共聚焦显微镜表征高分子纳米粒子的形成过程,步骤如下:
[0087]
将8-arm-peg-oh(40kda,10mg)和硫代吡啶化的ha(ha-pda)(10mg)溶于2-甲基咪唑水溶液(160mm,2ml)中,然后加入到硝酸锌水溶液(40mm,2ml)中,ha-pda的合成路线如路线2所示;
[0088][0089]
路线2
[0090]
混匀30分钟后取出反应液,离心并用水洗涤三次,最终分散于300μl水中;
[0091]
将交联剂8-arm-peg-sh进行荧光标记,然后把上述分散液与溶有8-arm-peg-sh(10kda,5mg/ml)的醋酸钠缓冲溶液(50mm,ph5.5)共混,再转移至截留分子量为3.5kda的透析袋中,透析袋置于醋酸钠缓冲溶液(50mm,ph5.5)后开始计时,分别在透析10分钟、20分钟、30分钟和70分钟时于透析袋中取出100μl反应液离心并用水清洗两遍,重新分散于100μl水中后使用共聚焦显微镜进行荧光成像,结果如图7所示。实验数据表明,交联剂8-arm-peg-sh首先会与逐渐从zif-8表面裸露出的高分子ha-pda进行交联,从而在共聚焦显微镜下观察到一个空心状结构,随着zif-8的进一步降解,8-arm-peg-tnb与ha-pda的交联也从外向内进行完全,最终得到实心的ha高分子纳米粒子。
[0092]
实施例7
[0093]
ova纳米粒子的制备及其在抗原递送方面的应用研究,步骤如下:
[0094]
将8-arm-peg-oh(40kda,10mg)和ova(2mg)溶于2-甲基咪唑水溶液(160mm,2ml)中,然后加入到硝酸锌水溶液(40mm,2ml)中混匀30分钟,制备得到ova@zif-8纳米粒子,随后以8-arm-peg-ndec作为交联剂在醋酸钠缓冲溶液(50mm,ph5.5)中完成交联反应,制备得到ova纳米粒子。ova是一种免疫治疗中常用的模型抗原蛋白,而该ova纳米粒子在还原性条件下可以发生降解释放出自由的ova,从而可以应用于抗原的递送。
[0095]
性能测试:
[0096]
(1)ova的响应性释放实验
[0097]
将荧光标记的ova纳米粒子加入到gsh(10mm)溶液中后,分别在1小时、2小时、3小时、5小时、8小时、12小时、24小时和48小时取出反应液,离心后使用nanodrop测试上清液中ova的浓度。绘制ova的释放曲线如图8所示。实验结果证明,在还原性条件下,ova纳米粒子会逐渐发生降解,从而实现ova的响应性持续释放。
[0098]
(2)细胞摄取实验
[0099]
在24孔板中每个孔铺10万个raw 264.7细胞,培养过夜使细胞贴壁。将标记了荧光的自由ova和ova纳米粒子与264.7细胞共孵育6小时后,收集细胞使用流式细胞仪进行检测。检测结果如图9所示,与自由ova相比,ova纳米粒子能够增加raw 264.7细胞的摄取。因此说明,ova纳米粒子能够促进ova的细胞摄取。
[0100]
(3)骨髓来源dc细胞(bmdc)的成熟实验
[0101]
将pbs、自由ova和ova纳米粒子与bmdc细胞共孵育24小时后,收集bmdc细胞后加入anti-cd11c和anti-ova257-264(siinfekl)-h-2kb进行染色,随后使用流式细胞仪对cd80和cd86的表达进行检测。实验结果如图10所示,相比于自由ova,该方法制得的ova纳米粒子能够促进bmdc的成熟。
[0102]
(3)抗原递呈实验
[0103]
将pbs、自由ova和ova纳米粒子与bmdc细胞共孵育24小时后,收集bmdc细胞后加入anti-cd11c,anti-cd80和anti-cd86进行染色,随后使用流式细胞仪对siinfekl的表达进行检测。实验结果如图11所示,相比于自由ova,该方法制得的ova纳米粒子能够显著促进抗原在bmdc中的递呈。
[0104]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。