regulatory factor,mrf)(如myod、mef2)和肌细胞生成素对成肌细胞(myoblast)分化的调节上(sabourin la和rudnicki ma.,clin genet.2000年一月;57(1):16-25)。由于通过药物治疗改善成肌细胞的分化能力和再生能力会导致肌肉肥大或改善肌肉功能,因此已经进行了许多尝试来利用这种方法解决年龄引起的肌肉功能下降(francesca riuzzi等人,j cachexia sarcopenia muscle,1255-1268,2018;mary f.o’leary,sci rep.12997,2017;jin-a kim和seong min kim,bmc complement altern med,287,2019)。也就是说,改善卫星细胞的功能并增加卫星细胞的数量,可以是抑制肌肉减少症发展并改善肌肉再生能力的一种策略。因此,需要开发可以促进成肌细胞分化的物质。
8.[现有技术文献]
[0009]
[非专利文献]
[0010]
(非专利文献1)ju yeon kwak,ki-sun kwon,ann geriatr med res.98-104,2019
[0011]
(非专利文献2)jiayu yin,xiang lu,zhiyuan qian,weiting xu和xiang zhou,theranostics,4019-4029,2019
[0012]
(非专利文献3)aj cruz-jentoft等人,age ageing,601,2019
[0013]
(非专利文献4)jessica hiu-tung lo,kin pongu,tszlamyiu,j orthop translat,38-52,2020
[0014]
(非专利文献5)carlson等人,j gerontol,b224-233,2001
[0015]
(非专利文献6)sabourin la,rudnicki ma.,clin genet.2000jan;57(1):16-25.
[0016]
(非专利文献7)francesca riuzzi,guglielmo sorci,cataldo arcuri,j cachexia sarcopenia muscle,1255-1268,2018,
[0017]
(非专利文献8)mary f.o’leary,sci rep.12997,2017,
[0018]
(非专利文献9)jin-a kim,seong min kim,bmc complement altern med,287,2019
技术实现要素:
[0019]
技术问题
[0020]
本发明人致力于开发可以促进成肌细胞分化从而增加肌肉质量并有效恢复肌肉功能的物质。作为结果,本发明人发现阿尔维林、4-羟基阿尔维林、其衍生物及其药学上可接受的盐促进成肌细胞的分化并恢复肌肉力量,从而完成了本发明。
[0021]
问题的解决方案
[0022]
为了解决上述问题,本发明的一个方面提供一种式1所示的化合物及其药学上可接受的盐。
[0023]
本发明的另一方面提供一种用于预防或治疗肌肉无力相关病症的药物组合物,其包含所述化合物或其药学上可接受的盐作为活性成分。
[0024]
本发明的另一方面提供一种用于促进离体成肌细胞分化的组合物,其包含所述化合物或其药学上可接受的盐作为活性成分。
[0025]
本发明的另一方面提供一种促进成肌细胞分化的方法,其包括用化合物或其药学上可接受的盐处理离体成肌细胞。
[0026]
本发明的另一方面提供一种制造肌管的方法,其包括用化合物或其药学上可接受
的盐处理离体成肌细胞,从而使成肌细胞分化。
[0027]
本发明的另一方面提供一种用于预防或减轻肌肉无力相关病症的食品组合物,其包含式1所示的化合物或其营养学上可接受的盐。
[0028]
本发明的另一方面提供一种用于肌肉力量增强的组合物,其包含所述化合物或其药学上可接受的盐作为活性成分。
[0029]
本发明的另一方面提供一种预防或治疗肌肉无力相关病症的方法,所述方法包括向受试者施用式1所示的化合物或其药学上可接受的盐。
[0030]
本发明的另一方面提供式1所示的化合物或其药学上可接受的盐用于预防或治疗肌肉无力相关病症的用途。
[0031]
本发明的另一方面提供式1所示的化合物或其药学上可接受的盐在制备用于预防或治疗肌肉无力相关病症的药物中的用途。
[0032]
发明的有益效果
[0033]
当施用于成肌细胞时,本发明的阿尔维林、4-羟基阿尔维林、其衍生物或其药学上可接受的盐促进成肌细胞分化为肌管。因此,本发明的阿尔维林、4-羟基阿尔维林、其衍生物或其药学上可接受的盐可以有利地用于促进成肌细胞的分化或预防或治疗与肌肉无力相关的病症。
附图说明
[0034]
图1显示通过用dmso、胰岛素或阿尔维林柠檬酸盐处理成肌细胞而分化的肌管的荧光图像。
[0035]
图2显示图表,其显示通过用dmso、胰岛素或阿尔维林柠檬酸盐处理成肌细胞而分化的肌管中的emyhc荧光染色面积。
[0036]
图3描绘使用动物确定阿尔维林柠檬酸盐的肌肉力量增强作用的实验方案。
[0037]
图4为显示根据阿尔维林柠檬酸盐施用浓度的小鼠握力测定值的图表。
[0038]
图5显示正常组和实验组中小鼠的跑动时间。
[0039]
图6为显示正常组和实验组中小鼠抓住转子杆(rotor-rod)的持续时间的图表。
[0040]
图7为显示从正常组小鼠和实验组小鼠获得的腓肠肌(ga)肌肉和胫骨前肌(ta)的肌肉质量的图表。
[0041]
图8描绘使用诱导了肌肉减少症的动物来确定阿尔维林柠檬酸盐的肌肉力量增强作用的实验方案。
[0042]
图9显示正常组、对照组和实验组中小鼠的跑动时间。
[0043]
图10显示图表,其显示从正常组、对照组和实验组中小鼠获得的腓肠肌(ga)肌肉和胫骨前肌(ta)的肌肉质量。
[0044]
图11显示通过用dmso、胰岛素、阿尔维林柠檬酸盐或4-羟基阿尔维林(4ha)处理成肌细胞而分化的肌管的荧光染色图像。
[0045]
图12显示图表,其显示通过用dmso、胰岛素、阿尔维林柠檬酸盐或4-羟基阿尔维林(4ha)处理成肌细胞而分化的肌管中的emyhc荧光染色面积。
[0046]
图13显示肌管的荧光染色图像,其中萎缩是由阿尔维林柠檬酸盐(ac)或4-羟基阿尔维林(4ha)中的癌细胞条件培养基(cm)诱导的。
[0047]
图14显示肌管的直径图,其中萎缩是由阿尔维林柠檬酸盐(ac)或4-羟基阿尔维林(4ha)中的癌细胞条件培养基(cm)诱导的。
[0048]
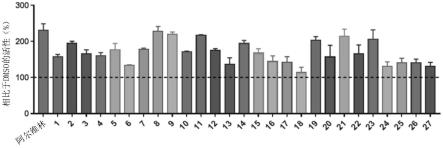
图15显示通过分别用dmso、阿尔维林和27种阿尔维林衍生物处理成肌细胞而分化的肌管的荧光染色图像。
[0049]
图16显示图表,其显示通过分别用dmso、阿尔维林和27种阿尔维林衍生物处理成肌细胞而分化的肌管的面积。
具体实施方式
[0050]
在下文中,将更详细地描述本发明。
[0051]
本发明的一个方面提供一种下式1所示的化合物及其药学上可接受的盐:
[0052]
[式1]
[0053][0054]
在式1中,
[0055]
r1、r2、r4和r5各自独立地为氢、卤素、-cf3、羟基、氰基、c
1-10
烷基、c
1-10
烷氧基、c
1-4
卤代烷基、c
1-10
卤代烷氧基、c
2-4
烯基、c
2-4
炔基、-nhra、-nhc(=o)rb、-nhc(=o)nhrc、氨基-c
1-10
烷氧基、c
1-10
烯氧基或c
6-10
芳基-c
1-10
烷氧基,
[0056]
r3为c
1-10
烷基、c
2-12
烯基、c
1-4
卤代烷基、c
2-4
烯基或c
2-4
炔基,
[0057]
ra至rc各自独立地为氢、c
1-6
烷基、c
1-6
烷氧基、c
1-4
卤代烷基、c
2-4
烯基、c
2-4
炔基或c
6-10
芳基;并且
[0058]
n和m各自独立地为1至10的整数。
[0059]
除非另有说明,如本文所使用的术语“卤代”或“卤素”是指f、cl、br或i。
[0060]
除非另有说明,术语“烷基”是指直链或支链饱和烃残基。例如,“c
1-10
烷基”是指在其骨架结构中具有1至10个碳原子的烷基。特别地,c
1-10
烷基可以包括基团例如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、正戊基、异戊基、叔戊基、仲戊基、新戊基、己基、庚基、辛基、壬基和癸基。
[0061]
除非另有说明,术语“烷氧基”是指具有-o-烷基结构的基团,其中如上定义的烷基经由氧原子与母体化合物连接。烷氧基的烷基部分可以含有1至20个碳原子(即c
1-c
20
烷氧基),1至12个碳原子(即c
1-c
12
烷氧基),或1至6个碳原子(即c
1-c6烷氧基)。合适的烷氧基的示例包括甲氧基(-o-ch3或-ome)、乙氧基(-och2ch3或-oet)、叔丁氧基(-o-c(ch3)3或-o-tbu)等。
[0062]
术语“卤代烷基”是指被一个或多个卤素原子取代的烷基。更具体地,卤代烷基可以是被两个或更多个相同卤素取代的烷基,或者被两个或更多个不同卤素取代的烷基。
[0063]
术语“卤代烷氧基”是指被一个或多个卤素原子取代的烷氧基。
[0064]
术语“氨基烷氧基”是指被一个或多个氨基取代的烷氧基。
[0065]
术语“氨基”是指-nr2,其中“r”各自独立地选自h、烷基、芳基等,典型的氨基可以包括但不限于-nh2、-n(ch3)2、-nh(ch3)、-n(ch2ch3)2、-nh(ch2ch3)、-nh(取代或未取代的苄基)、-nh(取代或未取代的苯基)等。
[0066]
术语“烯基”是指具有伯、仲、叔或环状碳原子的烃,其具有一个或多个不饱和部分,即碳-碳sp2键。例如,烯基可以含有2至20个碳原子(即c
2-c
20
烯基),2至12个碳原子(即c
2-c
12
烯基),或2至6个碳原子(即,c
2-c6烯基)。合适的烯基的示例包括但不限于乙烯或乙烯基(-ch=ch2)、烯丙基(-ch2ch=ch2)、环戊烯基(-c5h7)和5-己烯基(-ch2ch2ch2ch2ch=ch2)。
[0067]
除非另有说明,术语“烯氧基”是指具有-o-烯基结构的基团,其中如上定义的烯基经由氧原子与母体化合物连接。
[0068]
术语“炔基”是指具有伯、仲、叔或环状碳原子的烃,其具有一个或多个不饱和部分,即碳-碳三键。例如,炔基可以含有2至20个碳原子(即c
2-c
20
炔基),2至12个碳原子(即c
2-c
12
炔基),或2至6个碳原子(即,c
2-c6炔基)。合适的炔基包括例如乙炔基(-c≡h)、炔丙基(-ch2c≡h)等,但不限于此。
[0069]
如本文所使用的术语“芳基”是指通过从母体芳环系统的六个碳原子中去除一个氢原子而衍生的芳烃基团。例如,芳基可以具有6至20个碳原子,6至14个碳原子,或6至12个碳原子。
[0070]
如本文所使用的术语“取代”是指用取代基取代分子结构中的氢原子,由此从这种取代变成化学稳定的化合物,而不超过给定原子的化合价(valence)。例如,短语“基团a被取代基b取代”可以是指与构成基团a骨架的原子(即,碳)键合的氢原子被取代基b取代,从而在基团a和取代基b之间形成共价键。
[0071]
根据一个示例,在式1中,r1、r2、r4和r5可以各自独立地为氢、卤素、羟基、c
1-10
烷基、c
1-10
烷氧基、c
1-10
卤代烷氧基、-nhra、-nhc(=o)rb、-nhc(=o)nhrc、氨基-c
1-10
烷氧基、c
1-10
烯氧基或c
6-10
芳基-c
1-10
烷氧基,r3可以为c
1-10
烷基或c
2-12
烯基;ra至rc可以各自独立地为氢、c
1-6
烷基、c
1-6
烷氧基或c
6-10
芳基;并且n和m可以各自独立地为1至7的整数。
[0072]
根据一个示例,在式1中,r1和r2可以各自独立地为氢、卤素、羟基、c
1-10
烷基、c
1-10
烷氧基、c
1-10
卤代烷氧基、-nhra、氨基-c
1-10
烷氧基、c
1-10
烯氧基或c
6-10
芳基-c
1-10
烷氧基;r3可以为c
1-10
烷基,r4和r5可以各自独立地为氢、羟基、-nhra、-nhc(=o)rb或-nhc(=o)nhrc;ra至rc可以各自独立地为氢、c
1-4
烷基、c
1-6
烷氧基或c
6-10
芳基;并且n和m可以各自独立地为1至5的整数。
[0073]
根据另一个示例,在式1中,r1和r2可以各自独立地为氢、卤素、羟基、c
1-6
烷基、c
1-6
烷氧基、c
1-6
卤代烷氧基、-nhra、氨基-c
1-10
烷氧基、c
1-10
烯氧基或c
6-10
芳基-c
1-6
烷氧基,r3可以为c
1-6
烷基,r4可以为氢、卤素、羟基、-nhra、-nhc(=o)rb或-nhc(=o)nhrc,并且r5可以为氢;ra可以为氢或c
1-6
烷氧基;rb可以为氢或c
1-6
烷基;rc可以为氢或c
6-10
芳基;并且n和m可以各自独立地为1至3的整数。
[0074]
根据另一个示例,在式1中,如果n和m各自为2,r3为乙基,并且r1、r4和r5各自为氢,则r2为氢或羟基。在这种情况下,该示例可以为阿尔维林或4-羟基阿尔维林。
[0075]
特别地,阿尔维林具有下式2所示的结构。
[0076]
[式2]
[0077][0078]
在此处,阿尔维林对应于当n和m各自为2,r3为乙基,并且r1、r2、r4和r5均为氢时的式1化合物。
[0079]
如本文所使用的术语“阿尔维林”是指iupac名称为n-乙基-3-苯基-n-(3-苯基丙基)丙-1-胺的化合物,化学式为c
20h27
n,分子量为281.44g/mol。已知阿尔维林通常作为用于胃肠道疾病的药物,但是对其与成肌细胞分化的关系知之甚少。
[0080]
此外,4-羟基阿尔维林是阿尔维林的代谢物,4-羟基阿尔维林具有下式3的结构。
[0081]
[式3]
[0082][0083]
在此处,4-羟基阿尔维林对应于当n和m各自为2,r3为乙基,并且r1、r2、r4和r5中三个为氢一个为羟基时的式1化合物。特别地,r1、r2、r4和r5中三个为氢一个为羟基的情况可以包括以下几种情况:1)r2、r4和r5各自为氢,并且r1为羟基;2)r1、r4和r5各自为氢,并且r2为羟基;iii)r1、r2和r5各自为氢,并且r4为羟基;和iv)r1、r2和r4各自为氢,并且r5为羟基。
[0084]
根据具体示例,式1所示的化合物的具体示例包括以下:
[0085]
1)4-(3-乙基(3-苯基丙基)氨基)丙基)苯胺;
[0086]
2)n-乙基-3-(4-甲氧基苯基)-n-(3-苯基丙基)丙-1-胺;
[0087]
3)n-乙基-3-苯基-n-(3-(对甲苯基)丙基)丙-1-胺;
[0088]
4)3-(3-(乙基(3-苯基丙基)氨基)丙基)苯酚;
[0089]
5)n-甲基-3-苯基-n-(3-苯基丙基)丙-1-胺;
[0090]
6)4,4
’‑
((乙基氮杂二基))双(丙-3,1-二基))二苯酚;
[0091]
7)4-(3-(甲基(3-苯基丙基)氨基)丙基)苯酚;
[0092]
8)4-(3-((3-(4-(苄氧基)苯基)丙基)(乙基)氨基)丙基)苯胺;
[0093]
9)n-(4-(3-((3-)4-(苄氧基)苯基)丙基)(乙基)氨基)丙基)苯基)乙酰胺;
[0094]
10)4-(3-(乙基(苯乙基)氨基)丙基)苯酚;
[0095]
11)4-(3-(乙基(3-苯基丙基)氨基)丙基)-2-氟苯酚;
[0096]
12)2-溴-4-(3-(乙基(3-苯基丙基)氨基)丙基)苯酚;
[0097]
13)1-(4-(3-((3-(4-(苄氧基)苯基)丙基)(乙基)氨基)丙基)苯基)-3-苯基脲;
[0098]
14)乙基(4-苯基丁基)(3-苯基丙基)胺;
[0099]
15)乙基双(4-苯基丁基)胺;
[0100]
16)(4-苯基丁基)(3-苯基丙基)丙基胺;
[0101]
17)3-(4-丁氧基苯基)-n-乙基-n-(3-苯基丙基)丙-1-胺;
[0102]
18)3-(4-(丁-3-烯-1-基氧基)苯基)-n-乙基-n-(3-苯基丙基)丙-1-胺;
[0103]
19)3-(4-(4-溴丁氧基)苯基)-n-乙基-n-(3-苯基丙基)丙-1-胺;
[0104]
20)4-(4-(3-(乙基(3-苯基丙基)氨基)丙基)苯氧基)丁-1-胺;
[0105]
21)4-(3-(乙基(3-(4-甲氧基苯基)丙基)氨基)丙基)-2-氟苯酚;
[0106]
22)4-(3-((3-(4-(苄氧基)-3-氟苯基)丙基)(乙基)氨基)丙基)苯胺;
[0107]
23)n-(4-(3-((3-(4-(苄氧基)-3-氟苯基)丙基)(乙基)氨基)丙基)苯基)乙酰胺;
[0108]
24)3-(4-(苄氧基)-3-氟苯基)-n-甲基-n-(3-苯基丙基)丙-1-胺;
[0109]
25)4-(3-(乙基(3-(对甲苯基)丙基)氨基)丙基)-2-氟苯酚;
[0110]
26)n-乙基-3-苯基-n-(3-(4-(3-苯基丙基)苯基)丙基)丙-1-胺;
[0111]
27)n-乙基-3-苯基-n-(3-(4-((5-苯基戊基)氧基)苯基)丙基)丙-1-胺;
[0112]
28)n-乙基-3-苯基-n-(3-苯基丙基)丙-1-胺(即,阿尔维林);和
[0113]
29)4-[3-[乙基(3-苯基丙基)氨基]丙基]苯酚(即,4-羟基阿尔维林)。
[0114]
如本文所使用,术语“药学上可接受的盐”是指根据本领域已知的常用方法制备的盐,此类制备方法是本领域技术人员已知的。特别地,药学上可接受的盐包括来源于以下无机酸、有机酸和碱的药理学或生理学上可接受的盐,但不限于此。合适的此类酸的示例可以包括盐酸、氢溴酸、硫酸、硝酸、高氯酸、富马酸、马来酸、磷酸、乙醇酸、乳酸、水杨酸、琥珀酸、对甲苯磺酸、酒石酸、乙酸、柠檬酸、甲磺酸、甲酸、苯甲酸、丙二酸、萘-2-磺酸、苯磺酸等。来源于合适碱的盐可以包括碱金属如钠或钾,和碱土金属如镁。特别地,药学上可接受的盐可以是柠檬酸盐。在本发明的一个示例中,使用柠檬酸盐作为药学上可接受的盐。
[0115]
本发明的另一方面提供一种用于预防或治疗肌肉无力相关病症的药物组合物,其包含式1所示的化合物或其药学上可接受的盐作为活性成分。在此处,式1所示的化合物或其药学上可接受的盐与上面所描述的相同。
[0116]
肌肉无力相关病症是指由肌肉无力引起的任何和所有病症,特别是由于体内肌肉细胞减少或卫星细胞活性降低而导致成肌细胞效力降低或减弱的病症,因此有望通过促进成肌细胞分化来预防、缓解或治疗。特别地,肌肉无力相关病症可以为肌肉减少症、肌萎缩(muscular atrophy)、肌营养不良或恶病质(cachexia)。
[0117]
如本文所使用的术语“肌肉减少症”是指特征在于由老化引起的肌肉质量逐渐减少的症状,其导致肌肉力量的降低。作为肌肉减少症中肌肉质量减少的原因,卫星细胞活性降低被认为是主要原因。卫星细胞通过刺激(如运动或损伤)活化,增殖为成肌细胞,随着分化的进行,与其他细胞融合形成多核肌纤维。
[0118]
如本文所使用,术语“肌萎缩”是指特征在于四肢肌肉以接近对称的方式逐渐萎缩的症状。肌萎缩可以导致脊髓中运动神经纤维和细胞的进行性退化,并且可以导致肌萎缩侧索硬化症(amyotrophic lateral sclerosis,als)和脊髓进行性肌萎缩(spinal progressive muscular atrophy,spma)。
[0119]
如本文所使用的术语“肌营养不良”是指以肌纤维坏死为特征的退行性肌肉疾病,与中枢神经系统和外周神经系统无关。肌营养不良和肌萎缩在临床上存在细微差别。肌营养不良最常见的发病期是儿童期,肌萎缩的发病期通常在青少年时期。此外,近端肌肉发生肌营养不良,远端肌肉发生肌萎缩。肌肉僵硬存在于肌营养不良中,但不存在于肌萎缩中,而同时肌营养不良是明确的遗传性病症,但肌萎缩很少遗传。
[0120]
如本文所使用的术语“恶病质”是指可以在癌症、结核病、血友病等的末期看到的严重的全身性衰弱。此外,恶病质被认为是由体内各种器官功能障碍引起的中毒状态。恶病质的症状包括肌肉无力、体重迅速下降、贫血、嗜睡和皮肤发黄。可能导致恶病质的一些潜
在病症包括恶性肿瘤、巴塞多氏病和垂体功能减退。还发现生物活性物质(如巨噬细胞产生的肿瘤坏死因子(tumor necrosis factor,tnf))是加重恶病质的因素。
[0121]
在药物组合物中,式1所示的化合物或其药学上可接受的盐的浓度可以为10μg/ml至180μg/ml。更特别地,式1所示的化合物或其药学上可接受的盐的浓度可以为20μg/ml至160μg/ml,40μg/ml至140μg/ml,或60μg/ml至120μg/ml。
[0122]
此外,可以基于所施用的活性成分的量来确定药物组合物的剂量,所述活性成分为式1所示的化合物或其药学上可接受的盐。特别地,式1所示的化合物或其药学上可接受的盐的剂量可以为每天60mg至240mg,对于高剂量,可以在一天中进行1至3次分开的施用。优选地,式1所示的化合物或其药学上可接受的盐的剂量为60mg至120mg,可以每天施用一次或两次。
[0123]
药物组合物可以任选地包含药学上可接受的载体。载体为药物制造中常用的载体,可以包括乳糖、右旋糖、蔗糖、山梨醇、甘露醇、淀粉、阿拉伯胶、磷酸钙、海藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁、矿物油等。
[0124]
药物组合物可以进一步包含药学上可接受的添加剂,所述添加剂选自润滑剂、润湿剂、甜味剂、调味剂、乳化剂、混悬剂、防腐剂及其组合。
[0125]
药物组合物可以根据本领域常用的方法、施用途径和剂量适当地施用于受试者。特别地,可以根据本领域已知的方法选择药物组合物的合适剂量和合适给药频率,实践中药物组合物的剂量和给药频率可以由多种因素决定,如要预防或治疗的症状类型、施用途径、性别、身体状况、饮食、受试者的年龄、体重和疾病的严重程度等。
[0126]
本发明的另一方面提供一种用于促进离体成肌细胞分化的组合物,其包含式1所示的化合物或其药学上可接受的盐作为活性成分。在此处,式1所示的化合物或其药学上可接受的盐如上所述。
[0127]
如本文所使用的术语“离体”是指在“活有机体外部”提取并分离的活有机体的一部分(如细胞或组织)的状态。特别地,离体可以意味着在人工条件下“体外”对活生物体的一部分进行实验。
[0128]
成肌细胞是指处于未分化状态的肌肉细胞。在成肌细胞的分化中,单核成肌细胞融合成多核肌管。在成肌细胞的终末分化期间,肌球蛋白重链(myosin heavy chain,myhc)的表达增加。
[0129]
用于促进分化的组合物可以是含有血清的dmem分化介质,但可以包含任何能够促进成肌细胞分化的介质或组合物而没有限制。此外,该组合物可以进一步包含细胞生长或分化所需的额外材料。
[0130]
在药物组合物中,式1所示的化合物或其药学上可接受的盐的浓度可以为0.01μm至100μm。特别地,式1所示的化合物或其药学上可接受的盐的浓度可以为0.1μm至50μm,0.1μm至25μm,0.5μm至25μm,0.1μm至10μm,0.5μm至10μm,1μm至10μm,0.1μm至5μm,0.5μm至5μm,1μm至5μm,0.1μm至2μm,0.5μm至2μm,或1μm至2μm。在本发明的一个示例中,将式1所示的化合物或其药学上可接受的盐以1μm的浓度施用于小鼠来源的成肌细胞c2c12细胞。
[0131]
本发明的另一方面提供一种促进成肌细胞分化的方法,其包括用式1所示的化合物或其药学上可接受的盐处理离体成肌细胞。促进成肌细胞分化的方法可以在体外或离体
进行。
[0132]
本发明的另一方面提供一种制造肌管的方法,其包括用式1所示的化合物或其药学上可接受的盐处理离体成肌细胞,从而使成肌细胞分化。制造肌管的方法可以在体外或离体进行。
[0133]
本发明的另一方面提供一种用于预防或减轻肌肉无力相关病症的食品组合物,其包含式1所示的化合物或其营养学上可接受的盐。当作为食品添加剂使用时,食品组合物可以直接加入,或者可以与其他食品成分组合使用,可以根据常用方法适当使用。
[0134]
为了预防或减轻肌肉无力相关病症,食品组合物可以在肌肉无力相关病症发展之前或之后与用于疾病治疗的药物同时使用或独立地使用。特别地,食品组合物的特征在于促进成肌细胞的分化。肌肉无力相关病症与上述药物组合物所描述的相同。
[0135]
本发明的另一方面提供一种用于肌肉力量增强的组合物,其包含式1所示的化合物、其药学上可接受的盐或其营养学上可接受的盐作为活性成分。用于肌肉力量增强的组合物可以用作药物组合物或食品组合物。
[0136]
肌肉力量增强是指肌肉重量增加、肌肉恢复增强和肌肉疲劳减少。用于肌肉力量增强的组合物能够通过将成肌细胞分化为肌肉细胞的能力,可以增加肌肉质量并随后增加整体肌肉质量,因此可以减少肌肉疲劳。此外,肌肉细胞的快速替换能够使肌肉损伤快速恢复。本发明的用于肌肉力量增强的组合物可以用作饲料或饲料添加剂。
[0137]
本发明的另一方面提供一种预防或治疗肌肉无力相关病症的方法,其包括向受试者施用式1所示的化合物或其药学上可接受的盐。在此处,化合物、肌肉无力相关病症和受试者与上述相同。
[0138]
本发明的另一方面提供式1所示的化合物或其药学上可接受的盐用于预防或治疗肌肉无力相关病症的用途。在此处,化合物和肌肉无力相关病症与上述相同。
[0139]
本发明的另一方面提供式1所示的化合物或其药学上可接受的盐在制备用于预防或治疗肌肉无力相关病症的药物中的用途。在此处,化合物和肌肉无力相关病症与上述相同。
[0140]
发明方式
[0141]
在下文中,通过实施例详细说明本发明。以下实施例旨在进一步阐明本发明而不限制其范围。
[0142]
实验实施例1.阿尔维林柠檬酸盐促进成肌细胞分化的作用的确定
[0143]
实验实施例1.1.成肌细胞系c2cl2的培养
[0144]
c2cl2(美国典型培养物保藏中心,crl-1772
tm
)细胞是从c3h小鼠获得的成肌细胞系,用于成肌细胞分化研究。使用生长介质培养c2cl2细胞,然后使用分化介质培养以诱导分化。在此处,补充有10%胎牛血清的dmem用作生长介质(growth media,gm),补充有5%马血清(horse serum,hs)的dmem用作分化介质(differentiation media,dm)。
[0145]
实验实施例1.2.成肌细胞分化的促进
[0146]
为了证实阿尔维林柠檬酸盐促进成肌细胞分化的作用,将c2c12细胞分配在实施例1.1的gm中并培养24小时,然后用dmso、胰岛素或阿尔维林柠檬酸盐处理c2c12细胞,并诱导分化3天。随后,通过使用针对肌球蛋白h链(下文中称为myhc)的抗体进行荧光染色,观察细胞分化为肌管以及肌管厚度和直径的变化。在此处,实验中使用的dmso、胰岛素和阿尔维
林柠檬酸盐均购买自sigma-aldrich。胰岛素处理组用作阳性对照组。
[0147]
特别地,将c2c12细胞以每板5
×
105个细胞的浓度分配到经实施例1.1的gm处理的6孔板中,24小时后,用补充有5%hs的dmem介质替代并诱导分化。然后,用dmso、胰岛素(1.72μm)或阿尔维林柠檬酸盐(0.01μm、0.1μm、1μm或10μm)处理细胞。3天后,去除介质后,将细胞用磷酸盐缓冲溶液(1x pbs)洗涤,用多聚甲醛(4%)处理,在室温固定15分钟。然后,在用磷酸盐缓冲溶液(1x pbs)洗涤3次后,用透化缓冲液(permeabilization buffer)处理含有0.3%triton x-100的pbs,在室温反应10分钟。
[0148]
在用磷酸盐缓冲液(1x pbs)洗涤3次后,施用含有2%牛血清白蛋白的pbst(封闭缓冲液,含有0.5%tween 20的pbs),反应30分钟,以抑制抗体的非特异性结合。在用磷酸盐缓冲液(1x pbs)洗涤3次后,加入100μl稀释至1:500的myh3一抗(sc-20641,santa cruz biotechnology),在室温反应1小时。然后,在用磷酸盐缓冲液(1x pbs)洗涤3次后,加入100μl稀释至1:5,000的二抗(山羊抗兔igg-hrp),在室温反应1小时。1小时后,对于核染色,在用磷酸盐缓冲液(1x pbs)洗涤3次后,用稀释的dapi染料处理封闭缓冲液,在室温反应10分钟。然后,在用磷酸盐缓冲液(1x pbs)洗涤3次后,测定经洗涤的盖玻片在450nm波长的吸光度,用荧光显微镜拍摄荧光图像。使用imagej(基于java的图像处理程序)分析抗-myhc抗体染色区域。
[0149]
结果发现,用胰岛素或阿尔维林柠檬酸盐处理的成肌细胞比单独用dmso处理的成肌细胞更能分化为肌管。特别地,随着阿尔维林柠檬酸盐处理浓度的增加,肌管直径增加(图1和图2)。
[0150]
实验实施例2.使用正常小鼠确定阿尔维林柠檬酸盐的肌肉力量增强作用
[0151]
为了确认阿尔维林柠檬酸盐的肌肉力量增强作用,在将阿尔维林柠檬酸盐施用至小鼠后,测试小鼠的运动功能(如握力、跑动、平衡协调(balance coordination)等)。在运动功能测试后,测量肌肉重量。特别地,每只10周龄c57bl/6雄性小鼠口服200μl阿尔维林柠檬酸盐持续4周,每日剂量为17mg/kg/天(ac-l)、50mg/kg/天(ac-m)或150mg/kg/天(ac-h)。将该组小鼠作为实验组(图3)。10周龄c57bl/6雄性小鼠购买自daehan biolink。
[0152]
实验实施例2.1.握力测量
[0153]
使用小鼠握力计(bioseb,美国)测量握力。特别地,将小鼠放在与仪表板连接的金属网格上,通过该仪表板可以监测握力,在通过尾巴将小鼠向后拉的同时,测量小鼠抓住金属网格的握力。在此处,记录5次连续的重复测量,计算5次测量的平均值。
[0154]
作为结果,实验组小鼠的握力高于正常组小鼠的握力。通过以上,确认阿尔维林柠檬酸盐具有肌肉力量增强作用(图4)。
[0155]
实验实施例2.2.跑动能力测试
[0156]
使用专门为此实验设计的跑步机测量跑动能力。首先,通过让电刺激在起点流动来提供厌恶刺激。在测量前,使小鼠以8m/min适应10分钟。通过让各组中的小鼠在不同的跑道上跑动直到力竭来记录跑动时间。将力竭定义为当小鼠在跑道外停留10秒或更长时间而不跑动时,确定小鼠力竭并记录时间。不能在同一只小鼠上重复这个实验。将小鼠放在跑步机上,以8rpm开始测试,速度每10分钟增加2rpm,最高速度为20rpm。跑道坡度从0度坡度开始,从开始30分钟后升高至5度坡度。
[0157]
结果表明,与正常组小鼠相比,实验组小鼠的跑动时间增加,特别地,在经150mg/
kg/天阿尔维林柠檬酸盐处理的实验组中观察到跑动时间的显著增加(图5)。
[0158]
实验实施例2.3.平衡协调测试
[0159]
使用旋转杆测试(rota-rod test)来测量平衡协调。旋转杆测试装置由4个测试区(轴径为3cm,跑道宽度为9cm)、5个可旋转的圆形隔板(直径为60cm)和一个圆杆组成。测试从转速10rpm开始,速度经5分钟增加至最大40rpm,记录小鼠停留在旋转杆装置内、紧贴圆杆而不掉落的持续时间。每次测试后让小鼠休息15分钟,共进行3次测试。计算三次测量值的平均值。
[0160]
结果显示,与正常组小鼠相比,实验组小鼠紧贴圆杆的持续时间增加,随着阿尔维林柠檬酸盐施用剂量的增加,实验组小鼠紧贴圆杆的持续时间也成比例增加(图6)。
[0161]
实验实施例2.4.肌肉重量测量
[0162]
对于肌肉重量测量,取出各组小鼠后肢的腓肠肌(gastrocnemius,ga)胫骨前肌(tibialis anterior,ta)肌肉并称重。结果表明,与正常组小鼠相比,实验组小鼠的ga和ta肌肉重量增加,特别地,随着阿尔维林柠檬酸盐施用剂量的增加,实验组小鼠的ga和ta肌肉重量也增加(图7)。
[0163]
实验实施例3.使用肌肉减少症诱导的小鼠确定阿尔维林柠檬酸盐的肌肉力量增强作用
[0164]
为了确定阿尔维林柠檬酸盐的肌肉力量增强作用,向肌肉减少症诱导的小鼠施用阿尔维林柠檬酸盐并测试跑动能力。在跑步机跑动测试后,测量肌肉重量。特别地,使用外科缝合器(autosuture royal 35w缝合器)固定10周龄c57bl/6雄性小鼠的后肢。5天后移除缝合器,让小鼠重新活动3天。这之后,测量跑动能力。小鼠口服200μl阿尔维林柠檬酸盐,每只小鼠剂量为17mg/kg/天(ac-l)、50mg/kg/天(ac-m)或150mg/kg/天(ac-h),将这些小鼠设置为实验组。将未经处理的肌肉减少症诱导的小鼠设置为对照组(图8)。10周龄c57bl/6雄性小鼠购买自daehan biolink。
[0165]
实验实施例3.1.跑动能力测试
[0166]
通过与实施例2.2相同的方法测量跑动能力。结果发现,与正常组小鼠相比,对照组小鼠的跑动时间减少约10分钟。另一方面,实验组小鼠的跑动时间随着阿尔维林柠檬酸盐的剂量浓度成比例地增加,特别地,与正常小鼠相比,口服150mg/kg/天(ac-h)剂量阿尔维林的实验组的跑动时间增加。
[0167]
实验实施例3.2.肌肉重量测量
[0168]
对于肌肉重量测量,取出各组小鼠后肢的ga和ta肌肉并称重。结果发现,与正常组相比,对照组的ga和ta肌肉重量显著降低。然而,在实验组的情况下,随着阿尔维林柠檬酸盐剂量浓度的增加,实验组小鼠的ga和ta肌肉重量也增加(图10)。
[0169]
实验实施例4.4-羟基阿尔维林促进成肌细胞分化的作用的确定
[0170]
为了确定4-羟基阿尔维林促进成肌细胞分化的作用,按照与实施例1相同的方法,分别施用dmso、胰岛素(1.72μm)、阿尔维林柠檬酸盐(0.01μm、0.1μm、1μm或10μm)、4-羟基阿尔维林(0.01μm、0.1μm、1μm或10μm),观察细胞向肌管的分化以及肌管厚度和直径的变化。在此处,阿尔维林和4-羟基阿尔维林如表1所示。
[0171]
[表1]
[0172][0173][0174]
结果发现,用阿尔维林柠檬酸盐或4-羟基阿尔维林处理的成肌细胞比用dmso或胰岛素处理的成肌细胞更能分化为肌管(图11和图12)。当在相同浓度下比较时,4-羟基阿尔维林的分化促进作用优于阿尔维林。
[0175]
实验实施例5.阿尔维林柠檬酸盐和4-羟基阿尔维林的恶病质治疗作用的确定
[0176]
为了确定阿尔维林柠檬酸盐和4-羟基阿尔维林的恶病质治疗作用,作为离体方法进行了通过癌细胞条件介质(conditioned medium,cm)处理来模拟肿瘤生长环境的实验。首先,使用c26癌细胞系制备癌细胞cm。在此处,作为癌细胞生长介质(growth media,gm),使用补充有10%胎牛血清的rpmi 1640介质。使用100mm细胞培养板和癌细胞gm培养c26癌细胞系。在此处,当细胞融合达到90%时去除介质。然后,在用磷酸盐缓冲液(1x缓冲液)洗涤后,按照与实施例1相同的过程处理制备的分化介质。24小时后,获得c26癌细胞系cm,在使用前使用瓶顶过滤器(thermo,pes,1l)过滤。
[0177]
将c2c12细胞以每板5
×
105个细胞的浓度分配到经实施例1.1的gm处理的6孔板中,24小时后,用补充有5%hs的dmem介质替代并诱导分化。4天后,用补充有33%cm的分化介质处理分化的肌管并诱导肌管萎缩持续3天。在此处,通过用1μm阿尔维林柠檬酸盐(ac)和4-羟基阿尔维林(4ha)处理实验组,评价抑制肌管萎缩的作用。dmso用作阴性对照组,乌索酸(ursolic acid,ua)用作阳性对照组。按照与实施例1.2相同的方法,通过使用针对myhc的抗体进行荧光染色,测量myhc的表达量。
[0178]
结果发现,阴性对照组的肌管因cm而萎缩。另一方面,发现当用阿尔维林柠檬酸盐或4-羟基阿尔维林处理时肌管萎缩被抑制(图13和图14)。
[0179]
实施例1.阿尔维林衍生物促进成肌细胞分化的作用的确定
[0180]
实施例1.1.成肌细胞系c2cl2的生长
[0181]
c2cl2(美国典型培养物保藏中心,crl-1772
tm
)细胞是从c3h小鼠获得的成肌细胞系,用于成肌细胞分化研究。使用生长介质培养c2cl2细胞,然后使用分化介质培养以诱导分化。在此处,补充有10%胎牛血清的dmem用作生长介质(gm),补充有5%马血清(hs)的dmem用作分化介质(dm)。
[0182]
实施例1.2.成肌细胞系的分化的加速
[0183]
为了确定阿尔维林衍生物促进成肌细胞分化的作用,将c2c12细胞分配在实施例1.1的gm中并培养24小时。然后,用dmso(sigma-aldrich)、胰岛素、阿尔维林(sigma-aldrich)或27种阿尔维林衍生物处理c2c12细胞,每种的浓度均为1μm,诱导分化4天。然后,使用针对myhc的抗体进行荧光染色来监测肌管的分化以及肌管厚度和直径的变化。在此处,27种阿尔维林衍生物是由韩国生物科学与生物技术研究所和jd生物科学根据要求设计
并合成的,实验中使用的阿尔维林和27种阿尔维林衍生物1至27如下表2所示。
[0184]
[表2]
[0185]
[0186]
[0187][0188]
特别地,将c2c12细胞以每板5
×
105个细胞的浓度分配到经实施例1.1的gm处理的6孔板中,24小时后,用补充有5%hs的dmem介质替代并诱导分化。然后,用dmso、阿尔维林或27种阿尔维林衍生物以1μm的浓度处理细胞。4天后,去除介质后,将细胞用磷酸盐缓冲液(1x pbs)洗涤,用多聚甲醛(4%)处理,在室温固定15分钟。然后,在用磷酸盐缓冲液(1x pbs)洗涤3次后,用透化缓冲液处理含有0.3%triton x-100的pbs,在室温反应10分钟。
[0189]
在用磷酸盐缓冲液(1x pbs)洗涤3次后,施用含有2%牛血清白蛋白的pbst(封闭缓冲液,含有0.5%tween 20的pbs),反应30分钟,以抑制抗体的非特异性结合。在用磷酸盐缓冲液(1x pbs)洗涤3次后,加入100μl稀释至1:500的myh3一抗(sc-20641,santa cruz biotechnology),在室温反应1小时。然后,在用磷酸盐缓冲液(1x pbs)洗涤3次后,加入100μl稀释至1:5,000的二抗(山羊抗兔igg-hrp),在室温反应1小时。1小时后,对于核染色,在用磷酸盐缓冲液(1x pbs)洗涤3次后,用稀释的dapi染料处理封闭缓冲液,在室温反应10分
钟。然后,在用磷酸盐缓冲液(1x pbs)洗涤3次后,测定经洗涤的盖玻片在450nm波长的吸光度,用荧光显微镜拍摄荧光图像。
[0190]
结果证实,与单独用dmso处理的成肌细胞相比,用27种阿尔维林衍生物中每一种处理的成肌细胞也都促进了向肌管的分化,就像用阿尔维林处理的成肌细胞一样。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。