一种i型胶原羧基端肽抗体包被的磁性微粒及其制备方法与试剂盒
技术领域
1.本发明属于试剂盒技术领域,涉及一种i型胶原羧基端肽抗体包被的磁性微粒及其制备方法与试剂盒。
背景技术:
2.骨质疏松症是以骨量减少,骨微观结构退化为特征,致使骨的脆性及骨折危险性增加的全身性骨骼疾病。骨量减少,应包括骨矿物质和骨基质等比例的减少,仅骨矿物质减少,骨基质不减少,是矿化障碍所致,对儿童来说则为佝偻病,对成年人则为骨软化症。微观结构退化,由骨吸收所致,表现为皮质骨更薄,骨小梁变细、变稀,乃至断裂,这实际上是一种微骨折,致使周身骨骼疼痛。该病可发生于不同性别和年龄,但多见于绝经后妇女和老年男性,已成为全球重要的健康问题之一。近年来,随着人口老龄化社会的到来,高龄老年骨质疏松症患者越来越多。高龄老年骨质疏松症的发生与高龄老人体内性激素(包括雌性激素和雄性激素)水平下降、营养物质摄入减少、活动量下降、某些疾病等因素有关。
3.i型胶原羧基端肽(c-terminal telopeptide of type i collagen,ctx-i)是破骨细胞分解i型胶原后的产物,也是国际骨质疏松基金会推荐临床应用的主要骨转换标志物之一。大量临床研究表明,ctx-i不仅与老年人髋部和腰椎骨密度呈负相关,而且是老年人骨折的重要预测因子。因此,多采用测定i型胶原羧基端肽来进行骨质疏松症的检测,能够及时诊治,避免病症的加重。
4.中国专利申请文件(公开号:cn102650637a)公开了采用酶联免疫法,检测尿β-胶原降解产物,虽然有较好的特异性、灵敏度,但是该试剂盒的制备过程和检测过程均需要微孔板,步骤繁琐。中国专利申请文件(公开号:cn104694639b)公开了用于扩增mir-214的引物,以及用于从血液中提取mirna的试剂组成一种血液检测试剂盒进行检验,证明了mir-214的水平与骨吸收速率的敏感指标i型胶原羧基端(ctx)的量呈现显著的正相关(r2=0.4864);并且检出率为94.7%。但是该试剂盒进行的是定量pcr检测,操作技术要求高,实验过程中生物污染较大,含毒物品较多,检测时间长,对检测人员要求高,不适于广泛应用。因此需要研发一种操作简单,检测速度快,结果准确,人为因素影响小的试剂盒。
技术实现要素:
5.本发明的目的是针对现有技术存在的上述问题,提出了一种i型胶原羧基端肽抗体包被的磁性微粒的制备方法,并且制得的i型胶原羧基端肽抗体包被的磁性微粒组成了一种具有良好特异性、精密度的磁微粒化学发光法测定人血中i型胶原羧基端肽的试剂盒。
6.本发明的目的可通过下列技术方案来实现:
7.一种i型胶原羧基端肽抗体包被的磁性微粒的制备方法,包括如下步骤:
8.1)预处理:用ph7.5~8.0的0.01~0.05m pbst缓冲液进行清洗,再用ph7.5~9.5的0.01~0.05m硼酸缓冲液1进行清洗后,再用ph9.0~10.0的0.05~0.2m硼酸缓冲液2将磁
性微粒稀释至5~20mg/ml;
9.2)混悬反应:将预处理的磁性微粒与i型胶原羧基端肽抗体反应,并加入与0.05~0.2m硼酸缓冲液2具有相同ph的1~4m硫酸铵进行混悬反应,加入体积为磁珠体积的一半,再加入i型胶原羧基端肽抗体进行反应,抗体加入量为0.005~0.03mg每毫克磁珠,24~42℃震荡反应20~40小时;
10.3)封闭处理:反应后磁珠进行清洗,用ph至7.0~~8.0的0.05~0.2m硼酸缓冲液3进行清洗、混匀,每毫克磁珠再加入10ul封闭剂进行封闭反应,20~42℃震荡反应24~40小时,经清洗、稀释得i型胶原羧基端肽抗体包被的磁性微粒。
11.步骤1中用pbst清洗,是为去除磁珠原有保存缓冲液的影响成份,用ph7.5~9.5的0.01~0.05m硼酸缓冲液1进行清洗,是为调整磁珠的缓冲体系,再用反应缓冲液混匀,准备进行反应。步骤2中硫酸铵与缓冲液的ph相同的目是使缓冲体系整体保持一致,保持磁珠基团的活性。步骤3中用ph至7.0~8.0的0.05~0.2m硼酸缓冲液3进行清洗、混匀,再加入封闭剂是为了调整ph到封闭剂最适ph范围,使封闭剂中的蛋白更换与磁珠结合,封闭掉多余的位点,把非共价结合的抗体置换下去。
12.作为优选,所述磁性微粒为粒径0.5~3μm的甲苯磺酰基磁性微粒。
13.进一步优选,所述磁性微粒的粒径为0.5~1μm。
14.作为优选,所述硫酸铵的浓度为2.5~3.5m。
15.作为优选,所述混悬反应温度为20~30℃,时间为30~40h。
16.作为优选,所述封闭反应温度为20~30℃,时间为20~40h。
17.本发明在封闭反应时保持较低温度能更好的保证抗体的活性,并且延长时间使反应更充分,提高标记率。
18.作为优选,所述封闭剂包括ce210、1~5%bsa,0.5~5%鱼皮明胶、0.5~5%酪蛋白中的一种或多种。
19.进一步优选,所述封闭剂中包括质量比为1:(0.01~0.05):(0.001~0.01):(0.001~0.01)的ce210、bsa、鱼皮明胶、酪蛋白。
20.本发明封闭剂中以ce210为主要封闭剂,其它蛋白进行补充封闭,调整抗体与磁珠连接的空间位点。
21.作为优选,所述预处理的磁性微粒与i型胶原羧基端肽抗体的质量比为1:(50~200)。
22.本发明还公开了一种i型胶原羧基端肽抗体包被的磁性微粒。
23.作为优选,所述i型胶原羧基端肽抗体包被的磁性微粒的工作浓度为5~20mg/ml。
24.本发明也公开了一种磁微粒化学发光法测定人血中i型胶原羧基端肽的试剂盒,包括:i型胶原羧基端肽抗体包被的磁性微粒、碱性磷酸酶标记的i型胶原羧基端肽抗体、i型胶原羧基端肽校准品、质控品。
25.作为优选,所述i型胶原羧基端肽校准品的制备方法包括采用稀释液将i型胶原羧基端肽抗原稀释至0.01~0.02mg/ml。
26.进一步优选,所述每升稀释液中包括0.05~0.08mpbs、0.8~1.2g猪皮明胶、8~10gnacl、8~12g胰蛋白胨、45~55g海藻糖、0.5~0.8%表面活性剂s7、0.1~0.3%蛋白保护剂001、0.1~0.2%曲拉通405、0.2~0.5%proclin
tm
300缓冲液,ph为7.2~7.6。
27.更进一步优选,所述蛋白保护剂001的ph为6~6.8。
28.蛋白保护剂001的作用是保护抗原的生物活性,使其更稳定。
29.作为优选,所述碱性磷酸酶标记的i型胶原羧基端肽抗体的磁性微粒的制备方法包括:活化后的i型胶原羧基端肽抗体与活化后的碱性磷酸酶按照质量比为1:1混合,再加入体积为反应总体积的1
‰
~5
‰
毫升0.1~0.5m氯化镁溶液,纯化后备用。
30.与现有技术相比,本发明具有以下有益效果:
31.1、本发明通过使用含有多种不同的蛋白混合封闭剂缓冲液,并降低封闭反应温度,延长封闭反应时间,有效的调整抗体与磁性微粒结合的空间构象,封闭磁性微粒上更多的未使用位点,从而降低样本中的物质与抗体、磁性微粒之间的非特异性反应,使磁性微粒分散效果更好,进一步提高试剂的灵敏度、重复性、特异性、降低信噪比,稳定性更好。
32.2、本发明先用pbst清洗磁珠,是为去除磁珠原有保存缓冲液的影响成份,再用硼酸缓冲液1进行清洗,是为调整磁珠的缓冲体系,再用ph较大的硼酸缓冲液2稀释,准备进行反应;反应后又采用硼酸缓冲液3调整ph到封闭剂最适ph范围,使封闭剂中的蛋白更换与磁珠结合,封闭掉多余的位点,把非共价结合的抗体置换下去;均有利于增加试剂盒的准确度和稳定性。
33.3、本发明采用与硼酸缓冲液2具有相同ph的硫酸铵进行混悬反应,使缓冲体系整体保持一致,制得的试剂盒能够获得更优的最低检测限。
34.4、本发明调整校准品稀释液,使i型胶原羧基端肽抗原更容易保存,并保持了i型胶原羧基端肽的生物活性不影响检测,同时也使i型胶原羧基端肽校准品更加稳定,延长试剂使用周期。
35.5、采用本发明的试剂盒操作简单,检测速度快,结果准确,人为因素影响小。
36.说明书附图
37.图1为本发明制得的磁微粒化学发光法测定人血中i型胶原羧基端肽的试剂盒中校准品测试发光标准曲线图。
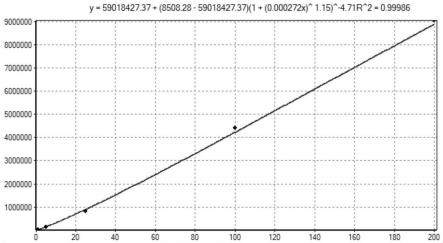
38.图2为本发明制得的磁微粒化学发光法测定人血中i型胶原羧基端肽的试剂盒的样本测试相关性测试结果图。
具体实施方式
39.以下是本发明的具体实施例,对本发明的技术方案作进一步的描述,但本发明并不限于这些实施例。
40.磁性微粒购自jsr;
41.碱性磷酸酶购自bbi,alpi2g;
42.曲拉通405购自sigma;
43.表面活性剂s7购自西宝生物;
44.蛋白保护剂001购自西宝生物;
45.bsa(牛血清白蛋白)购自pranlint;
46.鱼皮明胶购自sigma;
47.酪蛋白购自sigma;
48.pd-10脱盐柱购自ge,17-0851-01;
49.其他i型胶原羧基端肽检测试剂盒购自ids(艾狄斯,ac-02f1);
50.其余原料均为常规的市售品。
51.实施例1
52.1)i型胶原羧基端肽抗体包被的磁性微粒:
53.预处理:将粒径为1μm的甲苯磺酰基磁性微粒用ph7.5的0.01m pbst缓冲液进行清洗,再用ph7.5的0.01m硼酸缓冲液1进行清洗,最后用ph9.5的0.05m硼酸缓冲液2进行清洗后再用该硼酸缓冲液将磁性微粒稀释至5mg/ml;
54.混悬反应:按照磁性颗粒:i型胶原羧基端肽抗体质量比为1:25混合,并加入ph9.5的3m硫酸铵在室温混悬反应30h,硫酸铵的加入量为磁性颗粒与抗体总体积的2倍;
55.封闭处理:反应后磁珠进行清洗,用ph7.5
±
0.1的0.1m硼酸缓冲液3重新混匀,每毫克磁珠再加入10ul封闭剂在室温封闭反应20h;其中封闭剂包括质量比为100:2:0.6:0.6的ce210、bsa,鱼皮明胶、酪蛋白;然后使用0.1m tris缓冲液对磁珠进行清洗,用稀释液稀释到10mg/ml,获得i型胶原羧基端肽抗体包被的磁性微粒,2~8℃保存待用;使用时进行含有0.05m tris、1%bsa、1%鱼皮明胶、0.2%proclin
tm
300 ph8.0的稀释液进行稀释,终浓度0.5mg/ml。
56.2)碱性磷酸酶标记的i型胶原羧基端肽抗体:
57.活化抗体:将抗体用pd-10脱盐柱更换为无氨基及巯基缓冲液,用浓缩管浓缩到3mg/ml,使用三(2-羰基乙基)磷盐酸盐(tcep),按抗体体积每毫升加入1
‰
微升,室温反应20分钟;加入与tcep相同体积的1m甘氨酸ph7.3,室温反应7分钟。使用pd-10脱盐柱更换缓冲液,浓缩到3mg/ml备用。
58.活化碱性磷酸酶:将抗体用pd-10脱盐柱更换为无氨基及巯基缓冲液,用浓缩管浓缩到3mg/ml,使用dmf溶解至5mg/ml的smcc,按抗体体积每毫升加入1
‰
微升,室温反应15分钟;加入与smcc相同体积的1m甘氨酸ph7.3,室温反应7分钟。使用pd-10脱盐柱更换缓冲液,浓缩到3mg/ml备用。
59.将活化后的i型胶原羧基端肽抗体与活化后的碱性磷酸酶按照质量比为1:1混合,再加入体积为反应总体积的3
‰
毫升0.2m氯化镁溶液在3℃反应30h,纯化后备用;使用时通过含有0.05m tris、1%bsa、1%海藻糖、0.2%tween20、1%鱼皮明胶、1mm氯化镁、0.2%proclin
tm
300 ph6.0的稀释液进行稀释,工作浓度为0.3μg/ml。
60.3)i型胶原羧基端肽校准品:
61.用稀释液将i型胶原羧基端肽抗体稀释至0.015mg/ml;每升稀释液中含有0.05mpbs、1g猪皮明胶、9gnacl、10g胰蛋白胨、50g海藻糖、0.5%表面活性剂s7、0.1%蛋白保护剂001、0.1%曲拉通405、0.2%proclintm300缓冲液,其ph为7.4。
62.4)具体检测过程:
63.将i型胶原羧基端肽抗体包被的磁性微粒和待测样本、碱性磷酸酶标记的i型胶原羧基端肽抗体在37℃孵育10min,形成磁性复合物悬浮液;将所述的磁性复合物悬浮液置于磁场内,磁分离2min,洗涤所述磁性复合物;向洗涤后的磁性复合物中加入化学发光底物液,检测化学发光光子强度。
64.对比例1
65.与实施例1的区别在于,i型胶原羧基端肽抗体包被的磁性微粒的制备方法包括:
将粒径为1μm的磁性颗粒用ph7.0的hepes缓冲液进行清洗并稀释至5mg/ml;按照磁性颗粒、i型胶原羧基端肽抗体质量比为1:100混合后,加入3m硫酸铵,37℃反应18h,直接用仅含ce210的封闭液进行封闭处理。
66.将对比例1中的抗体包被的磁性微粒制成的试剂盒(以下简称普通试剂盒)、本发明制得的i型胶原羧基端肽抗体包被的磁性微粒试剂盒(以下简称本发明试剂盒)同时进行检测,具体的性能测试如下:
67.实验1、标准曲线
68.两个试剂盒使用相同工作浓度,平行检测校准品0ng/ml、1ng/ml、5ng/ml、25ng/ml、100ng/ml、200ng/ml,计算平均发光值,用四参数方程拟合标准曲线。校准品测试发光值如表1所示,标准曲线如图1所示。
69.表1、校准品测试发光值
[0070][0071][0072]
根据表1和图1的结果可知,i型胶原羧基端肽优化后试剂检测校准品反应梯度更好,信噪比更低,曲线拟合度r2=0.99986,改善效果明显。
[0073]
实验2、最低检测限和检出限性能测试
[0074]
两个试剂盒平行测定20次零值校准品的发光值(rlu),计算其平均值(m)和标准差(sd),得出m 2sd所对应的rlu值,根据零浓度校准品和相邻校准品之间的浓度-发光值(rlu)结果进行两点回归拟合得出一次方程,将m 2sd发光值带入上述方程中,求出对应的浓度值,结果不高于最低检测限值(0.2ng/ml)。结果如表2所示。
[0075]
表2、最低检测限测试结果
[0076]
测试次数普通试剂盒本发明试剂盒141173852126497085313522218536444974851955716384966539828540754531839187483385129522298594104618283421162919832012692398461
1342788839114485058591156040583761678699849417513358520187771284231956933831420556678490最低检测限0.860ng/ml0.009ng/ml
[0077]
两个试剂盒分别与5份浓度近似检出限(1ng/ml)的低值样本进行检测,每份样本检测5次,低于最低检测限(0.2ng/ml)的检测结果小于或等于3个,无高于检出限(1ng/ml)的数值。结果如表3所示。
[0078]
表3、检出限测试结果
[0079][0080]
根据表2和表3可知,本发明的i型胶原羧基端肽试剂盒最低检测限为0.2ng/ml,检出限为1ng/ml。
[0081]
实验3、线性关系
[0082]
取接近线性范围上限的高浓度样本和接近线性范围下限的低浓度样本,按照一定比例混合成至少5个稀释浓度。每个稀释浓度测试3次,计算出检测结果均值。以稀释浓度作为自变量,检测结果均值作为应变量,求出线性回归方程,计算相关系数r。结果如表4所示。
[0083]
表4、线性测试结果
[0084][0085]
如表4所示,虽然在浓度为1~200ng/ml的范围内,两者的线性检测均符合要求,相关系数r》0.99,但普通试剂盒各点偏差较大。
[0086]
实验4、精密度
[0087]
取本发明试剂盒、普通试剂盒中的高值质控品、中值质控品和低值质控品各一份,各重复测试10次,计算平均值和标准差。根据公式:变异系数cv=(标准差/平均值)
×
100%,计算精密度。结果如表5所示。
[0088]
表5、精密度测试结果
[0089][0090]
根据表5可知,普通试剂盒的高中低值质控检测结果的cv均大于10%,不符合要求;而本发明试剂盒的高中低值质控检测结果的cv均小于3%,符合要求,改善效果明显。
[0091]
实验5、稳定性
[0092]
将本发明试剂盒中校准品、磁珠工作液分别储存于37℃和2~8℃,储存于37℃时于第0天、第7天,测试两次发光值(rlu),计算平均值,并与第0天结果计算相对偏差;结果如表6、表7所示。试剂盒储存于2~8℃时于第0个月、第6个月、第9个月、第12个月和第14个月,测试两次发光值(rlu),计算平均值,并与第0个月结果计算相对偏差,结果如表8所示。
[0093]
表6、校准品37℃稳定性测试结果
[0094][0095]
表7、磁珠工作液37℃稳定性测试结果
[0096][0097]
表8、试剂盒2~8℃稳定性测试结果
[0098][0099]
表6、8中的数据显示校准品的所有相对偏差均《10%,试剂稳定性良好;表7中数据显示本发明的试剂盒具有更好的稳定性,即通过本发明中i型胶原羧基端肽抗体包被的磁
性微粒及优化后的稀释液可以使试剂的稳定性更好,有助于延长定标周期,延长试剂周期。
[0100]
实验6、相关性
[0101]
取200份血清样本,将本发明的试剂盒与ids的i型胶原羧基端肽检测试剂盒进行检测结果的相关性测试,结果如图2所示。
[0102]
从图2可知,两个试剂线性回归方程y=0.9806x 1.115,相关系数r2=0.9813;即本发明的i型胶原羧基端肽试剂盒检测样本与ids产品结果一致。
[0103]
综上所述,本发明通过优化磁珠,并且控制反应过程中的ph值,使磁珠能更好地与抗体结合;并且通过使用含有不同种类的蛋白混合封闭剂缓冲液,并降低封闭反应温度,延长封闭反应时间,有效的调整抗体与磁性微粒结合的空间构象,封闭磁性微粒上更多的未使用位点,从而降低样本中的物质与抗体、磁性微粒之间的非特异性反应,使磁性微粒分散效果更好,进一步提高试剂的灵敏度、重复性、特异性、降低信噪比,稳定性更好。
[0104]
本文中所描述的具体实施例仅仅是对本发明精神作举例说明。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,但并不会偏离本发明的精神或者超越所附权利要求书所定义的范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。