sars-cov-2快速检测测试
1.相关申请的交叉引用
2.本发明要求2020年2月9日提交的美国临时专利申请号为62/972005的优先权,其全部内容通过引用整体并入本文。
3.序列表声明
4.与本发明同时提交的、创建于2021年2月9日,名为82013序列表.txt(82013sequencelisting.txt)的ascll文件包括70,597,807字节,该文件通过引用并入本文。
技术领域
5.本发明总体上涉及病毒传感(viral sensing)和快速诊断领域,具体而言,涉及用于检测测试样本中sars-cov-2的方法、试剂和试剂盒。该方法涉及3c-l蛋白酶的检测。
背景技术:
6.及时准确的covid-19检测是当前流行病管理的重要组成部分。covid-19的病原体是严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,sars-cov-2),其是冠状病毒科(family coronaviridae)、冠状病毒亚科(subfamily coronavirinae)、包括sars-3和mers-3病毒的β冠状病毒属(genusβcoronaviridae)的新成员。这些病毒涉及在过去二十年中爆发的严重急性呼吸综合征(severe acute respiratory syndrome,sars)。us 10130701 b2描述了包含变体复制酶基因的减毒冠状病毒sars-cov,其导致病毒具有降低的致病性。
7.sars-cov-2病毒基因组是一种单链、正义的rna,大小约为30kb,其包含许多开放阅读框(open-reading frames)。三分之二的病毒基因组编码16种非结构蛋白(nsp1-16),而剩余的基因组编码4种结构和9种辅助蛋白(orf3a、orf3b、orf6、orf7a、orf7b、orf8、orf9b、orf9c和orf10)。几种非结构蛋白具有酶活性,例如蛋白酶活性和rna指导的rna聚合酶活性。
8.sars-cov-2在鼻和口中的复制水平比sars-cov和mers高得多,这导致有症状前或无症状的人在环境中传播的病毒水平高得多。因此,很大比例的感染者可以传播病毒,而没有意识到自己已经被感染。由于这些原因,快速、低成本和准确的sars-cov-2检测方法对于显著减慢病毒传播和用于未来的群体监测是至关重要的。
9.目前,定量实时聚合酶链式反应(quantitative real time polymerase chain reaction,qrt pcr)的分子技术是使用来自呼吸道分泌物的样本进行sars-cov-2检测的金标准(gold standard)。pcr测试(pcr tests)的循环阈值(cycle threshold,ct)值指示在pcr中用于靶样本的指数扩增的ct,与样本中的病毒载量成反比。ct40是可以通过高端pcr技术检测的可接受的最小病毒载量。然而,如上所述,对于下游应用进行大量pcr反应的成本和组织复杂性使得这种选择可行但没有吸引力。此外,sars-cov-2病毒会随着时间的推移而发生突变(mutating),导致循环病毒株群体的遗传变异(genetic variation),这些变
异通过常规pcr测试变得难以区分。因此,如果通过该测试评估的病毒基因组的部分发生了某种特定的突变,则任何用于检测sars-cov-2的分子测试都经常出现假阴性结果(negative results)。最后,基于pcr的测定(pcr-based assays)可产生假阳性结果(positive results),因为它们无法区分来自活病毒、死病毒、腐烂病毒或失活病毒的核酸片段。
10.最近,基于酶联免疫吸附测定(enzyme-linked immunosorbent assay,elisa)和旨在检测针对病毒的抗体或病毒抗原本身的快速测试,已经开发了几种其它分子测定来检测当前的sars-cov-2病毒。然而,这些免疫化学测定中的大多数最近由于大量假阴性或假阳性结果而失败了。这些测定也存在同样的问题,即不能区分活性或非活性病毒产物。
11.此外,针对新病毒的特定蛋白质的抗体可能不是即时和持续可用的(例如,单克隆抗体)。抗体的产生使用生物系统。为了产生抗体,诱导免疫应答(immune response)是必要的。然而,这种方法可能会鉴别出与内源性蛋白质结构相似的靶蛋白质(target proteins)或会杀死动物的有毒化合物。体内产生抗体的另一个并发症是抗体只能在生理条件下起作用。这限制了抗体的应用范围和功能。值得注意的是,elisa的最后一个但并非最不重要的问题是,不同动物产生的相同抗体在结构和功能上可能存在显著差异。因此,用于检测某种分析物的任何基于elisa的生物测定或生物传感系统在灵敏度和特异性方面会有所不同,并且可能难以校准和通用化。
12.因此,尽管几十年来抗体识别一直是金标准,但是上述许多问题大量涉及新设计、有限的蛋白质贮存寿命、耗时的洗涤程序和生产规模扩大中。这些问题是可以克服的,但只能通过付出巨大代价的艰苦研究程序来解决。尽管最近已经开发了上述pcr方法和免疫测定法来检测sars-cov-2病毒的存在或暴露于sars-cov-2病毒,但是它们不能区分活性与降解的病毒残余物。由于现有检测方法的不足,需要一种改进的检测方法,其能够在感染的早期阶段准确且快速地检测病毒如sars-cov-2病毒的存在。这样的测试将使那些表现出covid-19症状的人受益,因为它允许监测他们的感染过程和随后的恢复。此外,快速、灵敏和选择性的测试将使疑似感染者受益,因为它允许未感染者免于隔离。还需要自动测试来避免人工干预的需要。这种测试将防止疾病在测试过程中由于感染而扩散。
13.在许多病毒的复制过程中,病毒遗传物质被转录和翻译形成多蛋白,多蛋白最终被必需的病毒编码的半胱氨酸蛋白酶切割(cleave)成具有生物活性的蛋白质。3c样蛋白酶(3c-like protease,3clpro),正式名称为c30内肽酶(c30 endopeptidase),是在冠状病毒中发现的主要蛋白酶。它在11个保守位点切割冠状病毒多聚蛋白,它是在sars-cov-1和sars-cov-2中发现的主要蛋白酶,负责病毒复制。两种病毒都具有这种3c-样半胱氨酸蛋白酶(3c-like cysteine protease),其表现出与小核糖核酸病毒3c蛋白酶相似但不相同的切割位点特异性,因此被称为“3c-样蛋白酶(3c-like protease)”,3cl蛋白酶(3cl protease)。本发明人的us 7635557描述了用于检测样本中sars-cov-1病毒的方法、组合物和试剂盒。该方法通过使样本与能够被3cl蛋白酶切割以形成肽化合物片段的肽化合物接触来确定3cl蛋白酶的存在。肽化合物片段的检测证实了病毒的存在。
14.3cl蛋白酶活性的定量给病毒诊断提供了独特的方法。诊断测试的前提是收集临床样本,例如鼻咽拭子、唾液、颊拭子(buccal swab)等,并在肽底物存在下孵育,所述肽底物含有与特定分析探针连接的独特病毒切割序列,例如氨基和羧基末端的供体和淬灭剂荧
光团。然后可以通过肽切割检测活性sars cov-2 3cl蛋白酶的存在,随后可以通过肽切割来检测,这导致可以用任何合适的分析技术,例如荧光或发光光谱、太赫兹光谱(terahertz spectroscopy)、横向流(lateral flow)等容易地定量视觉信号。
技术实现要素:
15.除非另有定义,本文中使用的所有技术和/或科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。尽管与本文所述的那些类似或等同的方法和材料可用于实践或测试本发明的实施方式,但下文描述了示例性方法和/或材料。如有冲突,以专利说明书(包括定义)为准。此外,材料、方法和实施例仅是说明性的,并不意味着必须是限制性的。
16.本发明实施方式的方法和/或装置的实现可以涉及手动、自动或其组合来执行或完成所选择的任务。此外,根据本发明的方法和/或装置的实施方式的实际仪器和设备,可以使用操作系统通过硬件、软件或固件或其组合来实现几个所选择的任务。
17.例如,根据本发明的实施方式,用于执行所选择的任务的硬件可以通过芯片或电路实现。作为软件,根据本发明的实施方式,所选择的任务可以被实现,为由使用任何合适的操作系统的计算机执行的多个软件指令。在本发明的示例性实施方式中,根据本文描述的方法和/或装置的示例性实施方式的一个或多个任务由数据处理器执行,例如用于执行多个指令的计算平台。可选地,数据处理器包括用于存储指令和/或数据的易失性存储器和/或用于存储指令和/或数据的非易失性存储器,例如磁性硬盘和/或可移动介质。可选地,还提供网络连接。还可选地提供显示器和/或用户输入设备(例如键盘或鼠标)。
18.本发明描述了一种诊断主体样本中严重急性呼吸综合征冠状病毒2(sars-cov-2)感染的方法,所述方法包括使所述样本与包含检测所述sars-cov-2病毒的3cl-蛋白酶的试剂的组合物接触,其中所述样本中所述3cl-蛋白酶的存在指示sars-co-v2感染。
19.在另一个实施方式中,在疑似患有covid-19的主体的样本中检测sars-cov-2病毒的方法,所述方法包括使所述样本与包含监测sars-cov-2病毒的3cl蛋白酶的活性的试剂的组合物接触,其中所述样本中所述3cl蛋白酶的活性水平指示所述样本中sars-cov-2的存在。
20.在具体实施方式中,所述样本选自由以下部分组成的组:粘液、唾液、咽喉洗液、鼻洗液、脊髓液、痰液、尿液、精液、汗液、粪便、血浆、血液、支气管肺泡液、阴道液、泪液、组织活检,以及鼻咽、口咽、鼻中鼻甲、前鼻和颊拭子。
21.在其他实施方式中,所述可检测部分是荧光部分。在一个具体实施方式中,所述可检测部分是供体和受体部分的福斯特共振能量转移(resonance energy transfer,fret)对,并且底物肽的切割产生或调节来自fret对的信号。特定的供体部分是量子点。
22.在一些实施方式中,所述供体和受体部分以允许能量从所述供体转移到所述受体的构型连接到所述肽上,从而通过fret过程淬灭荧光。在一些其它实施方式中,所述供体部分和受体部分间隔不超过3、5、10、15或20个氨基酸残基。
23.在另一个实施方式中,所述受体部分是辐射性或非辐射性的。用于本发明的所述受体的具体示例是四甲基-6-羧基罗丹明(tetramethyl-6-carboxyrhodamine,tamra)和黑
洞淬灭剂(black hole quenchers,bhqs),所述黑洞淬灭剂包括黑洞淬灭剂-1(bhq-1)、黑洞淬灭剂-2(bhq-2)、黑洞淬灭剂-3(bhq-3)。具体的fret对是alexa488(af488)(供体)/bhq1(受体)、af488(供体)/qsy9(受体)、edans(供体)/dabcyl(受体)
[0024][0025][0026]
在其他实施方式中,所述肽的c-末端与所述受体部分连接,所述肽的n-末端与所述供体部分连接。在其它实施方式中,所述肽的c-末端与所述受体部分连接,所述供体部分与来自n末端的不超过3个氨基酸连接。在一个具体实施方式中,所述供体部分与分离部分z连接。
[0027]
在另一个实施方式中,所述可检测部分是连接到所述底物肽切割区一侧的化学发光信号部分,受体部分连接到所述底物肽切割区的另一侧。所述化学发光信号部分的非限制性示例是1,2-二氧杂环丁烷化合物。
[0028]
在另一个实施方式中,所述可检测部分是酶原,其在底物肽切割时被活化并通过
检测其催化活性来检测。所述酶原非限制性示例是凝血酶原(因子ii)或该级联(cascade)中的其它酶。
[0029]
在一些实施方式中,所述底物肽y包含8至12个氨基酸的序列。在一个具体的实施方式中,该序列是氨基酸序列,所述氨基酸序列选自由seq id no:13-23组成的组,特别是选自seq id no:13,更特别地是选自由seq id no:24-33和seq id no:1-10组成的组。
[0030]
在某个实施方式中,在本发明的方法中测试的样本是唾液样本,并且所述组合物还包含蛋白酶抑制剂,所述蛋白酶抑制剂选自由以下部分组成的组:抗痛素、ac-devd-cho、抑肽酶、eglin c、gw、pmsf和2,6pda。所述样本可以是颊样本(buccal sample),所述组合物包含蛋白酶抑制剂,所述蛋白酶抑制剂选自由以下部分组成的组:pmsf、gw、抑肽酶、eglinc和胃蛋白酶抑制剂(pepstatin)。
[0031]
在另一个实施方式中,本发明的方法还包括使所述样本与不是所述sars-cov-2的病毒的病毒蛋白酶的至少一种底物接触,其中所述至少一种底物不被切割指示所述样本中不存在所述病毒。
[0032]
在另一个实施方式中,适于在本发明的方法中读取信号的设备是光学或光谱设备。所述光学或光谱设备是模块化的。在又一个实施方式中,所述光学或光谱设备被配置成作为便携式和高灵敏度的荧光分光光度计(荧光计)、光度计、荧光显微镜或其组合来操作,用于测量荧光、发光或磷光。这些光学或光谱设备方便地放置在公共场所,例如剧院、餐馆和工作场所的入口处。他们可以是小型化的,并用于公共场所、工作场所和家中的快速现场及时诊断(rapid point-of-care diagnostics)。
[0033]
在另一个实施方式中,所述测定可适于全自动机器人系统。所述光学或光谱设备包括荧光读取模块、样本处理机构和分配器/移液管模块。将样本装载到样本处理机构上,在那里对其进行处理,并通过分配器/移液管模块添加所有试剂。然后通过荧光读数监测样本,并用指定的软件分析。该实施方式旨在用于多个患者的快速实验室,高通量诊断。
[0034]
在另一个实施方式中,所述光学或光谱设备包括激发模块、样本室和采集和/或检测器模块。所述样本室可以是荧光多板读数器,用于对多个样本进行实验室高通量和快速的多路分析,用于现场及时诊断(point-of-care diagnostics)。
[0035]
在一个具体实施方式中,所述光学或光谱设备还包括计算单元。在另一个具体实施方式中,所述采集和/或检测器模块以及所述计算单元被组合在单个单元中,所述单个单元被设计成执行荧光发射的采集、测量其强度、处理荧光发射数据,并且可选地以可读格式显示所述数据和/或将其输出到外部存储器或用户界面。
[0036]
在又一个具体实施方式中,所述采集模块是智能手机或适于执行期望测量的任何其它移动设备或小配件的一部分。
[0037]
在一些实施方式中,所述检测器是电子倍增电荷耦合设备(electron-multiplying charge-coupled device,emccd)成像器、电荷耦合设备(charge-coupled device,ccd)成像器、雪崩光电二极管(avalanche photodiode,apd)、光电倍增管(photomultiplier tube,pmt)、科学互补金属氧化物半导体(scientific complementary metal-oxide-semiconductor,scmos)成像器或智能手机摄像头的cmos成像器、独立照相机,或任何移动设备或配件的照相机,所述检测器可选地具有聚焦装置和计算机链接。
[0038]
在一个具体实施方式中,所述检测器是智能手机的cmos成像器。
[0039]
在一些实施方式中,所述适用于读取信号的设备是横向流设备,其可以是棒或堆的形式。在一个具体实施方式中,所述横向流设备基于常规硝化纤维素膜或纤维素(纸)膜。所述横向流设备适用于所述病毒的家庭或现场检测。
[0040]
本发明还提供了一种微流体芯片或实验室-芯片(lab-on-a-chip),适于执行本发明的任何实施方式的方法。
[0041]
本发明的另一方面是一种分离的肽,包含seqid nos:25-33所列的氨基酸序列,所述肽长不超过14个氨基酸。所述分离的肽还包含可检测部分。在一个具体实施方式中,所述分离的肽,由seq id no:2-10中任一个所列的氨基酸序列组成。
[0042]
本发明的另一方面是一种制品,包含与固体载体(solid support)连接的本发明的所述的分离的肽。所述固体载体是试管、微量滴定板、微量滴定孔、珠粒、试纸(dipstick)、聚合物微粒、磁性微粒、硝化纤维、纤维素或芯片阵列。
[0043]
本发明的另一方面是一种用于检测样本中sars-cov-2的诊断试剂盒,所述试剂盒包含本发明的分离的肽或本发明的制品和用于检测所述肽切割的试剂。所述试剂盒还包含至少一种试剂,其特异性检测所述sars-cov-2以外的病毒的存在。
[0044]
根据本发明的另一方面,提供了一种在主体中诊断严重急性呼吸综合征冠状病毒2(sars-cov-2)感染的方法,包括使所述主体的样本与包含检测所述sars-co-v2病毒的3cl-蛋白酶的试剂的组合物接触,其中所述样本中所述3cl-蛋白酶的存在指示sars-co-v2感染。
[0045]
根据本发明的另一方面,提供了一种在疑似患有covid的主体的样本中检测sars-cov-2病毒的方法,所述方法包括使所述样本与包含监测所述sars-cov-2病毒的3cl蛋白酶的活性的试剂的组合物接触,其中所述样本中所述3cl蛋白酶的活性水平指示所述样本中sars-cov-2的存在。
[0046]
根据本发明的实施方式,所述样本选自由以下部分组成的组:粘液、唾液、咽喉洗液、鼻洗液、脊髓液、痰液、尿液、精液、汗液、粪便、血浆、血液、支气管肺泡液、阴道液、泪液和组织活检。
[0047]
根据本发明的实施方式,所述样本是唾液或颊样本。
[0048]
根据本发明的实施方式,所述试剂监测所述3cl蛋白酶的活性。
[0049]
根据本发明的实施方式,所述试剂是所述3cl蛋白酶的底物肽,所述肽连接到至少一个部分,所述至少一个部分在所述sars-cov-2的所述3cl蛋白酶切割所述肽时产生可检测的信号。
[0050]
根据本发明的实施方式,所述肽介于10至12个氨基酸之间。
[0051]
根据本发明的实施方式,所述至少一个部分是fret对,并且其中所述肽的切割产生来自所述fret对的信号。
[0052]
根据本发明的实施方式,所述fret对是af488和bhq1。
[0053]
根据本发明的实施方式,所述fret对是edans和dabcyl。
[0054]
根据本发明的实施方式,所述底物肽还包含分离部分。
[0055]
根据本发明的实施方式,所述试剂由以下通式表示:
[0056]
x-y-z,
[0057]
其中:
[0058]
y包含sars-cov-2的3cl蛋白酶的底物肽,所述3cl蛋白酶对x-y-z的切割形成切割产物x-y'和y"-z,其中y'是y的第一切割产物,y"是y的第二切割产物;
[0059]
x包含可检测部分;以及
[0060]
z包含能够结合至两相分离系统的分离相的分离部分;
[0061]
其中所述x-y-z不形成所述3cl蛋白酶的天然底物的邻接部分。
[0062]
根据本发明的实施方式,可检测部分x包含标记试剂,所述标记试剂选自由以下部分组成的组:酶、荧光团、发色团、蛋白质、酶原、化学发光物质和放射性同位素。
[0063]
根据本发明的实施方式,分离部分z选自由以下部分组成的组:免疫结合试剂、磁性结合部分、肽结合部分、亲和结合部分和核酸部分。
[0064]
根据本发明的实施方式,所述底物肽包含氨基酸序列,所述氨基酸序列选自由seq id no:13-23组成的组。
[0065]
根据本发明的实施方式,所述底物肽包含选自seq id no:13中列出的氨基酸序列。
[0066]
根据本发明的实施方式,所述底物肽的所述氨基酸序列由选自由seq id no:24-33组成的组的序列组成。
[0067]
根据本发明的实施方式,所述底物肽是选自由seq id no:1-10组成的组中列出的序列。
[0068]
根据本发明的实施方式,所述底物肽如seq id no:8所示。
[0069]
根据本发明的实施方式,所述底物肽与荧光部分连接。
[0070]
根据本发明的实施方式,当所述样本是唾液样本时,所述组合物包含蛋白酶抑制剂,所述蛋白酶抑制剂选自由以下部分组成的组:抗痛素、ac-devd-cho、抑肽酶、eglin c、gw、pmsf和2,6pda。
[0071]
根据本发明的实施方式,所述蛋白酶抑制剂包括pmsf和gw。
[0072]
根据本发明的实施方式,当所述样本是颊样本时,所述组合物包含蛋白酶抑制剂,所述蛋白酶抑制剂选自由以下部分组成的组:pmsf、gw、抑肽酶、eglinc和胃蛋白酶抑制剂。
[0073]
根据本发明的实施方式,所述蛋白酶抑制剂包括pmsf、gw、抑肽酶(aprotinin)和eglinc。
[0074]
根据本发明的实施方式,所述方法还包括使所述样本与不是所述sars-cov-2的病毒的病毒蛋白酶的至少一种底物接触,其中所述至少一种底物不被切割指示所述样本中不存在所述病毒。
[0075]
根据本发明的另一个方面,提供了一种分离的肽,包含seq id nos:25-34所列的氨基酸序列,所述肽长不超过14个氨基酸。
[0076]
根据本发明的实施方式,所述分离的肽还包含可检测部分。
[0077]
根据本发明的实施方式,所述分离的肽由seq id no:2-10中任一个所列的氨基酸序列组成。
[0078]
根据本发明的另一个方面,提供了一种制品,包含与固体载体连接的本文公开的所述的分离的肽。
[0079]
根据本发明的实施方式,所述固体载体是珠粒。
[0080]
根据本发明的另一个方面,提供了一种用于检测样本中sars-cov-2的诊断试剂
盒,所述试剂盒包含本文所述的肽或本文所述的制品和用于检测所述肽切割的试剂。
[0081]
根据本发明的实施方式,所述诊断试剂盒还包含至少一种试剂,其特异性检测所述sars-cov-2以外的病毒的存在。
[0082]
根据本发明的另一个方面,提供了一种治疗有需要的主体的sars-cov-2感染的方法,所述方法包括:
[0083]
(a)根据权利要求2所述的方法诊断所述主体中的sars-cov-2感染;以及
[0084]
(b)治疗所述主体。
[0085]
不同实施方式会具有不同的益处,并且可与各种应用结合使用。在附图和下面的描述中阐述了一个或多个实施方式的细节。根据说明书和附图以及权利要求书,所描述的技术的其它特征、目的和优点将变得显而易见。
附图说明
[0086]
从以下结合附图的详细描述中,将更全面地理解和领会所公开的实施方式。本文所包括和描述的附图是示意性的,并不限制本发明的范围。还要注意的是,在附图中,一些元件的尺寸可能被放大,因此,出于说明的目的,没有按比例绘制。尺寸和相对尺寸不一定对应于本发明实践的实际缩减。
[0087]
图1显示了具有从histrap柱洗脱的不同级分的sds page凝胶。洗脱以线性梯度进行,以20mm开始,以250mm咪唑结束,分19步进行。使用500mm咪唑进行最终洗脱,以确保洗脱所有蛋白质。(1 2)分别来自在18℃和30℃下诱导的细菌培养物的总细胞裂解物(total cell lysate)。3clpro明显存在于裂解物中,并且18℃诱导显示3clpro丰度更高。(3)结合到histrap柱后,18℃诱导的裂解物的流动。
[0088]
图2显示了评估229e-3clpro纯度和sars-cov-2 3clpro的tev-切割的sds-page凝胶。
[0089]
(1)blueye预染蛋白梯(protein ladder)。
[0090]
(2)储存缓冲液2中的纯化229e-3clpro。
[0091]
(3)未切割(uncleaved)的sars-cov-2 3clpro。
[0092]
(4 5)tev-切割的sars-cov-2 3clpro分别在30℃下1小时和4℃下过夜。将样本装载到histrap柱上,并收集非结合流过的样本。切割版的重量减少约1.7kda。
[0093]
(6)空白道(blank lane)。
[0094]
(7 8)分别在4℃和30℃下未纯化的tev切割的sars-cov-2 3clpro。tev蛋白酶(28kda)是可见的。
[0095]
(9 10)分别在4℃和30℃下tev切割后结合到histrap柱的蛋白质的洗脱。tev-蛋白酶是可见的,少量可能是未切割的sars-cov-2-3clpro。
[0096]
图3a-3c显示了唾液样本y中的尖峰效应(spike effect):
[0097]
图3a-市售缓冲液(commercial buffer)。
[0098]
图3b-启始缓冲液(starting buffer)。
[0099]
图3c-最终缓冲液(final buffer)。
[0100]
图4显示了比较五种不同底物(序列号(seqidno):2-6)和市售底物(seqidno:1)的3clpro活性的图。
[0101]
图5a-5f显示了说明使用五种不同测试底物(seq id no:2-6)和市售底物(seqidno:1)的3clpro和唾液活性的图。
[0102]
图6显示了比较四种不同底物(seq id no:7-10)的3clpro活性的图。
[0103]
图7a-7d显示了说明使用四种不同底物(seq id no:7-10)的3clpro和唾液活性的图。
[0104]
图8示意性地示出了本发明方法背后的检测机制。
[0105]
图9显示了使用本发明方法的进行sars-cov-2检测的酶活性测试。
[0106]
图10显示了颊与鼻咽(np)样本的测试结果。条形代表5个健康对照(hc)样本与6个患者样本的平均斜率值(mean slope values),比较来自每个主体的匹配的鼻咽和颊样本。
[0107]
图11显示了颊与鼻咽(np)样本的测试结果。
[0108]
图12显示了患者出院时的叠加结果。框(p12-p16、p18、p21和p24)指示在蛋白酶测定结果的48h内出院的患者。至少三个患者样本仍显示出明显高于对照组的蛋白酶活性。这些结果清楚地表明,应重新考虑基于pcr值或临床症状消退的患者出院。
[0109]
图13示出了与pcr ct(循环阈值)值的相关结果。条形代表7个患者样本的平均斜率比,在3cl蛋白酶测定的样本收集的48小时内测定了这些患者样本的匹配pcr ct值。3cl蛋白酶结果与ct值一致,ct值可充当病毒载量的替代量度。
[0110]
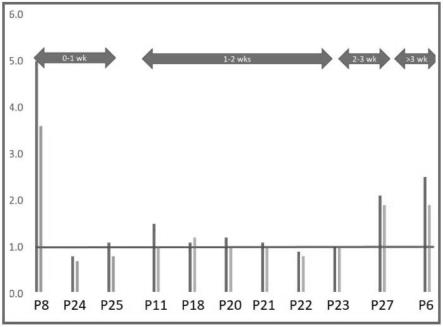
图14显示了测定结果与症状发作后天数的叠加图。在来自测试前症状首先出现超过3周的个体的样本中,仍然可以看到活性3cl蛋白酶的证据。
[0111]
图15显示了样本稳定性曲线。保持在4℃的样本在24小时内保留了高于背景约40-50%的酶活性。最显著的减少发生在0-2小时之间。从时间0起保持在-20℃的样本甚至在48小时后仍保持活性。颊和鼻(中鼻甲)底物产生了类似的结果。
[0112]
图16是显示了25名阳性covid-19患者的实验组内,患者样本斜率与平均对照蛋白酶斜率之比的图。
[0113]
图17a-c是说明与各种基因的pcr测定的灵敏度相比较,该测定的灵敏度的图。
具体实施方式
[0114]
在下面的描述中,将描述本发明的各个方面。出于解释的目的,阐述了具体的配置和细节,以便提供对本发明的透彻理解。然而,对于本领域技术人员来说,显然可以在没有本文给出的具体细节的情况下实施本发明。此外,为了不混淆本发明,可以省略或简化公知的特征。
[0115]
权利要求中使用的术语“包括(comprising)”是“开放式的(open ended)”,表示所列举的元件,或其在结构或功能上的等同物,加上未列举的任何其它元件。不应将其解释为限于其后列出的元件;它不排除其它元件或步骤。它需要被解释为指定所提及的所述特征、整数、步骤或组件的存在,但不排除一个或多个其它特征、整数、步骤或组件或其组合的存在或添加。因此,表述“包含x和z的组合物(a composition comprising x and z)”的范围不应限于仅由组分x和z组成的组合物。同样,表述“包括步骤x和z的方法(a method comprising the steps x and z)”的范围不应限于仅由这些步骤组成的方法。术语“由
……
组成(consisting of)”表示“包括并限于(including and limited to)”。术语“基本上由
……
组成(consisting essentially of)”表示组合物、方法或结构可以包括另外的
成分、步骤和/或部分,但前提是另外的成分、步骤和/或部分不会实质上改变所要求保护的组合物、方法或结构的基本和新颖特征。除非特别指出,否则如本文所用,术语“约(about)”应理解为在本领域中的正常公差范围内,例如在平均值的两个标准偏差内。在一个实施方式中,术语“约(about)”表示在所使用的数值的报告数值的10%以内,优选在所报告数值的5%以内。例如,术语“约(about)”可立即理解为在规定值(stated value)的10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或0.01%之内。在其它实施方式中,术语“约(about)”可以表示更高的变化容限,这取决于例如所使用的实验技术。特定值的所述变化是本领域技术人员理解的,并且在本发明的范围内。作为说明,“约1至约5(about 1to about 5)”的数值范围应被解释为不仅包括明确列举的约1至约5的值,还包括所示范围内的单个值和子范围。因此,包括在该数值范围内的是单个值,例如2、3和4,以及子范围,例如1-3、2-4和3-5,以及1、2、3、4、5或6。这一原理同样适用于仅列举一个数值作为最小值或最大值的范围。除非从上下文另有说明,否则本文提供的所有数值均由术语“约(about)”修饰。其它类似的术语,例如“基本上(substantially)”、“一般(generally)”、“至多(up to)”等应被解释为修饰术语或值,以使其不是绝对的。这些术语将由环境和它们所修饰的术语来定义,因为这些术语是本领域技术人员所理解的。这至少包括用于测量值的给定实验、技术或仪器的预期实验误差、技术误差和仪器误差的程度。每当本文指出数值范围时,其意味着包括在所指出的范围内的任何引用的数字(分数或整数)。短语“第一指示数字和第二指示数字之间的范围(ranging/ranges between a first indicate number and a second indicate number)”和“从第一指示数字到第二指示数字的范围(ranging/ranges from a first indicate number to a second indicate number)”在本文中可互换使用,并且意味着包括第一和第二指示数字以及它们之间的所有分数和整数。
[0116]
如本文所用,术语“方法(method)”是指用于完成给定任务的方式、手段、技术和程序,包括但不限于化学、药理学、生物学、生物化学和医学领域的从业者已知的或容易从已知的方式、手段、技术和程序开发的那些方式、手段、技术和程序。如本文所用,术语“治疗(treating)”包括消除、基本上抑制、减缓或逆转病症的发展,基本上改善病症的临床或美学症状,或基本上预防病症的临床或美学症状的出现。如本文所用,术语“诊断(diagnosing)”是指确定主体体内病毒的存在或不存在、对感染进行分类、确定感染的严重程度、监测病毒进展、预测病理学结果和/或恢复前景和/或对主体进行病毒筛查。
[0117]
如本文所用,术语“和/或(and/or)”包括一个或多个相关列出项目的任何和所有组合。除非另有定义,本文使用的所有术语(包括技术和科学术语)具有与本发明所属领域的普通技术人员通常理解的相同的含义。还应当理解,术语,例如在常用词典中定义的那些术语,应当被解释为具有与它们在说明书和相关领域的上下文中的含义一致的含义,并且不应该以理想化的或过于正式的含义来解释,除非在本文中明确如此定义。为了简洁和/或清楚起见,可能不详细描述公知的功能或构造。如本文所用,单数形式“一(a、an)”和“所述(the)”包括复数,除非上下文另有明确指示。例如,术语“化合物(a compound)”或“至少一种化合物(at least one compound)”可包括多种化合物,包括其混合物。
[0118]
应当理解,当一个元件被称为“在
……
上面(on)”、“附着到(attached to)”、“连接到(connected to)”、“耦合到(coupled with)”、“接触(contacting)”等另一个元件时,它可以直接在另一个元件上、附着到另一个元件、连接到另一个元件、耦合到或接触另一个元
件,或者也可以存在中间元件。相反,当一个元件被称为例如“直接在
……
上(directly on)”、“直接附着到(directly attached to)”、“直接连接到(connected to)”、“直接耦合到(coupled with)”或“直接接触(contacting)”另一个元件时,不存在中间元件。本领域技术人员还将理解,当提到与另一个特征“相邻”设置的结构或特征时,该结构或特征可以具有与相邻特征重叠或位于相邻特征之下的部分。
[0119]
本发明提供了检测测试样本中sars-cov-2的方法、试剂和试剂盒,并涉及检测3c-l蛋白酶。本发明涉及使用3c-l蛋白酶测定法诊断covid-19,所述3c-l蛋白酶测定法选择性地检测病毒复制和传播所需的sars-cov-2编码酶的活性形式,该酶也可能在细胞凋亡中起作用。活病毒(与病毒片段相反)的检测进一步允许诊断感染性状态的能力。
[0120]
在将本发明付诸实践的同时,本发明人已经表明,可以在来自无症状和有症状患者的上呼吸道和口腔样本中鉴定出sars-cov-2病毒。活性测定在≤15分钟内提供结果(参见图3a-c、4、5a-f、6和7a-d)。此外,本发明人能够在恢复的个体,包括早期症状和无症状的个体中检测持续的、活性的病毒贮源(active viral reservoirs)。
[0121]
在进一步将本发明付诸实践的同时,本发明人证明了他们可以检测来自另外的冠状病毒的3cl蛋白酶活性(表4-6)。部署可检测不同冠状病毒的基于机制的测定的能力确保即使出现新的突变时,测定性能也不会下降。该测定显示出特异性识别冠状病毒而非微小核糖核酸病毒(参见表4-6)。
[0122]
该测试的执行速度及其高准确度使得该测试特别适合于在人口密集的场所(例如,疗养院和学校)进行现场即时(point-of-care,poc)快速诊断。由于该测试可靠地识别无症状的个体,因此该测试还适用于旅游业和卫生保健工作者。还可以使用所提出的诊断测试进行通过测试废水/池合样本的群体监测。测定形式可容易地适于家庭测试。
[0123]
因此,根据本发明的第一方面,提供了一种诊断主体样本中严重急性呼吸综合征冠状病毒2(sars-cov-2)感染的方法,所述方法包括使样本与包含检测sars-cov-2病毒的3cl-蛋白酶的试剂的组合物接触,其中样本中所述3cl-蛋白酶的存在指示sars-co-v2感染。
[0124]
在另一个实施方式中,检测疑似患有covid-19的主体的样本中sars-cov-2病毒的方法包括,使样本与包含监测(monitors)sars-cov-2病毒的3cl-蛋白酶的活性的试剂的组合物接触,其中样本中3cl-蛋白酶的活性水平指示样本中sars-cov-2的存在。活性水平也可以对样本中的sars-cov-2病毒进行定量。
[0125]
在一些实施方式中,可检测部分是荧光部分。在一个具体的实施方式中,可检测部分是供体和受体部分的福斯特共振能量转移(resonance energy transfer,fret)对,底物肽的切割产生或调节来自所述fret对的信号。特定的供体部分是量子点。
[0126]
另一个方面,本发明提供了一种非均相测定(heterogeneous assay)的方法,其中在测定过程中将固相与另一种测定组分分离,用于对疑似患有covid-19的主体样本中的sars-cov-2病毒进行生物分子诊断,该方法包括:
[0127]
(a)使所述样本与包含由以下通式表示的切割试剂的组合物接触:
[0128]
x-y-z,
[0129]
其中:
[0130]
i)y是能够被sars-cov-2 3cl蛋白酶切割的底物肽;
[0131]
ii)所述3cl蛋白酶对x-y-z的切割形成切割产物x-y'和y"-z,其中y'和y"是所述底物肽y的两个切割片段;
[0132]
iii)z是能够结合至两相分离系统的分离相的可选的分离部分;
[0133]
iv)所述切割试剂x-y-z不形成所述3cl蛋白酶的天然底物的邻接部分;以及
[0134]
v)x是能够在所述3cl蛋白酶切割底物肽时产生可检测信号的可检测部分,从而监测样本中3cl蛋白酶的活性,
[0135]
其中与所述可检测信号相关的3cl蛋白酶的活性水平是i)指示样本中sars-cov-2病毒的存在;以及ii)允许对样本中的sars-cov-2病毒进行定量。
[0136]
(b)用适用于读取所述信号的设备记录或读取所述信号。
[0137]
在一些实施方式中,可检测部分x包括选自酶、荧光团、发色团、蛋白质、酶原(pre-enzyme)、化学发光物质和放射性同位素的标记试剂。分离部分z选自由以下部分组成的组:免疫结合试剂、磁性结合部分、肽结合部分、亲和结合部分、核酸部分、生物素/链霉亲和素部分、量子点、超材料、导电聚合物部分、树枝状聚合物部分(dendrimer moiety)、冠醚或印迹聚合物部分、适体部分、电化学结合部分和金属纳米颗粒部分。
[0138]
在具体实施方式中,样本选自选自由以下部分组成的组:粘液、唾液、咽喉洗液、鼻洗液、脊髓液、痰液、尿液、精液、汗液、粪便、血浆、血液、支气管肺泡液、阴道液、泪液、组织活检以及鼻咽、口咽、鼻中鼻甲、前鼻(anterior nasal)和颊拭子。
[0139]
在其它实施方式中,可检测部分x是荧光部分。在一个具体实施方式中,可检测部分x是供体和受体部分的福斯特共振能量转移(resonance energy transfer,fret)对,底物肽的切割产生或调节来自所述fret对的信号。特定的供体部分是量子点。图8示意性地示出了本发明的该方法背后的检测机制。图9显示了使用本发明的方法进行sars-cov-2检测的酶活性测试。
[0140]
在某些实施方式中,供体和受体部分以允许能量从供体转移到受体的构型附着到肽上,从而通过fret过程淬灭荧光。在一些其它实施方式中,供体和受体部分间隔不超过3、5、10、15或20个氨基酸残基。
[0141]
可根据本发明的该方面进行测试的主体可以是有症状的或无症状的感染。它们可能会随着感染而传染或不传染。应当理解,该测定的非常高的准确度和灵敏度允许检测非常低水平的sars-cov-2病毒。因此,该方法可用于在最初感染后很快检测主体样本中的病毒,或者甚至检测通过其它方法(临床评估,基于分子、抗原、抗体的测试)检测为阴性但仍含有低水平的活性病毒的样本中的病毒。此外,该方法可用于检测无症状主体样本中的病毒。
[0142]
在一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过1天。
[0143]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过2天。
[0144]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过3天。
[0145]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过4天。
[0146]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过5天。
[0147]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过6天。
[0148]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后不超过7天。
[0149]
在另一个具体的实施方式中,对取自未显示covid-19症状的主体的样本实施本发明的方法,该样本在暴露于已知患有covid-19的主体后7天以上。
[0150]
在另一个具体的实施方式中,对取自具有循环阈值ct40或更小值的阴性pcr测试或阳性pcr测试的主体的样本实施本发明的方法。
[0151]
sars-cov-2病毒的3cl蛋白酶是一种34kd胰蛋白酶样半胱氨酸蛋白酶。根据一个具体的实施方式,3cl蛋白酶包含seq id no:34所列出的氨基酸序列。
[0152]
可检测到sars-cov-2的示例性样本包括但不限于唾液、粘液、咽喉洗液、鼻洗液、脊髓液、痰液、尿液、精液、汗液、粪便、血浆、血液、支气管肺泡液、阴道液、泪液和组织活检。
[0153]
在一些实施方式中,样本是污水样本。
[0154]
在其它实施方式中,样本包含唾液。
[0155]
样本可取自口腔、咽喉后部或面颊内部(例如,使用颊拭子)。
[0156]
可用于获取样本的拭子的示例包括脸颊拭子(cheek swabs)、口咽拭子和鼻咽拭子。
[0157]
为了测定sars-cov-2病毒的3cl的活性,可以使用作为酶底物的肽。该肽连接到至少一个部分,该部分在被3cl蛋白酶切割时产生可检测的信号。
[0158]
该肽的长度通常为8至30个氨基酸,更优选10至20个氨基酸,甚至更优选10至15个氨基酸。根据一个具体的实施方式,肽的长度不超过14个氨基酸。根据一个具体的实施方式,肽的长度介于8至12个氨基酸之间。
[0159]
本文所述的肽可包括天然或非天然存在的氨基酸。
[0160]
术语“氨基酸(amino acid或amino acids)”应理解为包括20种天然存在的氨基酸;这些氨基酸通常在体内翻译后被修饰,包括例如羟脯氨酸、磷酸丝氨酸和磷酸苏氨酸;以及其它不常见的氨基酸,包括但不限于2-氨基己二酸、羟基赖氨酸、异锁链赖氨素(isodesmosine)、正缬氨酸(nor-valine)、正亮氨酸(nor-leucine)和鸟氨酸。此外,术语“氨基酸(amino acid)”包括d-和l-氨基酸。
[0161]
下表a和b列出了天然存在的氨基酸(表a)和非常规(non-conventional)或修饰的氨基酸(例如,合成的,表b),其可用于本发明的一些实施方式。应当理解,可以使用非常规氨基酸以降低测定中的背景噪声。
[0162]
表a
[0163][0164][0165]
表b
[0166]
[0167]
[0168]
[0169][0170]
选择肽的氨基酸序列,使其可被sars-cov-2的3cl切割。优选地,在相同的测定条件下,所述肽不作为人类鼻病毒(human rhinovirus,hrv)的3c的底物。在另一个实施方式中,选择肽使得其可以在相同的测定条件下区分人类样本中的sars-cov-2和冠状病毒科(coronavirus family)中的其它人类病原体(例如cov-229e)的3cl活性。
[0171]
根据一个具体的实施方式,所述肽包含seqid nos:13-23中列出的氨基酸序列中的至少一种。
[0172]
在另一个实施方式中,所述肽包含与seq id no:13-23中列出的序列至少90%相同的氨基。
[0173]
根据一个具体的实施方式,所述肽包含seq id no:13中列出的氨基酸序列。
[0174]
包含seq id no:13中列出的氨基酸序列的示例性肽序列在seq id no:24-33中列出,这些肽序列已被证明是sars-cov-2的有效底物。
[0175]
在一个具体的实施方式中,测定中使用的肽具有与seq id no:24-33所列的序列至少90%相同的氨基酸序列。
[0176]
在另一个实施方式中,测定中使用的肽具有与seq id no:1-12所列的序列至少
90%相同的氨基酸序列。
[0177]
本发明肽的氨基酸可以被保守地或非保守地取代。
[0178]
根据一个具体的实施方式,肽的氨基酸被保守地取代。
[0179]
本文所用的术语“保守取代(conservative substitution)”是指用天然或非天然存在的氨基或具有相似空间性质(steric properties)的肽模拟物替换肽中天然序列中存在的氨基酸。在待替换的天然氨基酸的侧链是极性或疏水性的情况下,保守取代应该是用天然存在的氨基酸、非天然存在的氨基酸或用也是极性或疏水性的肽模拟部分(除了与被替换的氨基酸的侧链具有相同的空间性质之外)进行。
[0180]
由于天然存在的氨基酸通常根据它们的性质分组,因此可以容易地确定天然存在的氨基酸的保守取代,记住这样的事实,即根据本发明,用空间相似的非带电氨基酸替换带电氨基酸被认为是保守取代。
[0181]
为了通过非天然存在的氨基酸产生保守取代,还可以使用本领域熟知的氨基酸类似物(合成氨基酸)。天然存在的氨基酸的肽模拟物在本领域技术人员已知的文献中有详细的记载。
[0182]
当影响保守取代时,取代氨基酸应当在侧链中具有与原始氨基酸相同或相似的官能团。
[0183]
本文所用的短语“非保守取代”是指存在于亲本序列中的氨基酸被替换为另一种具有不同电化学和/或立体性质的天然或非天然存在的氨基酸。因此,取代氨基酸的侧链可以明显大于(或小于)被取代的天然氨基酸的侧链,和/或可以具有与被取代的氨基酸具有明显不同的电子性质的官能团。这种类型的非保守性取代的示例包括用苯丙氨酸或环己基甲基甘氨酸取代丙氨酸,用异亮氨酸取代甘氨酸,或用
‑‑
nh
‑‑
ch[(
‑‑
ch2)5‑‑
cooh]
‑‑
co
‑‑
取代天冬氨酸。
[0184]
根据一个具体的实施方式,底物肽的氨基酸序列选自由seq id nos:25-33组成的组。
[0185]
根据一个具体的实施方式,底物具有seq id no:31所列的氨基酸序列,其中x是半胱氨酸、天冬氨酸、谷氨酸、精氨酸或赖氨酸。根据一个具体的实施方式,x是半胱氨酸。
[0186]
根据一个具体的实施方式,底物具有seq id no:30所列的氨基酸序列,其中x是半胱氨酸、天冬氨酸、谷氨酸、精氨酸或赖氨酸。根据一个具体的实施方式,x是半胱氨酸。
[0187]
因此,本发明人考虑的示例性序列是seq id no:38或39中列出的序列。
[0188]
本发明的肽可以通过肽合成领域技术人员已知的任何技术合成。对于固相肽合成,许多技术的总结可以在以下文献中找到:stewart j.m.和young j.d.(1963),(固相肽合成(solid phase peptide synthesis)),w.h.freeman公司(旧金山);和meienhofer j(1973),“激素蛋白和肽(hormonal proteins and peptides)”,第2卷,第46页,学术出版社(academic press)(纽约)。关于经典溶液合成的综述,请参见schroder g.和lupke k.(1965),肽(the peptides),第1卷,学术出版社(academic press)(纽约)。
[0189]
通常,肽合成方法包括将一个或多个氨基酸或适当保护的氨基酸顺序添加到生长的肽链中,第一个氨基酸的氨基或羧基被适当的保护基团保护。然后,在适于形成酰胺键的条件下,被保护或修饰的氨基酸可以附着到惰性固体载体上,或者通过添加序列中具有适当保护的互补(氨基或羧基)基团的下一个氨基酸而在溶液中使用。然后从该新添加的氨基
酸残基中除去保护基团,然后添加下一个氨基酸(适当保护的),依此类推;传统上,该过程也伴随有洗涤步骤。在所有期望的氨基酸以适当的序列连接后,依次或同时除去任何剩余的保护基团(和任何固体载体),得到最终的肽化合物。通过对该通用过程的简单修饰,有可能在生长链上一次添加一个以上的氨基酸,例如,通过将受保护的三肽与适当保护的二肽偶联(在不外消旋手性中心的条件下),在去保护后形成五肽等。
[0190]
肽合成的进一步描述公开于美国专利us 6,472,505中。制备本发明肽化合物的优选方法包括利用固体载体的固相肽合成。andersson生物聚合物(biopolymers)2000,55(3),227-50描述了大规模肽合成。
[0191]
如上所述,本发明该方面的肽与至少一个部分连接,该部分在肽被sars-cov-2的3cl蛋白酶切割时产生可检测的信号。
[0192]
在一些实施方式中,可检测部分可以使用本领域技术人员已知的任何键合方法(conjugation method)与本发明的肽化学键合(偶联)。例如,使用3-(2-吡啶基二硫代)丙酸n-羟基琥珀酰亚胺酯(3-(2-pyridyldithio)propionic acid n-hydroxysuccinimide ester)(也称为n-琥珀酰亚胺基3-(2-吡啶基二硫代)丙酸酯(n-succinimidyl 3-(2-pyridyldithio)propionate))(“sdpd”)(sigma公司,目录号:p-3415;参见例如cumber等人,1985年,酶学方法(methods of enzymology)112:207-224),戊二醛键合过程(conjugation procedure)(参见例如g.t.hermanson,1996,“生物结合技术中的抗体修饰和结合(antibody modification and conjugation,in bioconjugate techniques)”,学术出版社(academic press)(纽约))或碳二亚胺键合过程(例如参见j.march,高级有机化学:反应、机理和结构(advanced organic chemistry:reaction's,mechanism,and structure),第349-350页和第372-374页(第3版),1985;b.neises等人,1978,德国应用化学国际版(angew chem.,int.ed.engl.)17:522;a.hassner等人,1978,四面体通讯(tetrahedron lett.)4475;e.p.boden等人,1986,有机化学期刊(j.org.chem.)50:2394,以及l.j.mathias,1979,合成(synthesis)561),可以将可检测部分键合至本文公开的底物肽。
[0193]
可选地或可替代地,通过翻译融合编码本发明肽的多核苷酸与编码可检测部分的核酸序列,可检测部分与肽键合。
[0194]
可检测信号可以是可直接检测的,例如荧光信号、磷光信号、放射性信号或颜色信号(例如由发色团发射的)。可替代地,可检测信号可以是间接可检测的,例如前酶,如下文进一步描述。可检测部分的其它示例详细描述于申请号为20050048473的美国专利申请中,其通过引用完全并入本文。
[0195]
根据本发明的这一方面,可以使用本领域已知的用于监测蛋白水解底物切割的任何测定法。
[0196]
在一个实施方式中,测定是均相测定。如本文所用,短语“均相测定(homogeneous assay)”是指不需要将信号部分与其它测定组分分离的测定。
[0197]
使该组合物与测试sars-cov-2病毒存在的样本接触。如果病毒存在于样本中,病毒3cl蛋白酶也存在于样本中。该蛋白酶切割底物,并且可以观察到来自信号部分的信号变化。此类均相荧光和比色测定是本领域技术人员已知的。参见,例如:生物化学(biochemistry),allinger,wang q.m.等人,“以肽硝基酰苯胺为底物的鼻病毒-14 3c蛋白
酶的连续量热测定”,分析化学(anal.biochem.),第252卷,第238-245页(1997),和basak s.等人,“使用分子内淬灭的荧光肽在体外阐明前蛋白转化酶4的底物特异性和生物测定(in vitro elucidation of substrate specificity and bioassay of proprotein convertase 4using intramolecularly quenched fluorogenic peptides)”,生物化学期刊(biochem.j.),第380卷,第505-514页(2004)。
[0198]
在一个实施方式中,底物肽在被所述3cl蛋白酶切割时产生可检测信号的部分是福斯特共振能量转移(resonance energy transfer,fret)对,由此底物肽的切割产生来自所述fret对的信号。fret对包含如下文进一步描述的供体部分和受体部分。
[0199]
检测分子相互作用的传统方法,例如在生化系统中,是拉下一个分子,并在显微镜中观察。这是对分子相互作用的直接测量,通过空间上的重合推断相互作用。普通宽场显微镜(wide-field microscope)的问题在于衍射极限是可观察的元素。因此,可以用宽场显微镜分辨的典型体积元件的数量级为10-15
米,相当于大约一微米立方(a micron cubed)。然而,需要被检测的相互作用的生物分子实体具有10-22
米数量级的小得多的体积。这比传统的宽场显微镜所提供的要小几个数量级。尽管在这种情况下可以使用共定位以推断相互作用,但是在共定位的情况下观察到分子相互作用的概率非常低。fret出现了,它实际上可以显著降低检测体积。
[0200]
如上所述,fret是一种非辐射能量转移,其中术语“非辐射(non-radiative)”特别重要。非辐射能量转移本质上是基于激发态中相互作用分子对的供体和受体之间的偶极-偶极耦合机制。这不是一个普通的光子发射,而是供体和受体的重新吸收(re-absorption)。
[0201]
存在许多可用于本发明的fret量化方法:
[0202]
1)敏化发射是使用校正激发和发射串扰的算法的一种直接双通道成像技术;
[0203]
2)受体光漂白(有时称为供体去淬灭)是一种当受体被光漂白时能够测量增加的供体发射的技术;
[0204]
3)荧光寿命成像显微镜fret(flim fret)是一种能够检测供体荧光寿命变化的技术;以及
[0205]
4)荧光团供体光谱成像是一种涉及在一个或两个波长激发并测量供体和受体的光谱分布的技术。
[0206]
如果fret对的供体被正常激发,例如用蓝光激发,则它通过相互转换或预备弛豫从高激发态非常快速地弛豫到第一电子激发态。从那里,它可以通过非辐射衰变的相互转换,或者通过发射光子的辐射路径,回到基态。在这种情况下,供体的分子轨道可以与受体的轨道能量耦合,发生偶极-偶极耦合,从而为激发态寿命短得多的非辐射衰减产生额外的通道。这导致供体实际上发射较少的光,或者换句话说,当敏化发射fret发生时淬灭供体。同时,当供体辐射发射被淬灭时,由于相同的偶极-偶极耦合,受体被该过程激发并开始发射荧光。因此,通过在该过程中激发供体,也部分地从受体接收发射。敏化发射可能是最简单的fret方法,因为只有一个激发源,供体荧光团从该激发源被激发,并且使用针对供体荧光和受体荧光选择的发射滤光片收集信号。存在供体时,受体荧光增强,而受体存在时,供体荧光减弱。然后荧光强度的比率变化可以用于测量fret。这是测量fret过程的最直接的方法。它本质上基于该过程中供体分子的淬灭,从而增加受体的荧光强度。在这种方法中记
录的光谱图像实际上是供体激发时的供体发射(dd)和供体激发时的受体发射(da)。它们的强度之间的比率可以指示fret效率。
[0207]
然而,如上所述,fret的直接测量是不实际的,因为供体渗出和受体直接激发,这将在下面解释。这本质上是两个荧光团(供体和受体)之间的串扰。因此,用这种方法很难获得定量准确的fret数据。为了确定样本中是否存在fret,需要另外的对照实验。
[0208]
尽管有上述限制,但是可以从供体或受体发射的变化中推断fret是可能的。用于量化fret的主要参数是fret效率e,其基本上是将能量转移到受体的受激供体的数量除以供体吸收的光子的数量。因此,这基本上是供体中将能量转移到受体的供体的分数。fret效率e也可以表示为以下比率:
[0209][0210]
其中r是福斯特半径(radius)(通常为纳米量级),表示fret效率是50%(当一半受激发的供体分子将其能量转移给受体时),r是供体和受体之间的距离。由于其是r6,使得相关性(dependence)非常陡峭。因此,测量fret效率e可以评估供体和受体之间的距离r。
[0211]
有几种方法可以测量fret效率。这里要考虑的重点是光谱的形状。典型的激发光谱总是具有朝向光谱的蓝色部分拖尾,并且在光谱的红色部分是陡峭的。典型的发射光谱看起来与激发光谱相反并且对称,并且在光谱的蓝色部分非常陡峭,但是朝向红色拖尾。因此,受体可以在不激发供体的情况下被特异性地激发,但是供体在不激发受体的情况下通常不能被激发。类似地,可以在不检测受体的情况下检测供体发射,但是在不检测供体的情况下不能特异性地检测受体。因此,受体的特异性激发和供体的特异性检测变得与用显微镜进行fret测量非常相关。
[0212]
由于供体和受体之间的上述串扰问题,该方法只有在供体和受体在相同的分子中,例如在相同多肽中时才是可行的。在这种情况下,供体和受体的化学计量在每个像素中可以保持恒定。这在例如生物测定和生物传感器中特别起作用,所述生物测定和生物传感器可以测量生理参数如钙的变化,或测量磷酸化。因此,敏化发射测量可用于检测快速动态变化,当检测fret动态范围大的荧光蛋白时尤其有用,并且供体和受体的化学计量以1:1的比例固定。
[0213]
敏化发射fret可以在各种类型的光学和光谱设备中实现,例如,在具有适当滤波器的宽场成像中,并且它非常快,因为在该方法中仅需要获取两个光谱图像。然而,这种方法不是定量的,因为它只允许测量激发态的差异,并且供体和受体的化学计量应该是恒定的,这基本上意味着在许多情况下,它们必须标记相同分子的不同部分。换句话说,特别是在本发明中,敏化发射被用作简单的fret方法,用于获取关于感兴趣对象(例如某种病原体的dna分子)的存在或不存在的初步信息。在这种情况下的答案提供了样本中分子存在的初始指示。基于该初始指示,可以校准系统。此外,本发明的算法将进行进一步的样本定量灵敏测量,其基于fret测量的另一种方法。这方面将在下面描述。
[0214]
在一些理想的情况下,如果可以在不激发受体的情况下特异性地激发供体,并且仅监测受体的荧光,那么当存在能量转移时,人们能够观察到受体发射。因此,有可能在供
体被激发而只有受体被检测的情况下产生图像。上面讨论的问题是受体被直接激发,而供体的渗漏发生在受体通道中。因此,当供体被激发,并且记录的受体发射不等于敏化发射时的情况下,图像基本上被直接激发和渗漏污染。因此,不可能精确地测量有多少受体通过。然而,当在其激发峰被直接激发时,可以精确地测量受体的量。这是可能的,因为供体通常不会在受体的激发最大值处被激发,并且测量将是非常特定的。
[0215]
由于对于相同的分子,摩尔消光系数(molar extinction coefficient,ε)是恒定的,所以在相同光谱中两个特定激发之间的比率是恒定的。因此,通过在其发射最大值处激发受体,可以精确地确定在供体发射最大值时受体的量。供体渗漏是完全相同的情况。由于供体的发射光谱重叠,不可能精确地测量含有供体和受体两者的样本中的受体,但是有可能在不存在受体的情况下专门在该波长下测量供体。
[0216]
实际上,fret测量的校正因子的确定如下。首先,对于仅含有供体的样本,测定以下两者之间的强度比s1:(a)在受体发射最大值(供体渗入受体检测通道的波长)处的供体发射,和(b)在供体发射最大值处。第二,对于仅含有受体的样本,测定以下两者之间的强度比s2:(a)在供体激发最大值处的受体激发,和(b)受体激发最大值。然后,通过测量同时含有供体和受体的样本,通过在供体存在下仅激发受体,可以确定直接激发多少受体。
[0217]
因此,在fret实验中,在表达供体之后,最初确定渗漏校正。在不存在受体的情况下,在样本中激发供体,因此,记录的是两个光谱图像:在其发射最大值(fd)处和受体的发射波长(ff)下测量供体。因此,渗漏的校正(标量(scalar))因子s1=ff/fd。它仅取决于光谱仪设置和所使用的供体,并且仅使用供体专用样本校准一次。
[0218]
类似地,引入了对直接激发的校正。在不存在供体的情况下测量样本中的受体。记录的是两个图像:在供体激发最大值(ff)处和在受体的激发波长(fa)处激发的受体。直接激发的标量因子s2=ff/fa,它仅取决于显微镜设置和所使用的受体,并且仅使用受体专用样本校准一次。因此,对于敏化发射,并且假设供体没有被受体激发所激发,则拍摄三个图像:
[0219]
1)供体激发/受体发射(ff),
[0220]
2)用于确定渗漏因子s1的供体激发/供体发射(fd),和
[0221]
3)用于确定直接激发标量因子s2的受体激发/受主发射(fa)。
[0222]
然后将缩放的图像强度ff除以缩放的受体强度fa,以获得与实际fret效率和相互作用分子的分数成比例的fret表观效率。这种缩放在大多数传统光学仪器,例如具有适当滤光器的宽场光谱仪或照相机中很容易实现。整个测量是快速的,因为人们可以在滤光轮或共焦显微镜上快速切换滤光器。然而,这种方法仍然是半定量的,因为在缩放和校正之后获得的结果图像与相互作用分子的相对浓度成比例,并且它取决于上述外部校准。这种方法的信噪比也很低,因为缩放需要测量三个单独的样本。另外,分子的光谱应该不受环境影响,例如在脂质环境和细胞质环境中应该是相同的。幸运的是,这是许多荧光蛋白就是这种情况。
[0223]
fret测量的另一种方法是受体光漂白,它实际上是定量的。受体光漂白是一种基于以下事实的方法:当一些供体荧光能量转移至受体时,供体荧光在fret期间被淬灭。但是受体荧光团的光漂白会阻止其发出荧光,并因此阻止了受体荧光团使用一些供体的能量,导致供体荧光的总体增加。这一现象可用于计算fret效率,方法是从受体光漂白后的强度中减去受体存在时的供体强度,然后将结果除以漂白后的供体强度。
[0224]
这种方法的优点是它非常耐用(robust)并且是定量的。在这种方法中,激发供体,然后记录其发射。如果发生fret,则供体被淬灭,因此发射强度降低,因为这是用于非辐射衰减的实际通道。在这种方法中,最初应该在没有受体的情况下测量供体强度,并相应地计算fret效率。问题是,这种方法假定应当进行一个单独的实验,在不存在受体的情况下测量供体。然而,对于不同浓度的分子,这将是完全不同的配置,因此应该避免单独的测量,这也是因为上面讨论的定量问题。溶液专门激发受体,直到它完全饱和并且不能吸收更多的光子,然后重新测量供体。在受体激发期间使所述受体荧光团进入短寿命且可逆的暗态(例如三重态)也将阻止其吸收更多的光子。这种方法在这里也称为“受体饱和(acceptor saturation)”。
[0225]
通常,荧光团可以通过吸收光子和电子从低能级(通常为基态)到较高能级(通常为第一激发态)而激发。电子可能会通过声子损失一些能量,然后在发射光子的同时自发返回基态(这个过程称为荧光或自发发射)。荧光发射的寿命通常以纳秒计。荧光团(不同于荧光)的受激发电子的第二弛豫机理是通过系统间交叉进入三重态。这种跃迁(transition)是量子力学禁止的,因此,它具有相对低的横截面和微秒的典型寿命(明显长于荧光寿命)。此外,电子可以随后移动到其它亚稳态电子能级,例如,通过遇到其它分子。值得注意的是,这些跃迁不涉及光子发射(或者在这样做时效率很低)。因此,这些状态被有效地认为是暗状态(dark states)。在本发明中,受体电子进入三重态和其他暗态的电子系统间交叉有助于fret受阻(frustration),因为受体不能再与受激发的供体共享能量。如果暗态相对于受体激发的调制时间是短暂的(几微秒至几毫秒),并且跃迁是可逆的,那么这种受阻在本发明中是有用的。因此,在受体激发期间,受体荧光团进入短暂且可逆的暗态(例如,三重态)的过程也包括在“受体饱和(acceptor saturation)”的定义中。
[0226]
在这种方法中,当受体饱和时,供体变成未淬灭的,并且其发射强度将上升,这实际上与不存在受体的情况相同。这种方法中的fret表观效率如下:
[0227][0228]
其中fd是当供体被活性受体淬灭时记录的供体光谱图像,f
d≠
是当受体被光漂白时记录的供体光谱图像。其将在实施例中更精确地定义。
[0229]
尽管是半定量的,但是这种方法产生的读数与复杂的真实效率(complex true efficiency)的分数成比例。因此,从这个意义上来说,它是基于强度的方法中最定量的方法,并且不需要外部校准,这是敏化发射测量的情况。在这种方法中,控制实际上是通过漂白在内部进行的。
[0230]
除了上述fret荧光技术,其他先进的光谱技术,如邻近连接(proximity ligation,pla)、双分子荧光互补(bimolecular fluorescence complementation,bifc)和荧光交叉相关光谱(fluorescence cross-correlation spectroscopy,fcs)可用于本发明。
[0231]
本文所用的术语“供体荧光团(donor fluorophore)”是指光敏荧光发射分子,其最初处于其电子激发态,可通过非辐射偶极-偶极偶联将能量转移至“受体荧光团(acceptor fluorophore)”。供体荧光团必须明亮(具有高量子产率和高吸收系数)、稳定
(具有长寿命荧光激发态和低光漂白),并且对受体荧光团激发光不敏感。
[0232]
本文所使用的术语“受体荧光团(acceptor fluorophore)”是指光敏分子,其最初处于其基态电子状态下,可通过非辐射偶极-偶极耦合从“供体荧光团(donor fluorophore)”接收能量。受体荧光团必须具有离供体荧光团大的斯特距离r0(受体荧光团的吸收光谱与供体荧光团的荧光发射光谱的高光谱重叠)、低的光漂白,必须对供体荧光团激发光不敏感,其荧光发射光谱与供体荧光团的荧光发射光谱没有串扰,并且必须能够在光激发下经历其荧光发射的可逆饱和。
[0233]
本发明中使用的合成荧光团可以包括但不限于下表c中列出的通用或专有荧光团:
[0234]
表c.适用于本发明的通用或专有示例性荧光团
[0235][0236]
可以与本发明的肽一起使用的供体荧光团的示例包括但不限于:calgold 540、calorange 560、670、705、5-fam(也称为5-羧基荧光素;也称为螺(异苯并呋喃-1(3h)、)、9'-(9h)氧杂蒽)-5-羧酸、3',6'-二羟基-3-氧代-6-羧基荧光素)、5-六氯-荧光素([4,7,2',4',5',7'-六氯-(3',6'-二戊酰基-荧光素基)-6-羧酸])、6-六氯-荧光素([4,7,2',4',5',7'-六氯-(3',6'-二戊酰荧光素基)-5-羧酸])、5-四氯-荧光素([4,7,2',7'-四氯-(3',6'-二戊酰荧光素基)-5-羧酸])、6-四氯-荧光素([4,7,2',7'-四氯-(3',6'-二戊酰荧光素基)-6-羧酸])、5-tamra(5-羧基四甲基罗丹明、9-(2,4-二羧基苯基)-3,6-双(二甲基-氨基))、6-tamra(6-羧基四甲基罗丹明、呫吨鎓
(xanthylium)、9-(2,5-二羧基苯基)-3,6-双(二甲基氨基))、edans(5-((2-氨基乙基)氨基)萘-1-磺酸))、1,5-iaedans(5-((((2-碘乙酰基)氨基)乙基)氨基)萘-1-磺酸)、dabcyl(4-((4-(二甲基氨基)苯基)偶氮)苯甲酸)、cy5(吲哚二羰花青-5)、cy3(吲哚-二羰花青-3),以及bodipy fl(2,6-二溴-4,4-二氟-5,7-二甲基-4-硼杂-3a,4a-二氮杂-s-茚-3-丙酸)、rox,及其合适的衍生物。另外的示例包括但不限于荧光素、荧光素氯三嗪基、罗丹明绿、罗丹明红、四甲基罗丹明、fitc、俄勒冈绿、alexa fluor(例如af488)、fam、joe、hex、德克萨斯红、tet、tritc、花青基染料和硫代二羰花青染料。根据一个具体的实施方式,荧光团是af488或edans。
[0237]
在一个实施方式中,供体部分是量子点。量子点是由半导体材料制成的涂覆纳米晶体,其中发射光谱由纳米晶体的尺寸控制。量子点具有宽的吸收光谱,允许用单个激发源同时发射各种颜色的荧光。量子点可以用大量的小分子和连接基团进行修饰,例如氨基(peg)或羧基量子点与链霉抗生物素蛋白的键合(量子点公司(quantum dot corporation),美国加利福尼亚,海沃德)。
[0238]
在本发明的一些实施方式中,供体和受体部分以允许能量从供体转移到受体的构型连接到肽上,从而通过fret淬灭荧光。
[0239]
在一个实施方式中,供体部分和受体部分间隔不超过3或5个氨基酸残基。在另一个实施方式中,供体和受体间隔不超过10个氨基酸残基。在另一个实施方式中,供体和受体间隔不超过15个氨基酸残基。在另一个实施方式中,供体和受体间隔不超过20个氨基酸残基。
[0240]
在一些实施方式中,上述fret效率e本身不受限制,除了淬灭效应应当最低限度地可由任何使用的检测仪器检测到。当供体在受体存在下发射的荧光减少至少10%,例如15%、20%、30%、40%、50%、60%、70%、80%、90%、95%、98%、99%、99.9%或更多时,认为荧光被“淬灭(quenched)”。如上所述,本发明中使用的受体部分可以是放射性或非放射性的,这取决于所使用的fret机理和技术。一些受体荧光团,例如四甲基-6-羧基罗丹明(tetramethyl-6-carboxyrhodamine,tamra),可以在一定波长或使用一种信号类型重新发射从供体荧光团吸收的能量,该信号类型也是可检测的,但与供体荧光团发射不同。其它受体部分,例如黑洞淬灭剂(black hole quenchers,bhqs),包括黑洞淬灭剂-1(bhq-1)、黑洞淬灭剂-2(bhq-2)、黑洞淬灭剂-3(bhq-3),不具有天然荧光,因此基本上可以消除上述其它受体上看到的问题以及背景问题。可用于淬灭几乎所有的供体荧光团的黑洞淬灭剂是市售的,例如,购自biosearch technologies公司。(加利福尼亚,诺瓦托)。
[0241]
本发明所考虑的fret对的示例包括异硫氰酸荧光素/四甲基-6-羧基罗丹明(fitc/tamra)、荧光素脒(fluorescein amidite)/tamra(fam/tamra)、fam/黑洞淬灭剂-1(fam/bhq1)、af488和bhq1(af488/bhq1),以及edans和dabcyl(edans/dabcyl)。
[0242]
在一个实施方式中,肽的c-末端与受体部分连接,肽的n-末端与供体部分连接。
[0243]
在另一个实施方式中,肽的c末端与受体部分连接,供体部分与n末端不超过3个氨基酸连接。
[0244]
在另一个实施方式中,供体部分与本身不是底物序列本身的一部分的分离部分连接(例如与半胱氨酸连接)。
[0245]
包含fret对的预期肽包括seq id no:1-10中列出的那些。在一个实施方式中,肽
是seq id no:2-10中列出的那些。在一个具体的实施方式中,所述肽具有seq id no:8所列出的氨基酸序列。
[0246]
在本发明的另一个实施方式中,信号部分是化学发光信号部分。化学发光信号部分连接到底物切割区的一侧,受体部分连接到切割区的另一侧。美国专利us 6243980(其内容通过引用并入本文)描述了这种检测系统,包括使用化学发光的1,2-二氧杂环丁烷化合物作为信号部分。如果样本中不存在病毒蛋白酶,则不会发生底物的切割。来自1,2-二氧杂环丁烷分解的能量转移到受体部分,并在不同于1,2-二氧杂环丁烷的发射光谱的波长下释放。如果底物被切割,则受体部分与1,2-二氧杂环丁烷分离,观察到来自二氧杂环丁烷化合物的化学发光发射。
[0247]
sars-cov-2 3cl蛋白酶的酶活性可以使用如以下文献中所述的显色底物检测:wang,q.m.等人,“使用肽对硝基苯胺作为底物的鼻病毒-14 3c蛋白酶的连续比色分析”,分析生物化学(anal.biochem.),第252卷,第238-245页(1997),其内容通过引用并入本文。标记的底物用于测定蛋白酶切割的能力。使用对硝基苯胺对所用的第一肽底物进行标记。当对硝基苯胺从肽上被切割下来时,产生信号。这种切割会形成芳族π电子体系,它的存在会在405纳米范围内吸收电磁光谱。切割的对硝基苯胺的纳摩尔消光系数为104摩尔-1cm31。
[0248]
可替代地,构造一端连接有荧光标签,另一端连接有淬灭剂的衬底。当肽被切割时,检测到荧光。其它标签使用类似原理,使用颜色反应。
[0249]
在另一个实施方式中,用于检测3cl蛋白酶活性的测定是非均相测定。“非均相测定(heterogeneous assay)”是指在测定过程中将固相与另一种测定组分分离的测定。在这种情况下,底物包含在可以具有以下通式的组合物中:
[0250]
x-y-z,
[0251]
其中:
[0252]
y包含病毒蛋白酶的底物,所述病毒蛋白酶对x-y-z的切割形成切割产物x-y'和y"-z,其中y'是y的第一切割产物,y"是y的第二切割产物;
[0253]
x包含可检测部分;以及
[0254]
z包含能够结合至两相分离系统的分离相的分离部分;
[0255]
其中所述x-y-z不形成所述病毒蛋白酶的天然底物的邻接部分。
[0256]
可检测部分x可直接或间接检测,并可包含标记试剂,例如酶、荧光团、发色团、蛋白质(例如,表位标签)、化学发光物质和放射性同位素。
[0257]
分离部分z能够直接或间接结合到两相分离系统的分离相(例如固相和液相)。分离部分z的示例包括免疫结合试剂、磁性结合部分、肽结合部分、亲和结合部分、核酸部分。
[0258]
本发明的组合物可以在与样本孵育之前、同时或之后与分离系统一起孵育。
[0259]
应当采取措施使可检测部分不与分离部分结合。
[0260]
在一个实施方式中,本发明的可检测部分是酶原。因此,在底物切割时,该酶可以被活化并检测(通过检测其催化活性)。这种酶原的一个示例是凝血酶原(pro-thrombin)(因子ii)或该级联(cascade)中的其它酶。
[0261]
在本文描述的任何实施方式中,任何部分可以通过共价键直接连接到肽上,或通过在每一末端具有偶联官能团的间隔分子间接地连接到肽上。这种连接因子(linkers)的示例包括烷基、二醇、醚、聚醚、多核苷酸和多肽分子。
[0262]
适用于非均相测定的固相包括但不限于试管、微量滴定板、微量滴定孔、珠粒、试纸(dipsticks)、聚合物微粒、磁性微粒、硝化纤维、芯片阵列和本领域技术人员熟悉的其它固相。用于非均相测定的信号部分可以是本领域技术人员已知的任何标记。这些标记包括放射性、量热(calorimetric)、荧光和发光标记。
[0263]
用于检测蛋白酶的非均相化学发光测定法描述于美国专利us 56243980中,其内容通过引用并入本文。在一个实施方式中,本发明的均相或非均相测定方法是自动化的,从而可以直接获得结果,而不需要医务人员接触被认为受待测病毒性疾病感染的主体。例如,主体可以在一个干净的房间中进行测试(例如,但不限于p3式房间)。主体可以在进入房间之前拾取或获得诊断试剂盒,所述诊断试剂盒可以包括涂覆有上述类型的标记肽的固相。例如,固相可以是预先浸有肽的组织,或可以是用于测试妊娠的类型的测试棒。主体可以向固相上预先制备好的点处提供样本,例如唾液样本。
[0264]
然后孵育含有样本的固相,以使酶反应发生。在一个实施方式中,将反应温度控制在37℃,以提供酶反应的最佳条件。孵育完成后,可以在分光光度计上,使用遥控器或在室外手动操作的机械系统,测量待测样本。可以对样本进行定性颜色或紫外检测。测试后,样本可以被自动系统丢弃,或者被远程操作的手柄丢弃。在一个实施方式中,本文所述的肽在一端与生物素部分连接,在另一端与hcg激素连接。3cl蛋白酶可以使用为妊娠测试(或类似测试)而配置的横向流设备来检测。
[0265]
分析或监测可检测信号的方法是本领域已知的。在一个实施方式中,在多孔板(例如96或384孔板)上进行测定,使用板读数器(例如tmg板读数器)来检测信号。这对于在公共场所如教育场所(例如学校和大学)和旅行相关场所如机场和旅馆中的快速检测可能特别相关。
[0266]
在本发明中可以使用许多不同配置的光学和光谱装置。例如,本发明的光学装置可以是模块化的,并且可以被配置成作为便携式的和高灵敏度的荧光分光光度计(荧光计)、光度计、荧光显微镜或其组合来操作,用于测量荧光、发光或磷光。这些光学装置可以方便地放置在公共场所的入口处,例如剧院、餐馆和工作场所。它们的小型化版本可用于公共场所、工作场所和家中的快速现场即时诊断。
[0267]
本发明的光学设备的激发模块、样本室和采集模块可以根据期望的应用来配置,并且适合于特定的应用。例如,可以选择样本室作为荧光多板读数器,用于对多个样本进行实验室高通量和快速的多路分析,用于现场即时诊断。
[0268]
在一些实施方式中,检测器和计算单元被组合在单个单元中,该单个单元被设计成执行荧光发射的采集、测量其强度、处理荧光发射数据,并可选地以可读格式显示该数据和/或将其输出到外部存储器或用户界面。在另一个具体实施方式中,采集模块(acquisition module)可以是智能手机或适于执行期望测量的任何其它移动设备或小配件(gadget)的一部分。在某个实施方式中,检测器是电子倍增电荷耦合设备(electron-multiplying charge-coupled device,emccd)成像器、电荷耦合设备(charge-coupled device,ccd)成像器、雪崩光电二极管(avalanche photodiode,apd)、光电倍增管(photomultiplier tube,pmt)、科学互补金属氧化物半导体(scientific complementary metal-oxide-semiconductor,scmos)成像器或智能手机摄像头(smartphone camera)的cmos成像器、独立照相机,或任何移动设备或配件的照相机,所述检测器可选地具有聚焦装
置和计算机链接。在一个具体实施方式中,检测器是智能手机摄像头的cmos成像器。在又一具体实施方式中,与采集模块组合的样本室构成荧光显微镜,或者所述光学装置是安装在单个壳体中的组合荧光计和荧光显微镜,或者所述光学装置结合在荧光显微镜内部。所述显微镜被设计成从单分子定位产生原始数据,作为视频或作为一系列静态图像,并进一步处理由显微镜产生的所述原始数据,以集成所述荧光发射强度数据和所述显微镜原始数据,并以可读格式提供关于分子相互作用和关于单分子的纳米接近度(nanometre proximity)的信息,或将所述信息输出到外部存储器或用户界面。在一个具体的实施方式中,所述样本室是适于多路复用多个样本的多路复用分光光度或成像设备或其部分。这种多路复用设备的一个例子是前述酶标仪(microplate reader)。
[0269]
在荧光计功能的情况下,激发源可以选自宽光谱卤素灯、弧光灯或汞蒸气灯,其被配置为分别在所述供体荧光团或所述受体荧光团的预定波长范围或峰值波长附近发射所述供体荧光团激发光和所述受体荧光团激发光。在这种情况下,激发单色器可以是光电倍增管(pmts),发射单色器可以是衍射光栅。
[0270]
在显微镜功能的情况下,第一和第二激发单色器分别是第一和第二激发滤光器,其被设计成用于选择和传输(transmit)来自相应激发源的光的激发波长的窄波长光束,而所述发射单色器是被设计成用于传输(transmit)所述供体荧光团发射的窄波长光束的发射滤光器。
[0271]
在本发明中用于分析可检测信号的另一种设备是横向流设备,其可以是棒或堆的形式。横向流设备可以基于常规硝化纤维素膜或纤维素(纸)膜。这种类型的装置可用于病毒的家庭或现场检测。
[0272]
在一个具体的实施方式中,将本发明的生物测定结合到微流体芯片或实验室-芯片中。本发明的方法可适用于在这种芯片上进行。
[0273]
(密迪斯技术公司(medis technologies ltd.)是可用于监测蛋白酶活性的血细胞计数器。cellscan的核心是含有多达10,000个孔的细胞载体。关于cellscan血细胞计数器及其用于诊断癌症和自身免疫性疾病诊断中的其他用途的描述可从以下网址获得:www.medisel.com。
[0274]
cellscan探针装载有肽底物,例如上文公开的那些。肽底物在切割区的一侧用供体基团标记,在另一侧用受体标记。将待测样本装载到探针上。如果存在活性蛋白酶,cellscan将检测由切割的肽引起的荧光。活性蛋白酶的存在及其在样本中的浓度是活性病毒的指示,并用作患者的传染性状态的指示。
[0275]
在另一个实施方式中,基于薄纸的自动化系统(paper-tissue-based automated system)可用于检测sars-cov-2。制备对sars-cov-2的3cl蛋白酶特异的颜色标记的肽底物(如上文公开的)的溶液。将薄纸(例如湿纸巾)浸入基质化合物溶液中,并保持湿润。将疑似含有sars-cov-2病毒的标本与组织接触。如果存在sars-cov-2病毒,则3cl蛋白酶切割标记的肽序列,反应混合物显色或变色。
[0276]
对于有色反应产物的检测存在几种可能性。对于定性分析,可以视觉检测颜色反应。对于定性分析,将组织转移到分光光度分析仪上进行荧光或颜色检测。该过程可以是自动化的,以便保护进行测定的人员免受感染。
[0277]
根据一个具体的实施方式,该测定可以在不到30分钟,优选在不到20分钟内检测
clin chem clin biochem),18:197-208;schuurs ah.和van weemen bk.,1980,免疫测定杂志(j immunoassay)1:229-49。
[0289]
亲和标签(affinity tag)(或结合对的成员)可以是可由相应抗体识别的抗原[例如,digoxigenin(dig),其由抗-dig抗体识别),或对标签具有高亲和力的分子[例如,抗生物素蛋白链菌素(streptavidin)和生物素(biotin)]。结合亲和标签的抗体或分子可以如上所述被荧光标记或键合到酶上。
[0290]
本领域广泛实施的各种方法可用于将抗生物素蛋白链菌素或生物素分子连接到抗体上。例如,生物素分子可以通过生物素蛋白连接酶(例如,bira)的识别序列链接到本发明的抗体上,如以下实施例部分和denkberg,g.等人所述,2000,欧洲免疫学杂志(eur.j.immunol.),30:3522-3532。可替代地,抗生物素蛋白链菌素分子可链接到抗体片段,如单链fv,基本上如以下文献所述:cloutier sm.等人,2000,分子免疫学(molecular immunology)37:1067-1077;dubel s.等人,1995,免疫学方法杂志(j immunol methods)178:201;huston js.等人,1991,酶学方法(methods in enzymology)203:46;kipriyanov sm.等人,1995,人类抗体和杂交瘤(hum antibodies hybridomas)6:93;kipriyanov sm.等人,1996,蛋白工程(protein engineering)9:203;pearce la.等人,1997,生物化学分子生物国际(biochem molec biol intl)42:1179-1188。
[0291]
蛋白质印迹:该方法涉及通过丙烯酰胺凝胶将底物与其它蛋白质分离,然后将底物转移到膜(例如尼龙或pvdf)上。然后通过对底物特异的抗体来检测底物的存在,该抗体又通过抗体结合试剂来进行检测。抗体结合试剂可以是例如蛋白a或其它抗体。如上所述,抗体结合试剂可以是放射性标记的或酶连接的。检测可以通过放射自显影、比色反应(colorimetric reaction)或化学发光进行。该方法既可以定量底物的量,又可以通过膜上的相对位置来确定其身份,该相对位置表示电泳过程中丙烯酰胺凝胶中的迁移距离。
[0292]
放射免疫测定(radio-immunoassay,ria):在一种形式中,该方法涉及用固定在可沉淀载体如琼脂糖珠上的特异性抗体和放射性标记的抗体结合蛋白(例如,用i125标记的蛋白a)沉淀所需的蛋白(即,底物)。沉淀颗粒中的计数与底物的量成比例。
[0293]
在ria的替代形式中,使用了标记的底物和未标记的抗体结合蛋白。以不同的量加入含有未知量底物的样本。来自标记底物的沉淀计数的减少与加入的样本中底物的量成比例。
[0294]
荧光活化细胞分选(fluorescence activated cell sorting,facs):该方法涉及通过底物特异性抗体在细胞中原位检测底物。底物特异性抗体与荧光团连接。检测是通过细胞分选机进行的,当细胞通过光束时,该细胞分选机读取每个细胞发出的光的波长。该方法可同时使用两种或多种抗体。
[0295]
免疫组织化学分析:该方法涉及通过底物特异性抗体在固定细胞中原位检测底物。底物特异性抗体可以是酶连接的或与荧光团连接的。通过显微镜和主观或自动评价进行检测。如果使用酶连接的抗体,可能需要比色反应。应当理解,免疫组织化学之后通常使用例如苏木精(hematoxyline)或姬姆萨染色(giemsa stain)对细胞核进行复染。
[0296]
一旦作出sars-cov-2感染阴性的诊断,本发明人进一步考虑产生消息或发出通知,将诊断结果通知给主体。
[0297]
一旦作出sars-cov-2感染阳性的诊断,本发明人进一步考虑治疗和/或控制感染。
[0298]
covid治疗的示例包括施用抗病毒剂、抗病毒疗法、入院、机械通气、侵入性监测、最后手段药物(last-resort drug)、镇静、重症监护入院、手术干预、入院和隔离。
[0299]
根据进一步的实施方式,一旦诊断出阳性感染,该方法进一步考虑提供隔离主体的建议。
[0300]
还提供了包含本发明的肽的试剂盒。不同的试剂盒组分可以包装在单独的容器中,并在使用前立即混合。组分的这种单独包装可以允许长期储存而不丧失活性组分的功能。还考虑了在同一容器中发现两种或多种组分的实施方式。示例性试剂盒可包含一种或多种以下试剂:(a)用于非均相测定的洗涤缓冲液试剂;(b)不含能够切割底物的蛋白酶的阴性对照试剂;(c)含有能够切割底物的蛋白酶的阳性对照;(d)用于从信号部分产生可检测信号的信号产生试剂;和(e)样本采集装置,例如注射器、咽喉拭子或其它样本采集装置,其具有适当的采集缓冲液(与样本类型匹配)。
[0301]
在一个实施方式中,阳性对照中使用的蛋白酶包含seq id no:34所列的氨基酸序列。
[0302]
在另一个实施方式中,阳性对照中使用的蛋白酶包含组氨酸标签(例如,如seq id no:35所列)。
[0303]
在一个实施方式中,阴性对照中使用的的蛋白酶具有seq id no:36所列的氨基酸序列。
[0304]
对于多重病毒检测试剂盒,其中如上所述检测一种或多种病毒,每个多组检测试剂盒将优选地根据共同主题设计,例如引起相同或相似疾病的不同病毒,感染相同组织或器官的病毒,亲缘关系密切的病毒(viruses of close phylogenetic relationship),例如分类为相同科、亚科等的病毒,可以在相同体液,例如唾液、鼻分泌物、血液、尿液、粪便等中检测到的病毒,常见和广泛传播的病毒,通过相同体液传播的病毒等。
[0305]
试剂盒中包含的试剂可以在任何种类的容器中提供,使得不同组分的保存期得以保存,并且不会被容器的材料吸附或改变。例如,密封的玻璃安瓿可以包含冻干的试剂,或中性、不起反应的气体(如氮气)条件下包装的缓冲液。安瓿可以由任何合适的材料组成,例如玻璃、有机聚合物,例如聚碳酸酯、聚苯乙烯等;陶瓷、金属或通常用于容纳类似试剂的任何其它材料。合适的容器的其它示例包括简单瓶子和封套,其中瓶子由与安瓿和封套类似的物质制成,封套可以包括箔衬里的内部,例如铝或合金。其它容器包括试管、小瓶、烧瓶、瓶子、注射器等。容器可以具有无菌入口,例如瓶子,该瓶子具有塞子,塞子可以被皮下注射针头刺穿。其它容器可具有两个隔室,这两个隔室被容易移除的膜隔开,该膜在移除时允许组分混合。可移除膜可以是玻璃、塑料、橡胶等。
[0306]
试剂盒还可以包含适于分析蛋白酶的缓冲液。
[0307]
用于分析唾液的示例性缓冲液包括5mm bolt(稳定的dtt)、50mm tris(ph 8.0)、0.75m na2so4。可选地,缓冲液可进一步包含bsa(例如0.2mg/ml)。试剂盒还可以包含对sars-cov2 3cl蛋白酶没有活性的蛋白酶抑制剂。这些蛋白酶抑制剂包括但不限于抗痛素(antipain)、ac-devd-cho、抑肽酶、eglin c、gw、pmsf和2,6pda中的至少一种。根据一个具体实施方式,蛋白酶抑制剂包括pmsf和gw。
[0308]
用于颊样本的试剂盒还可以包含蛋白酶抑制剂。这种蛋白酶抑制剂优选对sars-cov-2 3cl蛋白酶没有活性。预期的蛋白酶抑制剂的示例包括但不限于pmsf、gw、抑肽酶、
eglinc和胃蛋白酶抑制剂(pepstatin)中的至少一种。根据一个具体实施方式,蛋白酶抑制剂包括pmsf、gw、抑肽酶和eglinc。
[0309]
试剂盒还可以提供有说明书(指导材料)。说明书可印刷在纸上或其它基底上,和/或可提供为电子可读介质,例如软盘、cd-rom、dvd-rom、zip盘、录像带、录像带等。详细的说明书可以不与试剂盒物理关联;取而代之的是,用户可以被引导到由试剂盒的制造商或经销商指定的互联网网站,或者以电子邮件的形式提供。
[0310]
如上文所述和如以下权利要求部分所要求保护的本发明的各种实施方式和方面在以下实施方式中得到实验支持。
[0311]
实施例
[0312]
现在参考以下实施例,其与以上描述一起以非限制性方式说明本发明的一些实施方式。
[0313]
通常,本文使用的命名法和本发明中使用的实验室方法包括分子、生物化学、微生物和重组dna技术。这些技术在文献中有详尽的解释。参见,例如,“分子克隆:实验室手册(molecular cloning:a laboratory manual)”,sambrook等人,(1989);“分子生物学实验手册(current protocols in molecular biology)”,第i-iii卷,ausubel,r.m.编辑(1994);ausubel等人,“分子生物学实验手册(current protocols in molecular biology)”,约翰威立国际出版公司(john wiley and sons),马里兰州巴尔的摩(1989);perbal,“分子克隆实用指南(a practical guide to molecular cloning)”,约翰威立国际出版公司(john wiley&sons),纽约(1988);watson等人,“重组dna(recombinant dna)”,科学美国人书(scientific american books),纽约;birren等人(编辑),“基因组分析:实验室手册系列(genome analysis:a laboratory manual series)”,第1-4卷,冷泉港实验室出版社(cold spring harbor laboratory press),纽约(1998);如以下专利中的方法:美国专利us4,666,828;us 4,683,202;us4,801,531;us5,192,659和us5,272,057;“细胞生物学:实验室手册(cell biology:a laboratory handbook)”,第i-iii卷,cellis,j.e.编辑(1994);freshney的“动物细胞培养-基础技术手册(culture of animal cells-a manual of basic technique)”,wiley-liss公司,n.y.(1994),第三版;“免疫学实验室手册(current protocols in immunology)”,i-iii卷coligan j.e.编辑(1994);stites等人(编辑),“基础和临床免疫学(basic and clinical immunology)”(第8版),appleton&lange公司,诺瓦克ct(1994);mishell和shiigi(编辑),“细胞免疫学中的选择方法(selected methods in cellular immunology)”,w.h.freeman and co.公司,纽约(1980);可用的免疫测定在专利和科学文献中有广泛的描述,参见,例如,美国专利us3,791,932;us3,839,153;us3,850,752;us3,850,578;us3,853,987;us3,867,517;us3,879,262;us3,901,654;us3,935,074;us3,984,533;us3,996,345;us4,034,074;us4,098,876;us4,879,219;us5,011,771和us5,281,521;“寡核苷酸合成(oligonucleotide synthesis)”,gait,m.j.编辑(1984);“核酸杂交(nucleic acid hybridization)”,hames,b.d.和higgins s.j.编辑(1985);“转录和翻译(transcription and translation)”,hames,b.d.和higgins s.j.编辑(1984);“动物细胞培养(animal cell culture)”,freshney,r.i.编辑(1986);“固定化细胞和酶(immobilized cells and enzymes)”,irl出版社(1986);“分子克隆实用指南(a practical guide to molecular cloning)”,perbal,
3cpro的抗体特异性检测条带,见图3。
[0322]
2007年发表的一项研究表明,向3clpro添加c-末端或n-末端his-标签会严重影响酶活性(grum-tokars等人,病毒研究(virus research),2007)。因此,his-标签被添加为可切割标签(enlyfqg-seq id no:37),其可以在通过tev蛋白酶纯化后被切割。用tev蛋白酶切割纯化的sars-cov-23clpro,并将其活性与未切割的蛋白酶进行比较。在两种不同的条件下进行切割:在30℃下1小时或在在4℃下过夜。tev蛋白酶购自纽英伦公司(new england biolabs),并包括his标签。这样,通过在histrap柱上运行反应混合物并收集流出物,可以随后从切割的3clpro中除去tev-蛋白酶和潜在的未切割的3clpro。从图2可以看出,3clpro的切割是成功的(未切割的分子量为35.6kda,切割的分子量为33.9kda)。
[0323]
实施例2
[0324]
3cl活性的最佳反应条件
[0325]
为了找到最终和最佳的反应条件,测试了几个参数:
[0326]
反应稳定剂(bsa):在室温下与0.2mg/ml bsa孵育5小时的酶保持其活性。
[0327]
还原剂:在不同浓度下测试dtt和tcep,以观察酶活性是否受到影响。5mm dtt显示出在保持酶活性方面最有效。dttbolt(英杰生命技术有限公司(invitrogen)cat号:b0009)显示出改善的效果。
[0328]
甘油(glycerol)、nacl和na2so4:这些参数被测试为潜在的酶介质(enyme mediators)。对于nacl和甘油,没有注意到对酶活性的积极影响。na2so4增强了酶活性。选择浓度0.75m的na2so4。
[0329]
ph-酶活性:测试了宽ph范围(6.5、7、7.4、8、8.5)下的ph-酶活性。随着ph增加到8.0(最大活性),活性增加,当ph为8.5时活性降低。
[0330]
推荐的最终测定条件:96孔黑色非结合平底(ref 655900greiner bio-one),反应体积100μl(50μl底物溶液加入到50μl酶/唾液/刺突溶液(spike solution)中),在bmg clariostar plus上监测反应,发射/激发波长为340/510nm,增益2000(读板器灵敏度),酶浓度150,300ng/反应,底物浓度5μm;反应缓冲液5mm bolt(稳定的dtt),50mm tris(ph 8.0),0.75m na2so4和0.2mg/ml bsa。
[0331]
进行了总结实验,以验证优化工作、最终测定条件和反应速率提高。通过向45μl反应缓冲液中加入5μl唾液进行测定,掺入300ng 3cl以及未掺入300ng 3cl。通过加入50μl的10μm试剂盒底物(5μm终浓度,来自市售试剂盒bps,cat号:79955-1)引发反应。测试了3种不同的唾液样本,在此由样本y表示,图3a-c。
[0332]
如图3a-c和表1清楚表明的,与市售缓冲液(186rfu/min)和起始缓冲液(110rfu/min)相比,优化程序导致在最终缓冲液条件(2986rfu/min)下酶活性的显著提高。记录了超过一个数量级的改善。这种改善效果在唾液临床样本条件和3clpro掺入下得以保持。最终缓冲区(1586)中的尖峰效应(δ(delta))与市售缓冲区(303rfu/min)和起始缓冲区(82rfu/min)中的δ相比较。这相当于信噪比从0.1到0.5-1,提高了十到五倍。
[0333]
表1
[0334] 市售缓冲液起始缓冲液最终缓冲液酶186 /-2025 /-242986 /-90唾液2996 /-322215 /-333024 /-126
唾液 酶3299 /-212297 /-384572 /-73空白(blank)-15 /-5-84 /-292 /-32δ刺突(delta spike)303821586
[0335]
实施例3
[0336]
底物序列和fret对对3cl特异性和唾液非特异性活性的影响
[0337]
设计了5种底物并与已知的试剂盒底物(biosyn)进行比较。
[0338]
试剂盒底物-dabcyl-ktsavlqsgfrkme-edans(seq id no:1)
[0339]
底物#1-dabcyl-tsavlqsgfrk-edans(a4760-1-seq id no:2)
[0340]
底物#2-dabcyl-tsavlqsgf-edans(a4760-2-seq id no:3)
[0341]
底物#3-dabcyl-avlqsgf-edans(a4760-3-seq id no:4)
[0342]
底物#4-dabcyl-avlqsgfrk-edans(a4760-4-seq id no:5)
[0343]
底物#5-dabcyl-tsavlqsgfyk-edans(a4760-5-seq id no:6)
[0344]
对于这些酶促反应,在最终和优化的测定条件(即5μm底物)下,使用150ng/孔的酶。实验用3种不同的唾液样本进行测试;显示了代表性的结果。
[0345]
结果示于图4和图5a-f,总结于表2。
[0346]
表2
[0347] 市售底物#1#2#3#4#5酶2312 /-25978 /-14449 /-36354 /-181077 /-35527 /-7唾液2309 /-641123 /-35187 /-747 /-51515 /-404688 /-53空白94 /-1634 /-87 /-415 /-241 /-166 /-1
[0348]
为了提高测定灵敏度,合成了另外四种底物,并用bhq1/af488 fret对(剑桥研究生物化学品公司(cambridge research biochemicals))进行了测试:
[0349]
底物#1-[bhq-1]-tsavlqsgfrk-[cys(af488)]-酰胺(4168-3)-seq id no:7
[0350]
底物#2-[bhq-1]-tsavlqsgf-[cys(af488)]-rk-酰胺(41469-2)-seq id no:8
[0351]
底物#3-[bhq-1]-avlqsgf-[cys(af488)]-rk-酰胺(41470-2)-seq id no:9
[0352]
底物#4-[bhq-1]-avlqsgfrk-[cys(af488)]-酰胺(a4771-1)-seq id no:10。
[0353]
使用了以下测定条件:
[0354]
方法:发射/激发波长为488/535nm,增益1400。
[0355]
缓冲液-5mm bolt(dtt)、50mm tris(ph 8.0)、0.75m na2so4无bsa(因为它对底物切割有影响)。
[0356]
底物浓度1um。
[0357]
用3个其他唾液样本进行实验;代表性结果示于图6和图7a-d中,并总结于表3中。
[0358]
表3
[0359] cbr#1cbr#2cbr#3cbr#4biosyn#1酶5508 /-866425 /-41461 /-18657 /-630 /-1.3唾液1356 /-37512 /-16154 /-6726 /-25 空白38 /-323 /-428 /-141 /-14 /-0.2
[0360]
新底物导致更高的测定灵敏度(与biosynthesis肽相比)。对于底物2(seq id no:8),信噪比提高了两个数量级以上(从0.1到12.5)。
[0361]
sars-cov-2 3cl pro比酶活性(specific enzymatic activity)评估
[0362]
用四种不同的底物(biosyn#1、6、7和bps底物)测试了sars-cov-2的3cl pro的比酶活性(specific enzymatic activity),并与人类鼻病毒(human rhinovirus,hrv)和常见的人类冠状病毒物种cov-229e的酶活性进行了比较。运行条件:底物浓度-5μm,酶浓度150ng/反应。
[0363]
bps底物(cov19)-dabcyl-ktsavlqsgfrkme-edans(seq id no:1;79955-1,bps bioscience公司)
[0364]
biosyn#1(cov19)-dabcyl-tsavlqsgfrk-edans(seq id no:2;a4760-1,biosynthesis公司)
[0365]
biosyn#6(229e)-dabcyl-ygstlqaglrk-edans(seq id no:11;a4911-1,biosynthesis公司)
[0366]
biosyn#7(hrv)-dabcyl-lealfqgp[asp-(edans)sq[酰胺](seq id no:12,a4911-2,biosynthesis公司)。
[0367]
结果总结于下表4和5中。
[0368]
表4:使用4种底物的sars-cov-2、hcov-229e和hrv的酶活性(rfu/min)
[0369][0370]
表5:使用4种底物时,hocov-19与hcov-229e和hrv相比的比酶活性
[0371]
底物/%酶活性(enz activity)sars-cov-2hcov-229ehrvbps(市售的)100261biosyn#110095-1*biosyn#6190100-7*biosyn#700100
[0372]
hocov-19的比酶活性可以从表4和表5所示的结果种得出。检测biosyn#1底物的交叉反应性。对于biosyn#1底物,hocov-19的酶活性类似于hcov-229e的酶活性。由于3cl蛋白酶的高度进化保守性,这种交叉反应性在某种程度上是可以预料的。然而,bps和biosyn#6底物对sars-cov-2的活性都高于hcov-229e蛋白酶。这种活性差异可作为这些病毒之间的区别因素。
[0373]
对于最大量的普通感冒病毒hrv,观察到完全特异性(无交叉反应性)。biosyn#7底物对hrv是特异性的。
[0374]
使用肽(seq id no:8)时,sars-cov-2、hcov-229e和hrv 3cl以及3c蛋白酶的酶活性(rfu/min)总结于表6中。底物浓度-1μm,酶浓度150ng/反应。
[0375]
表6:使用4种底物时,sars-cov-2、hcov-229e和hrv的酶活性(rfu/min)
[0376][0377]
实施例4
[0378]
优化抑制剂混合物(cocktail)以最大化唾液非特异性蛋白酶活性抑制
[0379]
向缓冲液中加入蛋白酶抑制剂的目的是降低非特异性唾液活性,并增加信噪比。使用唾液样本中的3cl蛋白酶的竞争性酶活性测定来测试29种抑制剂。
[0380]
抗痛素、ac-devd-cho、抑肽酶、eglin c、gw、pmsf和2,6pda均降低唾液中的非特异性蛋白酶活性,而对3cl特异性活性的抑制不明显。
[0381]
还测试了不同抑制剂混合物:
[0382]
混合物1(pmsf、gw、抑肽酶、胃蛋白酶抑制剂和肝素(heparin));
[0383]
混合物2(pmsf和gw)
[0384]
混合物3(pmsf、gw和抑肽酶)。
[0385]
在不同抑制剂混合物之间没有发现明显差异。
[0386]
实施例5
[0387]
优化抑制剂混合物以最大化颊样本非特异性蛋白酶活性抑制
[0388]
使用颊样本中3cl蛋白酶的竞争性酶活性测定测试了29种抑制剂。
[0389]
pmsf、gw、抑肽酶、eglinc和胃蛋白酶抑制剂均降低唾液中的非特异性蛋白酶活性,而对3cl特异性活性的抑制不明显。
[0390]
四种最佳抑制剂是eglin c、gw、pmsf和2,6pda。
[0391]
还测试了不同抑制剂混合物:
[0392]
混合物1(pmsf、gw);
[0393]
混合物2(eglin c、gw、pmsf和2,6pda)
[0394]
混合物2比混合物1更大程度地减少了非特异性蛋白酶。
[0395]
实施例6
[0396]
样本的储存
[0397]
在4℃下储存样本(颊、nmt和刺突(spike)),24小时后酶活性保留约50%。最明显的降低发生在0至2小时之间。所有样本的酶活性在4至8小时之间保持稳定。然而,在4℃下放置24小时后,以及在-20℃下储存样本的冷冻/解冻循环后,可以清楚地检测到颊和nmt拭子中掺入了3cl重组蛋白酶。
[0398]
实施例7
[0399]
pcr测试与3cl活性测定的比较
[0400]
将该测定的灵敏度与各基因(rdr基因-图17a,e基因-图17b,以及n基因-图17c)的pcr测定的灵敏度进行比较。如图所示,较高的3cl蛋白酶活性比率与指示较高病毒rna拷贝数的pcr ct值相关。
[0401]
如表7中所总结的,使用3cl蛋白酶活性测定从症状发作后一个多月收集的样本中获得了阳性结果。
[0402]
表7
[0403][0404][0405]
nd=未测定,无数据
[0406]
nt=未测试
[0407]
另外,本发明的任何一个或多个优先权文件通过引用整体并入本文。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。