1.本发明属于生物监测技术领域,具体涉及一种检测人巨细胞病毒核酸的引物探针组合物、试剂盒及其使用方法。
背景技术:
2.人巨细胞病毒(human cytomegalovirus,hcmv)又称人类疱疹病毒5型,属于疱疹病毒科β亚科,属于疱疹病毒科β亚科,是巨细胞包涵体病的病原体。人巨细胞病毒圆形、直径100~200nm,基因组为线性dsdna。人类是hcmv唯一的天然宿主,是一个广泛传播的人类致病原,可通过唾液、尿或者泌乳自然传播。还可通过性接触,输血和器官移植传播。
3.hcmv在人群中的感染率很高,我国成人的hcmv抗体阳性率达90%。原发性感染多发生在2岁以下,通常以隐性感染为主,仅仅少数人有临床症状。但在一定条件下,病毒可以侵袭多个器官和系统产生严重疾病。感染常见于孕妇、胎儿和新生儿,在孕期感染原发性hcmv的胎儿及新生儿中,80%可导致智力低下、畸形和死亡;婴幼儿感染后会导致肝脾肿大、智力低下、脉络膜视网神经炎等严重疾病。免疫缺陷患者、器官移植后接受免疫抑制治疗、恶性肿瘤治疗后常导致严重的hcmv感染,常发生全身性疾病,病死率高。
4.因此,建立快速、准确的检测人巨细胞病毒感染的方法具有重要意义。
5.目前,病毒分离培养是临床实验室hcmv感染检测的标准,但其检测周期长达30天,因此不适合临床实验室使用。目前国内有hcmv检测方面的产品较多,多是基于免疫方法检测人巨细胞病毒igg/igm的产品,基于pcr技术检测人巨细胞病毒的试剂盒较少,自动化程度不高,假阴性较高。
技术实现要素:
6.本发明针对现有临床人巨细胞病毒检测的困难,提供一种检测人巨细胞病毒核酸的引物探针组合物、试剂盒及其使用方法。用这种试剂盒对人巨细胞病毒核酸进行检测时,灵敏度高、检测时间短、假阴性低、快捷简便。
7.本发明通过以下技术方案实现:
8.第一方面,本发明提供一种检测人巨细胞病毒核酸的引物探针组合物,这种引物探针组合物包括实时荧光pcr引物和探针;
9.上述实时荧光pcr引物包括seq id no.1~2所示的的核苷酸序列;
10.上述探针包括seq id no.3所示的的核苷酸序列;
11.具体地,该引物探针组合物的序列如下:
[0012][0013]
进一步地,在本发明较佳的实施例中,上述探针为taqman探针,taqman探针的5’端标记有荧光报告基团,3’端标记有荧光淬灭基团。
[0014]
进一步地,荧光报告基团包括fam、cy5、rox、vic和ned中的至少一种;优选地,荧光报告基团为fam。
[0015]
进一步地,所述荧光淬灭基团包括mgb-nfq、qsy和bhq1中的至少一种;荧光淬灭基团为mgb-nfq。
[0016]
第二方面,本发明提供一种检测人巨细胞病毒核酸的试剂盒,其包括:上述引物探针组合物。
[0017]
进一步地,在本发明较佳的实施例中,上述试剂盒还包括针对人类hbb基因保守序列特异性的内参引物和内参探针;
[0018]
优选地,所述内参引物包括seq id no.4~5所示的的核苷酸序列;
[0019]
优选地,所述内参探针包括seq id no.6所示的的核苷酸序列;
[0020]
具体地,该引物探针组合物的序列如下:
[0021]
hbb核苷酸序列序号正向序列(f)5
’‑
ttggacccagaggttctttga-3’seq id no.4反向序列(r)5
’‑
gccatgagccttcaccttagg-3’seq id no.5内参探针(p)vic-5
’‑
tccactcctgatgctg-3
’‑
mgbnfqseq id no.6
[0022]
优选地,试剂盒中hcmv引物浓度为100nm,探针浓度为100nm;hbb引物浓度为500nm,探针浓度为200nm。
[0023]
进一步地,在本发明较佳的实施例中,上述试剂盒还包括pcr反应液和/或染料;
[0024]
优选地,pcr反应液包括taq酶、ung酶、mg2 缓冲液、dntps;
[0025]
优选地,染料包括rox矫正染料。
[0026]
更为优选地,在本发明较佳的实施例中,试剂盒中的扩增反应体系包括:
[0027]
hcmv反应液:含针对hcmv pp65基因保守区域特异性的引物探针组合物,序列如seq id no.1~3;针对hbb保守序列特异性的内参引物及探针,序列如seq id no.1~3,rox矫正染料;
[0028]
hcmv预混液a:taq酶、ung酶;
[0029]
hcmv预混液b:pcr缓冲液、dntps、mg
2
等;
[0030]
阳性对照:含hcmv靶序列的假病毒,人hbb基因靶序列的质粒。
[0031]
阴性对照:rnase-free ddh2o。
[0032]
第三方面,本发明还提供一种上述试剂盒以非疾病诊断和/或治疗为目的的使用方法,其包括:
[0033]
提取待测样本的基因组,使用所述试剂盒对所述待测样本的基因组进行扩增,检测荧光信号,再进行分析。
[0034]
进一步地,在本发明较佳的实施例中,上述扩增的程序包括:
[0035][0036]
进一步地,在本发明较佳的实施例中,对荧光信号进行分析包括:
[0037]
当fam荧光通道中扩增曲线呈s型,且ct≤36时,判断所述待测样本为人巨细胞病毒阳性;
[0038]
当fam荧光通道中ct》36或无扩增,vic荧光通道中扩增曲线呈s型,且ct≤36时,判断样品为人巨细胞病毒阴性。
[0039]
其中,当fam荧光通道中ct》36或无扩增,且vic荧光通道中ct》36或无扩增,判定为实验异常,需要重新提取标本检测或重新取样检测。
[0040]
与现有技术相比,本发明至少具有如下技术效果:
[0041]
本试剂盒通过将采集的样本经常规方法提取核酸后,在taq dna聚合酶的作用下,使用taqman探针,利用实时荧光信号实现人巨细胞病毒核酸检测。本试剂盒没有复杂的核酸提取过程,荧光定量pcr过程采用一步法进行。采用这种试剂盒检测人巨细胞病毒,至少具有如下有益效果:
[0042]
1.加快临床诊断效率:本发明提供了人巨细胞病毒实时荧光pcr检测的引物探针组、试剂盒及使用方法,能够快速、准确且灵敏地检测出人巨细胞病毒,实验结果重复性好,精密度高。本发明检测时间周期短,最快能在70分钟内完成检测,极大的节约了检测时间,加快临床诊断效率。
[0043]
2.全程质量控制:本发明加入了内参基因的监测,可对标本提取和扩增整个过程进行质量监控,能监控dna是否成功提取和pcr过程是否顺利进行,以及监控是否出现人工操作失误(整个过程在闭管状态下进行)。
[0044]
3.操作简单:本方法仅需操作者将人巨细胞病毒核酸检测液和模板进行混合即可上机检测,检测仪器仅依赖于荧光定量pcr仪器,结果ct值仪器可自动判读,对操作人员的要求极其简单,临床可推广性高。
[0045]
说明书附图
[0046]
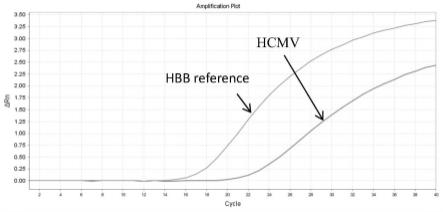
图1为实施例2中阳性对照品的检测结果;
[0047]
图2为实施例2中阴性对照品的检测结果。
具体实施方式
[0048]
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围,实施例中未注明的具体条件,按照常规条件或者制造商建议的条件进行,所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0049]
以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
[0050]
实施例1荧光定量pcr试剂盒的开发
[0051]
根据文献报道,本发明最终选定针对人巨细胞病毒基因区域设计引物探针,在ncbi数据库中选取人巨细胞病毒pp65基因全长进行序列比对,在其保守区域设计引物探针,从而保证一对引物和一条探针能够检测出所有人巨细胞病毒株系,并经过blsat比对,保证该引物探针只能比对到人巨细胞病毒,而不能比对到其他病原菌上。
[0052]
同时,本实例中以人hbb基因作为内参基因,设计特异引物和探针。
[0053]
a)人巨细胞病毒hcmv(pp65基因保守区域)扩增引物、探针如下所示:
[0054]
hcmv核苷酸序列序号正向序列(qf)5
’‑
ccggcaagctctttatgca-3’seq id no.1反向序列(qr)5
’‑
tcatcgtcaggtcctcttcca-3’seq id no.2荧光探针(qp)5
’‑
fam-tcacgctgggctct-3
’‑
mgbnfqseq id no.3
[0055]
b)内参人hbb基因(保守区域)扩增引物、探针如下表所示:
[0056][0057][0058]
荧光定量pcr试剂盒包括:
[0059]
(1)引物探针组:hcmv引物浓度为100nm,探针浓度为100nm;hbb引物浓度为500nm,探针浓度为200nm。
[0060]
(2)一步法扩增反应液:购自南京诺唯赞生物科技有限公司(货号:q222-cn),该反应体系包括taq酶、ung酶、pcr缓冲液、dntps和各种pcr扩增反应液所需离子。
[0061]
(3)阳性对照品(含有人巨细胞病毒靶序列的假病毒、人hbb基因靶序列的工程菌菌株)、
[0062]
(4)阴性对照品(rnase-free ddh2o)。
[0063]
试剂盒保存于-20℃。
[0064]
实施例2人巨细胞病毒核酸荧光定量pcr检测方法
[0065]
本实施例提供一种实施例1中试剂盒的使用方法,即人巨细胞病毒核酸荧光定量pcr检测方法,包括:
[0066]
(1)样本处理:取200μl待测样本,按照常规核酸提取即可得到所需dna。
[0067]
(2)实时荧光定量pcr扩增:
[0068]
a.按表1.配制pcr扩增mix(每个反应25μl):
[0069]
表1.pcr扩增反应体系
[0070][0071]
将配置好的pcr扩增mix按每个反应管25μl进行分装。将已处理待测样本、阳性对照品、阴性对照品各5μl加入相应反应孔,上机进行pcr扩增。
[0072]
b.扩增程序:
[0073][0074]
荧光定量pcr仪参数设定中,以rox作为参比荧光。本发明使用abi 7500进行检测。
[0075]
(3)结果分析:
[0076]
当fam荧光通道中扩增曲线呈s型,且ct≤36时,判断样品为人巨细胞病毒阳性;
[0077]
当fam荧光通道中ct》36或无扩增;vic荧光通道中扩增曲线呈s型,且ct≤35时,判断样品为人巨细胞病毒阴性;
[0078]
当fam荧光通道中ct》36或无扩增,且vic荧光通道中ct》36或无扩增,判定为实验异常,需要重新提取标本检测或重新取样检测。
[0079]
其中,阳性对照品的检测结果如图1所示;阴性对照品的检测结果如图2所示。
[0080]
实施例3 hcmv试剂盒的性能测定
[0081]
一、准确性测定:
[0082]
取9份来自临床的诊断为人巨细胞病毒感染的阳性阴道拭子,作为待测样本,提取
总dna,调整浓度,得到待测样本dna溶液;
[0083]
按照表1配制pcr扩增mix,再加入待测样本dna溶液、阳性对照品、阴性对照品各5μl加入相应反应孔,上机进行pcr扩增。
[0084]
结果如表2所示:
[0085]
表2.临床阳性样本检测结果
[0086][0087]
由表2可知,用该试剂盒对上述9个临床阳性样本进行检测,结果均显示为阳性,阳性符合率为100%,由此说明,该试剂盒的检测准确性高。
[0088]
二、特异性测定:
[0089]
分别取肺炎支原体、解脲支原体、人型支原体、沙眼衣原体等16种病原菌为阴性的临床样本,作为供试样本,采用实施例1中提供的试剂盒按照实施例2中的使用方法,进行荧光pcr检测。
[0090]
结果如表3所示:
[0091]
表3.试剂盒对不同病原菌的检测结果
[0092][0093]
其中,表3中ud表示无ct值或ct》36。
[0094]
由表3的结果可知,通过对多种病原菌进行检测,只有人巨细胞病毒的检测结果为阳性,其他病原菌的检测结果均为阴性,由此说明,该试剂盒对人巨细胞病毒检测的特异性强。
[0095]
三、重复性实验
[0096]
用2份阳性对照进行检测,每个样品重复10次,计算检测结果ct值的变异系数。
[0097]
其中,变异系数(cv,%)的计算公式如下:
[0098][0099]
式中:
[0100]
cv—变异系数;
[0101]
s—ct值的标准差;
[0102]
—ct值的平均值。
[0103]
结果如表4所示:
[0104]
表4.重复性测定结果
[0105][0106][0107]
由表4可知,通过对2份样品分别进行10次重复性测定,检测结果的ct值的变异系数(cv%)≤5%。由此说明,该试剂盒对hcmv检测的重复性好。
[0108]
四、最低检测限
[0109]
使用10份浓度不高于1.0
×
104copies/ml含有人巨细胞病毒靶序列的液体室内质控品,作为自建阳性对照,使用实施例1中提供的试剂盒按照实施例2中的使用方法,进行最低检测限检测。
[0110]
结果如表5所示:
[0111]
表5.检测限测定结果
[0112][0113][0114]
由表5可知,10个样本的检测结果fam信号通道ct值均小于36,均为阳性,该试剂盒对hcmv检测的最低检测限为1.0
×
104copies/ml,由此说明,该试剂盒的检测灵敏度高。
[0115]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。