1.本发明涉及一种农作物的农药技术领域,特别是一种喹诺里西啶生物碱及其制备方法和应用。
背景技术:
2.植物病毒是一类特殊的分子寄生物,不具有细胞结构,一般由核酸和蛋白质组成,需要利用寄主完成自身的复制、移动、包装以及致病等生物学过程。许多重要的作物病害是由植物病毒引起的,植物病毒病素有“植物癌症”之称,导致世界范围内的粮食和经济作物减产和品质下降。
3.番茄斑萎病毒(tomato spotted wilt virus,tswv)属于布尼亚病毒目(bunyavirale),番茄斑萎病毒科(tospoviridae),正番茄斑萎病毒属(orthotospovirus),是负义rna病毒。番茄斑萎病毒是最致命的病毒之一,导致全球损失超过10亿美元,其寄主范围包括15个科1090种的单子叶植物,69个科的双子叶植物和一个科的蕨类植物,感染危害番茄、马铃薯、莴苣、大豆、花生、辣椒、烟草、花卉及观赏植物等多种重要经济作物,tswv的症状主要是可以在寄主叶片、叶茎、果实等出现环状病斑,严重时可导致整个植株坏死、萎焉。因此,世界各国高度重视对于该属病毒的研究,根据科学研究价值和经济重要性,tswv在全球10大危害性植物病毒中位列第二位,位于烟草花叶病毒之后。与此同时,tswv也被列入入侵我国的危险检疫性有害生物名单。
4.现有技术中对tswv的防治主要采用喷施抗植物病毒的化学药剂、种植抗病品种等措施,一些广谱的抗菌药剂一定程度上也可以抑制tswv的感染,但都不能很好地解决tswv的感染问题,而抗病品种也因为资源少且易出现抗性缺失等问题而收效不高。迄今为止,仍没有发现能够彻底根除或有效防治tswv的化学农药或措施。
技术实现要素:
5.本发明的目的在于,提供一种喹诺里西啶类生物碱及其制备方法和用途。本发明从披针叶野决明种子提取到一种新的喹诺里西啶类生物碱,经药效试验证明具有有效防治番茄斑萎病毒和杀虫的特点。
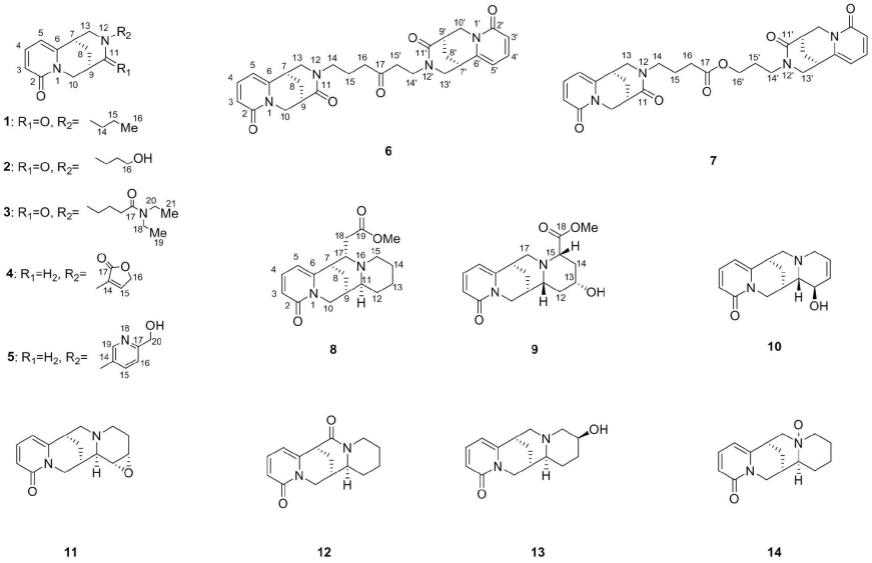
6.本发明的技术方案:一种喹诺里西啶类生物碱,所述喹诺里西啶类生物碱选自以下化学结构的化合物1~化合物14中的任意一种:
[0007][0008]
前述的喹诺里西啶类生物碱中,所述喹诺里西啶类生物碱是从披针叶野决明种子中提取分离获得或通过人工合成获得。
[0009]
上述的喹诺里西啶类生物碱的制备方法,包括以下步骤:
[0010]
(1)取干燥的披针叶野决明种子以甲醇回流提取,合并提取液浓缩得浸膏,浸膏采用酸碱处理得总生物碱;
[0011]
(2)取总生物碱经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为0:100~100:0为流动相进行梯度洗脱,得馏分a、馏分b、馏分c和馏分d;
[0012]
(3)将馏分b经rp-18柱层析,用甲醇:水以体积比为5:95~100:0为流动相进行梯度洗脱,得b-1、b-2、b-3和b-4;
[0013]
(4)将b-3经甲醇凝胶分离,再经半制备hplc纯化,流动相为乙腈-水,体积比为10:90,得化合物3、化合物4、化合物5、化合物6和化合物7;
[0014]
(5)将馏分c经300~400目硅胶柱层析,用石油醚:丙酮:二乙胺以体积比为25:1:0.005~1:1:0.005为流动相进行梯度洗脱,得c-1、c-2、c-3、c-4和c-5;
[0015]
(6)将c-1经甲醇凝胶分离,再经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为50:1~2:1为流动相进行梯度洗脱,得化合物8、化合物9和化合物10;
[0016]
(7)将c-2经甲醇凝胶分离,再经半制备hplc纯化,流动相为乙腈-水,体积比为8:92,得化合物1和化合物2;
[0017]
(8)将c-3经甲醇凝胶分离,再经300~400目硅胶柱层析,用石油醚:丙酮:二乙胺以体积比为10:1:0.005~1:1:0.005为流动相进行梯度洗脱,得化合物13和化合物14;
[0018]
(9)将c-5经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为50:1为流动相进行梯度洗脱,再经半制备hplc纯化,流动相为甲醇-水,体积比为40:60,得化合物11和化合物12。
[0019]
前述的制备方法中,步骤(1)中,所述回流提取为回流提取3次,每次2~3小时。
[0020]
前述的制备方法中,步骤(1)中,所述酸碱处理具体为,先用3%的盐酸溶解,然后
用石油醚萃取除去非生物碱成分,酸水层再用25%的浓氨水调ph为9~10,然后碱水层使用二氯甲烷萃取。
[0021]
前述的制备方法中,步骤(1)中,所述披针叶野决明为豆科野决明属植物。
[0022]
前述的制备方法中,步骤(2)中,所述馏分a是二氯甲烷:甲醇以体积比为20:80洗脱得到,馏分b是二氯甲烷:甲醇以体积比为40:60洗脱得到,馏分c是二氯甲烷:甲醇以体积比为60:40洗脱得到,馏分d是二氯甲烷:甲醇以体积比80:20洗脱得到。
[0023]
前述的制备方法中,步骤(3)中,所述b-1是甲醇:水以体积比为30:70洗脱得到,b-2是甲醇:水以体积比为50:50洗脱得到,b-3是甲醇:水以体积比为70:30洗脱得到,b-4是甲醇:水以体积比为90:10洗脱得到。
[0024]
前述的制备方法中,步骤(5)中,所述c-1是石油醚:丙酮:二乙胺以体积比为20:1:0.005洗脱得到,c-2是石油醚:丙酮:二乙胺以体积比为10:1:0.005洗脱得到,c-3是石油醚:丙酮:二乙胺以体积比为5:1:0.005洗脱得到,c-4是石油醚:丙酮:二乙胺以体积比为2:1:0.005洗脱得到,c-5是石油醚:丙酮:二乙胺以体积比为1:1:0.005洗脱得到。
[0025]
前述的制备方法中,步骤(6)中,化合物8是二氯甲烷:甲醇以体积比为20:1洗脱得到,化合物9是二氯甲烷:甲醇以体积比为10:1洗脱得到,化合物10是二氯甲烷:甲醇以体积比为5:1洗脱得到;步骤(8)中,化合物13是石油醚:丙酮:二乙胺以体积比为5:1:0.005洗脱得到,化合物14是石油醚:丙酮:二乙胺以体积比为2:1:0.005洗脱得。
[0026]
上述方法制备得到的喹诺里西啶类生物碱为无色油状物,化合物1~化合物14的核磁氢谱(1h-nmr)和碳谱(
13
c-nmr)数据如表1~表5所示,其中表1为化合物1~化合物5的氢谱(1h-nmr)数据,表2为化合物6~化合物7的氢谱(1h-nmr)和碳谱(
13
c-nmr)数据,表3为化合物8~化合物14的氢谱(1h-nmr)数据,表4为化合物1~化合物5的碳谱(
13
c-nmr)数据,表5为化合物8~化合物14的碳谱(
13
c-nmr)数据。
[0027]
表1.化合物1~化合物5的1hnmr数据(δin ppm,j in hz)
[0028]
[0029][0030]a600mhz in cdcl3.
[0031]
表2.化合物6和化合物7的1h nmr数据和
13
c nmr(δin ppm,j in hz)
[0032][0033][0034]a600mhz in cdcl3;b800mhz in cdcl3.
[0035]
表3 化合物8~化合物14的1h nmr数据(δin ppm,j in hz)
12
ꢀꢀꢀꢀꢀ
1356.0,ch256.1,ch255.8,ch254.4,ch257.1,ch21448.0,ch242.8,ch245.9,ch2138.7,c146.0,c1519.9,ch229.0,ch221.9,ch2116.8,ch124.9,ch1610.9,ch357.8,ch229.6,ch268.2,ch2120.5,ch17
ꢀꢀ
171.1,c169.1,c150.6,c18
ꢀꢀ
41.9,ch2ꢀꢀ
19
ꢀꢀ
13.1,ch
3 137.6,ch20
ꢀꢀ
40.2,ch
2 63.9,ch221
ꢀꢀ
14.2,ch3ꢀꢀ
[0040]a600mhz in cdcl3.
[0041]
表5.化合物8~化合物14的
13
c nmr
[0042][0043][0044]a600mhz in cdcl3;b800mhz in cdcl3.
[0045]
经过上述结构鉴定,得化合物1~化合物14为:
[0046]
化合物1:无色油状物;[α]25d-30.3(c 0.05,meoh);uv(meoh)λ
max
(logε):310(3.94),260(3.31)nm;ir(kbr)v
max 2963,2359,1681,1203cm-1
;;1h and 13
c nmr数据(cdcl3,600and 150mhz)见表1和表4;hresims m/z 247.14354[m h]
,(计算值c
14h19
n2o2,247.14410)。
[0047]
化合物2:无色油状物;[α]25d-37.6(c 0.05,meoh);uv(meoh)λ
max
(logε):300(3.95),280(3.90)nm;ir(kbr)v
max 3420,2919,2359,1682,1203cm-1
;1h and 13
c nmr数据(cdcl3,800 and 200mhz)见表1和表4;hresims m/z 285.12082[m na]
(计算值
nmr数据(cdcl3,600 and 150mhz)见表3和表5;hresims m/z 259.14371[m h]
(计算值c
15h19
n2o2,259.14410)。
[0058]
化合物13:无色油状物;[α]25d-52.7(c 0.06,meoh,);uv(meoh)λ
max
(logε):220(3.15),230(3.24),255(2.34),310(3.23)nm,ir(kbr)v
max 3366,2919,2851,2359,1733,1645,1541,1456,1384cm-1
;1h and 13
c nmr数据(cdcl3,600 and 150mhz)见表3和表5;hresims m/z 261.15903[m h]
(计算值c
15h21
n2o4,261.15975)。
[0059]
化合物14:无色油状物;[α]25d-104.5(c 0.04,meoh);uv(meoh)λ
max
(logε):305(3.48),265(3.03)nm;ir(kbr)v
max 3421,2918,2359,1683,1648,1550,1204,1127,804cm-1
;1h and 13
c nmr数据(cd3od,600and 150mhz)见表3和表5;hresims m/z 261.15909[m h]
(计算值c
15h21
n2o2,261.15975)。
[0060]
本发明还提供一种药物组合物,包括上述的喹诺里西啶类生物碱或其在农药学上可接受的衍生物或其盐及其农药上可接受的载体。
[0061]
所述的药物组合物为药物制剂。药物制剂包括:粉剂、可湿性粉剂、乳油、颗粒剂、悬浮剂、可溶性液剂、乳粉、水剂、烟剂、种衣剂、微囊剂等。
[0062]
本发明还提供上述的喹诺里西啶类生物碱或上述的药物组合物在制备抗植物病毒农药和杀虫剂中的应用。
[0063]
与现有技术相比:
[0064]
本发明以披针叶野决明种子为原料,采用了一种新的提取分离方式,提取出了新化合物,制备方法简便易操作,新化合物的结构新颖,经鉴定为喹诺里西啶类生物碱。经试验验证,该喹诺里西啶类生物碱对番茄斑萎病毒,在治疗和预防方面均具有较强的抗tswv活性,在杀虫上也起到了较强的作用,效率高。
具体实施方式
[0065]
下面结合实施例对本发明作进一步的说明,但并不作为对本发明限制的依据。
[0066]
实施例:
[0067]
喹诺里西啶类生物碱,所述喹诺里西啶类生物碱选自以下化学结构的化合物1~化合物14中的任意一种:
[0068][0069]
喹诺里西啶类生物碱的制备方法,包括以下步骤:
[0070]
(1)取干燥的披针叶野决明种子50kg以甲醇回流提取3次,每次2~3小时,合并提取液浓缩得浸膏,浸膏采用酸碱处理,即先用3%的盐酸溶解,然后用石油醚萃取除去非生物碱成分,酸水层再用25%的浓氨水调ph为9~10,然后碱水层再使用二氯甲烷萃取,得总生物碱为3.5kg;
[0071]
(2)取总生物碱经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为0:100~100:0为流动相进行梯度洗脱,以体积比为20:80洗脱得馏分a、以体积比为40:60洗脱得馏分b、以体积比为60:40洗脱得馏分c和以体积比80:20洗脱得馏分d;
[0072]
(3)将馏分b经rp-18柱层析,用甲醇:水以体积比为5:95~100:0为流动相进行梯度洗脱,以体积比为30:70洗脱得b-1、以体积比为50:50洗脱得b-2、以体积比为70:30洗脱得b-3和以体积比为90:10洗脱得b-4;
[0073]
(4)将b-3经甲醇凝胶纯化,再经半制备hplc纯化,流动相为乙腈-水,体积比为10:90,得化合物4为14.5mg、化合物5为12.3mg、化合物6为6.7mg、化合物7为32mg和化合物3为17.8mg;
[0074]
(5)将馏分c经300~400目硅胶柱层析,用石油醚:丙酮:二乙胺以体积比为25:1:0.005~1:1:0.005为流动相进行梯度洗脱,以体积比为20:1:0.005洗脱得c-1、以体积比为10:1:0.005洗脱得c-2、以体积比为5:1:0.005洗脱得c-3、以体积比为5:1:0.005洗脱得c-4和以体积比为2:1:0.005洗脱得c-5;
[0075]
(5)将c-1经甲醇凝胶纯化,再经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为50:1~2:1为流动相进行梯度洗脱,以体积比为20:1洗脱得化合物8为25.4mg,以体积比为10:1洗脱得化合物9为33.3mg和以体积比为5:1洗脱得化合物10为28.7mg;
[0076]
(6)将c-2经甲醇凝胶纯化,再经半制备hplc纯化,流动相为乙腈-水,体积比为8:92,得化合物1为28.4mg和化合物2为31.2mg;
[0077]
(7)将c-3经甲醇凝胶纯化,再经300~400目硅胶柱层析,用石油醚:丙酮:二乙胺
以体积比为10:1:0.005~1:1:0.005为流动相进行梯度洗脱,以体积比为5:1:0.005洗脱得化合物13为24.1mg和以体积比为2:1:0.005洗脱得化合物14为18.3mg;
[0078]
(8)将c-5经300~400目硅胶柱层析,用二氯甲烷:甲醇以体积比为50:1为流动相进行梯度洗脱,再半制备hplc纯化,流动相为甲醇-水,体积比为40:60,得化合物11为25.8mg和化合物12为22.3mg;
[0079]
一种药物组合物,包括上述的喹诺里西啶类生物碱或其在农药学上可接受的衍生物或其盐及其农药上可接受的载体。
[0080]
本发明还提供上述的喹诺里西啶类生物碱或者药物组合物在制备抗植物病毒(番茄斑萎病毒)农药和杀虫剂中的应用。
[0081]
实验例1:
[0082]
将实施例得到的喹诺里西啶类生物碱进行抗tswv活性研究验证,具体方法如下:
[0083]
a、寄主为普通烟栽培品种k326(nicotiana tabacum cv.k326),种子由本实验保存提供并栽培于玻璃温室中。番茄斑萎病毒(tswv)毒源由本实验室保存提供。宁南霉素购于黑龙江德强生物股份有限公司。
[0084]
b、接种病毒和施药:
[0085]
先接病毒后施药:选择生长一致的5~6片真叶期的烟苗摩擦接种tswv,tswv接种于第4片和第5片真叶上,10min后用清水冲洗,24h后再分别涂抹1ml浓度为100μg/ml的化合物1~化合物14,涂抹均匀,10min后用清水冲洗;阳性对照2个,一个阳性对照为先摩擦接种tswv,24h后涂抹dmso(用无菌水稀释成100μg/ml),用于计算抑制率;另一个阳性对照为先摩擦接种tswv,24h后涂抹宁南霉素,24h后涂抹dmso作为空白对照。植物生长于无虫温室中。试验重复3次,涂抹3d后统计枯斑数,计算抑制率。
[0086]
抑制率(%)=(阳性对照枯斑数-处理枯斑数)/阳性对照枯斑数
×
100%
[0087]
先施药后接病毒:选择生长一致的5~6片真叶期的烟苗,于第4片和第5片真叶上分别均匀涂抹1ml浓度为100μg/ml的化合物1~化合物14,10min后用清水冲洗,6h后摩擦接种tswv,10min后用清水冲洗。阳性对照2个,一个阳性对照为先涂抹dmso(100μg/ml),6h后接种tswv,用于计算抑制率;另一个阳性对照为先施宁南霉素,6h后接种tswv,只涂抹dmso作为空白对照。烟苗生长于无虫温室中,重复3次,接种病毒3d后统计枯斑数,并计算抑制率。检测结果见表3。
[0088]
表3.化合物1~化合物14的抗tswv活性结果
[0089]
[0090][0091]a三次平均值;b宁南霉素作为阳性对照。
[0092]
体内抗tswv试验表明;化合物9和化合物10(100μg/ml)在先施药后接种病毒的处理中表现出较强的预防作用,其抑制率分别为74.2%和78.5%,高于阳性对照宁南霉素64.5%。化合物6、化合物9和化合物10(100μg/ml)在先接种病毒后施药后的处理中表现出较强的治疗作用,其抑制率分别为75.0%、70.5%和64.0%,高于阳性对照宁南霉素58.9%。
[0093]
实验例2:
[0094]
对实施例的喹诺里西啶类生物碱的杀虫活性进行研究验证,具体如下:
[0095]
供试靶标:蚕豆蚜(aphisfabae)系室内以蚕豆苗饲养多年的敏感品系,试验用虫为3日龄若蚜;稻飞虱(nilaparvata lugens)系室内以水稻苗饲养多年的敏感品系,试验用虫为3龄若虫;棉红蜘蛛(tetranychus urticae)系室内以蚕豆苗饲养多年的敏感品系,试验用虫为健康成螨。
[0096]
培养条件:供试靶标及试验后靶标的培养条件为温度为25
±
5℃,相对湿度为65
±
5%,光照周期为12/12h(l/d)。
[0097]
仪器设备:电子天平(感量万分之一)、喷雾塔、100ml烧杯、玻璃试管、量筒、培养皿、帕拉膜、海绵、滤纸、移液管、镊子、毛笔、显微镜等。
[0098]
试验药剂:实施例中的化合物1~化合物14,含量均以100%计。
[0099]
试验浓度:蚕豆蚜:500mg/l;棉红蜘蛛:500mg/l;稻飞虱:500mg/l。
[0100]
药剂配制:原药:用电子天平称取所需量;溶剂:n,n二甲基甲酰胺(dmf),0.2%;乳化剂:tween 80,0.2%;加入清水稀释到所需浓度。
[0101]
试验方法:
[0102]
参照《农药生物活性评价sop》。
[0103]
蚕豆蚜采用喷雾法:将带有3日龄蚕豆若蚜的蚕豆苗连根拔出,置于装有清水的烧杯中,用parafilm封口膜封住烧杯口,卡上塑料垫片,将试验药剂用电动喉头喷雾器进行喷雾处理,喷雾量2ml/株,每处理4次重复。待植株晾干后,罩上马灯罩,放到恢复室内培养,48h后检查并记载死亡情况,计算死亡率,阳性对照为唑虫酰胺,阴性对照为等量n,n-二甲基甲酰胺和tw-80浓度的溶液(ck)。
[0104]
稻飞虱采用稻茎浸渍法:将试验药剂溶于n,n-二甲基甲酰胺中,用含tw-80(0.2ml/l)的蒸馏水稀释至所需浓度。将15株双叶水稻幼苗浸泡在测试溶液中30秒。将浸过水的稻苗取出,自然晾干,用湿的吸水棉包裹根部,然后放入玻璃试管中(200
×
30mm)。每管感染15
±
5个稻飞虱(stal),3天后测定死亡率。阳性对照为呋虫胺,阴性对照为等量n,n-二甲基甲酰胺和tw-80浓度的溶液(ck)。
[0105]
棉红蜘蛛采用喷雾法:将带有红蜘蛛成虫的两叶一心期蚕豆苗连根拔出,置于装有清水的烧杯中,用parafilm封口膜封住烧杯口,卡上塑料垫片,将试验药剂用电动喉头喷雾器进行喷雾处理,喷雾量为2ml/株,每处理4次重复。待植株晾干后,罩上马灯罩,放到恢复室内培养,72h后检查并记载死亡情况,计算死亡率,阳性对照为螺虫乙酯,阴性对照为等量n,n-二甲基甲酰胺和tw-80浓度的溶液(ck)。
[0106]
调查方法:
[0107]
48或者72h后检查试虫死亡情况,并进行记录,试虫死亡判断标准为:以毛笔轻轻接触试虫无反应计为死亡。记录结果见表4。
[0108]
表4.化合物1~化合物14的对蚕豆蚜、稻飞虱、棉红蜘蛛的毒杀效果
[0109][0110][0111]
以上表4的结果显示,化合物3、化合物4和化合物5在供试浓度下对蚕豆蚜虫表现出较高的灭杀活性;化合物5在供试浓度下对稻飞虱表现出较高的灭杀活性;化合物9和化合物10在供试浓度下对棉红蜘蛛表现出较高的灭杀活性。
[0112]
实验例3:
[0113]
对化合物3、化合物4和化合物5对蚕豆蚜虫的杀虫活性进行进一步评价,具体方法如下:
[0114]
分别设定200mg/l、50mg/l、12.5mg/l、3.125mg/l、0.7813mg/l和0.1953mg/l六个浓度的化合物3、化合物4和化合物5,采用实验例2的方法进行抗蚕豆蚜虫的活性研究。
[0115]
数据统计分析:所有试验数据均采用dps v 7.0统计软件进行分析。根据试验数据
计算死亡率,求出毒力回归方程、相关系数(r)、lc
50
、lc
90
及其95%置信限,结果见表5。
[0116]
表5.lc
50
化合物3、化合物4和化合物5对蚕豆蚜虫的活性测试结果
[0117][0118][0119]
由表5可得,化合物5具有较高的对蚕豆蚜虫的灭杀活性。
[0120]
实验例4:
[0121]
对化合物5对稻飞虱的杀虫活性进行进一步评价,具体方法如下:
[0122]
分别设定200mg/l、50mg/l、12.5mg/l、3.125mg/l、0.7813mg/l和0.1953mg/l六个浓度的化合物5,采用实验例2的方法进行抗稻飞虱活性研究。
[0123]
数据统计分析:所有试验数据均采用dps v 7.0统计软件进行分析。根据试验数据计算死亡率,求出毒力回归方程、相关系数(r)、lc50、lc90及其95%置信限,结果见表6。
[0124]
表6.lc
50
化合物5对稻飞虱的活性测试结果
[0125]
化合物毒力回归方程lc
50
(mg/l)95%置信限相关系数(r)毒效比5y=2.3978 1.6482x37.9128.41-50.590.97050.058呋虫胺y=4.2063 2.3147x2.201.65-2.950.97091
[0126]
由表6可知:化合物5具有较高的对稻飞虱的灭杀活性。
[0127]
实验例5:
[0128]
对化合物9和化合物10对棉红蜘蛛的杀虫活性进行进一步评价,具体方法如下:
[0129]
分别设定200mg/l、50mg/l、12.5mg/l、3.125mg/l、0.7813mg/l和0.1953mg/l六个浓度的化合物9和化合物10,采用实验例2的方法进行抗红蜘蛛活性研究。
[0130]
数据统计分析:所有试验数据均采用dps v 7.0统计软件进行分析。根据试验数据计算死亡率,求出毒力回归方程、相关系数(r)、lc50、lc90及其95%置信限,结果见表7。
[0131]
表7.lc
50
化合物9和化合物10对棉红蜘蛛的活性测试结果
[0132]
化合物毒力回归方程lc
50
(mg/l)95%置信限相关系数(r)毒效比9y=-1.6542 3.6693x65.0935.18-120.430.90450.04210y=1.4621 2.0887x49.4128.15-86.740.90610.055螺虫乙酯y=4.5147 1.1122x2.731.70-4.390.93041
[0133]
由表7可知:化合物10具有较高的对棉红蜘蛛的灭杀活性。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。