1.本发明涉及纳米药物化学和辐射生物医学领域,具体涉及一种肝癌靶向性负载碳硼烷中空介孔二氧化硅的制备及其在肝癌硼中子俘获治疗药物中的应用。
背景技术:
2.肝细胞癌(hcc)是肝组织中最常见的原发性恶性肿瘤之一。临床上,肝癌的主要治疗策略为手术,放疗和化疗。然而,迄今为止,常规疗法对肝癌的治愈率低且疗效较差。因此,寻求新的针对hcc的治疗方法对于hcc患者的治疗具有重要意义。
3.硼中子俘获治疗(bnct)是基于热中子或超热中子照射蓄积于肿瘤部位的稳定性同位素硼-10(
10
b)从而产生具有高传能线密度的α粒子和锂-7(7li)离子进而杀伤癌细胞;由于bnct中产生的α粒子和反冲核的路径大约为一个细胞的直径(5-9μm),同时伴有2.4mev能量,所以通过使用含
10
b药物或递送剂对癌细胞进行靶向摄取后,对肿瘤部位进行热中子照射可实现对肿瘤细胞的选择性损伤,同时周围的正常细胞在治疗中不受影响,从而做到对癌细胞的精准打击。bnct作为一种新的肿瘤靶向二次放射治疗模式给常规疗法无效的恶性肿瘤患者的治疗带来了新希望。目前,低分子量化合物巯基十二硼烷二钠盐(bsh)和(l)-4-二羟基硼基苯丙氨酸(bpa)作为含
10
b药物已在临床上通过bnct用于对恶性脑胶质瘤、头颈癌、恶性黑色素瘤和弥漫性肝癌等恶性肿瘤的治疗。但是,该类含
10
b药物向肿瘤组织递送有效治疗剂量
10
b的能力有限,通过bnct治疗恶性肿瘤的疗效较差。此外,bnct治疗期间,由于发生的中子俘获反应伴随产生高辐射能,因此会在体内产生大量的活性氧簇(ros)从而通过信号传导等方式对正常组织产生氧化损伤以及引起炎症等不良反应。因此,新型高肿瘤靶向性、高安全性的含
10
b药物或递送剂的开发是bnct应用发展的迫切需要。
4.随着纳米技术的不断发展,纳米药物在医学领域的应用引起了人们的广泛关注。其中,中空介孔二氧化硅由于其空腔结构可以有效的封装存储药物,并且其表面易于修饰,可实现肿瘤微环境响应型释放药物、防护药效基团负载以及肿瘤靶向特性。碳硼烷由于其化学性质稳定,体内易清除,含硼量高而被广泛作为含硼基团用于bnct治疗研究。因此,对中空介孔二氧化硅表面进行肝癌靶向基团、肿瘤微环境响应基团和防护药效基团修饰,随后进行碳硼烷负载可得到安全、有效的用于肝癌硼中子俘获治疗的药物。
技术实现要素:
5.本发明的目的在于提供一种肝癌靶向性负载碳硼烷的中空介孔二氧化硅,同时本发明提供该负载碳硼烷中空介孔二氧化硅的制备方法及其在肝癌硼中子俘获治疗药物中的应用。
6.为实现上述目的,本发明所采用的技术方案如下:
7.一种肝癌靶向性负载碳硼烷中空介孔二氧化硅,以表面修饰有乳糖酸/硫辛酸化壳聚糖中空介孔二氧化硅为药物载体,以邻碳硼烷为含硼药物基团。
8.本发明的肝癌靶向性负载碳硼烷中空介孔二氧化硅制备方法,包括以下步骤:
9.(a)中空介孔二氧化硅和3-巯丙基三甲氧基硅烷溶于甲苯溶液中,60℃氮气环境下反应24h,离心收集沉淀,将沉淀溶于甲醇和盐酸的混合溶液中,80℃反应24h,离心、洗涤后,将沉淀分散在含乙酸的乙醇溶液中,加入3-(2-吡啶基二硫)丙酸,室温反应48h,离心、洗涤、真空干燥可得表面羧基化中空介孔二氧化硅;
10.(b)乳糖酸、硫辛酸、n-羟基琥珀酰亚胺及1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐溶于二甲基亚砜溶液中,向该混合溶液中加入壳聚糖乙酸缓冲溶液,室温反应24h,调节溶液ph至9.0,离心收集沉淀,沉淀溶于甲醇,使用阳离子交换树脂调节溶液ph至中性,乙醚沉淀,沉淀物进行透析、冻干可得中间产物乳糖酸/硫辛酸化壳聚糖;
11.(c)表面羧基化中空介孔二氧化硅、乳糖酸/硫辛酸化壳聚糖、n-羟基琥珀酰亚胺及1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐溶于n,n-二甲基甲酰胺与乙酸混合溶液中,室温反应24h,离心、洗涤、真空干燥可得表面经乳糖酸/硫辛酸化壳聚糖修饰的中空介孔二氧化硅;
12.(d)邻碳硼烷与表面修饰有乳糖酸/硫辛酸化壳聚糖的中空介孔二氧化硅溶于乙酸缓冲液中,室温搅拌24h后,使用0.2m氢氧化钠溶液调节ph值至7.4,离心、洗涤、真空干燥可得终产物肝癌靶向性负载碳硼烷中空介孔二氧化硅。
13.上述步骤(a)中中空介孔二氧化硅、3-巯丙基三甲氧基硅烷和3-(2-吡啶基二硫)丙酸的质量比优选为5:15:3。
14.上述步骤(a)中甲醇和盐酸的体积比为50:3。
15.上述步骤(a)中乙醇和乙酸的体积比为30:1。
16.上述步骤(b)中乳糖酸、硫辛酸、n-羟基琥珀酰亚胺、1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐和壳聚糖的反应摩尔之比优选为1:1:4:6:20。
17.上述步骤(c)中羧基化中空介孔二氧化硅、乳糖酸/硫辛酸化壳聚糖、n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐的质量比优选为4:15:20:20。
18.上述步骤(c)中n,n-二甲基甲酰胺和乙酸溶液的体积比为3:1。
19.上述步骤(d)中邻碳硼烷和表面修饰有乳糖酸/硫辛酸化壳聚糖的中空介孔二氧化硅的质量比优选为1:2。
20.本发明还提供了所述的肝癌靶向性负载碳硼烷中空介孔二氧化硅在硼中子俘获治疗药物中的应用。
21.优选地,所述应用包括可作为含硼递送剂将碳硼烷高选择性的递送至肝癌细胞内。
22.优选地,所述应用包括在bnct期间可引起肝癌细胞的细胞周期阻滞在g2/m期。
23.优选地,所述应用包括在bnct期间可诱导肝癌细胞凋亡。
24.优选地,所述应用包括在bnct期间可发挥抗氧化损伤作用。
25.优选地,所述应用包括在bnct期间可产生抗炎作用。
26.本发明的有益效果为:
27.本发明提供了一种肝癌靶向性负载碳硼烷中空介孔二氧化硅(lbhmsi)的制备方法,肝癌靶向性负载碳硼烷中空介孔二氧化硅具有良好的生物相容性和低毒性,在药物输送领域具有重要的应用前景。生物活性测定结果表明,lbhmsi对肝癌细胞(huh-7)具有高选
择性摄取,在硼中子俘获治疗中对肝癌细胞具有较强杀伤作用,同时能够在硼中子俘获治疗中协同发挥抗氧化损伤和抗炎作用,降低放疗的副作用,具有良好的应用前景。
附图说明
28.图1为本发明lbhmsi纳米颗粒透射电镜tem示意图。
29.图2为本发明lbhmsi的粒径分布示意图。
30.图3为本发明lbhmsi和对照组的细胞摄取结果;图a为人正常肝细胞(lx-2)摄取,图b为人肝癌细胞(huh-7)摄取。
31.图4为本发明lbhmsi和对照组的细胞毒性测试结果;图a为lx-2细胞毒性检测,图b为huh-7细胞毒性检测。
32.图5为本发明lbhmsi和对照组在bnct期间对huh-7细胞的抗氧化作用检测结果;图a为细胞内超氧化物歧化酶(sod)活性检测,图b为细胞内丙二醛(mda)活性检测。
33.图6为本发明lbhmsi和对照组在bnct期间对huh-7细胞的抗炎作用检测结果;图a为细胞中il-12含量测定,图b为细胞中il-1β含量测定,图c为细胞中il-10含量测定。
具体实施方式
34.下面通过实施例对本发明的技术方案进行说明,但是本发明的技术方案并不限于以下实施例。
35.实施例1:肝癌靶向性负载碳硼烷中空介孔二氧化硅的制备,具体包括以下步骤:
36.(a)中空介孔二氧化硅和3-巯丙基三甲氧基硅烷按质量比1:3溶于甲苯溶液中,60℃氮气环境下反应,生成表面巯基修饰的中空介孔二氧化硅,将其溶于甲醇和盐酸的混合溶液中,其中甲醇与盐酸的体积比为50:3,加热至80℃反应24h,离心收集沉淀,水洗后真空干燥,将干燥后产物分散在含1ml乙酸的30ml乙醇溶液中,按中空介孔二氧化硅和3-(2-吡啶基二硫)丙酸质量比为5:3的比例加入3-(2-吡啶基二硫)丙酸,室温反应48h,离心收集沉淀,分别用乙醇和水洗涤沉淀,沉淀真空干燥可得表面羧基化中空介孔二氧化硅;
37.(b)乳糖酸、硫辛酸、n-羟基琥珀酰亚胺及1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐按反应摩尔比1:1:4:6溶于二甲基亚砜溶液中,随后加入20倍量壳聚糖乙酸缓冲溶液,室温反应24h,调节溶液ph至碱性(ph=9.0),离心收集沉淀,沉淀溶于甲醇,使用阳离子交换树脂调节溶液ph至中性,乙醚沉淀,沉淀物进行透析,冻干可得中间产物乳糖酸/硫辛酸化壳聚糖;
38.(c)表面羧基化中空介孔二氧化硅、乳糖酸/硫辛酸化壳聚糖、n-羟基琥珀酰亚胺及1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐按质量比4:15:20:20溶于n,n-二甲基甲酰胺与乙酸混合溶液中,其中n,n-二甲基甲酰胺与乙酸溶液的体积比为3:1,离心收集沉淀,沉淀分别使用蒸馏水和乙醇洗涤,真空干燥可得表面经乳糖酸/硫辛酸化壳聚糖修饰的中空介孔二氧化硅;
39.(d)邻碳硼烷与表面修饰有乳糖酸/硫辛酸化壳聚糖的中空介孔二氧化硅溶于乙酸缓冲液中,其中邻碳硼烷与乳糖酸/硫辛酸化壳聚糖中空介孔二氧化硅的质量比为1:2,使用0.2m氢氧化钠溶液调节溶液ph值至7.4,离心收集沉淀,用ph 7.4的pbs洗涤沉淀,真空干燥可得终产物肝癌靶向性负载碳硼烷中空介孔二氧化硅。
40.如图1所示,本发明制备的肝癌靶向性负载碳硼烷中空介孔二氧化硅具有轮廓分明的中空结构和孔壳;如图2所示,肝癌靶向性负载碳硼烷中空介孔二氧化硅的平均粒径为138nm。
41.实施例2:肝癌靶向性负载碳硼烷中空介孔二氧化硅在细胞内的摄取检测
42.将处于对数生长期,细胞含量为80-85%的人正常肝细胞(lx-2)和人肝癌细胞(huh-7)分别接种到6孔板中(每孔1
×
106个细胞)。待细胞贴壁后,用浓度分别为2、5或10μg
10
b/ml的对照组(bsh)或lbhmsi分别作用于细胞24h(每组设置4个平行实验)。作用完毕,弃去培养液,用pbs洗涤细胞3次;随后每孔加入1ml浓度为2mg/ml的链霉蛋白酶溶液并于4℃下孵育4h,用来除去细胞表面结合的化合物。弃去含链霉蛋白酶溶液,pbs洗涤细胞3次,用ripa裂解液裂解细胞,收集细胞裂解液,10000rpm离心收集上清液。通过icp-ms检测上清液中的
10
b浓度。细胞内摄取结果如图3所示,结果表明lbhmsi在lx-2和huh-7细胞中的摄取均为浓度依赖性。相同给药浓度下,lbhmsi在huh-7细胞中的摄取量高于lx-2细胞中;在huh-7细胞中,lbhmsi的摄取量高于对照组bsh可在肝癌细胞中大量摄取,符合bnct治疗中对含硼递送剂高肿瘤选择性的要求。
43.实施例3:细胞毒性检测
44.将lx-2和huh-7细胞分别接种到96孔板中(每孔1
×
105个细胞),细胞贴壁后,弃去培养液,每孔加入不同浓度的bsh或lbhmsi(2,5或10μg
10
b/ml,每组设置4个平行实验,并设置空白对照组)作用细胞24h。按10μl/孔加入cell counting kit-8溶液并孵育2.5h。孵育结束,使用酶标仪测量每孔在450nm处的吸光度并计算细胞活性。如图4所示,bsh和lbhmsi在给药浓度下对lx-2和huh-7的细胞毒性较小;低毒性是bnct应用中含硼药物或者递送剂需满足重要条件,因此lbhmsi具有成为应用于bnct的含硼递送剂的潜力。
45.实施例4:细胞周期测定
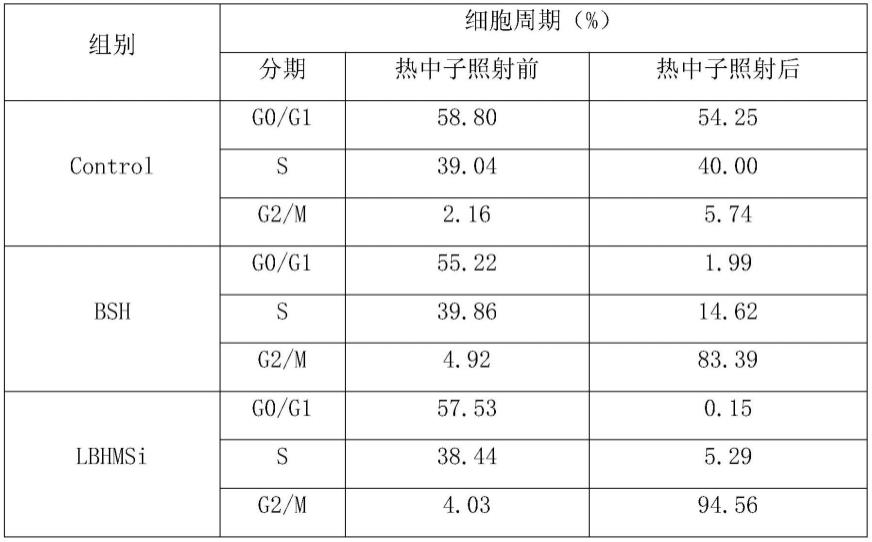
46.收集经待测样品作用并辐照过热中子的huh-7细胞。离心弃去上清,细胞沉淀使用70%预冷乙醇固定2小时,pbs洗涤3次,向洗涤后的细胞沉淀中加入rnase溶液,37℃水浴30min,加入pi染液,4℃避光孵育30min,随后使用流式细胞仪分析测定细胞周期。如表1所示,bsh和lbhmsi作用后的huh-7细胞在bnct治疗中细胞周期被阻滞在g2/m期。
47.表1细胞周期测定结果
[0048][0049]
实施例5:细胞凋亡测定
[0050]
收集经待测样品作用并辐照过热中子的huh-7细胞。离心弃去上清,细胞沉淀使用pbs洗涤3次,向洗涤后的细胞悬液中加入annexin v-fitc/pi染液室温避光染色15min,随后使用流式细胞仪分析测定凋亡细胞群的百分比。
[0051]
表2细胞凋亡测定结果
[0052][0053]
由表2可知,本发明所提供的肝癌靶向性负载碳硼烷中空介孔二氧化硅在bnct中可有效诱导肝癌(huh-7)细胞发生凋亡。
[0054]
实施例6:抗氧化损伤作用检测
[0055]
收集经待测样品作用并辐照过热中子的huh-7细胞到离心管内,离心后弃上清,加入细胞提取液,超声波破碎细胞,8000g 4℃离心10min,取上清,按商品超氧化物歧化酶(sod)活性检测试剂盒和丙二醛(mda)含量检测试剂盒的标准步骤利用分光光度计分别测定和计算各组huh-7细胞内sod和mda的表达。测定结果如图5所示,bsh作用后的huh-7细胞在bnct期间细胞内活性氧水平明显上升;相反,lbhmsi作用后的huh-7细胞在bnct期间细胞内活性氧表达水平较低,表明lbhmsi在bnct治疗肝癌期间可有效降低活性氧水平,减小bnct治疗副作用。
[0056]
实施例7:抗炎作用检测
[0057]
在酶标包被板的孔中加入样品稀释液40μl,随后向每孔加入10μl待测样品。向每
孔(空白组除外)加入酶标试剂100μl,封板后37℃温育1h。孵育结束,弃去液体,每孔洗涤5次。随后,向每孔加入显色剂a和b各50μl,37℃条件下避光显色20min。显色结束,每孔加入50μl终止液,使用酶标仪检测每孔450nm处的吸光度,根据标准曲线计算相应细胞因子(促炎细胞因子il-12和il-1β,抗炎细胞因子il-10)含量。如图6所示,bsh作用后的huh-7细胞在bnct期间细胞内炎症水平明显上升;不同的是,lbhmsi作用后的huh-7细胞在bnct期间细胞内炎症水平较低。因此,lbhmsi在bnct治疗肝癌期间可有效发挥抗炎作用,降低bnct治疗中伴随产生的炎症反应。
[0058]
综合以上实验结果,本发明提供的肝癌靶向性负载碳硼烷中空介孔二氧化硅对肝癌细胞具有较强的选择性富集能力,同时表现出良好的生物相容性和低毒性,在硼中子俘获治疗中对肝癌细胞具有较强的细胞周期阻滞、诱导凋亡和杀伤作用,同时能够在硼中子俘获治疗中协同发挥抗氧化损伤和抗炎作用,降低放疗的副作用,具有良好的bnct治疗应用前景。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。