bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途
技术领域
1.本发明涉及生物医学技术领域,特别涉及bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途。
背景技术:
2.膀胱癌是泌尿生殖系统中常见恶性肿瘤之一。在我国,随着老龄化形势的严峻、工业防护不足、烟草消耗量增加等因素膀胱癌发病率和病死率逐年上升。膀胱癌疾病负担极重,非肌层浸润性膀胱癌患者术后需常规行膀胱镜检查,检查频次依据风险分级来定。肌层浸润性膀胱癌患者切除膀胱术后行尿流改道术,患者生活质量严重降低。因此,寻找膀胱癌高效的靶点对膀胱癌精准治疗具有重要意义。
3.因此,临床急需寻找用于抑制膀胱癌细胞的药物。
技术实现要素:
4.本发明目的是提供bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途,本发明通过研究,发现上调bms1p4能抑制膀胱癌细胞5637和j82糖酵解能力,并能降低糖酵解相关蛋白的表达,促进膀胱癌细胞5637和j82凋亡。表明linrodostat为治疗膀胱癌提供新的治疗方案。
5.为实现所述目的,本发明采用如下技术方案:
6.在本发明的第一方面,提供了bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途。
7.进一步地,所述用途选自以下一种或多种:
8.(a)上调bms1p4的表达能抑制膀胱癌细胞的糖酵解能力;
9.(b)上调bms1p4的表达能降低糖酵解相关蛋白的表达,所述糖酵解相关蛋白包括glut1、hif-1a、hk2中的一种;
10.(c)上调bms1p4的表达能促进膀胱癌细胞的凋亡。
11.进一步地,所述上调bms1p4表达的方式包括加入过表达质粒。
12.进一步地,所述过表达质粒的制备方法包括:
13.将seq id no.2-seq id no.3所示的引物对核苷酸序列如seq id no.1所示的目的基因进行pcr,获得基因片段;
14.将载体fv115进行ecori/xbai双酶切后与所述基因片段连接,后转化,获得过表达质粒。
15.本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
16.本发明提供bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途,本发明通过研究,发现上调bms1p4能抑制膀胱癌细胞5637和j82糖酵解能力,并能降低糖酵解相关蛋白的表达,促进膀胱癌细胞5637和j82凋亡。表明bms1p4基因可用于制备抑制膀胱癌细胞的药物,本发明为治疗膀胱癌提供新的治疗方案。
附图说明
17.为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。
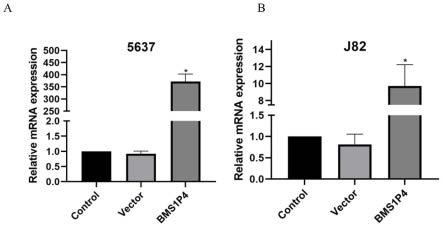
18.图1为过表达bms1p4效果;其中,图1a为膀胱癌细胞5637中分别加入空白对照组、载体组、过表达bms1p4组的bms1p4表达量;图1b为膀胱癌细胞j82中分别加入空白对照组、载体组、过表达bms1p4组的bms1p4表达量。
19.图2为过表达bms1p4促进膀胱癌细胞5637和j82凋亡的结果;其中,图2a为5637细胞对照组,图2b为5637细胞过表达组,图2c为j82细胞对照组,图2d为j82细胞过表达组;图2e为e凋亡统计结果。
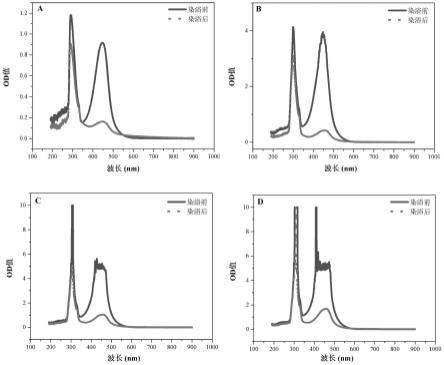
20.图3为过表达bms1p4抑制膀胱癌细胞5637和j82糖代谢能力的结果;其中,图3a为5637细胞外酸化率,图3b为j82细胞外酸化率,图3c为基础糖酵解水平,图3d为糖酵解峰值;
21.图4为过表达bms1p4抑制膀胱癌细胞糖酵解相关蛋白glut1、hif-1a、hk2的表达的结果;
22.图5为载体fv115的质粒图谱。
具体实施方式
23.下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
24.在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
25.除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买获得或者可通过现有方法获得。
26.下面将结合实施例及实验数据对本技术的bms1p4基因在制备用于抑制膀胱癌细胞的药物中的用途进行详细说明。
27.实施例1、过表达质粒的构建与转染
28.1、过表达质粒的构建
29.(1)目的基因(序列)信息
30.基因名称:bms1p4 bms1 pseudogene 4[homo sapiens(human)]
[0031]
gene id:729096
[0032]
转录本信息:nr_026592.2
[0033]
基因大小:1960bp
[0034]
基因序列:如seq id no.1所示;
[0035]
(2)载体信息
[0036]
载体编号:fv115
[0037]
载体大小:10kb
[0038]
原核抗性:amp
[0039]
筛选标记:zsgreen/puromycin
[0040]
框架结构:cmv-mcs-3flag-ubi-zsgreen-ires-puromycin
[0041]
多克隆位点(mcs)区正向测序引物:5'-cgcaaatgggcggtaggcgtg-3'
[0042]
mcs区反向测序引物:5'-agtcccgtcctaaaatgtc-3'
[0043]
常用酶切位点:ecori、xhai、noti
[0044]
载体图谱如图5所述。
[0045]
(3)目的基因(片段)获取
[0046]
化学合成法获取目的基因序列:如seq id no.1所示;
[0047]
(4)pcr扩增
[0048]
pcr体系配制:(以q5 dna polymerase为例)
[0049]
表1
[0050][0051]
其中,表1中primer-f、primer-r的引物序列为:
[0052]
primer-f:5
’‑
accagcagatgttactttacgg-3’(seq id no.2);
[0053]
primer-r:5
’‑
gtggagtgggtggagatga-3’(seq id no.3);
[0054]
所述pcr反应条件为:
[0055]
表2
[0056][0057]
克隆载体制备
[0058]
载体酶切(以ecori和xbai为例)
[0059]
酶切体系配制:
[0060]
表3
[0061][0062]
(说明:一般酶切反应条件37℃/30min,具体条件可根据使用的酶种类做调整)
[0063]
琼脂糖凝胶dna回收:
[0064]
根据样品数,配制相应孔数的1%琼脂糖凝胶;将完成酶切反应的体系加至上样孔中进行电泳,电泳条件220v/30min;电泳结束后将胶块放置在切胶台上,切下目的片段放入已灭菌1.5mlep管中;按照tiangen普通琼脂糖凝胶dna回收试剂盒说明书进行dna回收操作;将回收的dna测定其浓度及260/280值,储存于-20℃备用。
[0065]
(5)载体和目的片段连接
[0066]
1t4连接法:
[0067]
按摩尔比配制连接体系:目的片段:载体=3:1;
[0068]
表4
[0069][0070]
无缝克隆连接法
[0071]
计算使用量:目的基因回收产物大小(bp)x0.04(ng)
[0072]
线性化载体大小(bp)
×
0.02(ng)(根据具体的产物浓度换算成使用体积)
[0073]
表5
[0074][0075]
(6)连接产物转化及涂板
[0076]
150μl top10感受态放冰上融化,取5μl连接产物和感受态细胞混匀;冰浴30min,42℃水浴热击90sec,冰浴2min;转化产物转移到含500μl无抗性lb液体培养基的ep管中,置于摇床中,37℃,250rpm培养30min;将含有转化菌的ep管,1000g离心1min;在超净台中倒去上清,留下约100ul培养基将沉淀混匀,均匀涂于lb抗性培养平板上;将平板倒扣置于37℃细菌培养箱培养过夜(12~16h)。
[0077]
(7)单克隆培养与鉴定
[0078]
从上述平板中挑取单克隆菌落于6ml lb液体培养基中,37℃,250转/分,培养过夜(12~16h);质粒提取(按照tiangen质粒提取试剂盒说明书操作);质粒测序鉴定,将测序结果与目的基因序列进行比对鉴定。鉴定结果为正确的质粒,进行后续慢病毒包装实验。
[0079]
2、将所述过表达质粒加入到培养的膀胱癌细胞5637和j82中
[0080]
moi摸索:根据实验需要对膀胱癌细胞5637和j82铺48孔板,与细胞传代方法相同,将细胞根据实验需要进行稀释,每孔1
×
104个细胞,均匀的铺到细胞培养板中,做好标记,放置培养箱中培养,待细胞完全贴壁后进行实验。病毒浓度为1
×
108iu/ml,设置不同的浓度梯度,
[0081]
过表达:moi值分别为0,5,10,25,50,75,100,每孔病毒分别加入0,0.5μl,1μl,2.5μl,5μl,7.5μl,10μl,并加入聚凝胺助转,聚凝胺浓度为10μg/ml,72h后在荧光显微镜下观察荧光强度。
[0082]
根据细胞荧光强度过表达及空载moi选择为:
[0083]
5637细胞:50;j82细胞:50。
[0084]
细胞稳筛:按照病毒感染浓度摸索选出的moi感染细胞,72h后加入5μg/ml的含嘌呤霉素培养基筛选细胞,最初加入后会在药物的作用下将大部分未成功感染病毒的细胞杀死,每隔2~3天换液,已去除死细胞并维持药物浓度,直至细胞90%以上含绿色荧光,且细胞可以稳定增殖,换用1ug/ml的含嘌呤霉素培养基培养维持细胞稳转特性。细胞状态良好,干扰和过表达验证通过pcr进行验证。
[0085]
过表达bms1p4的结果如图1所示,表明膀胱癌细胞5637和j82过表达bms1p4成功。
[0086]
实施例2、上调bms1p4促进膀胱癌细胞5637和j82凋亡
[0087]
将实施例1转染后的细胞悬液做如下检测:
[0088]
1、荧光定量pcr:收集细胞及处理组织样本,trizon使样本充分裂解,提取rna进行浓度、纯度测定,将rna通过逆转录hifiscript cdna第一链合成试剂盒合成cdna,以cdna为模板,在荧光定量pcr仪上进行检测,以β-actin为内参,计算出各组组织/细胞bms1p4的表达的相对表达水平。
[0089]
用于检测bms1p4时使用的引物序列如下:
[0090]
bms1p4 f:5
’‑
accagcagatgttactttacgg-3’(seq id no.2);
[0091]
bms1p4 r:5
’‑
gtggagtgggtggagatga-3’(seq id no.3)。
[0092]
用于检测β-actin(内参)的引物如下:
[0093]
β-actin f:5
’‑
tggcacccagcacaatgaa-3’(seq id no.4);
[0094]
β-actin r:5
’‑
ctaagtcatagtccgcctagaagca-3’(seq id no.5)。
[0095]
本发明提供检测bms1p4表达水平的引物,通过qrt-pcr可定量检测所述假基因在组织和细胞中的表达水平。
[0096]
如图1可知,过表达bms1p4显著增加膀胱癌细胞5637和j82的bms1p4水平。
[0097]
3、流式检测凋亡:收集1
×
10
6-3
×
106个细胞,加1ml pbs 1500rpm离心3min,洗两遍。用双蒸水将5
×
binding buffer稀释为1
×
binding buffer。取500ul预冷的1
×
binding buffer重悬细胞。每管各加入5μl annexin v-apc和10μl 7-aad。轻微混匀后,室温避光孵育10min。上流式仪检测。
[0098]
流式结果如图2所示,表明过表达bms1p4促进膀胱癌细胞凋亡。
[0099]
实施例3、过表达bms1p4抑制膀胱癌细胞糖代谢能力
[0100]
将实施例1转染后的细胞悬液做如下检测:
[0101]
ecar检测:根据分组取100μl 105/ml的单细胞悬浮液37℃孵育至贴壁,再补充150ml生长培养基(注意保持生长时间恒定,过程中不能拍或者摇动板子);测试换液:吸掉175ul原生长培养基,利用600ul海马专用测试培养基润洗两次,最后加450ul至525ul,在显微镜下观察每孔内细胞的连续性,之后将它放置non-co2培养箱孵育1h;在每孔的四道加药槽中根据实验设计加药75ul,各种呼吸链抑制剂保存浓度及使用浓度:葡萄糖(glucose,10mm);寡霉素(oligomycin,1μm);2-dg使用浓度10mm。仪器方法编辑及校准板校准;校准板换上细胞板运行。
[0102]
结果如图3所示,表明过表达bms1p4抑制膀胱癌细胞糖代谢能力。
[0103]
实施例4、过表达bms1p4抑制膀胱癌细胞糖酵解相关蛋白表达
[0104]
将实施例1转染后的细胞悬液做如下检测:
[0105]
提取过表达bms1p4膀胱癌5637和j82细胞,弃掉培养皿中的细胞培养液,每孔加入100μl的细胞裂解液,将细胞消化下来,冰上裂解30min。4℃,12000rpm高速离心机离心15min,收集上清。根据bca试剂盒测定蛋白浓度,蛋白变性,上样进行十二烷基苯磺酸钠凝胶电泳(sds-page)1.5h,后用300ma恒流转膜1.5h。用pvdf膜孵育一抗,4℃过夜,次日pvdf膜室温孵育二抗2h,洗膜,用发光液浸湿pvdf膜后放置于超高灵敏度化学发光成像系统样品放置区运行程序显影成像。
[0106]
结果如图4所示,表明过表达bms1p4抑制膀胱癌细胞糖酵解相关蛋白glut1、hif-1a、hk2的表达。
[0107]
最后,还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
[0108]
尽管已描述了本发明的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。
[0109]
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。