1.本发明涉及一种基于微流控芯片的核酸检测方法及系统。
背景技术:
2.目前,在核酸检测过程中,采集的核酸样本至少需要先后经过如下步骤:裂解提取核酸,与核酸扩增试剂(如酶等)、引物混合进行扩增。其中的一种较为方便的检测方式为在一个微流控芯片内完成上述全部的步骤,但需要在芯片内额外设置较多的腔室,以用于存放裂解及中和液等核酸提取试剂,或提供核酸样本和这些试剂混合反应的空间;此外,还需要在芯片上设置活塞、阀门等来控制样本和试剂的混合、流动等。这都使得微流控芯片的结构较为复杂,而且与其配套的核酸分析仪也需对应设置用于驱动这些活塞、阀门的驱动机构,使得整个检测系统较为复杂,设备成本较高。而传统的手动测试方法需要多次移液,难以准确定量移液或需要使用昂贵的移液枪,且污染风险较高。
技术实现要素:
3.针对上述技术问题,本发明提供一种基于微流控芯片的核酸检测方法,其保证检测准确性的同时减小设备成本。
4.本发明还提供一种基于微流控芯片的核酸检测系统,其避免使用结构复杂的核酸分析仪及移液枪,同时保证检测准确性,减小设备成本。
5.一种基于微流控芯片的核酸检测方法,包括如下步骤:(1)将样本放入样本采集管内,所述样本采集管内预先存放有核酸裂解液,使所述样本和所述核酸裂解液混匀反应,得到裂解产物混合液;(2)将定量移液装置插入所述样本采集管内并定量吸取所述裂解产物混合液,所述定量移液装置的移液腔中预先存放有固体形式的核酸扩增试剂,在移液的过程中使所述裂解产物混合液和所述核酸扩增试剂混匀;(3)所述定量移液装置将其移液腔中的液体定量加入微流控芯片内,所述微流控芯片具有一或多个预先存放有环介导等温扩增引物的反应仓,在加样的过程中,液体进入所述反应仓中和所述环介导等温扩增引物混合;(4)将所述微流控芯片装入lamp检测仪中,进行环介导等温扩增和荧光分析检测。
6.该核酸检测方法不是用于免疫诊断治疗目的。
7.优选地,步骤(2)中的所述核酸扩增试剂以冻干球形式存放在所述移液腔中。
8.更优选地,所述冻干球包括扩增用酶、三磷酸脱氧核苷酸和缓冲液。具体地,所述冻干球包括datp、dttp、dctp、dgtp、甜菜碱、tris-hcl、kcl、mgso4、(nh4)2so4、tritonx-100、bst dna聚合酶及冻干保护剂。当裂解产物混合液进入移液腔中后和冻干球接触,使其复溶,裂解出的核酸分子和这些扩增用酶、三磷酸脱氧核苷酸和缓冲液混合。在移液的过程中即实现核酸分子和扩增试剂的混合,减少了移液次数,减小了多次移液导致的人为操作误差。
9.优选地,所述样本通过口腔拭子或咽拭子采集,所述核酸裂解液包括生理盐水,所述核酸检测方法的检测对象为呼吸道病毒。
10.优选地,所述定量移液装置包括筒体、可相对所述筒体上下移动的活塞杆、连接于所述活塞杆上的活塞、及与所述活塞杆连接或一体设置的定位件,所述筒体包括内筒及套于所述内筒外的外筒,所述移液腔形成于所述内筒中,所述活塞可上下移动地设置于所述移液腔中,且所述活塞和所述内筒的内壁之间密封,所述定位件可上下移动地插设于所述内筒和所述外筒之间,所述定位件上具有第一限位部,所述外筒上具有与所述第一限位部相配合的第二限位部,所述定位件具有第三限位部;步骤(2)中,所述定量移液装置在插入所述样本采集管之前处于初始状态,此时所述第三限位部抵在所述外筒的上端面上;插入后,向上拉所述活塞杆,将所述裂解产物混合液吸至所述移液腔中,和所述核酸扩增试剂混合;直至所述第一限位部抵在所述外筒上的第二限位部后,吸液停止;步骤(3)中,向下推所述活塞杆,将所述移液腔中混匀后的液体推入所述微流控芯片内,直至所述第三限位部抵在所述外筒和/或内筒的上端面,加样停止。
11.该定量移液装置能够以简单的结构实现定量吸液,避免了使用昂贵且复杂的专用精密移液枪。
12.更优选地,所述内筒的下端形成有和所述移液腔连通的移液口,在所述初始状态时所述活塞和所述移液口之间具有一段距离,所述核酸扩增试剂位于所述活塞和所述移液口之间。
13.更优选地,所述内筒的外径小于所述样本采集管的外径,所述内筒的下端开设有通孔作为移液口,步骤(2)中,所述内筒插入所述样本采集管中,使所述移液口浸入所述样本采集管内的裂解产物混合液中。内筒能够直接插入样本采集管中,不需要额外配置吸头等部件。
14.更优选地,步骤(3)中,所述定量移液装置的移液口插入所述微流控芯片的加样口中,通过所述活塞的推力驱使所述液体自所述加样口进入所述反应仓内,加样完成后,将所述微流控芯片的密封折耳折弯后盖在所述加样口上。不需要在微流控芯片上配置控制液流的阀门、活塞等;相应地,lamp检测仪中也不要对应配置驱动机构,lamp检测仪中只要配置基本的加热机构和荧光检测机构即可。
15.更优选地,所述加样口和所述反应仓之间通过微通道直接连通,所述微通道具有一或多个弯折部。
16.本发明还采用如下技术方案:一种基于微流控芯片的核酸检测系统,包括:样本采集管,其中预先存放有核酸裂解液;定量移液装置,其具有预先存放有固体形式的核酸扩增试剂的移液腔;微流控芯片,其具有一或多个预先存放有环介导等温扩增引物的反应仓。
17.优选地,所述定量移液装置包括筒体、可相对所述筒体上下移动的活塞杆、连接于所述活塞杆上的活塞、及与所述活塞杆连接或一体设置的定位件,所述筒体包括内筒及套于所述内筒外的外筒,所述移液腔形成于所述内筒中,所述内筒的外径小于所述样本采集管的外径,所述内筒的下端开设有通孔作为移液口,所述活塞可上下移动地设置于所述移
液腔中,且所述活塞和所述内筒的内壁之间密封,所述定位件可上下移动地插设于所述内筒和所述外筒之间,所述定位件上具有第一限位部,所述外筒上具有与所述第一限位部相配合的第二限位部;所述定量移液装置具有初始状态和最大容积状态,在所述初始状态时所述第一限位部位于所述第二限位部的下方,所述活塞和所述移液口之间具有一段距离,所述核酸扩增试剂位于所述活塞和所述移液口之间;在所述最大容积状态时所述第一限位部和所述第二限位部抵紧接触。
18.优选地,所述定位件具有第三限位部,在所述初始状态时所述第三限位部抵在所述外筒的上端面上;在所述最大容积状态时所述第三限位部位于所述外筒的上端面的上方。
19.优选地,所述微流控芯片包括芯片本体和芯片壳,所述芯片本体上设有加样口和多个排气口,所述芯片本体内设有一或多个反应仓,所述反应仓分别通过一个第一微通道连通所述加样口,各所述第一微通道分别具有一或多个弯折部,每个所述反应仓还分别通过一个第二微通道连通与一相对应的所述排气口连通,所述芯片壳包括壳主体和密封折耳,所述芯片本体装于所述壳主体内,所述微流控芯片具有检测状态和初始状态,在所述检测状态时所述密封折耳和所述壳主体相互连接并盖在所述加样口和/或所述排气口上;在所述初始状态时所述密封折耳脱离所述加样口和所述排气口。
20.本发明采用以上方案,相比现有技术具有如下优点:本发明的基于微流控芯片的核酸检测方法及系统,自采样至荧光分析检测的整个过程中,只需要依次移液,即通过定量移液装置从样本采集管移至微流控芯片中,在样本采集管中进行核酸裂解提取,在移液的过程中和扩增试剂混合,加到微流控芯片中后即和反应仓内的引物混合,通过lamp检测仪进行加热即可进行环介导等温扩增以及实时荧光定量分析,减少了移液次数避免了多次移液引入操作误差,保证了检测结果的准确性,操作方便;同时,避免使用结构复杂的微流控芯片,进而简化了相配套的lamp检测仪的结构,降低了设备成本。
附图说明
21.为了更清楚地说明本发明的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
22.图1为根据本发明实施例的核酸检测方法的流程示意图;图2为根据本发明实施例的定量移液装置的立体示意图;图3为根据本发明实施例的定量移液装置先微流控芯片加样时的示意图;图4为图3的剖视图;图5为根据本发明实施例的定量移液装置在初始状态的剖视图;图6为根据本发明实施例的定量移液装置在最大容积状态的剖视图;图7为根据本发明实施例的微流控芯片的正面示意图,其中折耳覆于芯片本体上;图8为根据本发明实施例的微流控芯片的背面示意图,其中折耳覆于芯片本体上;图9为芯片本体的示意图;图10为芯片背面的示意图;
图11为微流控芯片在初始时的正面示意图;图12为微流控芯片在初始时的正面示意图,其中覆膜未示出;图13为微流控芯片在初始时的背面示意图。
23.其中,100、样本采集管;101、核酸裂解液;200、定量移液装置;1、筒体;11、移液腔;111、台阶面;12、第二限位部;13、内筒;131、引导斜面;14、外筒;141、缺口;16、移液口;17、移液管部;2、活塞杆;3、活塞;4、定位件;41、第一限位部;42、第三限位部;5、装配间隙;6、核酸扩增试剂冻干球;60、液体;300、微流控芯片;70、芯片本体;701、加样口;702、溢流槽;703、排气口;704、反应仓;705、第一微通道;705a、第一弧形弯折部;705b、第二弧形弯折部;706、第二微通道;707、凹槽;709、第二凹槽;71、覆膜;73、密封膜;74、芯片壳;741、壳主体;741a、第一凸耳;741b、第二凸耳;742、密封折耳;742a、第一凹槽;743、折叠线;75、密封垫;400、lamp检测仪。
具体实施方式
24.下面结合附图对本发明的较佳实施例进行详细阐述,以使本发明的优点和特征能更易于被本领域的技术人员理解。在此需要说明的是,对于这些实施方式的说明用于帮助理解本发明,但并不构成对本发明的限定。
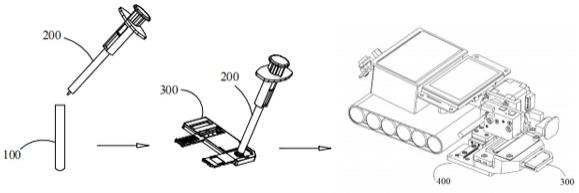
25.本实施例提供一种基于微流控芯片的核酸检测方法,该核酸检测方法采用本实施例的核酸检测系统。参照图1所示,该核酸检测系统包括样本采集管100、定量移液装置200及微流控芯片300。样本采集管100中预先存放有核酸裂解液;具体到本实施例中,检测对象为呼吸道病毒,核酸裂解液包括生理盐水,样本和生理盐水混合后即可将其中的呼吸道病毒的核酸释放出。定量移液装置200具有预先存放有固体形式的核酸扩增试剂的移液腔11,具体参见图2至图6所示。微流控芯片300具有一或多个预先存放有环介导等温扩增引物的反应仓704,具体参见图7至13所示。
26.如图1所示,该非免疫诊断治疗目的的核酸检测方法具体包括如下步骤:(1)将样本放入样本采集管100内,使样本和样本采集管100内的核酸裂解液混匀反应,得到裂解产物混合液;(2)将定量移液装置200插入样本采集管100内并定量吸取裂解产物混合液,定量移液装置200的移液腔11中预先存放有固体形式的核酸扩增试剂,在移液的过程中使裂解产物混合液和核酸扩增试剂混匀;(3)定量移液装置200将其移液腔中的液体定量加入微流控芯片300内,微流控芯片300具有一或多个预先存放有环介导等温扩增引物的反应仓704,在加样的过程中,液体进入反应仓704中和环介导等温扩增引物混合;(4)将微流控芯片300装入lamp检测仪400中,进行环介导等温扩增和荧光分析检测。
27.步骤(1)中,样本通过口腔拭子或咽拭子采集得到,将拭子浸入样本采集管100内的核酸裂解液中,将样本中的核酸分子裂解出,形成裂解产物混合液。
28.步骤(2)中,核酸扩增试剂以冻干球形式存放在移液腔中。冻干球包括扩增用酶、
三磷酸脱氧核苷酸和缓冲液。具体地,冻干球包括datp、dttp、dctp、dgtp、甜菜碱、tris-hcl、kcl、mgso4、(nh4)2so4、tritonx-100、bst dna聚合酶及冻干保护剂。当裂解产物混合液进入移液腔中后和冻干球接触,使其复溶,裂解出的核酸分子和这些扩增用酶、三磷酸脱氧核苷酸和缓冲液混合。
29.参照图2至图6所示,定量移液装置200包括具有移液腔11的筒体1、可相对筒体1上下移动的活塞杆2及连接于活塞杆2上的活塞3,活塞3可上下移动地设置于移液腔11中,活塞3和筒体1的内壁之间密封。进一步地,筒体1包括内筒13及套于内筒13外的外筒14,移液腔11形成于内筒13中。活塞3由柔性材料制成,其和筒体1的内壁紧密配合,并能够在筒体1内上下移动。该移液装置还包括定位件4,定位件4可上下移动地插设于内筒13和外筒14之间。定位件4和活塞杆2连接或一体设置。定位件4上具有第一限位部41,筒体1上具有与第一限位部41相配合的第二限位部12。更具体地说,第一限位部41为形成于定位件4下部的凸耳,第二限位部12为形成于外筒14上的面向下方的表面。外筒14具有沿上下方向延伸的缺口141,凸耳可上下移动地位于缺口141内。
30.参照图5和图6所示,该移液装置具有初始状态和最大容积状态。在初始状态时,第一限位部41位于第二限位部12的下方;在最大容积状态时,第一限位部41和第二限位部12抵紧接触。也就是说,该移液装置可以定量地吸取或放出液体,使用方便且提高了工作效率。
31.进一步地,内筒13的上端低于外筒14的上端,内筒13的上端和外筒14的内壁之间具有供定位件4插入的装配间隙5,内筒13、外筒14及凸耳中的至少一个部件上设有便于定位件4插入装配间隙5的引导斜面131。具体结合到本实施例中,内筒13上具有引导斜面131,通过该引导斜面131,定位件4可以较为方便地插入装配间隙5中。
32.进一步地,定位件4具有第三限位部42,在初始状态时第三限位部42抵在外筒14的上端面上;在最大容积状态时第三限位部42位于外筒14的上端面的上方。在排液时,将活塞杆2向下推到底,直至第三限位部42抵在外筒14的上端面上,从而实现定量排液。
33.该定量移液装置200还包括设置于移液腔11中的多个核酸扩增试剂冻干球6。筒体1的下端形成有和移液腔11连通的移液口16,该移液口16具体为开设在内筒13下端的通孔。在初始状态时活塞3和移液口16之间具有一段距离,且在初始状态时多个核酸扩增试剂冻干球6位于活塞3和移液口16之间。具体地,在初始状态时,通过在定位件4上设置第三限位部42,其抵在外筒14的上端面,而阻止活塞杆2进一步下移,确保活塞3下方有一定空间,可以容置核酸扩增试剂冻干球6。
34.参照图3和图4所示,当该移液装置在采样管中吸取液体后,需要将液体释放到微流控芯片300中的加样口101中。筒体1的下端部具有外径较小的移液管部17,移液口16形成于移液管部17内,移液腔11具有台阶面111,移液管部17自台阶面111向下延伸,核酸扩增试剂冻干球6置于台阶面111上。换句话说,移液管部17的外径较小,不仅方便在采样管中吸取液体,而且也可以更好地插入加样口101中。
35.步骤(2)中,定量移液装置200在插入样本采集管100之前处于初始状态,此时第三限位部42抵在外筒14的上端面上;插入后,向上拉活塞杆2,将裂解产物混合液吸至移液腔11中,和核酸扩增试剂混合;直至第一限位部41抵在外筒14上的第二限位部12后,此时活塞杆不能继续上移,吸液停止,实现定量吸液。
36.步骤(3)中,向下推活塞杆2,将移液腔11中混匀后的液体60推入微流控芯片300内,直至第三限位部42抵在外筒和/或内筒的上端面,此时加样停止,实现定量加样。
37.该定量移液装置200能够以简单的结构实现定量吸液,避免了使用昂贵且复杂的专用精密移液枪。
38.内筒13的外径小于样本采集管100的外径,内筒13的下端开设有通孔作为移液口16,步骤(2)中,内筒13的下部插入样本采集管100中,使移液口16浸入样本采集管100内的裂解产物混合液中。内筒13能够直接插入样本采集管100中,不需要额外配置吸头等中间部件。
39.参照图7至图13所示,微流控芯片300包括芯片本体70,芯片本体70上设有一个加样口701、多个反应仓704和多个排气口703。每个反应仓704分别通过一个第一微通道705连通加样口701,各第一微通道705分别具有一或多个弯折部。每个反应仓704还分别通过一个第二微通道706连通与一相对应的排气口703连通。该微流控芯片300为一种小型化的微流控芯片300,其无需配置任何控制液流的活塞或阀门,体积小巧,适于用于手持式lamp检测仪中。其中,每个反应仓704的第一微通道705都在一处或多处弯折从而形成有一或多个弯折部,不需要设置阀门或活塞的情况下也能够有效防止反应仓704内的引物倒流出第一微通道705,避免对其他反应仓704造成污染。反应仓704中预先设置有针对呼吸道病毒的引物,不同反应仓704中的引物可以相同,也可以不同,以检测不同的病原体。
40.上述的弯折部包括整体呈弧形的弧形弯折部,弧形弯折部所呈弧形的圆心角大于90度,优选为170至190度。进一步地,弧形弯折部包括第一弧形弯折部705a和第二弧形弯折部705b,第一弧形弯折部705a的圆心位于其右侧,第二弧形弯折部705b的圆心位于其左侧。第一弧形弯折部705a和第二弧形弯折部705b的圆心角均为180度。如图11所示,第一弧形弯折部705a和第二弧形弯折部705b交错设置,相邻的第一弧形弯折部705a和第二弧形弯折部705b直接相接或通过直线形通道相接,即,每个第一微通道705分别具有呈波浪形的部分,有效防止反应仓704内的引物倒流。
41.微流控芯片300还包括设于芯片本体70的表面上并覆盖排气口703的允许气体通过而不允许液体通过的覆膜71。芯片本体70的背面上还开设有环绕加样口701设置的溢流槽702,避免加样时污染芯片本体70的背面。微流控芯片300还包括用于将反应仓704、第一微通道705和第二微通道706封闭的密封膜73,密封膜73覆设于芯片本体70的正面上。
42.该微流控芯片300还包括芯片壳74,芯片本体70的四周边缘上分别设有与芯片壳74相互配合的卡接定位机构。芯片壳74包括壳主体741和密封折耳742,芯片本体70装于壳主体741内。该微流控芯片300具有检测状态和初始状态,在检测状态时密封折耳742和壳主体741相互连接并盖在加样口701和/或排气口703上;在初始状态时密封折耳742脱离加样口701和排气口703。也就是说,本实施例中加样口701和排气口703是通过密封折耳742封闭。进一步地,如图7所示,该微流控芯片300还包括密封垫75,在检测状态时密封折耳742将密封垫75压紧在加样口701和/或排气口703上。密封垫75设在密封折耳742上,如通过胶黏剂粘贴在密封折耳742上。本实施例中,芯片壳74包括两个密封折耳742,一个密封折耳742用于将加样口701封闭,另一个密封折耳742用于将覆膜71下的排气口703封闭。
43.壳主体741具有第一连接部,密封折耳742具有第二连接部,在检测状态时第一连接部和第二连接部相连接,在初始状态时第一连接部和第二连接部相互脱离。具体地,第一
连接部包括第一凸耳741a,在检测状态时第二连接部卡于第一凸耳741a和芯片本体70之间。第二连接部上进一步具有用于容纳第一凸耳741a的第一凹槽742a。
44.密封折耳742能够相对壳主体741转动地和壳主体741连接。在加样完成后,将密封折耳742翻转并压在芯片本体70上。进一步地,密封折耳742通过一能够变形的薄弱部连接于壳主体741。具体到本实施例中,薄弱部为沿芯片本体70的长边方向延伸的折叠线743。密封折耳742和壳主体741通过一体注塑形成,折叠线743在注塑后即形成,其厚度小于周围部分的厚度,从而能够易于被折叠。
45.芯片本体70嵌入壳主体741内,壳主体741的四周设有第二凸耳741b,上述的卡接定位机构具体是指设于芯片本体70上的与第二凸耳741b相配合的第二凹槽709,第二凸耳741b位于第二凹槽709内。
46.如图11至13所示,初始时,芯片本体70的正面覆有密封膜73,芯片本体70的背面的排气口703处覆有覆膜71,芯片本体70嵌入芯片壳74内,芯片壳74的密封折耳742伸至壳主体741外,位于芯片本体70的旁侧。
47.步骤(3)中,自加样口701加入定量移液装置200中的液体60,直至该液体60流至覆膜71处将覆膜71封闭,甚至多加的液体溢出至溢流槽702中;将密封折耳742沿折叠线743翻转至芯片本体70的背面上,并将其边缘部分压入第一凸耳741a之下直至第一凸耳741a卡在第一凹槽742a内,使用较为方便且密封垫75被密封折耳742压紧在加样口701和覆膜71上,使微流控芯片300内形成一个与外界空气隔绝的密闭环境。该过程中,步骤(3)中,定量移液装置200的移液口插入微流控芯片300的加样口中,通过活塞的推力即可驱使液体自加样口进入反应仓内,不需要其他外力驱动。
48.步骤(4)中,将该微流控芯片300插入lamp检测仪4中,在引物和含有待测核酸内的液体在芯片内的密闭环境中进行恒温扩增和荧光检测。该lamp检测仪4中配置用于加热的加热机构及用于收集荧光的荧光检测机构,无需配置液流控制及驱动机构,因而结构简单,设备成本较低。
49.采用本实施例的测试方法对咽拭子上的样本进行甲流病毒检测,从采样至检测结果出来共耗时25~40min,而所得的ct至与常规的测试方法的ct值相当。
50.上述实施例只为说明本发明的技术构思及特点,是一种优选的实施例,其目的在于熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限定本发明的保护范围。凡根据本发明的原理所作的等效变换或修饰,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
