tim-3抗体、制备方法及其应用
技术领域
1.本发明属于细胞免疫学、分子生物学领域,涉及tim-3抗体、制备方法及其应用。
背景技术:
2.tim-3属于t细胞免疫球蛋白及黏蛋白结构域(t cell immunoglobulin domainand mucin domain containing molecules family,tim)家族成员,最初发现于克隆哮喘小鼠模型中,小鼠tim家族包括8个成员,人体中3个成员(tim1、tim3和tim4)定位于人类染色体5q33.2,其中tim-3包含301个氨基酸,在免疫调节中起重要作用,主要表达在活化的cd4 t细胞、已分化的th1细胞和cd8 t细胞表面,在th17细胞、treg细胞、nk细胞和其他淋巴细胞亚群也发现了它的表达。tim-3是一种负性调节分子,通过影响免疫细胞活性对免疫系统进行调节。主要表现为在急性感染、超敏反应和自身免疫中对机体起保护作用。因此,阻断tim-3的作用通路则有利于恢复机体免疫平衡,缓解疾病。
3.但遗憾的是目前国内外没有任何一个通过注册的可用于临床体外诊断(in vitro diagnostics,ivd)用的tim-3抗体。本发明研制出一种特异性高、表现稳定且效价高的抗tim-3蛋白的单克隆抗体,可用于tim-3蛋白的检测。主要用于对包括脓毒症、系统性红斑狼疮或相关感染和自身免疫性疾病的辅助诊断和治疗方案选择。
技术实现要素:
4.本发明提供了一种抗tim-3的单克隆抗体或其抗原结合片段,所述抗体或其抗原结合片段包括重链可变区的互补性决定区域cdr1、cdr2、cdr3以及轻链可变区的互补性决定区域cdr1、cdr2、cdr3;重链cdr1、cdr2、cdr3的氨基酸序列分别如seq id no:1、seq id no:2、seq id no:3所示,或者分别与seq id no:1、seq id no:2、seq id no:3所示的序列至少具有80%同源性;轻链cdr1、cdr2、cdr3的氨基酸序列分别如seq id no:5、seq id no:6、seq id no:7所示,或者分别与seq id no:5、seq id no:6、seq id no:7所示的序列至少具有80%同源性。
5.优选地,重链cdr1具有seq id no:1所示的氨基酸序列;重链cdr3具有seq id no:2所示的氨基酸序列;重链cdr3具有seq id no:3所示的氨基酸序列;轻链cdr1具有seq id no:5所示的氨基酸序列;轻链cdr2具有seq id no:6所示的氨基酸序列;轻链cdr3具有seq id no:7所示的氨基酸序列。
6.进一步,所述单克隆抗体的重链可变区具有seq idno:4所示的氨基酸序列或与其具有至少80%同源性的氨基酸序列,所述单克隆抗体的轻链可变区具有seq id no:8所示的氨基酸序列或与其具有至少80%同源性的氨基酸序列。
7.优选地,所述单克隆抗体的重链可变区具有seq idno:4所示的氨基酸序列;所述单克隆抗体的轻链可变区具有seq id no:8所示的氨基酸序列。
8.包括优选抗体氨基酸序列的保守序列变体的抗体也包括在本发明的范围之内。保守氨基酸序列变体包括不显著改变本发明的单克隆中和抗体结合性质和中和性质的氨基
酸序列的修饰,如源于本领域熟知的相似氨基酸替代的变体,氨基酸的缺失、增加导致的变体。
9.本发明的抗体还包括人源与非人源抗体,以及具有与本发明的单克隆抗体相同功能或改造及优化的一切抗体。
10.进一步,所述抗体的抗原结合片段包括fab、fab
′
、f(ab
′
)2、fv或单链fv。
11.本发明还提供了一种分离的核酸分子,所述核酸分子编码前面所述的抗tim-3的单克隆抗体或其抗原结合片段。
12.本发明的编码前面所述的单克隆抗体或其抗原结合片段的核酸分子包括具有上述核苷酸序列的保守核苷酸序列变体的核酸分子。所谓的保守核苷酸序列变体源于遗传密码简并和沉默的变体,核苷酸的替代、缺失和增加也包含在内。
13.本发明还提供了一种前面所述的核酸分子的dna片段。所述dna片段可以编码抗体重链或轻链可变区的任何区域,包括重链cdr1、cdr2、或cdr3,或轻链cdr1、cdr2、或cdr3。
14.本发明还提供了一种包括前面所述的核酸分子的表达载体,除了前面所述的核酸分子之外,表达载体还包括与所述核酸分子序列操作性相连的表达调控序列。
15.表达载体是指可将编码某蛋白的多聚核苷酸插入其中并使蛋白获得表达的一种核酸运载工具。载体可通过转化、转导或转染宿主细胞,使其携带的遗传物质元件在宿主细胞内得以表达。载体的种类包括本领域熟知的细菌质粒、噬菌体、酵母质粒、植物细胞病毒、哺乳动物细胞病毒如腺病毒、逆转录病毒或其他载体。总之,只要能在宿主体内复制和稳定,任何质粒和载体都可以用。在表达载体中,除了含有复制起点外,还可含有标记基因和其他翻译控制元件。
16.本发明还提供了一种含有前面所述的核酸分子或前面所述的表达载体的宿主细胞。
17.宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。代表性例子有:大肠杆菌,链霉菌属;鼠伤寒沙门氏菌的细菌细胞:真菌细胞如酵母;植物细胞;果蝇s2或sf9的昆虫细胞;cho,cos,293细胞、或bowes黑素瘤细胞的动物细胞等。
18.在本发明的具体实施方案中,所述宿主细胞是哺乳动物细胞,更优选cho细胞。
19.用重组dna转化、转染宿主细胞可用本领域技术人员熟知的常规技术进行。
20.本发明提供了一种药物组合物,所述药物组合物包括治疗有效量的本发明的抗体或其抗原结合片段。
21.所述药物组合物还包括药学上可接受的载体,所述载体包括但不限于已经被美国食品与药品管理局认可的而可用于人类或动物的任何佐剂、载体、赋形剂、助流剂、稀释剂、表面活性剂、润湿剂、分散剂、助悬剂、稳定剂、等渗压剂、溶剂或乳化剂等对组成药物组合物无副作用的各种形式的载体。
22.本发明还提供了一种包括本发明的抗tim-3的单克隆抗体或其抗原结合片段的检测产品。
23.所述检测产品包括但不限于检测试剂、试剂盒、芯片或试纸。凡是包括前面所述的抗tim-3的单克隆抗体或其抗原结合片段能够检测出tim-3的检测产品均包括在本发明的范围之内。
24.本发明还提供了一种非诊断目的的检测tim-3水平的方法,其特征在于,所述方法包括如下步骤:
25.(1)提取含有tim-3的样品;
26.(2)将步骤(1)获取的样品与前面所述的单克隆抗体或其抗原结合片段的接触;
27.(3)检测样品与单克隆抗体或其抗原结合片段的免疫反应。
28.本发明提供了一种应用,所述应用包括以下任一项:
29.1)前面所述的单克隆抗体或其抗原结合片段在制备tim-3蛋白检测产品中的应用;
30.2)前面所述的单克隆抗体或其抗原结合片段在制备抑制tim-3蛋白活性的药物中的应用;
31.3)前面所述的单克隆抗体或其抗原结合片段在制备阻断tim-3与tim-3的配体结合的药物中的应用;
32.4)前面所述的单克隆抗体或其抗原结合片段在制备促进t细胞中ifn-γ表达的药物中的应用;
33.5)前面所述的单克隆抗体或其抗原结合片段在制备调节免疫系统的药物中的应用;
34.6)前面所述的单克隆抗体或其抗原结合片段在制备治疗与tim-3异常表达相关的疾病的药物中的应用;优选地,所述疾病包括脓毒症、感染性疾病、自身免疫性疾病。
35.本发明的公开的抗体可以在重链和轻链可变区包含一个或多个糖基化位点,如本领域内熟知的,在可变区中存在的一个或多个糖基化位点可以导致增强的抗体免疫原性,或者由于改变了抗原结合而改变抗体的药物动力学。
36.本发明的抗体可以被设计为在fc区域内包含修改,通常是改变抗体的1个或多个功能特性,如血清半衰期、补体结合、fc受体结合、和/或抗原依赖的细胞毒性。此外,本发明的抗体可以被化学修饰(如,可以将一个或多个化学基团连接于抗体),或被修饰以改变其糖基化,从而再改变抗体的一个或多个功能特性。
37.本发明的单克隆抗体或其抗原结合片段可以以化学方法或者通过基因工程与其他因子缀合。这些因子提供将抗体靶向所需功能位点的作用或者为抗体提高或提供其他性能。
38.根据本发明的的抗体可以以化学方法或者通过基因工程标记,以提供可检测的抗体,可检测的抗体包括可检测部分。可检测的部分包括但不限于酶、辅基、荧光材料、发光材料,生物发光材料、放射性材料、正电子发射金属以及非放射性顺磁性金属离子。
39.为了检测和/或分析和/或诊断目的标记依赖于使用的特定检测/分析/诊断技术和/或方法例如免疫组织化学染色(组织)样品、流式细胞计量术、激光扫描细胞计量术检测、荧光免疫测定、酶联免疫吸附测定(elisa)、放射免疫测定(ria)、生物测定(例如吞噬作用测定)、蛋白质印迹应用等。对于本领域已知的检测/分析/诊断技术和/或方法合适的标记为本领域技术人员所熟知。
40.本文所用的术语“单克隆抗体”指从一类基本均一的群体获得的抗体,除少数可能存在的天然发生的突变外,该群体中包含的单个抗体是相同的。修饰语“单克隆”仅表示抗体的特性,是从基本均一的抗体群中获得的,这不能解释成需要用任何特殊方法来生产抗
体。
41.本文所用的术语“可变”表示抗体中可变区的某些部分在序列上有所不同,它形成了各种特定抗体对其特定抗原的结合和特异性。可变性集中于轻链和重链可变区中称为互补决定区(cdr)或超变区中的三个片段中。天然重链和轻链的可变区中各自包含四个fr区(可变区中较保守的部分),它们大致上呈β-折叠构型,由形成连接环的三个cdr相连,可形成部分β折叠结构。每条链中的cdr通过fr区紧密地靠在一起并与另一链的cdr一起形成了抗体的抗原结合部位。恒定区不直接参与抗体与抗原的结合,但是它们表现出不同的效应功能,例如参与抗体的依赖于抗体的细胞毒性。
附图说明
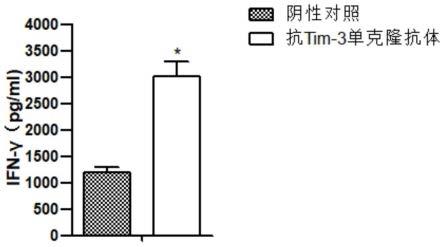
42.图1为本发明的单克隆抗体调节t细胞分泌ifn-γ的能力的结果图。
具体实施方式
43.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。
44.下列实施例中未注明具体条件的实验方法,通常按照常规条件如sambrook等人,分子克隆:实验室手册(new york:coldspring harbor laboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
45.下列实施例中未注明来源的实验试剂,均可从商业途径获得。
46.实施例1抗tim-3单克隆抗体制备
47.使用重组人tim-3蛋白(百奥莱博,jn0532)免疫balb/c小鼠,首次免疫后,每隔14天做加强免疫,共免疫4次,取小鼠血清进行抗体效价评价。评价有效的小鼠取b细胞,提取rna反转录,构建噬菌体展示库。将浓度为4μg/ml的重组人tim-3蛋白包板,加入展示的噬菌体,进行噬菌体库筛选,筛选后的未被洗掉的噬菌体收集后感染宿主菌,获得第一轮筛选文库,按照此法进行二轮和三轮筛选。筛选完成后,进行phage-elisa鉴定,鉴定阳性的送测序获得抗tim-3单克隆抗体的序列。
48.抗tim-3单克隆抗体的序列如下所示:
49.重链可变区的序列:
50.evklvesggglvqpggslrlscatsgftfsdyymswvrqppgkalewlgfirnkangytteysasvkgrftiyrdnsqsilylqmntlraedsatyycvrdsw(seq id no.4)
51.轻链可变区序列:
52.elvmtqtpsslavsagekvtmsckssqslfnsrtrknflawyqqrpgqspklliywastresgvpdrftgsgsgtdftltissvqtedlavyyckqsyilwtf(seq id no.8)
53.将以上单克隆抗体轻链可变区编码序列,轻链恒定区基因装入pcdna3.1质粒,得含单克隆抗体轻链基因的载体;将获得的单克隆抗体重链可变区基因,重链恒定区基因装入pcdna3.1质粒,获得含单克隆抗体重链基因的载体。将含有单克隆抗轻链基因的载体、重链基因的载体共转染转入哺乳动物细胞freestyle293f中进行表达。培养120h后收集细胞培养物,使用抗体亲和介质和akta层析系统纯化培养上清中的单克隆抗体。
54.实施例2抗tim-3单克隆抗体亲和力检测
55.1)将抗tim-3单克隆抗体注入传感芯片(10μl/min,50s),蛋白捕获为45-100ru。然后将重组人tim-3蛋白蛋白分别以200、100、50、25、12.5、6.25、3.125、1.5625或0.78125nm的浓度注入传感芯片(30μl/min,100-400s),解离时间为300-1000s。用ph2.0的甘氨酸(30μl/min,10-30s)再生芯片后读取检测结果。动力结合速率和动力解离速率可通过bioacore t200测评软件进行1:1朗缪尔结合模型拟合获得。亲和力速率常数kd=动力解离速率/动力结合速率,结果显示,本发明制备的抗tim-3单克隆抗体的kd为3.27
×
10-10
m。
56.2)将免疫酶标板以2μg/ml的重组人tim-3蛋白包被,4℃孵育过夜。次日将孔板清洗,并进一步使用5%的脱脂牛奶在室温封闭1小时。将不同浓度稀释的抗tim-3单克隆抗体加入酶标板,室温孵育1小时。使用pbs清洗后,加入hrp偶联的anti-human igg抗体,室温孵育1小时。再次洗净后,加入tmb底物显色,加入10%硫酸后,检测在450nm波长处的吸光度。elisa实验显示本发明制备的抗tim-3单克隆抗体的ec50为0.042586μg/ml。
57.3)实验设对照组1、对照组2、阳性对照组。其中对照组1包被无关抗原tnf-α;对照组2包被bsa;实验组包被重组人tim-3蛋白。包被过夜后清洗,封闭2h,之后加入抗tim-3单克隆抗体,37℃反应1h,pbst清洗后加入二抗孵育。1h后加入tmb,室温避光孵育10min后,加入50μl/孔的1mol/l的硫酸终止反应,酶标仪检测450nm处od值。检测结果如下:对照组1的od
450nm
值为0.147,对照组2的od
450nm
值为0.169,阳性对照组的od
450nm
值为1.843。上述结果表明本发明制得的单克隆抗体对人tim-3蛋白结合具有特异性。
58.实施例3抗tim-3单克隆抗体中和活性检测
59.1、pbmc分离
60.1)抽取人的外周血于肝素抗凝管中,取足5ml新鲜血液,加入pbs按1:1稀释血液。
61.2)取淋巴细胞分离液5ml于15ml灭菌离心管中待用。
62.3)吸取稀释血液,在离分层液上方1cm处,沿试管壁徐徐加入,使稀释血液重叠于分层液上,并与分离液形成明显界面。
63.4)室温,离心2000rpm,20min。此时离心管中形成5层:最上面是血浆,血浆层和淋巴细胞分离液之间是淋巴细胞层呈白膜状。
64.5)小心吸取中间呈白膜状的单个核细胞层,尽量全部吸出单个核细胞。加5倍以上体积的pbs洗2次,每次离心1500rpm,10min。
65.6)去上清液,加入培养基1ml混匀,取少量进行细胞计数。
66.7)用台盼蓝染液检查所分离的细胞活性:取2滴细胞悬液加1滴2%台盼蓝染液,5-10min后取样作湿片高倍镜检。活细胞不着色,死细胞染成蓝色。计数200个细胞,计算活细胞百分率,活性在95%以上。
67.2、富集cd14 单核细胞
68.按照人单核细胞分选试剂盒(美国美天旎公司,cat#130-117-337)的说明书富集cd14 单核细胞。
69.3、诱导mo-dc
70.用rpmi完全培养基将cd14 单核细胞按照每孔106/500μl的密度接种至48孔细胞培养板中,并按照10ng/ml的浓度加入细胞因子il-4及gm-csf,隔天补加100μl rpmi完全培养基及细胞因子,培养至第5天,将细胞吹起,瞬时离心,计数,用于后续实验。
71.4、磁珠分选cd4 t细胞
72.使用mojosort
tm human cd4 t cell isolation kit(biolegend,cat#480009)按照试剂盒操作说明书进行cd4 t细胞分选。
73.5、将cd4 t细胞和mo-dc细胞按照5:1比例混合接种至96孔细胞培养板中,加入本发明的单克隆抗体或igg阴性对照。培养箱培养96h后,轻轻吸取上清,稀释后利用elisa试剂盒(biolegend,cat#430104)检测450nm处的吸光度值计算出上清中ifn-γ的含量。
74.6、结果
75.结果如图1所示,以人igg作为阴性对照组,抗tim-3抗体可显著增强cd4 t细胞分泌ifn-γ的能力。
76.以上仅是本发明的优选实施方式,应当指出的是,上述优选实施方式不应视为对本发明的限制,本发明的保护范围应当以权利要求所限定的范围为准。对于本技术领域的普通技术人员来说,在不脱离本发明的精神和范围内,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
