植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途
技术领域
1.本发明涉及发酵乳制品领域,特别是涉及植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途。
背景技术:
2.自闭症(也称孤独症)谱系障碍(autism spectrum disorder,asd)是一种以沟通障碍及社会交往障碍、兴趣狭窄及重复刻板动作等为主要特征的严重神经发育障碍性疾病。据报道,asd的患病率在全球范围内持续增加,男性儿童发病率是女性儿童发病率的4-5倍。asd目前被认为是遗传因素和环境风险因素相互作用后的结果,产前或产后接触化学品和药物、空气污染、压力、宫腔感染和饮食因素等都会增加asd的发病风险。然而遗憾的是,asd目前尚无可治愈的药物或手段,这给社会和家庭都带来了沉重的负担。
3.在asd的多种合并症中,不同程度的胃肠道功能障碍和肠道微生物组改变是最常被报道的。asd儿童患胃肠道疾病的可能性是正常儿童的3.5倍,包括慢性便秘、腹痛、腹泻、胃食管反流以及胃肠道炎症和肠神经系统异常等。他们也更容易出现烦躁、焦虑、社交退缩等问题,而在改善了胃肠道症状后,asd患者病情的严重程度也有所减轻。许多研究发现肠道菌群紊乱与asd的发生有一定的相关性,共生微生物通过其代谢产物、免疫功能、神经内分泌调节以及迷走神经等途径影响人类和小鼠的大脑神经发育,从而影响多种复杂的行为症状,包括社交、情感和焦虑样行为。有临床研究表明粪菌移植可以有助于自闭症行为的改善。现阶段对自闭症的干预研究也主要集中在如何缓解自闭症相关症状上。一些研究发现,一种或多种特定益生菌的干预可能可以改善asd小鼠肠道屏障的完整性,恢复特定微生物群的丰度,并逆转与asd相关的行为异常。通过益生菌和饮食干预来调节asd患者的肠道微生物群已成为一种潜在的改善措施。
4.植物乳杆菌(lactiplantibacillus plantarum)是一种乳酸杆菌,是少数可以定殖于人体胃肠道黏膜的益生菌之一,常被发现于植物类发酵食品,同时也是一种对肠道健康、代谢紊乱和精神健康具有多种有益影响的重要益生菌。植物乳杆菌st-iii是从中国传统泡菜中分离出来的益生菌菌株,此前研究报道具有调节血脂、抑制有害菌等作用。大多数植物乳杆菌,包括植物乳杆菌st-iii,在动物乳汁中几乎不生长,不能发酵凝乳。目前尚无植物乳杆菌发酵乳对自闭症改善作用的报道。
技术实现要素:
5.鉴于以上所述现有技术的缺点,本发明的目的在于提供植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途,用于解决现有技术中的问题。
6.为实现上述目的及其他相关目的,本发明提供植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途,所述植物乳杆菌st-iii的保藏编号为cgmcc.no.0847。
7.在本发明的某些实施方式中,所述用途为在制备治疗丙戊酸类药物所造成的自闭症的产品中的用途。
8.本发明还提供保藏编号为cgmcc no.0847的植物乳杆菌st-iii发酵乳或发酵乳粉在制备提高肠道菌群丰富度、均匀性、多样性产品中的用途。
9.如上所述,本发明的植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途,具有以下有益效果:首次披露了植物乳杆菌st-iii发酵乳或发酵乳粉具有改善丙戊酸(valproic acid,vpa)导致的自闭症行为和改善肠道菌群结构的新用途,干预时间只需2周即可明显改善自闭症相关行为症状。植物乳杆菌st-iii发酵乳或发酵乳粉产生比植物乳杆菌菌粉单独使用(不发酵)更佳的效果。
附图说明
10.图1.雄性正常对照组、vpa自闭症模型组、st-iii发酵乳组、st-iii发酵乳粉组与牛奶组小鼠在旷场实验中的(a)总移动距离、(b)进入中心区次数、(c)在三箱社交实验中的社交时间比例图、(d)三箱社交实验示意图;(e)植物乳杆菌st-iii发酵乳、st-iii发酵乳粉与st-iii菌粉单独使用在改善自闭症相关行为效果方面的对比图
11.图2.粪便样本测序得到的雄性正常对照组、vpa模型组、st-iii发酵乳组、st-iii发酵乳粉组与牛奶组微生物群的(a)丰富度、(b)多样性和(c)均匀度图
12.图3.雄性正常对照组、vpa自闭症模型组、st-iii发酵乳组与牛奶组小鼠基于bray-curtis距离的肠道菌群所有otu的pcoa图
13.图4.雄性正常对照组、vpa自闭症模型组、st-iii发酵乳组与牛奶组小鼠粪便样本测序得到的植物乳杆菌(lactiplantibacillus plantarum)相对丰度图
14.图5.(a)雄性正常对照组、vpa自闭症模型组、st-iii发酵乳组与牛奶组小鼠肠道菌群在门水平上的组成差异;(b)雄性st-iii发酵乳组与vpa自闭症模型组相比小鼠肠道菌群在门水平上的组成差异
15.图6.(a)雄性正常对照组、vpa自闭症模型组、st-iii发酵乳组与牛奶组小鼠肠道菌群在科水平上的组成差异;(b)雄性st-iii发酵乳组与vpa自闭症模型组相比小鼠肠道菌群在科水平上的组成差异
16.图7.(a)雄性vpa自闭症模型组与正常对照组相比小鼠肠道菌群在属水平上的组成差异;(b)雄性st-iii发酵乳组与vpa自闭症模型组相比小鼠肠道菌群在属水平上的组成差异
具体实施方式
17.本发明提供植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗自闭症的产品中的用途,所述植物乳杆菌st-iii的保藏编号为cgmcc.no.0847。
18.所述植物乳杆菌st-iii为申请号cn03116377专利中公开的菌株,该菌株的分类命名为植物乳杆菌lactobacillus plantarum,保藏日期为2002年12月6日,保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市海淀区中关村北一条13号,中国科学院微生物研究所。
19.所述植物乳杆菌st-iii从泡菜汁和苜蓿汁中分离得到。
20.所述植物乳杆菌st-iii为革兰氏阳性菌,杆状。
21.所述发酵乳的制备方法包括以下步骤:将所述植物乳杆菌st-iii接种至牛乳和增殖剂的混合物中,发酵至凝乳即得到植物乳杆菌st-iii发酵乳。
22.在一种实施方式中,以接种后的总体积为基准,所述植物乳杆菌st-iii的接种终浓度为1.0
×
105~1.0
×
108cfu/ml。
23.在一种实施方式中,所述增殖剂是通过蛋白酶或含有蛋白酶的物质降解植物蛋白反应后的酶解混合物。所述发酵乳或发酵乳粉中含有增殖剂干物质的质量百分比为0.5-20%。所述增殖剂中的蛋白酶选自植物蛋白酶、动物蛋白酶或者微生物蛋白酶中一种或多种的混合物;含有蛋白酶的物质是含有植物蛋白酶的物质、动物蛋白酶的物质或者微生物蛋白酶的物质中一种或多种的混合物。
24.在一种实施方式中,所述牛乳和增殖剂的混合物中,牛乳和增殖剂(固形物)的质量比为100:0.5-20。
25.在一种实施方式中,将所述牛乳和增殖剂的混合物灭菌、冷却后再接种所述植物乳杆菌st-iii。
26.在一种实施方式中,发酵时间不超过12小时。
27.在本发明的某些实施方式中,所述植物乳杆菌st-iii发酵乳中植物乳杆菌st-iii的活菌数为1.0
×
108cfu/ml~9.0
×
109cfu/ml。所述植物乳杆菌st-iii发酵乳中植物乳杆菌st-iii的活菌数例如为1.0
×
108cfu/ml~5.0
×
108cfu/ml、5.0
×
108cfu/ml~1.0
×
109cfu/ml、1.0
×
109cfu/ml~5.0
×
109cfu/ml或5.0
×
109cfu/ml~9.0
×
109cfu/ml。所述植物乳杆菌st-iii发酵乳粉中植物乳杆菌st-iii的活菌数为2.0
×
109cfu/ml~9.0
×
10
10
cfu/ml。所述植物乳杆菌st-iii发酵乳粉中植物乳杆菌st-iii的活菌数例如为2.0
×
109cfu/ml~5.0
×
109cfu/ml、5.0
×
109cfu/ml~1.0
×
10
10
cfu/ml、1.0
×
10
10
cfu/ml~5.0
×
10
10
cfu/ml或5.0
×
10
10
cfu/ml~9.0
×
10
10
cfu/ml。
28.在一种实施方式中,所述发酵乳的制备方法可参考申请号为cn201610826426.1的专利中公开的方法。
29.在一种实施方式中,所述发酵乳粉的制备方法为:将所述发酵乳干燥脱水即得到发酵乳粉。合适的对发酵产物进行干燥的方法对于本领域技术人员来说应该是已知的,例如,可以是冻干等。
30.在本发明的某些实施方式中,所述治疗自闭症的产品通过以下方式治疗或矫正自闭症:提高自闭症患者的社交时间、总运动距离、提高肠道菌群的丰富度、均匀性、多样性、提高厚壁菌门与拟杆菌门的比值。
31.在一种实施方式中,st-iii发酵乳干预两周后,社交时间比例较vpa造模组提高了1.21倍以上,总运动距离较vpa造模组提高了0.69倍以上。社交时间比例计算方法为a室(社交室)停留时间/总测试时间
×
100%。
32.在一种实施方式中,提高小鼠肠道菌群的多样性可以是降低脱铁杆菌门(deferribacteres)、campilobacterota等有害菌的丰度,提高firmicutes、lachnospiraceae等有益菌的丰度。
33.在本发明的某些实施方式中,所述植物乳杆菌st-iii发酵乳或发酵乳粉在制备治疗丙戊酸类药物所造成的自闭症的产品中的用途。
34.在本发明的某些实施方式中,所述丙戊酸类药物选自丙戊酸、丙戊酸钠、丙戊酸镁等。
35.所述产品必然包括所述植物乳杆菌st-iii发酵乳或发酵乳粉,并以所述植物乳杆菌st-iii和/或其代谢产物作为前述功效的有效成分。
36.所述产品中,发挥功用的有效成分可仅为所述植物乳杆菌st-iii发酵乳或发酵乳粉,亦可包含其他物质。
37.亦即,所述植物乳杆菌st-iii发酵乳或发酵乳粉为所述产品的唯一有效成分或有效成分之一。
38.所述产品可以为单成分物质,亦可为多成分物质。
39.所述产品主要针对的对象为哺乳动物。所述哺乳动物优选为啮齿目动物、偶蹄目动物、奇蹄目动物、兔形目动物、灵长目动物等。所述啮齿目动物优选为鼠。所述灵长目动物优选为猴、猿或人。
40.所述产品包括但不限于药物、保健品、食品等。
41.在本发明的某些实施方式中,所述产品为药物,所述药物中还包括药学上可接受的载体或辅料。
[0042]“药学上可接受的”是指当药物适当地给予动物或人时,它们不会产生不利的、过敏的或其它不良反应。
[0043]“药学上可接受的载体或辅料”应当与所述有效成分相容,即能与其共混而不会在通常情况下大幅度降低药物的效果。可作为药学上可接受的载体或辅料的一些物质的具体例子是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纤维素及其衍生物,如甲基纤维素钠、乙基纤维素和甲基纤维素;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如丙二醇、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化剂,如tween;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;无热原水;等渗盐溶液;和磷酸盐缓冲液等。这些物质根据需要用于帮助配方的稳定性或有助于提高活性或它的生物有效性或在口服的情况下产生可接受的口感或气味。
[0044]
本发明还提供保藏编号为cgmcc no.0847的植物乳杆菌st-iii发酵乳或发酵乳粉在制备提高肠道菌群丰富度、均匀性、多样性产品中的用途。
[0045]
ace指数、shannoneven指数、shannon指数分别用于评价菌群丰富度、均匀性和多样性。
[0046]
shannoneven指数反映的是群落内物种的分配状况,即各物种相对丰度的均匀程度。计算公式如下:
[0047][0048]hshannon
:shannon多样性指数
[0049]
ln(s):物种丰富度的自然对数
[0050]
用st-iii发酵乳干预的vpa模型小鼠,干预后小鼠的ace指数较vpa造模组增加40%以上;shannoneven指数增加14%以上;shannon指数增加21%以上。
[0051]
用st-iii发酵乳粉组干预的vpa模型小鼠,干预后小鼠的ace指数较vpa造模组增
加39%以上;shannoneven指数增加13%以上、shannon指数增加20%以上。
[0052]
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
[0053]
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。
[0054]
当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。
[0055]
实施例中统计分析采用spss 23.0软件进行,用graphpad prism 7进行各种统计图的制作。所有数据均以均值
±
标准差表示,组间差异性比较采用独立样本t检验或单因素方差分析或kruskal-wallis检验。p《0.05被认为具有统计学意义。显著差异由*p《0.05,**p《0.01,***p《0.001表示。
[0056]
实施例1
[0057]
植物乳杆菌st-iii发酵乳及发酵乳粉的制备及其活菌检测(参考专利cn201610826426.1):
[0058]
配方:生牛乳:植物乳杆菌增殖剂(固形物含量):水的比例为80:2:18。(增殖剂的制备方法:将大豆蛋白和菠萝全汁在水溶液中在25℃-80℃下酶解反应0.5~8h制成植物乳杆菌增殖剂。参考专利:一种添加有植物乳杆菌增殖剂的发酵产品及其制作方法cn201610826426.1)。
[0059]
制备方法:将上述混合料液预热升温,在65℃、20mpa下均质后,95℃保温杀菌10min,冷却至37℃。接种(st-iii接种量终浓度1.0
×
106cfu/ml),发酵至凝乳、摇匀或均质即得到植物乳杆菌st-iii发酵乳。该发酵乳中植物乳杆菌st-iii活菌数可达1.0
×
109cfu/ml,于4℃冷藏保存21d内其活菌数仍可大于3.0
×
108cfu/ml。该发酵乳通过冻干脱去水分,即得到植物乳杆菌st-iii发酵乳粉。
[0060]
干预动物时,发酵乳粉按原发酵乳的固形物和水分含量比例,加无菌水复溶还原为液态发酵乳后,与前述原发酵乳等剂量条件使用。例如:一定体积x ml的原发酵乳的总质量为mt g,冻干脱去水分后的发酵乳粉质量为ms g,则原发酵乳中固形物和水分的含量比例为ms:(mt-ms)。干预动物时,即按ms:(mt-ms)的比例添加无菌水,即取质量为ms g的冻干发酵乳粉,添加(mt-ms)g的无菌水,复溶后还原成x ml质量为mt g的液态发酵乳。
[0061]
植物乳杆菌st-iii菌粉的制备及其活菌计数:
[0062]
将植物乳杆菌st-iii(cgmcc no.0847)在mrs液体培养基(德国merck公司,商品号:1106610500)中培养(37℃,18-24小时)后富集菌体,添加冻干保护剂,通过冻
干脱去水分,即得到植物乳杆菌st-iii菌粉,st-iii活菌计数为3
×
10
11
cfu/g。
[0063]
实施例2
[0064]
自闭症模型小鼠的建立:
[0065]
小鼠适应:育龄期健康spf级icr小鼠饲养于标准动物房,恒定温度23℃,相对湿度50%-60%,12h/12h日/夜交替光照。小鼠适应1周后,于下午17:00将雌雄(雌性:雄性=2:1)小鼠合笼过夜,次日上午9点分笼时检查雌鼠是否有阴栓存在。
[0066]
vpa造模:将成功受孕的雌鼠随机分为2组,妊娠的第12.5天单次腹腔注射vpa 500mg/kg或等体积无菌生理盐水,并分别命名为vpa组和vpa-对照组。子代小鼠出生后6周-8周内进行行为学检测。与vpa-对照组对比后,筛选出具有明显自闭症样行为的雄性小鼠为vpa自闭症模型小鼠并用于后续干预实验。
[0067]
实施例3
[0068]
植物乳杆菌st-iii发酵乳干预vpa自闭症模型小鼠:
[0069]
总计50只雄性vpa自闭症模型小鼠随机分成5组,每组10只。分别为vpa模型组(记作:vpa)、st-iii发酵乳组、st-iii发酵乳粉组、牛奶组(含有增殖剂的牛奶,记作:milk)以及st-iii菌粉组。另有10只正常雄性小鼠作为正常对照组(记作:control)。st-iii发酵乳组、st-iii发酵乳粉组和牛奶组每只小鼠早晚各一次灌胃400μl对应样品,持续干预2周。对于st-iii菌粉组,植物乳杆菌st-iii冻干菌粉悬浮于10mm pbs(ph7.2-7.4)中,配制成浓度为5
×
108cfu/ml的st-iii菌粉悬液,早晚各一次灌胃400μl。在干预期间,小鼠自由饮水进食。
[0070]
实施例4
[0071]
植物乳杆菌st-iii发酵乳或发酵乳粉干预vpa模型小鼠,改善其自闭症相关行为,且比单独使用st-iii菌粉效果更佳:旷场实验:将受试小鼠放入50
×
50
×
40cm的开放场地并允许自由探索10min以适应环境。随即,打开摄像系统(1/3“sony super had ccd)记录小鼠接下来10min的总运动距离和中心区域进入次数,并进行后续分析。三箱社交实验:如图1d所示,将一个60
×
40
×
22厘米的有机玻璃盒分成三个相互连接的小室(a、b、c)。小鼠首先在空场地适应10分钟,然后将小鼠限制在b室(中心室)中。在a室中放置一只匹配的,具有相同基因型、年龄、性别和治疗的陌生小鼠,而在c室中放置一个小物体。在接下来的10分钟内,让测试小鼠在三个小室内自由移动,头顶摄像头(1/3“sony super had ccd)记录了被测小鼠与陌生小鼠的嗅觉交互时间。
[0072]
受试小鼠按旷场实验和三箱社交实验的顺序进行行为学测试。每次测试结束后,轻轻取出受试小鼠放回笼子,然后用75%的酒精擦拭装置,待其干燥后进行下一只小鼠的测试。
[0073]
在旷场实验中,总移动距离和进入中心区的次数可以反映小鼠的活动力和焦虑状态。如图1a所示,vpa模型组小鼠的总运动距离相比正常对照组显著减少(p《0.01)。同时,与vpa模型组相比,st-iii发酵乳、st-iii发酵乳粉组小鼠则显著提高了总运动距离(p《0.001),且st-iii发酵乳和st-iii发酵乳粉组相比正常对照组的运动距离更长(p《0.01)。图1b所示,vpa模型组小鼠进入中心区的次数相比正常对照组显示出减少趋势,但无统计学意义。st-iii发酵乳和st-iii发酵乳粉组相较vpa模型组略微增加了进入中心区的次数(无统计学意义),相较牛奶组显著增加了进入中心区的次数(p《0.05)。提示st-iii发酵乳和发
酵乳粉的干预都能够改善雄性自闭症模型小鼠的活动力。
[0074]
三箱社交实验结果如图1c所示,与正常对照组相比,雄性vpa模型小鼠的社交时间比例显著减少(p《0.01),而在st-iii发酵乳和st-iii发酵乳粉干预后得到了显著的恢复(p《0.01),牛奶组也显示出一定的恢复趋势,但与vpa模型组相比其差异没有统计学意义。提示st-iii发酵乳和发酵乳粉的干预都能够明显改善雄性自闭症模型小鼠的社交互动障碍。
[0075]
如图1e所示,与vpa模型组相比,st-iii发酵乳组和st-iii发酵乳粉组小鼠的社交时间比例分别提高了1.21倍和0.94倍,总运动距离分别提高了0.69倍和0.68倍;单独使用st-iii菌粉组小鼠的社交时间比例提高了0.63倍,总运动距离提高了0.13倍。提示相比单独使用植物乳杆菌st-iii菌粉,st-iii发酵乳或发酵乳粉的干预效果更好。
[0076]
实施例5
[0077]
植物乳杆菌st-iii发酵乳干预vpa模型小鼠,改善其肠道菌群:
[0078]
样品采集和16s rrna基因序列检测:收集小鼠粪便样本,-80℃保存至dna提取。根据试剂盒的操作说明,使用qiaamp dna粪便迷你试剂盒(qiagen,hilden,germany)从0.3g小鼠粪便中提取细菌基因组dna。使用1.5%琼脂糖凝胶电泳检测所提取的dna完整性。对16s rrna基因v3-v4可变区进行pcr扩增。用于扩增v3-v4可变区的引物为341f(5
′‑
cctacgggnggcwgcag-3
′
)和805r(5
′‑
gactachvgggtatctaatcc-3
′
)。热循环步骤如下:95℃5min;95℃45s,55℃30s,72℃30s进行20个循环;最后72℃10min。每个样品的pcr扩增进行3次。使用2%琼脂糖凝胶回收各个样品pcr产物,并用axyprep dna gel extraction kit(axygen)进行纯化,tris-hcl洗脱,使用2%琼脂糖凝胶电泳再次检测。应用分光光度法(quantifluor
tm-st,promega)进行定量检测。根据illumina miseq平台标准操作规程将纯化后的扩增片段构建pe 2
×
300的文库并进行测序。
[0079]
生物信息学分析:alpha和beta多样性分析分别反映微生物群落的丰富度、多样性和物种组成的相似性和差异关系。为了解样本测序结果中的菌种、菌属等数目信息并进行后续分析,将序列按照97%相似度对非重复序列进行聚类,得到otu代表序列。使用qiime2(版本2021.4)对具有相同序列深度(每个样本24797个序列)的样本进行群落丰富度、均匀度和多样性分析(ace指数,shannoneven指数和shannon指数)。在otu水平上用weight-unifrac算法进行主坐标分析(principal co-ordinates analysis,pcoa)评估物种组成的差异性。使用基于bray-curtis距离的anosim评估组间细菌群落组成的多样性(正常对照/vpa造模/st-iii发酵乳/st-iii发酵乳粉/牛奶)。基于ribosomal database project数据库,使用在线软件rdp分类器在默认参数(80%阈值)下分类。为了确定各组中分类群的显著差异丰度,应用stamp评估从门水平到物种水平的丰度,p值《1e-5。
[0080]
如图2所示,正常对照组与vpa造模组小鼠肠道菌群ace、shannoneven和shannon指数值之间均无统计学差异,提示两组样本物种的丰富度、均匀性和多样性无显著差异。vpa模型组与干预组(st-iii发酵乳组、st-iii发酵乳粉组和牛奶组)相比,各干预组的肠道菌群丰富度分别增加40.93%、39.94%和26.94%、均匀性分别增加14.42%、13.41%和10.14%、多样性分别增加21.72%、20.74%和14.98%,均显著提高,增加的百分比的计算公式为:(干预组-vpa组)/vpa组*100%。其中,st-iii发酵乳组和st-iii发酵乳粉组的菌群丰富度显著高于牛奶组。一般认为较高的肠道菌群多样性有益于个体健康。
[0081]
如图3所示,pcoa分析显示vpa模型组与正常对照组小鼠肠道菌群的构成存在一定
差异。在使用发酵乳和牛奶干预后,st-iii发酵乳组和牛奶组小鼠的饮食结构发生了重大变化,两组干预组小鼠的肠道菌群组成与vpa模型组和正常对照组这两组相比均有显著差异,且干预组两组之间也有显著差异,提示使用st-iii发酵乳干预2周后可以改变小鼠的肠道菌群组成。
[0082]
如图4所示,没有用st-iii干预的正常对照组、vpa模型组以及牛奶组的小鼠粪便中不存在或仅含有极低水平的植物乳杆菌,而st-iii发酵乳组小鼠粪便中植物乳杆菌相对丰度显著升高,差异具有统计学意义(p《0.01),提示植物乳杆菌st-iii能耐胃酸,在自闭症小鼠肠道中能存活。
[0083]
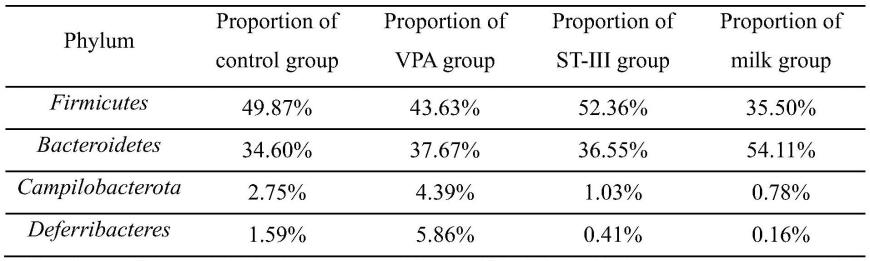
如图5和表1所示,在门水平上,四组小鼠肠道微生物群落的主要组成是厚壁菌门(firmicutes)和拟杆菌门(bacteroidetes)。vpa模型组和牛奶组小鼠的厚壁菌门相对含量下降,厚壁菌门/拟杆菌门比值在正常对照组小鼠中为1.44,在vpa模型组和牛奶组小鼠中分别降为1.15和0.65,而在st-iii发酵乳组中比值为1.43,与正常小鼠接近。vpa模型组中脱铁杆菌门(deferribacteres)的含量从正常组的1.59%上升至5.86%,这主要归因于mucispirillum schaedleri种的otu水平增加。mucispirillum schaedleri是啮齿动物肠道黏液层中普遍存在但丰度较低的菌种,通常被认为是一种与肠道炎症相关的致病菌。st-iii发酵乳和牛奶的干预能够降低脱铁杆菌门(deferribacteres)含量(分别为降低至0.41%和0.16%)。此外,与vpa造模组相比,st-iii发酵乳组campilobacterota菌门的丰度水平显著降低了76.54%(p=1.97e-3)。已有研究发现campilobacterota菌门在接受可预测轻度应激的抑郁症小鼠肠道中含量显著上升。
[0084]
表1正常对照组、vpa模型组、st-iii发酵乳组和牛奶组在门水平上肠道菌群相对含量
[0085][0086]
如图6和表2所示,在科水平上,vpa造模组小鼠的毛螺菌科(lachnospiraceae)、阿克曼氏菌科(akkermansiaceae)和普雷沃氏菌科(prevotellaceae)丰度相比正常对照组有下降的趋势,而螺杆菌科(helicobacteraceae)和脱铁杆菌科(deferribacteraceae)的相对丰度则分别上升了59.64%和2.69倍。毛螺菌科可以产生短链脂肪酸、将初级胆汁酸转化为次级胆汁酸,并能提高肠道对病原体的定植抵抗力;阿克曼氏菌科与肥胖及相关代谢紊乱发生率呈负相关关系;普雷沃氏菌科的减少与帕金森病及重度抑郁症相关;螺杆菌科dna的高表达与克罗恩病相关;脱铁杆菌科作为致病性或条件致病性微生物与溃疡性结肠炎和腹泻相关。将前两组(control、vpa)和后两组(st-iii、milk)进行对比可以发现即使单独使用牛奶(含增殖剂)干预也会导致小鼠肠道微生物群发生显著变化,说明宿主饮食的改变是肠道微生物组成的主要决定因素。具体而言,在前两组(control、vpa)中占据优势的乳杆菌科(lactobacillaceae)在后两组(st-iii、milk)中显著下降,这可能是由于摄入含有增殖
剂的牛乳为小鼠提供了额外的脂肪和糖类来源,改变了原本的饮食结构。文献(scientific reports,doi:10.1038/s41598-017-07428-w)报道在小鼠食用高脂肪、高糖饮食期间,摄入的植物乳杆菌的存活率和持久性得到显著改善,且与肠道内原本的乳杆菌科含量呈负相关。另一方面,丰度较低的其他菌科(记作:others)的相对含量则显著上升,对应了图2所示的分析结果,说明发酵乳和牛奶的干预能显著提高小鼠肠道微生物群的多样性。值得注意的是,添加了植物乳杆菌st-iii的发酵乳组相比vpa模型组还显著提高了毛螺菌科(lachnospiraceae)的相对丰度(2.46倍,p=2.78e-3),降低了螺杆菌科(helicobacteraceae)和eggerthellaceae的丰度(3.26倍,p=3.43e-3;7.58倍,p=4.11e-3)。
[0087]
表2正常对照组、vpa模型组、st-iii发酵乳组和牛奶组在科水平上肠道菌群相对含量
[0088][0089]
如图7所示,在属水平上,vpa模型组与正常对照组相比有4个属丰度显著降低,包括malacoplasma(p=0.026)、kineothrix(1.69倍,p=0.035)、jeotgalicoccus(p=0.035)和longibaculum(p=0.042),另有1个属butyricimonas(p=0.045)丰度显著升高。其中kineothrix属已被其他研究发现在帕金森患者和便秘小鼠肠道中表现出显著的丰度下降。st-iii发酵乳组与vpa模型组相比,st-iii发酵乳显著提高了包括kineothrix(6.17倍,p=9.74e-3)和植物乳杆菌(lactiplantibacillus)(p=0.011)在内2个属的丰度;同时显著降低了包括helicobacter(3.26倍,p=0.023)、乳杆菌(lactobacillus)(5.19倍,p=0.01)和limosilactobacillus(4.5倍,p=9.91e-3)在内3个属的丰度。
[0090]
本发明的实施例中让怀孕小鼠暴露于丙戊酸(vpa)以诱导后代雄性小鼠出现与asd相关的行为异常,主要表现为社交互动受损、活动力下降和焦虑行为。再用植物乳杆菌st-iii发酵乳(粉)灌胃vpa模型小鼠,观察干预组和vpa对照组的行为学以及肠道菌群差异。结果表明,植物乳杆菌st-iii发酵乳(粉)干预两周就能有效改善雄性vpa小鼠社会交往障碍并提高整体活动能力,特别是植物乳杆菌st-iii发酵乳或发酵乳粉产生比植物乳杆菌st-iii菌粉单独使用(不发酵)更佳的效果。同时发现st-iii发酵乳能恢复厚壁菌门与拟杆菌门的比值,显著提高小鼠肠道菌群的多样性,降低脱铁杆菌门(deferribacteres)等有害菌丰度,提高毛螺菌科(lachnospiraceae)等有益菌丰度。而且st-iii发酵乳(粉)干预仅需
2周即可表现出明显的改善自闭症相关行为的作用,比文献报道的其他菌株干预哺乳动物起作用的时间(至少3周)明显缩短。
[0091]
以上的实施例是为了说明本发明公开的实施方案,并不能理解为对本发明的限制。此外,本文所列出的各种修改以及发明中方法的变化,在不脱离本发明的范围和精神的前提下对本领域内的技术人员来说是显而易见的。虽然已结合本发明的多种具体优选实施例对本发明进行了具体的描述,但应当理解,本发明不应仅限于这些具体实施例。事实上,各种如上所述的对本领域内的技术人员来说显而易见的修改来获取发明都应包括在本发明的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。