通过非终点扩增进行的单细胞的靶标拷贝数的分区型确定
1.在先申请的交叉引用
2.本技术基于2019年11月14日提交的美国临时专利申请序列号62/935,538并根据35u.s.c.
§
119(e)要求其权益,该申请通过引用全部纳入本文用于所有目的。
3.引言
4.非侵入性测试方法可能无法确定人类样品中是否存在全部或部分染色体重复或缺失。染色体重复可以包括驱动癌症的局部化(局部)基因扩增,或整体或部分染色体重复,如发育中胎儿的非整倍体中所见(例如,常见的三体性,如唐氏综合征)。在妊娠测试中,在产前筛查测试后,高危个体采用金标准、侵入性诊断方法(即荧光原位杂交(fish)和/或核型分析)进行检测。这些侵入性诊断方法需要通过绒毛膜绒毛取样(cvs)或羊膜穿刺术收集胎儿细胞,它们各自的流产风险都很小(通常《1%)。较新的筛查方法,称为无创产前检测(nipt),利用母体血浆中存在的无细胞dna的下一代测序(ngs)评估非整倍性。然而,这些较新的方法通常需要来自10-20ml血液样品的总无细胞dna和来自胎儿细胞的足够高的贡献(胎儿分数,或ff%)才能提供准确的结果。
5.需要新的无创分子筛选/诊断方法来确定单细胞(single cells)中靶标的拷贝数。
技术实现要素:
6.本公开提供了分析包含细胞和/或无细胞细胞核(cell-free nuclei)的样品的方法。在示例性方法中,可以形成分区,每个分区包括样品的部分。至少所述分区的子集的各分区可包含来自样品的细胞/细胞核中的仅一种。可以在分区中裂解来自样品的细胞和/或无细胞细胞核。可以对分区中的一个靶标或一组靶标进行至少一个扩增反应。可以在各扩增反应的指数/线性阶段从分区中收集扩增数据。可以利用扩增数据来确定个体分区(individual partitions)的靶标或靶标组的拷贝数,以确定在所分析的全部细胞或细胞子集中是否存在重复或缺失。
7.附图简要说明
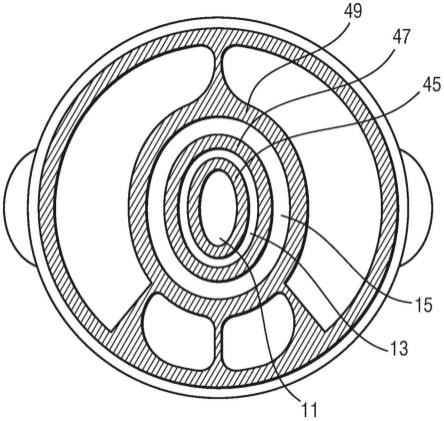
8.图1是列出示例性步骤的流程图,这些步骤可以在用于分析包括细胞或细胞核的样品的分区型(partition-based)扩增方法中进行,以确定样品的个体细胞或细胞核的至少一种靶标或靶标组的拷贝数。
9.图2是说明在包含母体细胞和胎儿细胞的样品上对于两种不同靶标或靶标组进行的示例性分区型扩增方法的多个方面的示意图,其中,母体细胞对于靶标或靶标组两者均是二体性的,其中胎儿细胞针对靶标或靶标组中仅一者是三体性的,并且其中从两个不同波长范围(wavelength regime)的分区检测光致发光以评估靶标扩增。
10.图3是概念直方图,显示了可以从图2方法中的分区中检测到的示例性荧光,其中荧光强度对应于染色体中靶标的拷贝数,该染色体在母体细胞中是二体性且在胎儿细胞中是三体性的。指示了存在于直方图的各不同分区组(patition group)的分区中的第一靶标的拷贝数,以及细胞数。
11.图4是概念散点图,显示了可以从图2方法中的分区中检测到的两种不同波长范围(a和b)中的示例性荧光,其中荧光a的强度对应于在母体细胞中是二体性且在胎儿细胞中是三体性的染色体中的第一靶标的拷贝数,并且其中荧光b的强度对应于在母体细胞和胎儿细胞中均为二体性的染色体中的第二靶标的拷贝数。指示了存在于各分区簇(partition cluster)的分区中的第一靶标的拷贝数,以及细胞数。
12.图5的图表绘制了从七个不同组的液滴测量的fam荧光强度的曲线图,各组液滴预加载有不同量的fam染料(即,50nm、100nm、200nm等)。
13.图6的图表绘制了fam荧光幅度,作为靶标扩增的指标,该指标随着pcr循环次数的增加,从四个不同组的液滴的个体液滴(事件)中检测到。
14.图7显示的一对图表比较了使用超螺旋模板(左侧)或该模板的线性形式(右侧)作为相同靶标序列的来源的基于液滴的扩增试验,其中fam荧光的幅度由一系列液滴(事件)中检测到,且与靶标序列的扩增量直接相关。
15.图8是从含有各种组合的野生型(wt)和突变体(g12d)n-ras靶标序列的液滴收集的扩增数据的二维荧光散点图,其中检测到野生型和突变体靶标序列在hex和fam荧光方面分别有所增加。
具体实施方式
16.本公开提供了分析包含细胞和/或无细胞细胞核(cell-free nuclei)的样品的方法。在示例性方法中,可以形成分区,每个分区包括样品的部分。至少所述分区的子集的各分区可包含来自样品的细胞/细胞核中的仅一种。可以在分区中裂解来自样品的细胞和/或无细胞细胞核。可以对分区中的一个靶标或一组靶标进行至少一个扩增反应。可以在各扩增反应的指数/线性阶段从分区中收集扩增数据。可以利用扩增数据来确定个体分区的靶标或靶标组的拷贝数,以确定在所分析的全部细胞或细胞子集中是否存在重复或缺失。
17.本公开的方法结合了单细胞测定的准确性益处,如在荧光原位杂交(fish)中那样,以及单细胞扩增方法的简单性。产前检测可以相对非侵入性地使用从母体血液中获得的胎儿细胞进行。可以稳健地测量一个或多个所选核酸靶标(dna或rna)的拷贝数/细胞。所述方法可以应用于非侵入性产前测试(nipt)和/或非侵入性产前诊断(nipd)。换言之,使用该方法的产前筛查或诊断可以确定从母体血液分离的细胞中是否存在任何部分/完全染色体缺失或重复(例如,唐氏综合征中的chr21)。这些方法可能对母体血液中胎儿细胞的百分比(即胎儿分数)不太灵敏,因为各细胞是针对三体性个别地评分的。该方法还可以应用于肿瘤学测试/诊断,其中可以评估分离的循环肿瘤细胞(ctc)以确定肿瘤中是否存在基因扩增(例如,转移性乳腺癌中的her2扩增或胃肠间质瘤(gist)中的fgfr2扩增)。可以分析混合细胞样品(例如,多个母体淋巴细胞中的胎儿细胞,或多个淋巴细胞中的ctc)。在一维或二维分区图中,具有靶标或靶标组的异常拷贝数(cn)的细胞可以被鉴别为与接收正常细胞的分区分开的不同分区组。
18.本公开的其它方面描述于以下小节中:(i)定义、(ii)方法概述、(iii)实施例,和(iv)所选方面。
19.i.定义
20.本公开所用技术术语具有本领域技术人员所公认的含义。然而,以下术语可以进
一步定义如下。
21.扩增子——扩增反应的产物。扩增子可以通过扩增靶标而产生,从而使得扩增子对应于靶标(即,与靶标匹配和/或互补)。然而,扩增子的序列,例如在引物结合位点处的序列,可能与靶标序列不完全匹配和/或不完全互补。
22.扩增——由对应于靶标的扩增子制备多个拷贝的过程。该过程可互换地称为靶标扩增。随着扩增的进行,扩增可能会产生拷贝数的指数增加。通常扩增可能会使扩增子的拷贝数增加1,000倍以上。本文所公开的方法的示例性扩增反应可以包括聚合酶链式反应(pcr)或连接酶链式反应(lcr),它们各自均由热循环驱动。该方法还或替代性地可以使用可以等温进行的其它扩增反应,例如分支探针dna测定、级联rca、解旋酶依赖性扩增、环介导等温扩增(lamp)、基于核酸的扩增(nasba)、切口酶扩增反应(near)、pan-ac、q-β复制酶扩增、滚环复制(rca)、自持序列复制、链置换扩增和/或类似手段。扩增可以利用线性或环状模板。
23.扩增试剂——促进靶标扩增的任何试剂。所述试剂可以包括以下各者的任何组合:用于扩增至少一种靶标的至少一对引物、用于检测所述至少一种靶标的扩增的至少一种标记物(例如,包括标记物和/或dna嵌入染料的至少一种探针作为标记物)、至少一种聚合酶和/或连接酶(其可以是热稳定的),和核苷三磷酸(dntp和/或ntp)等。
24.液滴——由不混溶的液体包封的小样份(volume)液体(例如,由不混溶的液体包封,其可能形成乳液的连续相)。不混溶的液体可以包括油和/或可以主要由油构成。用于本文公开的方法的液滴可例如具有小于约500nl、100nl、10nl或1nl等的平均尺寸。
25.标记物——与结构相关联的、识别性和/或区别性标志物或标识符,该结构例如引物、探针、扩增子、液滴等。标记物可以与结构共价结合,例如标记物与寡核苷酸共价连接,或非共价结合(例如,通过嵌入、氢键、静电相互作用、封装等)。示例性标记物包括光学标记物、放射性标记物、磁性标记物、电学标记物、表位、酶、抗体等。光学标记物可通过它们与光的相互作用进行光学检测。可能合适的示例性光学标记物包括光致发光团,猝灭剂(quencher),和嵌入式染料等。
26.光——光辐射,包括紫外线、可见光和/或红外线。
27.裂解——任何损害细胞或细胞核(特别是其外膜)完整性的操作。可对细胞或细胞核进行以促进裂解的示例性操作可包括加热、超声处理、与表面活性剂接触、利用酶催化反应和/或通过渗透施加压力等。全细胞(包含细胞核)或无细胞细胞核的裂解可能会从细胞核(和/或细胞质)释放基因组dna(和rna/蛋白质),并可能破坏由基因组dna形成的染色质结构,任选地从基因组dna分离组蛋白。
28.裂解试剂——促进细胞/细胞核裂解和/或增加扩增反应靶标序列可及性的任何试剂。裂解试剂可以包括表面活性剂、至少一种酶(例如核酸酶和/或蛋白酶)、盐等。
29.核酸寡聚物——相对短的多核苷酸(即寡核苷酸)或相对短的多核苷酸类似物(即寡核苷酸类似物)。示例性类似物包括肽核酸、锁核酸、硫代磷酸酯等。核酸寡聚物可以具有偶联单元的非支化(或支化)链,即核苷酸或核苷酸类似物,各自都含有碱基(例如核碱基)。例如,核酸寡聚物可以包含少于约200、100、75或50个偶联单元,其中各单元是核苷酸或核苷酸类似物。核酸寡聚物可以是化学合成的或生物合成的等等。核酸寡聚物可以用至少一种标记物进行标记,所述标记物可以与链偶联并且被视为是寡聚物的一部分。所述至少一
种标记物可以包括至少一种光致发光团,因此可以是光致发光标记物。各标记物可以在任何合适的位置偶联至核酸寡聚物的链,包括5'端、3'端或中间的5'和3'端。
30.分区——彼此隔开的液体样份的组。各液体样份可以包含含相同样品流体(same sample-containing fluid)的部分。可以利用不混溶的液体(例如,油)、装置的壁或它们的组合等将液体样份彼此分离。因此,液体样份可以是乳液的液滴,或由孔、室(例如,容量小于1μl的纳米室)或管(例如,直径小于1mm的微管)等保持的样份。液体样份可以具有基本相同的大小和/或可以包含基本相同量的流体。
31.光致发光——光的发射,其中所述发射是由电磁辐射引起的。响应于电磁辐射(例如光)的光子吸收,任何形式的物质都可以产生光致发光。示例性的光致发光形式包括荧光和磷光等。
32.光致发光团——能够响应电磁辐射吸收而发光的物质(例如标记物)。因此,光致发光团例如可以是荧光团或磷光体。合适的光致发光团可包括染料,例如fam、vic、hex、rox、tamra、joe、cyanine-3或cyanine-5染料等。
33.探针——标记的核酸寡聚物(寡核苷酸或其类似物),其用于报告靶标的扩增。探针可以是包括用光致发光团标记的核酸寡聚物的光致发光探针。探针可以用于与由靶标扩增产生的扩增子的至少部分杂交。探针(例如,水解探针)可以用于在扩增反应期间与扩增子的至少部分杂交,或者探针(例如,分子信标探针)可以用于在扩增反应已经完成之后与扩增子杂交,等等。
34.猝灭-导致光致发光团的光致发光降低的任何与邻近度相关的过程。猝灭可以通过任何合适的机制或机制的组合进行,包括动态猝灭(例如,福斯特共振能量转移(fret),德克斯特电子转移(dexter electron transfer),激基复合体)和/或静态/接触猝灭等。猝灭效率可能对光致发光体与其猝灭剂之间的距离非常敏感。例如,在fret中,猝灭的效率与该距离成反比(升至六次方)。因此,光致发光团与猝灭剂之间的分隔距离的微小变化可导致猝灭效率的较大变化。淬灭效率下降到50%的距离可以小于10纳米。
35.猝灭剂是能够通常以高度邻近依赖性方式猝灭光致发光团的光致发光的标记物。淬灭剂可以是另一种光致发光团,或者可以是基本上不发光的暗淬灭剂(dark quencher)。示例性暗猝灭剂可包括黑洞猝灭剂(例如,bhq0、bhq1、bhq2、bhq3)、atto猝灭剂、iowa black、qsy 7/9/21/35等。
36.参考物——作为内参的靶标或靶标组,可将感兴趣靶标或感兴趣靶标组与其做比较。因此,参考物通常在被测试的细胞或细胞核中具有基本恒定(或至少更恒定)的拷贝数,例如一个或两个拷贝数,而感兴趣的靶标或靶标组可能在细胞或细胞核中具有可变性更高的拷贝数(例如,由于重复和/或缺失)。
37.靶标组——被共同检测且任选地难以区分的具有不同序列的两种或更多种靶标。靶标的组,可互换地称为“靶标组”(例如两个或更多个第一靶标的第一靶标组),可以由两个或更多个靶标构成,其中各靶标位于或表达自同一染色体的拷贝、染色体区域或基因等,或至少所述组的靶标中至少两个可位于或表达自不同染色体。所述组的各靶标可至少在初始时用不同的引物对进行扩增。所述组的各靶标的扩增可采用不同靶标特异性探针、采用相同探针(例如,退火至通过引物纳入各类型的扩增子中的相同探针结合位点的探针)、采用相同的间插染料等来报告。靶标组的各靶标的扩增可由相同检测信号(也称为扩增报告
信号)来报告。例如,如果信号是检测到的光致发光,则该光致发光可以针对该靶标组中的各靶标在相同波长范围内(例如,从存在于不同探针中的相同种类的光致发光团发射)检测。
38.靶标——具有任何合适长度的核酸序列(dna和/或rna)或蛋白质。示例性核酸靶标是约20-1000个核苷酸,或约30-500个核苷酸等。示例性蛋白质靶标可通过邻近连接测定法(pla)或邻近延伸测定法(pea)检测。靶标可互换地称为靶标序列。
39.模板——包含被扩增的序列的核酸。
40.ii.方法概述
41.本节概述了用于分析样品以确定样品的个体细胞或细胞核的至少一种靶标或靶标组的拷贝数的分区型扩增方法;见图1-4。
42.图1显示了分区型扩增方法的示例性步骤的流程图40,以确定个体细胞/细胞核的靶标拷贝数。这些步骤可以针对该方法以任何合适的顺序和组合来进行,并且可以通过本文的任何其它公开内容来修改或补充。
43.可以制备样品,如41所示。样品包括可能基本上完整的感兴趣的细胞和/或无细胞细胞核。各感兴趣的细胞/细胞核包含要在该方法中测定的至少一个靶标的至少一个拷贝。在该方法中待测定的一种或多种靶标的拷贝数可能在感兴趣的细胞/细胞核中表现出拷贝数异质性。因此,感兴趣的细胞/细胞核可以包括至少两种不同类型或种类的感兴趣的细胞/细胞核,例如母体和胎儿、正常和肿瘤、具有靶标异质性/不稳定性的肿瘤、具有靶标异质性/不稳定性的转基因等。样品还可以包含不感兴趣且不包含至少一个靶标的其它细胞/细胞核。
44.样品的制备可以包括形成含样品的流体,也称为主体相。更具体地,样品的细胞/细胞核和其它成分(例如,周围液体、缓冲液、盐、碎片等)可以与一种或多种裂解试剂、一种或多种扩增试剂、水性稀释液和/或类似物组合。扩增试剂可以用于扩增至少一个靶标或靶标组,并且可以包括:用于各靶标的引物对、至少一个标记物(例如,相同的标记物)以报告靶标或靶标组的扩增、聚合酶/连接酶以催化靶标扩增、dntp/ntp等。可以添加水性稀释液以调节每单位体积的细胞/细胞核的数量,以促进形成具有感兴趣的个体细胞/细胞核的分区。可能合适的裂解试剂和扩增试剂的其它方面描述于上文第i节。
45.可以形成分区,如42所示。可以形成和/或使用任何合适数量的分区,例如至少10、25、50、100、200、500、1000、10,000、100,000或一百万等。分区可以使用在样品制备步骤41中产生的含样品流体(或主体相)形成,并且可以在尺寸上基本均一。例如,可以将含样品流体划分以形成分区,各分区基本上完全由含样品流体构成,并且这些分区可以用于该方法的后续步骤。在其它情况下,可通过将含样品流体的部分引入预先形成的、隔开的流体样份中(例如通过移液或微注射),以形成用于该方法的后续步骤的分区。在其它情况下,用于该方法的后续步骤的分区可通过如下方式形成:划分含样品流体以产生分隔的流体样份,其随后在细胞/细胞核裂解前用附加的流体补充。
46.各分区包括含样品流体的部分(并因此包括样品的部分)。在一些实施方式中,仅分区子集的各分区可以接收来自样品的至少一个感兴趣的细胞/细胞核。换言之,另一分区子集的各分区可能不接收来自样品的感兴趣的细胞/细胞核。任选地,又一分区子集接收来自样品的至少两个感兴趣的细胞/细胞核。因此,如果细胞/细胞核在含样品流体中彼此分
离(例如,不聚集或群集在一起),则细胞/细胞核向分区的分布可以是基本上随机的(例如,通常具有泊松分布)。在其它实施方式中,微流体装置可用于增加只确切地有一个细胞或细胞核的分区的百分比。例如,如果分区是液滴,则微流体装置可以在且仅在存在细胞或细胞核时触发液滴形成,从而允许基本上各液滴仅包含一个细胞或细胞核。
47.在一些实施方式中,少于二分之一的分区可以包含至少一个细胞(或无细胞细胞核)。例如,少于约30%、20%或10%的分区可包含至少一个细胞或无细胞细胞核。如果假设个体细胞/细胞核在分区形成时彼此独立地被定位到分区,则若无细胞核/细胞分区的百分比相对较高,两个或更多个细胞(和/或无细胞细胞核)偶然共定位到同一分区的频率可以保持在基本上可以忽略不计的水平。例如,如果仅约10%的分区接收至少一个细胞/细胞核,那么预期统计上仅约1%的分区会通过偶然共定位接收两个细胞/细胞核。
48.在其它实施方式中,包含两个或更多个细胞的分区的频率可能是显著的。对于这些实施方式,所述方法可鉴别具有多于一个细胞/细胞核的分区(并且任选地将这些分区排除以不计它们对分析的最终结果所产生的贡献),如下所述。
49.可以裂解分区中的细胞/细胞核,如43所示。可以通过物理和/或化学处理的任何合适组合来促进裂解。例如,可以将分区升温到高于室温,例如升温到至少37、40、50、60、70、80、85、90或95摄氏度的温度。升温可进行任何合适的时间长度,例如1-120、2-90或3-60分钟,或至少约1、2、3、5、10、20、30、45或60分钟。各分区可以包括非离子或离子表面活性剂以促进裂解和/或提高对靶标序列的可及性。细胞/细胞核裂解的其它方面在上文第i节和本公开内容他处进行描述。
50.流体任选地可以添加到分区中,如44所示。流体可以是液体并且可以包含任何合适的试剂,并且可以将相同量的流体添加到各分区中。流体可以携载试剂,例如热敏(和/或裂解敏感性)试剂(例如,核酸酶、蛋白酶、聚合酶和/或连接酶),或者可以稀释分区中存在的酶抑制性物质以降低它们的抑制活性。可以通过利用电场的微注射、通过移液等来添加流体。流体添加步骤44可以显著增加各分区的大小(例如,体积增加至少约50%、100%或200%等),或者可以使各分区的体积增加小于约50%。
51.分区中的dna和/或蛋白质可以被切割(cleave),如45所示。这种切割可能是受限且选择性的。可以通过用核酸酶切割核酸和/或用蛋白酶切割蛋白质来促进对靶标序列的可及性,以确保在扩增开始时各靶标的各拷贝对于扩增试剂而言是可接近的。可以通过在相对较高的裂解温度(例如,80摄氏度)孵育之后在酶有活性的相对较低的温度(例如,37摄氏度)孵育来催化切割。可在流体添加步骤44中添加一种或多种外来(外源)裂解酶以催化切割,或它们可在分区形成时就存在(例如,包括在含样品流体中)。
52.可以在分区中进行靶标扩增,如46所示。可以扩增任何合适数量的不同靶标和/或不同靶标组,以产生对应于靶标和/或靶标组的扩增子。可以针对各靶标进行不同的扩增反应。可以通过将分区升温到固定孵育温度以进行等温扩增,或在不同温度之间热循环分区,以通过pcr(聚合酶链式反应)或lcr(连接酶链式反应)等来促进靶标扩增。不同的温度可以包括变性温度、退火温度和延伸温度;变性温度和退火/延伸温度;或之类。
53.可以在达到任何反应的扩增终点之前停止扩增反应。更具体地,各扩增反应可以在扩增的指数/线性阶段停止。然而,在指数阶段停止通常是首选,因为在这个阶段,各类型的扩增子的拷贝数能更准确且灵敏地反映个体分区中(以及这些分区中裂解的单细胞/细
胞核中)各相应靶标的初始拷贝数。
54.可以从分区收集扩增数据,如47所示。可以在任何扩增反应达到终点之前收集扩增数据,例如当各扩增反应处于扩增的指数/线性阶段时。在一些实施方式中,可以在完成相同热循环次数、任选地预定热循环次数之后收集所有扩增数据。在其它实施方式中,可以在多个时间点从分区收集扩增数据,例如在两个或更多个不同数量的热循环中的每一个完成之后(例如,如果用于区分不同靶标拷贝数的最佳循环数量是未知的)。在其它实施方式中,对于等温扩增,所有扩增数据可在等温孵育的同一时程之后或在等温孵育起始后两个或更多个不同时间点收集。
55.可以通过检测来自各分区的一个或多个信号(扩增报告信号)来收集扩增数据。可以由各分区中存在的至少一个标记物检测一个或多个信号。在一些实施方式中,由不同种类的标记物检测各信号并且代表不同的靶标或靶标组。由于扩增数据是在达到扩增终点之前收集的,因此各信号的量(幅度)会根据个体分区中各相应靶标或相应靶标组的初始拷贝数直接或反向变化。一旦发生足够的扩增以区分靶标阳性分区和靶标阴性分区,幅度变化的程度通常在扩增的指数阶段期间最大。
56.各扩增报告信号可以代表从分区检测到的光致发光,例如荧光。各分区的光致发光强度可以对应于分区(因而在分区形成时最初存在的至少一个细胞/细胞核中(若有))中的靶标或靶标组的初始拷贝数。可以检测可区分的光致发光以测量各不同靶标或靶标组的扩增。例如,可以针对不同靶标/靶标组在不同波长范围内检测来自相应不同标记物的光致发光。例如,第一种类的光致发光团可以标记第一探针或第一探针组以产生第一光致发光,并且第二种类的光致发光团可以标记第二探针或第二探针组以产生第二光致发光,其中第一光致发光和第二光致发光代表彼此不同的波长(例如,不同颜色的发射光)。
57.可以利用扩增数据确定各靶标或靶标组的一个或多个拷贝数。例如,可以将分区分配给对于至少一个扩增报告信号具有相似(聚类)值的不同组(也称为簇)。各组可以为靶标或靶标组分配不同的拷贝数,其中组内的分区被分配相同的拷贝数。拷贝数可以是整数,例如0、1、2、3等。在一些情况下,可以排除其中至少一个扩增报告信号指示该分区不接收或接收样品中的多于一个细胞/细胞核的各分区。在一些情况中,样品可能是测试样品,而测定拷贝数包括:将至少一个扩增报告信号的值与用对照样品获得的相应值进行比较,所述对照样品包括具有已知靶标或靶标组拷贝数的细胞或无细胞细胞核。
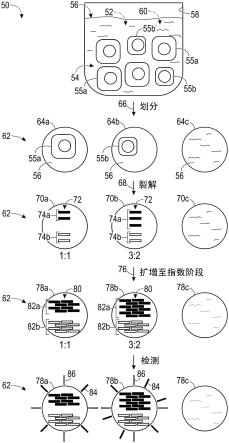
58.图2示意性地说明了分析包含细胞54和/或无细胞细胞核的样品52的示例性分区型扩增方法50的多个方面。方法50可以包括步骤41-48(参见图1)的任何合适组合,但图2中仅说明了这些步骤的子集。所述方法在此用于nipt(非侵入性产前测试),其中样品52获自妊娠女性,且细胞54包括母体细胞55a和胎儿细胞55b的混合物。样品52中的胎儿细胞55b中,通过所述方法的所述实施方式测定的两条染色体之一是三体性的,而母体细胞55a中,这两条染色体都是二体性的。
59.可以例如在容器58中制备含样品流体56。含样品流体56可以是包括样品52的水性液体,其可以包含细胞54和/或无细胞细胞核。含样品流体56也可以含有裂解/扩增试剂60。
60.可以形成分区62,如66处的箭头所示。例如,可以将含样品流体56的主体相分开,以形成体积基本相同的分区62。此处仅显示了三个说明性预裂解分区64a-c,以简化呈现的方式,并且对于方法50的各后续步骤保持相同的顺序,以区分该步骤对各不同分区的作用。
然而,可以形成任何合适数量的分区62,以获得对该方法的结果的期望水平的统计学置信度。
61.分区62可以包含不同数量的细胞/细胞核。多个分区62,由预裂解分区64c表示,其各自可不包含细胞54(或不包含无细胞细胞核)。由预裂解分区64a和64b表示的另外多个分区62各自可以包含来自样品52的个体细胞54(或无单细胞细胞核)。在一些实施方式中,另外多个分区62各自可以包含至少两个细胞/细胞核(未显示)。
62.可以裂解分区62中的细胞54和/或无细胞细胞核,如68所示,以分别从裂解前分区64a-64c产生裂解后分区70a-c。裂解可以释放和/或暴露待被检测和定量个体分区62的至少一个靶标(或靶标组(即,靶标的组))72的一个或多个拷贝。此处,一对不同的靶标(或靶标组)74a、74b显示为通过裂解后分区70a中的母体细胞55a的裂解和裂解后分区70b中的胎儿细胞55b的裂解而释放。各靶标74a、74b代表细胞54中的不同染色体。靶标74a代表在母体细胞55a中为二体性且在胎儿细胞55b中为三体性的染色体。靶标74b代表在两种类型的细胞55a、55b中都为二体性的染色体。
63.裂解后分区70c中无第一靶标74a(或第二靶标74b)的拷贝存在,其没有从含样品流体56接收任一类型的细胞(55a或55b)。第一靶标74a的两个和三个拷贝分别存在于裂解后分区70a和70b中(即,来自母体细胞55a的两个拷贝和来自胎儿细胞55b的三个拷贝)。换言之,第一靶标74a的拷贝数在裂解后分区70a、70b和70c中分别为2、3和0,因此在细胞54之间于至少两个值(即,2和3)之间变化。裂解后分区70a和70b各自包含第二靶标74b的两个拷贝。因此,在被测试的两个细胞中,第一靶标74a表现出拷贝数变化,而第二靶标74b无此表现。第一和第二靶标74a、74b的拷贝数比率在裂解后分区70a和70b下方给出,分别为1:1和3:2。
64.一个或多个扩增反应可以在裂解后分区70a-c中进行,如76所示,以分别产生扩增的分区78a-c。扩增反应产生对应于被扩增的一个或多个靶标72的扩增子80。可以对各靶标72进行不同的扩增反应以产生相应的扩增子。例如,此时,第一靶标74a和第二靶标74b的扩增分别产生两种类型的扩增子82a和82b的拷贝。在其它情况下,可以针对要确定的各拷贝数扩增靶标组。例如,扩增子82a(和/或82b)可以是对应于靶标组74a(或74b)的不同扩增子的组。
65.扩增反应可以在达到扩增终点之前停止。更具体地,各扩增反应可以在扩增的指数/线性阶段停止。然而,在指数阶段停止通常是首选,因为在这个阶段,各类型的扩增子82a、82b的拷贝数能更准确且灵敏地反映个体分区(以及单细胞/细胞核)中各相应靶标的初始拷贝数。例如,扩增的分区78a和78b中的扩增子82a与扩增子82b的比率可以与预裂解分区64a和64b的细胞54中的第一靶标74a与第二靶标74b的比率大致相同。
66.可以通过检测来自分区的一个或多个信号来收集扩增数据。此时,来自分区,任选地来自各靶标(或靶标组)74a、74b的光致发光团的一种或两种或更多种不同种类的可区分的第一和第二光致发光84、86在不同波长处被检测。从扩增的分区78a、78b检测到的第一和第二光致发光84、86的强度对应于裂解后分区70a、70b中第一和第二靶标74a、74b的初始拷贝数。从扩增的分区78b检测到的第一光致发光84的强度显著高于从扩增的分区78a检测到的情况,因为裂解后分区70b中第一靶标74a的拷贝数比裂解后分区70a高50%。相反,从扩增的分区78a、78b检测到的第二光致发光86的强度基本相同,因为第二靶标74b的拷贝数在
裂解后分区70a、70b中相同。
67.图3显示了说明示例性扩增数据的概念直方图,所述扩增数据可以从分区62收集以用于方法50中的靶标74a的扩增(也参见图2)。可以将扩增数据检测为来自各分区62的荧光强度(即,第一光致发光84)。直方图具有分成多个强度区间的荧光轴。具有落入各强度区间内的荧光强度值的分区62的数量用具有与数量成比例的高度的条来表示。
68.在直方图中可识别具有不同荧光强度的分区的四个不同组88、90、92和94。各组代表最初存在于各个分区62中的第一靶标74a的不同数量的拷贝。无拷贝组群88没有接收到细胞并且没有接收到靶标74a的拷贝。组群88可以包含比其它组群显著更多的分区,以减少多个细胞共定位到同一分区的发生率。单拷贝组群90不接收细胞并且仅接收第一靶标74a的无细胞(和无细胞核)形式的一个拷贝。单拷贝组群90中的分区频率可与样品52的质量和在分区62形成之前发生的过早细胞裂解(若有)的量有关。双拷贝组群92接收了一个母体细胞55a,其中包含两个拷贝的第一靶标74a(即,母体细胞对于提供第一个靶标74a的染色体来说是二体性的)。三拷贝组群94仅接收一个胎儿细胞55b,其包含三个拷贝的第一靶标74a(即,胎儿细胞对于提供第一靶标74a的染色体是三体性的)。
69.在一些情况下,包含一个二体性细胞(第一靶标74a的两个拷贝)的分区也可接收来自过早裂解的细胞的第一靶标的第三拷贝。这些分区在分析中引入了错误,因为它们似乎错误地代表了三体性细胞。然而,这些潜在的假阳性三体性分区的频率可以通过使用第一靶标组(来自单个染色体或来自两个、三个或更多个不同的染色体)而不是单个第一靶标来最小化。使用第一靶标组可能会增加噪声水平,因为更高百分比的分区接收一个或多个靶标,但可能会减少错误拷贝数分配的数量。
70.图4显示概念二维散点图,其说明可从分区62收集用于在方法50中扩增第一和第二靶标74a和74b的示例性扩增数据(也参见图2)。扩增数据可以作为来自各分区62的不同波长范围内的荧光强度来检测。第一光致发光84(荧光a)对应于第一靶标74a,而第二光致发光86(荧光b)对应于第二靶标74b。各分区由散点图中的一个点表示,但此处未显示各个点。相反,各可识别的点簇都表示为由围绕该簇的圆圈表示的一个组群。
71.图4的数据可以在方法50以较高细胞54与分区62比率进行时产生,从而显著百分比的分区接收两个细胞54。散点图中可鉴别出具有不同荧光强度的三组簇,各代表在形成时包含不同数量的细胞54的分区:无细胞组96、一细胞组98和二细胞组100。组内的分区的各簇可以被描述为组群。列出了各组群中第一靶标74a的拷贝数。
72.无细胞组96包含组群102、104和106。双阴组102的分区不包含第一靶标74a的拷贝和第二靶标74b的拷贝。单个拷贝组104的分区最初不包含第一靶标74a的拷贝但包含(无细胞的)第二靶标74b的一个拷贝。单拷贝组106的分区最初不包含第二靶标74b的拷贝但包含(无细胞的)第一靶标74a的一个拷贝。
73.一细胞组98由组群108和110构成。母体组群108的分区最初包含由母体细胞55a提供的第一靶标74a的两个拷贝(和第二靶标74b的两个拷贝)。胎儿组群110的分区最初包含由胎儿细胞55b提供的三个拷贝的第一靶标74a(和两个拷贝的第二靶标74b)。
74.二细胞组100由组群112、114和116构成。双母体组群112的分区最初包含两个母体细胞55a,其各自提供第一靶标74a的两个拷贝(即,2 2拷贝)。母体-胎儿组群114的分区最初包含一个母体细胞55a和一个胎儿细胞55b,分别提供第一靶标74a的两个拷贝和三个拷
贝(即,2 3个拷贝)。双胎儿组群116的分区最初包含两个胎儿细胞55b,其各自提供第一靶标74a的三个拷贝(即,3 3拷贝)。
75.iii.实施例
76.本节描述了与通过非终点扩增进行的单细胞的靶标拷贝数的分区型测定相关的本公开的附加方面。这些方面旨在用于说明并且不应限制本公开的整体范围。
77.实施例1.含有系列染料浓度的液滴的荧光
78.图5显示绘制fam荧光强度的图表,由七个分开液滴组测量,其各自预加载了不同量的fam染料(即,以实现50nm、100nm、200nm等的染料浓度,如所指示的那样)。液滴显示基本上与染料浓度成比例的荧光强度。在12倍的范围内,不同的染料浓度可以清楚地彼此区分,甚至可以分辨20%的染料浓度差异(500对比600)。
79.实施例2.来自液滴的荧光强度的扩增循环依赖性
80.图6显示了绘制fam荧光幅度的图表,所述fam荧光幅度作为pcr靶标扩增的指标,该指标随着pcr循环次数的增加,从四个不同组的液滴的个体液滴(事件)中检测到。
81.实施例3.模板拓扑对靶标扩增的作用
82.图7显示了比较使用超螺旋模板(左侧)或线性化模板(右侧)作为相同靶标序列来源的基于液滴的pcr扩增试验的一对图表。从一系列液滴(事件)中检测fam荧光的幅度,并且最高荧光的重条带(heavy band)代表已达到靶标序列扩增终点的液滴。
83.使用超螺旋模板可以看到较浅条带的条带图案,但采用线性化模板则无此现象。可能会产生这种条带图案,因为来自超螺旋模板的靶标扩增效率低下,直至模板在热循环期间被形成切口。fam幅度增加的各连续带可代表连续的更早的循环,其中超螺旋模板被形成切口,但还不足以让靶标扩增达到终点。这些数据表明,在扩增反应开始之前提供对靶标序列的高效可及性可能会产生针对各类型的分区的更紧密聚类的扩增信号,从而更准确地分配分区类型和确定拷贝数。
84.实施例4.液滴中可检测的n-ras等位基因组合
85.图8显示了从含有各种组合的野生型(wt)和突变型(g12d)n-ras靶标序列的液滴收集的扩增数据的二维荧光散点图。野生型和突变型靶标序列分别被检测为hex和fam荧光的增加。这些数据很重要,因为它们反映了基于液滴的扩增系统通过其2d荧光幅度的差异来区分包含两个可区分靶标的不同比率的液滴簇的能力。
86.iv.选择的方面
87.本节将本公开选择的方面描述为一系列带索引的段落。
88.a1.一种分析包含细胞和/或无细胞细胞核的样品的方法,所述方法包括:(a)形成分区,各分区包括样品的部分,其中所述分区的至少子集的各分区包含来自样品的仅一个细胞/细胞核;(b)裂解分区中的来自样品的细胞和/或无细胞细胞核;(c)对分区中的靶标或靶标组进行至少一个扩增反应;(d)在各扩增反应的指数/线性阶段从分区收集扩增数据;和(e)利用扩增数据确定个体分区的靶标或靶标组的拷贝数。
89.a2.如段落a1所述的方法,其中进行至少一个扩增反应包括使分区热循环预定循环次数,并且其中用于确定靶标或靶标组的拷贝数的全部扩增数据代表相同预定循环次数的完成。
90.a3.如段落a1或a2所述的方法,其中所述细胞/细胞核包括:具有针对所述靶标或
靶标组的第一拷贝数的一个或多个细胞/细胞核的第一群体,和,具有所述靶标或靶标组的第二拷贝数的一个或多个细胞/细胞核的第二群体,所述方法还包括:枚举第一群体的分区和第二群体的分区。
91.a4.如段落a3所述的方法,其中所述第一群体对于所述靶标或靶标组的拷贝数是2,并且其中所述第二群体对于所述靶标或靶标组的拷贝数是1,或拷贝数是至少3。
92.a5.如段落a4所述的方法,其中第二群体对于所述靶标或靶标组的拷贝数是3。
93.a6.如段落a1至a5中任一项所述的方法,其中收集扩增数据包括:检测来自分区的光致发光,并且其中光致发光的强度根据个体分区中靶标或靶标组的拷贝数在分区之间变化。
94.a7.如段落a6所述的方法,其中检测光致发光包括检测荧光。
95.a8.如段落a1至a7中任一项所述的方法,其中靶标或靶标组是单个靶标。
96.a9.如段落a1至a7中任一项的所述方法,其中所述靶标或靶标组是两个或更多个靶标的组。
97.a10.如段落a9所述的方法,其中收集扩增数据包括:检测光致发光,所述光致发光具有根据个体分区中的靶标组的拷贝数在分区之间变化的强度。
98.a11.如段落a9或a10所述的方法,其中所述靶标组中的各靶标代表细胞/细胞核中的相同染色体。
99.a12.如段落a1至a11中任一项所述的方法,其中所述靶标或靶标组代表细胞/细胞核中的人染色体13、18、21、x或y。
100.a13.如段落a1至a12中任一项所述的方法,其中所述靶标或靶标组是第一靶标或第一靶标组,其中进行至少一个扩增反应包括:对第二靶标或第二靶标组进行至少一个扩增反应,并且其中确定包括:确定个体分区的第二靶标或第二靶标组的拷贝数。
101.a14.如段落a13所述的方法,其中第一靶标或第一靶标组代表细胞/核中的第一染色体,并且其中第二靶标或第二靶标组代表细胞/核中不同的第二染色体,并且其中,任选地,第二染色体是在胎儿发育期间与第一染色体相比在统计学上对非整倍性更不敏感(例如,通常不敏感)的参考染色体。
102.a15.如段落a14所述的方法,其中第一染色体选自人类染色体13、18、21、x和y。
103.a16.如段落a14或a15所述的方法,其中第二染色体是人类染色体1。
104.a17.如段落a13至a16中任一项所述的方法,其中收集扩增数据包括:检测具有对应于第一靶标或第一靶标组的扩增的强度的第一光致发光和具有对应于第二靶标或第二靶标组的扩增的强度的第二光致发光。
105.a18.如段落a1至a17中任一项所述的方法,其中所述样品的细胞/细胞核包括母体细胞/细胞核和胎儿细胞/细胞核。
106.a19.如段落a1至a18中任一项所述的方法,其还包括枚举具有异常拷贝数的靶标或靶标组的细胞/细胞核。
107.a20.如段落a19所述的方法,其还包括枚举具有正常拷贝数的靶标或靶标组的细胞/细胞核。
108.a21.如段落a1至a20中任一项所述的方法,其还包括基于扩增数据鉴别形成时不包含完整细胞或细胞核的分区。
109.a22.如段落a21所述的方法,其中收集扩增数据包括:检测来自各分区的信号,其中鉴别分区包括:将来自个体分区的信号与阈值进行比较,并且其中信号小于阈值的个体分区被鉴别为形成时就已不包含来自样品的细胞或细胞核。
110.a23.如段落a1至a22中任一项所述的方法,其中样品的细胞/细胞核包括肿瘤细胞/细胞核。
111.a24.如段落a1至a23中任一项所述的方法,其中样品的细胞/细胞核包括转基因细胞/细胞核。
112.a25.如段落a24所述的方法,其中所述转基因细胞/细胞核含有两个或更多个不同拷贝数的插入的核苷酸序列,其包括靶标或靶标组。
113.a26.如段落a25的所述方法,其中转基因细胞/细胞核来自在第一时间点从转基因来源获得的第一样品,并且其中形成、裂解、进行、收集和确定采用在更晚的第二时间点从转基因来源获得的至少第二样品再进行至少一次,以测量插入的核苷酸序列(如有)的不稳定性。
114.a27.如段落a1至a26中任一项所述的方法,其中所述靶标或靶标组包括rna靶标序列或dna靶标序列。
115.a28.如段落a1至a27中任一项所述的方法,其还包括在裂解期间和/或之后使细胞/细胞核的核酸暴露于外源核酸酶。
116.a29.如段落a1至a28中任一项所述的方法,其还包括在裂解期间和/或之后将细胞/细胞核的蛋白质暴露于外源蛋白酶。
117.a30.如段落a1至a29中任一项所述的方法,其中裂解包括:使分区升温至至少50、60、70、80、85或90摄氏度。
118.a31.如段落a30所述的方法,其中升温包括:使分区升温约1-120、2-90或3-60分钟。
119.a32.如段落a30或a31所述的方法,其中升温包括使分区升温至少约1、2、3、5、10、20、30、45或60分钟。
120.a33.如段落a1至a32中任一项所述的方法,其中裂解包括使细胞/细胞核暴露于表面活性剂。
121.a34.如段落a1至a33中任一项所述的方法,其中形成分区包括:将含相同样品的流体分成被不混溶的液体包围的水性液滴。
122.a35.如段落a34所述的方法,其中不混溶的液体包括油。
123.a36.如段落a1至a35中任一项所述的方法,其中各分区包括含相同样品的第一流体的部分,所述方法任选地还包括在裂解后将第二流体添加至分区。
124.a37.如段落a36所述的方法,其中添加第二流体包括:将第二流体微注射到分区中,任选地利用电场。
125.a38.如段落a36的所述方法,其中添加第二流体包括:将第二流体移液至分开的隔室中,各隔室仅容纳一个分区,并且其中分开的隔室包括孔、纳米室或微管。
126.a39.如段落a1至a38中任一项所述的方法,其中进行至少一个扩增反应包括:进行pcr。
127.a40.如段落a1至a39中任一项所述的方法,其中分区在形成时每分区包含来自样
品的平均少于一个细胞/细胞核。
128.a41.如段落a1至a40中任一项所述的方法,其中多个分区不包含细胞/细胞核中的至少一者。
129.a42.如段落a1至a41中任一项所述的方法,其中收集扩增数据包括:检测来自分区的至少一个扩增报告信号,并且其中确定拷贝数包括:鉴别对于至少一个扩增报告信号具有聚类值的分区的组群,和,将相同拷贝数分配至该组群的各个分区。
130.a43.如段落a1至a42中任一项所述的方法,其中所述样品是测试样品,其中收集扩增数据包括:检测来自所述分区的至少一个扩增报告信号,并且其中确定拷贝数包括:比较至少一个扩增报告信号的值与采用对照样品获得的相应值,所述对照样品包含具有已知拷贝数的靶标或靶标组的细胞或无细胞细胞核。
131.a44.如段落a43所述的方法,其中已知拷贝数是整数。
132.a45.如段落a42至a44中任一段所述的方法,其中确定拷贝数包括:基于至少一个扩增报告信号鉴别分区的第一组群和第二组群,其中第一组群和第二组群分别针对靶标或靶标组被分配第一和第二拷贝数,并且其中,第一和第二拷贝数彼此不同。
133.a46.如段落a45所述的方法,其中第一和第二拷贝数是整数。
134.a47.如段落a1至a46中任一项所述的方法,其中收集扩增数据包括:检测来自分区的两个或更多个不同的扩增报告信号,其中两个或更多个不同的扩增报告信号各自代表细胞/细胞核中的不同靶标或靶标组。
135.a48.如段落a47所述的方法,其中两个或更多个扩增报告信号各自代表细胞/细胞核中的不同染色体。
136.a49.如段落a1至a48中任一项所述的方法,其中收集扩增数据包括:检测来自分区的至少一个扩增报告信号,并且其中确定拷贝数包括:排除其中至少一个扩增报告信号指示未从样品接收细胞/细胞核或从样品接收多于一个细胞/细胞核的各分区。
137.a50.如段落a42至a49中任一项所述的方法,其中各扩增报告信号被检测为来自分区的光致发光。
138.a51.如段落a1、a3-a38和a40-a50中任一项所述的方法,其中进行至少一个扩增反应包括:进行至少一个等温扩增反应。
139.a52.如段落a1至a51中任一项所述的方法,其还包括将拷贝数与至少一个阈值进行比较,并且如果比较满足一个或多个预定标准,则诊断非整倍性或癌症。
140.a53.如段落a1至a52中任一项所述的方法,其还包括将拷贝数与至少一个阈值进行比较,并且如果比较满足一个或多个预定标准,则给与治疗。
141.如在本公开中使用的术语“示例性”是指“说明性的”或“用作示例”。同样,术语“举例”的意思是“举例说明”。这两个词都不暗示可取性或优越性。
142.上述公开内容可以包括具有独立效用的多个不同的发明。虽然已经以其优选的形式公开了这些发明中的各种,但是本文所公开和阐释的本发明的特定实施方式不应被认为是限制性的,因为可以进行多种变化。本发明的主题包括本文所公开的各种元件,特征,功能和/或特性的所有新颖且非显而易见的组合和子组合。下述权利要求特别指出了新颖且非显而易见的某些组合和子组合。可以在要求本技术或相关申请的优先权的申请中要求保护以特征,功能,元素和/或特性的其他组合和子组合体现的发明。这样的权利要求,无论是
针对不同的发明还是相同的发明,以及与原始权利要求的范围相比更宽、更窄、相同或不同,也被视为包括在本公开的发明的主题内。此外,用于鉴别的元素的序数指示用语,例如第一、第二或第三,用于区分元素,且不指示这些元素的特定位置或顺序,除非另有特别说明。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。