cct6a基因及其表达产物在肠癌诊断和治疗中的应用
技术领域
1.本技术涉及生物医药的领域,尤其是涉及一种cct6a基因及其表达产物在肠癌诊断和治疗中的应用。
背景技术:
2.肠癌是目前临床上最为常见的癌症之一。肠癌具有高发病率和高致死率的特点,每年的死亡率居全世界恶性肿瘤中的第二位。由于饮食和环境因素,目前肠癌的发生和发展在世界范围内呈现出迅猛增加的趋势,而且许多肠癌患者被确诊时已是晚期阶段。
3.虽然化疗仍是肠癌临床治疗的主要手段之一,但约一半的患者在进行化疗过程中产生耐药性,降低了治疗效果和患者的生存率。因此寻找新的诊断和治疗靶点是攻克该疾病的关键。
4.人类基因组中编码蛋白的基因约2万多个,这些基因有序表达产生的蛋白在维持生命体的正常运行起重要作用,一旦这些基因表达紊乱,常导致疾病发生。研究证实蛋白基因的异常表达与肿瘤的发生,侵袭和转移密切相关。一些异常表达的蛋白能够作为癌症的基因诊断和治疗靶点,并且可以作为判断癌症类型提供新的依据。因此,寻找肠癌相关蛋白基因标志物,对于肠癌患者的诊断和治疗具有重要意义。
技术实现要素:
5.为了弥补现有方法的不足,本发明的目的之一是提供一种cct6a基因及其表达产物在肠癌诊断和治疗中的应用,用于肠癌的早期诊断的工具,相比现有的肠癌诊断方法,使用基因标志物来诊断肠癌具有及时性、灵敏性和普及性。
6.本技术提供的一种检测cct6a基因及其表达产物的产品在制备诊断肠癌的工具中的应用。
7.通过采用上述方法方案,相比现有的肠癌诊断方法,使用cct6a基因标志物来诊断肠癌具有及时性、灵敏性和普及性。
8.优选的,所述产品包括检测cct6a基因mrna水平的产品和/或检测cct6a蛋白水平的产品。
9.优选的,所述产品包括通过核酸扩增方法、核酸杂交方法、免疫检测、芯片检测或高通量测序方法,检测cct6a基因及其表达产物表达水平的产品中的至少一种。
10.优选的,所述产品包括芯片、试剂盒、试纸或高通量测序平台中的至少一种。
11.优选的,所述用核酸扩增方法诊断的产品包括至少一对特异扩增cct6a基因的引物;所述用核酸杂交方法诊断的产品包括与cct6a基因的核酸序列杂交的探针;所述用免疫检测诊断检测的产品包括与cct6a蛋白特异性结合的抗体;所述用芯片检测的产品包括蛋白芯片和基因芯片;其中,蛋白芯片包括与cct6a蛋白特异性结合的抗体,基因芯片包括与cct6a基因的核酸序列杂交的探针。
12.优选的,所述特异性扩增cct6a基因的引物序列如seq id no.3~4所示。
13.本发明的目的之二是提供一种采用上述任意一项cct6a基因和/或其表达产物的抑制剂在制备治疗肠癌的药物中的应用。
14.优选的,所述抑制剂包括抑制cct6a基因表达的试剂和/或抑制cct6a基因表达产物的试剂。
15.优选的,所述抑制cct6a基因表达的试剂包括核酸抑制和/或蛋白抑制物,能够在基因或蛋白水平上抑制cct6a基因或其编码的蛋白的表达或活性。
16.优选的,所述cct6a基因或其编码的蛋白的抑制剂选自以cct6a基因或其转录本为靶序列、且能够抑制cct6a基因表达或基因转录的干扰分子,包括shrna(小发夹rna)、sirna(小干扰rna)、dsrna、微小rna、反义核酸,或能表达或形成所述shrna、小干扰rna、dsrna、微小rna、反义核酸的构建物;或特异性与cct6a编码的蛋白结合的结合分子(如能够抑制cct6a蛋白活性的抗体或配体);所述shrna的序列如seq id no.5~8所示。
17.有益效果:
18.本发明首次发现了cct6a基因的差异表达与肠癌相关,提示该基因可用作制备诊断肠癌的工具。本发明首次通过实验证明,shrna沉默cct6a基因可抑制肠癌细胞的增殖,提示cct6a基因可作为药物靶点用于治疗肠癌的药物。
附图说明
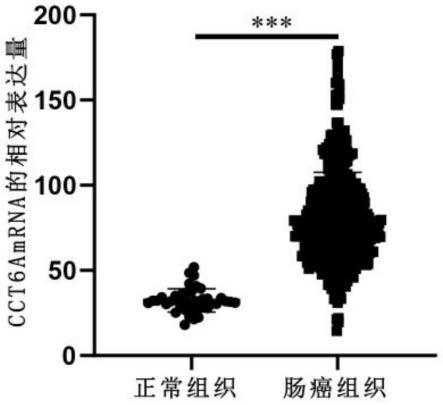
19.图1显示利用tcga高通量测序数据分析cct6a基因在正常组织和肠癌组织中的表达差异;
20.图2显示利用肠癌临床信息评估cct6a基因的表达高低与患者预后生存的相关性;
21.图3显示与正常肠上皮细胞ncm460相比,cct6a的mrna和蛋白表达水平在肠癌细胞(ht29和hct116和lovo)中均上调;
22.图4和图5显示shrna对cct6a基因的mrna水平的干扰效率;
23.图6和图7显示cct6a基因干扰后蛋白水平的变化;
24.图8和图9显示抑制cct6a基因对肠癌细胞增殖的影响。
具体实施方式
25.以下结合附图和实施例对本发明作进一步详细说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条例,或者按照制造厂商所建议的条件。本领域技术人员应当理解,测定基因表达的手段不是本发明的重要方面。
26.本发明经过广泛而深入的研究,分析肠癌标本中肿瘤组织和癌旁组织的基因表达,发现了cct6a基因在肠癌患者中高表达,用shrna沉默该基因能显著抑制肠癌细胞的增殖,提示cct6a基因可用于肠癌细胞的鉴别,评估人群肠癌的患病风险,为肠癌的诊断和治疗提供了一种新途径。
27.分子标志物
[0028]“分子标志物”是其在组织或细胞中的表达水平与正常或健康细胞或组织的表达水平相比发生改变的任何基因或蛋白。
[0029]
本发明并不局限于对本发明的标志物基因的任何特定变体的基因表达进行定量。
作为非限制性的实例,标志物基因可具有seq id no.3~4指定的核苷酸序列和氨基酸序列。
[0030]
实施例1
[0031]
验证cct6a基因在肠癌病人样本中的差异表达的方法,包括以下步骤:
[0032]
1、获取数据:数据来源为cct6a基因的rna-seq数据来自癌症基因组图谱(the cancer genome atlas,tcga),样本量为正常组织:肠癌组织=41:458。
[0033]
2、数据处理,将来自tcga的数据通过graphpad prism 8软件计算,生成cct6a基因在正常组织和肠癌组织中的对比图。
[0034]
3、结果分析,得到如图1所示,与正常组织相比,cct6a基因在肠癌组织中表达水平上调,差异具有统计学意义(p《0.05),*代表重要程度:*p《0.05,**p《0.01,***p《0.001,提示cct6a基因表达水平的产品可用于制备诊断肠癌的工具中。
[0035]
实施例2
[0036]
评估cct6a基因对肠癌患者愈后影响的方法,包括以下步骤:
[0037]
1、获取数据,肠癌患者的临床信息来自tcga,基于患者的生存时间、生存事件和cct6a基因的表达进行单因素生存分析。
[0038]
2、数据处理,根据生物标志物的中位表达水平,将患者样本分为高表达和低表达两组,通过kaplan-meier生存图对两组患者进行比较。
[0039]
3、结果分析,如图2所示,cct6a基因高表达与总体生存(overall survival,os)呈负相关。p值《0.05表示具有统计学意义,提示cct6a可用于评估肠癌患者的预后。
[0040]
实施例3
[0041]
验证细胞系中cct6a的差异表达的方法,包括以下步骤:
[0042]
1、细胞培养,人正常肠上皮细胞ncm460用含有10%胎牛血清和1%青霉素-链霉素的rpmi-1640培养液,置于37℃、5%co2的孵箱中培养。人coad细胞(ht29,hct116和lovo)用含有10%胎牛血清和1%青霉素-链霉素mccoy’s 5a培养液,置于37℃、5%co2的孵箱中培养。2-3天更换新鲜培养基,使用含0.25%乙二胺四乙酸(ethylene diamine tetraacetic acid,edta)的胰蛋白酶消化传代。
[0043]
2、rna提取和实时定量pcr
[0044]
1)用qiagen的细胞rna提取试剂盒进行总rna的提取;
[0045]
2)用紫外分光光度仪测定rna浓度和纯度,goscript reverse transcription system试剂盒将rna逆转录成cdna;
[0046]
3)引物设计:
[0047]
参照基因gapdh的引物序列:
[0048]
正向引物:5
′‑
ctgggctacactgagcacc-3
′
(seq id no.1)
[0049]
反向引物:5
′‑
aagtggtcgttgagggcatg-3
′
(seq id no.2)
[0050]
cct6a基因的引物序列:
[0051]
正向引物:5
′‑
gcagcagaagtaggcgtatgg-3
′
(seq id no.3)
[0052]
反向引物:5
′‑
tcgcatgatctcatcaaccaag-3
′
(seq id no.4)
[0053]
4)采用sybr green方法进行qpcr实验,反应体系如下:
[0054]
sybr green聚合酶链式反应体系10ul
[0055]
双向引物1μl
[0056]
cdna模板2μl
[0057]
ddh2o 7μl5)反应条件:95℃10min,(95℃15s,60℃60s)
×
40个循环,60℃60s,以gapdh作为参照基因,δδct法进行相对定量。
[0058]
3、蛋白提取和免疫印迹
[0059]
1)收集处于对数生长期的细胞,用含有pmsf的ripa裂解液裂解10分钟提取总蛋白,
[0060]
bca方法测定蛋白浓度;
[0061]
2)10%的聚丙烯酰胺对等量的蛋白(30ug)进行sds-page电泳,将蛋白转至pvdf膜并用5%的脱脂牛奶封闭,然后将膜孵育在gapdh或cct6a的一抗中4℃过夜,tbst洗膜3次,并用辣根过氧化物酶标记的二抗孵育1小时,tbst洗膜3次,用ecl试剂曝光条带;
[0062]
3)将蛋白条带的灰度值使用image j软件进行分析,以gapdh为内参,将cct6a蛋白条带的灰度值进行归一化处理,结果数据都是以平均值
±
标准差的方式来表示,采用graphpad prism 8统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p《0.05时具有统计学意义。
[0063]
4、结果分析,如图3所示,与正常肠上皮细胞ncm460相比,cct6a的mrna和蛋白表达水平在肠癌细胞(ht29、hct116和lovo)中均上调,差异具有统计学意义(p《0.05),与肠癌组织样本的rna-seq数据分析结果一致。
[0064]
实施例4
[0065]
验证抑制cct6a基因表达的方法,包括以下步骤:
[0066]
1shrna干扰设计合成
[0067]
针对cct6a的shrna干扰序列:
[0068]
cct6a干扰1号:
[0069]
正义链:5
′‑
gatcgaagggcaccatgaagatgctcctcgaggagcatcttcatggtgccctttttttg-3
′
(seq id no.5)
[0070]
反义链:5
′‑
aattcaaaaaaagggcaccatgaagatgctcctcgaggagcatcttcatggtgcccttc-3
′
(seq id no.6)
[0071]
cct6a干扰2号:
[0072]
正义链:5
′
gatcgaacgtgtcattagagtatgagctcgagctcatactctaatgacacgtttttttg-3
′
(seq id no.7)
[0073]
反义链:5
′
aattcaaaaaaacgtgtcattagagtatgagctcgagctcatactctaatgacacgttc-3
′
(seq id no.8)
[0074]
以上序列由生工生物工程(上海)股份有限公司合成。
[0075]
2、载体构建
[0076]
1)酶切
[0077]
反应所需试剂:
[0078]
plvx-shrna1质粒10ul
[0079]
所需内切酶反应缓冲液 2ul
[0080]
所需限制性内切核酸酶1ul
[0081]
ddh2o 37ul
[0082]
将加好的ep管置于37℃保温1-2h。
[0083]
2)电泳检测
[0084]
将酶切产物进行琼脂糖凝胶电泳,检测酶切是否成功。通过切胶回收去除非目的片段,然后用omega胶回收试剂盒进行纯化。
[0085]
3)载体与目的基因连接
[0086]
连接体系:
[0087]
载体0.5ul
[0088]
dna片段1.5ul
[0089]
连接酶 1ul
[0090]
连接缓冲液 1ul
[0091]
ddh2o 6ul
[0092]
置于恒温箱,22℃,保温15min。
[0093]
4)转化
[0094]
将上述连接产物进行转化实验,涂板培养,37℃,12-16h。
[0095]
5)单克隆检测
[0096]
取1.5ml ep管10支,给每支管中加500μl培养液,然后用接种环(或白枪头)挑单克隆,置于摇床培养6小时。通过pcr鉴定阳性菌落,并测序进一步确认。
[0097]
6)质粒提取
[0098]
根据单克隆检测结果,继续培养含有阳性质粒的菌。使用omega质粒提取试剂盒提取相应菌液的质粒。
[0099]
3、慢病毒包装
[0100]
慢病毒包装采用三质粒系统,用lipofectamine
tm
2000根据说明书进行293t细胞转染。转染48h后收集细胞上清液,于4℃,4000g离心10min,除去细胞碎片,浓缩纯化病毒液,并测定病毒滴度。
[0101]
4、干扰cct6a基因的肠癌稳定细胞系构建
[0102]
待细胞长到40-60%融合度,加入病毒浓缩液和polybrene8ug/ml,24h后换液继续培养,48h后进行puro筛选,连续筛选7d后存活下来的细胞为cct6a沉默的稳定细胞系。
[0103]
5、cct6a干扰效率检测
[0104]
利用qpcr实验和免疫印迹实验检测shrna的干扰效率,步骤同实施例3。
[0105]
6、结果分析,如图6和图7所示,与对照组相比,干扰组的cct6a表达量明显降低,差异具有统计学意义(p《0.05)。
[0106]
实施例5
[0107]
结晶紫检测细胞增殖实验
[0108]
1、用4%多聚甲醛固定细胞10-20分钟,然后用蒸馏水漂洗两次,每次2-5分钟。加入适当体积的结晶紫染色液,室温孵育10-30分钟,用蒸馏水洗涤两次,每次2分钟,image j软件进行染色分析。
[0109]
2、结果分析,如图8所示如图5所示,与对照组相比,cct6a干扰显著抑制细胞增殖,差异具有统计学意义(p《0.05)。
[0110]
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通方法人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
