用于治疗癌症的vs-6063与ch5126766的组合
背景技术:
1.可靠的证据表明粘着斑激酶(fak),即ptk2(一种细胞质的非受体酪氨酸激酶)在细胞-基质信号转导通路中发挥着重要作用(clark and brugge 1995,science 268:233-239),并且它的异常活化与肿瘤转移潜能的增加有关(owens等人,1995,cancer research 55:2752-2755)。fak最初是在被v-src转化的细胞中鉴定出的一种高度酪氨酸磷酸化的125kda蛋白质。fak在人体中由ptk2基因编码。随后发现fak是一种定位于粘着斑的酪氨酸激酶,所述粘着斑是培养细胞与其底层基质之间的接触点以及是强烈的酪氨酸磷酸化的位点。fak被磷酸化,并由此在响应细胞外基质(ecm)与整合素的结合时而被激活。最近,研究表明fak mrna水平的增加伴随着肿瘤的侵袭性转化和fak表达的减弱(通过使用反义寡核苷酸),这诱导了肿瘤细胞的凋亡(xu等人,1996,cell growth and diff.7:413-418)。除了在大多数组织类型中表达外,还在大多数人类癌症中发现fak水平升高,例如在高侵袭性转移灶中,包括甲状腺癌、前列腺癌、宫颈癌、结肠癌、直肠癌、口腔上皮癌、卵巢癌和乳腺癌。因此,用于在受试者中抑制fak的化合物、化合物组合、组合物和方法是所期望的。
2.ras/raf/mek/erk信号转导途径的组成部分也代表了治疗异常细胞生长的机会,例如,癌症。
3.wo 2015/120289公开了一种治疗患有癌症的受试者的方法,该方法包括向受试者组合施用治疗有效量的fak抑制剂(例如vs-6063)与mek抑制剂(例如gdc-0623、考比替尼、曲美替尼、哌吗色替、azd6244),从而治疗受试者。
4.wo 2014/059095和br j cancer.2019 may;120(10):975-981涉及使用包含特定fak抑制剂和特定mek抑制剂(曲美替尼)的组合治疗癌症。
技术实现要素:
5.fak抑制剂(例如,vs-6063)和raf/mek双重抑制剂(例如,ch5126766)的组合可以增强肿瘤特异性细胞毒性淋巴细胞的产生和有效性,并为更有效地治疗本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))提供了有前景的方法。vs-6063或其药学上可接受的盐(fak抑制剂)可与ch5126766或其药学上可接受的盐(raf/mek双重抑制剂)组合使用以治疗本文所述的疾病或病症,例如,异常细胞生长(例如,本文所述的癌症)。
6.因此,本文提供了一种特定的组合(例如,本文所述的组合(例如,fak抑制剂与raf/mek双重抑制剂的组合)),其可用于例如在受试者(例如,人类)中治疗异常细胞生长,例如癌症(例如,具有ras突变的癌症)。
7.本文描述了治疗患有癌症的受试者的方法,该方法包括向受试者组合施用治疗有效量的vs-6063或其药学上可接受的盐(fak抑制剂)与ch5126766或药学上可接受的盐(raf/mek双重抑制剂),从而治疗受试者,其中癌症是具有ras突变的癌症。在一些实施方案中,ras突变是kras突变或nras突变。
8.本文描述了治疗患有癌症的受试者的方法,该方法包括向受试者组合施用治疗有
效量的vs-6063或其药学上可接受的盐与raf/mek双重抑制剂,其中raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。在一些实施方案中,癌症是由ras、braf或nf-1的突变引起的。在一些实施方案中,癌症是具有ras突变的癌症。在其它方面,癌症具有kras突变或nras突变。
9.本文描述了vs-6063或其药学上可接受的盐与raf/mek双重抑制剂的组合的用途,用于治疗癌症,其中raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。在一些实施方案中,癌症是由ras、braf或nf-1的突变引起的。在一些实施方案中,癌症具有ras突变。在其它方面,癌症具有kras突变或nras突变。
10.本文描述了治疗患有癌症的受试者的方法,该方法包括向受试者组合施用治疗有效量的ch5126766或其药学上可接受的盐与fak抑制剂,其中,fak抑制剂是vs-6063或其药学上可接受的盐。在一些实施方案中,癌症是由ras、braf或nf-1的突变引起的。在一些实施方案中,癌症具有ras突变。在其它方面,癌症具有kras突变或nras突变。
11.本文描述了ch5126766或其药学上可接受的盐与fak抑制剂的组合的用途,用于治疗癌症,其中fak抑制剂是vs-6063或其药学上可接受的盐。在一些实施方案中,癌症是由ras、braf或nf-1的突变引起的。在一些实施方案中,癌症具有ras突变。在其它方面,癌症具有kras突变或nras突变。
12.本文描述了治疗患有癌症的受试者的方法,该方法包括向受试者组合施用治疗有效量的raf/mek双重抑制剂与fak抑制剂,其中所述raf/mek双重抑制剂是ch5126766或其药学上可接受的盐,以及所述fak抑制剂为vs-6063或其药学上可接受的盐。
13.本文描述了raf/mek双重抑制剂与fak抑制剂的组合的用途,用于治疗癌症,其中所述raf/mek双重抑制剂为ch5126766或其药学上可接受的盐,以及所述fak抑制剂为vs-6063或其药学上可接受的盐。
14.在一些实施方案中,癌症是由ras、braf或nf-1的突变引起的。
15.在一些实施方案中,癌症选自卵巢癌、肺癌、结肠癌,和胰腺癌。在一些实施方案中,癌症是卵巢癌。在一些实施方案中,卵巢癌是低级别浆液性卵巢癌。在一些实施方案中,癌症是肺癌。在其它实施方案中,癌症是结肠癌。在一些实施方案中,癌症是胰腺癌。在一些实施方案中,癌症选自低级别浆液性卵巢癌、肺癌、结肠癌和胰腺癌。
16.在一些方面,所述raf/mek双重抑制剂(例如,ch5126766)每周给药两次。在一些方面,所述fak抑制剂(例如,vs-6063)每天给药两次。在其它方面,所述fak抑制剂(例如,vs-6063)每天给药一次。在一些实施方案中,所述raf/mek双重抑制剂(例如ch5126766)和所述fak抑制剂(例如vs-6063)给药至少三周。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)和fak抑制剂(例如,vs-6063)独立地周期性给药,其中连续给药三周然后停药一周。在一些实施方案中,所述raf/mek双重抑制剂(例如,ch5126766)和所述fak抑制剂(例如,vs-6063)同时周期性给药,其中连续给药三周然后停药一周。
17.在一些方面,raf/mek双重抑制剂(例如,ch5126766)以约0.5mg至约10mg的剂量给药。在进一步的实施方案中,raf/mek双重抑制剂(例如,ch5126766)以约4mg的剂量给药。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)以3.2mg的剂量给药。在一些实施方案中,fak抑制剂(例如,vs-6063)以约100mg至约400mg的剂量给药。在一些实施方案中,fak抑制剂(例如,vs-6063)以约100mg至约500mg的剂量给药。在进一步的实施方案中,fak
抑制剂(例如,vs-6063)以约200mg至约500mg的剂量给药。在其它实施方案中,fak抑制剂(例如,vs-6063)以约200mg至约600mg的剂量给药。在一些方面,raf/mek双重抑制剂(例如,ch5126766)以约0.5mg至约10mg的剂量给药,以及fak抑制剂(例如,vs-6063)以约100mg至约400mg的剂量给药。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)以约4mg的剂量每周两次给药,以及fak抑制剂(例如,vs-6063)以约200mg的剂量每天两次给药。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)以3.2mg的剂量每周两次给药,以及fak抑制剂(例如,vs-6063)以200mg的剂量每天两次给药。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)以约4mg的剂量每周两次给药,以及fak抑制剂(例如,vs-6063)以约400mg的剂量每天两次给药。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)以3.2mg的剂量每周两次给药,以及fak抑制剂(例如,vs-6063)以400mg的剂量每天两次给药。
18.发明详述
19.除其它事项外,本文还描述了用于治疗异常细胞生长(例如,癌症)的方法,该方法包括施用fak抑制剂和raf/mek双重抑制剂,其中所述fak抑制剂是vs-6063或其药学上可接受的盐,以及所述raf/mek双重抑制剂为ch5126766或其药学上可接受的盐。
20.治疗和给药方法
21.本文所述的方法涉及用fak抑制剂与raf/mek双重抑制剂组合治疗患有本文所述疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))的受试者(例如,人类受试者),其中,所述fak抑制剂为vs-6063或其药学上可接受的盐,以及所述raf/mek双重抑制剂为ch5126766或其药学上可接受的盐。如本文所用,“组合”给药是指在受试者患有疾病的过程中向受试者递送两种(或更多种)不同的治疗,例如,在受试者被诊断患有所述疾病之后且在该病症已经被治愈或消除或因其它原因停止治疗之前,递送两种或更多种治疗。在一些实施方案中,当第二种治疗开始递送时第一种治疗的递送仍在进行,因此在施用方面存在重叠。这在本文中有时被称为“同时”或“并行递送”。在其它实施方案中,一种治疗的递送在另一种治疗的递送开始之前结束。在任一情况的一些实施方案中,治疗由于组合施用而更有效。例如,第二治疗更有效,例如,与在不施用第一治疗的情况下施用第二治疗相比,组合施用使用更少的第二治疗可以观察到相同的效果,或者第二治疗在更大程度上减轻了症状,或者针对第一治疗也观察到类似的情况。在一些实施方案中,与在不存在另一种治疗时递送一种治疗相比,本发明的递送使得与病症相关的症状或其它参数减少得更多。两种治疗的效果可以是部分相加的、完全相加的或大于相加的。递送可以是在递送第二种治疗时,仍然可检测到递送的第一种治疗的效果。
22.方案中,该方法包括在施用raf/mek双重抑制剂(例如,ch5126766)之前施用fak抑制剂(例如,vs-6063)。在一些实施方案中,该方法包括在施用raf/mek双重抑制剂(例如,ch5126766)之后施用fak抑制剂(例如,vs-6063)。在一些实施方案中,该方法包括在施用raf/mek双重抑制剂(例如,ch5126766)的同时施用fak抑制剂(例如,vs-6063)。在一些实施方案中,fak抑制剂是vs-6063(pf-04554878;defactinib)或其药学上可接受的盐。在一些实施方案中,raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。
23.肿瘤微环境
24.本文所述化合物的组合还涉及调节或调理受试者(例如,患有本文所述癌症的受
试者)中的肿瘤微环境的方法。如本文所用,“肿瘤微环境”是指肿瘤存在的细胞环境,包括周围的血管、免疫细胞、成纤维细胞、骨髓来源的炎性细胞、淋巴细胞、信号分子和细胞外基质(ecm)。肿瘤与周围微环境密切相关并不断地相互作用。肿瘤可以通过释放细胞外信号、促进肿瘤血管生成和诱导外周免疫耐受来影响微环境,而微环境中的免疫细胞可以影响癌细胞的生长和进化。
25.如本文所用,术语“免疫抑制性细胞”是指有助于或促进免疫抑制性肿瘤微环境的细胞。肿瘤微环境中存在免疫抑制细胞群,本文也称为“肿瘤相关免疫抑制性细胞”,增加了肿瘤对免疫反应的抵抗力,导致肿瘤保护、肿瘤逃逸和/或肿瘤转移。除非以某种方式加以对抗,否则肿瘤相关免疫抑制性细胞会降低免疫介导的抗癌治疗的功效。有大量的肿瘤相关的免疫抑制性细胞,其包括骨髓来源的抑制性细胞(mdsc)和调节性t细胞。
26.在一些实施方案中,本文所述化合物的组合增强了肿瘤特异性细胞毒性淋巴细胞或抗肿瘤毒性t细胞的有效性。在一些实施方案中,本文所述fak抑制剂(例如,vs-6063)靶向肿瘤微环境中的免疫抑制性细胞。在一些实施方案中,本文所述fak抑制剂(例如,vs-6063)通过致密促结缔组织增生基质的肿瘤-基质调节和/或fak调节的促炎和/或促纤维化细胞因子分泌作为t细胞浸润的屏障。在一些实施方案中,braf抑制激活基质细胞(例如,癌症活化的成纤维细胞、细胞粘附因子),导致fak依赖性癌症存活信号传导(例如,在黑素瘤中)。
27.异常细胞生长
28.本文所述方法涉及治疗受试者(例如,人类受试者)中的异常细胞生长。如本文所用且除非另有说明,异常细胞生长,是指不依赖于正常调节机制的细胞生长(例如,失去接触抑制)。这包括:(1)肿瘤细胞(肿瘤)的异常生长,通过例如,表达突变的酪氨酸激酶或受体酪氨酸激酶的过表达而增殖;(2)其它增殖性疾病的良性和恶性细胞的异常生长,例如,发生异常的酪氨酸激酶活化的疾病;(3)任何肿瘤的异常生长,例如,通过受体酪氨酸激酶而增殖的疾病;(4)任何肿瘤的异常生长,例如,通过异常的丝氨酸/苏氨酸激酶活化而增殖的疾病;(5)其它增殖性疾病的良性和恶性细胞的异常增长,例如,发生异常的丝氨酸/苏氨酸激酶活化的疾病。异常细胞生长可以是指上皮细胞生长(例如,癌、腺癌);间叶细胞生长(例如,肉瘤(例如,平滑肌肉瘤,尤文氏肉瘤));造血细胞生长(例如,淋巴瘤、白血病、骨髓发育不良(例如,癌前病变));或其它(例如,间皮瘤和其它起因不明的肿瘤)细胞。
29.在一些实施方案中,该方法在治疗非血液恶性肿瘤中是有效的。在一些实施方案中,该方法可有效治疗胰腺癌、非小细胞肺癌(nsclc)、小细胞肺癌(sclc)、间皮瘤、乳腺癌和卵巢癌。在一个实施方案中,乳腺癌是三阴性乳腺癌(例如,不表达雌激素受体、孕酮受体和her2/neu基因的乳腺癌)。在一个实施方案中,肺癌是非小细胞肺癌(nsclc),例如,kras突变的nsclc。在一个实施方案中,卵巢癌是晚期卵巢癌(例如,晚期卵巢癌或转移性卵巢癌)。在一个实施方案中,卵巢癌是低级别浆液性卵巢癌。在一个实施方案中,低级别浆液性卵巢癌是kras突变的低级别浆液性卵巢癌。在一个实施方案中,该方法可有效治疗间皮瘤(例如,恶性胸膜间皮瘤,例如,可手术切除的恶性胸膜间皮瘤)。在一些实施方案中,癌症是胰腺癌。
30.赘生性疾病
31.异常细胞生长可以是指赘生性疾病。“赘生性疾病”是以具有自主生长或复制能力
的细胞为特征的疾病或病症,例如,以增殖性细胞生长为特征的异常状态或状况。由异常细胞生长或分裂导致的异常组织块,或“赘生物”,可以是良性的、癌变前的(原位癌)或恶性的(癌症)。
32.示例性的赘生疾病包括:癌、肉瘤、转移性疾病(例如,源自前列腺、结肠、肺、乳腺和肝脏的肿瘤)、造血性赘生疾病(例如,白血病、转移性肿瘤)。使用化合物治疗可以是以有效改善赘生性疾病的至少一种症状(例如细胞增殖减少、肿瘤质量减少等)的用量进行。
33.癌症
34.在一些实施方案中,本发明的方法可用于治疗癌症,包括例如实体瘤、软组织肿瘤和转移瘤。在一些实施方案中,本发明的方法可用于治疗mek-erk途径被激活的癌症。本发明公开的方法也可用于治疗非实体癌。示例性实体瘤包括各种器官系统的恶性肿瘤(例如,肉瘤、腺癌,和癌),所述器官系统为例如肺、乳腺、淋巴、胃肠道(例如,结肠),以及泌尿生殖(例如肾、尿路上皮或睾丸肿瘤)道、咽部、前列腺和卵巢。示例性腺癌包括结肠直肠癌、肾细胞癌、肝癌(例如,肝细胞癌)、非小细胞肺癌、胰腺癌(例如,转移性胰腺癌)和小肠癌。
35.癌症还可以包括子宫癌(子宫内膜癌、子宫赘生物、宫颈癌等)、胆源性癌和胆道癌(胆管上皮癌、胆管癌、胆囊癌等)。
36.癌症可以是原发性肿瘤,即,位于肿瘤生长起始的解剖部位。癌症也可以是转移性的,即,至少出现在不同于肿瘤生长起始的解剖部位的第二个解剖部位。癌症可以是复发性癌症,即,在治疗之后,以及在未检测到癌症的一段时间后复发的癌症。复发性癌症可以在解剖学上位于原始肿瘤的局部,例如在解剖学上靠近原始肿瘤;或位于原始肿瘤的区域内,例如位于原始肿瘤附近的淋巴结中;或位于远离原始肿瘤处,例如在解剖学上远离原始肿瘤的区域。
37.癌症还可以有ras突变,这意味着癌症是由ras基因(hras、nras或kras)的突变引起的。癌症还可以有kras突变,这意味着癌症是由kras基因的突变引起的。癌症还可以有nras突变,这意味着癌症是由nras基因的突变引起的。在一些实施方案中,癌症是由ras基因(例如,kras基因)的突变引起的卵巢癌。在一些实施方案中,癌症是低级别卵巢癌或粘液性卵巢癌,两者均由ras基因(例如,kras基因)的突变引起。在一些实施方案中,癌症是由ras基因(例如,kras基因)的突变引起的肺癌。在一些实施方案中,癌症是由ras基因(例如,kras基因或nras基因)的突变引起的结肠癌。在一些实施方案中,癌症是由ras基因(例如,kras基因)的突变引起的胰腺癌。
38.癌症还可以包括,例如,上皮癌、乳腺癌、肺癌、胰腺癌、结肠直肠癌(例如,转移性结肠直肠癌,例如,转移性kras突变型结肠直肠癌)、前列腺癌、头颈癌、黑色素瘤、急性髓细胞性白血病和胶质母细胞瘤。示例性乳腺癌包括,三阴性乳腺癌、基底样乳腺癌、claudin-low型乳腺癌、浸润性、炎性、化生性,以及对治疗有抗性的晚期her-2阳性或er阳性癌症。
39.在癌症中突变的基因的例子还包括egfr、fgfr、alk、ros1、pi3k、nf-1、braf、hras、kras和nras。所述癌症优选为kras突变和/或nras突变的癌症,更优选为kras突变或nras突变的结肠癌,或kras突变的实体癌(优选卵巢癌、肺癌(尤其是非小细胞肺癌)、结肠癌和胰腺癌)。
40.其它癌症包括脑癌、腹部癌、食道癌、胃肠癌、神经胶质瘤、肝癌、舌癌、神经母细胞瘤、骨肉瘤、卵巢癌、视网膜母细胞瘤、威尔姆氏瘤、多发性骨髓瘤、皮肤癌、淋巴瘤、血液和
骨髓癌(例如晚期血液恶性肿瘤、白血病,例如急性骨髓性白血病(例如原发性或继发性)、急性成淋巴细胞性白血病、急性淋巴细胞性白血病、t细胞白血病、血液恶性肿瘤、晚期骨髓增生性疾病、骨髓增生异常综合征、复发性或难治性多发性骨髓瘤、晚期骨髓增生性疾病)、视网膜癌、膀胱癌、宫颈癌、肾癌、子宫内膜癌、脑膜瘤、淋巴瘤、皮肤癌、子宫癌、肺癌、非小细胞肺癌、鼻咽癌、神经母细胞瘤、实体瘤、血液系统恶性肿瘤、鳞状细胞癌、睾丸癌、甲状腺癌、间皮瘤、脑癌、外阴癌、肉瘤、肠癌、口腔癌、内分泌癌、唾液腺癌、精母细胞性精原细胞瘤、散发性髓样甲状腺癌、非增殖性睾丸细胞癌、与恶性肥大细胞相关的癌症、非霍奇金淋巴瘤和弥漫性大b细胞淋巴瘤。
41.示例性癌症包括急性成淋巴细胞性白血病、急性骨髓性白血病、肾上腺皮质癌、艾滋病相关淋巴瘤、艾滋病相关恶性肿瘤、肛门癌、星形细胞瘤、胆管癌、肝外癌、膀胱癌;骨癌、骨肉瘤/恶性纤维组织细胞瘤、脑干胶质瘤、脑肿瘤、脑干胶质瘤、小脑星形细胞瘤、脑星形细胞瘤/恶性胶质瘤、室管膜瘤、髓母细胞瘤、幕上原始神经外胚层肿瘤、视觉通路和下丘脑胶质瘤;乳腺癌;支气管腺瘤/类癌、类癌瘤,胃肠道类癌瘤;肾上腺皮质癌;胰岛细胞癌;未知原发性癌;原发性中枢神经系统淋巴瘤;小脑星形细胞瘤、脑星形细胞瘤/恶性胶质瘤、宫颈癌;慢性淋巴细胞性白血病;慢性髓性白血病;慢性骨髓增生性疾病;腱鞘透明细胞肉瘤;结肠癌;结肠直肠癌;皮肤t细胞淋巴瘤;子宫内膜癌;室管膜瘤、上皮癌、卵巢癌;食道癌;尤文氏肿瘤家族食道癌;颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤;肝外胆管癌;眼癌、视网膜母细胞瘤;胆囊癌;胃部(胃)癌;胃部(胃)癌;胃肠道类癌瘤;生殖细胞肿瘤,颅外;生殖细胞肿瘤,性腺外;生殖细胞肿瘤,卵巢;妊娠滋养层肿瘤;胶质瘤;视觉通路和下丘脑胶质瘤;毛细胞白血病;头颈癌;肝细胞(肝)癌;霍奇金淋巴瘤;霍奇金淋巴瘤;妊娠霍奇金淋巴瘤;下咽癌;下丘脑和视觉通路胶质瘤;胰岛细胞癌(内分泌胰腺);卡波西肉瘤;肾癌;喉癌;喉癌;急性淋巴细胞性白血病;急性淋巴细胞性白血病;急性髓性白血病;急性髓性白血病;慢性淋巴细胞性白血病;慢性髓性白血病;毛细胞白血病;唇癌和口腔癌;肝癌;非小细胞肺癌;小细胞肺癌;成淋巴细胞性白血病,淋巴细胞性白血病,慢性;艾滋病相关淋巴瘤;中枢神经系统(原发性)淋巴瘤;皮肤t细胞淋巴瘤;霍奇金淋巴瘤;霍奇金淋巴瘤;妊娠霍奇金淋巴瘤;非霍奇金淋巴瘤;非霍奇金淋巴瘤;妊娠非霍奇金病;原发性中枢神经系统淋巴瘤;巨球蛋白血症,华氏(waldenstrom’s)巨球蛋白血症;男性乳腺癌;成人恶性间皮瘤;恶性间皮瘤;恶性胸腺瘤;髓母细胞瘤、默克尔细胞癌;恶性间皮瘤;隐匿性原发性转移性鳞状颈癌;多发性内分泌赘生性综合征、多发性骨髓瘤/浆细胞肿瘤;蕈样真菌病;骨髓增生异常综合征;慢性髓性白血病;骨髓性白血病,多发性骨髓瘤;慢性骨髓增生性疾病;鼻腔和鼻窦癌;鼻咽癌;鼻咽癌;神经母细胞瘤;非霍奇金淋巴瘤,妊娠期非霍奇金淋巴瘤;非小细胞肺癌;口腔癌;口腔和唇癌;口咽癌;骨肉瘤/恶性骨纤维组织细胞瘤;卵巢癌;卵巢上皮癌;卵巢生殖细胞肿瘤;卵巢低度恶性潜能肿瘤;胰腺癌;胰腺癌;胰岛细胞性胰腺癌;鼻窦和鼻腔癌;甲状旁腺癌;阴茎癌;嗜铬细胞瘤;松果体和幕上原始神经外胚层肿瘤;脑垂体瘤;浆细胞新生物/多发性骨髓瘤;胸膜肺母细胞瘤;妊娠和乳腺癌;妊娠和霍奇金淋巴瘤;妊娠和非霍奇金淋巴瘤;原发性中枢神经系统淋巴瘤;原发性肝癌;原发性肝癌;前列腺癌;直肠癌;肾细胞(肾)癌;肾细胞癌;肾盂和输尿管,移行细胞癌;视网膜母细胞瘤;横纹肌肉瘤;唾液腺癌;唾液腺癌;肉瘤,尤文氏肿瘤家族;卡波西肉瘤;肉瘤(骨肉瘤)/骨恶性纤维组织细胞瘤;肉瘤,横纹肌肉瘤;软组织肉瘤;肉瘤,软组织;塞扎里综合症(sezary syndrome);皮肤
癌;皮肤癌;皮肤癌(黑色素瘤);默克尔细胞皮肤癌(skin carcinoma);小细胞肺癌;小肠癌;软组织肉瘤;软组织肉瘤;转移性隐匿性原发性鳞状颈癌;胃(胃部)癌;胃(胃部)癌;幕上原始神经外胚层肿瘤;皮肤t细胞淋巴瘤;睾丸癌;胸腺瘤;恶性胸腺瘤;甲状腺癌;甲状腺癌;肾盂和输尿管移行细胞癌;妊娠期滋养层肿瘤;未知原发部位癌症;输尿管和肾盂,移行细胞癌;尿道癌;子宫肉瘤;阴道癌;视觉通路和下丘脑胶质瘤;外阴癌;华氏巨球蛋白血症;和维尔姆斯瘤(wilms’tumer)。上述癌症的转移也可以采用本文所述的方法进行治疗。
42.在一些实施方案中,肿瘤是造血和淋巴组织的肿瘤或影响血液、骨髓、淋巴和淋巴系统的肿瘤。血液恶性肿瘤包括急性成淋巴细胞性白血病、急性髓性白血病、慢性淋巴细胞性白血病、慢性髓性白血病、急性单核细胞性白血病、其它白血病、霍奇金淋巴瘤和非霍奇金淋巴瘤。
43.在一些实施方案中,肿瘤是实体瘤。在一些实施方案中,实体瘤是局部晚期或转移性的。在一些实施方案中,实体瘤在标准治疗后是顽固性的(例如,抗性的)。
44.本文所述的方法可以减少、改善或完全消除疾病和/或其相关症状,以防止其恶化,减缓进展速度,或将疾病在最初被消除后的复发率降至最低(即,避免复发)。合适的剂量和治疗方案可以根据所使用的具体化合物和/或药物组合物以及化合物和/或药物组合物的递送方式而变化。在一些实施方案中,该方法以统计学显著的方式增加了用本文所述的组合治疗的受试者的平均生存期、增加了无进展生存期的平均长度和/或降低了复发率。
45.在一些实施方案中,所述癌症是肺癌(例如,非小细胞肺癌(nsclc),例如,kras突变nsclc;转移性癌症)、骨癌、胰腺癌、皮肤癌、头颈癌、子宫癌、卵巢癌(例如,不可切除的低级别卵巢癌,晚期或转移性卵巢癌),直肠癌、肛门区癌、胃癌、结肠癌、乳腺癌(例如,三阴性乳腺癌(例如,不表达雌激素受体、孕激素受体和her2/neu的基因的乳腺癌)、子宫癌、输卵管癌、子宫内膜癌、宫颈癌、阴道癌、外阴癌、霍奇金病、食道癌、小肠癌、内分泌系统癌、甲状腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道癌、阴茎癌、前列腺癌、慢性或急性白血病、淋巴细胞性淋巴瘤、膀胱癌、肾癌(例如,维尔姆斯瘤、横纹肌瘤;肾瘤(例如,中胚层肾瘤))或输尿管、肾细胞癌、肾盂癌、中枢神经系统(cns)肿瘤、原发性cns淋巴瘤、脊髓轴肿瘤、脑干胶质瘤、垂体腺瘤、间皮瘤(例如,恶性胸膜间皮瘤,例如,手术可切除的恶性胸膜间皮瘤)或一种或多种前述癌症的组合。在一些实施方案中,癌症是卵巢癌、胰腺癌、非小细胞肺癌、头颈癌。在一些实施方案中,癌症是转移性的。在一些实施方案中,异常细胞生长是局部复发的(例如,受试者患有局部复发的疾病,例如癌症)。
46.本发明的方法考虑治疗有效量的fak抑制剂与raf/mek双重抑制剂的单次和多次组合施用,其中fak抑制剂是vs-6063或其药学上可接受的盐,以及raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。组合,例如本文所述的组合,例如fak抑制剂(例如,vs-6063)与raf/mek双重抑制剂(例如,ch5126766)的组合可以根据受试者病症的性质、严重度和程度而定期施用。在一些实施方案中,如本文所述的组合,例如fak抑制剂与raf/mek双重抑制剂的组合,以单剂量施用,其中,fak抑制剂是vs-6063或其药学上可接受的盐,以及raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。在一些实施方案中,如本文所述的组合,例如fak抑制剂与raf/mek双重抑制剂组合,以多剂量施用,其中,fak抑制剂是vs-6063或其药学上可接受的盐,以及raf/mek双重抑制剂是ch5126766或其药学上可接受的盐。在一些实施方案中,本文所述的组合的治疗有效量,例如fak抑制剂(例如,vs-6063)与
raf/mek双重抑制剂(例如,ch5126766)的组合的治疗有效量可以每隔一段时间定期口服施用(例如,每1、2、3、4、5或6天,或每1、2、3、4、5、6、7、8或9周,或每1、2、3、4、5、6、7、8、9个月或更长时间,给药1、2、3、4、5、6、7、8、9、10次或更多次)。在一些实施方案中,如本文所述的治疗有效量的组合为例如定期口服施用的fak抑制剂(例如,vs-6063)(例如,每天两次)和定期口服施用的raf/mek双重抑制剂(例如,ch5126766)(例如,每周两次)的组合。在一些实施方案中,治疗有效量的本文所述的组合,为例如每天一次口服施用的fak抑制剂(例如,vs-6063)与定期口服施用的raf/mek双重抑制剂(例如,ch5126766)(例如,每周两次)的组合。在一些实施方案中,如本文所述的治疗有效量的组合为例如每天两次口服施用的fak抑制剂(例如,vs-6063)和定期口服施用的raf/mek双重抑制剂(例如,ch5126766)(例如,每周三次)的组合。vs-6063和ch5126766可以各自为药学上可接受的盐的形式。
47.在一些实施方案中,对于本文所述的组合,例如,定期口服施用的fak抑制剂(例如,vs-6063)(例如,每天两次)和以预先确定的时间间隔口服施用的raf/mek双重抑制剂(例如,ch5126766)(例如,每周两次)组合,持续施用三周,然后停药一周(或一个间隔期内不给予fak抑制剂(例如,vs-6063)或raf/mek双重抑制剂(例如,ch5126766)),然后周期性重复(例如,施用三周、停药一周、施用三周、停药一周等)。在一些实施方案中,ch5126766或其药学上可接受的盐,和vs-6063或其药学上可接受的盐各自给药至少三周。在一些实施方案中,ch5126766或其药学上可接受的盐,和vs-6063或其药学上可接受的盐,各自给药至少4周。在一些实施方案中,ch5126766或其药学上可接受的盐,和vs-6063或其药学上可接受的盐,各自给药至少五周。在一些实施方案中,ch5126766或其药学上可接受的盐,和vs-6063或其药学上可接受的盐,各自以给药4周然后至少停药1周的形式周期给药。在其它实施方案中,ch5126766或其药学上可接受的盐和vs-6063或其药学上可接受的盐,各自以给药五或六周然后停药一或两周的形式周期给药。
48.vs-6063或其药学上可接受的盐的一周停药的时间安排,和ch5126766或其药学上可接受的盐的一周停药的时间安排可以同时或不同。在一个优选的实施方案中,vs-6063或其药学上可接受的盐的一周停药的时间安排和ch5126766或其药学上可接受的盐的一周停药的时间安排是同时的。
49.在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)每周口服一次。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)每周口服两次。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)每周口服三次。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)每周口服四次。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)每周口服五次。在其它实施方案中,raf/mek双重抑制剂(例如,ch5126766)每天口服一次。在其它实施方案中,raf/mek双重抑制剂(例如ch5126766)每天口服两次。ch5126766可以是药学上可接受的盐的形式。
50.在一些实施方案中,fak抑制剂(例如,vs-6063)每天口服两次。在一些实施方案中,fak抑制剂(例如,vs-6063)每天口服一次。在一些实施方案中,fak抑制剂(例如,vs-6063)以约100mg至约400mg的剂量施用。在一些实施方案中,fak抑制剂(例如,vs-6063)以约100mg至约500mg的剂量施用。在一些实施方案中,fak抑制剂(例如,vs-6063)以约200mg至约500mg的剂量施用。在一些实施方案中,fak抑制剂(例如,vs-6063)以约200mg至约600mg的剂量施用。在一些实施方案中,fak抑制剂(例如vs-6063)以约200mg的剂量施用。在
一些实施方案中,fak抑制剂(例如,vs-6063)以约400mg的剂量施用。应当理解,fak抑制剂(例如,vs-6063)可以在本文所述的任何周期性时间段以一定剂量给药。例如,fak抑制剂(例如,vs-6063)可以以每天两次约200mg的剂量给药。fak抑制剂(vs-6063)可以以每天两次约400mg的剂量给药。
51.在一些实施方案中,raf/mek双重抑制剂(例如ch5126766)以约0.5mg至约10mg的剂量给药。在其它实施方案中,raf/mek双重抑制剂(例如ch5126766)以约0.5mg至约7mg的剂量给药。在其它实施方案中,raf/mek双重抑制剂(例如ch5126766)以约0.5mg至约5mg的剂量给药。在其它实施方案中,raf/mek双重抑制剂以约1mg至约10mg的剂量给药。在一些实施方案中,raf/mek双重抑制剂(例如,ch5126766)以约4mg的剂量给药。在其它实施方案中,raf/mek双重抑制剂(例如ch5126766)以3.2mg的剂量给药。应当理解,raf/mek双重抑制剂(例如ch5126766)可以以本文所述的任何周期性时间模式以一定剂量给药。例如,raf/mek双重抑制剂(例如ch5126766)可以约0.5mg至约10mg的剂量给药,每周两次。raf/mek双重抑制剂(例如ch5126766)可以约4mg的剂量给药,每周两次。双重raf/mek抑制剂(例如,ch5126766)可以3.2mg的剂量给药,每周两次。ch5126766可以是药学上可接受的盐的形式。
52.如本文所述,fak抑制剂(例如vs-6063)可以与raf/mek双重抑制剂(例如ch5126766)一起施用。例如,ch5126766或其药学上可接受的盐可以约0.5mg至约10mg的剂量给药,vs-6063或其药学上可接受的盐可以约100mg至约400mg的剂量给药。ch5126766或其药学上可接受的盐可以约3mg至约5mg的剂量给药,vs-6063或其药学上可接受的盐可以约100mg至约400mg的剂量给药。ch5126766或其药学上可接受的盐可以约3mg至约5mg的剂量每周两次给药,vs-6063或其药学上可接受的盐可以约100mg至约400mg的剂量每天两次给药。ch5126766或其药学上可接受的盐可以约4.0mg的剂量每周两次给药,vs-6063或其药学上可接受的盐可以约200mg的剂量每天两次给药。ch5126766或其药学上可接受的盐可以约3.2mg的剂量每周两次给药,vs-6063或其药学上可接受的盐可以约200mg的剂量每天两次给药。ch5126766或其药学上可接受的盐可以约3.2mg每周两次给药,vs-6063或其药学上可接受的盐可以约400mg的剂量每天两次给药。
53.在一些实施方案中,根据以下步骤施用双重raf/mek抑制剂(例如,ch5126766),包括:
54.(a)施用raf/mek双重抑制剂每周施用两次,持续3周,
55.(b)在接下来的1周暂停施用所述化合物或盐,和
56.(c)随后重复步骤(a)和(b),至少一次。
57.在一些实施方案中,raf/mek双重抑制剂(例如ch5126766)由以下(r1)或(r2)的方式施用:
58.(r1)
59.(a1)
60.(a1a)raf/mek双重抑制剂(例如,ch5126766)以每次施用4mg的剂量每周施用两次,持续3周,
61.(a1b)raf/mek双重抑制剂(例如,ch5126766)的施用在接下来的1周暂停(即,以施用三周、停药一周为基础,共4周为1个周期),以及
62.(a1c)随后重复步骤(a1a)和(a1b)至少一次;或者
63.(r2)
64.(a2)首先:
65.(a2a)raf/mek双重抑制剂(例如,ch5126766)以每次施用4mg的剂量每周施用两次,持续3周,
66.(a2b)raf/mek双重抑制剂(例如,ch5126766)的施用在接下来的1周暂停,以及
67.(a2c)随后重复步骤(a2a)和(a2b),至少一次;
68.(b2)以下:
69.(b2a)raf/mek双重抑制剂(例如,ch5126766)以每次施用3.2mg的剂量每周施用两次,持续3周,
70.(b2b)raf/mek双重抑制剂(例如,ch5126766)的施用在接下来的1周暂停,以及
71.(b2c)随后重复步骤(b2a)和(b2b),至少一次;
72.在一些实施方案中,例如,将(i)由步骤(a)和(b)组成的4周的周期,和(ii)由步骤(a1a)和(a1b)组成的4周的周期重复两次(8周)至90次(大概6年11个月),以及更具体地,例如,重复8次(32周)至18次(72周)。即使预先确定了要重复的周期数,也可以基于医生或兽医的判断,例如,根据受试者的状况来改变周期数。此外,基于医生或兽医的判断,例如,根据例如受试者的状况,甚至可以在周期期间停止施用。
73.在一些实施方案中,例如,将由步骤(a2a)和(a2b)组成的4周的周期重复两次(8周)至45次(大概3年5个月),以及更具体地,例如重复8次(32周)至18次(72周)。即使预先确定了要重复的周期数,也可以基于医生或兽医的判断,例如根据受试者的状况来改变周期数。此外,基于医生或兽医的判断,例如,根据例如受试者的状况,甚至可以在周期期间停止施用。
74.在一些实施方案中,例如,将由步骤(b2a)和(b2b)组成的4周的周期重复两次(8周)至45次(大概3年5个月),以及更具体地,例如重复8次(32周)至18次(72周)。即使预先确定了要重复的周期数,也可以基于医生或兽医的判断,例如根据受试者的状况来改变周期数。此外,基于医生或兽医的判断,例如,根据受试者的状况,甚至可以在周期期间停药。
75.在一些实施方案中,raf/mek双重抑制剂(例如ch5126766)每次施用的剂量优选为3.2mg或4mg。剂量更优选为4mg,可减至3.2mg。fak抑制剂(例如vs-6063)每次施用的剂量优选为200mg或400mg。剂量更优选为200mg,可增加至400mg。
76.raf/mek双重抑制剂(例如,ch5126766)与fak抑制剂(例如,vs-6063)联合使用的时间段可以基于医生或兽医的判断(例如,根据受试者的状况)来确定。此外,根据医生或兽医的判断,例如,根据患者的状况,可以停止施用raf/mek双重抑制剂(例如,ch5126766)和fak抑制剂(例如,vs-6063)中的任一个或两个。
77.化合物
78.除其它事项外,本文所述的方法包括向患有癌症的受试者组合施用fak抑制剂与raf/mek双重抑制剂,其中fak抑制剂是vs-6063,或其药学上可接受的盐,以及raf/mek双重抑制剂是ch5126766,或其药学上可接受的盐。
79.vs-6063
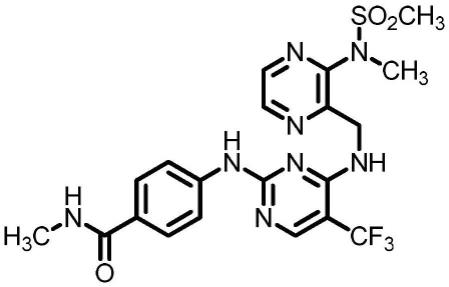
80.示例性fak抑制剂包括vs-6063或其药学上可接受的盐(例如,vs-6063盐酸盐)。vs-6063和相关化合物也被公开,例如,美国专利no.7,928,109,其内容通过引用并入本文。
vs-6063也称为defactinib和pf-04554878,具有以下结构:
[0081][0082]
在一些实施方案中,vs-6063可以形成药学上可接受的盐(例如,vs-6063盐酸盐)。在一些实施方案中,vs-6063或其药学上可接受的盐以5、10、11、12、12.5、13、14、15、20、25、30、35、40、45、50、55、60%w/w或更高的量存在于组合物中。在一些实施方案中,vs-6063或其药学上可接受的盐以约5至约60%w/w、约5至约50%w/w、约10至约50%w/w,或约10至约40%w/w的量存在于组合物中。
[0083]
ch5126766
[0084]
ch5126766是一种raf/mek双重抑制剂,也称为ro5126766。本文包括使用ch5126766或其药学上可接受的盐的方法。ch5126766(游离碱)由下式表示:
[0085][0086]
用于本发明的ch5126766或其药学上可接受的盐优选为ch5126766的钾盐。ch5126766的钾盐优选为,例如下式表示的盐:
[0087][0088]
例如,ch5126766及其药学上可接受的盐公开在wo 2007/091736和wo 2009/014100中并且可以根据这些出版物中描述的方法制备。
[0089]
癌症组合治疗
[0090]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐,与ch5126766或其药学上可接受的盐的组合)与额外的疗法(例如,癌症治疗)一起施用。在一个实施方案中,一种或多种化合物的混合物或药物组合物可以与本文所述的组合(例如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐)组合施用。在另一个实施方案中,一种或多种化合物或组合物(例如,药物组合物)可以与本文所述的组合(例如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)组合施用,用于治疗各种疾病,包括例如癌症。
[0091]
在不同的实施方案中,包含本文所述的化合物或药物组合物的组合疗法可以是指
(1)药物组合物,其包含一种或多种化合物与本文所述的组合(例如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)的组合;以及(2)本文所述的一种或多种化合物或药物组合物与本文所述的组合(如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)共同施用,其中,所述本文所述的化合物或药物组合物没有配制在相同的组合物中。在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐,与ch5126766或其药学上可接受的盐的组合)与额外的治疗(例如,额外的癌症治疗)一起施用。在一些实施方案中,额外的治疗(例如,额外的癌症治疗)可以同时(例如,在同一时间)、在相同或分开的组合物中、或依次施用。依次施用是指在施用额外的治疗(例如,化合物或疗法)之前(例如,就在小于5、10、15、30、45、60分钟前;在1、2、3、4、6、8、10、12、16、20、24、48、72、96或更多小时前;在4、5、6、7、8、9或更多天前;在1、2、3、4、5、6、7、8或更多周前)施用一种治疗。第一种和第二种化合物或疗法的施用顺序也可以颠倒。在一些实施方案中,fak抑制剂(例如,vs-6063)和raf/mek双重抑制剂(例如,ch5126766)以不同的周期性时间间隔施用。例如,fak抑制剂(例如,vs-6063)可以每天一次或每天两次施用,而raf/mek双重抑制剂(例如,ch5126766)每周两次、每周一次或每三或四天施用一次。
[0092]
本发明的方法可以与一种或多种额外的疗法(例如,癌症治疗,例如,手术、额外的药物或治疗剂)组合使用或施用以治疗所提及的病症/疾病。所述额外的疗法(例如,癌症治疗,例如,本文所述的药物或治疗剂)可以在同一制剂或单独的制剂中施用。如果以单独的制剂施用,本发明的化合物可以与其它药物依次或同时施用。
[0093]
除了能够与一种或多种额外的疗法(例如,癌症治疗,例如手术、额外的药物或治疗剂)组合施用之外,本发明的方法还可以同时(作为组合的制剂)或依次施用以达到预期的效果。这在每种化合物的治疗性质不同的情况下是尤其可取的,使得两种药物的组合作用提供了改善的治疗结果。
[0094]
示例性癌症治疗包括,例如,化学疗法、靶向疗法如抗体疗法、免疫疗法和激素疗法。下面提供了这些治疗中的每一种的实例。
[0095]
化学疗法
[0096]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)与化学疗法一起施用。化学疗法是用可以破坏癌细胞的药物治疗癌症。与靶向治疗相反,“化学疗法”通常是指影响快速分裂细胞的细胞毒性药物。化疗药物以各种可能的方式干扰细胞分裂,例如,干扰dna的复制或新形成的染色体的分离。大多数形式的化学疗法把所有快速分裂的细胞作为攻击目标,并且对癌细胞没有特异性,尽管一定程度的特异性可能来自许多癌细胞无法修复dna损伤,而正常细胞通常可以。
[0097]
用于癌症化学疗法的化学治疗剂的实例包括,例如,抗代谢物(例如,叶酸、嘌呤和嘧啶衍生物)和烷化剂(例如,氮芥类、亚硝基脲类、铂类、烷基磺酸盐、肼类、三氮烯类、氮丙啶类、纺锤体毒素、细胞毒剂、拓扑异构酶抑制剂等)。示例性药剂包括阿柔比星、放线菌素;alitretinon、六甲蜜胺、氨基蝶呤、氨基酮戊酸、氨柔比星、安吖啶、阿那格雷、三氧化二砷、天冬酰胺酶、阿曲生坦、贝洛替康、贝沙罗汀、苯达莫司汀(endamstine)、博来霉素、硼替佐米、白消安、喜树碱、卡培他滨、卡铂、卡波醌、卡莫氟、卡莫司汀、塞来昔布、苯丁酸氮芥、氮芥、顺铂、克拉屈滨、氯法拉滨、克瑞他酶、环磷酰胺、阿糖胞苷、达卡巴嗪、放线菌素d、柔红
霉素、地西他滨、地美可辛、多西他赛、多柔比星、乙法昔罗、伊利司莫、依沙芦星、依诺他滨、表柔比星、雌莫司汀、依托格鲁、依托泊苷、氟尿苷、氟达拉滨、氟尿嘧啶(5fu)、福莫司汀、吉西他滨、gliadel植入物、羟基脲(hydroxycarbamide)、羟基脲(hydroxyurea)、伊达比星、异环磷酰胺、伊立替康、伊洛福芬、伊沙匹隆、拉洛他赛、亚叶酸钙、多柔比星脂质体、柔红霉素脂质体、洛尼达明、洛莫司汀、硫蒽酮、甘露舒凡、马索罗酚、美法仑、巯基嘌呤、美司钠、甲氨蝶呤、氨基酮戊酸甲酯、二溴甘露醇、米托胍腙、米托坦、丝裂霉素、米托蒽醌、奈达铂、尼莫司汀、奥利默森、奥马西他辛、奥他赛(ortataxel)、奥沙利铂、紫杉醇、培门冬酶、培美曲塞、喷司他丁、吡柔比星、匹杉琼、普卡霉素、卟吩姆钠、泼尼莫司汀、丙卡巴肼、雷替曲塞、雷莫司汀、鲁比替康、沙帕他滨、司莫司汀、塞西马集(sitimagene ceradenovec)、赛特铂(strataplatin)、链脲菌素、他拉泊芬、替加氟-尿嘧啶、替莫泊芬、替莫唑胺、替尼泊苷、替司他赛、睾内酯、戊四硝酯(tetranitrate)、噻替派、噻唑呋林、硫鸟嘌呤、替吡法尼、拓扑替康、曲贝替定、三亚胺醌、曲他胺、三铂(triplatin)、维甲酸、曲奥舒凡、曲磷胺、乌拉莫司汀、戊柔比星、维替泊芬、长春碱、长春新碱、长春地辛、长春氟宁、长春瑞滨、伏立诺他、佐柔比星,和本文所述的其它细胞生长抑制剂或细胞毒剂。
[0098]
由于某些药物联合使用比单独使用效果更好,因此通常同时或依次给予两种或更多种药物。通常,两种或更多种化疗剂被用作联合化疗。在一些实施方案中,化疗剂(包括联合化疗)可以与本文所述的组合(例如,fak抑制剂与raf/mek双重抑制剂的组合)联合使用。
[0099]
靶向治疗
[0100]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐,与ch5126766或其药学上可接受的盐的组合)与靶向治疗一起施用。靶向治疗包括使用特异性针对癌细胞的失调蛋白的试剂。小分子靶向治疗药物通常是癌细胞内突变、过表达或其它关键蛋白质上的酶结构域的抑制剂。突出的例子是酪氨酸激酶抑制剂,如阿昔替尼、博舒替尼、西地尼布、达沙替尼(desatinib)、埃罗替尼、伊马替尼、吉非替尼、拉帕替尼、来他替尼、尼罗替尼、司马沙尼、索拉非尼、舒尼替尼和凡德他尼,以及细胞周期蛋白依赖性激酶抑制剂,如阿伏西地和塞利西利。单克隆抗体疗法是另一种策略,其中,治疗剂是特异性结合癌细胞表面上的蛋白质的抗体。示例包括典型地用于乳腺癌的抗her2/neu抗体曲妥珠单抗以及典型地用于各种b细胞恶性肿瘤的抗cd20抗体利妥昔单抗和托西莫单抗。其它示例性抗体包括ctuximab、帕尼单抗、曲妥珠单抗、阿伦单抗、贝伐单抗、依决洛单抗和吉妥珠单抗。示例性融合蛋白包括阿柏西普和地尼白介素2(denileukin diftitox)。靶向治疗也可以涉及小肽作为“归巢装置”,它可以结合细胞表面受体或影响肿瘤周围的细胞外基质。如果核素在细胞附近衰变,则附着在这些肽(例如,rgd)上的放射性核素最终会杀死癌细胞。这种疗法的一个例子包括
[0101]
免疫疗法
[0102]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)与免疫疗法一起施用。癌症免疫疗法是指旨在诱导患者的自身免疫系统对抗肿瘤的多种治疗策略。产生针对肿瘤的免疫反应的现代方法包括针对膀胱癌使用il-2和囊内bcg免疫疗法,以及在患有肾细胞癌、黑色素瘤、多发性骨髓瘤、慢性髓性白血病和毛细胞白血病的受试者中使用干扰素和其它细胞因子来诱导免疫反应。
[0103]
同种异体基因造血干细胞移植可以被认为是免疫疗法的一种形式,因为供体的免疫细胞通常会以移植物抗肿瘤效应攻击肿瘤。在一些实施方案中,免疫治疗剂可以与本文所述的组合(例如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)一起使用。
[0104]
在一些实施方案中,免疫治疗剂是抑制免疫检查点阻断途径的化合物(例如,配体、抗体)。癌症免疫疗法是指利用免疫系统来治疗癌症。用于治疗癌症的三种主要免疫疗法包括基于细胞的、基于抗体的和细胞因子疗法。所有免疫疗法都利用癌细胞在其表面上展示的细微不同的结构(例如,分子结构、抗原、蛋白质、分子、糖类),这些结构可以被免疫系统检测到。癌症免疫治疗(即,抗肿瘤免疫疗法或抗肿瘤免疫治疗剂)包括免疫检查点抗体(例如,pd-1抗体、pd-l1抗体、pd-l2抗体、ctla-4抗体、tim3抗体、lag3抗体、tigit抗体)和癌症疫苗(即,抗肿瘤疫苗)。
[0105]
在一些实施方案中,免疫治疗剂是抗ctla-4抗体(例如,易普利姆玛、替西利姆单抗)、抗tim3、抗lag3或抗tigit。在一些实施方案中,免疫治疗剂是抗pd-1配体(例如pd-li(例如,b7-hi或cd274);或pd-l2(例如,b7-dc或cd273))。在一些实施方案中,免疫治疗剂是抗pd-1抗体(例如,抗pd-1或抗pd-ll,(例如,纳武单抗(即,mdx-1106、bms-936558、ono-4538);ct-011;amp-224;帕姆单抗;匹地利珠单抗(pidilizumab);或mk-3475)。在一些实施方案中,免疫治疗剂是抗pd-l1抗体(例如,bms936559(即,mdx-1105);medi4736;msb0010718c(阿维单抗);或mpdl-3280a)。在一些实施方案中,免疫治疗剂是基于细胞的疗法。在一些实施方案中,基于细胞的疗法是car-t疗法。在一些实施方案中,免疫治疗剂是共刺激抗体(例如,抗4-1bb、抗ox40、抗gitr、抗cd27、抗cd40)。在一些实施方案中,该方法还包括施用额外的化学治疗剂或放射疗法。在一些实施方案中,该方法还包括施用细胞毒剂。在一些实施方案中,细胞毒剂是吉西他滨或紫杉醇(例如,白蛋白结合型紫杉醇)。在一些实施方案中,免疫治疗剂是共刺激抗体(例如,抗4-1bb、抗ox40、抗gitr、抗cd27、抗cd40)。
[0106]
抗炎剂
[0107]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)可以与抗炎剂一起施用。抗炎剂包括非甾体抗炎剂(例如,水杨酸盐(阿司匹林(乙酰水杨酸)、二氟尼柳、双水杨酯)、丙酸衍生物(布洛芬、萘普生、非诺洛芬、酮洛芬、氟比洛芬、奥沙普秦、洛索洛芬)、乙酸衍生物(吲哚美辛、舒林酸、依托度酸、酮咯酸、双氯芬酸、萘丁美酮)、烯醇酸(昔康类)衍生物(吡罗昔康、美洛昔康、替诺昔康、屈昔康、氯诺昔康、伊索昔康)、芬那酸衍生物(芬那酸类)(甲芬那酸、甲氯芬那酸、氟芬那酸、托芬那酸)、选择性cox-2抑制剂(昔布类)(塞来昔布)、磺苯胺类(尼美舒利)。甾体类(例如,氢化可的松(皮质醇)、醋酸可的松、强的松、泼尼松龙、甲泼尼龙、地塞米松、倍他米松、曲安西龙、倍氯米松、醋酸氟氢可的松、醋酸脱氧皮质酮、醛固酮)。
[0108]
镇痛剂
[0109]
在一些实施方案中,本文所述的组合(例如vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)可以与镇痛剂一起施用。镇痛剂包括阿片类(例如,吗啡、可待因、羟考酮、氢可酮、双氢吗啡、哌替啶、丁丙诺啡、曲马朵、文拉法辛)、对乙酰氨基酚和非甾体抗炎剂(例如,水杨酸盐类(阿司匹林(乙酰水杨酸)、二氟尼柳、双水杨酯)、丙酸衍生物(布洛芬、萘普生、非诺洛芬、酮洛芬、氟比洛芬、奥沙普秦、洛索洛芬)、乙酸衍生
物(吲哚美辛、舒林酸、依托度酸、酮咯酸、双氯芬酸、萘丁美酮)、烯醇酸(昔康类)衍生物(吡罗昔康、美洛昔康、替诺昔康、屈昔康、氯诺昔康、伊索昔康)、芬那酸衍生物(芬那酸类)(甲芬那酸、甲氯芬那酸、氟芬那酸、托芬那酸)、选择性cox-2抑制剂(昔布类)(塞来昔布)、磺苯胺类(尼美舒利)。
[0110]
止吐剂
[0111]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)可以与止吐剂一起施用。止吐剂包括5-ht3受体拮抗剂(多拉司琼(anzemet)、格拉司琼(kytril,sancuso)、昂丹司琼(zofran)、托烷司琼(navoban)、帕洛诺司琼((aloxi)、米氮平(remeron))、多巴胺拮抗剂(多潘立酮、奥氮平、氟哌利多、氟哌啶醇、氯丙嗪、异丙嗪、丙氯拉嗪、甲氧氯普胺(reglan)、阿立必利、丙氯拉嗪(compazine,stemzine,buccastem,stemetil,phenotil))、nk1受体拮抗剂(阿瑞匹坦(emend)、抗组胺药(赛克力嗪、苯海拉明(benadryl)、茶苯海明(gravol,dramamine)、美克洛嗪(bonine,antivert)、异丙嗪(pentazine,phenergan,promacot)、羟嗪)、苯并二氮杂环庚三烯类(劳拉西泮、咪达唑仑)、抗胆碱能类(东莨菪碱)、类固醇类(地塞米松)。
[0112]
激素疗法
[0113]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)与激素疗法一起施用。一些癌症的生长可以通过提供或阻断某些激素来抑制。激素敏感性肿瘤的常见例子包括某些类型的乳腺癌和前列腺癌。去除或阻断雌激素或睾酮通常是一种重要的额外治疗。在某些癌症中,激素激动剂例如孕激素的施用可能对治疗有益。在一些实施方案中,激素治疗剂可与本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)组合使用。
[0114]
放射治疗
[0115]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)可以与定向能量或粒子,或与放射性同位素治疗联合使用,例如放射疗法,例如放射肿瘤科,用于治疗增殖性疾病,例如癌症,例如与癌症干细胞相关的癌症。本发明的方法可以与定向能量或粒子,或放射性同位素治疗同时或依次施用于受试者。例如,本发明的方法可以在定向能量或粒子,或放射性同位素治疗或其组合之前、期间或之后施用。定向能量或粒子疗法可包括全身辐照、局部身体辐照或点辐照。定向能量或粒子可能源自加速器、同步加速器、核反应、真空管、激光,或源自放射性同位素。该疗法可以包括外束放射疗法、远距放射疗法、近距放射疗法、密封源放射疗法、全身放射性同位素疗法,或非密封源放射疗法。治疗可以包括摄入或放置在放射性同位素附近,所述放射性同位素为例如放射性碘、钴、铯、钾、溴、氟、碳。外部束辐射可包括暴露于定向α粒子、电子(例如,β粒子)、质子、中子、阳电子,或光子(例如,无线电波、毫米波、微波、红外线、可见光、紫外光、x射线,或γ-射线光子)。辐射可以定向至需要治疗的受试者的任何部分。
[0116]
手术
[0117]
在一些实施方案中,本文所述的组合(例如,vs-6063或其药学上可接受的盐与ch5126766或其药学上可接受的盐的组合)可以与手术(例如手术探查、介入、活检)联合使用,用于治疗增殖性疾病,例如癌症,例如与癌症干细胞相关的癌症。本发明的方法可以与手术同时或依次施用于受试者。例如,本发明的方法可以在手术之前(术前)、期间或之后
(术后)施用,或它们的组合。fak抑制剂(例如,vs-6063)可以在手术之前(术前)施用,而raf/mek双重抑制剂(例如,ch5126766)可以在手术期间或之后(术后)施用。可选地,raf/mek双重抑制剂(例如,ch5126766)可以在手术之前(术前)施用,而fak抑制剂(例如,vs-6063)可以在手术期间或之后(术后)施用。手术可以是在此期间收集一个或多个细胞用于进一步分析的活检。活检可以例如用手术刀、针、导管、内窥镜、抹刀或剪刀来完成。活检可以是切除活检、切开活检、核心活检或针活检,例如针吸活检。手术可能涉及切除疑似或确定为癌变的局部组织。例如,该程序可能涉及切除癌性病变、肿块、息肉或痣。该过程可能涉及切除大量的组织,例如乳房、骨骼、皮肤、脂肪或肌肉。该程序可能涉及去除器官或结节的部分或全部,例如肺、咽喉、舌、膀胱、子宫颈、卵巢、睾丸、淋巴结、肝、胰腺、脑、眼、肾、胆囊、胃、结肠、直肠或肠道。在一个实施方案中,癌症是乳腺癌,例如三阴性乳腺癌,以及手术是乳房切除术或病灶切除术。
[0118]
一线治疗
[0119]
在一些实施方案中,本文描述了一种治疗患有癌症的人类受试者的方法,其中,受试者一线治疗(例如,针对癌症的一线治疗)已经失败(例如,复发、不敏感、没有或几乎没有从中受益)。本发明还描述了治疗患有癌症的人类受试者的方法,其中,本发明的方法与额外的药物一起施用。在一些实施方案中,额外的药物是癌症的一线疗法。
[0120]
一线疗法通常是针对疾病(例如,本文所述的癌症)给予的第一种治疗。它通常是一组标准治疗的一部分,例如手术后化疗和放疗。当单独使用时,一线治疗通常是公认的最佳治疗方法。如果它不能治愈疾病或引起严重的副作用,则可以添加或替代使用其它治疗方法。一线治疗也称为诱导治疗、初级疗法和初级治疗。
[0121]
例如,一线治疗(例如霍奇金淋巴瘤)可能包括:adcetris(本妥昔单抗)、adriamycin pfs(盐酸多柔比星)、adriamycin rdf(盐酸多柔比星)、ambochlorin(苯丁酸氮芥)、amboclorin(苯丁酸氮芥)、blenoxane(博来霉素)、博来霉素、本妥昔单抗、苯丁酸氮芥、clafen(环磷酰胺)、环磷酰胺、cytoxan(环磷酰胺)、达卡巴嗪、盐酸多柔比星、dtic-dome(达卡巴嗪)、leukeran(苯丁酸氮芥)、linfolizin(苯丁酸氮芥)、洛莫司汀、matulane(盐酸丙卡巴肼)、neosar(环磷酰胺)、盐酸丙卡巴肼、velban(硫酸长春碱),velsar(硫酸长春碱),硫酸长春碱,vincasar pfs(硫酸长春新碱)和硫酸长春新碱。
[0122]
在一些实施方案中,的一线疗法(例如,霍奇金淋巴瘤)包括治疗剂的组合施用,例如本文所述的治疗剂。例如,该组合可以包含盐酸多柔比星(adriamycin)、博来霉素、硫酸长春碱,和达卡巴嗪(即,abvd)。作为另一个例子,该组合可以包含盐酸多柔比星(阿霉素)、博来霉素、硫酸长春碱,和依托泊苷(即abve)。在一些实施方案中,该组合包含盐酸多柔比星(adriamycin)、博来霉素、硫酸长春碱、依托泊苷、强的松,和环磷酰胺(即abve-pc)。在一些实施方案中,该组合包含硫酸长春新碱、盐酸多柔比星(adriamycin)、甲氨蝶呤,和强的松(即vamp)。
[0123]
可在美国国立卫生研究院癌症网站http://www.cancer.gov/cancertopics/druginfo/drug-page-index的美国国立癌症研究所找到已批准的针对不同类型癌症的治疗剂和组合。
[0124]
二线治疗
[0125]
在一些实施方案中,本文描述的是治疗患有癌症的人类受试者的方法,其中受试
者的二线治疗或更多的治疗(例如,癌症二线治疗或癌症三线治疗)已经失败(例如,复发、不敏感、没有或几乎没有从中受益)。本发明还描述了治疗患有癌症的人类受试者的方法,其中,本发明的方法与额外的药物一起施用。在一些实施方案中,额外的药物是癌症的一线或二线治疗。二线治疗一般是指初始治疗(如一线治疗)未达到预期结果,如失效、无效、停止起效时给予的治疗。当受试者对初始治疗(例如,一线治疗)没有反应或产生抗性时,通常考虑或给予二线治疗。例如,二线治疗通常被考虑或给予患有复发或难治性疾病的受试者。
[0126]
施用和剂量
[0127]
本发明的组合可以口服、肠胃外、局部、直肠或通过植入储库施用,优选通过口服施用或注射施用。在一些情况下,可以用药学上可接受的酸、碱或缓冲剂调节组合物(例如药物组合物)的ph以增强组合物的稳定性或功效。
[0128]
在一些实施方案中,受试者口服施用组合物(例如,药物组合物)。在一些实施方案中,组合物(例如药物组合物)以任何口服可接受的剂型口服施用,包括液体凝胶、片剂或胶囊、糖浆、乳剂和水性混悬剂。液体凝胶可包括明胶、增塑剂,和/或遮光剂,根据需要以获得合适的粘稠度,并且可以用批准使用的肠溶衣进行包衣,例如虫胶。当用作口服剂量时,可以添加额外的增稠剂,例如胶类(例如,黄原胶)、淀粉(例如,玉米淀粉)或谷蛋白,以实现组合物(例如,药物组合物)的所需粘稠度。如果需要,可以添加某些甜味剂和/或调味剂和/或着色剂。
[0129]
在一些实施方案中,以适合口服施用的形式例如片剂、胶囊、丸剂、散剂、缓释制剂、溶液和混悬剂给受试者施用组合物(例如,药物组合物)。组合物(例如,药物组合物)可以是适合单次施用精确剂量的单位剂型。除了如本文所述的化合物(例如,fak抑制剂(例如,vs-6063);raf/mek双重抑制剂(例如,ch5126766))之外,药物组合物可以包含药学上可接受的载体,并且可以任选地进一步包含一种或更多种药学上可接受的辅料,例如赋形剂、润滑剂(包衣剂)、粘合剂、崩解剂、稳定剂、调味剂、基质、分散剂、稀释剂、表面活性剂、乳化剂等。此外,片剂可以包括其它药物或药剂、载体和/或佐剂。
[0130]
赋形剂的实例包括淀粉类(淀粉、马铃薯淀粉、玉米淀粉等)、乳糖、结晶纤维素和磷酸氢钙。
[0131]
润滑剂(包衣剂)的例子包括乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、虫胶、滑石粉、巴西棕榈蜡和石蜡。
[0132]
粘合剂的例子包括聚乙烯吡咯烷酮和聚乙二醇,以及与赋形剂所述相同的化合物。
[0133]
崩解剂的实例包括化学改性淀粉和纤维素,例如交联羧甲基纤维素钠、羧甲基淀粉钠和交联聚乙烯吡咯烷酮,以及与赋形剂所述相同的化合物。
[0134]
稳定剂的实例包括:对羟基苯甲酸酯类,例如对羟基苯甲酸甲酯和对羟基苯甲酸丙酯;苯扎氯铵;苯酚类,例如苯酚和甲酚;硫柳汞;脱氢乙酸;和山梨酸。
[0135]
调味剂的实例包括常用的甜味剂、酸化剂和香料。
[0136]
基质的例子包括:脂肪,例如猪油;植物油,例如橄榄油和芝麻油;高级醇,例如硬脂醇和鲸蜡醇;动物油;羊毛脂酸;凡士林;石蜡;膨润土;甘油;和二醇油类。
[0137]
分散剂的例子包括纤维素衍生物(阿拉伯胶、黄芪胶、甲基纤维素等)、硬脂酸聚酯、失水山梨醇倍半油酸酯、单硬脂酸铝、海藻酸钠、聚山梨醇酯和脂肪酸失水山梨醇酯。
[0138]
液体制剂中的溶剂和稀释剂的例子包括苯酚、氯甲酚、纯净水和蒸馏水。
[0139]
表面活性剂和乳化剂的例子包括聚山梨醇酯80、聚乙二醇40硬脂酸酯和聚桂醇。
[0140]
制剂中所含的raf/mek抑制剂(例如,ch5126766)或fak(例如,vs-6063)抑制剂的优选百分比将根据剂型而有所不同,但按重量份计通常为制剂的总重量的0.01%至100%。
[0141]
制剂中raf/mek抑制剂(例如,ch5126766)的含量可以根据预定剂量适当设定。例如,优选的含量为0.01mg至10mg;例如,对于胶囊,含量可能为0.1mg至4mg。例如,更优选的含量为0.8mg。
[0142]
示例性药物组合物包括压制片剂(例如直接压制片剂),例如包含fak抑制剂(例如vs-6063);或raf/mek双重抑制剂(例如ch5126766)。
[0143]
还提供了包含活性或治疗成分(例如本文所述的化合物(例如fak抑制剂(例如vs-6063)和raf/mek双重抑制剂(例如ch5126766)))的片剂。除了活性成分或治疗成分外,片剂还可能含有许多惰性材料,例如载体。药学上可接受的载体可以是无菌液体,例如水和油,包括石油、植物或合成来源的油,例如花生油、芝麻油等。盐水溶液和葡萄糖水溶液也可用作液体载体。因此,根据本发明使用的口服剂型可以使用一种或更包含辅料和助剂的多种药学上可接受的载体以常规方式配制,便于将活性成分加工成可药用的制剂。
[0144]
辅料可以赋予被压缩材料良好的粉末流动和压缩特性。辅料的例子描述于例如raymond c rowe、paul j.sheskey和sian c.owen编辑的handbook of pharmaceutical excipients(5
th edition);出版商:pharmaceutical press.
[0145]
对于口服给药,可以通过将活性成分与本领域熟知的药学上可接受的载体组合而容易地对活性成分(例如是本文所述的化合物(例如,fak抑制剂(例如,vs-6063);raf/mek双重抑制剂(例如,ch5126766))进行配制。此类载体能够将本发明的活性成分配制成片剂、丸剂、胶囊、液体、凝胶、糖浆剂、浆液、散剂或颗粒剂、水或非水介质中的悬浮液或溶液等,用于受试者口服摄入。可使用固体赋形剂制备口服药用制剂,任选研磨所得混合物,并在视需要添加合适的助剂后加工颗粒混合物,获得例如片剂。可能需要合适的辅料,例如稀释剂、粘合剂或崩解剂。此外,fak抑制剂(例如,vs-6063)和raf/mek双重抑制剂(例如,ch5126766)可以根据上述方法单独配制。
[0146]
剂量可以根据所用的剂型和采用的给药途径而变化。各医生可以鉴于患者的状况选择确切的配方、给药途径和剂量。(参见,例如finglet al.,1975,in
ꢀ“
the pharmacological basis of therapeutics”中)。所需剂量可能比上述剂量更低或更高。任何特定受试者的具体剂量和治疗方案将取决于多种因素,包括所用具体化合物的活性、年龄、体重、整体健康状态、性别、饮食、给药时间、排泄率、药物联合、疾病、病情或症状的严重程度和病程、受试者针对疾病、病情或症状所表现出的倾向,以及治疗医师的判断。一个疗程可以包括一次或多次单独施用如本文所述的化合物(例如vs-6063或其药学上可接受的盐,和/或ch5126766或其药学上可接受的盐)。
[0147]
如果需要,口服剂型可以以包装或分配装置的形式呈现,例如fda批准的试剂盒,其可以包含一种或多种含有活性成分的单位剂型。例如,该包装可以包括金属或塑料箔,例如泡罩包装。所述包装或分配装置可以附有给药的使用说明。所述包装或分配器还可以附有与容器相关的公告,其形式由管理药品的制造、使用或销售的政府机构规定,该公告反映了该机构对组合物的形式或人或兽医施用的形式的批准。例如,此类公告可能是美国食品
和药物管理局批准的处方药说明书或批准的产品插页。
[0148]
本发明中使用的给药方案使得可以长期组合施用raf/mek双重抑制剂(例如,ch5126766)与fak抑制剂(例如,vs-6063),同时最大限度地减少副作用并保持药物的疗效。此外,给药方案和组合可以治疗或预防细胞增殖性疾病,特别是癌症,同时最大限度地减少患者的负担。
[0149]
定义
[0150]
如本文所用,冠词“一”是指冠词的语法对象中的一个或多于一个(例如,至少一个)。
[0151]
如本文所用,“约”和“大概”是指考虑到测量的性质或精度,针对所测量的值的可接受的误差程度。示例性误差程度在给定值或值范围的20%(%)以内,通常在10%以内,更通常在5%以内。
[0152]
如本文所用,有效治疗本文所述疾病或病症(例如异常细胞生长,例如癌症(例如本文所述癌症))的化合物的量、“有效量”或“有效进程”是指在向受试者单剂量或多剂量给药后有效治疗受试者,或治愈、减轻、缓解或改善患有本文所述的疾病或病症(例如异常细胞生长(例如,癌症(例如,本文所述的癌症)))的受试者的化合物的量,超出了在不存在此类治疗(例如,安慰剂治疗)时的预期。
[0153]
如本文所用,术语“药学上可接受的”是指可以与本文所述的化合物(例如,vs-6063或其药学上可接受的盐,和/或ch5126766或其药学上可接受的盐)一起施用给受试者的化合物或载体(例如辅料),并且不破坏其药理活性,以及当以足以递送治疗量的化合物的剂量给药时是无毒的。
[0154]
如本文所用,术语“药学上可接受的盐”是指本文所述的化合物(例如,vs-6063,或其药学上可接受的盐,和/或ch5126766或其药学上可接受的盐)的衍生物,其中,该化合物通过将现有酸或碱的部分转化为其盐形式来修饰。药学上可接受的盐的例子包括碱性残基如胺的无机酸盐或有机酸盐;酸性残基如羧酸的碱金属盐或有机盐;等等。本发明的药学上可接受的盐包括本文所述化合物的常规无毒盐,例如由无毒无机或有机酸形成。本发明的药学上可接受的盐可以由本文所述的包含碱性或酸性部分的化合物(例如vs-6063或其药学上可接受的盐,和/或ch5126766或其药学上可接受的盐)通过常规的化学方法合成。通常,此类盐可以通过将这些化合物的游离酸或碱形式与化学计量的合适的碱或酸在水中或有机溶剂中或在两者的混合物中反应来制备;通常,非水介质如乙醚、乙酸乙酯、乙醇、异丙醇或乙腈是优选的。合适的盐的列表可见于remington's pharmaceutical sciences,17
th ed.,mack publishing company,easton,pa.,1985,p.1418 and journal of pharmaceutical science,66,2(1977),其每一篇都通过引用整体并入本文。药学上可接受的盐的例子还包括:无机酸盐,例如盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐和磷酸盐;磺酸盐,例如甲磺酸盐、苯磺酸盐和甲苯磺酸盐;羧酸盐,例如甲酸盐、乙酸盐、草酸盐、马来酸盐、富马酸盐、柠檬酸盐、苹果酸盐、琥珀酸盐、丙二酸盐、葡糖酸盐、扁桃酸盐、苯甲酸盐、水杨酸盐、氟乙酸盐、三氟乙酸盐、酒石酸盐、丙酸盐和戊二酸盐;碱金属盐,例如锂盐、钠盐、钾盐、铯盐和铷盐;碱土金属盐,例如镁盐和钙盐;铵盐类,例如铵盐、烷基铵盐、二烷基铵盐、三烷基铵盐、四烷基铵盐。
[0155]
如本文所用,术语“口服剂型”是指用于向受试者施用药剂(例如治疗剂,例如本文
所述的化合物)的组合物或介质。通常,口服剂型通过口腔施用,然而,“口服剂型”旨在涵盖任何施用于受试者并通过消化道的膜(例如粘膜)吸收的物质,所述消化道包括例如,口腔、食道、胃、小肠、大肠和结肠。例如,“口服剂型”涵盖了通过营养管给药到胃中的溶液。
[0156]
如本文所用,术语“治疗”是指将化合物单独或与额外的药物联合应用或施用至受试者,例如该受试者患有本文所述疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))或正遭受本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))之苦、具有本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))的症状、倾向于患有本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症)),目的是治疗、治愈、减轻、缓解、改变、补救、改良、改善或影响本文所述的疾病或病症(例如异常细胞生长,例如癌症(例如本文所述的癌症))。
[0157]
如本文在施用本文所述的化合物或本文所述的疗法的上下文中使用的短语“组合”和术语“共同施用”或“共同提供”意指在受试者患有疾病或病症(例如癌症)的过程中将两种(或更多种)不同的化合物或疗法递送至受试者,例如在受试者被诊断患有疾病或病症(例如,本文所述的疾病或病症,例如癌症)之后以及在疾病或病症被治愈或消除或因其它原因导致治疗停止之前,将两种(或更多种)不同的化合物或疗法递送至受试者。组合可以实现协同的结果,即大于加合结果,例如,比加合结果增大至少20、50、70或100%。
[0158]
如本文所用,短语“协同效应”是指两种或更多种化合物或组合物的效果大于加合的效果(例如,治疗效果)。示例性协同效应包括施用一定量的fak抑制剂(例如,vs-6063),其与一定量的raf/mek双重抑制剂(例如,ch5126766)组合使用(例如,施用),由此导致的治疗效果大于单独使用每种抑制剂的累加治疗效果。
[0159]
如本文所指的“疗程”包括治疗剂的一次或多次单独施用。一个疗程可以包括一个或多个治疗剂周期。
[0160]
如本文在药物施用周期的上下文中使用的“周期”是指将对病人施用药物的一段时期。优选地,一个周期等于四个星期。
[0161]
本文提供了许多范围,例如每天施用的药物量的范围。在一些实施例中,该范围包括两个端点。在其它实施例中,该范围不包括一个或两个端点。例如,该范围可以不包括下限端点。因此,在这样的实施方案中,100至400mg/天的范围不包括下限端点,其涵盖大于100并且小于或等于400mg/天的量。
[0162]
如本文所用,术语“受试者”旨在包括人类和非人类动物。在一些实施方案中,受试者是人。示例性人类受试者包括患有本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))或正遭受本文所述的疾病或病症(例如,异常细胞生长,例如,癌症(例如,本文所述的癌症))之苦的受试者。本发明的术语“非人类动物”包括所有脊椎动物,例如非哺乳动物(例如鸡、两栖动物、爬行动物)和哺乳动物,例如非人类灵长类动物、家养和/或农业上有用的动物,例如羊、狗、猫、牛、猪等。
[0163]
短语“每周两次”是指raf/mek双重抑制剂(例如,ch5126766)在一周期间施用两次。施用可以在同一天进行两次,或者在不同的日子(可以是连续的)进行一次,但优选在不同的日子进行。更优选地,例如,在该周期的第1天和第4天,或第2天和第5天进行施用,以便在剂量间隔尽可能均匀的情况下施用raf/mek双重抑制剂(例如,ch5126766),即,剂量间隔为3至4天。例如,一周的期间可以从星期一开始,或者例如可以从星期二开始。当在不同的
日子进行两次施用时,每次都可以在一天中的任何时间进行,但它们优选在一天中的同一时间进行(例如,早餐后)。
实施例
[0164]
下面的代表性实施例旨在帮助说明本发明,而不是也不应被解释为限制本发明的范围。
[0165]
在下面的实施例1和2以及下面的表1至4中,“ch5126766”是指ch5126766的钾盐,以及“vs-6063”是指vs-6063盐酸盐。
[0166]
实施例1 vs-6063(fak抑制剂)和ch5126766(raf/mek双重抑制剂)的组合在晚期实体瘤患者中的i期临床试验[nct03875820]
[0167]
方法
[0168]
该研究探索了剂量递增组、强制性活检组和扩展组。ch5126766每周给药两次,以及vs-6063每天给药两次(bd)。每个周期由基于两种药物施用3周、停药1周(1个周期=4周)的给药方式组成。递增组探索了3个剂量水平。剂量水平1包括3.2mg ch5126766 200mg bd vs-6063的安排、剂量水平2a包括4mg ch5126766 200mg bd vs-6063的安排和剂量水平2b包括3.2mg ch5126766 400mg bd vs-6063的安排。确定了在相同剂量水平的6名患者中不超过1名出现方案中规定的药物相关毒性(dlt)的最大剂量。评估了ch5126766和vs-6063的安全性和毒性特征。美国国家癌症研究所(nci)不良事件通用术语标准(ctcae)4.0版确定了每个不良事件的因果关系和严重程度分级。每两个周期检查一次recist标准1.1版的疾病反应。还检查了符合条件的患者的血清肿瘤标志物。还收集了与无进展生存相关的数据。
[0169]
发现
[0170]
剂量递增中最常见的副作用是皮疹和非剂量限制性恶心和高胆红素血症。在组1和2a中均未观察到dlt。在组2b(对应于剂量水平2b)中观察到需要在第1周期中断剂量或减少剂量的2级皮疹dlt,因此组2a(对应于剂量水平2a)被宣布为推荐的第2期剂量(r2pd)。针对具有kras突变的卵巢癌(3例低级别浆液性腺癌和1例粘液性腺癌)和可评估应答的kras突变肺癌,已获得部分应答。已经治疗了两种nras突变的结肠/直肠癌,显示cea水平的降低高于50%,疾病稳定。具有kras突变体的胰腺癌表现出轻微缓解(在第2、4和6周期分别为-19%、-14%和-11%),显示ca19-9水平的降低高于50%。
[0171]
迄今为止获得的疾病应答、血清肿瘤标志物和治疗持续时间的代表性结果显示在实施例2中。
[0172]
结论
[0173]
ch5126766和vs-6063的组合在患有卵巢癌和其它具有kras和/或nras突变的肿瘤的患者中是可耐受和高活性的。
[0174]
实施例2在晚期实体瘤患者中的ch5126766和vs-6063的组合
[0175]
在如下表1至4中,“ch”代表ch5126766的钾盐,每周施用两次,以及“vs”代表vs-6063盐酸盐,每天施用两次(bid)。每个周期由基于两种药物施用3周、停药1周的给药方式组成(1个周期=4周)。“pr”代表部分应答;“sd”代表疾病稳定;“n/a”代表不可用。
[0176]
表1 ch5126766和vs-6063的组合施用于卵巢癌患者
[0177][0178]
**数据截止日期为2019年6月18日
[0179]
表2 ch5126766和vs-6063的组合施用于nsclc患者
[0180][0181]
**数据截止日期为2019年6月18日
[0182]
表3 ch5126766和vs-6063的组合施用于结直肠癌患者
[0183][0184]
[0185]
表4 ch5126766和vs-6063的组合施用于胰腺癌患者
[0186][0187]
**数据截止日期为2019年6月18日。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。