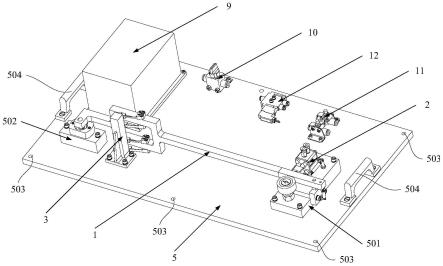
一种基于同位素内标-quechers-uplc-ms法检测中药饮片丙烯酰胺的方法
技术领域
1.本发明涉及药物分析检测技术领域,具体涉及一种同位素内标
ꢀ‑
uplc-ms/ms联用quechers法检测“浙八味”等道地药材中丙烯酰胺含量的方法。
背景技术:
2.丙烯酰胺(acrylamide,am)是一种不饱和酰胺,如下所示:
[0003][0004]
德国研究人员于1949年首次研发上市,主要用于合成聚丙烯酰胺,作为黏合剂、增强剂、絮凝剂或者食品包装材料而广泛使用。作为一种水溶性物质,am极易被人体消化道、皮肤等其他组织吸收,在体内外均表现有致突变致癌性。1994年,国际癌症研究中心 (international agency for research on cancer,iarc)将其列为二类致癌物。2002年瑞典科学家在油炸马铃薯中首次发现丙烯酰胺的存在,由此开启了食品、水质和材料等领域对am毒性和产生机制的广泛和深入的研究。之后陆续发现了am的危害主要有神经毒性、基因毒性和生殖毒性等。其中,神经毒性研究广泛而深入,并且有对人类确诊病例的研究,如lars hagmar,chen jh等分别通过对病例的统计学分析和细胞实验验证了am的神经毒性及毒理作用。同时对am的产生机制研究表明,以还原糖和天冬酰氨酸等氨基酸通过美拉德反应生成am,为其主要产生途径。
[0005]
我国也已颁布am相关的食品国家标准,但仍未规定具体品种的限量要求。而中药饮片中am的检测技术、残留水平、限量标准以及风险评估研究均处在刚刚起步阶段,除了河北大学2010年前后有过相关的硕士研究生论文外,至今国内外有关中药中am研究报道较少。中药材大多来源于植物,且很多是“药食同源”品种,类似于食品的高淀粉高蛋白品种较多,大多需经过高温炮制后使用,因此高温炮制工艺带来的am残留风险客观存在,需要引起研究人员和监管部门的重视。
[0006]
浙江道地中药材资源丰富,自古以来以“浙八味”(浙贝母、杭白菊、白术、浙麦冬、杭白芍、延胡索、玄参、温郁金)为代表的中药材享誉中外。2018年,浙江省确定铁皮石斛、衢枳壳、乌药、三叶青、覆盆子、前胡、灵芝、西红花为新“浙八味”道地药材培育品种,其中白术、白芍、杭白菊、温莪术、浙贝母、延胡索等均以炒制品为习用品,由此引发诸如高温炒制工艺是否会造成中药材和饮片中am 残留哪些炮制品种am残留风险较高等疑问。
[0007]
因此,有必要对新老“浙八味”为代表的中药材和饮片的am含量进行检测,以期为am这一新兴的中药材和饮片中有害物质控制及相关指导原则的制定提供技术支持。
技术实现要素:
[0008]
本发明所要解决的技术问题是克服背景技术的技术缺陷,提供一种基于同位素内标-quechers-uplc-ms法检测中药饮片丙烯酰胺的方法。本发明以收集的新老“浙八味”为代表的中药材和饮片生品和炮制品共计247批次样品为研究对象,通过优化的quechers法建立了简便通用的净化方法,并通过uplc-ms/ms对丙烯酰胺的含量进行了检测,方法简便、准确且重复性好,为丙烯酰胺这一新兴的中药材和饮片中有害物质控制及监测提供技术支持。
[0009]
本发明解决上述技术问题所采用的技术方案如下:
[0010]
一种基于同位素内标-quechers-uplc-ms法检测中药饮片丙烯酰胺的方法,包括如下步骤:
[0011]
(1)内标贮备溶液的制备:
[0012]
精密量取
13
c3丙烯酰胺内标对照品溶液,加乙腈制成每1ml含 10μg的溶液,作为内标贮备溶液;
[0013]
(2)对照品贮备液的制备:
[0014]
取丙烯酰胺对照品适量,精密称定,加乙腈制成每1ml含1mg 的溶液,作为对照品贮备液;
[0015]
(3)系列对照品溶液的制备:
[0016]
分别精密量取上述内标贮备溶液及对照品贮备液适量,用乙腈稀释并摇匀制成质量浓度分别为5、10、50、200、500、5000、10000μg
·
l-1
含内标质量浓度为100μg
·
l-1
的系列对照品溶液;
[0017]
(4)供试品溶液的制备:
[0018]
取药材样品粉末2g,精密称定,置50ml离心管中,加无水硫酸镁4g、氯化钠0.5g、水10ml、乙腈10ml及内标溶液200μl,涡旋混匀,置摇床上剧烈振荡30分钟;离心10分钟,取上清液1ml,置预置有psa0.2g的离心管中,涡旋混匀,离心,取上清液,即得供试品溶液;
[0019]
(5)线性回归方程的获得:
[0020]
分别精密量取上述系列浓度对照品溶液各1μl,注入液相色谱质谱联用仪,测定相应丙烯酰胺及其内标的峰面积,以各标准系列工作液的丙烯酰胺进样浓度为横坐标,以丙烯酰胺定量离子对和
13
c3丙烯酰胺内标定量离子对的峰面积比为纵坐标,绘制标准曲线,得线性回归方程;
[0021]
(6)样品的检测:
[0022]
取供试品溶液进行超高效液相色谱-串联质谱检测;
[0023]
(7)丙烯酰胺浓度测定:
[0024]
采用同位素内标法定量:根据试样中丙烯酰胺定量离子对和
13
c3 丙烯酰胺内标定量离子对色谱峰的面积,采用步骤(5)的线性回归方程,计算得到丙烯酰胺的浓度。
[0025]
优选地,所述步骤(4)中,所述振荡时的频率为450次/分钟。
[0026]
优选地,所述步骤(4)中,所述离心10分钟时的离心频率为 4000转/分钟。
[0027]
优选地,所述步骤(5)和步骤(6)中,所述色谱条件为:
[0028]
色谱柱为phenomenex kinetex c18色谱柱(100
×
2.1mm, 1.7μm;柱温:40℃;以甲醇(a)-0.1%甲酸(b)为流动相,按下表的梯度比例进行梯度洗脱,流速:1.0ml
·
min-1
;
isotope laboratories,1 mg
·
ml-1
);cleanert psa(天津博纳艾杰尔科技有限公司,粒径:40~60 μm);药材及饮片购自上药凯仑(杭州)医药有限公司、浙江英特中药饮片有限公司、杭州华东中药饮片有限公司和亳州市良心药业销售有限公司。
[0041]
2实验方法
[0042]
2.1色谱条件与系统适用性实验
[0043]
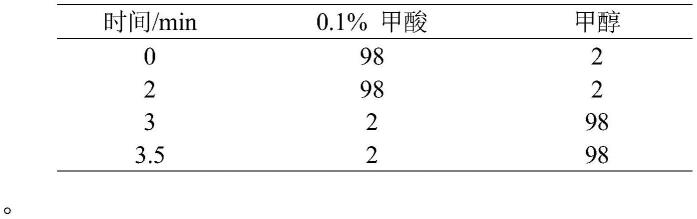
色谱柱为phenomenex kinetex c18色谱柱(100
×
2.1mm,1.7μm;柱温:40℃;以甲醇(a)-0.1%甲酸(b)为流动相,按表1的梯度比例进行梯度洗脱,流速:1.0ml
·
min-1
。
[0044]
表1丙烯酰胺残留实验中梯度洗脱程序
[0045][0046]
2.2质谱
[0047]
电喷雾离子源;正离子扫描方式;电离电压:4kv;离子源温度: 300℃;雾化器流量:3l
·
min-1
;干燥器流量:10l
·
min-1
。监测方式:多反应监测(mrm)模式。丙烯酰胺定量离子对为[m h]
,m/z 71.90/55.20;丙烯酰胺内标定量离子对为[m h]
,m/z 75.10/58.05。
[0048]
2.3溶液配置
[0049]
2.3.1内标贮备溶液的制备
[0050]
精密量取
13
c3丙烯酰胺内标对照品溶液,加乙腈制成每1ml含 10μg的溶液,作为内标贮备溶液。
[0051]
2.3.2对照品贮备液的制备
[0052]
取丙烯酰胺对照品适量,精密称定,加乙腈制成每1ml含1mg的溶液,作为对照品贮备液。
[0053]
2.3.3供试品溶液制备
[0054]
取药材样品粉末2g,精密称定,置50ml离心管中,加无水硫酸镁4g、氯化钠0.5g、水10ml、乙腈10ml及内标溶液200μl,涡旋混匀,置摇床上剧烈振荡(450次/分钟)30分钟;离心(4000转/分钟) 10分钟,取上清液1ml,置预置有psa 0.2g的离心管中,涡旋混匀,离心,取上清液,即得。
[0055]
2.4方法学考察
[0056]
2.4.1专属性实验
[0057]
取空白溶剂,按“供试品溶液制备”方法项下操作,得到图1所示色谱图,可见样品基质对am与内标均没有干扰。
[0058]
2.4.2线性与定量下限
[0059]
分别精密量取上述内标贮备溶液及对照品贮备液适量,用乙腈稀释并摇匀制成质量浓度分别为5、10、50、200、500、5000、10000μg
·
l-1
含内标质量浓度为100μg
·
l-1
的系列对照品溶液。分别精密量取上述系列浓度对照品溶液各1μl,注入液相色谱质谱联用仪,测定相应丙烯酰胺及其内标的峰面积,以各标准系列工作液的丙烯酰胺进样浓度 (μg
·
l-1
)为横坐标,以丙烯酰胺(m/z 71.90/55.20)和
13
c3丙烯酰胺内标(m/z 75.10/58.05)的峰面
积比为纵坐标,绘制标准曲线。结果表明,回归方程为y=8.2251x 135.22,r2=0.9972,am在5.08 ~10160ng
·
ml-1
内线性关系良好,最低定量下限为5.0μg
·
l-1
。
[0060]
2.4.3精密度实验
[0061]
取“2.4.2”项下质量浓度为200μg
·
l-1
对照品溶液,重复连续进样6 次,记录am峰面积,am峰面积rsd为1.8%,表明仪器精密度良好。
[0062]
2.4.4加样回收率
[0063]
取样品(麸白芍,批号:20201226)各9份约1.0g,精密称定,分别置50ml离心管中,精密加入质量浓度为1
×
104μg
·
l-1
的对照品溶液250μl、400μl、1000μl、同“供试品溶液制备”方法制备,即得低 (255μg
·
l-1
)、中(408μg
·
l-1
)、高(1019μg
·
l-1
)3个浓度的样品溶液各3份,进行分析,结果见表2,表明该方法准确性良好。
[0064]
表2丙烯酰胺回收率实验结果
[0065][0066]
2.5样品测定
[0067]
2019~2021年三年共收集到的247批药品涉及生品、炒制、炒焦、麸炒、醋制和酒制6种炮制方式。按上述方法进行测定,并采用随行质量控制(包括随性空白实验及随行回收试验)来评估方法的可行性,结果均符合残留检测要求。同时开展了样品筛查普查,涉及浙产常用中药材和饮片、部分中成药制剂。am的总体检出率约为61.2%(表3)。
[0068]
表3“浙八味”等道地药材丙烯酰胺含量筛查数据
[0069]
[0070]
[0071]
[0072][0073]
在对同种药材的比较分析中发现,麸炒白术的丙烯酰胺含量显著高于白术;麸炒白芍的丙烯酰胺含量显著高于酒白芍;延胡索和醋延胡索的丙烯酰胺含量之间以及白芍和酒白芍的丙烯酰胺含量之间没有显著性差异。对于中药材和饮片的不同炮制方式来说,高温的炮制方式,如炒制、麸炒、炒焦和烧炭等深度炮制加工,都会使中药材和饮片中的丙烯酰胺含量明显提高,而同为高温炮制方法,如醋制、酒制等因特殊溶剂存在并对加工时间、温度等有一定限制的情况下,未发现显著提高中药材和饮片中丙烯酰胺的含量(表4)。这也进一步证实了丙烯酰胺来源的机理(高温的炮制方式有利于美拉德反应的发生)。
[0074]
表4新老“浙八味”丙烯酰胺筛查数据统计
[0075]
[0076][0077]
3讨论
[0078]
来源于植物的中药材,根据药用部位不同,可来自根、茎、花、叶、果实、种子等,基质的复杂为精确高灵敏度分析方法的建立带来了极大的挑战。本发明参考各类文献报道,特别是国标gb5009.204-2014标准方法,采用同位素内标法结合液质联用仪,借助了液质在痕量分析中的高灵敏度,同时解决了中药复杂基质效应问题。同时创造性地改良优化quechers法,相较于国标和文献报道的单柱和双柱spe法,大大简化和降低检测成本,测得量表明本发明研发的方法具有更高的回收效率,具体见表5。同时也比较了乙腈-1%甲酸溶液和甲醇-1%甲酸溶液两种流动相系统,安捷伦6430、ab5500等同类液质联用仪,常见的亚二微米液相柱,如kinetex c18 (2.1
×
100mm,1.7μm)、agilent eclipse plus(2.1
×
100mm,1.8μm)、 acquitybeh(2.1
×
100mm,1.7μm)等进行耐用性研究,常见的超高压液相和亚二微米色谱柱均可以得到良好分离,方法耐用性良好。
[0079]
表5不同的前处理方法测得结果
[0080][0081]
4结语
[0082]
本发明收集样品时除传统炮制工艺为趁鲜切片的郁金和制枫斗的铁皮石斛外,针对性选取了新老“浙八味”药材饮片样品,共计14个品种涉及247批不同炮制样品,从丙烯酰胺测定结果分析,247批样品中161批检出丙烯酰胺,检出率为61.2%。其中检出量1000μg
·
kg-1
以下为43.3%,1000~3000μg
·
kg-1
为10.3%,3000μg
·
kg-1
以上占比6.8%。作为新兴污染物,am在中药材和饮片中并非普遍存在,仅在某些高温炮制品中有较高的检出率和含量。
[0083]
本发明采用优化的quechers净化前处理技术,联用同位素内标
ꢀ‑
超高压液相-质谱法,测定“浙八味”及新“浙八味”共计247批样品中 am含量,方法简便、准确且重复性好。247批次样品中,经过炒制、麸炒等典型高温炮制工艺的药材,am含量显著高于未经过高温处理的生药及饮片。
[0084]
上述说明并非对本发明的限制,本发明也并不限于上述举例。本技术领域的普通技术人员在本发明的实质范围内,做出的变化、改型、添加或替换,也应属于本发明的保护
范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。