1.本发明涉及生物医药技术领域,特别涉及一种从人血浆或人血浆衍生原料中去除内毒素的方法。
背景技术:
2.内毒素是由革兰氏阴性菌的菌体裂解后释出的毒素,是细菌细胞壁的成分,单位为eu/ml。内毒素化学成分为磷脂多糖-蛋白质复合物,其毒性成分主要为类脂质a。人体对内毒素极为敏感。内毒素进入动物或人体可引起发热、微循环障碍、内毒素休克及播散性血管内凝血等。因此注射用生物制品内毒素含量是重要质量指标,需要采用有效的手段进行控制。
3.目前生物制品中去除或降低内毒素含量的手段有triton x-114萃取法、纳米膜超滤法、亲和层析(吸附)法、离子交换层析法、活性炭吸附法。萃取法作为一种相分离技术,只能够按批处理,不能够实现连续处理;纳米膜超滤法去除内毒素所使用的纳米膜虽然可以多次使用,但其价格昂贵,初次设备投入较大,限制了其推广使用;亲和层析和离子交换层析法的情况与纳米膜超滤法情况类似,初次投入较大;活性炭吸附法不能单独使用,还需要结合活性炭去除步骤。
技术实现要素:
4.有鉴于此,本发明旨在提出一种从人血浆或人血浆衍生原料中去除内毒素的方法。利用具有内毒素吸附功能的深层过滤技术,并通过条件的优化,去除人血浆或人血浆衍生原料中的内毒素,并同时保持极高的蛋白回收率和制品的澄清度。
5.为达到上述目的,本发明的技术方案是这样实现的:
6.一种从人血浆或人血浆衍生原料中去除内毒素的方法,包括如下步骤:
7.s1.配制平衡液,并调节所述平衡液至设定的ph和电导率;
8.s2.将待处理的人血浆或人血浆衍生原料进行预处理至至与步骤s1相同的ph和电导率;
9.s3.将深层滤器进行平衡处理;
10.s4.将步骤s2中预处理好的人血浆或人血浆衍生原料溶液通过泵系统泵入步骤s3中平衡完成的深层滤器中进行过滤;
11.s5.待人血浆或人血浆衍生原料溶液经深层滤器过滤完成后,再次泵入平衡液进行过滤后的后平衡,将后平衡滤液和步骤s4中过滤后制品进行混合。
12.进一步的,步骤s1中,所述平衡液为三羟甲基氨基甲烷-盐酸溶液或甘氨酸-氢氧化钠溶液。
13.进一步的,步骤s1中,调节所述平衡液的ph为6.6-8.7,且电导率为不高于18ms/cm。
14.进一步的,采用盐酸或氢氧化钠溶液调节所述平衡液的ph,采用中性盐调节所述
平衡液的电导率。
15.进一步的,所述中性盐选择氯化钠、硫酸铵中的至少一种。
16.进一步的,步骤s2中,可通过在待处理的人血浆或人血浆衍生原料溶液加入盐酸或氢氧化钠溶液调节溶液至设定的ph,加入中性盐调节溶液至设定的电导率,或者可通过待处理的人血浆或人血浆衍生原料溶液与步骤s1的平衡液混合。
17.进一步的,步骤s3中,通过泵系统将所述平衡液泵入滤器,直至经过滤器后的溶液的ph值和电导率与步骤s1中的平衡液相同,平衡完成。具体的,本技术的ph值和电导率与步骤s1中的平衡液相同,可以允许有
±
0.5的误差。
18.进一步的,所述深层滤器为zetaplus
tm
zb系列滤器。
19.进一步的,步骤s4中,泵入过程中,控制过滤中压力不大于0.12mpa,流速不大于3.6ml/cm2/min,每平方厘米膜上内毒素吸附载量不超过370eu/ml。
20.进一步的,步骤s5中,再次泵入的平衡液的用量为4-5ml/cm2。
21.相对于现有技术,本发明所述的一种从人血浆或人血浆衍生原料中去除内毒素的方法具有以下优势:
22.采用深层过滤工艺,操作简单,不依赖昂贵设备,容易开发,普适性强;在过滤过程中,在工艺条件范围内选择合适的ph、电导率及参数组合,在兼顾去除内毒素的同时保持较高的蛋白回收率,对制品无不利影响,适宜大规模推广应用。
具体实施方式
23.下面结合具体实施方式,进一步阐述本发明。首先应说明的是,下述实验例中的数据是由发明人通过大量实验获得,限于篇幅,在说明书中只展示其中的一部分,且本领域普通技术人员可以在此数据下理解并实施本发明。这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些改动或修改同样落于本技术所保护的范围。
24.本发明中所用的平衡液为三羟甲基氨基甲烷-盐酸溶液或甘氨酸-氢氧化钠溶液。
25.三羟甲基氨基甲烷-盐酸(tris-hcl)平衡液的配制:将三羟甲基氨基甲烷和水按照质量体积比为2.42g:1l混合得到三羟甲基氨基甲烷溶液,并加入盐酸调节至所需的ph值,然后加入适量中性盐调节溶液至所需电导率数值。
26.甘氨酸-氢氧化钠(gly-naoh)平衡液的配制:将甘氨酸和水按照质量体积比为1.50g:1l混合得到甘氨酸溶液,并加入氢氧化钠调节溶液至所需的ph值,然后加入适量中性盐调节溶液至所需电导率数值。
27.内毒素母液的配制:用luria-bertani(lb)培养基培养5微升大肠杆菌14小时,然后加入100ml纯化水中,振荡混匀,即为内毒素母液。该内毒素母液经检测内毒素含量为2217eu/ml。内毒素检测用试剂盒为湛江安度斯生物有限公司生产的鲎试剂(动态浊度法)。鉴于内毒素的检测方法为现有技术,在此不再进行赘述。
28.实施例一 人血浆中内毒素的去除
29.1、人血浆预处理
30.取人血浆(采集自华兰生物长垣单采血浆站)600ml,加入0.5mol/l氢氧化钠溶液调节溶液ph值至7.8。在血浆中加入9.5ml内毒素母液并混匀。取样分别检测内毒素和蛋白
质含量。
31.需要说明的是由于人血浆的自然电导率为14.2ms/cm左右,因此不需要额外对人血浆调节至设定电导率。
32.2、zetaplus
tm
zb滤器平衡处理
33.取zeta plus
tm
zb滤器(产品货号为bc0025l90zb),用硅胶软管连接好蠕动泵和滤器;用0.5mol/l的盐酸调节三羟甲基氨基甲烷溶液至ph为7.8,用氯化钠调节三羟甲基氨基甲烷溶液至电导率为14.2ms/cm,得到三羟甲基氨基甲烷-盐酸(tris-hcl)平衡液即平衡液1;通过蠕动泵向滤器中泵入调节好ph和电导率的平衡液1,直至出液口(即经过滤器后)平衡液1的ph为7.8,电导率为14.2ms/cm,停止泵入平衡液1。
34.3、将步骤1中预处理好的人血浆通过蠕动泵压入预处理(平衡)好的zeta plus
tm
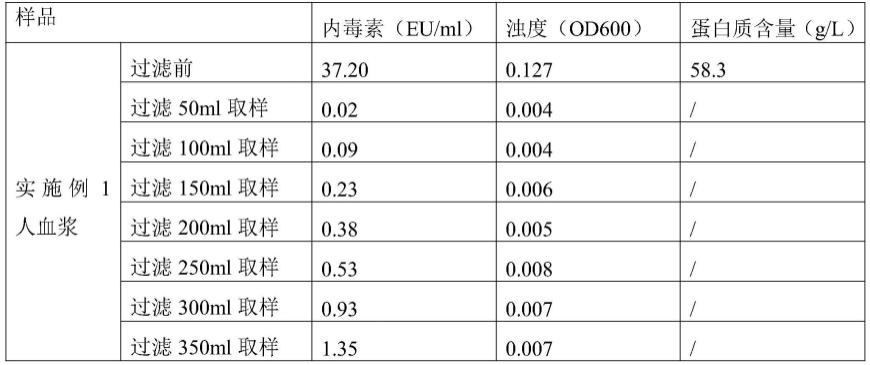
zb滤器中,并调节泵速使流速为90ml/min,过滤中压力范围为0.07~0.12mpa。过滤过程中每过滤50ml取滤过血浆3ml,用于检测内毒素含量、浊度。待人血浆全部过滤完毕后,再泵入100ml平衡液1。过滤后的平衡液1与过滤后的血浆合并混匀,取合并后滤过液进行检测。
35.zeta plus
tm
zb深层滤器在上述实验条件下,血浆中内毒素、浊度和蛋白质含量的数据见下表1。
36.实施例二 人血浆冷沉淀溶解液中内毒素的去除
37.1、冷沉淀制备
38.合并融解冻存人血浆3袋(采集自华兰生物长垣单采血浆站)体积约1800ml,溶解后混合血浆温度为2.1℃,血浆用j-26xpi型号离心机(beckman公司生产)12000g离心力离心20分钟,收集冷沉淀,冷沉淀共计1.74g。
39.2、冷沉淀溶解调制
40.用0.5mol/l的盐酸溶液调节三羟甲基氨基甲烷溶液至ph为6.6,然后用硫酸铵调节三羟甲基氨基甲烷溶液至电导率为1.6ms/cm,得到三羟甲基氨基甲烷-盐酸(tris-hcl)平衡液即平衡液1。将冷沉淀用450ml平衡液1溶解,溶解温度22℃。在冷沉淀溶解液中加入8.0ml内毒素母液并混匀。
41.3、zetaplus
tm
zb滤器平衡处理
42.取zeta plus
tm
zb滤器(产品货号bc0025l90zb),用硅胶软管连接好蠕动泵和滤器,通过蠕动泵向滤器中泵入平衡液1,直至出液口(即经过滤器后)平衡液1的ph为6.6,电导率为1.6ms/cm,停止泵入平衡液1。
43.4、将步骤2中溶解好的冷沉淀溶解液,通过蠕动泵泵入预处理(平衡)好的zeta plus
tm
zb滤器中,调节泵速使流速为50ml/min,过滤中压力波动范围为0.03~0.04mpa。过滤过程中每过滤50ml取滤过血浆3ml,用于检测滤过液内毒素含量和浊度。待冷沉淀溶解液全部过滤完毕后,再泵入125ml平衡液1,过滤后的平衡液1与过滤后冷沉淀溶解液合并混匀,取混匀后滤过液进行检测。
44.zeta plus
tm
zb深层滤器在上述实验条件下,冷沉淀溶解液中内毒素、浊度和蛋白质含量的数据见下表1。
45.实施例三 人血浆组分i溶解液中内毒素的去除
46.1、人血浆组分i制备
47.融合并解冻人血浆3袋(采集自华兰生物长垣单采血浆站)体积1773ml,溶解后混
合血浆温度为1.6℃,ph值为7.25,电导率13.3ms/cm。搅拌加入165ml的低温95%乙醇(乙醇温度-18℃),乙醇加入完毕后,混合液温度为-2.1℃。搅拌反应1.5小时后,用j-26xpi型号离心机(beckman公司生产)8000g离心力离心10分钟,收集组分i沉淀,沉淀共计10.8g。
48.2、组分i沉淀溶解调制
49.用0.5mol/l的氢氧化钠溶液调节甘氨酸溶液至ph为8.7,然后用氯化钠调节甘氨酸溶液至电导率为18.0ms/cm,得到平衡液2。将沉淀用300ml平衡液2溶解,溶解温度为12℃。在组分i沉淀溶解液中加入5ml内毒素母液并混匀。
50.3、zetaplus
tm
zb滤器平衡处理
51.取zeta plus
tm
zb滤器(产品货号bc0025l60zb),通过蠕动泵向滤器中泵入500ml平衡液2,直至出液口(即经过滤器后)平衡液2的ph为8.7,,电导率为18.0ms/cm,停止泵入平衡液2。
52.4、从将步骤2中溶解好的组分i沉淀溶解液,通过蠕动泵泵入预处理(平衡)好的zeta plus
tm
zb滤器中,并调节泵速使流速为50ml/min,过滤中压力波动范围为0.02~0.06mpa。过滤过程中每过滤50ml取滤过血浆3ml,用于检测滤过液内毒素含量和浊度。待组分i沉淀溶解液全部过滤完毕后,再泵入100ml平衡液2,过滤后的平衡液2与过滤后组分i沉淀溶解液合并混匀,取混匀后滤过液进行检测。
53.zeta plus
tm
zb深层滤器在上述实验条件下,组分i沉淀溶解液中内毒素、浊度和蛋白质含量的数据见表1。
54.对比例一人血浆中内毒素的去除
55.1、人血浆预处理
56.取人血浆(采集自华兰生物长垣单采血浆站)600ml,加入0.5mol/l氢氧化钠溶液调节溶液ph值至8.9。血浆中加入9.5ml内毒素母液并混匀。取样检测内毒素和蛋白质含量。
57.2、zetaplus
tm
zb滤器平衡处理
58.取zeta plus
tm
zb滤器(产品货号bc0025l90zb),用硅胶软管连接好蠕动泵和滤器;用0.5mol/l的氢氧化钠调节三羟甲基氨基甲烷溶液至ph为8.9,用氯化钠调节三羟甲基氨基甲烷溶液至电导率为19.4ms/cm,得到平衡液1;通过蠕动泵向滤器中泵入500ml平衡液1,直至出液口(即经过滤器后)平衡液1的ph为8.9,电导率为19.4ms/cm,停止泵入平衡液1。
59.3、从将步骤1中预处理好的人血浆通过蠕动泵压入预处理(平衡)好的zeta plus
tm
zb滤器中,调节泵速使流速为90ml/min,过滤中压力范围为0.07~0.11mpa。过滤过程中每过滤50ml取滤过血浆3ml,用于检测内毒素含量、浊度。人血浆过滤完毕后,再泵入100ml平衡液1,过滤后平衡液1与过滤结血浆合并混匀,取合并后滤过液进行检测。
60.zeta plus
tm
zb深层滤器在上述实验条件下,血浆中内毒素、浊度和蛋白质含量的数据见下表1。
61.表1
62.63.[0064][0065]
需要说明的是,在取样检测过程中,每过滤50ml取滤过血浆3ml进行检测,后一次的取样并不包括前次的取样。即除了最后过滤完成需要合并滤过液,在之前的每次取样中,并不将每次的取样溶液混合进行检测。此外深层滤器的产品货号bc0025l90zb、bc0025l60zb中,其中0025对应的是深层滤器的面积为25cm2,90、60对应的是深层滤器支持介质的孔径。
[0066]
通过表1可知,采用本技术去除内毒素方法的实施例1-3,经过处理后,内毒素的含量降低较多,不会对人体产生不利影响,且能明显改善制品的澄清度,制品的蛋白质含量无明显改变。例如实施例1采用本技术方法从人血浆中去除内毒素,内毒素含量由过滤前的37.20eu/ml降低至1.51eu/ml,浊度由过滤前的od600为0.127降低至od600为0.007。而对比例1改变了本技术的实验条件,内毒素含量降低较少,过滤前内毒素含量为36.40eu/ml,过滤后内毒素含量依然高达29.63eu/ml。可见采用本技术的方法,能有效去除制品中的内毒素,且不影响制品的蛋白质含量,并改善制品的澄清度,使制品使用更安全。
[0067]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。