1.本发明涉及核酸检测领域,具体涉及一种等温核酸检测酶组合物、试剂盒及其用途和检测方法。
背景技术:
2.crispr(clustered regularly interspaced short palindromic repeats)是细菌和古细菌种抵御病毒入侵的一种获得性免疫的方式。当病毒入侵时,细菌或古细菌生成对应的能识别病毒基因组的crrna,可以引导具有核酸内切酶活性的cas蛋白对病毒靶序列进行识别和切割。crispr-cas13是基于细菌免疫系统的rna靶向和编辑系统,可保护其免受病毒侵袭。该系统类似于crispr-cas9系统,但与靶向dna的cas9不同,cas13蛋白仅靶向切割单链rna。cas13a(又叫c2c2)最初是2015年被成功鉴定出来,是crispr-cas系统中的第二大类第vi型,是家族中目前发现的唯一只靶向ssrna的系统。它的结合和切割的对象为rna。
3.从结构上来看,cas13a含有两个hepn(higher eukaryotes and prokaryotes nucleotide-binding,hepn)结构域。hepn结构域对cas13a割rna目标是必需的。目前科学家们已经从leptotrichia buccalis、leptotrichia wadei、leptotrichia shahii以及lachnospiraceae bacterium等多种细菌中解析出了cas13a的结构,根据其来源不同分别称为lbucas13a、lwacas13a、lshcas13a和lbacas13a。cas13家族包括4中亚型,即cas13a、cas13b、cas13c和cas13d。目前用在核酸检测方面的,大多是用cas13a。
4.cas13a有一个特别之处,那就是cas13a一旦识别并切割由crrna序列指定的rna目标,它就转入了一种酶促“激活”状态,这时它将结合并切割其他的rna,而不管它们是否与crrna同源,或是否存在pfs。这个活性也就是平时听到最多的“附带切割(collateral cleavage)”效应。
5.2017年,张锋等利用cas13a开发了sherlock(specific high sensitivity enzymatic reporter unlocking)的检测系统。利用该方法,研究人员灵敏地检测了各种dna或rna靶标,包括寨卡病毒、登革热病毒、细菌分离株、抗性基因、人类dna基因型和癌症突变等。随后,科学家们利用cas13a蛋白结合等温核酸扩增技术,开发出来检测各种病毒细菌以及其他的核酸的工具,并且表现出了优秀的灵敏度和特异性。
6.在检测核酸时,由于核酸的数量比较少,通常需要先将核酸进行扩增,再对扩增产物进行检测,使用cas13a检测核酸时,主要分为两个步骤,第一步为核酸扩增,第二步为cas13a检测,步骤相对复杂,由于扩增和检测需要分开进行,增加了操作的复杂性和污染的风险。
技术实现要素:
7.因此,本发明要解决的技术问题在于克服现有技术中的cas13a蛋白检测核酸技术操作复杂、并且需要两步法检测的缺陷,从而提供一种一种等温核酸检测酶组合物、试剂盒及其用途和检测方法,将核酸扩增和cas13a蛋白检测相结合,在检测过程中,将核酸扩增和
检测整合到一起,实现对目的片段的一步法扩增及检测,操作简单、反应速度快,将会极大的解决使用cas13a蛋白在核酸检测过程中的缺陷。
8.为此,本发明提供了如下的技术方案:
9.一种等温核酸检测的酶组合物,包括重组酶、单链结合蛋白、dna聚合酶、重组酶辅助蛋白、t7rna聚合酶和cas13a蛋白。
10.可选的,所述重组酶包括uvsx蛋白;可选的,所述uvsx蛋白包括t4 uvsx蛋白、t6 uvsx蛋白或rb69 uvsx蛋白;或
11.所述重组酶辅助蛋白包括uvsy蛋白;可选的,所述uvsy蛋白包括t4 uvsy蛋白、t6 uvsy蛋白或rb69 uvsy蛋白;或
12.所述单链结合蛋白包括gp32蛋白;可选的,所述gp32蛋白包括t4gp32蛋白、t6 gp32蛋白或rb69 gp32蛋白;或
13.所述dna聚合酶包括链置换dna聚合酶;可选的,所述链置换dna聚合酶包括金黄色葡萄球菌的dna聚合酶i的大片段、枯草芽孢杆菌dna聚合酶i大片段或大肠杆菌dna聚合酶i大片段;或
14.所述cas13a蛋白为韦德纤毛菌来源的lwcas13a蛋白。
15.可选的,所述uvsx蛋白为如下a1)-a2)中任意一种:
16.a1)氨基酸序列如seq id no:9所示;
17.a2)如seq id no:9所示的氨基酸序列的任意一个或几个氨基酸残基经过一个或几个氨基酸残基的取代和/或缺失和/或添加得到的与a1)所示的氨基酸序列具有90%以上的同一性的蛋白;
18.和/或,
19.所述uvsy蛋白为如下b1)-b2)中任意一种:
20.b1)氨基酸序列如seq id no:10所示;
21.b2)如seq id no:10所示的氨基酸序列的任意一个或几个氨基酸残基经过一个或几个氨基酸残基的取代和/或缺失和/或添加得到的与b1)所示的蛋白具有90%以上的同一性的蛋白;
22.和/或,
23.单链结合蛋白gp32为如下c1)-c2)中任意一种:
24.c1)氨基酸序列如seq id no:11所示;
25.c2)如seq id no:11所示的氨基酸序列的任意一个或几个氨基酸残基经过一个或几个氨基酸残基的取代和/或缺失和/或添加得到的与c1)所示的蛋白具有90%以上的同一性的蛋白;
26.和/或,
27.所述cas13a蛋白为如下d1)-d2)中任意一种:
28.d1)氨基酸序列如seq id no:12所示;
29.d2)如seq id no:12所示的氨基酸序列的任意一个或几个氨基酸残基经过一个或几个氨基酸残基的取代和/或缺失和/或添加得到的与d1)所示的蛋白具有90%以上的同一性的蛋白。
30.可选的,所述酶组合物中,重组酶、重组酶辅助蛋白、单链结合蛋白、dna聚合酶
cas13a蛋白的质量比为1:(0.2-4.6):(0.77-2.3):(0.2-1):0.1-1.2);t7 rna聚合酶在使用时的终浓度为0.2-1u/μl,所述在使用时的终浓度是指配制的等温核酸检测反应体系中的终浓度。
31.可选的,所述酶组合物为液态混合物或冻干粉混合物。
32.可选的,还包括扩增缓冲液、报告分子和反应启动剂中的至少一种;
33.可选的,所述等温核酸检测试剂盒中,分为独立包装的三部分,第一部分为包括酶组合物、扩增缓冲液和报告分子的冻干粉,第二部分为反应缓冲液,第三部分为反应启动剂;所述反应缓冲液中含有缓冲液a、醋酸盐或拥挤试剂中的至少一种;
34.可选的,所述扩增缓冲液中包含dntps、ntps、atp、缓冲液、磷酸肌酸、肌酸激酶、醋酸盐或拥挤试剂中的至少一种;其中,dntps为脱氧核糖核苷三磷酸包括datp,dgtp,dttp,dctp,ntps为核苷三磷酸,包括腺苷三磷酸(atp)、鸟苷三磷酸(gtp)、胞苷三磷酸(ctp)以及尿苷三磷酸(utp);atp中文名称为腺苷三磷酸。
35.可选的,所述缓冲液a包括tris缓冲液、hepes缓冲液或mops缓冲液;
36.可选的,所述醋酸盐包括醋酸钾或醋酸钠;
37.可选的,所述拥挤试剂包括聚乙二醇、聚乙烯醇、聚氧化乙烯、葡聚糖或聚蔗糖;
38.可选的,所述拥挤试剂为平均分子量范围为8000-35000的聚乙二醇;
39.可选的,所述拥挤试剂为平均分子量为35000的聚乙二醇。
40.可选的,所述报告分子为单链rna,所述单链rna的一端修饰荧光基团,另一端修饰淬灭基团;
41.可选的,所述单链rna的5’端修饰荧光基团f,3’端修饰淬灭基团q;
42.可选的,所述报告分子为:5
’‑
f-uuuuu-q-3’;
43.可选的,所述荧光基团f为fam、hex、tet、joe或vic,淬灭基团q为bhq1、bhq2或bhq3。
44.所述反应启动剂为含mg
2
的溶液;
45.可选的,所述反应启动剂为醋酸镁溶液或氯化镁溶液;
46.可选的,还包括:针对待测核酸设计的正向引物和反向引物;和/或
47.针对待测核酸的sgrna;
48.可选的,所述正向引物或反向引物中一条引物中含有t7 rna聚合酶启动子序列;
49.可选的,待测核酸为dna或rna;可选的,所述dna为双链dna或单链dna;
50.可选的,待测核酸为rna时,所述酶组合物中还包括逆转录酶;可选的,所述逆转录酶为m-mlv逆转录酶。
51.可选的,利用所述的等温核酸检测试剂盒配制的等温核酸检测反应体系,按50μl反应体系计,包括如下终浓度的组分:
52.引物:正向引物和反向引物的浓度各为300-500nm;sgrna:浓度为50-200nm;
53.所述酶组合物:重组酶、重组酶辅助蛋白、单链结合蛋白、dna聚合酶、cas13a蛋白和t7 rna聚合酶;重组酶、重组酶辅助蛋白、单链结合蛋白、dna聚合酶和cas13a蛋白的质量比为1:(0.2-4.6):(0.77-2.3):(0.2-1):(0.1-1.2);其中,重组酶200-500ng/μl,t7 rna聚合酶0.2-1u/μl;
54.所述扩增缓冲液:dntps中每种碱基的浓度均为150-300μm、ntps中每种碱基的浓
度均为1-3mm,atp为1-5mm、醋酸盐为60-100mm、tris缓冲液为30-100mm、磷酸肌酸为40-100mm,肌酸激酶50-100ng/μl,聚乙二醇35000 5-8%w/v;
55.所述报告分子浓度为100-500nm;
56.所述反应启动剂浓度为10mm-30mm;
57.可选的,包括如下终浓度的组分:
58.引物:正向引物和反向引物的浓度各为420nm;sgrna:浓度为100nm;
59.所述酶组合物:重组酶260ng/μl,重组酶辅助蛋白88ng/μl,单链dna结合酶300ng/μl,链置换dna聚合酶90ng/μl,cas13a蛋白35ng/μl,t7 rna聚合酶20u;
60.所述扩增缓冲液:dntps中每种碱基的浓度均为240μm、ntps中每种碱基的浓度均为2mm,atp为5mm、醋酸盐为100mm、tris缓冲液为100mm、磷酸肌酸为40mm,肌酸激酶90ng/μl,聚乙二醇35000 5%w/v,t7 rna聚合酶20u;
61.所述报告分子浓度为250nm;
62.所述反应启动剂浓度为20mm。
63.一种所述的等温核酸检测试剂盒在核酸检测中的用途;
64.可选的,在检测核酸突变中的用途;
65.可选的,所述核酸突变包括单个碱基突变和>1个碱基突变;
66.可选的,在检测单核苷酸多态性中的用途。
67.一种利用所述的等温核酸检测试剂盒的等温核酸检测方法,包括:
68.取待测核酸,然后利用所述的等温核酸检测试剂盒配制等温核酸检测反应体系,随后恒温反应,并进行检测;
69.可选的,所述恒温反应的条件为:温度35-42℃,时间为20-60min;
70.可选的,所述检测中,为实时荧光定量检测。
71.本发明技术方案,具有如下优点:
72.1、本发明提供了一种用于等温核酸检测的酶组合物,包括重组酶、单链结合蛋白、dna聚合酶、重组酶辅助蛋白、t7 rna聚合酶和cas13a蛋白;利用所述酶组合物进行等温核酸检测时,将核酸扩增和检测整合到一起,实现对目的片段的一步法扩增及检测,将会对操作和应用带来极大的方便。
73.2、本发明提供的一种等温核酸检测试剂盒,包括:酶组合物、扩增缓冲液、报告分子和反应启动剂;利用所述试剂盒进行等温核酸检测时,将核酸扩增和检测整合到一起,实现对目的片段的一步法扩增及检测。
74.3、本发明提供的一种等温核酸检测方法,不需要大型仪器设备,可在短时间内,实现目的片段的检测,适用于现场检测及适用于大规模的筛选。
75.4、本发明提供的一种等温核酸检测方法,可将等温扩增和crispr-cas13a蛋白检测有机结合起来,可通过在一管中一步法来实现。
附图说明
76.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前
提下,还可以根据这些附图获得其他的附图。
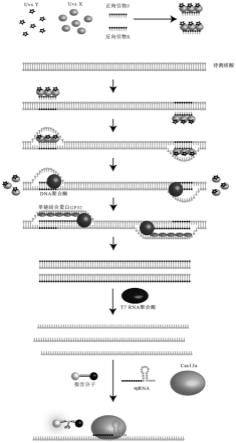
77.图1是本发明实施例6中等温核酸检测的原理;
78.图2是本发明实施例1中表达载体pet-28a-uvsx的质粒图谱;
79.图3是本发明实施例2中表达载体pet-28a-uvsy的质粒图谱;
80.图4是本发明实施例3中表达载体pet-28a-gp32的质粒图谱;
81.图5是本发明实施例4中表达载体pet-28a-cas13a的质粒图谱;
82.图6是本发明实施例6中等温核酸检测结果;
83.图7是本发明实施例8中等温核酸检测结果。
具体实施方式
84.提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
85.实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
86.下述实施例中的金黄色葡萄球菌的dna聚合酶i大片段,购自北京百奥莱博科技有限公司,货号mt0192。t7 rna聚合酶购自thermofisher,货号ep0112。
87.实施例1 uvsx蛋白的获取
88.(1)构建表达载体
89.在ncbi上查找埃希氏杆菌属噬菌体rb69病毒(enterobacteria phage rb69)编码重组酶uvsx的基因序列,genbank序列号为nc_004928.1,uvsx基因的核苷酸序列如seq id no:1所示,uvsx基因编码的蛋白的氨基酸序列如seq id no:9所示。委托上海生工合成uvsx基因全长片段(核苷酸序列如seq id no:1所示),并克隆至pet-28a表达载体的ndei和saci酶切位点之间,构建表达载体pet-28a-uvsx,上述表达载体pet-28a-uvsx为委托上海生工合成,其质粒图谱如图2所示。
90.(2)构建重组工程菌及发酵
91.将重组表达载体pet-28a-uvsx转化到大肠杆菌bl21(de3)中,并涂于含30μg/ml kan的平板(lb琼脂平板)上,37℃培养12h-16h,挑取单克隆菌株,加入1l终浓度为30μg/ml的kan的lb液体培养基中培养4h,加入终浓度为0.7mm的iptg诱导,30℃过夜培养,收取菌液,5000rpm离心30min,得到菌体。
92.(3)uvsx蛋白纯化
93.首先用缓冲液将其菌体进行超声破碎,取上清,10000rpm离心30min,使用ni swpharose
tm 6 fast flow(购买的公司及货号:ge,11-0008-87af)在akta仪器上纯化,缓冲液冲洗至基线水平,然后用含咪唑浓度为250mm的缓冲液洗脱蛋白,洗脱后的蛋白经过sephadex g25(ge,17-0033-01)色谱柱脱盐(脱盐洗脱溶液:含250mm nacl,20mm tris-hcl(ph 7.5),1mm edta)最终得到蛋白,-70℃保存,得到纯化后的uvsx蛋白。
94.实施例2 uvsy蛋白的获取
95.(1)构建表达载体
96.在ncbi上查找埃希氏杆菌属噬菌体rb69病毒(enterobacteria phage rb69)编码重组酶uvsy的基因序列,genbank序列号为nc_004928.1。uvsy基因的核苷酸序列如seq id no:2所示,该基因编码的蛋白的氨基酸序列如seq id no:10所示,委托上海生工合成uvsy基因全长片段(核苷酸序列如seq id no:2所示),克隆至pet-28a 表达载体的ndei和bamhi酶切位点之间,构建得到pet-28a-uvsy表达载体,上述表达载体pet-28a-uvsy表达载体由上海生工合成,其质粒图谱如图3所示。
97.(2)构建重组工程菌及发酵
98.将重组表达载体uvsy转化到大肠杆菌bl21(de3)中,并涂于含30μg/ml kan平板(lb琼脂平板)上,37℃培养12h-16h,挑取单克隆菌株,加入1l终浓度为30μg/ml的kan的lb液体培养基中培养4h,加入终浓度为0.5mm的iptg诱导,30℃过夜培养,收取菌液,5000rpm离心30min,得到菌体。
99.(3)uvsy蛋白纯化
100.同实施例1中“(3)uvsx蛋白纯化”的步骤,得到纯化后的uvsy蛋白。
101.实施例3gp32蛋白的获取
102.(1)构建表达载体
103.在ncbi上查找埃希氏杆菌属噬菌体rb69病毒(enterobacteria phage rb69)编码单链结合蛋白gp32的基因序列,genbank序列号为nc_004928.1。gp32基因的核苷酸序列如seq id no:3所示,该基因编码的蛋白的氨基酸序列如seq id no:11所示。委托上海生工合成gp32基因全长片段(核苷酸序列如seq id no:3所示),将此片段克隆至pet-28a 表达载体的ndei和bamhi酶切位点之间,构建表达载体pet-28a-gp32,上述的表达载体pet-28a-gp32由上海生工合成,其质粒图谱见图4。
104.(2)构建重组工程菌及发酵
105.将重组表达载体pet-28a-gp32转化到大肠杆菌bl21(de3)中,并涂于含30μg/ml kan平板(lb琼脂平板)上,37℃培养12h-16h,挑取单克隆菌株,加入1l终浓度为30μg/ml的kan的lb液体培养基中培养4h,加入终浓度为1mm的iptg诱导,30℃过夜培养,收取菌液,5000rpm离心30min,得到菌体。
106.(3)gp32蛋白的纯化
107.同实施例1中“(3)uvsx蛋白纯化”的步骤,得到纯化后的gp32蛋白。
108.实施例4cas13a蛋白的获取
109.(1)构建表达载体
110.在ncbi上查找韦德纤毛菌(leptotrichia wadei)编码cas13a基因序列(leptotrichia wadei,lwacas13a)的基因序列,genbank序列号为nz_ki271421.1。cas13a基因的核苷酸序列如seq id no:4所示,该基因编码的蛋白的氨基酸序列如seq id no:12所示。委托上海生工合成cas13a基因全长片段,将合成的cas13a基因克隆到t载体上,然后用ndei和saci双酶切,并将此片段克隆至pet-28a表达载体的ndei和saci酶切位点之间,构建表达载体pet-28a-cas13a,上述表达载体pet-28a-cas13a由上海生工合成,其质粒图谱见图5。
111.(2)构建重组工程菌及发酵
112.将重组表达载体pet-28a-cas13a转化到大肠杆菌bl21(de3)中,并涂于含30μg/ml kan平板(lb琼脂平板)上,37℃培养12h-16h,挑取单克隆菌株,加入1l终浓度为30μg/ml的kan的lb液体培养基中培养4h,加入终浓度为1mm的iptg诱导,30℃过夜培养,收取菌液,5000rpm离心30min,得到菌体。
113.(3)cas13a蛋白的纯化
114.同实施例1中“(3)uvsx蛋白纯化”的步骤,得到纯化后的cas13a蛋白。
115.实施例5一种酶组合物、等温核酸检测试剂盒
116.酶组合物:实施例1制备的uvsx蛋白,实施例2制备的uvsy蛋白,实施例3制备的gp32蛋白,金黄色葡萄球菌的dna聚合酶i大片段,实施例4制备的cas13a蛋白;上述的uvsx蛋白、uvsy蛋白、gp32蛋白、dna聚合酶和cas13a蛋白的质量比为1:88/260:300/260:90/260:35/260,t7 rna聚合酶在使用时的终浓度为0.4u/μl
117.本实施例提供了一种等温核酸检测试剂盒,包括:
118.上述的酶组合物;
119.扩增缓冲液:dntps,ntps、atp,tris缓冲液,磷酸肌酸,肌酸激酶,聚乙二醇35000或醋酸钾;
120.报告分子:序列为:5
’‑
f-uuuuu-q-3’,其中f为fam荧光基团,q为bhq1淬灭基团;
121.反应启动剂:醋酸镁溶液。
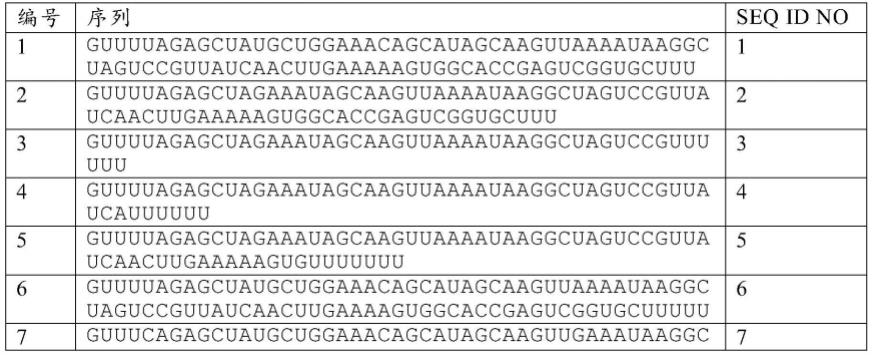
122.进一步的,还包括针对待测核酸(拟南芥基因组dna序列见seq id no:7的6-203位)设计的正向引物(核苷酸序列如seq id no:5所示)和反向引物(核苷酸序列如seq id no:6所示);
123.进一步的,还包括针对待测核酸(拟南芥基因组dna)的sgrna序列如seq id no:8所示。
124.利用上述等温核酸检测试剂盒可以配制等温核酸检测反应体系,按50μl反应体系计,包括如下终浓度的组分:
125.引物:正向引物和反向引物的浓度各为420nm;
126.所述报告分子浓度为250nm;
127.sgrna浓度为100nm;
128.所述酶组合物:实施例1制备的uvsx蛋白260ng/μl,实施例2制备的uvsy蛋白88ng/μl,实施例3制备的gp32蛋白300ng/μl,金黄色葡萄球菌的dna聚合酶i大片段90ng/μl,实施例4制备的cas13a蛋白35ng/μl;t7 rna聚合酶20u。
129.所述扩增缓冲液:dntps中datp、dttp、dctp、dgtp均为240μm、ntps中atp、utp、ctp、gtp均为2mm、atp为5mm、醋酸钾100mm、tris缓冲液为100mm、磷酸肌酸为40mm,肌酸激酶90ng/μl,聚乙二醇35000的浓度为5%w/v;
130.所述反应启动剂浓度为20mm。
131.实施例6一种等温核酸检测方法
132.本实施例提供了一种等温核酸检测方法,包括如下步骤:
133.(1)采用takara的植物dna提取试剂盒,按照试剂盒说明书提取拟南芥(中国农业大学提供)叶片的基因组dna,备用。
134.(2)以步骤(1)中的基因组dna(不同浓度)或双蒸水为模板,然后利用实施例5中的
no:5所示)和反向引物(核苷酸序列如seq id no:6所示)
149.所述报告分子:序列为:5
’‑
f-uuuuu-q-3’,其中f为fam荧光基团,q为bhq1淬灭基团,浓度为250nm;
150.sgrna浓度为100nm(核苷酸序列如seq id no:8所示);
151.所述酶组合物:实施例1制备的uvsx蛋白260ng/μl,实施例2制备的uvsy蛋白88ng/μl,实施例3制备的gp32蛋白300ng/μl,金黄色葡萄球菌的dna聚合酶i大片段90ng/μl,实施例4制备的cas13a蛋白35ng/μl;t7 rna聚合酶20u。
152.所述扩增缓冲液:dntps中datp、dttp、dctp、dgtp均为240μm、ntps中atp、utp、ctp、gtp均为2mm、atp为5mm、tris缓冲液为50mm、磷酸肌酸为40mm,肌酸激酶90ng/μl,聚乙二醇35000的浓度为2%w/v;
153.将上述混合试剂分装到200μl离心管中,-70℃冷冻1-2小时后,冻干机中过夜冻干,得到干粉管。
154.所述独立包装的醋酸镁溶液浓度为200mm。
155.所述独立包装的反应缓冲液:100mm tris缓冲液、200mm醋酸钾、6%(w/v)聚乙二醇35000。
156.实施例8一种等温核酸检测方法
157.本实施例提供了一种等温核酸检测方法,包括如下步骤:
158.(1)拟南芥基因组dna提取:同实施例6中步骤(1),备用。
159.(2)以步骤(1)中的基因组dna(不同浓度)或双蒸水为模板,然后利用实施例7中的等温核酸检测试剂盒,配制如下的等温核酸检测反应体系,按50μl反应体系计,如下表1。
160.表1
[0161][0162]
表1中的模板分别为双蒸水、拟南芥基因组dna原液(拟南芥基因组dna终浓度为106ng/μl)、10倍体积稀释的拟南芥基因组dna(拟南芥基因组dna终浓度为10.6ng/μl)、100倍体积稀释的拟南芥基因组dna(拟南芥基因组dna终浓度为1.06ng/μl)。混合均匀后,加入到干粉管中进行反应。
[0163]
将上述反应体系在37℃下在天隆荧光定量pcr仪器(gentier 96e)中反应60min,程序设置如下:变性(37℃,15s)-复性(37℃,15s)-延伸(37℃,30s),设定60个循环,检测通道为fam荧光检测通道。
[0164]
检测结果如图7所示,本实施例的等温核酸检测方法,本实施例的冻干后的检测酶
组合物,可以很好的将核酸的扩增和检测整合到一起,操作方便,结果良好。
[0165]
实施例9一种酶组合物、等温核酸检测试剂盒
[0166]
酶组合物:实施例1制备的uvsx蛋白,实施例2制备的uvsy蛋白,实施例3制备的gp32蛋白,金黄色葡萄球菌的dna聚合酶i大片段,实施例4制备的cas13a蛋白;上述的uvsx蛋白、uvsy蛋白、gp32蛋白、dna聚合酶和cas13a蛋白的质量比为1:0.2:0.77:0.2:0.1,t7 rna聚合酶在使用时的终浓度为0.2u/μl
[0167]
本实施例提供了一种等温核酸检测试剂盒,包括:
[0168]
上述的酶组合物;
[0169]
扩增缓冲液:dntps,ntps、atp,hepes缓冲液,磷酸肌酸,肌酸激酶,聚乙二醇35000或醋酸钠;
[0170]
报告分子:序列为:5
’‑
f-uuuuu-q-3’,其中f为tet荧光基团,q为bhq2淬灭基团;
[0171]
反应启动剂:氯化镁溶液。
[0172]
进一步的,还包括针对待测核酸(拟南芥基因组dna序列见seq id no:7的6-203位)设计的正向引物(核苷酸序列如seq id no:5所示)和反向引物(核苷酸序列如seq id no:6所示);
[0173]
进一步的,还包括针对待测核酸(拟南芥基因组dna)的sgrna序列如seq id no:8所示。
[0174]
利用上述等温核酸检测试剂盒可以配制等温核酸检测反应体系,按50μl反应体系计,包括如下终浓度的组分:
[0175]
引物:正向引物和反向引物的浓度各为300nm;
[0176]
所述报告分子浓度为100nm;
[0177]
sgrna浓度为50nm;
[0178]
所述酶组合物:实施例1制备的uvsx蛋白、实施例2制备的uvsy蛋白、实施例3制备的gp32蛋白、金黄色葡萄球菌的dna聚合酶i大片段和实施例4制备的cas13a蛋白的质量比例为1:0.2:0.77:0.2:0.1;其中实施例1制备的uvsx蛋白500ng/μl;t7 rna聚合酶终浓度为0.2u/μl。
[0179]
所述扩增缓冲液:dntps中datp、dttp、dctp、dgtp均为150μm、ntps中atp、utp、ctp、gtp均为1mm、atp为1mm、醋酸钠为60mm,hepes缓冲液为30mm、磷酸肌酸为100mm,肌酸激酶50ng/μl,聚乙二醇8000的浓度为8%w/v;
[0180]
所述反应启动剂浓度为10mm。
[0181]
实施例10
[0182]
本实施例与实施例6的区别在于,采用实施例9的试剂盒进行等温核酸检测,反应体系在35℃下在天隆荧光定量pcr仪器(gentier 96e)中反应40min,检测通道为tet荧光检测通道。
[0183]
实施例11一种酶组合物、等温核酸检测试剂盒
[0184]
酶组合物:实施例1制备的uvsx蛋白,实施例2制备的uvsy蛋白,实施例3制备的gp32蛋白,金黄色葡萄球菌的dna聚合酶i大片段,实施例4制备的cas13a蛋白;上述的uvsx蛋白、uvsy蛋白、gp32蛋白、dna聚合酶和cas13a蛋白的质量比为1:4.6:2.3:1:1.2,t7 rna聚合酶在使用时的终浓度为1u/μl;
[0185]
本实施例提供了一种等温核酸检测试剂盒,包括:
[0186]
上述的酶组合物;
[0187]
扩增缓冲液:dntps,ntps、atp,mops缓冲液,磷酸肌酸,肌酸激酶,聚乙二醇35000或醋酸钾;
[0188]
报告分子:序列为:5
’‑
f-uuuuu-q-3’,其中f为vic荧光基团,q为bhq3淬灭基团;
[0189]
反应启动剂:醋酸镁溶液。
[0190]
进一步的,还包括针对待测核酸(拟南芥基因组dna序列见seq id no:7的6-203位)设计的正向引物(核苷酸序列如seq id no:5所示)和反向引物(核苷酸序列如seq id no:6所示);
[0191]
进一步的,还包括针对待测核酸(拟南芥基因组dna)的sgrna序列如seq id no:8所示。
[0192]
利用上述等温核酸检测试剂盒可以配制等温核酸检测反应体系,按50μl反应体系计,包括如下终浓度的组分:
[0193]
引物:正向引物和反向引物的浓度各为500nm;
[0194]
所述报告分子浓度为500nm;
[0195]
sgrna浓度为200nm;
[0196]
所述酶组合物:实施例1制备的uvsx蛋白、实施例2制备的uvsy蛋白、实施例3制备的gp32蛋白、金黄色葡萄球菌的dna聚合酶i大片段和实施例4制备的cas13a蛋白的质量比例为1:4.6:2.3:1:1.2;其中,实施例1制备的uvsx蛋白200ng/μl;t7 rna聚合酶的终浓度为1u/μl。
[0197]
所述扩增缓冲液:dntps中datp、dttp、dctp、dgtp均为300μm、ntps中atp、utp、ctp、gtp均为3mm、atp为3mm、醋酸钾为100mm、mops缓冲液为60mm、磷酸肌酸为70mm,肌酸激酶100ng/μl,聚乙二醇8000的浓度为6%w/v;
[0198]
所述反应启动剂浓度为30mm。
[0199]
实施例12
[0200]
本实施例与实施例6的区别在于,采用实施例11的试剂盒进行等温核酸检测,反应体系在42℃下在天隆荧光定量pcr仪器(gentier 96e)中反应20min,检测通道为vic荧光检测通道。
[0201]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。