1.本发明涉及一种掺入抗微生物剂的可溶胀聚合物纤维及其制备方法,特别是,但不限于,涉及一种用作伤口敷料的掺入抗微生物剂的可溶胀聚合物纤维。
背景技术:
2.已经开发出了多种不同的敷料以用于治疗从擦伤和割伤到更严重和疑难的伤口(例如烧伤或溃疡)的多种不同类型的伤口。特别地,后一种类型的伤口往往会产生大量的更常规的护垫和绷带所不能吸收的渗出物。
3.伤口敷料可以由纱布、薄膜、机织织物或无纺布和可溶胀材料形成,所述可溶胀材料包括水胶体、海藻酸盐、水凝胶、多糖。此类伤口敷料可以是天然的或合成的,并且专门针对它们的生物相容性而设计。
4.对于诸如烧伤或溃疡之类的重大伤口,通过向伤口中引入抗微生物剂来防止感染是有利的。这可以直接在施用新鲜敷料之前施用,或者最近可以将抗微生物剂掺入随后将直接放置在伤口上的敷料中。几个世纪以来,人们就知道碘的治疗性和抗微生物性,富碘植物被用于制备局部贴剂以减少疼痛并帮助伤口愈合。碘载体是碘与增溶剂或载体的络合物。当将载体掺入伤口敷料中并呈递至与伤口渗出物接触的伤口上时,该载体还起控制碘的解离以提供持续释放的作用。最近在医学应用中发现的特别碘载体是聚维酮碘(povidone-iodine,pvp-i),它是聚乙烯吡咯烷酮与三碘化离子的复盐。存在于伤口敷料中的碘载体的抗微生物活性取决于可释放到伤口中或伤口上的“游离”碘(可选地称为“可用”碘)的量。这种可用碘可以通过碘量法定量地识别出。
5.wo 2013/140362 a1公开了一种具有抗微生物和生物可降解性能的聚合物复合材料。所述材料用于形成具有防腐作用的医疗装置,所述材料由海藻酸盐的基质和pvp-i形成。该复合材料可用于制备可释放碘的薄膜、微胶囊和缝合线。
6.ep 0532275 b1描述了一种伤口敷料,其具有由多糖或纤维素聚合物与润湿剂一起形成的无水水溶性凝胶。该敷料还可包含药物或添加剂,例如氯己定、银化合物或抗微生物剂如pvp-i。
7.us 2011/0171284 a2描述了一种用于伤口愈合的医用敷料,其包括蔗糖、pvp-i和足以使组合物增稠以控制蔗糖和碘向伤口释放的胶凝剂。
8.wo 2013/078998 a1描述了用于治疗急性眼科感染的含有pvp-i的缓释眼科组合物。该组合物包括药学上可接受的赋形剂(如水)和与海藻酸钠形成微球的pvp-i。
9.us 6,897,349 b2描述了用于制备适于用作伤口敷料以控制和处理渗出物引流的含银抗微生物亲水材料的方法和组合物。
10.us 2014/0356454 a1描述了一种抗微生物伤口敷料,其来自具有均匀掺入基质中的银离子的凝胶形成纤维,例如纤维素或海藻酸盐纤维。
11.然而,需要提供增强的渗出液处理和药物活性剂的持续释放和控制释放的抗微生物伤口敷料。
技术实现要素:
12.本发明的一个目的是提供一种具有药物活性的纤维、单丝(filament)、纱线或适合作为伤口敷料的材料,其具有吸湿性,同时提供抗微生物剂的持续释放和控制释放。本发明的另一个目的是提供一种具有用于治疗从轻微的切割和擦伤到诸如烧伤和溃疡的更严重的形式的各种不同类型的伤口所需物理和机械特性的纤维、无纺毡、机织材料或针织材料。
13.这些目的是通过提供一种纤维、纱线、多丝(multi filament)和/或具有增强的吸湿性能以及碘(作为抗微生物剂)的控制释放和持续释放的材料来实现的。特别地,当使本发明的材料定位于伤口处时,其可有效地实现从伤口以及穿过材料的所需的湿蒸气透气率(moisture vapour transmission rate,mvtr),实现所需的物理完整性以便在吸收湿气和渗出物时不降低保湿性,以提供潮湿的润湿剂,同时当需要时还能够方便地从伤口上释放或分离。
14.根据本发明的第一方面,提供了一种可溶胀生物相容性材料,其通过使具有吸水性的可溶胀聚合物与含有抗微生物剂的溶液接触以使抗微生物剂被可溶胀聚合物吸收的方法形成;该溶液包括:水;聚维酮碘;和配置成控制碘从材料中的释放的水溶性控制化合物。
15.将本发明的材料和方法专门设计用于提供具有所需的湿蒸气透气率、物理完整性的吸湿的抗微生物结构,从而除了在伤口处提供抗微生物剂的控制释放和持续释放之外,当暴露于渗出物并且处于吸湿溶胀构型时不会降解。
16.本发明的材料和方法可以使用各种不同的一次聚合物(primary polymer),包括天然或合成的材料。该一次聚合物是吸湿性可溶胀聚合物,并且包括例如多糖或多糖基材料、水胶体、生物聚合物。一次聚合物的优选形式是水溶性聚合物。此类聚合物可以是多糖海藻酸盐。
17.任选地,基材可以包括非水溶性合成聚合物材料,例如聚酯、聚酰胺、纤维素聚合物、丙烯酸聚合物或生物聚合物。
18.本发明的纤维和方法可以使用另外的化合物来进一步控制碘从纤维中的释放。此类另外的组分可以包括二次化合物(优选水溶性但可以是非水溶性的),例如聚醚、烷基醚、二醇(如丙二醇(pg))、多元醇或具有c-o-c键的化合物(例如聚丙二醇(ppg)或聚乙二醇(peg))。
19.特别地,优选水溶性控制化合物是极性的或至少部分极性的。假定水溶性控制化合物可以通过静电学和/或结构构象相互作用,从而至少部分地抑制碘从pvp络合物中的解离。因此,通过碘和/或碘络合物与水溶性控制化合物的相互作用,可以抑制碘从材料中的不受控制的释放或自由释放。
20.任选地,可溶胀聚合物可包含:多糖;多糖基材料;水胶体形成化合物。
21.任选地,具有吸水性的可溶胀聚合物可包含以下物质中的任意一种或其组合:海藻酸盐;壳聚糖;几丁质;果胶;羧甲基纤维素;羟丙基甲基纤维素;结冷胶;魔芋;欧车前;或合成聚合物,例如聚酯、聚酰胺、聚丙烯腈。
22.更优选地,水溶性控制化合物包括丙二醇和/或聚乙二醇,其中水溶性控制化合物的浓度使得当暴露于伤口处的湿气/渗出物时提供碘从材料的所需的持续释放。基于材料
的总重量,最终材料(适合用作伤口敷料)中的这种浓度可以在0.5重量%至40重量%、0.5重量%至30重量%、0.5重量%至25重量%、或1.0重量%至20重量%的范围内。
23.优选地,该溶液还包含极性有机溶剂。该极性有机溶剂作为减少形成水溶液的水量的替代物是有利的。已经发现这有助于干燥处理过的材料以除去多余的液体。向与本发明材料接触的溶液中引入极性有机溶剂还有利于提高最终材料的柔软度。如将认识到的,这样的性能对于用作伤口敷料是有利的。任选地,极性有机溶剂包括以下中的任意一种或其组合:醛、酮、醇、缩醛或具有羟基或羰基的化合物。更优选地,极性有机溶剂可以包括丙酮和/或异丙醇。
24.根据本发明的另一方面,提供了一种可溶胀的生物相容性材料,其包含:具有吸水性的可溶胀聚合物;聚维酮碘;和配置成控制碘从可溶胀聚合物中的释放的水溶性控制化合物。
25.任选地,基于材料的总重量,所述材料可包含0.5重量%至40重量%、0.5重量%至30重量%、0.5重量%至25重量%、或1.0重量%至20重量%的聚维酮碘。
26.根据本发明的另一方面,提供了一种形成可溶胀生物相容性材料的方法,所述方法包括:提供溶液,该溶液包括:水;聚维酮碘;和配置成控制碘从所述材料的释放的水溶性控制化合物,使具有吸水性的可溶胀聚合物与所述溶液接触,以使聚维酮碘至少能被所述可溶胀聚合物吸收;和去除水和/或使可溶胀聚合物干燥。
27.任选地,使可溶胀聚合物与溶液接触的步骤包括将聚合物浸入、浸泡、沉浸、蘸入在含有pvp-i的溶液中或在含有pvp-i的溶液中染色(dyeing)。可溶胀材料与溶液之间的这种接触可以分批进行,或者可以是使用例如滚筒、输送系统、移动喷头、压延等的连续过程。这样的系统是可以通过使用采用传感器、可编程逻辑控制器、电子控制板、计算机等运行软件和适当的用户界面来提供本地或远程控制和状态监测的电子控制而自动化的。
28.任选地,该方法可包括使用输送系统,其中相对于至少一个喷嘴或喷头移动或输送可溶胀聚合物以将溶液喷施到可溶胀聚合物上;或者相对于所述可溶胀聚合物移动或输送所述至少一个喷嘴或喷头以将所述溶液喷施到所述可溶胀聚合物上。这样的系统可以包括多个喷嘴或喷头,以将溶液以并联或串联的方式施加到可溶胀聚合物上。可以理解,多次喷施应用配置成根据需要改变pvp-i在材料中的浓度。优选地,基于最终材料的总重量,该材料包括浓度为0.5重量%至10重量%、0.5重量%至8重量%、0.5重量%至6重量%或1重量%至4重量%的“游离”pvp-i。然而,本发明的吸湿材料可包含高达20重量%级别的较高浓度pvp-i。这样的浓度对于某些应用可能是有利的,在这些应用中存在高感染风险和需要高细菌控制。
29.任选地,使可溶胀聚合物与溶液接触的步骤包括在高压容器内使所述聚合物与所述溶液接触,并对溶液施加压力以促进聚维酮碘向可溶胀聚合物中的吸收。
30.任选地,使可溶胀聚合物与溶液接触的步骤包括在轻微张力下将聚合物材料均匀地沉浸在溶液中。这避免了变形和将材料移出溶液。随后在受控压力下压延,以便于聚维酮碘向可溶胀聚合物中的吸收。
31.任选地,本发明的材料可以是各种不同的形式,例如纤维基材料、棉条(sliver)或粗纱。任选地,本发明的材料可以是无纺材料、机织材料或针织材料。优选地,本发明的材料是由用于形成复合纤维的多丝纱线形成的毡基材料。
32.重要的是,本发明的纤维和材料一旦被制造,就包含所需的含湿量(moisture content)。这避免了所得纤维的聚集,这对于多丝基材料是特别重要的。另外,重要的是提供一种所得材料,该材料包括总体均匀的结构,该结构没有裂纹或不希望的大内部空腔或另外与允许完全干燥的材料相关的空隙。具有所需含湿量的材料便于用作放置在伤口上的伤口敷料,并获得所需的物理和机械特性,例如所需的湿蒸气透气率,渗出物吸收等。任选地,本发明的纤维和材料包含5%至60%、10%至60%、15%至55%、20%至50%、25%至50%、30%至50%、30%至45%或35%至40%的湿气范围内的含湿量。含湿量可以通过任何合适的方法测定。例如,含湿量可以通过从适当润湿的纤维或材料中减去纤维或材料的干重,然后将该差值(含湿量)除以完全润湿的纤维/材料的总重量来确定。因此,本文所报告的含湿量的值是润湿材料内液体量的相对湿度(重量%)范围。
33.本发明的纤维和材料可以包括润湿液体,所述润湿液体是以下中的任意一种或其组合:水、水基溶液、有机液体、有机溶液、丙酮、异丙醇。
34.任选地,本发明的纤维和/或材料可包含至少一种附加的或另外的抗微生物剂。另外的抗微生物剂可以包括银、银离子、或含银化合物。任选地,另外的抗微生物剂包含金属物质,该金属物质是zn、cu、ti、pt、pd、bi、sn、sb中的一种或其组合。
35.优选地,该方法还包括在允许润湿的基材干燥之前,压缩、挤压或压制润湿的基材以排出多余的水分。压缩或压制润湿的基材有利于驱动用碘络合物浸渍纤维。另外,该步骤有助于碘络合物在纤维表面上和任选地在纤维体的芯部或内部区域中的均匀分布。
36.根据本发明材料的另一个方面,提供了一种伤口敷料,其包含本文所述和所要求保护的材料。本发明的材料可包括在材料平面(侧向:纵向和横向)内以及在相应的第一接触面和第二接触面之间穿过材料的深度或厚度(垂直于材料平面)的均匀浓度的抗微生物剂。任选地,本发明的材料可包括在横向方向上或穿过材料的厚度或深度的渐变浓度或不均匀浓度的抗微生物剂。例如,第一接触面可以包括相对于第二表面更高浓度的pvp-i。这样的构型可以提供一种材料,该材料通过以一个或两个取向(即正面或反面接触)放置在伤口处而提供不同水平的抗微生物活性。
37.根据本发明的另一个方面,提供了一种如本文所述和要求保护的材料,它是下列材料中的任何一种:鼻腔填充材料;牙科填充材料;缝合线;或泄液线(seton)。任选地,当用作伤口敷料或填充材料时,本发明的材料是无纺布。任选地,当用作缝合线或泄液线时,本发明的材料是纤维状的。
附图说明
38.现在将仅通过示例方式并参考附图来描述本发明的具体实施方式,其中:
39.图1示意性地示出了用于将聚维酮碘(pvp-i)引入到可溶胀生物相容性材料中的装置,其包括多孔滚筒和溶液分配容器;
40.图2示意性地示出了图1的装置的变型,该装置还包括位于多孔滚筒和高压容器之间的泵;
41.图3示意性地示出了使用加压反应容器将pvp-i引入可溶胀材料所选择的部件;
42.图4示意性地示出了用于将pvp-i引入到可溶胀聚合物中的装置,该装置包括输送系统以横向平移喷头附近的可溶胀材料,该喷头适于将pvp-i溶液喷施到所输送的可溶胀
材料;以及
43.图5示意性地示出了用于将聚维酮碘(pvp-i)引入到可溶胀生物相容性材料或非溶胀材料的装置,该装置包括容纳溶液的浸渍槽、浸入导向辊和一对压延(mangling)辊;
44.图6示意性地示出了根据另一具体实施方式的用于将聚维酮碘(pvp-i)引入到可溶胀生物相容性材料或非溶胀材料中的装置,该装置包括容纳溶液的浸渍槽、浸入导向辊和一对压延辊;
45.图7示意性地示出了根据另一具体实施方式的用于将聚维酮碘(pvp-i)引入到可溶胀生物相容性材料或非溶胀材料中的装置,该装置包括容纳溶液的浸渍槽、浸入导向辊和一对压延辊;
46.图8示意性地示出了根据另一具体实施方式的用于将聚维酮碘(pvp-i)引入到可溶胀生物相容性材料或非溶胀材料中的装置,该装置包括容纳溶液的浸渍槽、浸入导向辊和一对压延辊,以及干燥室;
47.图9是使用葡萄球菌(staphyloccus)和克雷伯氏菌(klebsiella),在可溶胀材料内存在的抑制区域与可用碘的坐标图。
具体实施方式
48.本发明的抗微生物可溶胀纤维适用于制造无纺毡状材料、机织材料或针织材料,此类材料又可用作伤口敷料,用于治疗从割伤和擦伤到更严重的烧伤、溃疡(其中渗出液处理是关键的)等各种不同类型的伤口。本发明材料可方便地由浸制(infusing)工艺、浸泡工艺、沉浸(immersing工艺)或染色工艺形成,在这些工艺中将纤维、棉条、粗纱、机织材料、无纺材料或针织材料引入到通常含有聚维酮碘(pvp-i)的水性溶液中。本发明的材料和方法提供了用于生产在纤维/纱线芯部中和在纤维/纱线的表面掺入了“可用的”碘的高度可溶胀材料的工艺参数。碘是碘络合物的形式并以足以提供抗微生物活性的浓度水平而被包含。这样的浓度水平可以是在纤维的总重量中大于1重量%“游离”碘的级别。将本发明的材料和方法专门设计用于提供具有所需的湿蒸气透气率(mvtr)、物理完整性的材料,从而当暴露于渗出物并处于吸湿溶胀构型时不会降解,此外还在伤口处提供抗微生物的控制释放和持续释放。
49.本发明的材料和方法可以使用各种不同的一次聚合物,包括天然或合成材料。此类的一次聚合物是吸湿性可溶胀聚合物,并且包括例如多糖或多糖基材料、水胶体、生物聚合物。一次聚合物的优选形式是水溶性聚合物,例如但不限于多糖海藻酸盐。
50.本发明的纤维和方法可以使用另外的化合物来进一步控制碘从纤维中的释放。此类另外的组分可以包括二次水溶性控制化合物,例如聚醚、烷基醚、二醇(如丙二醇(pg))、多元醇或具有c-o-c键的化合物(例如聚丙二醇(ppg)或聚乙二醇(peg))。
51.本实施例描述了将pvp-i以各种形式(例如纤维、棉条、粗纱、无纺布、机织织物或针织织物)掺入海藻酸盐和类似生物材料中的方法。本方法均包括提供含有溶剂化pvp-i的溶液,然后使吸湿可溶胀聚合物与该溶液接触,以至少使pvp-i被聚合物吸收。可以理解,所得材料包括可溶胀聚合物,该聚合物具有吸附在材料纤维内的pvp-i以及吸附在纤维表面的pvp-i。pvp-i的这种双重存在提供了至少两种释放机制。例如,当伤口敷料与伤口接触时,吸附在纤维表面上的pvp-i可以迅速和/或立即释放,而吸附的pvp-i(合并在纤维/纱线
芯部)可以适合于随着时间的推移而更缓慢更持续的释放。也存在于该材料的纤维/纱线中的水溶性控制化合物提供了对“游离”碘释放的进一步控制以促进持续释放。
52.实施例
53.各种示例性方法均可用于制造根据本发明的可溶胀生物相容性材料。这些方法可以i)使用例如开放的或加压的腔室分批处理,或ii)例如在环境压力或高压下使用可旋转的滚筒或输送系统连续制造,或iii)使用浸渍槽和压延辊的分批或连续制造系统中进行。
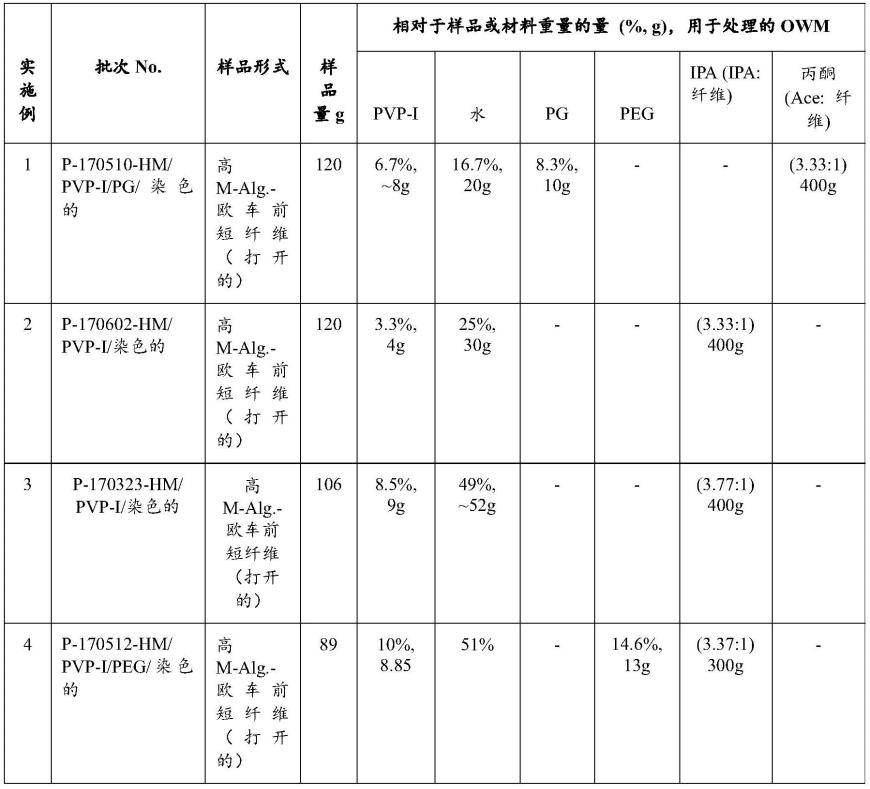
54.通常,参照表1的所用材料的浓度和用量,使用各种百分比(基于待处理的生物材料的重量)的pvp-i、水、ipa(和/或丙酮)、peg(和/或pg)来制备溶液。称取所需pvp-i到水中或水/peg或pg中,手动溶解或用graves小型高剪切搅拌机溶解。然后加入所需的其他物质并混合,直到获得均匀的本体溶液(bulk solution)用于染色。
55.初始实施例-分批
56.可溶胀吸湿材料可通过材料与pvp-i的简单“染色”来制备。在这种方法中,可使用容器、腔室或罐来容纳pvp-i溶液。在某些实施例中,然后可以根据常规染色方法将基于聚合物的无纺毡状材料浸入、放入或浸泡在溶液中。这种方法可以在环境压力和环境温度下进行。
57.特别地,将尺寸为65cm
×
130cm的海藻酸盐毡小心地折叠,避免拉伸以装入含有一半染色溶液的染色容器中。将现在折叠的毡(如20cm
×
20cm尺寸)转移到容器(例如10升桶)中,并使用桨叶或任何具有平底的不粘器具将毡压入溶液中。然后将溶液的后半部分倒入毡的顶部,轻轻向下压毡,直到所有表面由溶液均匀地覆盖。继续在容器中轻轻下压和移动材料,直到所有的溶液被吸收到材料中。取出染色的材料,将其放置在平坦的聚乙烯黑袋的顶部,轻轻展开,在通风柜的提取系统下留置干燥至少4小时。在干燥期间,将材料翻转,使得两侧同样干燥。适当干燥后,将材料折叠并放入密封的镀银袋中并储存以供分析。在一些情况下,将部分的染色材料切割,在没有遮盖的实验室中留置暴露,观察颜色变化以确定材料中pvi的稳定性。
58.由单一层处理的材料生产各种厚度或宽度的无纺布。为了生产双层处理毡,使用两个相同尺寸的单一层处理毡或折叠成一半的单一层处理毡。将毡的一面放置在干净的平坦表面上,并将相同毡的另一面(顶面)用包含与用于单一层处理的相同量的pvp-i和peg或pg的1-3%w/w的高g海藻酸盐溶液均匀地薄薄地涂抹。然后将毡折叠成一半,将涂抹面合在一起,或者如果使用两个单独的单一层处理的毡,则小心地将第二层对称地放置在涂抹的顶部上,并施加均匀的压力以将毡粘结在一起。这种压力是通过将尺寸稍大并含均匀分布的重量的平板放置在组合毡的顶部并使其在该位置保持至少2小时来实现。最后,将(现在合并的)毡取出,与燕尾夹(纸夹活页夹)一起悬挂以防止过度收缩,并在提取系统下适当干燥至少5小时。
59.为了生产三层处理的毡,使用三个相同的单独层的经处理的单一层毡。在一层的两面上如上所述的高g海藻酸盐/pvp-i/peg溶液涂抹,然后将其夹在另外两层之间并如上所述处理。
60.对于纤维,它们可以像粗纱那样粘结在一起并连续染色,但是当纤维为短纤维形式,适当地分离和打开时,获得最佳结果。一些纤维含有丝束油剂(例如吐温20(高达3.5%)并且无问题地处理。溶液制备和材料处理与如上所述的用于无纺布的相同。在处理过程中,
在干燥之前和之后,观察到一些短纤维滚动成小球。但是在干燥之后,它们是柔软的并且容易打开。
61.表1:通过“染色”工艺,向生物材料中掺入pvp-i
62.[0063][0064]
表2:一些海藻酸盐、海藻酸盐/欧车前纤维或用含有pg或peg的pvp-i染色的毡的吸液能力和滞留性能的一些示例。
[0065][0066]
因此,本发明的方法提供了一种用于将pvp-i掺入纤维、纱线、棉条、粗纱等基材(包括机织织物、无纺布和针织结构)中的通用处理路线。本方法和材料的优点在于:
[0067]
·
pvp-i可以均匀溶解,并且可以完全和容易地施加到基材上。
[0068]
·
使用的溶剂在任何程度上与水和组合物中的其它添加剂(例如二醇(如丙二醇)或多元醇(例如异丙醇))可混溶。
[0069]
·
使用的主要液体仅是pvp-i载体,其不与组合物中的pvp-i或其它化学物质反应
[0070]
·
主介质是挥发性溶剂,其在施用后通过简单的抽提容易地从基材/pvp-i/添加剂组合物或体系中去除。
[0071]
所用的有机溶剂优选为无毒醇、酮、乙酸酯或其混合物。这些溶剂可以相对于基材的2:1至5:1的比例加入。类似地,如本文所述,染色方法也可以通过从加压容器或填充有pvp-i/peg(或pg)/ipa/水的溶液的罐中喷施基材来实现。
[0072]
如表2所示,基于初始实施例的材料,该方法显著改善了所有实施例(特别是那些含有高g海藻酸盐的实施例)中的纤维和毡强度、吸收能力和碘滞留性。
[0073]
表3:用含有pg或peg的pvp-i染色的一些海藻酸盐、海藻酸盐/欧车前纤维或毡的碘含量的实施例。
[0074][0075][0076]
表3示出了被测试的一些样品中的碘含量(碘 可滴定碘)。所获得的结果都是可喜的,因为它们显示出与市售产品inadine
tm
(1600mg/kg)相当的含量(1200-2100mg/kg)。可用碘(可用硫代硫酸钠滴定的碘)的百分比也满足所有商业要求。表3还说明了在染色浴中使用3-10%的pvp-i实现了样品中1%可用碘的商业目标。
[0077]
如参照图6和表4所详细描述的,这些实施例证明了样品中可用碘的量与其对细菌(特别是葡萄球菌)的效力之间的相关性。对克雷伯氏菌的影响不太明显。
[0078]
表4:一些选定样品的抑制区域和抗微生物功效。
[0079][0080]
海藻酸盐-碘-乙二醇纤维和毡的生产
[0081]
通过将非复合碘掺入纤维和毡中,研究了二醇(pg和peg)对pvp-i从纤维中“浸出”的潜在控制作用,通过如下进行:
[0082]
·
挤出含溶解碘晶体的掺杂物
[0083]
·
用含有溶解的碘晶体的溶液对纤维或无纺布进行染色。
[0084]
除了使用0.5%w/w碘晶体(由alfa aesar提供,mp 183-1860c,mol.wt(或fw253.81,密度4.930g/cm3)代替pvp-i之外,样品制备如实施例1中针对海藻酸盐-pvp-i纤维所述。在加入到溶液中并混合均匀以得到非常深的溶液之前,使用少量的pg或peg使用moldal/杵研磨碘晶体。
[0085]
所生产的纤维最初具有深碘颜色,但是在暴露于空气中时,这种颜色很快褪色,甚至在密封之后,碘逐渐从纤维中蒸发出来,使其无色。pg或peg的加入延缓了蒸发,但并不停止蒸发。
[0086]
另外的实施例-分批
[0087]
参照图3,可使用高压容器18将无纺毡19与pvp-i(和添加剂)溶液31组合。特别是,氮气或压缩空气可以通过入口17引入容器18。容器18还包括减压阀22和连接到排出管20的
出口/出口30,排出管20又可连接到回流管系统(未示出)。泵21驱动pvp-i溶液31从混合罐25的引入。溶液31可以使用搅拌机24进行搅拌。溶液31通过导管32、33被泵入高压容器18,并被泵入喷头23以输送到基材19上。容器18内增加的压力将溶液驱入可溶胀材料的纤维中,然后可将其从容器18中抽出并干燥。
[0088]
另外的实施例-连续
[0089]
参照图1,可根据连续处理用pvp-i溶液处理无纺毡状基材,在所述连续处理中以非分批方式将含抗微生物剂的溶液施加或递送到基材上。参照图1,无纺基材19可被卷绕到安装在轴34上并可由发动机15可旋转地驱动的可旋转滚筒13上。滚筒13包括穿孔14。滚筒组件13、34、14可安装在提取室或系统(未示出)内。连接管道12在滚筒13和容纳pvp-i(和添加剂)溶液31的供应箱11之间提供联接。在操作中,溶液31通过管道12供应到滚筒13。溶液31从滚筒内部通过穿孔14流到基材19上,基材19连续地缠绕在滚筒外表面。可以对溶液31施加压力,迫使其通过穿孔14,以驱动pvp-i向基材19的可溶胀聚合物中的吸收。
[0090]
图2示出了图1的实施例的变型,其进一步包括泵16,以进一步在压力下将溶液31驱动到滚筒13中。pvp-i在可溶胀材料纤维上的吸收和吸附程度可以通过控制施加的压力10和/或泵16来控制。
[0091]
实施例4-连续
[0092]
参照图4,无纺可溶胀材料19可以通过输送系统用pvp-i饱和或浸渍。特别地,将无纺基材19传送到输送系统27上,该输送系统27在相对于各个输送器36安装在不同位置的多个喷头29下方提供基材19的横向平移。至少一些输送器36在通风和干燥室28内通过。作为连续过程,pvp-i(和添加剂)溶液31经由喷头29喷施到移动的基材19上。卷绕辊37可定位在输送器36的末端,以收集准备进行下游处理(即切割,冲压等)浸渍的基材。
[0093]
实施例5-连续
[0094]
参照图5,将来自加工线或卷轴的无纺布、丝束、丝或纱线形式的基材53通过浸渍辊58浸渍在包含在槽54中的pvp-i溶液55中。将载有pvp-i的基材缓慢地拉出溶液并在导向辊56上导向,并在具有可变压力系统的一对光滑压延辊57之间通过,其中pvp-i被轻轻压入基材中,多余的溶液被压出并返回到槽中。监测槽中溶液的液位并通过打开阀52从罐51补充溶液来使其保持恒定。使用搅拌机50来制备pvp-i溶液,并在必要时进行非定时的搅拌。然后,在进一步处理之前,将处理过的基材59通过干燥室(未示出)并干燥。
[0095]
参照图6,被强制驱动到传送传送带61的无纺布形式的基材53通过浸渍传送带62浸渍在包含在浴54中的pvp-i溶液55中。载有pvp-i的基材平铺在进料传送带64上并缓慢移动通过溶液,然后在一对具有可变压力系统65的变速光滑压延辊57之间供料,其中pvp-i被轻轻压入基材中,多余的溶液被压出并返回到浸渍浴54中。监测槽中的溶液液位并通过打开阀52从罐51补充溶液来使其保持恒定。使用搅拌机50来制备pvp-i溶液,并在必要时进行不定时的搅拌。在卷绕到卷轴上(如果需要的话)以便进一步处理之前,将处理过的基材59通过第二进料传送带64上的干燥室28(图6中未示出,但参照图4和8进行了描述)并进行干燥。
[0096]
参照图7,将正向驱动到进料传送带61的基材在可变压力下直接进料至变速压延辊中,但是在进入压延辊之前,使用蠕动泵以恒定的速率将pvp-i溶液从罐51供料,并通过合适的喷嘴将pvp-i溶液递送到基材上。载有pvp-i的基材平缓地通过辊之间,pvp-i溶液在
辊之间被压入基材中,多余的溶液(如果有的话)被压出到槽54中以重复使用。如前所述,然后将处理过的基材引导到通过干燥室的传送带上,干燥并卷绕到卷轴上以用于进一步处理。该方法简单,避免了传送带和pvp-i溶液的过度使用,也避免了pvp-i溶液因蒸发而过度损失。
[0097]
参照图8,将从卷轴正向驱动的基材平缓地放置在传送带62的顶部,在传送带62处用pvp-i溶液以受控的速度从花洒样系统29中喷施。然后,载有pvp-i的基材平缓地通过压延辊之间,在压延辊处pvp-i溶液被压入基材中,多余的溶液(如果有的话)被压出到槽54中以重复使用。如前所述,然后将处理过的基材引导通过干燥室的到传送带上,干燥并卷绕到卷轴67上以用于进一步处理。
[0098]
抗微生物活性测试
[0099]
从初步研究中并如图6和表4中详细描述的,上述实施例中选择的实施例证明了样品中可用碘的量与其对细菌(特别是葡萄球菌)的效力之间的相关性。对克雷伯氏菌的影响不太明显。然后根据aatcc测试方法100进一步测试上述各种实施例的抗微生物活性性能。
[0100]
特别地,将金黄色葡萄球菌(staphylococcus aureus,atcc 6538)和铜绿假单胞菌(pseudomonas aeruginosa,atcc 9027)悬浮液制备成在胰蛋白胨大豆肉汤(tsb)中为1.0
×
106cfuml-1
。通过在tsb中进行10倍稀释并将所得悬浮液铺在胰蛋白胨大豆琼脂(tsa)上来计数接种物。将每种细菌悬浮液的1ml等分试样用于接种对照并测试敷料(尺寸4.2
×
4.2cm)。测试敷料在37
±
2℃下温育24小时;之后,在10ml中和器中中和敷料。超声处理测试敷料样品5分钟以从敷料中回收微生物。将得到的悬浮液连续稀释并铺到tsa上以定量活的生物体。同时测试阴性对照、阳性对照和无菌对照样品。阴性对照是与测试样品相同的海藻酸盐基材料,但是未经聚维酮碘处理。阳性对照是含有银的商购羧甲基纤维素敷料。样品一式三份测试。
[0101]
性能结果
[0102]
金黄色葡萄球菌
[0103]
在0小时时,从阴性对照中回收平均5.61
±
0.27log
10
cfu/样品金黄色葡萄球菌。在检测限(最小检测限为1log)内测试的用实施例11至14(xirams 21s和21t)处理后,未回收到活的金黄色葡萄球菌。与阴性对照相比,这相当于4.61
–
5.61
±
0.27log
10
cfu/样品的对数减少。
[0104]
表5:金黄色葡萄球菌的抗微生物活性结果
[0105][0106]
铜绿假单胞菌
[0107]
在0小时时,从阴性对照中回收平均6.12
±
0.05log
10
cfu/样品铜绿假单胞菌。在检测限(最小检测限为1log)内测试的用实施例11至14(xirams 21s和21t)处理后,未回收到活的铜绿假单胞菌。与阴性对照相比,这相当于5.12
–
6.12
±
0.05log
10
cfu/样品的对数减少。
[0108]
表6:铜绿假单胞菌的抗微生物活性结果
[0109][0110]
生物膜破坏的测试-cdc生物反应器
[0111]
使用cdc生物反应器测试上述各种实施例破坏生物膜的性能。特别地,使用金黄色葡萄球菌(nctc 8325)和铜绿假单胞菌(ncimb 10434)的培养物来制备单种细菌接种物(1x107±
5x106cfuml-1
)。将制备的金黄色葡萄球菌和铜绿假单胞菌细菌悬浮液用于接种含有聚碳酸酯取样片(coupons)的独立的的无菌cdc反应器。将cdc反应器在轨道式微生物培养箱中在37℃
±
2℃下温育72小时以促进生物膜生长。温育后,将含有生物膜的取样片在pbs中洗涤以除去浮游细菌,然后用伤口敷料(2
×
2cm)处理24小时。同时检测阴性对照和阳性对照。阴性对照敷料是与测试样品相同的海藻酸盐基材料,但是未经聚维酮碘处理。阳性对照敷料是含银的商购羧甲基纤维素敷料。还包括内部阴性和阳性对照处理,它们分别是pbs 1%tsb和基于漂白剂的产物。样品一式三份测试。
[0112]
处理后,将取样片转移到10ml中和剂中,并将取样片超声处理5分钟以回收剩余的附着微生物。对所得回收培养基进行连续稀释,并定量总的活生物体。
[0113]
性能结果
[0114]
金黄色葡萄球菌
[0115]
从内部阴性对照和阴性对照敷料中分别回收到平均5.55
±
0.42log
10
cfuml-1
和5.71
±
0.49log
10
cfuml-1
的活的金黄色葡萄球菌。在用实施例11至14(xirams 21s和21t)、内部阳性对照和阳性对照敷料处理后,未回收到活的金黄色葡萄球菌。与内部阴性对照相比,这是5.55log
10
cfuml-1
的减少。
[0116]
表7:金黄色葡萄球菌的生物膜破坏(cdc生物反应器结果)
[0117][0118]
铜绿假单胞菌
[0119]
从内部阴性对照和阴性对照敷料中分别回收到平均7.09
±
0.06log
10
cfuml-1
和6.43
±
0.48log
10
cfuml-1
活的铜绿假单胞菌。在用实施例11至14(xirams 21s和21t)、内部阳性对照和阳性对照敷料处理后,未回收到活的铜绿假单胞菌。与内部阴性对照相比,这是7.09log
10
cfuml-1
的减少。
[0120]
表7:铜绿假单胞菌的生物膜破坏(cdc生物反应器结果)
[0121]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。