来自ipsc的皮质神经祖细胞
1.相关申请的交叉引用
2.根据35 u.s.c.
§
119(e),本技术要求2019年10月22日提交的美国临时申请号62/924,523的权益,以引用的方式将它们的内容以其整体并入本文。
技术领域
3.本文描述了源自人诱导多能干细胞(ipsc)的神经祖细胞(npc),所述ipsc可经工程化以可诱导的方式表达异位蛋白并用于移植宿主中的植入。要求保护的发明涉及再生医学和退行性疾病(包括神经退行性疾病)的技术领域。
背景技术:
4.神经退行性疾病是严重的经济和护理负担,对于老龄化群体而言这种负担只会继续增长。在这些疾病中,肌萎缩性侧索硬化症(als)在美国有约30,000个体受其困扰。目前,只有依达拉奉和利鲁唑这两种经fda批准的药物用于治疗该疾病,两者都只能稍微减缓疾病的进展。有希望的临床前治疗包括支持性胶质细胞的移植和胶质细胞系源性神经营养因子(gdnf)的递送。发明人的团队已经产生并广泛表征了人胎儿来源的神经祖细胞(fnpc),这些细胞可分化为星形胶质细胞,并且可用慢病毒转染以稳定地产生gdnf。这些产生gdnf的细胞有效地植入脊髓并减缓sod1 als大鼠中chat 运动神经元的损失。这些细胞已根据临床生产质量管理规范(cgmp)进行储存,并且发明人将所述细胞作为第一细胞和基因疗法递送至als患者的脊髓而完成了1/2a期试验。虽然很有希望,但fnpc的可扩展使用受到起始材料可得性的限制,并且扩增潜力有限。此外,用于在这些细胞中诱导gdnf表达的慢病毒转导产生了具有不同拷贝数和gdnf产生水平的异质群体。因此,本领域非常需要产生适用于神经退行性治疗的移植材料(包括克隆性)的可再生来源,以及能够植入移植宿主的细胞。
技术实现要素:
5.本文描述了源自人诱导多能干细胞(ipsc)的可扩展的、适用于临床生产质量管理规范(cgmp)的神经祖细胞系的生产。这些源自ipsc的细胞有效地植入als大鼠脊髓,并为患病的运动神经元提供神经保护,类似于临床研究中使用的胎儿来源的细胞。利用ipsc的克隆扩增能力,克隆品系由插入aavs1安全着陆位点的单拷贝gdnf构建体产生。这些品系均一地表达和产生gdnf。这为产生具有用于经调节的gdnf表达的更复杂的构建体(包括四环素诱导型启动子)的源自ipsc的神经祖细胞系提供了平台。这些新的基于ipsc的品系可扩展至临床相关的生产量,均一地生产gdnf,在体内安全长达三个月,并代表了用于als的有希望的新联合疗法。
附图说明
6.图1a-图1c示出了pb-rtp-tet-gdnf/memclover-fluc载体的示意图。(图1a)pb-rtp-tet-gdnf/memclover-fluc质粒被设计为在与pbase质粒组合转染时稳定整合至基因
组中。(图1b)pbase质粒。(图1c)组成型表达或仅在多西环素存在的情况下表达的转基因。
7.图2展示了aavs1-teton-hgdnf的载体图谱。示出的是ha-l和ha-r臂,其为可用于靶向基因组安全港(如aavs)的同源重组序列。
8.图3展示了pdonor-teton3g-2a-tagbfp-v5-nls-p2a-puror wpre_insulated mpclover-2a-luc2pest-2a-gdnf wpre的载体图谱。
9.图4示出了人ppp1r12c基因的外显子1和2之间的内源性基因座的aavs1靶向的示意图。最初,由报告子/筛选盒(用于荧光和抗生素筛选的tagbfp2和puror)和组成型cag启动子驱动的td-tomato红色荧光顺反子组成的接受者的“着陆位点”被稳定地整合;所述报告子/筛选盒由与上游ppp1r12c连接的剪接受体驱动;所述td-tomato红色荧光顺反子侧接有loxp和frt位点。随后,在这些报道基因的稳定筛选后,将这些细胞用表达flpo和cre的质粒、含有侧接有loxp和frt的筛选/报告子盒的供体质粒、以及含有dox诱导型的mpclover/luc2p/gdnf顺反子的质粒进行脂质体转染。
10.图5a-图5d示出了inpc在组成上与cns10-npc相似。cns10-npc和inpc直接从冷冻保存中解离成单细胞,并且经处理用于单细胞rnaseq或者在培养基中铺板并生长7天。(图5a)细胞的无偏聚类显示ipsc与inpc(粉色)和cns10-npc是分开的。观察到一些inpc与cns10-npc成簇。(图5b)以与每个类别25-50个基因构建的模块的相似性对每个簇的转录物表达进行评分。标度:黄色=高表达,紫色=低表达。(图5c)无偏聚类的特征图示出了成熟和未成熟的星形胶质细胞相关转录物在inpc和cns10-npc(而不在ipsc中)中的表达。(图5d)针对第7天的inpc和cns10-npc培养物的免疫细胞化学示出了在体外这两种细胞类型中s100β(灰色)和gfap(白色)蛋白的表达。inpc插图示出了用星形胶质细胞因子培养35天后的gfap(灰色)表达。比例尺=75μm,插图25μm。
11.图6a-图6d示出了用于对ipsc系中的gdnf表达进行工程化的组成型和诱导型构建体。(图6a)图例示出了靶向aavs1的gdnf表达构建体的组分。(图6b)gdnf elisa证明了容纳有组成型gdnf构建体的inpc产生与经慢病毒转导的inpc和cns10-npc细胞两者相似水平的gdnf。(图6c)具有v1诱导型构建体的inpc的gdnf elisa示出了响应于添加和撤掉多西环素的稳健且有效的诱导和衰减。(图6d)具有v1诱导型构建体的inpc在移植到给予处于饮用水中的多西环素的wt大鼠的腰脊髓中时不能表达gdnf。比例尺=75μm。
12.图7示出了aavs1的talen靶向。示意图示出了左侧和右侧的tale核酸酶以及aavs1同源性。
13.图8a-图8b示出了源自ipsc的细胞存活并保护chat 运动神经元。sod1
g93a
大鼠被移植有经慢病毒转导的当前inpc,以在腰脊髓中产生gdnf。(图8a)10k细胞/位点n=5只动物。移植保留了宿主chat 运动神经元。(图8b)每个位点50k细胞n=3只动物。细胞不是保护性的并取代了宿主神经元。比例尺250μm。
14.图9a-图9b示出了9个月后在裸大鼠脊髓中的inpc的植入。对腰脊髓进行切片并对于人细胞核(sc121,绿色)和增殖细胞(ki67,白色)进行染色。左侧,脊髓的内侧前角的一侧中的inpc-gdnfconst-v1植入物的lw放大图像。方框指示了示出阳性人细胞(图9a)和阴性人细胞(图9b)的更高放大倍数区域。星号指示中央管。比例尺为100μm且更高放大倍数中为25μm。
15.图10展示了aavs1-tet-on-3g-gdnf(seq id no:5)的载体图谱。
16.图11展示了示例性分化方案和时间线的示意图。
具体实施方式
17.如所描述的,发明人已经进行了胎儿神经祖细胞(fnpc)的临床研究,fnpc可分化成星形胶质细胞并且可用慢病毒转染以稳定产生gdnf。这些产生gdnf的细胞在sod1 als大鼠中有效地植入脊髓并减缓chat 运动神经元的损失。尽管取得了这些惊人的进步,胎儿神经祖细胞仍有数个缺点。首先,作为不可再生资源的胎儿组织的可得性和变异性。这包括发明人的基于胎儿组织单品系g010的临床试验。该品系的剩余材料的量有限,并且没有获得新原料的来源。干细胞的胎儿来源的第二个主要缺点是使用慢病毒方法产生随机的整合,这在使用胎儿神经祖细胞来源时产生异源群体。
18.这些限制通过本文提供的源自人诱导多能干细胞(ipsc)的神经祖细胞而被具体地解决。ipsc为能够按需生产的可再生细胞来源,解决了胎儿细胞来源的第一个限制。第二个限制被ipsc的克隆扩增能力所消除,其中可均一地引入基因构建体,包括诱导型表达系统或有效利用基因编辑技术(如crispr)。存在进一步的优势(例如自体疗法的前所未有的机会),可以想象到地规避与同种异体人细胞移植的免疫排斥紧密相关的复杂性。虽然ipsc(包括发明人自己的工作)已被用于产生神经祖细胞样细胞,但本文所述的源自ipsc的神经祖细胞能够植入到移植宿主中。这一重要特性支持通过移植将所述细胞用于再生医学的可行性。
19.将人神经祖细胞移植到脑或脊髓中以替代失去的细胞、调节损伤的环境或创造允许的环境以保护和再生宿主神经元长期以来一直是神经系统疾病的有希望的治疗策略。先前,发明人能够将粘附的ipsc转化为能够扩增的自由浮动的球状体(ez球状体)。使用全反式维甲酸(atra)和表皮生长因子(egf)和成纤维细胞生长因子-2(fgf-2)有丝分裂原的组合,这些ez球状体可向具有脊髓表型的npc球状体分化。然而,这些细胞不能有效地植入,从而限制了它们在再生医学疗法中的有效使用。
20.推进源自ipsc的npc向临床应用的发展可包括:1)安全性;2)维持正常细胞遗传学状态;3)缺乏残留的多能细胞以避免可能的恶性肿瘤形成;4)大量扩增细胞的重现性;以及5)本文提供的细胞的存活、整合和植入到相关的中枢神经系统区域。
21.虽然神经元替代是未来临床移植试验的一种策略,但星形胶质细胞是人脑和脊髓中最丰富的细胞类型,并且现在被认为对于脑的功能像神经元一样重要。它们还牵涉于许多神经退行性疾病,最好的实例可能是als。在als中,胶质功能障碍已被显示为引发运动神经元的非细胞自主死亡。无论是幼稚的还是分泌生长因子的星形胶质细胞的替代已被显示为在als模型中有益。发明人先前的研究表明,fnpc可产生星形胶质祖细胞,所述星形胶质祖细胞随后在啮齿动物脑和脊髓内于长时间段中分化为未成熟和成熟的星形胶质细胞。人psc也可被引导至更成熟的星形胶质细胞。虽然此种源自psc的成熟星形胶质细胞可在移植后存活,但从ipsc产生的未成熟npc可提供更容易在体外培养和扩增并且更适合在体内迁移、整合和恢复功能的细胞。
22.另外,使用源自干细胞的神经祖细胞将营养因子用于脑是绕过血脑屏障的有力方式。在肌萎缩性侧索硬化症(als)和帕金森氏病、亨廷顿氏病和阿尔茨海默氏病的疾病模型中,使用离体的遗传学上修饰的细胞将各种生长因子递送至受损部位已显示出支持宿主神
经元。同时,胶质细胞系源性神经营养因子(gdnf)的递送为帕金森病患者带来了益处,并且目前正在针对als患者的1/2a期临床试验中进行测试。为了充分利用营养因子的益处并避开通过细胞递送的营养因子的潜在的有害作用,调节生长因子的分泌是多种神经退行性疾病的有希望的途径。由于基因表达和下游信号传导激活是紧密相连的过程,因此在副作用事件中,长期的营养因子递送会关闭或阻止剂量调整。缺乏对基因表达的时机和量级的控制可限制治疗的功效并引入非计划的细胞效应。
23.为此目的,在各种方法学中,四环素(tet)调节系统已用于在时间和空间上调节基因表达。这包括细菌tet反式激活因子(tta),以在存在多西环素(dox)(tet类似物)时沉默tet调节的启动子下游的基因表达。除了此“tet-off”系统外,“tet-on”系统还使用反向tta(rtta)以在存在dox时激活转基因表达。尚未探索在神经干细胞群中的tta和rtta变体的使用。
24.此处,发明人报告了用于产生可扩增的源自人ipsc的神经祖细胞(源自ipsc的npc)的新方案。这些源自人ipsc的npc可很容易地作为悬浮培养物长期增殖,并且类似于在临床研究中被证明是安全有效的人胎儿来源的神经祖细胞(fnpc)。注射后,inpc成功植入,没有肿瘤形成或过度生长的迹象,并且再次表现出与类似的fnpc移植相似(如果不是更好的话)。发明人的结果描述了人神经祖细胞的新来源,它没有fnpc的供应、扩增和伦理问题,并因此可能对于神经退行性疾病(例如als)的基于干细胞的治疗方法而言是理想的。
25.基于所产生的源自ipsc的npc的多功能性,这些细胞可作为在als背景下成功的胎儿g010细胞的完全合适和优越的替代品。进一步的发展将涉及评价源自ipsc的npc在sod-1大鼠中的生长和植入,以及检查这些源自ipsc的npc的长期致瘤性。这进一步包括在sod-1大鼠中的额外的功效研究。此外,这些研究将确认观察到sod-1大鼠显示出在脊髓中的植入和在sod-1中某些细胞剂量下的神经保护作用的初步结果。另外,作为超过9个月的安全性/致瘤性研究,裸大鼠中的致瘤性研究正在进行。
26.额外的信息可见于例如:美国专利申请号62/644,332、62/773,752,pct申请号pct/us2019/022595,pct公开号wo 2017/131926,sareen等,“human neural progenitor cells generated from induced pluripotent stem cells can survive,migrate,and integrate in the rodent spinal cord”j.comp.neurol.2014年8月15日;522(12):2707
–
2728,以及akhtar等,“a transposon-mediated system for flexible control of transgene expression in stem and progenitor-derived lineages”stem cell reports.2015年3月10日;4(3):323
–
331,以引用的方式将其完全并入本文。
27.本文描述了产生源自诱导多能干细胞(ipsc)的神经祖细胞(inpc)的方法。在多种实施方式中,本文提供的inpc由多个诱导多能干细胞产生。在多种实施方式中,本文提供的inpc由表达至少一种干细胞标志物的多个细胞产生。ipsc的特征将在下文进一步讨论。
28.诱导多能干细胞
29.诱导多能细胞由分化的体细胞重编程而产生。尽管在生理背景下分化通常是不可逆的,但已经开发了数种方法来将体细胞重编程为诱导多能干细胞(ipsc)。示例性方法是本领域技术人员已知的并且在下文中简要描述。本文提供的ipsc可通过下文进一步描述的方法产生,或者它们可从商业来源获得,例如从thermofisherstemcell或applied可得的那些。
30.将体细胞重编程为ips细胞的方法描述于例如美国专利号8,129,187b2、8,058,065b2;美国专利申请2012/0021519a1;singh等,front.cell dev.biol.(2015年2月);以及park等,nature 451:141-146(2008);以引用的方式将其整体并入本文。具体而言,ipsc通过引入重编程转录因子的组合而由体细胞产生。可将重编程因子作为例如蛋白质、核酸(mrna分子、dna构建体或编码它们的载体)或其任意组合引入。小分子还可增强或补充引入的转录因子。虽然已确定额外的因子影响例如重编程的效率,但组合时足以将体细胞重编程为诱导的多能状态的四个重编程因子的标准组包括oct4(八聚体结合转录因子-4)、sox2(性别决定区y)-box2、klf4(kruppe样因子-4)和c-myc。额外的蛋白质或核酸因子(或编码它们的构建体)(包括但不限于lin28 nanog、esrrb、pax5 shrna、c/ebpβ、p53 sirna、utf1、dnmt shrna、wnt3a、sv40lt(t)、htert)或小分子化学试剂(包括但不限于bix-01294、bayk8644、rg108、aza、地塞米松、vpa、tsa、saha、pd0325901 chir99021(2i)和a-83-01)已被发现替代来自四个重编程因子的基础或标准组的一种或另外的重编程因子,或提高重编程的效率。
31.重编程是改变或逆转分化细胞(例如体细胞)的分化状态的过程。换而言之,重编程是将细胞分化逆向驱动为更为未分化或更为原始类型的细胞的过程。应当注意的是,在培养物中放置许多原代细胞可引起完全分化特征的一些损失。然而,对包括在术语分化细胞中的此类细胞进行简单培养不会使这些细胞成为非分化细胞或多能细胞。分化细胞向多能性的转变需要重编程刺激,所述刺激超出了在将分化细胞置于培养物中时引起分化特征部分丧失的刺激。相对于原代细胞亲本,重编程细胞还具有延长传代能力而不丧失生长潜力的特征,原代细胞亲本通常在培养物中仅具有有限数量的分裂的能力。
32.待重编程的细胞可在重编程之前部分分化或终末分化。因此,待重编程的细胞可为终末分化的体细胞以及成体或体干细胞。
33.在一些实施方式中,重编程涵盖将分化细胞(例如体细胞)的分化状态完全逆转为多能(pluripotent)状态或多潜能(multipotent)状态。重编程可引起细胞表达特定基因,其表达进一步有助于重编程。
34.源自起始细胞群的重编程效率(即重编程细胞的数量)可通过添加以下所示的各种小分子来增强:shi,y.等,(2008)cell-stem cell 2:525-528,huangfu,d.等,(2008)nature biotechnology 26(7):795-797,以及marson,a.等,(2008)cell-stem cell 3:132-135。增强重编程效率的试剂的一些非限制性实例包括可溶性wnt、wnt条件培养基、bix-01294(g9a组蛋白甲基转移酶)、pd0325901(mek抑制剂)、dna甲基转移酶抑制剂、组蛋白去乙酰化酶(hdac)抑制剂、丙戊酸、5'-氮杂胞苷、地塞米松、辛二酰苯胺异羟肟酸(saha)、维生素c和曲古抑菌素(tsa)等。
35.可对分离的ipsc克隆测试一种或多种干细胞标志物的表达。源自体细胞的细胞中的此种表达将所述细胞鉴别为诱导多能干细胞。干细胞标志物可包括但不限于ssea3、ssea4、cd9、nanog、oct4、fbx15、ecat1、esg1、eras、gdf3、fgf4、cripto、dax1、zpf296、slc2a3、rex1、utf1和nat1等。在一些实施方式中,表达nanog和ssea4的细胞被鉴别为多能的。
36.在本文所述的任一方面的一些实施方式中,本文所述的细胞表达至少一种多能干细胞标志物。用于检测干细胞标志物表达的方法可包括例如rt-pcr和检测编码多肽的存在
的免疫学方法(如蛋白质印迹、免疫细胞化学或流式细胞术分析)。细胞内标志物最好通过rt-pcr鉴别,而细胞表面标志物易于例如通过免疫细胞化学进行鉴别。
37.分离细胞的多能干细胞特性可通过评价ipsc分化为三个胚层中每一个的细胞的能力的测试来确认。作为一个示例,裸小鼠中的畸胎瘤的形成可用于评价经分离的克隆的多能特性。将所述细胞引入裸小鼠,并使用对不同生殖系谱系的标志物具有特异性的抗体对由所述细胞产生的肿瘤进行组织学和/或免疫组织化学。包含来自所有三个胚层(内胚层、中胚层和外胚层)的细胞的肿瘤的生长进一步表明或确认了这些细胞是多能干细胞。
38.通常,在整个分化过程中,多能细胞将遵循沿特定发育谱系(例如原胚层-外胚层、中胚层或内胚层)的发育途径。
39.胚胎胚层是所有组织和器官所源自的来源。所述胚层可通过特定生物标志物的表达和基因表达来鉴别。检测这些生物标志物的测定包括例如rt-pcr、免疫组织化学和蛋白质印迹。由早期中胚层细胞表达的生物标志物的非限制性实例包括hand1、esm1、hand2、hopx、bmp10、fcn3、kdr、pdgfr-α、cd34、tbx-6、snail-1、mesp-1和gsc等。由早期外胚层细胞表达的生物标志物包括但不限于trpm8、pou4f1、olfm3、wnt1、lmx1a和cdh9等。由早期内胚层细胞表达的生物标志物包括但不限于lefty1、eomes、nodal和foxa2等。本领域技术人员在执行分化方案的同时可基于细胞类型和在发育中该细胞所源自的胚层来确定监测何种谱系标志物。
40.方法
41.在体外的特定发育谱系的诱导通过在存在促进谱系定型的特定试剂、载体或其组合的情况下培养干细胞(例如本文提供的ipsc)来实现。通常,本文提供的方法包括向细胞培养基中逐步添加试剂(例如小分子、生长因子、细胞因子、多肽、载体等)或使细胞与促进ipsc向神经祖细胞谱系分化的试剂接触。具体而言,转录因子和生长因子信号传导可用于诱导分化,包括但不限于vegt、wnt信号传导(例如通过β-连环蛋白)、骨形态发生蛋白(bmp)途径、成纤维细胞生长因子(fgf)途径和tgfβ信号传导(例如激活素a)。参见例如sareen等,j comp neurol.(2014),baharvand h等,neural differentiation from human embryonic stem cells in a defined adherent culture condition.int j dev biol.2007;51:371
–
378,并通过引用的方式将其整体并入本文。
42.在细胞个体发育的上下文中,术语“分化(differentiate或differentiating)”是相对术语,意味着“分化细胞”是比其前体细胞沿发育途径进一步发展的细胞。因此,在一些实施方式中,重编程的细胞可分化为谱系限制的前体细胞(例如中胚层干细胞),其转而可进一步沿途径分化为其它类型的前体细胞(例如组织特异性前体),然后分化为终末期分化细胞,所述终末期分化细胞在某种组织类型中发挥特征性作用,并可能保留、也可能不保留进一步增殖的能力。
43.通常,体外分化的细胞将在整个逐步过程中表现出多能性标志物(例如hnf4-α、afp、gata-4和gata-6)的下调,并表现出谱系特异性生物标志物(例如中胚层、外胚层或内胚层标志物)的表达提高。例如参见tsankov等,nature biotech(2015),其描述了人多能干细胞系的表征和沿特定谱系的分化。可通过本领域已知的许多方法监测分化过程的效率。这包括使用标准技术检测胚层生物标志物的存在,所述标准技术例如免疫细胞化学、rt-pcr、流式细胞术、功能测定、显微镜检查等。
44.方法:
45.本文提供的方法包括以下步骤:(i)提供一批量的诱导多能干细胞(ipsc);(ii)在rho激酶抑制剂存在的情况下培养ipsc;(iii)产生单层;(iv)在ldn和sb存在的情况下进一步培养所述ipsc;并且在成纤维细胞生长因子(fgf)、表皮生长因子(egf)和白血病抑制因子(lif)存在的情况下另外地培养所述ipsc,从而产生源自ipsc的npc。
46.在各种实施方式中,本文提供的一批量的ipsc包括处于悬浮的ipsc。在各种实施方式中,产生所述单层包括振摇所培养的ipsc。
47.在各种实施方式中,将本文提供的ipsc在rho激酶抑制剂(rock抑制剂)存在的情况下进行培养。存在与当前方法相容的数种rho激酶抑制剂。在某些实施方式中,所述rho激酶抑制剂包括法舒地尔、ripasudil、netarsudil、rki-1447、y-27632、gsk429286a、y-30141或它们的任意组合。在某些实施方式中,所述rho激酶抑制剂包括y27632二氯化物水合物。在某些实施方式中,将本文提供的ipsc在浓度为至少约0.5μm至约12μm的rho激酶抑制剂中进行培养。在某些实施方式中,将本文提供的ipsc用浓度为约5μm的rho激酶抑制剂进行培养。在某些实施方式中,所述rho激酶抑制剂的浓度为至少1μm或更多、至少2μm或更多、至少3μm或更多、至少4μm或更多、至少5μm或更多、至少6μm或更多、至少7μm或更多、至少8μm或更多、至少9μm或更多、至少10μm或更多、至少11μm或更多、多达12μm。在某些实施方式中,在细胞铺板和用包含ldn和/或sb中的一种或多种的培养基进行处理之前,施用rho激酶抑制剂。
48.在一些实施方式中,将本文提供的ipsc在rho激酶抑制剂(rock抑制剂)存在的情况下培养至少8小时或更长、至少12小时或更长、至少24小时或更长、至少48小时或更长、至少36小时或更长、至少72小时或更长,上至培养3天。
49.在各种实施方式中,将本文提供的ipsc在ldn和sb中的一种或多种存在的情况下进行培养。
50.ldn为激活素受体样激酶(alk)多肽的小分子抑制剂。具体而言,ldn靶向激活素受体样激酶2(alk2)、alk3和alk6受体。sb为tgf-β/激活素/nodal途径的选择性和强效的抑制剂,通过竞争atp结合位点来抑制alk5(ic
50
=94nm)、alk4(ic
50
=140nm)和alk7。它不抑制bmp i型受体alk2、alk3和alk6(参见例如inman等,(2002)molecular pharmacology 62 1 65
‑‑
74.;以及tchieu等,cell stem cell 21(3)399-410.e7.(2017);以及laping等,(2002)molecular pharmacology.62 1 58—64,以引用的方式将其整体并入本文)。alk的抑制通过抑制骨形态发生(bmp)途径和tgfβ信号传导途径来促进祖细胞和ipsc的分化。ldn(例如ldn193189)与sb(例如sb431542)组合的抑制混合物允许通过双重smad抑制(dsmadi)有效产生中枢神经系统细胞。dsmadi的修饰可沿着胚胎的神经轴产生许多不同的神经亚型,包括前脑、中脑和脊髓祖细胞(参见例如tchieu等,cell stem cell 21(3)399-410.e7.(2017))。存在本领域已知的数种ldn小分子、sb小分子和alk抑制剂,包括但不限于ldn193189(例如stemcell technologies-目录号#72147)、sb-431542ldn189、ldn-212854及其衍生物。
51.在其它实施方式中,本文提供的方法进一步包括在ldn和sb存在的情况下将ipsc培养约7天,上至培养约13天。在其它实施方式中,所述方法包括在ldn存在的情况下将ipsc进一步培养至少48小时或更长、至少36小时或更长、至少72小时或更长、至少3天或更长、至少4天或更长、至少5天或更长、至少6天或更长、至少7天或更长、至少8天或更长、至少9天或
更长、至少10天或更长、至少11天或更长、至少12天或更长、至少13天或更长、至少14天或更长,上至培养约15天。在其它实施方式中,所述方法包括在sb存在的情况下将ipsc进一步培养至少48小时或更长、至少36小时或更长、至少72小时或更长、至少3天或更长、至少4天或更长、至少5天或更长、至少6天或更长、至少7天或更长、至少8天或更长、至少9天或更长、至少10天或更长、至少11天或更长、至少12天或更长、至少13天或更长、至少14天或更长,上至培养约15天。在其它实施方式中,所述方法包括在ldn和sb存在的情况下将ipsc进一步培养至少48小时或更长、至少36小时或更长、至少72小时或更长、至少3天或更长、至少4天或更长、至少5天或更长、至少6天或更长、至少7天或更长、至少8天或更长、至少9天或更长、至少10天或更长、至少11天或更长、至少12天或更长、至少13天或更长、至少14天或更长,上至培养约15天。
52.在其它实施方式中,所述方法包括在约4.75μg/ml至约5.75μg/ml存在的情况下对本文提供的ipsc进行培养。在其它实施方式中,所述方法包括在以下浓度的ldn存在的情况下对本文提供的ipsc进行培养:至少3.0μg/ml或更多ldn、至少3.25μg/ml或更多ldn、至少4.25μg/ml或更多ldn、至少4.5μg/ml或更多ldn、至少4.75μg/ml或更多ldn、至少5.0μg/ml或更多ldn、至少5.25μg/ml或更多ldn、至少5.5μg/ml或更多ldn、至少5.75μg/ml或更多ldn、至少6.0μg/ml或更多ldn、至少6.25μg/ml或更多ldn、至少6.5μg/ml或更多ldn、至少6.75μg/ml或更多ldn、至少7.0μg/ml或更多ldn、至少7.25μg/ml或更多ldn、至少7.5μg/ml或更多ldn、至少7.75μg/ml或更多ldn,上至8μg/ml ldn。
53.在其它实施方式中,所述方法包括在约0.5μm至约4μm sb存在的情况下对本文提供的ipsc进行培养。在其它实施方式中,所述方法包括在以下浓度的sb存在的情况下对本文提供的ipsc进行培养:至少0.5μm或更多sb、至少0.75μm或更多sb、至少1.0μm或更多sb、至少1.25μm或更多sb、至少1.5μm或更多sb、至少1.75μm或更多sb、至少2.0μm或更多sb、至少2.25μm或更多sb、至少2.5μm或更多sb、至少2.75μm或更多sb、至少3.0μm或更多sb、至少3.25μm或更多sb、至少3.5μm或更多sb、至少3.75μm或更多sb,上至4.0μm sb。
54.在其它实施方式中,将本文提供的ipsc在成纤维细胞生长因子(fgf)、表皮生长因子(egf)和白血病抑制因子(lif)中的一种或多种存在的情况下进一步培养至少8小时或更长、至少12小时或更长、至少24小时或更长、至少48小时或更长、至少36小时或更长、至少72小时或更长、至少3天或更长、至少4天或更长、至少5天或更长、至少6天或更长、至少7天或更长、至少8天或更长、至少9天或更长、至少10天或更长、至少11天或更长、至少12天或更长、至少13天或更长、至少14天或更长、至少15天或更长,上至培养16天。
55.在其它实施方式中,将本文提供的ipsc在成纤维细胞生长因子(fgf)、表皮生长因子(egf)和白血病抑制因子(lif)存在的情况下进一步培养至少8小时或更长、至少12小时或更长、至少24小时或更长、至少48小时或更长、至少36小时或更长、至少72小时或更长、至少3天或更长、至少4天或更长、至少5天或更长、至少6天或更长、至少7天或更长、至少8天或更长、至少9天或更长、至少10天或更长、至少11天或更长、至少12天或更长、至少13天或更长、至少14天或更长、至少15天或更长,上至培养16天。
56.在其它实施方式中,将本文提供的ipsc在至少约50ng/ml至多达约200ng/ml的浓度的成纤维细胞生长因子(fgf)存在的情况下进一步培养。在其它实施方式中,将本文提供的ipsc在以下浓度的成纤维细胞生长因子(fgf)存在的情况下进一步培养:至少50ng/ml或
更高、至少75ng/ml或更高、至少100ng/ml或更高、至少125ng/ml或更高、至少150ng/ml或更高、至少175ng/ml或更高至约200ng/ml。
57.在其它实施方式中,将本文提供的ipsc在至少约50ng/ml至多达约200ng/ml的浓度的表皮生长因子(egf)存在的情况下进一步培养。在其它实施方式中,将本文提供的ipsc在以下浓度的egf存在的情况下进一步培养:至少50ng/ml或更高、至少75ng/ml或更高、至少100ng/ml或更高、至少125ng/ml或更高、至少150ng/ml或更高、至少175ng/ml或更高至约200ng/ml。
58.在其它实施方式中,将本文提供的ipsc在至少约50ng/ml至多达约200ng/ml的浓度的白血病抑制因子(lif)存在的情况下进一步培养。在其它实施方式中,将本文提供的ipsc在以下浓度的lif存在的情况下进一步培养:至少50ng/ml或更高、至少75ng/ml或更高、至少100ng/ml或更高、至少125ng/ml或更高、至少150ng/ml或更高、至少175ng/ml或更高至约200ng/ml。
59.可将ipsc在上述任一种或多种因子存在的情况下进行培养。在其它实施方式中,将ipsc在以下因子中的每一种存在的情况下培养:rho激酶抑制剂;ldn;sb;fgf、egf和lif的组合。
60.在任一方面的一些实施方式中,本文提供的方法包括inpc分化的步骤。示例性的inpc分化方案如下:
61.1.以任意#个孔的ipsc开始,所述ipsc在6孔板中以约80%-100%汇合度生长。如果细胞密度较高且铺板良好,则可接受进行较大的拆分。例如:2孔-》接种3孔。通常,以1:1的比例拆分是最安全的。拆分后需要完全汇合的孔(无间隙),因此任何达到这点的拆分比都是可接受的。
62.2.吸出培养基并向每个孔加入1.5ml accutase
tm
。
63.3.在37℃、5%co2下孵育约5分钟(如果需要, 2至5分钟)。
64.a.在培养箱中3分钟后,轻轻敲击板的侧面,以促进细胞的上升。
65.4.细胞分离后,向每个孔加入1.5ml mtesr
tm
培养基,并继续轻轻地从孔底部洗去细胞。如果细胞仍然粘附至孔底,使用移液器吸头轻轻刮掉细胞,同时缓慢分配培养基。
66.5.将细胞悬液转移至经标记的15ml锥形管。
67.6.以1,500rpm(~300g)旋转沉降细胞悬液3min。
68.7.轻轻吸出上清液,注意不干扰细胞沉淀。
69.8.以工作浓度为5μm的rock抑制剂 mtesr培养基中轻轻重悬细胞沉淀。
70.a.重悬的体积取决于接种的孔的数量
71.9.每孔接种3ml细胞 mtesr rock抑制剂。
72.10.转移到培养箱,并以x-y方向轻轻振摇培养板,使细胞均匀分布。
73.11.次日:如果细胞已经充分附着并形成了良好的单层,则继续执行下面概述的分化方案-完全更换培养基,每天从孔的侧面轻轻进料3ml。
74.a.第1-10天-将培养基完全更换为神经诱导培养基(nim)。
75.b.在nim进料10次后,将每孔的培养基更换为含有5μm rock抑制剂的sefl。然后使用细胞刮刀从每个孔中取出细胞并转移至t25培养瓶中。
76.c.次日——用新鲜的sefl培养基更换50%-75%的培养基。尽可能多地清除碎片。
可在球状体培养的前几天进行较大的培养基更换,以根据需要去除碎片。
77.d.维持球状体——如果不更快地调整,则每3天进料50%。
78.球状体培养和维持:
79.·
如果未事先调节培养基,则每3天向球状体进料一次。
80.·
培养基通常应每隔一天进行一次调整,由橙-黄色培养基颜色指示。
81.·
根据大小和密度,每7-10天切碎一次球状体。
82.·
如果发生细胞团集和粘附在培养瓶底部,轻轻研磨球状体并沿培养瓶底部冲洗培养基以驱离细胞。
83.表1:用于神经诱导培养基的试剂
84.神经诱导培养基母液浓度工作浓度每100ml添加的体积dmem/f121x50%50mlneurobasal1x50%50mlb27 50x0.5x1mln2100x1x1mll-glut200mm(100x)1x(2mm)1mlneaa100x1x1mlp/s100x0.5x500ul胰岛素9.5-11.5mg/ml4.75-5.75ug/ml50ulldn10mm0.4um4ulsb10mm2um20ul
85.表2:用于皮质球生长培养基的试剂
86.皮质球生长培养基母液浓度工作浓度ex.100mlstemline nsc扩增培养基1x1x100ml肝素5mg/ml5ug/ml100ulfgf100ug/ml100ng/ml100ulegf100ug/ml100ng/ml100ullif10ug/ml10ng/ml100ul
87.载体
88.本文描述了一种方法,所述方法包括提供通过上述产生源自诱导多能干细胞(ipsc)的神经祖细胞(npc)的方法制备的一批量的源自ipsc的npc,以及将至少两种载体引入所述源自ipsc的npc中。本文描述了一种方法,所述方法包括提供通过上述产生源自诱导多能干细胞(ipsc)的神经祖细胞(npc)的方法制备的一批量的源自ipsc的npc,以及将至少一种载体引入所述源自ipsc的npc中。示例性载体在图1a-图4、图6a、图7和图10中描述。
89.通过本文所述的方法产生的源自ipsc的npc可经遗传工程化以表达肽和蛋白质,包括用于治疗疾病(例如als)的治疗剂。示例性载体在图1a-图4、图6a、图7和图10中示出。
90.载体为被设计用于递送至宿主细胞或用于在不同宿主细胞之间转移遗传物质的核酸构建体。如本文所用,载体可为病毒的或非病毒的。术语“载体”涵盖当与适当的控制元件相关联时能够复制并且可以将遗传物质转移到细胞的任何遗传元件。载体可包括但不限于克隆载体、表达载体、质粒、噬菌体、转座子、粘粒、人工染色体、病毒、病毒颗粒等。
91.在一些实施方式中,所述载体选自于由质粒和病毒载体所组成的组。
92.表达载体为指导rna或多肽从其中包含的与载体上的转录调节序列连接的核酸序列表达的载体。表达的序列通常但不必须对所述细胞是异源的。表达载体可包含额外的元件,例如表达载体可具有两个复制系统,从而允许它在两种生物体中得以维持(例如在动物细胞中用于表达以及在原核宿主中用于克隆和扩增)。“表达”是指参与产生rna和蛋白质以及适当时分泌蛋白质的细胞过程,在适用的情况下包括但不限于例如转录、转录物加工、翻译和蛋白质折叠、修饰和加工。“表达产物”包括从基因转录的rna,以及通过对从基因转录的mrna进行翻译获得的多肽。
93.在其它实施方式中,本文提供的一种或多种载体包括piggybac载体和pbase载体。在其它实施方式中,piggybac载体以5'至3'方向包括:表达盒、两个转座子元件和至少一种同源重组序列,所述表达盒包括组成型启动子、包含tet应答元件的诱导型的双向多顺反子启动子和编码蛋白质或肽的序列;其中,所述两个转座子元件侧接于所述表达盒。
94.在其它实施方式中,所述序列编码的蛋白质或肽包括神经营养因子。在其它实施方式中,神经营养因子包括胶质源性神经营养因子(gdnf)。人gdnf的编码序列是本领域已知的,例如ncbi基因id 2668,》nc_000005.10:c37840044-37812677智人(homo sapiens)5号染色体,grch38.p13初级装配体(seq id no:2)。人gdnf的rna转录物序列也是本领域已知的,例如ncbi参考序列:nm_000514.4智人胶质细胞源性神经营养因子(gdnf),转录物变体1,mrna(seq id no:3)。
95.此外,人gdnf的氨基酸序列及其变体是本领域已知的,例如胶质细胞系源性神经营养因子亚型1前原蛋白[智人],ncbi参考序列:np_000505.1(seq id no:4)。
[0096]
在其它实施方式中,本文提供的piggybac载体以5'至3'方向包括:表达盒、两个转座子元件和至少一种同源重组序列,所述表达盒包括组成型启动子、包含tet应答元件的诱导型的双向多顺反子启动子和编码gdnf的序列;其中,所述两个转座子元件侧接于所述表达盒。
[0097]
在其它实施方式中,tet应答元件驱动gdnf转基因的体内表达。
[0098]
在其它实施方式中,同源重组序列包括能够靶向基因组安全港的序列。在其它实施方式中,基因组安全港为以下中的一种:腺相关病毒位点1(aavs1)、趋化因子(c-c基序)受体5(ccr5)基因、小鼠rosa26基因座的人直系同源物。在其它实施方式中,神经祖细胞为植入的神经祖细胞。
[0099]
上述载体的实例包括在图1a中描述的“pb-rtp-tet-gdnf/memclover-fluc”[piggybac-反向反式激活因子/tagbfp2nls/pacr-tet诱导型-gdnf/膜clover-萤火虫荧光素酶](seq id no:1)。
[0100]
此处,所述载体包括两个启动子:组成型活性cmv/鸡β-肌动蛋白(又名cag)启动子和诱导型的双向tre-bi启动子。cag启动子驱动rtta-v10(又名tet-on)反式激活因子、tagbfp2-v5nls(具有v5标签和核定位序列的增强的蓝色荧光蛋白)和嘌呤霉素抗性基因的组成型表达。串联的转基因通过自切割肽接头(p2a)分开。此处,添加四环素类似物或衍生物(多西环素)引起rtta-v10反式激活因子结合至tre-bi启动子并催化下游转基因的转录。tre-bi启动子的第一顺反子容纳有豆蔻酰化和棕榈酰化(myrpalm)的clover报告子(mpclover),后随着不稳定的萤火虫荧光素酶(luc2p)。诱导型tre-bi启动子下游的第二顺
反子可编码神经营养因子(例如gdnf),后随着编码土拨鼠肝炎病毒转录后元件(wpre)以增加基因表达。将兔β-珠蛋白polya置于各自的元件的下游,以终止转录并防止假的转基因表达。可将pb-rtp-tet-gdnf/memclover-fluc载体随着pbase质粒转染,以促进稳定的基因组整合。前述载体的另一实例包括pdonor-teton3g-2a-tagbfp-v5-nls-p2a-puror wpre_insulated mpclover-2a-luc2pest-2a-gdnf wpre。
[0101]
在其它实施方式中,至少一种载体包括表达盒、至少一种同源重组序列,所述表达盒包括可操作地连接至编码蛋白质或肽的序列的诱导型或组成型启动子。在其它实施方式中,所述蛋白质或肽包括神经营养因子。在其它实施方式中,所述神经营养因子包括胶质源性神经营养因子(gdnf)。在其它实施方式中,所述组成型启动子为3-磷酸甘油酸激酶(pgk)启动子。在其它实施方式中,所述同源重组序列包括能够靶向基因组安全港的序列。在其它实施方式中,所述基因组安全港为以下中的一种:腺相关病毒位点1(aavs1)、趋化因子(c-c基序)受体5(ccr5)基因、小鼠rosa26基因座的人直系同源物。在其它实施方式中,所述诱导型启动子包括由四环素类抗生素调节的启动子。在其它实施方式中,所述四环素类抗生素包括多西环素。在其它实施方式中,所述诱导型启动子由反向四环素控制的反式激活因子(rtta)或tet-on高级反式激活因子(rtta2s-m2)调节。在其它实施方式中,所述源自ipsc的npc为植入的源自ipsc的npc。在其它实施方式中,所述源自ipsc的npc表达基因组学上整合的表达盒。在其它实施方式中,所述基因组学上整合的表达盒处于基因组安全港。
[0102]
本文还描述了通过前述方法制备的一批量的细胞,其中,所述源自ipsc的npc表达基因组学上整合的表达盒。例如,通过如下方法制备的能够诱导表达胶质源性神经营养因子(gdnf)的一批量的源自ipsc的npc,所述方法包括:提供一批量的源自ipsc的npc以及引入至少一种载体。在其它实施方式中,所述至少一种载体包括将piggybac载体和pbase载体引入源自ipsc的npc,其中,piggybac载体包括组成型启动子、包含tet应答元件的诱导型的双向多顺反子启动子以及编码gdnf的序列。在各种实施方式中,本文提供的细胞基本上是均质的。
[0103]
在各种实施方式中,所述载体包括至少一种同源重组序列。在其它实施方式中,所述细胞表达来自一种或多种载体的表达盒。在其它实施方式中,表达来自一种或多种载体的表达盒的细胞已被核转染、转染或电穿孔或本领域已知的其它基因递送技术。在其它实施方式中,所述一种或多种载体包括piggybac载体、pbase载体或两者。在其它实施方式中,piggybac载体包括至少两个启动子,其中,至少一个启动子为诱导型的。在其它实施方式中,所述至少一个诱导型的启动子为多顺反子的。在其它实施方式中,所述至少一个诱导型的多顺反子启动子为双向的。在其它实施方式中,表达盒为基因组学上整合的。在其它实施方式中,表达盒编码治疗性蛋白质或肽。在其它实施方式中,治疗性蛋白质或肽包括神经营养因子。
[0104]
在各种实施方式中,所述一种或多种载体包括具有侧接有两个转座子元件的基因表达盒的载体。在各种实施方式中,所述两个转座子元件包括piggybac末端重复(pb tr)。在各种实施方式中,所述载体包括组成型启动子,所述组成型启动子包括cmv/鸡β-肌动蛋白(又名cag)启动子。在各种实施方式中,所述载体包括诱导型的双向启动子,所述诱导型的双向启动子包括tre-bi启动子。在各种实施方式中,所述组成型启动子可操作地连接至tet应答元件。在各种实施方式中,“tet-on”元件包括例如rta。在其它实施方式中,rta包括
rtta-v10。在各种实施方式中,所述组成型启动子可操作地连接至选择因子,所述选择因子包括例如新霉素或嘌呤霉素。在各种实施方式中,所述诱导型的双向启动子为多顺反子的。在各种实施方式中,所述诱导型的双向启动子可操作地连接至第一、第二或第三或更多顺反子中的元件。在各种实施方式中,第一、第二或第三或更多顺反子包括转基因。在各种实施方式中,所述转基因后随着一个或多个转录后元件。在各种实施方式中,所述一个或多个转录后元件包括土拨鼠肝炎病毒转录后元件(wpre)。
[0105]
在各种实施方式中,所述转基因后随着一个或多个poly-a尾。其中包括例如兔β-珠蛋白polya。在各种实施方式中,所述转基因为神经营养因子。在各种实施方式中,所述神经营养因子包括胶质源性神经营养因子(gdnf)。在其它实施方式中,所述一种或多种载体包括编码重组酶的载体,所述重组酶包括vcre(vlox和衍生物)、scre(slox和衍生物)、dre(rox和衍生物)和phic31(attb)或本领域已知的其它重组酶。
[0106]
在各种实施方式中,所述载体包括促进安全着陆位点(包括aavs1)的靶向的一种或多种元件。在一些实施方式中,所述载体包括靶向aavs1的gdnf表达构建体。本文提供的aavs1位点保留在开放染色质区域中,此处插入的构建体可用于在分化细胞的后代(例如inpc的后代)中保持表达。
[0107]
在各种元件中,诱导型盒周围的一个或多个绝缘子元件在细胞分化期间减弱潜在的沉默。在各种实施方式中,所述表达盒包括一个或多个子盒,其中,各个子盒包括1)启动子,2)转基因和3)polya转录终止元件。在各种实施方式中,包括一个或多个子盒的表达盒包括组成型子盒和诱导型子盒。例如,组成型子盒包括表达rta反式激活因子的组成型启动子,且诱导型子盒包括表达神经营养因子(如gdnf)和任选的一种或多种报告蛋白的诱导型启动子。
[0108]
在各种实施方式中,所述载体包括至少一种同源重组序列。在其它实施方式中,所述同源重组序列包括能够靶向基因组安全港的序列。在其它实施方式中,所述基因组安全港为以下中的一种:腺相关病毒位点1(aavs1)、趋化因子(c-c基序)受体5(ccr5)基因、小鼠rosa26基因座的人直系同源物。
[0109]
在一些实施方式中,本文提供的载体能够使用哺乳动物表达载体驱动一种或多种序列在细胞中的表达。哺乳动物表达载体的实例包括pcdm8(seed,1987.nature 329:840)和pmt2pc(kaufman等,1987.embo j.6:187-195)。当用于哺乳动物细胞时,所述表达载体的控制功能通常由一种或多种调节元件提供。例如,常用的启动子来源于多瘤病毒、腺病毒2、巨细胞病毒、猿猴病毒40,以及本文公开的和本领域已知的其它启动子。对于原核和真核细胞二者的其它合适的表达系统,参见例如sambrook等,molecular cloning:a laboratory manual.第2版,cold spring harbor laboratory,cold spring harbor laboratory press,cold spring harbor,n.y.,1989的第16章和第17章。
[0110]
在一些实施方式中,重组表达载体能够指导外源序列优先在特定细胞类型中表达(例如组织特异性调节元件用于在例如本文提供的神经祖细胞或ipsc中表达核酸)。组织特异性调节元件是本领域已知的。例如在byrne和ruddle,1989.proc.natl.acad.sci.usa 86:5473-5477中讨论了神经元特异性启动子。发育调节的启动子也涵盖在内,例如鼠hox启动子(kessel和gruss,1990.science 249:374-379)和甲胎蛋白启动子(campes和tilghman,1989.genes dev.3:537-546)。
[0111]
产生本文提供的载体的方法是本领域已知的并且在上文讨论。仅通过举例的方式来说,多肽表达(例如神经营养因子,gdnf)可为可调节的。这可例如通过talen和同源重组方法来实现(参见例如图7和akhtar等,inducible expression of gdnf in transplanted ipsc-derived neural progenitor cells.stem cell reports.2018;10(6):1696-1704.doi:10.1016/j.stemcr.2018.03.024,通过引用的方式将其整体并入本文)。
[0112]
在一些实施方式中,本文提供的核酸序列通过整合载体递送至本文所述的细胞。整合载体将其递送的rna/dna永久整合至宿主细胞染色体中。非整合载体保持游离型,这意味着其中包含的核酸从未整合至宿主细胞染色体中。整合载体的实例包括逆转录病毒载体、慢病毒载体、杂合腺病毒载体和单纯疱疹病毒载体。
[0113]
在一些实施方式中,本文提供的核酸序列通过非整合载体递送至本文所述的细胞。非整合载体包括非整合病毒载体。非整合病毒载体消除了整合逆转录病毒带来的主要风险之一,因为它们不将其基因组整合至宿主dna中。一个实例是epstein barr orip/核抗原-1(“ebna1”)载体,它能够进行有限的自我复制并且已知在哺乳动物细胞中发挥作用。包含来自epstein-barr病毒的两个元件orip和ebna1,ebna1蛋白对病毒复制子区域orip的结合维持了哺乳动物细胞中的质粒的相对长期的游离型存在。orip/ebna1载体的这一特定特性使其对于产生无整合宿主细胞而言理想。其它非整合病毒载体包括腺病毒载体和腺相关病毒(aav)载体。
[0114]
另一非整合病毒载体是rna仙台病毒载体,其可在不进入受感染细胞的细胞核的情况下产生蛋白质。f缺陷型仙台病毒载体在受感染细胞的胞浆中保留数代,但在数代(例如10代)后迅速被稀释并完全丢失。这允许选定的一个或多个异源基因在靶细胞中自限性瞬时表达。
[0115]
非整合载体的另一实例是微环载体(minicircle vector)。微环载体是环化载体,其中质粒骨架已被释放,仅留下待表达的cdna和真核启动子。
[0116]
如上所述,在一些实施方式中,本文提供的核酸序列在细胞中由病毒载体表达。“病毒载体”包括核酸载体构建体,所述核酸载体构建体包括病毒来源的至少一种元件并且具有被包装到病毒载体颗粒中的能力。病毒载体可含有编码本文所述多肽的核酸来代替非必需的病毒基因。载体和/或颗粒可用于在体外或在体内将核酸转移至细胞的目的。
[0117]
将载体引入细胞的方法是本领域已知的,例如通过核转染、转染、电穿孔等。在其它实施方式中,引入至少两种载体的方法包括以下中的一种或多种:核转染、转染和电穿孔。在其它实施方式中,引入至少一种载体的方法包括以下中的一种或多种:核转染、转染和电穿孔。然而,本文提供的核酸序列和载体可使用任何转染试剂或促进核酸进入细胞的其它物理手段来递送。
[0118]
核酸的非病毒递送的方法包括脂质体转染、核转染、显微注射、生物弹道(biolistics)、病毒体、脂质体、免疫脂质体、聚阳离子或脂质:核酸缀合物、裸dna、人工病毒颗粒和试剂增强的dna摄取。脂质体转染描述于例如美国专利号5,049,386、4,946,787和4,897,355;并且脂质体转染试剂商业化出售(例如transfectam
tm
和lipofectin
tm
)。适用于多核苷酸的有效受体识别的脂质体转染的阳离子脂质和中性脂质包括felgner、wo 91/17424、wo 91/16024的那些。可递送至细胞(例如在体外或离体给予)或靶细胞(例如在体内给予)。
[0119]
脂质的制备:包括靶向的脂质体(例如免疫脂质复合物)的核酸复合物为本领域技术人员所熟知(参见例如crystal,science 270:404-410(1995);blaese等,cancer gene ther.2:291-297(1995);behr等,bioconjugate chem.5:382-389(1994);remy等,bioconjugate chem.5:647-654(1994);gao等,gene therapy 2:710-722(1995);ahmad等,cancer res.52:4817-4820(1992);美国专利号4,186,183、4,217,344、4,235,871、4,261,975、4,485,054、4,501,728、4,774,085、4,837,028和4,946,787)。
[0120]
可基于报告多肽的表达(例如gfp或荧光标签)来选择表达本文提供的期望的构建体和/或载体的克隆,并且可通过核酸测序确认向aavsl位点中的整合。可通过本领域已知的方法修饰最终载体以去除报告多肽序列或标签。在一些实施方式中,所述载体排除报告多肽序列。在一些实施方式中,待植入受试者中的inpc不表达荧光标签。
[0121]
inpc
[0122]
可通过本领域已知的方法选择表达本文提供的构建体的本文提供的诱导多能干细胞(ipsc)以用于分化、扩增和细胞储存。inpc将通过前文描述的上述方法培养ipsc来产生,并对inpc标志物进行评价。神经祖细胞标志物的非限制性实例包括:巢蛋白、vim、tubb3、map2、apq4、s100β、sc121、chat、bcl11b、satb2、膜联蛋白v和gfap。本文提供的inpc还将具有建立和产生星形胶质细胞的能力。星形胶质细胞标志物的非限制性实例包括gfap、eaat1/glast、eaat2/glt-1、谷氨酰胺合成酶、s100β和aldh1l1。
[0123]
在一些实施方式中,本文提供的inpc具有神经祖细胞的至少一种表型特征。inpc的表征可通过本领域已知的方法进行,例如用于已建立的npc基因或标志物的qpcr、plate-downs、免疫细胞化学(icc)、蛋白质印迹、显微镜检查和功能测定(例如代谢测定或电生理测定)。gdnf的icc和elisa可用于表征gdnf产生的体外水平和四环素调节的动力学。
[0124]
在各种实施方式中,源自ipsc的npc能够作为细胞系连续传代。
[0125]
在其它实施方式中,源自ipsc的npc(inpc)能够聚集。在其它实施方式中,inpc聚集为多个神经球。如本文所用,术语“神经球”是指表达至少一种神经元细胞标志物的多个细胞的聚集体。本文提供的inpc表达皮质神经祖细胞的标志物以及与成熟星形胶质细胞和未成熟星形胶质细胞二者相关的基因。本文提供的inpc可扩增为球状体或聚集体,在培养物中发展出丝状伪足(filopodia),表达神经祖细胞标志物(例如巢蛋白),和/或分化成星形胶质细胞。
[0126]
在其它实施方式中,源自ipsc的npc被植入到受试者的组织中。在其它实施方式中,inpc神经球被植入至受试者。
[0127]
用于植入的细胞组合物
[0128]
如本文提供的向受试者给予人inpc的方法涉及使用包含此类细胞的治疗组合物。治疗组合物包括生理学上可耐受的运载体以及在其中溶解或分散作为有效成分的细胞组合物和任选的至少一种额外的生物活性剂、多肽、编码所述多肽的核酸或如本文所述的因子。
[0129]
在各种实施方式中,除非期望如此,否则当出于治疗目的向哺乳动物或人类患者给予时,治疗组合物基本上不具有免疫原性。如本文所用,术语“药学上可接受的”、“生理学上可耐受的”及其语法变体在它们提到组合物、运载体、稀释剂和试剂时可互换使用,并且表示这些材料能够在不产生非期望的生理效应(例如恶心、头晕、胃部不适、移植排斥、过敏
反应等)的情况下给予至或到哺乳动物。除非期望如此,否则药学上可接受的运载体不会促进对与其混合的试剂的免疫应答的提高。含有溶解或分散于其中的活性成分的组合物的制备在本领域中是众所周知的并且不需要基于剂型进行限制。通常,此类组合物被制备为可注射的液体溶液或悬浮液,然而,也可制备适合使用前在液体中溶解或悬浮的固体形式。
[0130]
用于人的移植组合物可包括一种或多种药学上可接受的运载体或材料作为赋形剂。相比之下,细胞培养组合物(不用于人的移植)通常会使用研究试剂(如细胞培养基)作为赋形剂。inpc也可在fda批准的基质/支架中或与fda批准的适用于特定疾病或病症的药物(例如利鲁唑(由sanofi-aventis,制造)或依达拉奉(由mitsubishi tanabe pharma制造))组合给予。
[0131]
生理学上可耐受的运载体是本领域中众所周知的。示例性液体运载体是除活性成分和水之外不包含材料、或包含缓冲液(例如处于生理ph值的磷酸钠、生理盐水或两者)的无菌水性溶液,例如磷酸缓冲盐水。更进一步,水性运载体可包含多于一种缓冲盐、以及盐(例如氯化钠和氯化钾)、右旋糖、聚乙二醇和其它溶质。除了水并将水排除在外,液体组合物还可包含液相。此种额外的液相的示例是甘油、植物油(如棉籽油)和水-油乳液。对特定紊乱或病症的治疗有效的在本文所述的细胞组合物中使用的活性化合物的量将取决于紊乱或病症的性质,并且可通过标准临床技术确定。
[0132]
如本文所用,术语“移植(transplanting)”或“植入(engraftment)”用于如下的上下文中:将本文提供的细胞(例如inpc或神经球)通过使得所引入的细胞至少部分定位在期望位点(例如损伤或修复的位点)的方法或途径放置入受试者,从而产生期望的效应。所述细胞(例如inpc或其分化的后代(例如星形胶质细胞等))可直接植入脊髓或脑,或者通过使得递送至受试者中的期望位置的任何合适的途径给予,其中至少一部分植入的细胞或细胞组分保持活力。给予受试者后细胞的存活期可短至数小时(例如二十四小时)、至数天、长至数年(即长期植入)。如本领域技术人员将理解的,inpc的长期植入是期望的,因为成体神经祖细胞不会增殖到脊髓可从急性损伤或疾病(包括细胞死亡)中愈合的程度。在其它实施方式中,所述细胞可通过间接全身给予途径给予,例如腹膜内或静脉内途径。
[0133]
如本文所用,术语“给予”、“引入”和“移植”在如下的上下文中可互换使用:将本文所述的细胞(例如inpc)通过使得所引入的细胞至少部分定位在期望位点(例如损伤或修复或疾病的位点)的方法或途径放置入受试者,从而产生期望的效应。
[0134]
在一些实施方式中,根据本文所述的方法给予的inpc或其后代包括同种异体细胞或从一个或多个供体获得的细胞。如本文所用,“同种异体”是指获取自或源自(例如分化自)同一物种的一个或多个不同供体的细胞,其中一个或多个基因座处的基因不相同。例如,给予受试者的npc可源自从一个或多个不相关的供体受试者或从一个或多个不相同的同胞者获得的脐带血。在一些实施方式中,可使用同基因细胞群,例如从遗传学上相同的动物或从同卵双胞胎中获得的那些。在此方面的其它实施方式中,所述细胞为自体细胞;即所述细胞获得自或分离自(或源自)受试者并被给予至该受试者(即供体和受体是相同的)。
[0135]
在一些实施方式中,可用于本文所述组合物的细胞源自自体来源。由于本文提供的inpc(或其分化后代)基本上源自自体来源,因此与使用来自另一受试者或受试者组的细胞相比,移植排斥或过敏反应的风险降低。在一些实施方式中,本文提供的可用于植入的细胞源自非自体来源。此外,ipsc的使用无需从胚胎来源获得的细胞。因此,在一个实施方式
中,用于产生在本文所述的组合物和方法中使用的inpc的干细胞不是胚胎干细胞。在其它实施方式中,用于在本文所述的组合物和方法中使用的inpc是表达gdnf的inpc。
[0136]
治疗疾病的方法
[0137]
本文描述了一种治疗方法,所述方法包括向患有疾病或病症的受试者给予一批量的源自ipsc的npc(inpc),其中,所述细胞表达治疗性蛋白质或肽,并且进一步其中所述细胞、治疗性蛋白质或肽或两者都能够治疗疾病或病症。在其它实施方式中,所述细胞为源自ipsc的npc。在其它实施方式中,所述细胞为表达gdnf的inpc。
[0138]
本文描述了一种方法,所述方法包括向患有神经退行性疾病的受试者给予一批量的源自ipsc的npc,其中,所述细胞诱导性地表达能够治疗该疾病的神经营养因子。在其它实施方式中,源自ipsc的npc表达通过核转染引入的基因组学上整合的表达盒,所述表达盒包括组成型启动子、包含tet应答元件的诱导型的双向多顺反子启动子以及编码胶质源性神经营养因子(gdnf)的序列。在各种实施方式中,所述载体包括至少一种同源重组序列。在其它实施方式中,所述方法包括给予四环素、其类似物或衍生物。在其它实施方式中,所述载体排除多肽报告序列。在其它实施方式中,所述载体排除绿色荧光蛋白(gfp)序列。
[0139]
本文描述了一种治疗方法,所述方法包括:向患有疾病或病症的受试者给予一批量的细胞,其中,所述细胞表达治疗性蛋白质或肽,并且进一步地,其中,所述细胞、治疗性蛋白质或肽、或者两者能够治疗疾病或病症。在该方法的各个和所有的上述实施方式中,所述细胞为源自ipsc的npc。在该方法的各个和所有的上述实施方式中,所述细胞表达来自一种或多种载体的表达盒。在该方法的各个和所有的上述实施方式中,表达来自一种或多种载体的表达盒的细胞已被核转染、转染或电穿孔。在该方法的各个和所有的上述实施方式中,一种或多种载体包括piggybac载体、pbase载体或两者。在该方法的各个和所有的上述实施方式中,piggybac载体包括至少两个启动子,其中至少一个启动子为诱导型的。在该方法的各个和所有的上述实施方式中,所述至少一个诱导型的启动子为多顺反子的。在该方法的各个和所有的上述实施方式中,所述至少一个诱导型的多顺反子启动子为双向的。在该方法的各个和所有的上述实施方式中,所述表达盒为基因组学上整合的。在该方法的各个和所有的上述实施方式中,所述表达盒编码治疗性蛋白质或肽。在该方法的各个和所有的上述实施方式中,治疗性蛋白质或肽包括神经营养因子。在该方法的各个和所有的上述实施方式中,所述神经营养因子包括胶质源性神经营养因子(gdnf)。在该方法的各个和所有的上述实施方式中,所述疾病或病症为神经退行性疾病。在该方法的各个和所有的上述实施方式中,所述神经退行性疾病为肌萎缩性侧索硬化症(als)。在该方法的各个和所有的上述实施方式中,给予一批量的细胞包括注射。在该方法的各个和所有的上述实施方式中,该方法包括给予四环素、其类似物或衍生物。
[0140]
本文描述还描述了一种方法,所述方法包括向患有神经退行性疾病的受试者给予一批量的源自ipsc的npc,其中,所述细胞诱导性地表达能够治疗该疾病的神经营养因子。在该方法的各个和所有的上述实施方式中,源自ipsc的inpc表达通过核转染引入的基因组学上整合的表达盒,所述表达盒包括组成型启动子、包含tet应答元件的诱导型的双向多顺反子启动子、以及编码胶质源性神经营养因子(gdnf)的序列。在该方法的各个和所有的上述实施方式中,该方法包括给予四环素、其类似物或衍生物。
[0141]
经测量的或可测量的参数包括临床上可检测的疾病标志物,例如临床或生物标志
物的升高或降低水平,以及与疾病或紊乱的症状或标志物的临床学上接受的标度相关的参数。然而,应当理解的是,本文公开的组合物和剂型的总使用量将由主治医师在合理的医学判断范围内决定。所需的确切量将根据诸如所治疗疾病的类型等因素而有所不同。
[0142]
本文提供了用于治疗疾病、紊乱、脊髓损伤、肌萎缩性侧索硬化症(als)或感染的方法,所述方法包括向有需要的受试者给予inpc。在一些实施方式中,本文提供了用于预防预期的紊乱(例如als)的方法和组合物。
[0143]
经测量的或可测量的参数包括临床上可检测的疾病标志物,例如临床或生物标志物的升高或降低水平,以及与疾病或紊乱的症状或标志物的临床学上接受的标度相关的参数。然而,应当理解的是,本文公开的组合物和剂型的总使用量将由主治医师在合理的医学判断范围内决定。所需的确切量将根据诸如所治疗疾病的类型等因素而有所不同。
[0144]
如本文所用,术语“有效量”是指减轻疾病或紊乱的至少一种或多种症状所需的inpc群的量,所述疾病或紊乱包括但不限于损伤、疾病或紊乱。“有效量”涉及足以提供期望效应(例如在神经退行性损伤后保护运动神经元、代替神经祖细胞群等)的组合物的量。因此,术语“治疗有效量”是指inpc或此类细胞的组合物在向典型受试者(例如患有神经退行性疾病或紊乱或者处于神经退行性疾病或紊乱风险中的人)给予时足以促进特定效应的量。如本文所用的有效量还包括足以预防或延迟疾病症状的发展、改变疾病症状的进程(例如但不限于减缓疾病症状的进展)或逆转疾病的症状的量。可以理解的是,对于任何给定的情况,合适的“有效量”可由本领域普通技术人员使用常规实验来确定。
[0145]
在一些实施方式中,在根据本文描述的方法给予所述细胞之前,受试者首先被诊断为患有影响脑、脊髓或神经元的疾病或紊乱。在一些实施方式中,在给予所述细胞之前,受试者首先被诊断为处于发展出疾病(例如als)或紊乱的风险中。
[0146]
对于本文所述的各个方面的用途,inpc的有效量包括以下量的inpc:至少1
×
103、至少1
×
104、至少1
×
105、至少5
×
105、至少1
×
106、至少2
×
106、至少3
×
106、至少4
×
106、至少5
×
106、至少6
×
106、至少7
×
106、至少8
×
106、至少9
×
106、至少1
×
107、至少1.1
×
107、至少1.2
×
107、至少1.3
×
107、至少1.4
×
107、至少1.5
×
107、至少1.6
×
107、至少1.7
×
107、至少1.8
×
107、至少1.9
×
107、至少2
×
107、至少3
×
107、至少4
×
107、至少5
×
107、至少6
×
107、至少7
×
107、至少8
×
107、至少9
×
107、至少1
×
108、至少2
×
108、至少5
×
108、至少7
×
108、至少1
×
109、至少2
×
109、至少3
×
109、至少4
×
109、至少5
×
109或更多。inpc的有效量将取决于植入位点的大小和面积。例如,对于将inpc植入视神经,可使用约1000到10,000个inpc。相比之下,将inpc植入脊髓可能需要更多的细胞,数量级为约1
×
106至约5
×
109或更多inpc。熟练的从业者可确定给定植入程序所需的细胞数量。
[0147]
在一些实施方式中,将包含inpc的组合物用本文提供的任一种或多种载体处理,并使得能够以比当此种细胞被单独给予时的植入高至少20%的效率保护靶组织(例如脊髓)中的运动神经元;在其它实施方式中,此种效率比当inpc在没有本文提供的载体(例如包含编码gdnf的核酸序列的载体)的情况下单独给予时植入的效率高至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少1倍、至少2倍、至少5倍、至少10倍、至少100倍或更多。
[0148]
在一些实施方式中,将包含inpc的组合物用本文提供的任一种或多种载体处理,并使得能够以比当此种细胞被单独给予时的植入高至少20%的效率在靶组织(例如脊髓)
中植入细胞;在其它实施方式中,此种效率为比当inpc在没有本文所述的载体(例如包含编码gdnf的核酸序列的载体)的情况下单独给予时植入的效率高至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少1倍、至少2倍、至少5倍、至少10倍、至少100倍或更多。
[0149]
在一些实施方式中,通过脊柱内给予或递送向受试者给予有效量的inpc。在一些实施方式中,通过全身给予(例如静脉内给予)向受试者给予有效量的inpc。
[0150]
短语“全身给予”、“全身性给予”、“外周给予”和“外周性给予”在本文中用于指给予inpc群使其进入受试者的循环系统,而不是直接给予到靶位点、组织或器官中。
[0151]
剂型的选择将取决于所使用的具体组合物和待给予的inpc的数量;此种剂型可由熟练的从业者调整。然而,作为实例,当所述组合物为处于药学上可接受的运载体中的inpc时,所述组合物可为以每ml溶液的细胞的有效浓度在适当缓冲液(例如盐水缓冲液)中的细胞悬浮液。该剂型还可以包括细胞营养物、简单糖(例如用于调节渗透压)或用以维持细胞活力的其它成分。或者,该剂型可包含支架,例如可生物降解的支架。
[0152]
在一些实施方式中,可在如所述的用inpc治疗之前或之后给予帮助治疗受试者的额外试剂。此类额外的试剂可用于使靶组织为祖细胞的给予做准备。或者,可在inpc之后给予额外的试剂以支持经给予的细胞植入和生长到脊髓或其它期望的给予位点。在一些实施方式中,额外的试剂包括生长因子,例如fgf、egf或lif。
[0153]
治疗的功效可由熟练的临床医师确定。然而,如果在用如本文所述的包含人inpc的组合物治疗后,疾病(例如神经退行性疾病、als、脊髓损伤)和/或紊乱的任一种或所有症状或其它临床学上接受的症状或标志物减少(例如至少10%),那么治疗被认为是如本文所用的术语“有效治疗”。测量这些标志的方法是本领域技术人员已知的和/或在本文中描述的。
[0154]
神经退行性疾病或紊乱或者神经损伤的标志包括功能标志或参数,例如肌肉无力、协调问题、肌肉僵硬、肌肉丧失、肌肉痉挛或过度活跃的反射、疲劳或感觉头晕、说话困难或声带痉挛、吞咽困难、流涎、缺乏克制(lack of restraint)、轻度认知功能损害、严重便秘、严重非故意体重减轻、呼吸短促或肢体(limbs)/肢端(extremities)(例如脚或手臂)举起困难等。
[0155]
可用于评价神经功能参数的临床测试的非限制性示例包括:肌电图(emg)、mri、神经传导研究、血液测试、脊柱穿刺或肌肉活检。
[0156]
在必要或期望的情况下,损伤或疾病的动物模型可用于测量如本文所述的特定组合物的有效性。例如,als的遗传啮齿动物模型sod1
g93a
在工作示例中和在例如gurney me等,motor neuron degeneration in mice that express a human cu,zn superoxide dismutase mutation.science 1994;264:1772
–
1775中进行了详细描述,通过引用的方式将其整体并入本文。
[0157]
一些选择的定义:
[0158]
本领域技术人员将认识到与本文所述的方法和材料相似或等效的许多方法和材料,它们可用于本发明的实践中。实际上,本发明决不限于所描述的方法和材料。
[0159]
为方便起见,下文提供了说明书、实施例和所附权利要求中使用的一些术语和短语的含义。除非另有说明或从上下文中暗示,否则以下术语和短语包括以下提供的含义。提
供这些定义是为了帮助描述特定实施方式,而非旨在限制要求保护的技术,因为该技术的范围仅由权利要求限制。除非另有定义,否则本文使用的所有技术术语和科学术语具有与本技术所属领域的普通技术人员通常理解的相同的含义。如果本领域术语的使用与本文提供的定义存在明显差异,则以说明书中提供的定义为准。
[0160]
生物学和分子生物学中常用术语的定义可见于:the merck manual of diagnosis and therapy,第19版,由merck sharp&dohme corp.出版,2011(isbn 978-0-911910-19-3);robert s.porter等(编著),the encyclopedia of molecular cell biology and molecular medicine,由blackwell science ltd.出版,1999-2012(isbn 9783527600908);以及robert a.meyers(编著),molecular biology and biotechnology:a comprehensive desk reference,由vch publishers,inc.出版,1995(isbn1-56081-569-8);immunology by werner luttmann,由elsevier出版,2006;janeway's immunobiology,kenneth murphy,allan mowat,casey weaver(编著),taylor&francis limited,2014(isbn 0815345305,9780815345305);lewin's genes xi,由jones&bartlett publishers出版,2014(isbn-1449659055);michael richard green和joseph sambrook,molecular cloning:a laboratory manual,第4版,cold spring harbor laboratory press,cold spring harbor,n.y.,usa(2012)(isbn1936113414);davis等,basic methods in molecular biology,elsevier science publishing,inc.,new york,usa(2012)(isbn 044460149x);laboratory methods in enzymology:dna,jon lorsch(编著)elsevier,2013(isbn 0124199542);current protocols in molecular biology(cpmb),frederick m.ausubel(编著),john wiley and sons,2014(isbn 047150338x,9780471503385),current protocols in protein science(cpps),john e.coligan(编著),john wiley and sons,inc.,2005;以及current protocols in immunology(cpi)(john e.coligan,ada m kruisbeek,david h margulies,ethan m shevach,warren strobe,(编著)john wiley and sons,inc.,2003(isbn 0471142735,9780471142737),以引用的方式将它们的内容以其整体全部并入本文。
[0161]
本文引用的所有参考文献通过引用的方式以其整体并入,如同完全阐述一样。除非另有定义,本文使用的技术术语和科学术语具有本发明所属领域的普通技术人员通常理解的相同的含义。singleton等,dictionary of microbiology and molecular biology第3版,经修订,j.wiley&sons(new york,ny 2006);以及sambrook和russel,molecular cloning:a laboratory manual第4版,cold spring harbor laboratory press(cold spring harbor,ny 2012),为本领域技术人员提供了本技术中使用的许多术语的一般指南。
[0162]
本领域技术人员将认识到与本文描述的方法和材料相似或等效的许多方法和材料,它们可用于本发明的实践中。实际上,本发明决不限于所描述的方法和材料。
[0163]
术语“控制元件”统指启动子区域、多聚腺苷酸化信号、转录终止序列、上游调节结构域、复制起点、内部核糖体进入位点(“ires”)、增强子等,它们共同提供受体细胞中编码序列的复制、转录和翻译。只要所选择的编码序列能够在适当的宿主细胞中复制、转录和翻译,并非所有这些控制元件都需要始终存在。
[0164]
术语“启动子区域”在本文中以其通常含义使用,是指包括dna调节序列的核苷酸
区域,其中,所述调节序列来源于能够结合rna聚合酶并启动下游(3'-方向)编码序列转录的基因。
[0165]“可操作地连接”是指元件的布置,其中,如此描述的组件被配置为执行它们的通常功能。因此,可操作地连接至编码序列的控制元件能够实现编码序列的表达。控制元件不必与编码序列邻接,只要它们起到指导其表达的作用即可。因此,例如,在启动子序列和编码序列之间可存在插入的未翻译但被转录的序列,并且所述启动子序列仍然可被认为“可操作地连接”至所述编码序列。
[0166]
在本文提供的编码序列、启动子和其它遗传元件的上下文中,术语“异源的”表示该元件源自与其被比较的实体的其余部分在基因型上不同的实体。例如,本文提供的通过基因工程技术而被引入细胞中的启动子或基因被称为异源多核苷酸。“内源的”遗传元件是在其天然存在的染色体中位于相同位置的元件,尽管其它元件可被人为地引入邻近位置。
[0167]
术语“患者”、“受试者”和“个体”在本文中可互换使用,并且是指被提供治疗(包括预防性治疗)的动物(特别是人)。如本文所用,术语“受试者”是指人和非人动物。术语“非人动物”和“非人哺乳动物”在本文中可互换使用,包括所有脊椎动物,例如哺乳动物(如非人灵长类动物(特别是高等灵长类动物)、绵羊、狗、啮齿动物(如小鼠或大鼠)、豚鼠、山羊、猪、猫、兔、牛)和非哺乳动物(如鸡、两栖动物、爬行动物等)。在任意方面的一个实施方式中,所述受试者为人。在任意方面的另一实施方式中,所述受试者为作为疾病模型的实验动物或动物替代物。在任意方面的另一实施方式中,所述受试者为驯养的动物,包括伴侣动物(例如狗、猫、大鼠、豚鼠、仓鼠等)。受试者可在先前接受过针对疾病的治疗,或者从未接受过针对疾病的治疗。受试者可在先前被诊断为患有疾病,或从未被诊断为患有疾病。
[0168]
如本文所用,术语“标志物”用于描述细胞的特征和/或表型。标志物可用于选择包含感兴趣特征的细胞,并可随特定细胞而变化。标志物是特定细胞类型的细胞的特征(无论是形态特征、结构特征、功能特征或生化(酶)特征),或是由该细胞类型表达的分子。一方面,此类标志物为蛋白质。此类蛋白质可具有抗体或本领域可用的其它结合分子的表位。然而,标志物可由在细胞中或细胞上发现的任何分子组成,包括但不限于蛋白质(肽和多肽)、脂质、多糖、核酸和类固醇。形态特征或性状的实例包括但不限于形状、大小和核质比。功能特征或性状的实例包括但不限于粘附到特定底物的能力、掺入或排除特定染料的能力以及沿特定谱系分化的能力。可通过本领域技术人员可用的任何方法检测标志物。标志物也可为形态特征的缺失或蛋白质、脂质等的缺失。标志物可为多肽的存在和/或缺失与其它形态或结构特征的一组独特特征的组合。在一个实施方式中,所述标志物为细胞表面标志物。
[0169]
如本文所用,术语“支架”是指包含提供适合细胞粘附和增殖的表面的生物相容性材料的结构。支架可以进一步提供机械稳定性和支撑。支架可处于特定的形状或形式,以影响或界定由增殖细胞群体呈现的三维形状或形式。此类形状或形式包括但不限于膜(例如具有实质上大于第三维的二维的形式)、条带、线、片、平盘、圆柱体、球体、3维无定形形状等。
[0170]
短语“药学上可接受的”在本文中用于指在合理的医学判断范围内,适合用于与人和动物的组织接触,没有过度的毒性、刺激、过敏反应或其它问题或并发症,与合理的收益/风险比相称的那些化合物、材料、组合物和/或剂型。
[0171]
术语“降低(decrease)”、“减少(reduced/reduction)”或“抑制”在本文中均用于
意指性质、水平或其它参数降低或减弱统计学显著的量。在一些实施方式中,“减少”、“降低”或“抑制”通常意指与参考水平(例如不存在给定的治疗)相比降低至少10%,并且可包括例如降低至少约10%、至少约20%、至少约25%、至少约30%、至少约35%、至少约40%、至少约45%、至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约98%、至少约99%或更多。如本文所使用,“减少”或“抑制”不涵盖与参考水平相比的完全抑制或减少。“完全抑制”是与参考水平相比100%的抑制。降低可优选地下降到被接受为对于没有给定紊乱的个体而言的正常范围内的水平。
[0172]
术语“增加(increased/increase/increases)”或“增强(enhance)”或“激活”在本文中均用于普遍意指性质、水平或其它参数增加统计学显著的量;为避免任何疑问,术语“增加”或“增强”或“激活”意指与参考水平相比增加至少10%,例如与参考水平相比增加至少约20%、或至少约30%、或至少约40%、或至少约50%、或至少约60%、或至少约70%、或至少约80%、或至少约90%或高至并包括100%的增加、或10%-100%之间的任何增加,或与参考水平相比至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍或至少约10倍的增加、至少约20倍的增加、至少约50倍的增加、至少约100倍的增加、至少约1000倍的增加或更多。
[0173]
如本文所用,术语“调节”是指包括增加或降低如本文定义的那些术语给定的参数的效应。
[0174]
如本文所用,“参考水平”是指正常的、在其它方面未受影响的细胞群或组织,例如从健康受试者获得的生物样品,或在先前时间点从受试者获得的生物样品(例如在被诊断为患有疾病之前从患者获得的生物样品,或尚未与如本文公开的组合物、多肽或编码此类多肽的核酸接触的生物样品)。
[0175]
如本文所用,“适当的对照”是指未处理的、在其它方面相同的细胞或群体,例如未与本文所述的试剂或组合物接触或与非对照细胞相比未以相同方式(例如持续时间不同)接触的生物样品。
[0176]
如本文所用,应用于体外分化细胞(例如inpc)或体外分化细胞的培养物时,术语“表型特征”是指作为细胞功能的量度的本文描述的任何参数。如本文所述的“表型特征的变化”由相对于参考水平或适当的对照的功能特性方面的统计学显著的增加或降低来指示。
[0177]
如本文所使用,术语“包括/包含/含有”意指除了所呈现的限定的要素之外还可存在其它要素。“包括/包含/含有”的使用表示包括而非限制。
[0178]
术语“由
……
组成”是指排除了在实施方式的描述中未列举的任何要素的如本文所述的组合物、方法及其各自的组分。
[0179]
如本文所使用,术语“基本上由
……
组成”是指给定实施方式所需的那些要素。该术语允许不会实质影响该技术的实施方式的基础和新颖性或功能性特征的额外要素的存在。
[0180]
除非上下文另有明确指示,否则词语“或”旨在包括“和”。
[0181]
在一些实施方式中,用于描述和要求保护本发明的某些实施方式的表示成分的量、特性(如浓度)、反应条件等的数值应理解为在某些情况下通过术语“约”修饰。因此,在
30141或它们的任意组合。
[0193]
实施方式9:如前述实施方式中任一项所述的方法,其中,所述rock抑制剂为y-27632。
[0194]
实施方式10:如前述实施方式中任一项所述的方法,其中,将所述细胞在约5μm的y-27632中培养至少约7天至约16天。
[0195]
实施方式11:如前述实施方式中任一项所述的方法,其中,将所述细胞在fgf、egf和lif中培养至少约8小时至16天。
[0196]
实施方式12:如前述实施方式中任一项所述的方法,其中,将所述细胞在100ng/ml的fgf、100ng/ml的egf和100ng/ml的lif中培养至少约3天至约16天。
[0197]
实施方式13:如前述实施方式中任一项所述的方法,其中,所述源自ipsc的npc(inpc)聚集为神经球。
[0198]
实施方式14:如前述实施方式中任一项所述的方法,其中,所述源自ipsc的npc是植入的源自ipsc的npc。
[0199]
实施方式15:如前述实施方式中任一项所述的方法,其中,所述细胞与一种或多种载体接触。
[0200]
实施方式16:如前述实施方式中任一项所述的方法,其中,所述细胞与包含以下的载体接触:(a)表达盒,所述表达盒包括(i)组成型启动子,(ii)包含tet应答元件的诱导型的双向多顺反子启动子,以及(iii)编码蛋白质或肽的序列;(b)两个转座子元件,其中,所述两个转座子元件侧接于所述表达盒;以及(c)至少一种同源重组序列。
[0201]
实施方式17:如前述实施方式中任一项所述的方法,其中,所述细胞与包含编码神经营养因子的核酸序列的载体接触。
[0202]
实施方式18:如前述实施方式中任一项所述的方法,其中,所述神经营养因子为胶质细胞系源性神经营养因子(gdnf)。
[0203]
实施方式19:一种方法,所述方法包括:(i)提供通过如前述实施方式中任一项所述的方法制备的一批量的源自ipsc的npc;以及(ii)向所述源自ipsc的npc中引入至少两种载体。
[0204]
实施方式20:如前述实施方式中任一项所述的方法,其中,所述引入至少两种载体包括核转染、转染和电穿孔中的一种或多种。
[0205]
实施方式21:如前述实施方式中任一项所述的方法,其中,所述至少两种载体包括piggybac载体和pbase载体。
[0206]
实施方式22:如前述实施方式中任一项所述的方法,其中,至少一种载体包括病毒载体。
[0207]
实施方式23:如前述实施方式中任一项所述的方法,其中,所述载体为aav或慢病毒载体。
[0208]
实施方式24:如前述实施方式中任一项所述的方法,其中,所述piggybac载体包括:(a)表达盒,所述表达盒包括(i)组成型启动子,(ii)包含tet应答元件的诱导型的双向多顺反子启动子,以及(iii)编码蛋白质或肽的序列;(b)两个转座子元件,其中,所述两个转座子元件侧接于所述表达盒;以及(c)至少一种同源重组序列。
[0209]
实施方式25:如前述实施方式中任一项所述的方法,其中,所述蛋白质或肽包括神
经营养因子。
[0210]
实施方式26:如前述实施方式中任一项所述的方法,其中,所述神经营养因子包括胶质源性神经营养因子(gdnf)。
[0211]
实施方式27:如前述实施方式中任一项所述的方法,其中,所述同源重组序列包括能够靶向基因组安全港的序列。
[0212]
实施方式28:如前述实施方式中任一项所述的方法,其中,所述基因组安全港为以下中的一种:腺相关病毒位点1(aavs1)、趋化因子(c-c基序)受体5(ccr5)基因、小鼠rosa26基因座的人直系同源物。
[0213]
实施方式29:如前述实施方式中任一项所述的方法,其中,所述神经祖细胞为植入的神经祖细胞。
[0214]
实施方式30:通过如前述实施方式中任一项所述的方法制备的一批量的细胞。
[0215]
实施方式31:如前述实施方式中任一项所述的方法或一批量的细胞,其中,所述细胞表达基因组学上整合的表达盒。
[0216]
实施方式32:如前述实施方式中任一项所述的方法或一批量的细胞,其中,所述基因组学上整合的表达盒处于基因组安全港。
[0217]
实施方式33:一种方法,所述方法包括:(i)提供通过如前述实施方式中任一项所述的方法制备的一批量的源自ipsc的npc;以及(ii)向所述源自ipsc的npc中引入至少一种载体。
[0218]
实施方式34:如前述实施方式中任一项所述的方法,其中,所述引入至少一种载体包括核转染、转染和电穿孔中的一种或多种。
[0219]
实施方式35:如前述实施方式中任一项所述的方法,其中,所述至少一种载体包括:(a)表达盒,所述表达盒包括(i)组成型或诱导型启动子,所述组成型或诱导型启动子可操作地连接至编码蛋白质或肽的序列;以及(ii)至少一种同源重组序列。
[0220]
实施方式36:如前述实施方式中任一项所述的方法,其中,所述蛋白质或肽包括神经营养因子。
[0221]
实施方式37:如前述实施方式中任一项所述的方法,其中,所述神经营养因子包括胶质源性神经营养因子(gdnf)。
[0222]
实施方式38:如前述实施方式中任一项所述的方法,其中,所述组成型启动子为3-磷酸甘油酸激酶(pgk)启动子。
[0223]
实施方式39:如前述实施方式中任一项所述的方法,其中,所述同源重组序列包括能够靶向基因组安全港的序列。
[0224]
实施方式40:如前述实施方式中任一项所述的方法,其中,所述基因组安全港为以下中的一种:腺相关病毒位点1(aavs1)、趋化因子(c-c基序)受体5(ccr5)基因、小鼠rosa26基因座的人直系同源物。
[0225]
实施方式41:如前述实施方式中任一项所述的方法,其中,所述诱导型启动子包括由四环素类抗生素调节的启动子。
[0226]
实施方式42:如前述实施方式中任一项所述的方法,其中,所述四环素类抗生素包括多西环素。
[0227]
实施方式43:如前述实施方式中任一项所述的方法,其中,所述诱导型启动子由反
向四环素控制的反式激活因子(rtta)或tet-on高级反式激活因子(rtta2s-m2)调节。
[0228]
实施方式44:如前述实施方式中任一项所述的方法,其中,所述反向四环素控制的反式激活因子(rtta)或tet-on高级反式激活因子(rtta2s-m2)促进细胞中gdnf的表达。
[0229]
实施方式45:如前述实施方式中任一项所述的方法,其中,所述源自ipsc的npc为植入的源自ipsc的npc。
[0230]
实施方式46:通过如前述实施方式中任一项所述的方法制备的一批量的细胞,其中,所述源自ipsc的npc表达基因组学上整合的表达盒。
[0231]
实施方式47:如前述实施方式中任一项所述的一批量的细胞,其中,所述基因组学上整合的表达盒处于基因组安全港。
[0232]
实施方式48:如前述实施方式中任一项所述的一批量的细胞,其中,所述基因组安全港为aavs1。
[0233]
实施方式49:一种移植组合物,所述组合物包括如前述实施方式中任一项所述的一批量的细胞和药学上可接受的载体。
[0234]
实施方式50:如前述实施方式中任一项所述的移植组合物,其中,所述组合物被植入到受试者的脊髓中。
[0235]
实施方式51:用作神经退行性疾病的治疗的如前述实施方式中任一项所述的移植组合物。
[0236]
实施方式52:如前述实施方式中任一项所述的移植组合物,其中,所述神经退行性疾病为肌萎缩性侧索硬化症(als)。
[0237]
实施方式53:一种治疗als的方法,所述方法包括:(a)向受试者给予通过如前述实施方式中任一项所述的方法制备的inpc;以及任选地(b)向受试者给予用于als的额外的治疗。
[0238]
实施方式54:如前述实施方式中任一项所述的方法,其中,所述额外的治疗为利鲁唑或依达拉奉中的一种或多种。
[0239]
本文描述的各种方法和技术提供了实施本发明的多种方式。当然,应当理解的是,根据本文描述的任何特定实施方式,不一定实现所描述的所有目标或优点。因此,例如本领域技术人员将认识到,可以按实现或优化如本文所教导的一个优点或一组优点的方式执行所述方法,而不必实现可能如本文教导或建议的其它目标或优点。
[0240]
本文提及了多种有利和不利的替代方案。应当理解的是,一些优选实施方式具体地包括一个、另一个或数个有利特征,而另一些具体地排除一个、另一个或数个不利特征,同时还有另一些通过包括一个、另一个或数个有利特征来具体地减轻当前的不利特征。
[0241]
此外,技术人员将认识到来自不同实施方式的各种特征的适用性。类似地,本领域普通技术人员可混合和匹配上文讨论的各种要素、特征和步骤,以及每个此类要素、特征或步骤的其它已知等效物,以执行根据本文描述的原理的方法。在多种实施方式中,各种要素、特征和步骤中的一些将被具体地包括而另一些将被具体地排除。
[0242]
尽管本发明已经在某些实施方式和实例的上下文中公开,但是本领域技术人员将理解的是,本发明的实施方式超出具体公开的实施方式而延伸至其它替代实施方式和/或用途以及其修饰和等效物。
[0243]
在本发明的实施方式中已经公开了许多变化和替代要素。对于本领域技术人员来
说,更进一步的变化及替代要素将是显而易见的。这些变化非限制性地为与诱导多能干细胞(ipsc)、分化的ipsc(包括神经祖细胞)、用于操作上述细胞的载体相关的组合物和方法,与上述组合物的用途、技术及其中使用的溶液的组成和用途相关的方法和组合物,以及通过本发明的教导产生的产物的特定用途。本发明的各种实施方式可具体地包括或排除这些变化或要素中的任一个。
[0244]
本文公开的本发明的替代要素或实施方式的分组不应被解释为限制性的。各个组成员可单独地被提及和要求保护,或与该组的其它成员或见于本文中的其它要素任意组合地被提及和要求保护。出于方便和/或可专利性的原因,组的一个或多个成员可被包含在组中或从组中删除。当任何此类包含或删除发生时,本说明书在本文中被认为包含经修改的组,从而满足在所附权利要求中使用的所有马库什组的书面描述。
[0245]
本文描述了本发明的优选实施方式,包括发明人已知的用于实施本发明的最佳模式。在阅读先前的描述后,那些优选实施方式的变化对于本领域普通技术人员将变得显而易见。在考虑之列的是,熟练的技术人员可适当地采用此类变化,并且可以按不同于本文具体描述的方式实践本发明。因此,本发明的许多实施方式包括在适用法律的允许下在所附权利要求中记载的主题的所有修改和等效物。此外,除非本文另有说明或与上下文明显矛盾,否则本发明涵盖上述要素在其所有可能变化中的任意组合。
[0246]
此外,贯穿本说明书对专利和印刷出版物进行了大量参考。以上引用的参考文献和印刷出版物中的每一个都通过引用的方式将其整体各自地并入本文。
[0247]
应当理解的是,本文公开的本发明的实施方式是对本发明原理的说明。可采用的其它修改可在本发明的范围内。因此,通过示例而非限制,可根据本文的教导使用本发明的替代配置。因此,本发明的实施方式不限于精确地如所示和所描述的那样。
[0248]
本发明通过以下实施例进一步说明,这些实施例不应被解释为限制性的。
[0249]
实施例
[0250]
本文描述了要求保护的发明的非限制性实例。
[0251]
实施例1:通过产生经工程化以在四环素诱导型启动子下产生gdnf的主导的(master)ipsc系来开发inpc-gdnf
dox
细胞产物。
[0252]
诱导多能干细胞(ipsc)为可分化成期望的神经祖细胞的细胞疗法产物提供了安全、可再生和可扩展的来源。因为ipsc可进行克隆扩增,所以可能产生如下的主导的ipsc系,所述的主导的ipsc系包含处于诱导型启动子下的插入到安全基因组基因座(如aavs1)中的gdnf转基因的单拷贝。然后,当提供有四环素时,所衍生的inpc-gdnf细胞可均一地表达gdnf,并且可很容易地扩增至足以进行进一步测试和临床使用的规模。
[0253]
在此研究中,产生了经工程化以在四环素调节启动子下产生gdnf的ipsc的主导的细胞系。通过优化的分化方案和用于受控的gdnf表达的经工程化的品系,可扩增inpc-gdnf
dox
的临床前批次细胞并储存以用于疗效和安全性研究。
[0254]
慢病毒转导(例如在cns10-npc-gdnf中使用的慢病毒转导)引起异源拷贝数和随机基因组的插入。由于ipsc可从单个克隆扩增,因此可用插入至aavs1安全着陆位点的单个gdnf构建体建立经基因编辑的品系。
[0255]
经基因编辑的ipsc系因在分化后使经工程化的构建体沉默而尽人皆知
36,37
。由于aavs1位点保留在开放染色质区域中,因此插入此处的构建体能够更好地在分化的后代中
保持表达
38,39
。具体而言,aavs1基因座对于经工程化的构建体的插入是安全的,因为插入引起了最小化的内源细胞过程破坏
40
。cns10-npc-gdnf分泌可保护运动神经元的gdnf,但此种表达是组成型的,并且因此不能调节gdnf的时机和剂量。在本研究中,发明人对ipsc系进行工程化来表达可调节的gdnf,这与合作研究中使用的非常相似
27
。
[0256]
使用组成型启动子或驱动gdnf的四环素诱导型启动子(v1)产生了两种构建体(图6a)。使用先前建立的talen和同源重组方法将这些构建体靶向插入到aavs1基因座中(图7)。容纳有各构建体的ipsc系分化为inpc,然后使用elisa在体外进行测试以检测gdnf向培养基中的分泌。在24小时时,未转导的inpc不产生gdnf,但容纳有组成型gdnf构建体的inpc产生的gdnf水平与慢病毒转导的inpc和cns10-npc-gdnf细胞二者的相似(图6b)。用0.6μm多西环素(dox;四环素类似物)处理的具有v1诱导型构建体的inpc显示出gdnf的表达。所述诱导型构建体受到严格调节,在dox撤掉后72小时gdnf的产生衰减(图6c)。重要的是,在没有dox处理的情况下,来自经转导的inpc的gdnf水平保持在非转导的水平。
[0257]
尽管有来自体外数据的有希望的结果,vl四环素诱导型构建体在移植细胞中不起作用(图6d)。此外,初始构建体有10.7kb大,并且含有许多不适合治疗应用的元件
27
。因此,发明人从可得自clonetech
tm
的干净载体骨架设计了简化的构建体(图6a,v2)。这种新的四环素诱导系统(v2)小得多,为5.7kb,并且可更为干净以及更有效地表达gdnf转基因。
[0258]
为了对具有在诱导型启动子控制下表达的gdnf单拷贝的ipsc系进行工程化,可使用talen方法将新的v2构建体靶向至aavs1基因座中。此外,将gdnf构建体并入ipsc而不是inpc消除了后续在培养中对解离/慢病毒转导步骤的需要,从而进一步增加了扩增潜力。
[0259]
已经证明使用这种方法将靶向的构建体有效整合至aavs1基因座中
41
。相同的talen构建体可用于将v2诱导型gdnf转基因插入ipsc系,所述ipsc系用于更早的inpc方案评估。处于悬浮的ipsc可用右侧和左侧的talen构建体和诱导型gdnf构建体进行电穿孔。所述细胞能够以低密度铺板并被选择以建立克隆品系。可基于瞬时gfp表达来选择表达期望构建体的克隆,并可通过sanger测序确认对aavs1位点中的整合。确认后,这些ipsc克隆可作为用于获得诱导型inpc产物(inpc-gdnf
dox
)的材料。
[0260]
一旦建立了容纳有v2诱导型gdnf构建体的ipsc系,可对所述细胞进行分化和表征,例如通过针对已建立的npc基因(巢蛋白、vim、tubb3、map2、apq4、s100β和gfap)的qpcr、plate-downs和免疫细胞化学(icc)以建立npc产生星形胶质细胞的能力,以及对gdnf进行icc和elisa以表征体外gdnf产生的水平和四环素调节的动力学。
[0261]
一旦一批inpc-gndf
dox
已经被分化且表征,可对所述细胞扩增和储存。并行地,可使用相同的方法开发组成型表达gdnf的inpc的库(inpc-gdnf
const
)。对目前的inpc分化的先前的研究示出了inpc适应于可扩展的培养方法,这对下游开发成细胞疗法至关重要。
[0262]
除了以上讨论的ipsc系之外,还产生了组成型gdnf ipsc系,以及分化和储存的inpc-gdnf
const
细胞。这些inpc-gdnf
const
细胞可用于如下所述的功效和安全性测试。所述细胞产物能够进行如下所述的规模化生产。
[0263]
功效和安全性测试:为了进行安全性测试,可产生一批大约两亿个inpc。通过使用规模化生物反应器和新的传代方法,该批次大小易于实现。传统上,神经祖细胞被扩增为单层或作为聚集培养物处于悬浮。任一种培养方式的单细胞传代都不理想,因为此传代方法可引起限制扩增潜力的早期细胞衰老,或者可诱导细胞分化
13,42,43
。机械切碎已成功用于将
胎儿和ipsc来源的神经祖细胞二者扩增至适合早期临床试验的规模。然而,此方法耗时、劳动密集,并且难以大规模实施。开发了通过插入由具有200μm方形空间的超细钨丝制成的切割网进行机械传代的方法,以帮助本文所述细胞产物的下游制造。由于网格98%是开放的,因此流体流动的阻碍最小化,这允许大容积的培养基和细胞流过,然后大的球状体在它们通过网格时被切割。产生的球状体切片为约200μm方形片段,类似于传统机械切碎方法中的切片。除了显著更短的耗时和需要远远更少的操作员操作外,此种新的切碎方法可在线实施,完全消除对外部处理细胞的需要。这使得可以使用其中每次传代可增加培养容积的规模化的生物反应器培养物,而不是被用以产生cns10-npc-gndf细胞的其中每次传代增加培养瓶的数量的外扩(scale-out)培养方法。即使使用小型生物反应器培养物和此种新的机械传代技术,也可快速产生足够量的inpc-gdnf
dox/const
用于所有下游测定(图11)。
[0264]
实施例2:在sod1
g93a
als转基因大鼠的腰脊髓和运动皮质中移植的inpc-gdnf
dox
的功效。
[0265]
sod1
g93a
大鼠为als的良好表征的模型
44,45
,并已广泛用于细胞移植研究
8,12
,以及用于胎儿来源的cns10-npc-gdnf细胞的ind申报的临床前研究。与人的病理学非常相似,在该模型中疾病发作的位置是不可预测的,伴有后肢和/或前肢的明显的麻痹进展到完全瘫痪。在一些动物中也可观察到躯干和颈部肌肉的萎缩。这种缓慢恶化和疾病进展可使用行为测量来评价,例如体重以及basso、beattie和bresnahan(bbb)量表。这些大鼠的组织学分析示出了皮质脊髓运动神经元和脊髓运动神经元的丧失,以及神经肌肉连接的退化
14,46
。因此,此模型特别适合确定inpc-gdnf
dox
在保护易患als的神经元方面的功效和剂量。此目标聚焦于inpc-gdnf
dox
产物是否可在诱导型启动子控制下在als啮齿动物模型中提供保护性益处。
[0266]
dox剂量方案:在先前的研究中,通过口服强饲法每3-4天递送15μg dox/克来实现对小鼠皮质中源自ipsc的神经祖细胞移植的调节
27
。如通过荧光素酶测定所确定的,dox剂量的效应在给予后一周内可见。由于inpc-gdnf
dox
的功效是本研究的主要目标,因此只需要评价“on dox”或“off dox”的简单递送。可评价gdnf表达的体内动力学以及更复杂的剂量方案(例如脉冲表达和衰减)。此处,可使用野生型(wt)大鼠。每只动物都可接受inpc-gdnf
dox
单侧移植至腰脊髓,以便与每个脊髓切片的对侧进行比较。每只动物可在相距1mm的位点接受3次10k个细胞的注射。基于来自容纳有v1构建体的inpc的体外gdnf elisa,观察到经dox处理和未处理的细胞之间的效应量为4.91,允许99%的功效来检测使用3只动物的组规模的效应差异。在移植和手术恢复后,可以以两种方式之一向大鼠给予dox,每组评价三种不同的浓度,共18只动物(表3)。第一组能以如下浓度使用口服强饲法接受dox:每剂15μg、20μg和30μg。第二组能以如下浓度的饮用水接受dox:0.2mg/ml、2mg/ml和5mg/ml。评价dox在饮用水中递送时的功效的研究显示,dox在动物水瓶中的稳定性长达14天
47
,因此此处可每周两次用新鲜的混合物代替dox-水。每3-4天强饲4周或持续使用dox-水后,可处死动物并针对脊髓组织使用免疫组织化学(ihc)评价gdnf表达和移植存活率。在处理期间,可使用行为测量(体重和观察)来观察动物,以确保手术后脊髓的恢复和没有损伤。可在每次变化时测量饮用水的确切体积,以估计每只大鼠消耗的量。从手术前3天开始,大鼠可每天接受用于免疫抑制的10mg/kg环孢菌素的交替的腹膜内注射(ip)以避免移植排斥。可根据脊髓切片中检测到的gdnf量对每种dox给予方法和浓度进行评分,并与和dapi共定位的人细
胞核或细胞质标志物的百分比进行比较(这指示移植存活率)。
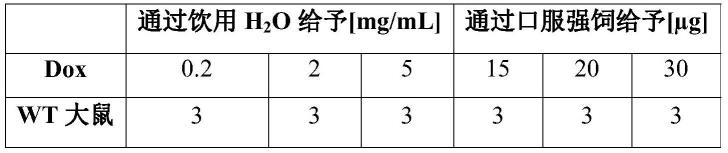
[0267]
表3.野生型(wt)动物中的针对inpc-gdnf
dox
的最佳dox递送的实验组。
[0268][0269]
inpc-gdnf在保护als的sod1
g92a
大鼠模型中的神经元方面的功效:已经示出了在cns10-npc-gdnf疗法移植到als和衰老的腰脊髓后对脊髓运动神经元的神经保护
8,12,26
。其它工作还示出了sod1
g93a
大鼠模型的运动皮质中的突变sod1的病毒敲减引起疾病发作延迟和生存延长
14
。在此als模型中,将cns10-npc-gdnf移植到运动皮质也保护了上运动神经元和下运动神经元二者、延迟了疾病病理学并且延长了als大鼠的生存
15
。两项研究都表明,上运动神经元和皮质的功能障碍可能对导致脑和脊髓中的运动神经元死亡以及随之而来的als瘫痪的事件产生重大影响。不受特定理论束缚地,移植到sod1
g93a
大鼠模型的(a)腰脊髓、(b)运动皮质和(c)这两个位点的inpc-gdnf
dox
细胞可提供类似于用cns10-npc-gdnf产物观察到的神经保护作用。
[0270]
基于先前对sod1
g93a
大鼠模型的经验,这些功效研究中的所有动物都可在70 /-5日龄时接受inpc-gdnf
dox
细胞的移植。以上讨论的dox的给予方法和最小有效浓度可在动物手术后恢复一周后使用。
[0271]
inpc-gdnf
dox
移植到腰脊髓:在先前的研究中,已经用慢病毒转导以表达gdnf的inpc在移植后50天在sod1
g93a
als大鼠的腰脊髓中显示神经保护作用。在这些动物中,每个位点10k细胞的移植剂量在保护宿主chat 运动神经元方面是有效的,但每个位点50k细胞的剂量并没有产生来自过密的移植物的神经保护和宿主神经元的取代(图8a-图8b)。
[0272]
在确定inpc-gdnf
dox
细胞的有效剂量时,可使用雄性sod1
g93a
大鼠。待在每个群组中使用的动物的统计调整是基于cns10-gdnf细胞的先前发表和未发表的数据
8,12,14,15,48
。在疾病发作时,预计在经溶媒处理的sod1
g93a
大鼠的脊髓中保持平均350
±
33个(平均值的标准误差,sem)大的chat 运动神经元(》700μm2)。因此,使用每个溶媒组10只动物和每个处理组15只动物的样本规模,以使在重复测量分析(同侧与对侧测量)中实现80%的功效,预期效应量为0.58。处理组涵盖每个位点的待移植细胞的三个逐渐增加的浓度,从1万(d1)直至3万个细胞(d3),每个位点接受2μl的体积(表4)。每个位点接受最高细胞剂量的d3组包括另外10只移植后不接受dox给予的动物(总共25只动物)。腰脊髓中的位点可间隔开1mm,总共有5个位点。移植可为单侧的(每个脊髓都在同一侧),对侧作为每只动物的内部对照。移植的一侧可在手术时随机选择,并且可对研究人员保持盲态直到完成组织的组织学分析和数据的完全解盲。sod1
g93a
大鼠将每天接受用于免疫抑制的10mg/kg环孢菌素的交替ip以避免移植排斥。移植后,可对动物观察详细的临床检查,包括体重、后肢运动功能、发病和死亡。这些观察可对处理组完全盲态。所有动物均可在疾病发作时处死以进行进一步分析,所述疾病发作由后肢或前肢的连续bbb评分为15或更低来确定。
[0273]
表4.用于腰脊髓移植inpc-gdnf
dox
的实验组。
[0274][0275]
*10只动物作为移植对照不被给予dox
[0276]
还可收集每只动物的脊髓并连续切片以通过ihc分析。运动神经元数量、植入程度(由检测到的人细胞核和胞浆的百分比确定)和gdnf的表达可使用针对各自的体视学和抗体来评价。该目标的次要目的是评价疾病环境中的体内细胞命运。为此,还将使用ihc评价移植的脊髓切片,以评估细胞类型(例如星形胶质细胞或神经祖细胞的表达,以及移植的细胞的整合或迁移程度)。可通过与溶媒对照和处理组中的相同切片的对侧区域相比的运动神经元保留的百分比、以及对行为数据没有效果或改善的效果,对inpc-gdnf
dox
的功效进行评分。
[0277]
inpc-gdnf
dox
移植到运动皮质:基于先前将cns10-npc-gdnf移植到sod1
g93a
大鼠运动皮质的经验,在每只动物的20个位点(每个半球10个)处移植2μl注射液。动物在横向
×
前/后的立体定向图谱(stereotaxic coordinates)处接受给药深度为1.45mm的双侧注射,所述立体定向图谱涵盖如下所示的来自前囟点(bregma loci)的运动皮质:(1)2mm
×
2mm,(2)2mm
×
1mm,(3)2mm
×
0mm,(4)2mm
×‑
1mm,(5)2mm
×‑
2mm,(6)3mm
×
2mm,(7)3mm
×
1mm,(8)3mm
×
0mm,(9)3mm
×‑
1mm,(10)3mm
×‑
2mm。动物可分为4组,其中10只大鼠接受溶媒对照移植(ctrl),并且3组每组15只大鼠接受逐渐增加的细胞剂量,范围为从每只动物400k细胞到2m细胞(表5)。最高处理剂量组d3具有另外10只移植后未接受dox的动物,共25只动物。所有大鼠通过交替侧的ip注射每天接受免疫抑制以避免移植排斥。移植后,可对动物观察详细的临床检查,包括体重、后肢的运动和感觉功能、发病和死亡。这些观察可对处理组(ctrl、d1、d2或d3)以及动物是否正在接受dox处理(即d3组包括10只未给予dox的动物)完全盲态。所有动物均可在疾病发作时处死以进行进一步分析,所述疾病发作由后肢或前肢的连续bbb评分为15或更低确定。
[0278]
表5.用于运动皮质移植inpc-gdnf
dox
的实验组。
[0279][0280]
*10只动物作为移植对照不被给予dox
[0281]
为了确定inpc-gdnf
dox
细胞的移植是否保护皮质第5层中的皮质脊髓运动神经元,以及可能保护脊髓的颈部、胸部和腰部区域中的脊髓运动神经元,可从每只动物采集脑和脊髓两者。可使用ihc评价感兴趣的植入区域的连续切片。在皮质中,由bcl11b或satb2的表达所指示的第5层锥体神经元可在植入物的近端和远端区域被量化。虽然在als中受影响的靶皮质脊髓运动神经元不表达satb2,但它可提供有关inpc-gdnf
dox
移植对除皮质脊髓运动
神经元外的邻近细胞类型的相对效应的信息。可如上所述评价脊髓的chat 运动神经元。
[0282]
inpc-gdnf
dox
的双位点移植:患者中的最终产物需要减缓皮质和腰运动神经元的退化,以成为最有效的治疗方法。因此,可确定如果向脊髓和运动皮质二者中的细胞递送保护了运动神经元池,其提供最佳疗法。在此目标中,一组25只sod1
g93a
大鼠可被在两种位点以根据每个位点确定的最有效剂量移植细胞。这些动物中的10只作为移植对照不被给予dox。然后,可将cns10-npc-gdnf在作为阳性对照的15只动物中以100k细胞/位点(cns10-npc-gdnf ind剂量范围研究的中间剂量)移植到腰脊髓中,并以20k细胞/位点移植到运动皮质中。为了减轻双移植动物的紧张,可以先进行皮质移植,在腰脊髓移植之前有两周的恢复期。作为模型对照,未接受处理的10只sod1
g93a
同窝仔(littermate)可与经移植的动物一起被评价。一旦从腰移植恢复,可对所有动物观察详细的临床检查,包括体重、后肢和前肢的运动和感觉功能、发病和死亡。这些观察可完全盲态。如前所述,所有大鼠都可接受每日免疫抑制,并且可在疾病发作时处死动物,所述疾病发作由前所述的行为鉴定所确定。脑和脊髓组织的评价可使用所述的ihc进行,并且皮质脊髓运动神经元和脊髓运动神经元的保护程度可结合行为观察进行评分。特别感兴趣的可为植入百分比,以及与上述讨论的经评价的单个位点相比的此双位点模型的保护性益处。
[0283]
inpc-gdnf
dox
疗法可引起sod1
g93a
大鼠的脊髓中chat 细胞的保护和运动皮质的bcl11b 细胞的保护。如果没有观察到gdnf表达和/或细胞植入,则可使用更高的剂量来确定dox处理在野生型大鼠中的功效。如果口服强饲和通过饮用水给予二者都证明能有效激活这些动物中的gdnf表达,则可使用通过饮用水给予,因为此方法可最好地转化为患者中的口服递送。在使用概括的递送机制不能激活这些构建体的情况下,可使用用于在sod1
g93a
大鼠的3位点模型中进行功效测试的实施例1中描述的组成型产物inpc-gdnf
const
。在观察到植入物的存活不良和/或宿主神经元的保护不良的情况下,可通过将诱导型细胞移植到野生型大鼠中来实现替代给药方案。
[0284]
实施例3:inpc-gdnf
dox
在培养中的安全性和在裸大鼠中的长期移植。
[0285]
在该研究中,评价了inpc-gdnf
dox/const
在没有免疫抑制的健康动物中的安全性和耐受性。源自ipsc组织的合理担忧是由于多能干细胞起源而产生失控增殖的危险。首先,可通过全基因组测序来确认细胞的基因组完整性,并且可使用临床接受的测量来验证多能细胞的不存在。一旦产生了可接受的细胞批次,将在裸大鼠的脊髓中评价inpc-gdnf
dox
疗法的长期安全性和致瘤性。不受特定理论束缚地,假设缺乏多能基因表达的分化的、基因组完整的细胞将被证明在免疫受损的大鼠中是安全的。
[0286]
多能基因的检测和基因组稳定性的验证:由于潜在的畸胎瘤形成是对于源自ipsc的产物的担忧,并且根据fda和isscr指南,可通过对多能因子oct-4的简单的qpcr筛选来验证储存的多批次的inpc-gdnf
dox
细胞。此种检测测定的限制可评估与ipsc相比的inpc-gdnf
dox
分化批次中的多能转录物的数量,并已被验证用于其它临床材料的gmp生产。如果细胞产物含有《0.1%的在起源的ipsc中检测到的oct-4转录物,则认为该细胞产物已通过。
[0287]
基因编辑技术和延长的细胞培养操作有可能产生基因组和核型异常,因此还必须验证inpc-gdnf产物在遗传水平上是稳定的。然后将通过oct-4检测的批次提交进行全基因组测序和g带核型分析二者。inpc-gdnf
dox
的批次的可接受评分被限定为已被验证在aavs1基因座中包含正确的gdnf构建体,表达《0.1%的在起源的ipsc中检测到的oct-4转录物,并
且具有正常的核型。
[0288]
致瘤性和体内安全性:根据fda指南,健康动物代表了用于进行传统毒理学研究的标准模型系统
50,51
。来自最初的inpc方案的移植100k细胞/位点的经慢病毒转导的细胞的初步研究显示,这些细胞在裸大鼠脊髓中有效植入,并且可以存活长达9个月。人细胞核标志物和增殖标志物ki67的组织学示出了这些移植物在这段时间内失去了它们的增殖行为(图9a-图9b)。ki67染色的缺乏证明inpc-gdnf移植中几乎没有不受控制的增殖危险。
[0289]
为了评价与inpc-gdnf
dox
长期移植相关的潜在风险,这些细胞的毒理学和致瘤潜能可通过移植到免疫受损的无胸腺裸大鼠的腰脊髓或运动皮质中来评估。每组可使用15只动物。如目标2中所确定的,在每个位置处保护宿主神经元的最高有效剂量可用于使对植入形成任何非期望效应或应答的机会最大化。接受腰脊髓移植的动物可接受以每个位点2μl的体积进行的双侧注射,沿腰脊髓在相隔1mm的6个位点(3个位点/侧)进行。接受向运动皮质中的植入的动物可接受以每个位点2μl的体积进行的双侧注射,在目标2.2b中列出的相同的前囟位置进行递送。如目标2.1中所确定的,dox给予和剂量可在手术后一周开始,并在整个研究期间持续。所有动物都可接受dox,因为这一目标的目的是确定由细胞本身和神经营养因子gdnf的分泌两者引起的效应程度。来自脊髓和皮质研究两者的动物可在移植后30天(3只动物/研究)和180天(12只动物/研究)进行评价。为了确定inpc产物的安全性,可对动物体重和总体生理学监测畸胎瘤形成或运动活动障碍的迹象。在每个时间点,可收集各自的植入组织,连续切片,然后使用免疫组织化学进行测定。移植存活的量化(检测人细胞核和胞浆蛋白)、增殖(检测与人标志物共定位的ki67)、宿主神经元健康(检测神经丝、chat、bcl11b、satb2和tunel染色)和宿主组织反应性(由激活的胶质细胞上调gfap表达或其它蛋白质)。还可对移植的组织切片和整个器官进行致瘤性分析。
[0290]
鉴于使用源自ipsc的组织作为安全的
20
细胞治疗剂的其它研究的成功,可在inpc-gdnf产物中检测到基因组稳定性和多能标志物的缺失。对inpc-gdnf
dox
的长期植入和致瘤性的评价可确定作为治疗产物使用的安全性,并且鉴于使用原始inpc-gdnf产物的研究中的植入量以及增殖细胞的缺乏,应证明所述细胞在皮质和脊柱移植中是安全的。在检测到明显的生长的情况下(这损害运动行为或似乎会导致动物疼痛),然后可评估次高剂量的细胞。cns10-npc-gdnf阳性对照可用于比较以确定迁移程度、ki67染色或反应性在治疗进展的可接受范围内。与cns10-npc-gdnf动物的观察相差大于20%的值可被认为是不可接受的(即检测到多20%的ki67 人细胞)。虽然不太可能,但如果inpc-gdnf
dox
表达极高水平的ki67表达,替代的方法可为用减少增殖的γ-分泌酶抑制剂处理培养中的细胞
52,53
,然后这些细胞可解离并在一小组的无胸腺大鼠中进行测试。
[0291]
上述各种方法和技术提供了实施本发明的多种方式。当然,应当理解的是,根据本文描述的任何特定实施方式,不一定实现所描述的所有目标或优点。因此,例如本领域技术人员将认识到,可以按实现或优化如本文所教导的一个优点或一组优点的方式执行所述方法,而不必实现如本文教导或建议的其它目标或优点。本文提及了多种有利和不利的替代方案。应当理解的是,一些优选实施方式具体地包括一个、另一个或数个有利特征,而另一些具体地排除一个、另一个或数个不利特征,而还有另一些通过包括一个、另一个或数个有利特征来具体地减轻当前的不利特征。
[0292]
此外,技术人员将认识到来自不同实施方式的各种特征的适用性。类似地,本领域
普通技术人员可混合和匹配上文讨论的各种要素、特征和步骤,以及每个此类要素、特征或步骤的其它已知等效物,以执行根据本文描述的原理的方法。在多种实施方式中,各种要素、特征和步骤中的一些将被具体地包括而另一些将被具体地排除。
[0293]
尽管本发明已经在某些实施方式和实例的上下文中公开,但是本领域技术人员将理解的是,本发明的实施方式超出具体公开的实施方式而延伸至其它替代实施方式和/或用途以及其修饰和等效物。
[0294]
在本发明的实施方式中已经公开了许多变化和替代要素。对于本领域技术人员来说,更进一步的变化及替代要素将是显而易见的。这些变化不受限制地为与诱导多能干细胞(ipsc)、分化的ipsc(包括神经祖细胞)、用于操作上述细胞的载体相关的组合物和方法,与上述组合物的用途、技术及其中使用的溶液的组成和用途相关的方法和组合物,以及通过本发明的教导产生的产物的特定用途。本发明的各种实施方式可具体地包括或排除这些变化或要素中的任一个。
[0295]
在一些实施方式中,用于描述和要求保护本发明的某些实施方式的表示成分的量、特性(如浓度)、反应条件等的数值将被理解为在某些情况下通过术语“约”修饰。因此,在一些实施方式中,书面描述和所附权利要求中阐述的数值参数是可根据特定实施方式寻求获得的期望特性而变化的近似值。在一些实施方式中,应该根据报告的有效数字位数的数量并通过应用普通的舍入技术来解释数值参数。尽管阐述本发明一些实施方式的宽泛范围的数值范围和参数是近似值,但在具体实施例中阐述的数值被尽可能准确地报告。在本发明的一些实施方式中呈现的数值可包含某些误差,这些误差由于在它们各自的测试测量中发现的标准偏差而不可避免地产生。
[0296]
在一些实施方式中,在描述本发明的特定实施方式的上下文中使用的术语“一个/一种(a/an)”和“该(the)”以及类似的指代(尤其是在所附权利要求中的某些的上下文中)可被解释为覆盖单数和复数二者。本文中数值范围的叙述仅意在用作单独指代落入该范围内的每个单独值的简写法。除非在本文中另有指示,否则每个单独的值都被并入说明书中,如同它在本文中被单独引用。除非本文另有指示或与上下文明显矛盾,否则本文所述的所有方法都可以以任何合适的顺序执行。关于本文中的某些实施方式提供的任何和所有实例或示例性语言(例如“比如/如”)的使用仅旨在更好地阐明本发明并且不对在其它的要求保护的本发明的范围构成限制。说明书中的任何语言都不应被解释为表示对本发明的实践必不可少的任何未要求保护的要素。
[0297]
本文公开的本发明的替代要素或实施方式的分组不应被解释为限制性的。各个组成员可单独地被提及和要求保护,或与该组的其它成员或见于本文中的其它要素任意组合地被提及和要求保护。出于方便和/或可专利性的原因,组的一个或多个成员可被包含在组中或从组中删除。当任何此类包含或删除发生时,本说明书在本文中被认为包含经修改的组,从而满足在所附权利要求中使用的所有马库什组的书面描述。
[0298]
本文描述了本发明的优选实施方式,包括发明人已知的用于实施本发明的最佳模式。在阅读先前的描述后,那些优选实施方式的变化对于本领域普通技术人员将变得显而易见。在考虑之列的是,熟练的技术人员可适当地采用此类变化,并且可以按不同于本文具体描述的方式实践本发明。因此,本发明的许多实施方式包括在适用法律的允许下在所附权利要求中记载的主题的所有修改和等效物。此外,除非本文另有说明或与上下文明显矛
盾,否则本发明涵盖上述要素在其所有可能变化中的任意组合。
[0299]
此外,贯穿本说明书对专利和印刷出版物进行了大量参考。以上引用的参考文献和印刷出版物中的每一个都通过引用的方式将其整体各自地并入本文。
[0300]
最后,应当理解的是,本文公开的本发明的实施方式是对本发明原理的说明。可采用的其它修改可在本发明的范围内。因此,通过示例而非限制,可根据本文的教导使用本发明的替代配置。因此,本发明的实施方式不限于精确地如所示和所描述的那样。
[0301]
序列
[0302]
seq id no:1-pb-rtp-tet-gdnf/memclover-fluc
[0303]
[0304]
[0305]
[0306]
[0307]
[0308]
[0309]
[0310]
[0311]
[0312]
[0313][0314]
seq id no:2-gdnf基因参考序列
[0315]
ncbi参考序列:nc_000005.10:c37840044-37812677
[0316]
seq id no:3-gdnf mrna转录序列
[0317]
ncbi参考序列:nm_000514.4
[0318]
智人胶质细胞源性神经营养因子(gdnf),转录物变体1,mrna
[0319]
[0320]
[0321][0322]
seq id no:4-gdnf氨基酸序列
[0323]
ncbi参考序列:np_000505.1
[0324]
胶质细胞系源性神经营养因子亚型1前原蛋白[智人]
[0325][0326]
seq id no:5-aavs1-tet-on-3g-gdnf
[0327]
[0328]
[0329]
[0330]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。