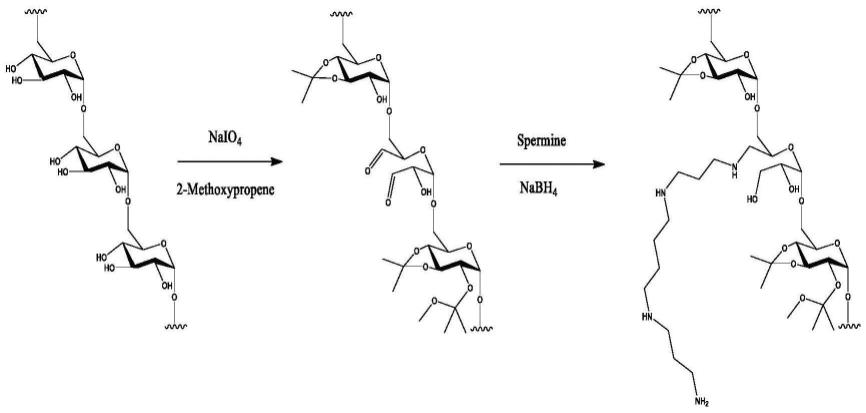
1.本发明属于抗纤维化和抗肿瘤药物技术领域,具体涉及一种吗替麦考酚酯的亚油酸偶联前药在抗纤维化药物或/和抗肿瘤中的应用。
背景技术:
2.吗替麦考酚酯(mycophenolate mofetil,mmf)的活性成分mpa(mycophenlic acid,mpa)是一种是非竞争性可逆的次黄嘌呤核苷单磷酸脱氢酶抑制剂,因其能够有效抑制t、b淋巴细胞增殖而被广泛用于防治器官移植术后的急性排斥。随着研究的深入,发现mmf对成纤维细胞以及肿瘤细胞均具有显著抑制作用,因而可能应用于抗纤维化及抗肿瘤治疗中。但是mmf水溶性极差,在临床上以口服用药为主,但胃肠道反应较大,且肝脏首过效应大幅降低了其体内生物利用度。
3.纳米制剂技术被认为是改善难溶性药物体内生物利用度的有效手段,且研究表明,纳米粒易于被成纤维细胞摄取;此外,肿瘤内高度纤维化使药物难以有效作用于肿瘤细胞。因此mmf纳米制剂将实现更高的体内生物利用度以及针对成纤维细胞的靶向杀伤作用,降低肿瘤内微环境纤维化基质从而实现更好的抗肿瘤效果。但是单mmf纳米制剂水溶性较差,在体内留存时间较短,且对肿瘤的靶向杀伤力低,治疗效果有限。
技术实现要素:
4.本发明提供一种吗替麦考酚酯的亚油酸偶联前药在抗纤维化药物或/和抗肿瘤中的应用;体外细胞实验显示,mmf-la纳米制剂能够有效抑制小鼠成纤维细胞及各肿瘤细胞增殖;体内动物实验显示,mmf-la纳米制剂能够有效减少肿瘤内的肿瘤相关成纤维细胞数量和胶原蛋白沉积,并显著抑制肿瘤生长。
5.本发明提供一种吗替麦考酚酯的亚油酸(mmf-la)偶联前药在抗纤维化药物中的应用,其中,所述吗替麦考酚酯的亚油酸偶联前药的结构式如下:
[0006][0007]
所述吗替麦考酚酯的亚油酸偶联前药能够实现自组装纳米化。
[0008]
研究表明mmf具有较好的抗纤维化作用,且成纤维细胞对纳米颗粒有较强的摄取能力。为更好实现mmf的抗纤维化效能,本发明通过利用亚油酸修饰前体药物的策略,构建出mmf-la偶联前药自组装纳米制剂和聚乙二醇化mmf-la偶联前药纳米制剂,较好地改善了mmf的药代动力学特性,延长药物体内循环时间,从而实现更好的成纤维细胞杀伤作用,达
3-磷酸乙醇胺-n-[甲氧基(聚乙二醇)]的质量比为10:1。作为优选,所述1,2-二硬脂酰基-sn-甘油-3-磷酸乙醇胺-n-[甲氧基(聚乙二醇)]为dspe-peg
2k
。
[0027]
作为具体优选,上述聚乙二醇化mmf-la偶联前药纳米制剂的制备方法,包括将溶有mmf-la偶联前药与含有dspe-peg
2k
的有机溶剂于超声条件下注入水相中,透析得到均匀分散的纳米颗粒。
[0028]
制备过程中,可将mmf-la偶联前药及dspe-peg
2k
分别溶于有机溶剂中,再将有机溶剂充分混匀,最后将混匀的有机溶剂于超声条件下注入水相,透析得到均匀分散的纳米颗粒。
[0029]
作为优选,有机溶剂为二甲基亚砜溶剂,二甲基亚砜与水相体积比为1:9。
[0030]
本发明提供了以上基于mmf-la偶联前药自组装纳米制剂、聚乙二醇化mmf-la偶联前药纳米制剂。前述形式的纳米制剂显著提高了mmf的水溶性,同时用于修饰的亚油酸为人体所需物质,生物相容性好,便于临床转化,具有较好的应用前景。更为重要的是,mmf-la纳米制剂显著改善了药物的药代动力学特性,延长其体内循环时间,并可将药物有效递送至纤维化的肿瘤微环境,发挥更强效的抗纤维化和抗肿瘤作用。
[0031]
与现有技术相比,本发明的优势效果体现在:
[0032]
1)本发明用于修饰mmf的亚油酸为人体必需脂肪酸,安全性及生物相容性好,便于临床转化;
[0033]
2)本发明通过对mmf修饰亚油酸,有效提高了药物水溶性,并通过降低药物在血液中的直接释放,从而降低mmf活性成分mpa的毒性;
[0034]
3)本发明构建的mmf-la偶联前药自组装纳米制剂避免使用增溶剂、表面活性剂等辅料,进一步提高了载药量;
[0035]
4)本发明构建的聚乙二醇化mmf-la偶联前药能实现更高的成纤维细胞靶向作用,从而达到更好的抗纤维化效能。
[0036]
5)本发明构建的mmf-la纳米制剂能够维持mmf的体内抗肿瘤有效浓度,并通过降低肿瘤内纤维化水平,增大瘤内药物蓄积,从而实现更强的抗肿瘤效果。
[0037]
综上所述,本发明将mmf-la偶联前药应用于抗纤维化药物和抗肿瘤药物中,提高了药物在体内的存留时间,进而提高了抗纤维化效能,并能有效抑制肿瘤生长,提高治疗效果,且用药安全性高。
附图说明
[0038]
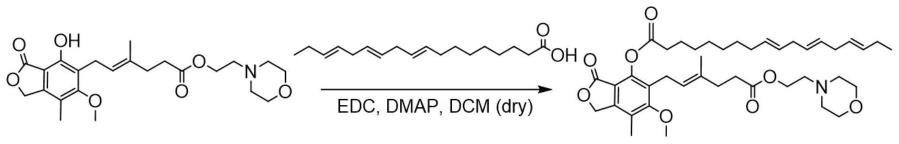
图1为实施例1中mmf-la偶联前药的合成路线图;
[0039]
图2为实施例1中制得的mmf-la偶联前药的核磁氢谱图;
[0040]
图3为实施例2中(2)成纤维细胞体外杀伤效果对比图;
[0041]
图4为实施例2中(3)α平滑肌肌动蛋白的抗纤维化效果对比图;
[0042]
图5为实施例2中(3)四型胶原蛋白的抗纤维化效果对比图;
[0043]
图6为实施例2中(4)肿瘤内成纤维细胞靶向作用对比图;
[0044]
图7a为实施例2中(5)肝癌细胞huh7体外生长对比图;
[0045]
图7b为实施例2中(5)肝癌细胞sun449体外生长对比图;
[0046]
图7c为实施例2中(5)肝癌细胞lm3体外生长对比图;
[0047]
图8a为实施例2中(6)高度纤维化肿瘤体内生长对比图;
[0048]
图8b为实施例2中(6)高度纤维化肿瘤体内生长曲线对比图;
[0049]
图8c为实施例2中(6)普通肿瘤体内生长对比图;
[0050]
图8d为实施例2中(6)普通肿瘤体内生长大小对比图;
[0051]
图8e为实施例2中(6)普通肿瘤增殖细胞核抗原表达对比图。
具体实施方式
[0052]
实施例1
[0053]
mmf-la偶联前药的合成,如图1所示:
[0054]
在100ml圆底烧瓶中依次加入mmf(65mg,0.15mmol)、亚油酸(42.1mg,0.15mmol)和dmap(18.3mg,0.15mmol),溶解于4ml无水二氯甲烷,再快速滴加edc(23.3mg,0.15mmol)。43℃搅拌3小时,利用薄层色谱观察反应情况。当反应基本结束时,冷却反应液,分别用0.1m盐酸溶液,饱和碳酸氢钠,饱和食盐水清洗;有机相用无水硫酸钠干燥,过滤,收集滤液后减压除去溶剂;通过柱层析色谱分离纯化(dcm:meoh=20:1)后得到产物mmf-la偶联前药(47mg,产率45.1%)。
[0055]
产物mmf-la偶联前药的1h nmr核磁数据如下,核磁谱图如图2所示:
[0056]1h nmr(400mhz,cdcl3):δ5.30-5.42(m,4h),5.14(s,2h),5.10(t,1h,j=13.3hz),4.16(t,2h,j=11.8hz),3.78(s,3h),3.68(t,4h.j=9.4hz),3.34(d,2h,j=6.9hz),2.78(t,2h,j=13.3hz),2.68(t,2h,j=15.4hz),2.57(t,2h,j=12.0hz),2.47(t,4h,j=9.2hz),2.36-2.41(m,2h),2.26-2.31(m,2h),2.22(s,3h),2.03-2.08(m,4h),1.75-1.81(m,5h),1.25-1.36(m,14h),0.89(t,3h,j=13.4hz).
[0057]
实施例2
[0058]
(1)聚乙二醇化mmf-la纳米制剂的制备:
[0059]
将实施例1中制得的聚乙二醇化mmf-la偶联前药溶于含有dspe-peg
2k
的二甲基亚砜溶剂中,得混合溶液,其中聚乙二醇化mmf-la偶联前药与dspe-peg
2k
的质量比为10:1;并将混合溶液于超声条件下注入水相中(二甲基亚砜与水相体积比为1:9),透析得到均匀分散的聚乙二醇化mmf-la纳米制剂,记为dspe-peg
2k
包被mmf-la纳米制剂。
[0060]
作为dspe-peg
2k
包被mmf-la纳米制剂的对照组,将聚乙酸-聚乙二醇(peg
5k-pla
8k
)代替上述dspe-peg
2k
,采用上述方法制备聚乙酸-聚乙二醇化mmf-la纳米制剂,记为peg
5k-pla
8k
包被mmf-la纳米制剂。
[0061]
(2)体外杀伤成纤维细胞实验:
[0062]
体外培养小鼠nih-3t3成纤维细胞,胰酶消化后吹散并用含有胎牛血清的培养基重悬,将细胞浓度调整为3*10^4个/毫升培养基。将细胞悬液种于96孔板中,每孔加入100ul,即每孔3*10^3个细胞,并于培养条件下放置24小时。之后,向不同孔的培养基中加入不同浓度的dspe-peg
2k
包被mmf-la纳米制剂、peg
5k-pla
8k
包被mmf-la纳米制剂或者mmf原药,分别形成含有不同浓度的dspe-peg
2k
包被mmf-la纳米制剂、不同浓度的peg
5k-pla
8k
包被mmf-la纳米制剂和不同浓度的mmf原药的培养基。药物作用48小时后,使用cck8检测试剂盒检测各用药组细胞活性。
[0063]
如图3所示,发现经dspe-peg
2k
包被mmf-la纳米制剂、peg
5k-pla
8k
包被mmf-la纳米
制剂或者mmf原药处理后,成纤维细胞活性均受明显抑制,呈现剂量依赖性,且纳米制剂与原药的抑制效果相似,表明dspe-peg
2k
包被mmf-la纳米制剂在体外与mmf原药相比,其杀伤成纤维细胞效果并未因纳米载药系统的缓释效应而减弱。另外,dspe-peg
2k
包被mmf-la纳米制剂对成纤维细胞的杀伤效果优于peg
5k-pla
8k
包被mmf-la纳米制剂对成纤维细胞的杀伤效果。
[0064]
(3)体内抗纤维化实验:
[0065]
将nih-3t3小鼠成纤维细胞与hep1-6细胞以2:1比例混合种于裸鼠皮下构建高度纤维化肿瘤模型。将小鼠分为对照组(未处理组),mmf原药处理组、dspe-peg
2k
包被mmf-la纳米制剂处理组以及peg
5k-pla
8k
包被mmf-la纳米制剂处理组,待皮下种瘤3天后开始用药处理小鼠,隔天给药,一共五次。用药结束后取下肿瘤组织并制成石蜡切片,通过免疫组化检测α平滑肌肌动蛋白(α-sma)和四型胶原蛋白以确定dspe-peg
2k
mmf-la纳米制剂体内抗纤维化效果。
[0066]
如图4和5所示,免疫组化结果表明,应用dspe-peg
2k
包被mmf-la纳米制剂与mmf原药相比能够显著减少肿瘤内α-sma阳性细胞(成纤维细胞)比例以及胶原蛋白沉积,表明其具有更强效的体内抗纤维化作用。然而应用peg
5k-pla
8k
包被mmf-la纳米制剂的抗纤维化效果并不显著,提示dspe-peg
2k
材料为本方案制备聚乙二醇化纳米制剂的优选。
[0067]
(4)肿瘤内靶向成纤维细胞实验:
[0068]
使用近红外染料dir标记dspe-peg
2k
包被mmf-la纳米颗粒后,尾静脉注射入荷瘤小鼠体内。24小时后,取下小鼠肿瘤组织并做冰冻切片。通过免疫荧光染色标记α-sma阳性细胞(成纤维细胞)并于共聚焦显微镜下检测dir标记的dspe-peg
2k
包被mmf-la纳米制剂与成纤维细胞的共定位情况。
[0069]
如图6所示,共聚焦显微镜下显示dspe-peg
2k
包被mmf-la纳米制剂主要集中在成纤维细胞聚集处,表明其具有较高的体内成纤维细胞靶向能力。
[0070]
(5)肿瘤体外生长抑制实验:
[0071]
体外培养肝癌细胞系lm3、sun449、huh7以及hep1-6,胰酶消化后用含有胎牛血清的培养基重悬,并将细胞浓度调整为3*10^4个/毫升培养基。将各种肝癌细胞悬液分别种于96孔板中,每孔加入100ul,即每孔3*10^3个细胞,并于培养条件下放置24小时。之后,加入不同浓度的dspe-peg
2k
包被mmf-la纳米制剂、peg
5k-pla
8k
包被mmf-la纳米制剂或者mmf原药。药物作用48小时后,使用cck8检测试剂盒检测各用药组细胞活性。
[0072]
如图7a、b、和c所示,结果表明,dspe-peg
2k
包被mmf-la纳米制剂、peg
5k-pla
8k
包被mmf-la纳米制剂或者mmf原药均能够显著抑制肿瘤细胞生长,且在lm3、sun449、huh7肝癌细胞系中应用dspe-peg
2k
包被mmf-la纳米制剂的最大杀伤肿瘤能力显著高于mmf原药以及peg
5k-pla
8k
包被mmf-la纳米制剂,提示dspe-peg
2k
包被mmf-la纳米制剂在体外能够更有效地提高mmf在这些细胞内的蓄积浓度。
[0073]
(6)肿瘤体内生长抑制实验:
[0074]
将nih-3t3小鼠成纤维细胞与hep1-6细胞以2:1比例混合种于裸鼠皮下构建高度纤维化肿瘤模型。将小鼠分为对照组(未处理组),mmf原药处理组、dspe-peg
2k
包被mmf-la纳米制剂处理组以及peg
5k-pla
8k
包被mmf-la纳米制剂处理组,待皮下种瘤3天后开始用药处理小鼠,隔天给药,一共四次。期间记录小鼠肿瘤体积,用药结束后取出肿瘤组织,比较各组
肿瘤大小并拍照。
[0075]
如图8a和b所示,结果表明dspe-peg
2k
包被mmf-la纳米制剂处理后肿瘤体积显著减少,提示其可能通过缓解肿瘤组织纤维化而增大肿瘤内药物蓄积浓度,从而实现更强的抗肿瘤效果。
[0076]
单独将hep1-6细胞以40万/只种于c57bl/6小鼠皮下构建无纤维化的普通肝癌模型。将小鼠分为对照组(未处理组),mmf原药处理组,dspe-peg
2k
包被mmf-la纳米制剂处理组以及peg
5k-pla
8k
包被mmf-la纳米制剂处理组,待皮下种瘤3天后开始用药处理小鼠,隔天给药,一共四次。用药结束后取出肿瘤组织,比较各组肿瘤大小并拍照。将肿瘤组织用福尔马林处理后制备成蜡块,通过免疫组化检测各组肿瘤内增殖细胞核抗原(pcna)阳性的肿瘤细胞数以确定肿瘤增殖活性。
[0077]
如图8c、d和e所示,结果表明经dspe-peg
2k
包被mmf-la纳米制剂处理组其肿瘤体积以及pcna阳性细胞比例相比未处理组及mmf原药处理组均显著减少,表明dspe-peg
2k
包被mmf-la纳米制剂与mmf原药相比在体内更能发挥直接抗肿瘤作用。此外,应用非dspe-peg
2k
材料(peg
5k-pla
8k
)包被的mmf-la纳米制剂处理组表现出较差的体内直接抗肿瘤作用,提示dspe-peg
2k
材料为上述聚乙二醇化mmf-la偶联前药纳米制剂制备方案的优选。
[0078]
注:图8c、d、e中非dspe-peg
2k
材料包被mmf-la纳米制剂处理组即为peg
5k-pla
8k
包被mmf-la纳米制剂处理组;mmf-la纳米制剂处理组为dspe-peg
2k
包被mmf-la纳米制剂处理组。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。