1.本发明涉及一种岩藻糖异构酶及使用该岩藻糖异构酶生产岩藻糖的方法,该岩藻糖异构酶可逆地催化l-岩藻糖和l-墨角藻糖之间的异构化反应并来源自从鲍鱼肠中分离的新拉乌尔菌属(raoultella sp.)kdh 14菌株。
背景技术:
2.l-岩藻糖(6-脱氧-l-半乳糖)是一种存在于从细菌到人类的多种生物体中的稀少糖。例如,l-岩藻糖以人乳寡糖(human milk oligosaccharide,hmo)或糖蛋白的形式存在,并且还作为微生物胞外多糖(exopolysaccharide,eps)和海藻的成分存在。l-岩藻糖因其多种生理活性特性,在医药领域可用作抗炎、抗肿瘤和增强免疫的药物,在化妆品行业可用作美白剂、皮肤保湿剂和抗衰老剂,或可用作营养素。由于l-岩藻糖具有多种生理活性,因此l-岩藻糖可应用于各个领域,如制药、医学、食品及化妆品。
3.对于工业应用,l-岩藻糖可通过三种主要方法(多糖水解、化学和酶促合成)生产。首先,水解多糖的方法是通过用酸或酶处理含有岩藻糖的海藻或微生物的胞外多糖来获得岩藻糖的方法。其次,化学合成是一种使用化学品从廉价的糖类如d-半乳糖或d-甘露糖来合成l-岩藻糖的方法。上述两种方法的缺点是收率低,产生副产品,并且需要大量的劳动。也就是说,经济效益低。相比之下,酶促合成法可特异性生产l-岩藻糖,对环境友好,被认为具有成本效益。基于酶法合成l-岩藻糖的主要的已知方法有两种,l-墨角藻糖作为中间体参与这两种反应。一种是基于l-岩藻糖代谢过程中的醛醇反应的方法,经乳醛与二羟丙酮磷酸(dihydroxyacetone phosphate,dhap)发生醛醇反应,再经酸性磷酸酶去磷酸化,产生l-墨角藻糖。二是酶化学法,首先使用d-半乳糖为起始原料,通过化学方法合成l-岩藻糖醇,然后将l-岩藻糖醇通过脱氢酶转化为l-墨角藻糖。这两种方法都需要l-岩藻糖异构酶(ec 5.3.1.25)将中间体l-墨角藻糖(l-fuculose)转化为l-岩藻糖。l-fuci是一种酮醇异构酶,其催化l-岩藻糖和l-墨角藻糖之间的相互转化。l-岩藻糖和l-墨角藻糖之间的反应是可逆的,由于达到平衡状态,增加l-岩藻糖的产量是有限的。因此,使用有利于逆反应(即从l-墨角藻糖到l-岩藻糖的反应)的l-fuci,有利于l-岩藻糖的酶促生产。尽管如上所述的酶法很有吸引力,但迄今为止只有两个案例研究了l-岩藻糖和l-墨角藻糖之间的可逆反应。尽管研究案例更有利地催化了逆反应,但他们没有研究将l-墨角藻糖作为底物。事实上,为了提高异构酶在l-岩藻糖合成中的适用性,需要使用l-墨角藻糖作为底物进行研究,但尚未报道过此类研究。因此,重要的是发现一种以逆反应为主的新型异构酶,检查该异构酶的可逆反应,并使用l-墨角藻糖为底物来研究生化性质。
技术实现要素:
4.技术问题
5.本发明的一个目的是提供一种使用岩藻多糖作为碳源的从鲍鱼肠中分离的新微生物。
6.本发明的另一个目的是提供一种新型l-岩藻糖异构酶及其制备方法,该l-岩藻糖异构酶从所述微生物中分离出来,并有利于l-岩藻糖和l-墨角藻糖之间的可逆反应中l-墨角藻糖向l-岩藻糖的转化反应。
7.本发明的再一个目的是提供一种使用该新微生物和来源自该新微生物的l-岩藻糖异构酶生产l-岩藻糖的方法。
8.技术方案
9.为了实现该目的,本发明提供了一种l-岩藻糖异构酶,其包含seq id no:1的氨基酸序列并有利于l-墨角藻糖和l-岩藻糖之间的可逆反应中l-墨角藻糖向l-岩藻糖的转化反应。
10.本发明还提供了一种编码l-岩藻糖异构酶的核酸分子。
11.本发明还提供了一种包含该核酸分子的重组载体。
12.本发明还提供了一种用该重组载体转化的宿主细胞。
13.本发明还提供了一种制备l-岩藻糖异构酶的方法,该方法包括:通过培养宿主细胞来表达l-岩藻糖异构酶;以及获得表达的l-岩藻糖异构酶。
14.本发明还提供了一种用于生产l-岩藻糖的组合物,该组合物包含:l-岩藻糖异构酶;和选自由l-墨角藻糖和d-核酮糖组成的组中的一种或多种底物。
15.本发明还提供了一种生产l-岩藻糖的方法,该方法包括:使l-岩藻糖异构酶与选自由l-墨角藻糖和d-核酮糖组成的组中的一种或多种底物反应。
16.有益效果
17.根据本发明的从鲍鱼肠中分离的来源于拉乌尔菌属kdh 14菌株的l-岩藻糖异构酶有利于l-岩藻糖与l-墨角藻糖之间的可逆反应中l-墨角藻糖向l-岩藻糖进行的反应,因此可应用于l-岩藻糖的生产。
附图说明
18.图1示出了本发明的拉乌尔菌属kdh 14菌株的基于16s rrna的系统发育树;
19.图2示出了本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci基因序列;
20.图3示出了本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci的凝胶过滤层析结果和使用his-trap柱通过亲和层析纯化的sds-page结果(插图);
21.图4a示出了通过本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci得到的l-岩藻糖向l-墨角藻糖的酶促转化(正反应);
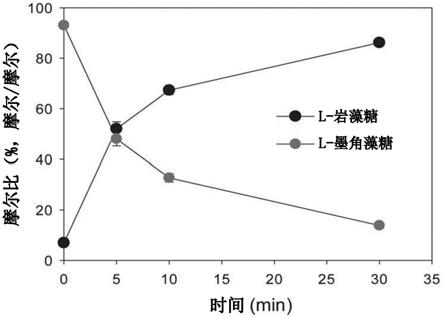
22.图4b示出了通过本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci得到的l-墨角藻糖向l-岩藻糖的酶促转化(逆反应);
23.图5a示出了温度对本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci得到墨角藻糖的影响;
24.图5b示出了ph对本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci得到墨角藻糖的影响;
25.图6示出了本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci的底物特异性;
26.图7a和图7b示出了本发明的来源于拉乌尔菌属kdh 14菌株的rdfuci的完整结构和寡聚形式;以及
墨角藻糖向l-岩藻糖进行的反应,因此即使在使用l-岩藻糖或l-墨角藻糖作为底物时,在平衡状态中也能表现出l-岩藻糖的比例为90%或更多。
44.此外,当使用l-墨角藻糖作为底物时,在30℃至50℃下显示出80%或更高的相对最大酶活性。然而,当温度超出上述温度范围时,酶活性下降到低于50%。此外,在醋酸钠缓冲液、磷酸钠缓冲液和甘氨酸-naoh缓冲液中,ph为6至11时,显示出相对最大活性为70%或更高,而在tris-hcl缓冲液的情况下,活性在上述ph条件下是低的,这意味着tris可能起到酶的抑制剂的作用。
45.此外,一般而言,糖异构酶需要金属离子作为辅因子,并且本发明的l-岩藻糖异构酶在选自由mn
2
、mg
2
、co
2
、cd
2
和zn
2
组成的组中的一种或多种金属离子下进行反应期间表现出高相对活性。特别是,在存在mn
2
的情况下,酶的活性提高了约7倍。此外,本发明的l-岩藻糖异构酶的活性可以被选自由fe
2
、ca
2
和cu
2
组成的组中的一种或多种金属离子抑制(参见表1)。
46.此外,一般而言,糖异构酶表现出各种底物反应性,本发明的l-岩藻糖异构酶对l-墨角藻糖和d-核酮糖表现出高活性,因此对酮糖底物比对醛糖底物反应更有优势得多(参见图6)。
47.同时,通过晶体结构分析证实,本发明的l-岩藻糖异构酶在活性位点附近具有环状构象,这与现有技术中揭示的l-fuci不同,具体描述如下。
48.单体rdfuci包括有包含n1结构域、n2结构域和c结构域的19个α螺旋和23个β链(图7a)。n1结构域(ser5-met172)采用α/β折叠并参与rdfuci六聚体形成的底物识别。n2结构域(lys173-leu352)和c结构域(thr353-arg591)包括参与催化活性的金属结合残基(图7a)。rdfuci亚基与三聚体的二聚体具有d3h虚拟对称性。底物结合口袋由亚基a的n2结构域和c结构域以及亚基b的n1结构域形成(图8a至图8c),且在同源六聚体rdfuci中共有六个底物结合位点。底物结合口袋的底物接近的入口约为(图8a)。其中形成金属结合位点的底物结合口袋具有约的带负电荷表面(图8b)。金属结合位点与底物结合口袋之间的距离约为(图8d),这意味着活性中心位于口袋深处。这表明底物的开放形式和环形式均可接近活性位点中心,但这也表明大体积的糖类不能接近存在于底物结合口袋内的活性位点。底物结合口袋的重叠表明,底物识别残基(arg16、w88、gln300、tyr437、trp496和asn524)表现出较小的三维结构,而金属结合残基glu337、asp361和his528(rdfuci中的编号)与其他蛋白的位置相同。相反,置于底物结合口袋的表面上的每个l-fuci的α7-α8环具有不同的构象。虽然l-fuci的序列比对展现出高的相似性,但每个l-fuci的α7-α8环的序列非常多样化(图9b)。每个l-fuci形成了独特的底物结合口袋,因为α7-α8环参与了底物结合口袋的结构形成(图9c)。虽然l-fuci通常在金属结合位点周围具有带负电荷表面,但底物结合口袋的表面展现出不同的电荷状态(图9c)。因此,α7-α8环结构的差异可能导致l-fuci的底物特异性的差异。
49.此外,本发明的l-岩藻糖异构酶不仅可以通过酶的编码区之前和之后的区域进行转录和翻译,还可以通过包含各个编码片段之间的插入序列的与多肽产生相关的dna片段(即编码基因)进行转录和翻译。例如,l-岩藻糖异构酶可以从seq id no:2所示的序列进行转录和翻译,但并不特别限于此。此外,有利于l-岩藻糖和l-墨角藻糖之间的可逆反应中l-墨角藻糖向l-岩藻糖的转化反应的、作为酶的具有一种或多种取代、缺失、转座、添加等的
变体蛋白的蛋白质也包括在本发明的酶的范围内,优选地,该蛋白质包括与seq id no:1中所示的氨基酸序列具有80%或更多、85%或更多、90%或更多、93%或更多的、94%或更多、95%或更多、96%或更多、97%或更多、98%或更多及99%或更多同一性的氨基酸序列。
50.在本说明书中,“蛋白质”和“多肽”在本技术中可互换使用。
51.在本发明中,多肽与另一序列具有特定百分比(例如,80%、85%、90%、95%或99%)的序列同一性的事实意味着当比对两个序列时,在比较序列时存在特定百分比的相同氨基酸残基。比对和百分比同源性或同一性可以使用在本领域公知的任何合适的软件程序中描述的那些来确定,例如,文件[current protocols in molecular biology(f.m.ausubel et al.,(eds)1987supplement 30section 7.7.18)]。优选程序的示例包括gcg pileup程序、fasta(pearson et al.,1988pr℃.natl acad.sci usa 85:2444-2448)和blast(blast manual,altschul et al.,natl.cent.biotechnol.inf.,natl lib.med.(ncib nlm nih),bethesda,md,and altschul et al.,1997nar25:3389-3402)。另一种优选的比对程序是align plus(scientific and educational software,pa),并且优选地是使用基本参数的比对程序。另一个可用的序列软件程序是序列软件包版本6.0(sequence software package version 6.0)中可用的tfasta data searching program(genetics computer group,university of wisconsin,madison,wi)。
[0052]
l-岩藻糖异构酶可以从本发明的使用岩藻多糖作为碳源的新菌株拉乌尔菌属kdh 14的培养物的上清液中分离和纯化,并且可以使用基因工程重组技术或人工化学合成方法通过除了拉乌尔菌属kdh 14以外的菌株生产和分离。
[0053]
当使用重组技术时,可以使用用于促进典型重组蛋白表达的因子,例如抗生素抗性基因,以及可用于亲和柱层析的报告蛋白或肽,这些技术都在可由本发明所属领域的技术人员容易地执行的范围内。例如,l-岩藻糖异构酶可以从用重组载体转化的宿主细胞或其培养物获得,该重组载体包括编码l-岩藻糖异构酶的基因,即seq id no:2所示的碱基序列。使用大肠杆菌作为宿主细胞,但宿主细胞不限于此。
[0054]
l-岩藻糖异构酶可以使用l-墨角藻糖、d-核酮糖等作为底物。
[0055]
本发明还提供了一种编码l-岩藻糖异构酶的核酸分子。
[0056]
如本文所用,术语“核酸分子”是指cdna、基因组dna、合成dna或rna、pnas或lna来源的任何单螺旋或双螺旋核酸分子、或其混合物。“核酸”和“多核苷酸”在本技术中可以互换使用。由于遗传密码是简并的,可以使用一个或多个密码子来编码特定氨基酸,并且本发明包括编码特定氨基酸序列的多核苷酸。前述“核酸分子”包括:a)编码根据本发明的l-岩藻糖异构酶的核酸碱基序列及其功能等价物;或b)在非常高的严格条件下与该序列杂交的序列。非常高的严格条件如公知文献(molecular cloning,cold spring harbor,new york,cold spring harbor laboratory press,1989)中所述。此外,核酸分子可以包括与a)和b)中的核酸碱基序列具有70%或更多、更优选80%或更多、甚至更优选90%或更多、并且最优选95%或更多的序列同源性的碱基序列。此外,核酸分子可以包括a)和b)的任何核酸分子的片段或互补物。
[0057]
本发明的编码l-岩藻糖异构酶的核酸分子可以具有编码由seq id no:1的氨基酸表示的l-岩藻糖异构酶的碱基序列和与上述碱基序列具有同源性的碱基序列,并且优选地,可以具有seq id no:2的碱基序列或与上述碱基序列具有同源性的碱基序列。
[0058]
本发明的编码l-岩藻糖异构酶的核酸分子可以由本发明公开的序列信息通过本领域公知的核酸分子的构建方法来获得。例如,作为起始原料的核酸分子可以从拉乌尔菌属kdh14菌株中分离和/或可以基于本发明公开的碱基序列合成制备。
[0059]
编码l-岩藻糖异构酶的核酸分子可以是分离的多核苷酸,即基本上不含其他染色体dna和rna以及其他碱基序列如染色体外dna和rna的多核苷酸,但不限于此。可以使用本领域技术人员公知的核酸分子纯化方法来获得分离的核酸分子。或者,本发明的核酸分子是功能性多核苷酸,在细菌细胞的情况下,该功能性多核苷酸根据需要可操作地与启动子、核糖体结合位点和终止子连接。
[0060]
本发明还提供了一种包含该核酸分子的重组载体。
[0061]
如本文所用,术语“质粒”、“载体”或“表达载体”在本发明中可互换使用,是指用于体内或体外表达的构建体。这些构建体可以用于将编码l-岩藻糖异构酶的核酸分子插入宿主细胞。在这些构建体中,编码l-岩藻糖异构酶的核酸可操作地连接到适当的调控序列以便在宿主细胞中表达,并且当插入宿主细胞时,载体可以独立于宿主基因组复制和发挥作用,或者在某些情况下,载体可以整合到宿主基因组本身中。通常,质粒载体具有包括以下的结构:有效复制使得每个宿主细胞包含数百个质粒载体的复制起点;允许选择插入质粒的宿主细胞的抗生素抗性基因;以及允许外源核酸分子插入的限制酶切割位点。即使在没有合适的限制酶切割位点的情况下,也可以根据典型方法使用合成的寡核苷酸适配子或接头容易地将载体与外源核酸分子连接。
[0062]“可操作地连接”是指以当合适的核酸分子与调控序列结合时使得基因能够表达的方式连接。
[0063]“重组体”是指复制异源核酸分子、或表达该核酸分子、或表达由肽、异源肽或异源核酸分子编码的蛋白质的细胞。重组细胞可以以有义或反义形式表达细胞的野生型形式中不存在的基因或基因片段。此外,重组细胞可以表达见于野生型状态的细胞中的基因,但是这些基因通过人工方式被修饰并重新引入细胞中。“载体”将核酸分子递送到细胞中。“载体”可以进一步包括用于调控转录的任何操纵子序列、编码适当的mrna核糖体结合位点的序列和调控转录和翻译终止的序列。
[0064]
可用于在宿主细胞中表达的载体是本领域公知的,特别是可用于在大肠杆菌中表达的合适的载体也是本领域公知的。根据本发明的具体示例性实施方式,使用pet28a作为载体,但载体不限于此。
[0065]
本发明还提供了一种用该重组载体转化的宿主细胞。
[0066]
如本文所用,术语“宿主细胞”包括包含了上述核酸分子或载体的任何细胞,并且可用于l-岩藻糖异构酶的重组生产。作为宿主细胞,通常使用导入核酸分子效率高且导入的核酸分子的表达效率高的宿主细胞。宿主细胞包括原核或真核细胞,作为包括这些宿主细胞的重组微生物,例如可以使用细菌、酶、霉菌等,并且在本发明的示例性实施方式中,使用大肠杆菌,但宿主细胞不限于此,可以使用任何类型的微生物,只要可以充分表达根据本发明的l-岩藻糖异构酶突变体。
[0067]
在本发明中,可以使用通常已知的操作方法将核酸分子插入宿主细胞。例如,可以使用微粒轰击、粒子枪轰击、碳化硅晶须、超声处理、电穿孔、peg介导的融合、显微注射、脂质体介导的方法、in planta转化法、真空渗透法、花分生组织浸渍法、以及农杆菌喷洒法。
[0068]
本发明还提供了一种制备l-岩藻糖异构酶的方法,该方法包括:通过培养宿主细胞来表达l-岩藻糖异构酶;以及获得表达的l-岩藻糖异构酶。
[0069]
多种培养方法可用于重组宿主细胞的(大量)培养,例如,可通过分批或连续培养方法实现由重组微生物表达或过表达的基因产物的大规模生产。分批和补料分批培养方法是本领域常规且已知的。用于连续培养过程的调节营养物和生长因子的方法,以及使产物形成速率最大化的技术在微生物工业领域中是已知的。此外,作为培养基,可以使用包含碳源、氮源、维生素和矿物质的培养基,并且可以根据本领域已知的方法构成组合物。
[0070]
本发明还提供了一种用于生产l-岩藻糖的组合物,该组合物包含:岩藻糖异构酶;和选自由l-墨角藻糖和d-核酮糖组成的组中的一种或多种底物。
[0071]
该组合物可以是液体或固体。该组合物还可以仅包含l-岩藻糖异构酶,还可以一起包含其他蛋白质或酶,并且还可以包含l-岩藻糖异构酶、其他蛋白质或补充酶的稳定性和/或活性的额外的添加剂。其实例包括甘油、山梨糖醇、丙二醇、盐、糖、ph缓冲剂、防腐剂和碳水化合物,但不限于此。通常,液体组合物是水基或油基浆料、悬浮液或溶剂。固体组合物可以由液体组合物通过喷雾干燥、冻干、下吸式蒸发、薄层蒸发、离心蒸发、传送带干燥或其组合来制备。可以将固体组合物制粒成适合应用于食品或饲料的尺寸。
[0072]
此外,本发明提供了一种生产l-岩藻糖的方法,该方法包括:使l-岩藻糖异构酶与选自由l-墨角藻糖和d-核酮糖组成的组中的一种或多种底物反应。
[0073]
反应可以在缓冲溶液中进行,l-岩藻糖异构酶的最适ph可以根据缓冲溶液的种类而不同,但可以为约ph 6至ph 11。反应温度可以为30℃至50℃。由于酶活性在50℃或更高时急剧下降,而l-岩藻糖异构酶即使在室温下也能够进行充分的酶促反应,因此具有可以经济地执行工艺而无需消耗能量来升高温度的优点。此外,酶可以通过在相对低于现有酶的温度下进行热处理而失活。
[0074]
因此,优选地,反应可以在作为反应条件的30℃至50℃和ph6至ph11的条件下进行5分钟至1小时。
[0075]
缓冲溶液可以是乙酸钠缓冲液、磷酸钠缓冲液、甘氨酸-naoh缓冲液等。作为例外,在tris-hcl缓冲液的情况下,tris可以作为酶的抑制剂,因此需要限制其使用。
[0076]
另外,作为确认金属离子对l-岩藻糖异构酶的酶活性的影响的结果,mn
2
、mg
2
、co
2
、cd
2
、和zn
2
提高了酶活性,但fe
2
、ca
2
和cu
2
抑制了酶活性。因此,可以通过在增加酶活性的金属离子下进行反应来增强l-岩藻糖的产生。
[0077]
在下文中,将通过根据本发明的实施例更详细地描述本发明,但本发明的范围不受以下提出的实施例的限制。
[0078]
《实施例1》微生物分离鉴定和基因鉴定
[0079]
fuci酶的微生物来源是属于拉乌尔菌属的细菌,并且基于其以作为海藻的成分的岩藻多糖作为唯一碳源而生长的能力而从鲍鱼肠中分离。分离的菌株通过基于16s rrna测序(使用细菌16s rrna引物27f(5'-ttgatcctggctcag-3':seq id no:3)和1492r(5'-ggctaccttgttacgactt-3':seq id no:4)通过pcr扩增16s rrna序列,并比较了与ncbi数据库中的rna序列的相似性)的系统发育树被鉴定为拉乌尔菌属的新物种,并在本发明中命名为拉乌尔菌属(raoultella sp.)kdh 14。为了找到岩藻糖的异构酶,进行了基因组序列分析,并通过确认基于blast的序列相似性来鉴定岩藻糖异构酶。菌株鉴定相关的系统发育树
如图1所示,以上内容的详细流程如下。
[0080]
1)将鲍鱼肠分解,用水稀释,并接种到含2%岩藻多糖的m9基本培养基中。
[0081]
2)将接种的细胞在30℃培养。
[0082]
3)通过synergy htx多功能酶标仪确认细胞生长,并分离出生长速率高的菌株。
[0083]
《实施例2》rd fuci的克隆、表达和纯化
[0084]
在克隆本发明中使用的rd fuci基因时,从分离的拉乌尔菌属kdh 14中提取基因组dna,然后通过聚合酶链式反应扩增目标基因。通过将扩增的目标基因插入表达载体pet28a中来完成克隆。图2示出了基因的碱基序列。
[0085]
使用大肠杆菌bl21(de3)作为重组酶蛋白表达宿主。在用重组基因转化大肠杆菌细胞后,将大肠杆菌细胞在20ml液体培养基(lb肉汤)中种菌培养约16小时。将大肠杆菌细胞重新接种到1l的lb中,于37℃进一步培养,当od600值达到约0.6至0.8时,降温至16℃,通过向其中加入异丙基β-d-1-硫代吡喃半乳糖苷(isopropylβ-d-1-thiogalactopyranoside,iptg)诱导表达,使终浓度为1mm。加入iptg后,进一步培养大肠杆菌约16小时,然后通过离心回收细胞。在整个过程中使用50μg/ml卡那霉素作为选择标记。将回收的细胞用超声发生器破碎,然后提取和纯化细胞中的粗蛋白。使用his-trap柱通过亲和层析进行纯化过程,从300mm咪唑中回收大部分目标蛋白。
[0086]
如图3所示,确认了大小为65.5kda的酶蛋白,该酶蛋白由591个氨基酸组成。
[0087]
《实施例3》酶的可逆反应
[0088]
为了确定在岩藻糖和墨角藻糖之间的反应中rdfuci有利于哪种反应,研究了重组酶随着时间推移的可逆反应。为此目的,将包含在20mm磷酸钠(ph7)中的10mm的l-岩藻糖(图4a)或l-墨角藻糖(图4b)用作底物,并在1mm的mncl2存在下分别与1.5μg的rdfuci于30℃反应,并通过实验对l-岩藻糖进行定量。相反,l-墨角藻糖以计算值表示。
[0089]
结果,无论是使用岩藻糖还是墨角藻糖作为底物,逆反应的反应速率快了约5倍,并且平衡状态下的岩藻糖和墨角藻糖的比例约为90:10。这意味着rdfuci的催化反应有利于逆反应,即产生岩藻糖的方向。
[0090]
《实施例3》rd fuci的针对墨角藻糖的生化特性(温度、ph、和金属离子)的研究
[0091]
对于rdfuci的潜在适用性,需要使用墨角藻糖作为底物来研究各种生化特性。
[0092]
1)温度影响:在各种温度(10℃至80℃)下于ph7用1.5μg酶处理10mm底物,结果在40℃显示出最高活性,并且在30℃、40℃和50℃显示出最大近似值(最大活性的80%或更多)(图5a)。
[0093]
2)ph影响:于40℃在各种ph条件(ph4至11:50mm乙酸钠(ph4至6)、50mm磷酸钠(ph6至8)、50mm的tris-hcl(ph7至9)、50mm甘氨酸-naoh(ph9至11))下用1.5μg酶处理10mm底物,结果在碱性条件下(ph9和ph10)表现出最高活性,而在ph值为6、7、8和11时也表现出最大近似值。同时,当在ph值为7、8和9时使用tris-hcl缓冲液时,其活性远低于在相同的ph下使用其他缓冲液类型时的活性,这表明tris可能起酶的抑制剂的作用,这意味着在研究或应用本发明的酶时应避免tris缓冲液(图5b)。
[0094]
3)金属离子影响:糖异构酶一般需要金属离子作为辅因子。因此,本发明还研究了各种金属离子对rdfuci活性的影响(表1)。结果,在mn
2
存在下,酶的活性提高了约7倍。
[0095]
[表1]
[0096]
金属离子影响
[0097]
金属离子相对活性(%)对照100
±
3edta77
±
12mncl2738
±
70mgcl2533
±
31cocl2353
±
83cdcl2183
±
9zncl2159
±
4cscl2101
±
16liso4101
±
15nicl291
±
13fecl374
±
3cacl264
±
8cucl258
±7[0098]
《实施例4》rd fuci的底物特异性
[0099]
通常,糖异构酶对各种糖表现出反应性。对各种醛糖(l-岩藻糖、d-阿拉伯糖、d-阿卓糖、d-半乳糖、d-甘露糖和d-葡萄糖)和酮糖底物(l-墨角藻糖、d-核酮糖、d-阿洛酮糖、d-塔格糖和d-果糖)进行测试,结果显示出对l-墨角藻糖(115.3u/mg)和d-核酮糖(127.3u/mg)的活性最高,这表明了活性与其他测试的醛糖和酮糖底物的活性相比要高得多。此外,仅在l-墨角藻糖和d-核酮糖的情况下,rdfuci对酮糖底物比对醛糖底物表现出有优势得多的反应(图6)。
[0100]
《实施例5》rd fuci的结晶和数据收集
[0101]
使用市售试剂盒index ht、salt rx ht和crystal screen ht,在20℃下通过坐滴蒸汽扩散法进行晶体筛选。微晶主要在含有0.1m的hepes(ph7.5)、20%(w/v)聚乙二醇10000的溶液中产生。通过悬滴法从同一溶液中获得高质量的晶体。将晶体浸入含有额外20%(v/v)甘油的储存溶液中,并在氮气流中快速冷却。使用pilatus 6m从pls-ii的光束线11c或使用adsc quantum q270ccd检测器从光束线6a在100k下收集晶体的x射线衍射数据集。使用hkl2000程序处理衍射数据。
[0102]
《实施例6》rd fuci的整体结构
[0103]
使用ecfuci(pdb代码:1fui)的晶体结构作为搜索模型,使用在molrep中实施的分子置换方法解析相。使用coot手动重建和纯化结构。使用phenix.refine程序phenix进行结构纯化。使用molprobity验证结构质量。
[0104]
单体rdfuci包括有包含n1结构域、n2结构域和c结构域的19个α螺旋和23个β链(图7a)。n1结构域(ser5-met172)采用α/β折叠并参与rdfuci六聚体形成的底物识别。n2结构域(lys173-leu352)和c结构域(thr353-arg591)包括参与催化活性的金属结合残基(图7a)。rdfuci亚基与三聚体的二聚体形成d3h虚拟对称性。
[0105]
《实施例7》基于结构的rd fuci的活性位点和结合位置研究
[0106]
底物结合口袋由亚基a的n2结构域和c结构域以及亚基b的n1结构域形成(图8a至
图8c),且在同源六聚体rdfuci中共有6个底物结合位点。底物结合口袋的底物接近的入口约为(图8a)。其中形成金属结合位点的底物结合口袋具有约的带负电荷表面(图8b)。金属结合位点与底物结合口袋之间的距离约为(图8d),这意味着活性中心位于口袋深处。这表明底物的开放形状和环形状均可接近活性位点中心,但这也表明大体积的糖类不能接近存在于底物结合口袋内的活性位点。
[0107]
《实施例8》通过结构比较鉴定rd fuci的特异性
[0108]
使用dali服务器,rdfuci为大肠杆菌(ecfuci,pdb代码1fui,z评分:60.6,在587cαs的情况下,rmsd:0.3)、苍白空气芽胞杆菌(aeribacillus pallidus)(apfuci,3a9r,z评分:56.6,在580cαs的情况下,rmsd:0.7)、肺炎链球菌(streptococcus pneumonia)(spfuci,4c20,z评分:55.9,在585cαs的情况下,rmsd:0.7)的l-fuci。底物结合口袋的重叠表明,底物识别残基(arg16、w88、gln300、tyr437、trp496和asn524)表现出较小的三维结构,而金属结合残基glu337、asp361和his528(rdfuci中的编号)与其他蛋白的位置相同。相反,置于底物结合口袋的表面上的每个l-fuci的α7-α8环具有不同的构象。虽然l-fuci的序列比对展现出高的相似性,但每个l-fuci的α7-α8环的序列非常多样化(图9b)。每个l-fuci形成了独特的底物结合口袋,因为α7-α8环参与了底物结合口袋的结构形成(图9c)。虽然l-fuci通常在金属结合位点周围具有带负电荷表面,但底物结合口袋的表面展现出不同的电荷状态(图9c)。因此,α7-α8环结构的差异将导致l-fuci的底物特异性的差异。
[0109]
工业适用性
[0110]
本发明的l-岩藻糖异构酶可应用于l-岩藻糖生产领域。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。