c5-2-脂肪胺基嘧啶唑类化合物的合成方法及其应用
技术领域
1.本技术属于药物合成技术领域,尤其涉及一种c5-2-脂肪胺基嘧啶唑类化合物的合成方法及其应用。
背景技术:
2.嘧啶胺类化合物在临床药物中发挥着重要作用,目前,已有相关研究报道了2-胺基嘧啶类化合物在临床医学上的广泛应用,如:瑞舒伐他汀(bioorg.med.chem.1997,5,437-444)、格列卫(nature reviews drug discovery.2002,1,493-502),并且c5-2-胺基嘧啶类化合物在临床医学上潜在的应用价值也受到很多研究学者的关注,也取得了相关的研究成果,如抗疟药物(乙胺嘧啶)(nature.2017,543,538-542),蛋白激酶抑制剂(mapk4k抑制剂)(j.med.chem.2014,57,3484-3493)。
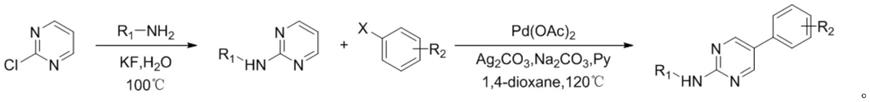
3.目前,对2-胺基嘧啶类化合物合成方法的探究有其重要的研究意义。das a等报道了c5-芳基-2-胺基嘧啶类化合物的合成方法,具体步骤为:2-氯嘧啶和伯胺在氟化钾的作用下,在溶剂中100℃反应17小时生成2-胺基嘧啶;然后2-胺基嘧啶再与芳基氯代物溶于,4-二氧六环溶液,在醋酸钯催化和碳酸银、碳酸钠与吡啶作用下,于120℃反应17小时生成c5-芳基-2-胺基嘧啶类化合物(chemical communications.2020,56),合成路线如下所示;
[0004][0005]
并且smith s m等也报道了通过氯嘧啶的胺化合成2-胺基嘧啶化合物,具体步骤为:5-溴-2,4-二氯嘧啶与三甲基氯硅烷反应生成2,4-二氯-5-(三甲基甲硅烷基)嘧啶;然后2,4-二氯-5-(三甲基甲硅烷基)嘧啶与芳香胺于碳酸铯和催化剂的作用下,生成4-氯-5-(三甲基甲硅烷基)嘧啶2-芳胺(organic letters.2016,2180),合成路线如下所示:
[0006][0007]
可以看出,目前报道的氯嘧啶的胺化合成2-胺基嘧啶类化合物的合成方法较为复杂,合成过程需要采用催化剂进行催化反应,采用催化剂进行合成的方法效率较低,反应复杂,不利于大量制备。
技术实现要素:
[0008]
本技术的目的在于提供一种c5-2-脂肪胺基嘧啶唑类化合物的合成方法及其应用,旨在解决现有技术中脂肪胺基嘧啶唑类化合物的合成方法均需要采用催化剂进行反应,导致反应复杂,不利于产物大量制备的问题。
[0009]
为实现上述申请目的,本技术采用的技术方案如下:
[0010]
第一方面,本技术提供一种c5-2-脂肪胺基嘧啶唑类化合物的合成方法,包括如下步骤:
[0011]
提供5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物、脂肪胺、无机碱、有机溶剂;
[0012]
在惰性气体保护下,将5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物、脂肪胺、无机碱于有机溶剂中进行胺化反应,得到5-(3-r
4-4-r3唑-5-基)-4-(r2)-6-(r1)-n-r5嘧啶-2-胺;
[0013]
其中,a选自氯、溴、碘中的任一种;
[0014]
r1、r2选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基、芳基、取代的芳基、杂芳基、取代的杂芳基、芳氧基、杂芳基氧基、醚基、饱和的胺基、卤素中的任一种;
[0015]
r3、r4选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基中的任一种。
[0016]
第二方面,本技术提供一种c5-2-脂肪胺基嘧啶唑类化合物,c5-2-脂肪胺基嘧啶唑类化合物由c5-2-脂肪胺基嘧啶唑类化合物的合成方法合成得到。
[0017]
第三方面,本技术提供一种c5-2-脂肪胺基嘧啶唑类化合物作为药物合成原料的应用。
[0018]
本技术第一方面提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法,该合成方法中,以5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物和脂肪胺为反应物进行反应,并提供无机碱促进脂肪胺中胺基的亲核能力,使反应物在无需催化剂的作用下发生胺化反应,生成c5-2-脂肪胺基嘧啶唑类化合物。反应过程无需使用催化剂进行反应,合成方法简单,制备时间短,方便安全,有利于进行大规模制备,使c5-2-脂肪胺基嘧啶唑类化合物能够广泛应用。
[0019]
本技术第二方面提供的c5-2-脂肪胺基嘧啶唑类化合物由提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法合成得到,得到的c5-2-脂肪胺基嘧啶唑类化合物纯度高,性能优异,适合广泛应用。
[0020]
本技术第三方面提供的c5-2-脂肪胺基嘧啶唑类化合物作为药物合成原料的应用,由于所提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法反应过程无需使用催化剂进行反应,合成方法简单,制备时间短,可大规模短时间制备c5-2-脂肪胺基嘧啶唑类化合物,适合广泛应用于药物合成领域。
具体实施方式
[0021]
为了使本技术要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。
[0022]
本技术中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b的情况。其中a,b可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
[0023]
本技术中,“至少一个”是指一个或者多个,“多个”是指两个或两个以上。“以下至
少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。例如,“a,b,或c中的至少一项(个)”,或,“a,b,和c中的至少一项(个)”,均可以表示:a,b,c,a-b(即a和b),a-c,b-c,或a-b-c,其中a,b,c分别可以是单个,也可以是多个。
[0024]
应理解,在本技术的各种实施例中,上述各过程的序号的大小并不意味着执行顺序的先后,部分或全部步骤可以并行执行或先后执行,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本技术实施例的实施过程构成任何限定。
[0025]
在本技术实施例中使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。在本技术实施例和所附权利要求书中所使用的单数形式的“一种”、
“”
和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。
[0026]
本技术实施例说明书中所提到的相关成分的重量不仅仅可以指代各组分的具体含量,也可以表示各组分间重量的比例关系,因此,只要是按照本技术实施例说明书相关组分的含量按比例放大或缩小均在本技术实施例说明书公开的范围之内。具体地,本技术实施例说明书中的质量可以是μg、mg、g、kg等化工领域公知的质量单位。
[0027]
术语“第一”、“第二”仅用于描述目的,用来将目的如物质彼此区分开,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。例如,在不脱离本技术实施例范围的情况下,第一xx也可以被称为第二xx,类似地,第二xx也可以被称为第一xx。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。
[0028]
本发明实施例中所涉及的化合物及其衍生物均是按照iupac(国际纯粹与应用化学联合会)或cas(化学文摘服务社,位于俄亥俄州哥伦布市)命名系统命名的。因此,本发明实施例中具体涉及到的化合物基团做如下阐述与说明:
[0029]
关于“碳氢基团”,碳氢基团中碳原子含量的最小值和最大值通过前缀表示,例如,前缀(ca-cb)烷基表示任何含“a”至“b”个碳原子的烷基。因此,例如,(c1-c6)烷基是指包含一至六个碳原子的烷基。
[0030]“烷氧基”是指与一氧原子键合的直链或带有支链的、单价的、饱和脂肪链,包括但不限于如甲氧基、乙氧基、丙氧基、丁氧基、异丁氧基、叔丁氧基以及其它类似基团。(ca-cb)烷氧基指任何含“a”至“b”个碳原子的烷基与一氧原子键合的直链或带有支链的、单价的、饱和脂肪链。
[0031]“烷基”是指直链或带有支链的、单价的、饱和脂肪链,包括但不限于如甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、异戊基、己基以及其它类似基团。
[0032]“杂烷基”是指直链或带有支链的、单价的、与至少一个杂原子连接的饱和脂肪链,例如但不限于甲基氨基乙基或其它类似基团。
[0033]“芳基”是指一种环状的芳香烃,包括但不限于如苯基、萘基、蒽基、菲基以及其它类似基团。
[0034]“杂芳基”是指单环或多环或稠环芳香烃,其中的一个或多个碳原子已被如氮、氧或硫等杂原子取代。如果杂芳基含有不止一个杂原子,则这些杂原子可能是相同,也可能是不同的。杂芳基包括但不限于如苯并呋喃基、苯并噻吩基、苯并咪唑基、苯并恶唑基、苯并噻唑基、苯并吡喃基、呋喃基、咪唑基、吲唑基、吲嗪基、吲哚基、异苯并呋喃基、异吲哚基、异喹啉基、异噻唑基、异恶唑基、萘啶基、噁二唑基、噁嗪基、噁唑基、酞嗪基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑基、哒嗪基、吡啶[3,4-b]吲哚基、吡啶基、嘧啶基、吡咯基、喹嗪基、喹啉
基、喹喔啉基、噻二唑基、噻三唑基、噻唑基、噻吩基、三嗪基、三唑基、呫吨基以及其它类似基团。
[0035]
本技术实施例第一方面提供一种一种c5-2-脂肪胺基嘧啶唑类化合物的合成方法,包括如下步骤:
[0036]
s01.提供5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物、脂肪胺、无机碱、有机溶剂;
[0037]
s02.在惰性气体保护下,将5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物、脂肪胺、无机碱于有机溶剂中进行胺化反应,得到5-(3-r
4-4-r3唑-5-基)-4-(r2)-6-(r1)-n-r5嘧啶-2-胺;
[0038]
其中,a选自氯、溴、碘中的任一种;
[0039]
r1、r2选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基、芳基、取代的芳基、杂芳基、取代的杂芳基、芳氧基、杂芳基氧基、醚基、饱和的胺基、卤素中的任一种;
[0040]
r3、r4选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基中的任一种。
[0041]
本技术实施例第一方面提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法,该合成方法中,以5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物和脂肪胺为反应物进行反应,并提供无机碱促进脂肪胺中胺基的亲核能力,使反应物在无需催化剂的作用下发生胺化反应,生成c5-2-脂肪胺基嘧啶唑类化合物。反应过程无需使用催化剂进行反应,合成方法简单,制备时间短,方便安全,有利于进行大规模制备,使c5-2-脂肪胺基嘧啶唑类化合物能够广泛应用。
[0042]
步骤s01中,提供5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物、脂肪胺、无机碱、有机溶剂。
[0043]
在一些实施例中,5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物的结构通式为式i所示,
[0044][0045]
其中,x选自o或s;
[0046]
y选自n、z选自c;或,y选自c,z选自n;
[0047]
a选自氯、溴、碘中的任一种;
[0048]
r1、r2选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基、芳基、取代的芳基、杂芳基、取代的杂芳基、芳氧基、杂芳基氧基、醚基、饱和的胺基、卤素中的任一种;
[0049]
r3、r4选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基中的任一种。
[0050]
在一些实施例中,r1、r2选自相同或不相同的c
1-c
10
烷基、c
1-c
10
杂烷基、c
1-c
10
的取代烷基。
[0051]
在一些具体实施例中,r1包括但不限于h、ch
3-、ch3ch
2-、ch3(ch2)
n-、ar-、ch3s-、ch3ch2s-、ch3(ch2)ns-、ch3o-、ch3ch2o-、ch3(ch2)no-;r2包括但不限于h、ch
3-、ch3ch
2-、ch3(ch2)
n-、ar-、ch3s-、ch3ch2s-、ch3(ch2)ns-、ch3o-、ch3ch2o-、ch3(ch2)no-。
[0052]
在一些实施例中,r3、r4选自相同或不相同的氢、c
1-c
10
烷基、c
1-c
10
杂烷基、c
1-c
10
的取代烷基中的任一种。
[0053]
在一些具体实施例中,r3包括但不限于h-、ch
3-;r4包括但不限于h-、ch
3-。
[0054]
在一些具体实施例中,当x选自o,y选自n、z选自c,得到的5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物的结构式如式i-1所示,
[0055][0056]
以式i-1所示的反应物进行反应,得到的产物为c5-2-脂肪胺基嘧啶异恶唑类化合物。
[0057]
在一些具体实施例中,当x选自o,y选自c、z选自n,得到的5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物的结构式如式i-2所示,
[0058][0059]
以式i-1所示的反应物进行反应,得到的产物为c5-2-脂肪胺基嘧啶恶唑类化合物。
[0060]
在一些具体实施例中,当x选自s,y选自n、z选自c,得到的5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物的结构式如式i-3所示,
[0061][0062]
以式i-3所示的反应物进行反应,得到的产物为c5-2-脂肪胺基嘧啶异噻唑类化合
(r2)-6-(r1)-n-r5嘧啶-2-胺。
[0079]
步骤s02的化学反应式如下:
[0080][0081]
在一些实施例中,惰性气体选自氮气、氦气、氩气中的至少一种,提供惰性气体,确保反应过程中不会引入其他杂质分子,使得到的产物纯度较高。
[0082]
在一些实施例中,5-(2-a-4-(r2)-6-(r1)嘧啶-5-基)-3-r
4-4-r3唑类化合物和脂肪胺的摩尔比为1:0.7~5;通过控制二者的摩尔比,确保反应速率最快,且确保在不需要催化剂的条件下可进行反应,生成纯度较高的产物。
[0083]
在一些实施例中,胺化反应的温度为75~120℃,胺化反应的时间为2~6小时。若反应温度过低,则反应不易发生,反应速度较慢;若反应温度过高,则反应生成的副产物较多,导致产物不纯,不利于后续使用。若反应时间过短,则易导致反应物反应不完全;若反应时间过长,则会导致反应效率较低。
[0084]
在一些具体实施例中,胺化反应的温度选自80℃、85℃、90℃、95℃、100℃、105℃、110℃、115℃。
[0085]
在一些实施例中,胺化反应过程中可采用油浴处理货微波处理,以达到反应温度进行反应。
[0086]
在一些实施例中,进行胺化反应后,还包括:将反应得到的产物进行萃取、洗涤、干燥、过滤、纯化,得到5-(3-r
4-4-r3唑-5-基)-4-(r2)-6-(r1)-n-r5嘧啶-2-胺。
[0087]
在一些具体实施例中,进行胺化反应后,还包括:将反应得到的产物用乙酸乙酯萃取,饱和食盐水洗3遍,收集乙酸乙酯萃取溶液,用无水硫酸钠干燥,过滤,然后用pe:ea=6:1进行柱层析纯化处理,得到5-(3-r
4-4-r3唑-5-基)-4-(r2)-6-(r1)-n-r5嘧啶-2-胺。
[0088]
本技术实施例第二方面提供一种c5-2-脂肪胺基嘧啶唑类化合物,c5-2-脂肪胺基嘧啶唑类化合物由c5-2-脂肪胺基嘧啶唑类化合物的合成方法合成得到。
[0089]
本技术实施例第二方面提供的c5-2-脂肪胺基嘧啶唑类化合物由提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法合成得到,得到的c5-2-脂肪胺基嘧啶唑类化合物纯度高,性能优异,适合广泛应用。
[0090]
在一些实施例中,5-(3-r
4-4-r3唑-5-基)-4-(r2)-6-(r1)-n-r5嘧啶-2-胺的结构通式如式iii所示,
[0091]
[0092]
其中,x选自o或s;
[0093]
y选自n、z选自c;或,y选自c,z选自n;
[0094]
r1、r2选自相同或不相同的c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基、芳基、取代的芳基、杂芳基、取代的杂芳基、芳氧基、杂芳基氧基、醚基、饱和的胺基、卤素中的任一种;
[0095]
r3、r4选自相同或不相同的氢、c
1-c
20
烷基、c
1-c
20
杂烷基、c
1-c
20
的取代烷基中的任一种;
[0096]
r5选自c
1-c
20
烷基、c
1-c
20
环烷基、四氢-2h-吡喃-烷基、四氢呋喃-烷基、苄胺、1,2,3,4-四氢萘胺、氨基茚满中的任一种。
[0097]
本技术实施例第三方面提供c5-2-脂肪胺基嘧啶唑类化合物作为药物合成原料的应用。
[0098]
本技术实施例第三方面提供的c5-2-脂肪胺基嘧啶唑类化合物作为药物合成原料的应用,由于所提供的c5-2-脂肪胺基嘧啶唑类化合物的合成方法反应过程无需使用催化剂进行反应,合成方法简单,制备时间短,可大规模短时间制备c5-2-脂肪胺基嘧啶唑类化合物,适合广泛应用于药物合成领域。
[0099]
下面结合具体实施例进行说明。
[0100]
实施例1
[0101]
当x为o,y为n,z为c,r2为甲氧基,r1,r3和r4都为氢时,所用原料为5-(2-氯-4-甲氧基嘧啶-5-基)异恶唑;脂肪胺选自叔丁胺;无机碱选自碳酸钾;有机溶剂选自1,4-二氧六环;
[0102]
c5-2-脂肪胺基嘧啶唑类化合物的合成方法,包括如下步骤:
[0103]
于25ml反应管中依次加入5-(2-氯-4-甲氧基嘧啶-5-基)异恶唑600mg(2.84mmol)、叔丁胺1.04g(14.2mmol),碳酸钾784mg(5.68mmol)在惰性气体保护下,加入10ml的1,4-二氧六环,于微波100℃下反应两个小时;反应结束后,用乙酸乙酯萃取,饱和食盐水洗3遍,收集乙酸乙酯萃取溶液,用无水硫酸钠干燥,过滤,然后用pe:ea=6:1进行柱层析,得到产品400mg。产物为白色固体,纯度为95%,收率为54%,所得到的产物经质谱和核磁共振确认结构,结果为:1h nmr(400mhz,cdcl3)δ8.62(1h,s),8.24-8.22(1h,d),6.50-6.49(1h,d),4.07(3h,s),1.45(9h,s).ms(esi):[m h
]249.
[0104]
实施例2
[0105]
当x为o,y为n,z为c,r2为甲氧基,r1,r3和r4都为氢时,所用原料为5-(2-氯-4-甲氧基嘧啶-5-基)异恶唑;脂肪胺选自α,α-二甲基苄胺;无机碱选自碳酸钾;有机溶剂选自1,4-二氧六环;
[0106]
c5-2-脂肪胺基嘧啶唑类化合物的合成方法,包括如下步骤:
[0107]
于10ml反应管中依次加入5-(2-氯-4-甲氧基嘧啶-5-基)异恶唑(19mmol)、α,α-二甲基苄胺20mg(15mmol),碳酸钾52mg(38mmol),在惰性气体保护下,加入3ml的1,4-二氧六环,于微波120℃下反应两个小时;反应结束后,用乙酸乙酯萃取,饱和食盐水洗3遍,收集乙酸乙酯萃取溶液,用无水硫酸钠干燥,过滤,然后用pe:ea=6:1进行柱层析,得到5-(异恶唑-5-基)-4-甲氧基-n-(2-苯基丙-2-基)嘧啶-2-胺产物7.6mg,其为白色固体,纯度为95%,收率为16.2%,所得到的产物经质谱和核磁共振确认结构,结果为:1h nmr(400mhz,cdcl3)δ8.64(1h,s),8.22-8.21(1h,d),7.47-7.43(2h,m),7.32-7.30(2h,m),7.23-7.19
(1h,m),6.43-6.42(1h,d),3.50(3h,s),1.86(6h,s).ms(esi):[m h ]310.
[0108]
实施例3
[0109]
当x为o,y为n,z为c,r2为甲氧基,r1和r3都为氢,r4为甲基时,所用原料为5-(2-氯-4-甲氧基嘧啶-5-基)-3-甲基异恶唑;脂肪胺选自环己胺盐酸盐;无机碱选自碳酸钾;有机溶剂选自1,4-二氧六环;
[0110]
c5-2-脂肪胺基嘧啶唑类化合物的合成方法,包括如下步骤:
[0111]
于10ml反应管中依次加入5-(2-氯-4-甲氧基嘧啶-5-基)-3-甲基异恶唑40mg(18mmol)、环己胺盐酸盐19mg(14mmol),碳酸钾49mg(36mmol),在惰性气体保护下,加入3ml的1,4-二氧六环,于100℃下反应6个小时。反应结束后,用乙酸乙酯萃取,饱和食盐水洗3遍,收集乙酸乙酯萃取溶液,用无水硫酸钠干燥,过滤,然后用pe:ea=6:1进行柱层析,得到n-环己基-4-甲氧基-5-(3-甲基异恶唑-5-基)嘧啶-2-胺产物16mg,其为白色固体,纯度为95%,收率为40%,所得到的产物经质谱和核磁共振确认结构,结果为:1h nmr(400mhz,cdcl3)δ8.67(1h,s),8.39-8.35(1h,d),6.58-6.53(1h,d),4.06(3h,s),3.45-3.41(1h,m),2.43(3h,s),2.07-2.02(2h,m),1.78-1.63(4h,m),1.41-1.34(4h,m).ms(esi):[m h ]289.
[0112]
实施例4
[0113]
当x为o,y为n,z为c,r2为甲氧基,r1和r4为氢,r3为甲基时,所用原料为5-(2-氯-4-甲氧基嘧啶-5-基)-4-甲基异恶唑;脂肪胺选四氢-2h-吡喃三胺;无机碱选自碳酸钾;有机溶剂选自1,4-二氧六环;
[0114]
于10ml反应管中依次加入5-(2-氯-4-甲氧基嘧啶-5-基)-4-甲基异恶唑40mg(18mmol)、四氢-2h-吡喃三胺14mg(14mmol),碳酸钾49mg(36mmol),在惰性气体保护下,加入3ml的1,4-二氧六环,于100℃下反应6个小时。反应结束后,用乙酸乙酯萃取,饱和食盐水洗3遍,收集乙酸乙酯萃取溶液,用无水硫酸钠干燥,过滤,然后用pe:ea=6:1进行柱层析,得到4-甲氧基-5-(4-甲基异恶唑-5-基)-n-(四氢-2h-吡喃-3-基)嘧啶-2-胺产物20mg,其为白色固体,纯度为95%,收率为50%,所得到的产物经质谱和核磁共振确认结构,结果为:1h nmr(400mhz,cdcl3)δ8.65(1h,s),8.40-8.35(1h,d),6.58-6.52(1h,d),4.08(3h,s),3.86-3.63(4h,m),2.71-2.60(1h,m),2.52(3h,s)1.90-1.63(4h,m).ms(esi):[m h ]291.
[0115]
以上所述仅为本技术的较佳实施例而已,并不用以限制本技术,凡在本技术的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。