一种控制污水硝化过程温室气体n2o产生量的方法
技术领域
1.本发明涉及污水处理技术领域,尤其涉及硝化过程温室气体n2o减排技术。
背景技术:
2.n2o是《京都议定书》中认定的三种重要温室气体(co2、ch4、n2o)之一,其温室效应约为co2的300倍,在大气层中的存在时间为114年。n2o也是臭氧层的潜在破坏者。在大气层中,n2o正以每年0.3%的速度持续积聚。经研究,世界上大约三分之二的n2o的排放是由土壤农业利用和污水生物脱氮中微生物作用造成的,污水生物脱氮已经成为温室气体排放的主要人为源,因此,在“碳中和、碳达峰”背景下,减少污水生物脱氮过程中n2o的排放具有重要意义。
3.硝化过程是全球氮循环的一个关键步骤。经典的硝化过程是nh3在氨氧化菌(aob)的作用下氧化为no
2-,然后no
2-在亚硝酸盐氧化菌(nob)的作用下被氧化为no
3-。nh3经aob氧化过程包括两个阶段,首先,nh3在细菌细胞膜上氨单加氧化酶(amo)的作用下,被氧化为羟胺(nh2oh)。其次,羟胺经过细菌周质中羟胺氧化酶的作用被氧化no
2-。羟胺被氧化为no
2-的过程会产生4个电子,其中2个电子提供给amo作用下的初始nh3氧化,另外两个电子与o2结合产生能量。aob作用下n2o的产生途径可能分为3个途径:(1)aob的好氧反硝化过程,即nh2oh提供2个电子,no
2-或no取代o2作为电子受体生成n2o,此过程no
2-还原酶和no还原酶参与其中。(2)在羟胺氧化过程中会生成中间体noh,noh是一种不稳定化合物,其经过化学分解作用会生成n2o或者no,no会在no还原酶或者某种细胞色素的作用下被还原成n2o。(3)nh2oh与no
2-或者o2的化学反应也可能生成n2o。
4.中国专利公开号为cn 101372374a的现有技术公开了实现污水脱氮过程中n2o产生的减量控制方法属于污水脱氮领域。通过水泵将污水打入密封反应器中,水加至设定的位置关闭水泵,打开电磁阀和曝气泵,并通过曝气头开始向反应器中曝压缩空气,在整个曝气过程中ph、dosbrorp测定仪在线检测水质的变化;温度感应探头在线感知反应器内的温度;在反应器内的曝气开始的同时,反应器底部磁力搅拌器也同时开始工作;整个过程都是利用电脑和plc控制系统自动完成的,产生的n2o气体通过气体采样口、气体干燥管后收集在气体采样袋之中,反应器中的压力用压力调节和平衡系统维持恒定;最后通过气相色谱仪对其进行定量分析。本发明确定出每一步污水脱氮过程中n2o的主要产生机理和影响因素。但是,该发明并没有以实际生活污水为研究对象,而且具有过窄的影响因素范围(ph为4~7、do为1~3),这与实际运行过程并不相符。
技术实现要素:
5.要解决的问题针对污水硝化过程强力温室气体n2o排放的问题,本发明提供了一种控制生活污水硝化过程温室气体n2o产生量的方法,本方法通过同步调节硝化过程菌群的最适do和ph值,以达到n2o具有最小释放量的目的。
6.技术方案申请人前期研究表明,硝化过程是do持续消耗和ph不断降低的过程,研究do与ph协同影响下的传统硝化过程n2o的产生更具有实际意义,但是现有技术中未见相关记载。
7.为了解决上述问题,本发明所采用的技术方案如下:一种控制生活污水硝化过程温室气体n2o产生量的方法,包括将曝气池do浓度控制在3mg/l,并将曝气池ph控制在8.5的步骤。
8.优选地,所述曝气池do浓度通过在线式do值测定仪实时监测。
9.优选地,所述曝气池ph在线式ph值测定仪实时监测。
10.优选地,所述方法中硝化过程包括进水、好氧、缺氧、静沉、排水循环的运行方式。
11.一种控制生活污水硝化过程温室气体n2o产生量的方法,包括:(1)利用在线式do值测定仪实时监测曝气池do浓度,并将其控制在3mg/l;(2)实施在线式ph值测定仪实时监测曝气池ph,并将其控制在8.5。
12.优选地,所述的硝化过程中污水的运行do值用plc自动控制曝气系统调节控制。
13.优选地,所述的硝化过程中污水的运行ph值用naoh或hcl溶液调节。
14.优选地,污水中cod的浓度为100-300mg/l。
15.优选地,污水中氨氮的浓度为40-80 mg/l。
16.有益效果相比于现有技术,本发明的有益效果为:(1)本发明不改变现有工艺,不增加额外构筑物,仅需要增加在线监测系统和plc加药控制系统和曝气控制系统;(2)本发明在运行中切实减少了n2o的排放,与未采取此办法的污水硝化过程相比,减排幅度为73.3%;(3)本发明在实现n2o减排的同时,提高了全程硝化过程no
2-‑
n生成率(87%),较高的no
2-‑
n生成率可为厌氧氨氧化工艺提供基质,也能节省反硝化过程中的碳源利用量和反应时间。
17.(4)本发明实现了硝化过程:(1)nh
4 -n的最大氧化率;(2)相对较大的no
2-‑
n生成率,较高的no
2-‑
n生成率可为厌氧氨氧化工艺提供基质,也能节省反硝化过程中的碳源利用量和反应时间;(3)有力的减少了硝化过程温室气体n2o的产生量,并将其降到最低。
附图说明
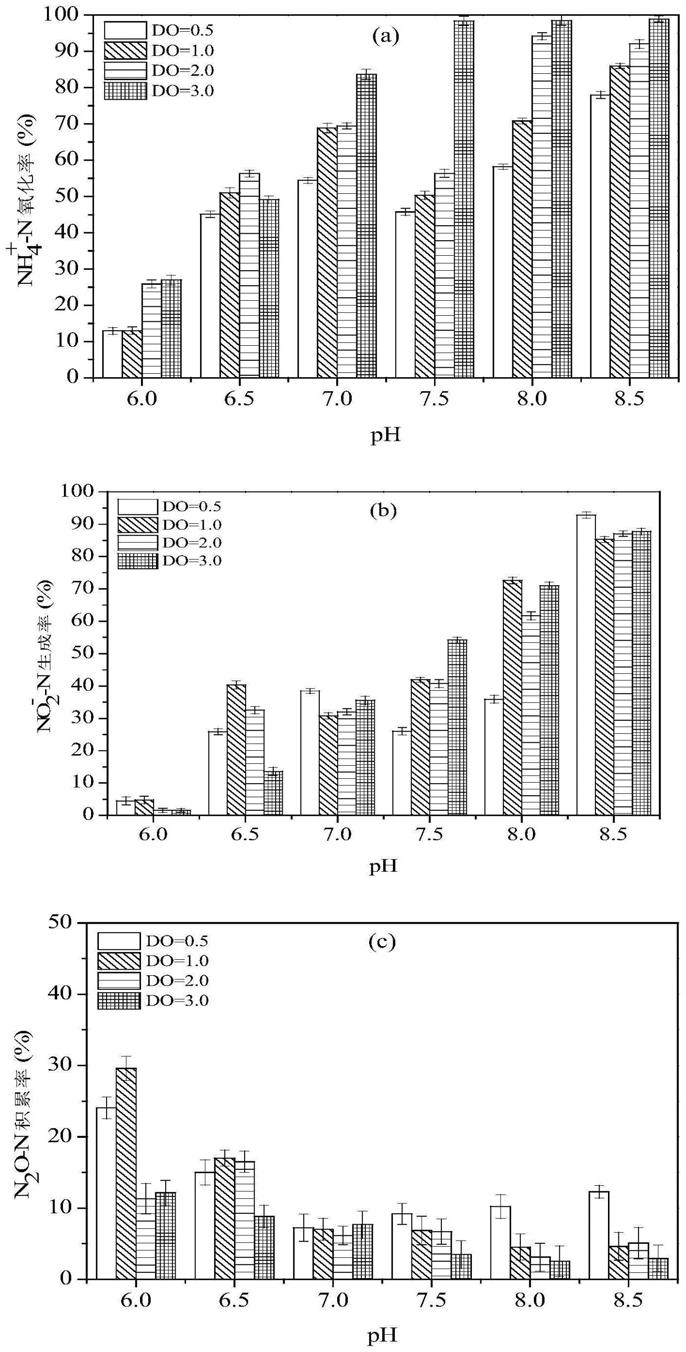
18.图1(a)do与ph协同作用下的nh
4 -n氧化率;(b)do与ph协同作用下的no
2-‑
n生成率;(c)do与ph协同作用下的n2o-n积累率;图2 本发明的运行工艺流程图。
具体实施方式
19.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同;本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
20.实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂
或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
21.如本文所使用,术语“约”用于提供与给定术语、度量或值相关联的灵活性和不精确性。本领域技术人员可以容易地确定具体变量的灵活性程度。
22.浓度、量和其他数值数据可以在本文中以范围格式呈现。应当理解,这样的范围格式仅是为了方便和简洁而使用,并且应当灵活地解释为不仅包括明确叙述为范围极限的数值,而且还包括涵盖在所述范围内的所有单独的数值或子范围,就如同每个数值和子范围都被明确叙述一样。例如,约1至约4.5的数值范围应当被解释为不仅包括明确叙述的1至约4.5的极限值,而且还包括单独的数字(诸如2、3、4)和子范围(诸如1至3、2至4等)。相同的原理适用于仅叙述一个数值的范围,诸如“小于约4.5”,应当将其解释为包括所有上述的值和范围。此外,无论所描述的范围或特征的广度如何,都应当适用这种解释。
23.下面结合具体实施例对本发明进一步进行描述。
实施例
24.试验污泥取自某高校sbr中试反应器(6m3),实验水为实际生活污水。中试反应器采用传统进水0.5h-好氧4h-缺氧2h-静沉1h-排水0.5h的运行方式,3周期/天,曝气量2mg/l,污泥浓度(mlss)约为3500mg/l。经过连续3个月的运行,成功实现了稳定的全程硝化。出水nh
4 -n、 no
2-‑
n、 no
3-‑
n均在1mg/l以下。污泥取出后先曝气12h,然后用去离子水反复清洗,沉淀浓缩后待用。
25.试验用水为某高校家属区生活污水,水质状况见表1。
26.表1 实际生活污水水质 cod(mg/l)nh
4 -n(mg/l)no
2-‑
n(mg/l)no
3-‑
n(mg/l)ph最大值210.780.32.62.77.7最小值161.048.50.107.0平均值185.864.41.31.37.5试验实验采用0.1m的盐酸和0.1m的氢氧化钠溶液调节所需ph,ph梯度为6、6.5、7、7.5、8、8.5。do采用恒do控制仪调节,批次实验do分别为0.5mg/l、1.0mg/l、2.0mg/l、3.0mg/l。试验分6个批次,每批次采用1个ph值,4个do梯度。
27.试验温度为即时室温30℃。
28.试验采用sbr反应器,此反应器有效容积3l,反应开始先加1l浓缩后的污泥,然后加入2l的生活污水,此时将泥水混合液(污泥浓度为3500mg/l左右)调到批次实验所需ph值和do,实验开始运行,硝化运行时间为4h。
29.图1(a)为do与ph共同影响下的硝化过程中nh
4 -n氧化率。此图表明,nh
4 -n氧化率随着ph的升高而变大,在ph为8.5时,nh
4 -n氧化率最大值为99%(do=3mg/l),而ph在6.0时,在4个do梯度下,nh
4 -n氧化率均在27%以下。do是制约nh
4 -n氧化的重要因素,如图1(a)所示,在相同ph下,增加do浓度有利于nh
4 -n的氧化。在低曝气量条件下(do=0.5mg/l),即使ph在8.5条件下,nh
4 -n氧化率也只有78%,而在ph为7.5时,do增加到3mg/l,仍旧可以保持较高的nh
4 -n氧化率,为98%。
30.图1(b)为do与ph协同作用下的no
2-‑
n生成率。由此图可知,no
2-‑
n生成率随着ph的升高而增大。当ph为8.5时,no
2-‑
n生成率最大值为93%(do=0.5mg/l),而当ph为6时,no
2-‑n生成率随do的不同变化不大,在2%~4%之间。do对no
2-‑
n生成率的影响规律性并不一致,当ph为7.5时,no
2-‑
n生成率随着do的增大而升高;当ph在6.0和6.5时,do为3mg/l时,no
2-‑
n生成率分别下降到2%和14%。此外当ph为6.0时,酸性环境严重抑制了微生物的活性,在do变化范围内,no
2-‑
n生成率始终保持在较低的生成率。
31.图1(c)为do与ph协同作用下的n2o-n积累率。如图所示,ph在6.0时,n2o-n的积累率较高,随着ph的逐渐升高,n2o-n积累率有下降趋势,而当ph在8.5时,n2o-n积累率在曝气量最小时出现了最小值,为2.9%。从图1(c)可以看出,n2o-n积累率总体随着do的增大而减少,这表明,增加曝气量有利于减少n2o积累。
32.由以上数据可知,当生活污水硝化过程运行在do=3mg/l、ph值为8.5时,实现最大的nh
4 -n氧化率(99%)、相对较大的no
2-‑
n生成率(87%)、最小的n2o-n积累率(2.9%),相比未调节do、ph在上述定值的实际生活污水,曝气池出水获得了较高的no
2-‑
n生成率,并减少了73.3% n2o-n排放。因此,如图2所示,在曝气池运行过程中,利用do浓度实时在线监测曝气池do,并将信号传送给电脑,然后由plc自动控制系统以及曝气强度调节系统控制曝气强度,将曝气池do值始终运行在3mg/l;利用ph值实时在线监测曝气池ph,并将信号传送给电脑,然后由plc自动控制系统以及ph调节系统控制ph,将曝气池ph值始终运行在8.5。
33.以上内容是对本发明及其实施方式进行了示意性的描述,该描述没有限制性,实施例中所示的也只是本发明的实施方式之一,实际的实施方式并不局限于此。所以,如果本领域的普通技术人员受其启示,在不脱离本发明创造宗旨的情况下,不经创造性的设计出与该技术方案相似的实施方式及实施例,均应属于本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
