1.本发明涉及用于治疗宫颈癌的照射器械及宫颈癌的治疗方法。
背景技术:
2.宫颈癌患者逐渐增加,特别是20~30多岁的年轻女性的患者数不断增加。现在的宫颈癌的治疗中,将在早期阶段(i期阶段)摘除整个子宫作为标准治疗,但是对年轻患者而言,需要能够保留子宫的局部治疗以维持生育能力。另外,在进展阶段(iii期阶段以后),由于癌症扩散至周围组织而难以通过手术来切除,因此结合了放射治疗与化学药物治疗的治疗作为标准治疗。然而,5年生存率在iii期阶段为50%,在iv期阶段低至20%,需要更有效地治疗。作为癌症的局部治疗,已知有使用了光反应性物质的治疗法。其中,使用了抗体-光敏物质(亲水性酞菁染料)的治疗法通过对肿瘤中积蓄的抗体-光敏物质照射近红外光,能够特异性杀死靶细胞而不会杀死正常细胞等非靶细胞,期待可减轻副作用且获得高的治疗效果。
3.现有技术文献
4.专利文献
5.专利文献1:美国专利申请公开第2018-0113246号说明书
技术实现要素:
6.发明要解决的课题
7.另一方面,为了获得抗体-光敏物质的高治疗效果,需要可靠地对吸附于肿瘤的抗体-光敏物质照射近红外光。然而,近红外光的侵入深度较浅,光非侵袭性地从体表到达实体癌是非常困难的。因此,需要极力抑制侵袭性的同时可使光可靠地到达体内肿瘤的手段。宫颈癌的情况下,癌症多已在宫颈管的大范围内扩散,需要极力从近处对大范围的癌症照射光的手段。另外,根据进展阶段,有时癌症已到达骨盆壁,此时,利用了阴道或腹腔镜等的微创的方法很难触到骨盆壁。例如,专利文献1中公开了将具备光纤的长条器械经血管插入肿瘤附近,并从血管内照射光的方法。
8.本发明是为了解决上述课题而完成的,其目的在于提供能够有效地对与宫颈癌的细胞膜结合的抗体-光敏物质照射近红外光的照射器械及治疗方法。
9.用于解决课题的手段
10.达成上述目的的本发明的治疗方法的一个方式为宫颈癌的治疗方法,其特征在于具有:将抗体-光吸收物质静脉给药的步骤;从上述静脉给药起经过12~36小时后,将具有第一光纤及位置确认标记的第一照射器械插入子宫动脉的步骤;利用上述位置确认标记确认上述第一照射器械的位置并使该第一照射器械朝目标位置前进的步骤;利用上述第一光纤向与该第一光纤大致垂直的方向照射近红外光的步骤;将上述第一照射器械拔出体外的步骤;将上述第一照射器械或作为其他照射器械的第二照射器械从阴道插入宫颈部的步骤;利用上述第二照射器械所具有的第二光纤向与该第二光纤大致垂直的方向进行照射的
步骤;将上述第二照射器械所具有的变形部的至少一部分拉出至宫颈外口,使上述变形部以追随器官的形状的方式膨胀的步骤;利用上述第二光纤向大致前端方向及/或与该第二光纤大致垂直的方向照射近红外光的步骤;使上述变形部收缩的步骤。
11.发明的效果
12.以上述方式构成的治疗方法将第一照射器械插入子宫动脉,从血管内向大致垂直方向照射近红外光,因此能够有效地对子宫动脉附近的癌细胞浸润的组织、器官照射近红外光。另外,本治疗方法将第二照射器械插入宫颈部并向大致垂直方向照射近红外光,因此能够有效地从宫颈部的内腔对宫颈部的癌细胞照射近红外光。进而,本治疗方法使从宫颈外口拉出的变形部膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地对宫颈阴道部附近的癌细胞照射近红外光。因此,本治疗方法能够有效地对与宫颈癌的细胞膜结合的抗体-光敏物质照射近红外光。
13.达成上述目的的本发明的治疗方法的另一个方式为宫颈癌的治疗方法,其也可具有:将抗体-光吸收物质静脉给药的步骤;从上述静脉给药起经过12~36小时后,将具有第一光纤及位置确认标记的第一照射器械插入子宫动脉的步骤;利用上述位置确认标记确认上述第一照射器械的位置并使该第一照射器械朝目标位置前进的步骤;利用上述第一光纤向与该第一光纤大致垂直的方向照射近红外光的步骤;将上述第一照射器械拔出体外的步骤;将上述第一照射器械或作为其他照射器械的第二照射器械从阴道插入宫颈部的步骤;使上述第二照射器械所具有的变形部以追随器官的形状的方式膨胀的步骤;利用上述第二光纤向大致前端方向及/或与该第二光纤大致垂直的方向照射近红外光的步骤;使上述变形部收缩的步骤。
14.以上述方式构成的治疗方法将第一照射器械插入子宫动脉,从血管内向大致垂直方向照射近红外光,因此能够有效地对子宫动脉附近的癌细胞浸润的组织、器官照射近红外光。另外,本治疗方法将第二照射器械插入宫颈部,使变形部膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地对宫颈部的大范围的宫颈癌照射近红外光。因此,本治疗方法能够有效地对与宫颈癌的细胞膜结合的抗体-光敏物质照射近红外光。
15.达成上述目的的本发明的治疗方法的又一个方式为宫颈癌的治疗方法,其也可具有:将抗体-光吸收物质静脉给药的步骤;从上述静脉给药起经过12~36小时后,将具有第二光纤的第二照射器械从阴道插入宫颈部的步骤;利用上述第二照射器械所具有的第二光纤向与该第二光纤大致垂直的方向进行照射的步骤;将上述第二照射器械所具有的变形部的至少一部分拉出至宫颈外口,以追随器官的形状的方式使上述变形部膨胀的步骤;利用上述第二光纤向大致前端方向及/或与该光纤大致垂直的方向照射近红外光的步骤;使上述变形部收缩的步骤。
16.以上述方式构成的治疗方法将第二照射器械插入宫颈部向大致垂直方向照射近红外光,因此能够有效地从宫颈部的内腔对宫颈部的癌细胞照射近红外光。进而,本治疗方法使从宫颈外口拉出的变形部膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地对宫颈阴道部附近的癌细胞照射近红外光。因此,本治疗方法能够有效地对宫颈部及自宫颈部向上下方向浸润的组织、器官的与癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
17.达成上述目的的本发明的治疗方法的又一个方式为宫颈癌的治疗方法,其也可具
有:将抗体-光吸收物质静脉给药的步骤;从上述静脉给药起经过12~36小时后,将具有第二光纤的第二照射器械从阴道插入宫颈部的步骤;使上述第二照射器械所具有的变形部以追随器官的形状的方式膨胀的步骤;利用上述第二光纤向大致前端方向及/或与该光纤大致垂直的方向照射近红外光的步骤;使上述变形部收缩的步骤。
18.以上述方式构成的治疗方法将第二照射器械插入宫颈管使变形部膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地对宫颈部的大范围的癌细胞照射近红外光。因此,本治疗方法能够有效地对宫颈部及自宫颈部向上下方向浸润的组织、器官的与癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
19.在本治疗方法的使上述变形部膨胀的步骤中,可以使上述变形部的一部分在较之宫颈外口而言靠基端侧以追随宫颈阴道部的形状的方式膨胀。由此,本治疗方法能够有效地对与包括宫颈阴道部的宫颈部及向宫颈部的下方浸润的组织、器官的癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
20.在本治疗方法的使上述变形部膨胀的步骤中,也可以使上述变形部的基端部在较之宫颈外口而言靠基端侧以追随宫颈阴道部的形状的方式膨胀,使上述变形部的前端部在较之宫颈内口而言靠前端侧以追随在宫腔的形状的方式膨胀。由此,本治疗方法能够有效地对与宫颈部及自宫颈部向上下方向浸润的组织、器官的癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
21.本治疗方法也可以在使上述变形部收缩的步骤之后,至少重复1次下述步骤:使上述第二照射器械旋转的步骤;使上述变形部以追随器官的形状的方式膨胀的步骤;利用上述第二光纤向前端方向及/或与第二光纤垂直的方向照射近红外光的步骤;使上述变形部收缩的步骤。由此,本治疗方法能够在宫颈部的圆周方向上以大范围照射近红外光。
22.上述第二照射器械与上述第一照射器械也可以为同一器械。由此,本治疗方法能够用1个照射器械进行从子宫动脉照射近红外光、和从宫颈部照射近红外光。因此,本治疗方法能够提高医疗经济性。
23.本治疗方法也可以在将上述第一照射器械拔出体外的步骤之后,清洗上述第一照射器械。由此,本治疗方法去除插入血管的第一照射器械上附着的血液,能够使第一照射器械成为对于从阴道插入宫颈部而言理想的状态。
24.本治疗方法也可以具有:在利用上述第一光纤照射近红外光的步骤之前,使上述第一照射器械所具有的变形部膨胀的步骤;在利用上述第一光纤照射近红外光的步骤之后,使上述第一照射器械所具有的变形部收缩的步骤。由此,从子宫动脉内的第一照射器械照射近红外光时,能够阻断子宫动脉内的血流。因此,能够降低血液对近红外光的影响,能够有效地对目标部位照射近红外光。
25.达成上述目的的本发明的照射器械为用于治疗宫颈癌的照射器械,其特征在于具有:长条的轴部、设置于上述轴部的前端部的可扩张的球囊、光纤、和设置于上述光纤的前端且配置于上述球囊的内部的可照射光的照射部,上述照射部可向与上述光纤的轴线大致垂直的方向及大致前端方向照射光。
26.上述照射部可以在上述球囊的收缩状态及扩张状态下照射光。
27.上述球囊的内部可以具有不透x射线的位置确认标记。
28.上述位置确认标记可以具有蓄光的结构、发出荧光的结构或透射光的结构。
附图说明
29.[图1]为示出第一实施方式的治疗方法中使用的照射器械的俯视图。
[0030]
[图2]为示出照射器械的前端部的剖面图。
[0031]
[图3]为示出第一实施方式的治疗方法中向子宫动脉插入照射器械时的体内的状态的概要图。
[0032]
[图4]为用于对利用插入子宫动脉的照射器械照射近红外光的状态进行说明的概要剖面图。
[0033]
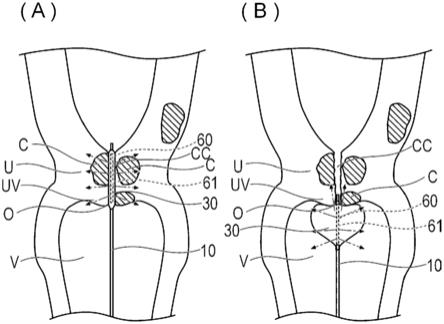
[图5]为示出从阴道插入宫颈部的照射器械的概要图,(a)示出从宫颈部照射近红外光的状态;(b)示出使拉出至宫颈外口的变形部变形而照射近红外光的状态。
[0034]
[图6]为示出第二实施方式的治疗方法中由从阴道插入宫颈部的照射器械照射近红外光的状态的概要图。
[0035]
[图7]为示出照射器械的第一变形例的俯视图,(a)示出使变形部变形前的状态;(b)示出使变形部变形后的状态。
[0036]
[图8]为示出照射器械的第二变形例的俯视图,(a)示出使变形部变形前的状态;(b)示出使变形部变形后的状态。
[0037]
[图9]为示出照射器械的第三变形例的俯视图,(a)示出使变形部变形前的状态;(b)示出使变形部变形后的状态。
具体实施方式
[0038]
以下,参照附图对本发明的实施方式进行说明。需要说明的是,为了便于说明,附图的尺寸有时被夸大而与实际尺寸不同。另外,本说明书及附图中,对于具有实质相同的功能构成的构成要素,通过添加相同的标记来省略重复说明。本说明书中,将器械的插入生物体管腔的一侧称为“前端侧”,将进行操作的一侧称为“基端侧”。
[0039]
<第一实施方式>
[0040]
第一实施方式的治疗方法为宫颈癌的治疗方法,其为涉及对与癌细胞的细胞膜结合的抗体-光敏物质照射近红外光来杀死癌细胞的光免疫疗法的治疗方法。该治疗方法使用使仅与位于癌细胞表面的特有抗原特异性结合的抗体、和与该抗体配对的光敏物质结合而成的抗体-光敏物质作为药剂。抗体没有特别限定,例如为帕尼单抗(日文:
パ
二
ツムバブ
;panitumumab)、曲妥单抗(trastuzumab)、huj591等。光敏物质例如为亲水性酞菁染料,其为与约700nm的波长的近红外光反应的物质(ir700),但并不限定于此。ir700接收到峰值在700nm附近的波长的近红外光时会吸收光,产生化学变化而在细胞膜上形成孔,由此能够杀死癌细胞。
[0041]
第一实施方式的治疗方法中,为了经血管及经阴道对与癌细胞结合的抗体-光敏物质照射近红外光,使用如图1所示的可插入血管及宫颈部的照射器械10。首先对照射器械10进行说明。
[0042]
如图1及图2所示,照射器械10具有长条的轴部20、设置于轴部20的前端部的作为变形部的球囊30、与轴部20的近处连接的毂部40、位置确认标记50、光纤60。照射器械10与光输出装置70连接来使用。
[0043]
轴部20具备前端及基端开口的作为管状体的外管21、配置于外管21内部的内管
22。外管21及内管22之间形成有供用于使球囊30扩张的扩张用流体流通的扩张管腔23,在内管22的内侧形成有可插入导丝80的导丝管腔24。
[0044]
球囊30的前端侧与内管22粘接,基端侧与外管21粘接,球囊30的内部与扩张管腔23连通。球囊30能够通过使流体流入内部而变形、膨胀。
[0045]
毂部40具备与外管21的扩张管腔23连通并作为供扩张用流体流入及流出的端口而发挥功能的第一开口部41、与导丝管腔24连通的第二开口部42、用于将光纤60连接于光输出装置70的连接电缆43。连接电缆43可相对于光输出装置70安装/脱离。
[0046]
球囊30优选利用具有一定程度挠性的材料而形成,作为这样的材料,例如能够使用聚乙烯、聚丙烯、聚丁烯、乙烯-丙烯共聚物、乙烯-乙酸乙烯酯共聚物、离聚物、或上述两种以上的混合物等的聚烯烃、软质聚氯乙烯树脂、聚酰胺、聚酰胺弹性体、聚酯、聚酯弹性体、聚氨酯、氟树脂等热塑性树脂、硅橡胶、乳胶橡胶等。
[0047]
光输出装置70能够对光纤60以任意剂量输出任意波长的近红外光。光输出装置70能够以例如660~740nm的波长、例如1~50jcm-2
的剂量照射光的方式对光纤60进行输出。
[0048]
光纤60在扩张管腔23内沿着内管22的外表面从毂部40延伸至球囊30。光纤60能够用1根纤维构成,也可以用成束的多根纤维构成。光纤60能够通过设置于毂部40的连接电缆43接收来自光输出装置70的近红外光。光纤60的前端设置有照射光的照射部61。
[0049]
照射部61将从光纤60的基端侧进入的光向外部照射。照射部61例如可利用透镜、漫射器、反射镜等而构成。照射部61可使用透镜、漫射器、反射镜等以能够向规定方向照射近红外光的方式适当设计。需要说明的是,只要能够向外部照射光,照射部61的结构没有限定。
[0050]
照射部61从球囊30的内部向包括与光纤60的轴线大致垂直的方向及大致前端方向(与光纤60的轴线平行的方向)这两个方向的范围照射近红外光。因此,可具有规定的照射角度而照射近红外光。或者,照射部61也可以仅向与光纤60的轴线大致垂直的方向或大致前端方向中的任意方向照射近红外光。
[0051]
位置确认标记50为用于供施术者确认体内的位置的部位。位置确认标记50配置于球囊30及照射部61的附近。位置确认标记50配置的位置、位置确认标记50的数目没有特别限定,例如位置确认标记50可配置于球囊30内部的内管22的外周面的两处。位置确认标记50例如也可以配置于外管21。位置确认标记50例如可利用不透x射线的材料而形成。不透x射线的材料例如为金、铂、钨等金属或包含上述金属的合金等金属材料。由此,施术者能够在体外的x射线造影下确认位置确认标记50的位置。需要说明的是,只要施术者能够确认在体内的位置,位置确认标记50也可以不是x射线造影性的标记。因此,位置确认标记50可用于插入宫颈部u的部位的位置确认。位置确认标记50在插入血管时作为能够通过x射线来确认位置的标记而发挥功能,也可在插入宫颈部u时作为能够用x射线、超声波等来确认位置的标记而发挥功能。位置确认标记50也可以为例如含可蓄光的材料的蓄光式标记。位置确认标记50能够放出事先储蓄的光。或者,位置确认标记50还可以为发出荧光的标记。发出荧光的荧光式标记可被来自光纤60及/或照射部61、或插入导丝管腔24的能够照射光的其他光纤等器械的照射光激发,发出不同波长的荧光。施术者能够介由仅透射特定波长的滤光片或能够截断照射光的波长的滤光片来观察其发光状态,从而进行治疗前的照射器械10的定位、用于治疗的照射中的照射器械10的位置确认。或者,位置确认标记50也可以为包含能
够透射来自轴部20内部的光那样的透明部位的透光式标记。此时,位置确认标记50可以以覆盖从轴部20的内周面贯穿至外周面的孔的方式配置,或者也可以配置于孔的内部。位置确认标记50能够使插入轴部20的导丝管腔24并能够照射光的其他光纤等器械放出的光透射,并向外部放射。施术者例如能够使用插入至阴道v的阴道镜等,观察蓄光式、荧光式或透光式的位置确认标记50放出的光。
[0052]
接着,对第一实施方式的治疗方法进行说明。
[0053]
首先,将抗体-光敏物质静脉给药。从静脉给药起经过约12~36小时后,如图3所示,施术者例如从股动脉将导丝80插入血管内。接着,将导丝80的基端插入照射器械10的导丝管腔24,使照射器械10沿着导丝80经髂内动脉到达子宫动脉ua。接着,施术者在x射线造影下确认位置确认标记50的位置并将照射器械10的前端部(特别是照射部61)从宫颈部u移动至癌细胞c浸润的组织、器官附近。形成有癌细胞c的组织、器官为宫颈部、子宫旁组织、骨盆、膀胱壁及直肠粘膜等。施术者将照射器械10的前端部配置于可向癌细胞c浸润的组织、器官照射近红外光的位置。
[0054]
接着,如图4所示,由光纤60照射近红外光。从静脉给药起经过12~36小时后开始近红外光的照射。来自光纤60的近红外光的照射方向包括与光纤60的轴线垂直的方向。因此,光纤60能够有效地从血管内对血管外的部位照射近红外光。需要说明的是,光纤60也可以向前端方向照射近红外光。施术者能够根据癌细胞c相对于插入照射器械10的血管的位置而适当选择所使用的光纤60。
[0055]
施术者也可在由光纤60照射近红外光之前,从照射器械10的基端侧向导丝管腔24供给生理盐水。由此,生理盐水从照射器械10被注入子宫动脉ua(冲洗)。其结果,照射器械10的前端部所在的血管内的血液被冲走,能够使近红外光的照射不易被血液影响。另外,施术者也可在由光纤60照射近红外光之前,从扩张管腔23向球囊30内供给扩张用流体,使球囊30膨胀。球囊30密合于血管壁而阻断血流。由此,球囊30与血管壁之间不存在血液,因此能够使近红外光的照射不易被血液影响。施术者在使球囊30膨胀的情况下,在完成近红外光的照射之后,从球囊30排出扩张用流体而使球囊30收缩。
[0056]
照射近红外光时,近红外光到达与癌细胞c的细胞膜结合的抗体-光敏物质。由此,发生光敏物质的化学变化,进而引起抗体-光敏物质的结构变化,从而能够在细胞膜上形成孔,杀死癌细胞c。
[0057]
施术者在判断已充分杀死癌细胞c时、判断不期望进一步照射时、或经过了规定时间时,停止近红外光的照射。
[0058]
接着,施术者将照射器械10拔出体外。接着,施术者清洗照射器械10。由此,从照射器械10上去除血液。需要说明的是,优选插入照射器械10的血管未被癌细胞c浸润。由此,照射器械10没有附着癌细胞c,能够在后续的阴道的治疗中使用同一照射器械10。
[0059]
接着,施术者确定进行了近红外线照射的癌细胞c的位置,并记录。期望将癌细胞c的位置以与预先获得的患者的ct图像、mri图像等数据的位置信息相对应的方式记录成电子数据。由此,能够使后续的操作顺利地进行,有效地进行术后的随访。例如,在对多个癌细胞c进行近红外线的照射等的情况下,能够正确地掌握已完成近红外线的照射的肿瘤c,从而能够顺利且可靠地进行对所有癌细胞c的照射。需要说明的是,在之后的近红外线的照射中也可适当进行确定癌细胞c的位置并记录。
[0060]
接着,如图5的(a)所示,施术者将从血管拉出并清洗的照射器械10从阴道v通过宫颈外口o插入宫颈部u的宫颈管cc。由此,球囊30位于宫颈管cc。接着,施术者由光纤60照射近红外光。来自光纤60的近红外光的照射方向包括与光纤60的轴线大致垂直的方向。因此,光纤60能够有效地从宫颈管cc向位于宫颈部u的癌细胞c照射近红外光。需要说明的是,光纤60也可以向前端方向照射近红外光。需要说明的是,施术者也可以将与从血管拉出并清洗的照射器械10不同的照射器械10从阴道v插入宫颈管cc。从宫颈管cc照射近红外光时,由于宫颈管cc狭窄,因此照射器械10的前端部密合于宫颈部u。因此,不需要使球囊30膨胀。需要说明的是,也可以在宫颈部u的内腔使球囊30膨胀。
[0061]
照射近红外光时,近红外光到达与宫颈部u的癌细胞c的细胞膜结合的抗体-光敏物质。由此,发生光敏物质的化学变化,进而引起抗体-光敏物质的结构变化,从而在细胞膜上形成孔,照射了红外光的宫颈部u的癌细胞c被杀死。
[0062]
施术者在判断已充分杀死癌细胞c时、判断不期望进一步照射时、或经过了规定时间时,停止近红外光的照射。
[0063]
接着,施术者牵拉照射器械10,将球囊30及照射部61的至少一部分(或全部)从宫颈外口o拉出。然后,从扩张管腔23向球囊30内供给扩张用流体,如图5的(b)所示,使球囊30膨胀。接着,施术者递送照射器械10,使膨胀的球囊30的前端部抵靠于宫颈阴道部uv。宫颈阴道部uv为宫颈部u的阴道v侧的部位,形成有宫颈外口o。因此,球囊30密合于宫颈阴道部uv的宫颈外口o附近,以追随宫颈阴道部uv(器官)的形状的方式膨胀。需要说明的是,当球囊30的一部分位于宫颈管cc时,即使施术者不递送照射器械10,也能够保持球囊30密合于宫颈阴道部uv的宫颈外口o附近的状态。
[0064]
接着,施术者由光纤60照射近红外光。来自光纤60的近红外光的照射方向包括大致前端方向及/或与光纤60的轴线大致垂直的方向。由光纤60向前端方向照射的近红外光能够有效地到达位于宫颈阴道部uv的癌细胞c。由光纤60向与光纤60的轴线垂直的方向照射的近红外光也能够从与图5的(a)中的照射不同的方向到达远离宫颈阴道部uv的宫颈外口o的部位的癌细胞c,能够有效地到达位于阴道v的癌细胞c。因此,光纤60能够有效地向位于宫颈阴道部uv、阴道v的癌细胞c照射近红外光。
[0065]
施术者在判断已充分杀死癌细胞c时、判断不期望进一步照射时、或经过了规定时间时,停止近红外光的照射。接着,施术者从球囊30排出扩张用流体而使球囊30收缩。
[0066]
接着,施术者以照射器械10的轴心为中心使照射器械10旋转规定角度。旋转的角度没有特别限定,例如为90
°
~180
°
。并且,施术者与上述同样地再次使球囊30膨胀,使球囊30密合于宫颈阴道部uv的宫颈外口o附近。球囊30以追随宫颈阴道部uv(器官)的形状的方式膨胀。然后,施术者由光纤60照射近红外光。由此,通过在与旋转前不同的部位照射近红外光,能够向宫颈阴道部uv、阴道v的不同位置的癌细胞c照射近红外光。然后,施术者停止近红外光的照射。能够重复进行1次以上的组合了照射器械10的旋转、球囊30的膨胀、近红外光的照射、照射的停止及球囊30的收缩的一系列工序。需要说明的是,该一系列工序也可一次也不进行。然后,施术者将照射器械10拔出体外。由此,完成本治疗方法。
[0067]
施术者在操作时,也能够利用x射线、超声波确认位置确认标记50的位置,且将照射器械10定位于宫颈部u的目标位置。位置确认标记50为蓄光式或透光式标记时,施术者能够介由阴道镜等从阴道v侧观察位置确认标记50放出的光,且将照射器械10从阴道部v插入
宫颈部u。并且,施术者通过无法观察到光来掌握照射器械10的设置有位置确认标记50的部位从阴道v已插入宫颈部u的宫颈管cc。因此,位置确认标记50能够作为用于正确地定位照射器械10以成为照射器械10的一部分已插入宫颈管cc的状态的定位机构而发挥功能。
[0068]
施术者还能够介由阴道镜等从阴道v侧观察位置确认标记50放出的光,且将插入宫颈部u的照射器械10从宫颈部u向阴道v侧拉出。并且,施术者通过能够观察到光来掌握照射器械10的设置有位置确认标记50的部位从宫颈部u已被拉出至阴道部v。因此,位置确认标记50能够作为用于正确地定位照射器械10以成为照射器械10的一部分已插入宫颈管cc的状态的定位机构而发挥功能。施术者重复进行插入宫颈部u及从宫颈部u拉出时,能够在各个动作中,从阴道v侧观察位置确认标记50放出的光,正确地定位照射器械10。
[0069]
如上所述,第一实施方式的治疗方法为宫颈癌的治疗方法,其具有:将抗体-光吸收物质静脉给药的步骤;从静脉给药起经过12~36小时后,将具有第一光纤60及位置确认标记50的第一照射器械10插入子宫动脉ua的步骤;利用位置确认标记50确认第一照射器械10的位置并使该照射器械10朝目标位置前进的步骤;利用第一光纤60向与该第一光纤60大致垂直的方向照射近红外光的步骤;将第一照射器械10拔出体外的步骤;将第一照射器械10或作为其他照射器械10的第二照射器械10从阴道v插入宫颈部u的步骤;利用第二照射器械10所具有的第二光纤60向与该第二光纤60大致垂直的方向进行照射的步骤;将第二照射器械10所具有的变形部的至少一部分拉出至宫颈外口o,使作为变形部的球囊30以追随器官的形状的方式膨胀的步骤;利用第二光纤60向大致前端方向及/或与该光纤60大致垂直的方向照射近红外光的步骤;使球囊30收缩的步骤。
[0070]
以上述方式构成的治疗方法将第一照射器械10插入子宫动脉ua,从血管内向大致垂直方向照射近红外光,因此能够有效地对子宫动脉ua附近的癌细胞c浸润的组织、器官照射近红外光。另外,本治疗方法由于将第二照射器械10插入狭窄的宫颈管cc,向大致垂直方向照射近红外光,因此能够有效地从宫颈部u的宫颈管cc向宫颈部u的癌细胞c照射近红外光。进而,本治疗方法使从宫颈外口o拉出的作为变形部的球囊30膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地向宫颈阴道部uv附近的宫颈癌照射近红外光。因此,本治疗方法能够有效地向与宫颈部u的癌细胞c及自宫颈部u浸润的组织、器官的癌细胞c的细胞膜结合的抗体-光敏物质照射近红外光。本治疗方法不仅是在癌细胞c局限于宫颈部的早期阶段,而且在癌细胞c浸润至子宫旁组织的iib期、阴道壁浸润到达阴道的下3分之1的iiia期、向子宫旁组织的浸润到达骨盆壁的iiib期、癌细胞c浸润至膀胱、直肠粘膜的iva期中也是有效的。
[0071]
另外,本治疗方法在使作为变形部的球囊30收缩的步骤之后,也可以至少重复1次下述步骤:使第二照射器械10旋转的步骤;使球囊30以追随器官的形状的方式膨胀的步骤;利用第二光纤60向大致前端方向及/或与第二光纤60大致垂直的方向照射近红外光的步骤;使球囊30收缩的步骤。由此,本治疗方法能够在宫颈部u的圆周方向上以大范围照射近红外光。另外,本治疗方法能够在阴道v的圆周方向上以大范围照射近红外光。
[0072]
另外,第二照射器械10与第一照射器械10相同。由此,本治疗方法能够以1个照射器械10进行从子宫动脉ua照射近红外光、和从宫颈部u照射近红外光。因此,本治疗方法能够提高医疗经济性。需要说明的是,第二照射器械10与第一照射器械10也可以不为同一器械。
[0073]
另外,本治疗方法在将第一照射器械10拔出体外的步骤之后,清洗第一照射器械10。由此,本治疗方法去除插入血管的第一照射器械10上附着的血液,能够使第一照射器械10成为对于从阴道v插入宫颈部u而言理想的状态。
[0074]
另外,本治疗方法也可以具有:在利用第一光纤60照射近红外光的步骤之前,使第一照射器械10所具有的球囊30膨胀的步骤;在利用第一光纤60照射近红外光的步骤之后,使第一照射器械10所具有的球囊30收缩的步骤。由此,由子宫动脉ua内的第一照射器械10照射近红外光时,能够阻断子宫动脉ua内的血流。因此,能够降低血液对近红外光的影响,能够有效地对目标部位照射近红外光。
[0075]
另外,第一实施方式中,治疗器械也可以不插入血管。即,第一实施方式的治疗方法的变形例为宫颈癌的治疗方法,将抗体-光吸收物质静脉给药的步骤;从静脉给药起经过12~36小时后,将具有第二光纤60的第二照射器械10从阴道v插入宫颈部u的步骤;利用第二照射器械10所具有的第二光纤60向与该第二光纤60大致垂直的方向进行照射的步骤;将第二照射器械10所具有的球囊30的至少一部分拉出至宫颈外口o,使球囊30以追随器官的形状的方式膨胀的步骤;利用第二光纤60向大致前端方向及/或与该第二光纤60大致垂直的方向照射近红外光的步骤;使球囊30收缩的步骤。
[0076]
以上述方式构成的治疗方法将照射器械10插入细小的宫颈部u,使球囊30膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地向宫颈部u的大范围的宫颈癌照射近红外光。因此,本治疗方法能够有效地向与宫颈部u的癌细胞c的细胞膜结合的抗体-光敏物质照射近红外光。本治疗方法不仅在癌细胞c局限于宫颈部的早期阶段,而且在癌细胞c浸润至阴道壁的iia期阶段及iiia期阶段中也是有效的。
[0077]
<第二实施方式>
[0078]
第二实施方式的治疗方法为将照射器械10从阴道v插入宫颈部u而进行的方法,与第一实施方式的治疗方法不同。需要说明的是,所使用的照射器械10与第一实施方式的治疗方法中使用的照射器械10相同。
[0079]
第二实施方式的治疗方法中,施术者与第一实施方式同样地将照射器械10插入子宫动脉ua,从子宫动脉ua内向癌细胞c浸润的组织、器官照射近红外光。
[0080]
施术者将照射器械10从血管拉出体外并清洗之后,如图6所示,从阴道v通过宫颈外口o插入宫颈管cc。由此,球囊30的前端部配置于较之宫颈内口i靠前端侧的宫腔uc,球囊30的基端部配置于较之宫颈外口o靠基端侧的阴道v。因此,球囊30贯穿宫颈管cc。接着,施术者由光纤60照射近红外光。由此,配置于宫颈管cc的光纤60能够有效地向位于宫颈部u的癌细胞c照射近红外光。另外,配置于宫腔uc内的光纤60的前端部能够有效地向位于宫腔uc、宫腔uc附近的宫颈部u的癌细胞c照射近红外光。另外,配置于阴道v内的光纤60的基端部能够有效地向位于宫颈阴道部uv、阴道v的癌细胞c照射近红外光。
[0081]
如上所述,第二实施方式的治疗方法为宫颈癌的治疗方法,其具有:将抗体-光吸收物质静脉给药的步骤;从静脉给药起经过12~36小时后,将具有第一光纤60及位置确认标记50的第一照射器械10插入子宫动脉ua的步骤;利用位置确认标记50确认第一照射器械10的位置并使该照射器械10朝目标位置前进的步骤;利用第一光纤60向与该第一光纤60大致垂直的方向照射近红外光的步骤;将第一照射器械10拔出体外的步骤;将第一照射器械10或作为其他照射器械10的第二照射器械10从阴道v插入宫颈部u的步骤;使第二照射器械
10所具有的球囊30以追随器官的形状的方式膨胀的步骤;利用第二光纤60向大致前端方向及/或与该第二光纤60大致垂直的方向照射近红外光的步骤;使球囊30收缩的步骤。
[0082]
以上述方式构成的治疗方法将第一照射器械10插入子宫动脉ua,从血管内向大致垂直方向照射近红外光,因此能够有效地对子宫动脉ua附近的癌细胞c浸润的组织、器官照射近红外光。另外,本治疗方法将第二将照射器械10插入细小的宫颈部u,使球囊30膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地向宫颈部u的大范围的宫颈癌照射近红外光。因此,本治疗方法能够有效地向与宫颈部u及浸润的骨盆壁等这两部位的癌细胞c的细胞膜结合的抗体-光敏物质照射近红外光。本治疗方法不仅是在癌细胞c局限于宫颈部的早期阶段,而且在癌细胞c浸润至子宫旁组织的iib期、阴道壁浸润到达阴道的下3分之1的iiia期、向子宫旁组织的浸润到达骨盆壁的iiib期、癌细胞c浸润至膀胱、直肠粘膜的iva期中也是有效的。
[0083]
另外,第二实施方式中,治疗器械也可以不插入血管。即,第二实施方式的治疗方法的变形例为宫颈癌的治疗方法,其具有:将抗体-光吸收物质静脉给药的步骤;从静脉给药起经过12~36小时后,将具有第二光纤60的照射器械10从阴道v插入宫颈部u的步骤;使照射器械10所具有的球囊30以追随器官的形状的方式膨胀的步骤;利用光纤60向大致前端方向及/或与该光纤60大致垂直的方向照射近红外光的步骤;使球囊30收缩的步骤。
[0084]
以上述方式构成的治疗方法将照射器械10插入细小的宫颈部u,使球囊30膨胀,向前端方向及/或垂直方向照射近红外光,因此能够有效地向宫颈部u的大范围的宫颈癌照射近红外光。因此,本治疗方法能够有效地向与宫颈部u的癌细胞c的细胞膜结合的抗体-光敏物质照射近红外光。本治疗方法不仅是在癌细胞c局限于宫颈部的早期阶段,而且在癌细胞c浸润至阴道壁的iia期阶段及iiia期阶段中也是有效的。
[0085]
另外,在本治疗方法的使作为变形部的球囊30膨胀的步骤中,也可以使球囊30的一部分在较之宫颈外口o靠基端侧以追随宫颈阴道部uv的形状的方式膨胀。球囊30的前端部可以位于宫颈部u,也可以位于宫腔uc。由此,本治疗方法能够有效地对与包括宫颈阴道部uv的宫颈部u及向宫颈部u的下方浸润的组织、器官的癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
[0086]
另外,在本治疗方法的使作为变形部的球囊30膨胀的步骤中,也可以使球囊30的基端部在较之宫颈外口o靠基端侧以追随宫颈阴道部uv的形状的方式膨胀,使球囊30的前端部在较之宫颈内口i靠前端侧以追随宫腔uc的形状的方式膨胀。由此,本治疗方法能够有效地对与宫颈部u及自宫颈部u向上下方向浸润的组织、器官的癌细胞的细胞膜结合的抗体-光敏物质照射近红外光。
[0087]
需要说明的是,本发明并不仅限于上述的实施方式,本领域技术人员可在本发明的技术构思内进行各种变更。例如,如图7的(a)所示的照射器械10的第一变形例那样,光纤60的照射部61也可以配置于球囊30的外表面侧,而非球囊30之中。光纤60可以为1个,也可以为2个以上。由此,能够缩短从照射部61至癌细胞c的距离,因此能够降低光能的损耗,使近红外光有效地到达癌细胞c。需要说明的是,光纤60与球囊30不同,不具有伸缩性。因此如图7的(b)所示,优选以能够追随伸缩的球囊30而变形的方式将光纤60设置成例如蜿蜒、或螺旋状。
[0088]
另外,例如如图8的(a)所示的照射器械10的第二变形例那样,变形部也可以为至
少1根的线材31,而非球囊30。线材31的前端部固定于内管22,线材31的基端部固定于外管21,需要说明的是,第二变形例中,内管22与外管21在轴向上可相对移动。因此,通过使内管22的前端与外管21的前端在轴向上靠近,各个线材31受到压缩力,如图8的(b)所示,可以以向径向的外侧凸出的方式变形。并且,各个线材31的外表面上配置有光纤60的照射部61。因此,能够缩短从照射部61至癌细胞c的距离,因此能够降低光能的损耗,使近红外光有效地到达癌细胞c。
[0089]
另外,例如,如图9的(a)所示的照射器械10的第三变形例那样,变形部为球囊30,光纤60也可具有配置于球囊30内部的内侧光纤62、和配置于球囊30外表面的外侧光纤63。内侧光纤62例如向大致前端方向照射近红外光。外侧光纤63向包括与外侧光纤63的轴线垂直的方向及前端方向的范围照射近红外光。由此,能够缩短从外侧光纤63的照射部61至癌细胞c的距离,因此能够降低光能的损耗,使近红外光有效地到达癌细胞c。另外,能够通过内侧光纤62有效地向前端方向照射。需要说明的是,外侧光纤63与球囊30不同,不具有伸缩性。因此如图9的(b)所示,优选以能够追随伸缩的球囊30而变形的方式将外侧光纤63设置成例如蜿蜒、或螺旋状。
[0090]
需要说明的是,本技术以2019年9月30日于日本提出申请的日本特愿申请2019-180489号为基础,参考其公开内容并将其整体并入本技术。
[0091]
附图说明
[0092]
10:照射器械;30:球囊(变形部);31:线材(变形部);50:位置确认标记;60:光纤;61:照射部;62:内侧光纤;63:外侧光纤;c:癌细胞;cc:宫颈管;i:宫颈内口;o:宫颈外口;ua:子宫动脉;u:宫颈部;uc:宫腔;uv:宫颈阴道部;v:阴道。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
