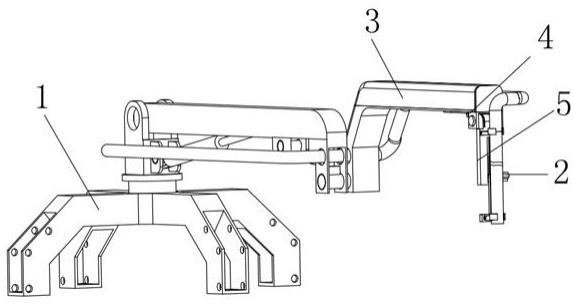
1.本发明属于生物医学领域,具体涉及一种二次纳米化的白蛋白紫杉醇药物及其应用。
背景技术:
2.上世纪60年代,美国科学家在太平洋紫杉树的树皮中发现了抗癌活性成分:紫杉醇。紫杉醇于1992年获批用于卵巢癌治疗。然而单靠从紫杉树中提取获得紫杉醇远不足以满足临床众多患者的需求,科学家们就继续开展研究,并从欧洲紫杉中发现了丰富的半成品,用它来半合成紫杉醇,解决了紫杉醇的供应问题。然而,紫杉醇只有依靠聚氧乙烯蓖麻油溶解才能保证一定的溶解性和稳定性,但在20%~40%的患者中,注射该溶剂会导致严重的过敏反应。
3.新一代紫杉类药物是纳米微粒白蛋白结合型紫杉醇nab-paclitaxel,采用最新白蛋白结合纳米微粒技术,去除了有毒溶剂,不仅解决了过敏问题,还提高了治疗效果。体外研究表明,白蛋白结合型紫杉醇在肿瘤组织内浓度为普通溶剂型紫杉醇的1.33倍,而在正常组织中药物浓度是普通型的1/2。现阶段指南均推荐白蛋白结合紫杉醇单药用于转移性乳腺癌、胰腺癌等实体肿瘤。
4.鉴于白蛋白结合型紫杉醇良好的可溶性,临床治疗中通常会通过提高药物使用剂量以取得更好的疗效。但高剂量的白蛋白结合型紫杉醇也诱发了明显的毒副反应,如骨髓抑制,脱发和周围神经毒性等。因此针对当前白蛋白结合型紫杉醇在临床应用过程中存在的问题,保持疗效的同时减少其毒副反应是一个非常值得的研究方向。
技术实现要素:
5.本发明为减少白蛋白紫杉醇在治疗中的毒副作用,对白蛋白紫杉醇的纳米颗粒进行二次纳米包装,得到的二次纳米化的白蛋白紫杉醇避免了骨髓抑制、血细胞生成受限的问题,结合放射治疗,表现出非常好的抗肿瘤效果,肺癌实验表明效果成倍增加。
6.制备方法
7.一方面,本发明提供了一种低毒副作用的药物的制备方法,所述方法包括对活性成分进行两次纳米化处理、或对纳米药物再次进行纳米化处理。
8.优选地,所述纳米化处理包括任何纳米颗粒的制备方法。具体地,例如:反溶剂法、乳化法、热凝胶法、白蛋白纳米结合技术、自组装技术、纳米喷雾干燥技术。
9.优选地,所述两次纳米化处理可以选用相同或不相同的纳米颗粒制备方法。
10.优选地,纳米化处理选用反溶剂法,所述反溶剂法的步骤包括:血清白蛋白(hsa)与活性成分或纳米药物混合,缓慢滴加乙醇或丙酮,最后加入交联剂,获得纳米颗粒。
11.优选地,所述反溶剂法的步骤包括以下步骤:
12.1)混合hsa 活性成分或纳米药物;优选地,大转速搅拌所述混合溶液;优选地,大转速指1000rpm;
13.2)向1)的溶液中加入乙醇或丙酮,继续搅拌;优选地,搅拌至少5分钟(具体包括5、6、7、8、9、10、11、12、13、14、15分钟);更优选地,搅拌10分钟;
14.3)向2)的溶液中加入交联剂;优选地,搅拌均匀后在25℃以上环境中孵育,至少孵育1小时(具体包括1、2、3、4、5、6、7、8、9、10小时);更优选地,孵育4小时。
15.优选地,所述交联剂包括甲醛、戊二醛;
16.优选地,所述交联剂是戊二醛;更优选地,是8%的戊二醛。
17.优选地,所述乙醇或丙酮是缓慢滴入的;更优选地,所述乙醇或丙酮的滴加速率是1ml/min;
18.优选地,所述操作步骤还包括取纳米溶液离心重悬的步骤。具体地,所述离心重悬的步骤是:12000rpm离心后,弃去上清,晾干后用灭菌水重悬。优选地,还需要经过0.22nm滤过膜过滤。
19.二次纳米化药物
20.另一方面,本发明提供了一种二次纳米化的药物,所述二次纳米化的药物是对活性成分进行两次纳米化处理、或对纳米药物再次进行纳米化处理所制备得到的药物。也就是说,本发明提供了前述制备方法所制备得到产品。
21.本发明中适宜的“活性成分”,示例性的包括5-氨基水杨酸(salicylica cid)、阿巴卡韦(abacayir)、阿巴瑞克(abarelix)、阿巴西普(abatacept)、阿坎酸(acamprosate)、阿卡波糖(acarbose)、醋氯芬酸(aceclofenac)、乙酰水杨酸、阿维a(acitretin)、阿柔比星(aclarubicin)、放线菌素(actinomycin)、阿昔洛韦(acyclovir)、阿达木单抗(adalimumab)、阿德福韦(adefovir)、阿德福韦二匹伏酯(adefovir dipivoxil)、腺苷、腺苷甲硫氨酸(adenosyl methionine)、肾上腺素、阿霉素(adriacin)。
22.优选地,所述活性成分是抗癌活性成分。
23.优选地,所述抗癌活性成分包括但不限于任何植物来源的具有抗癌活性的成分,包括来源于植物的活性成分,具体地,包括sulphoraphane、紫杉醇(paclitaxel,taxol)、epipodophyllotoxin、长春新碱(vincristine)、长春花碱(vinblastine)、长春瑞滨(vinorelbine)、长春地辛(vindesine)、长春花碱(vinflunine)、蒜黄素(pomiferin)、epigallacotechin-3-gallate、combretastatin a-4phosphate、罗斯科维汀(roscovitine)、黄吡利多(flavopiridol)、诺卡品(noscapine)、formononetin、cabazitaxel、秋水仙碱(colchicine)、combretastatin、多西紫杉醇(docetaxol)、异甘草素(isoliquiritigenin)、larotaxel、podophyllotoxin、resveratrol、2s-abyssinone ii、verubulin。
24.优选地,所述抗癌活性成分是紫杉醇。
25.优选地,所述纳米药物包括但不限于白蛋白结合的紫杉醇(例如专利wo2014105644和wo2008057562中所述)和脂质体柔红霉素(例如专利ep0004467和us20070286897中所述)。
26.优选地,所述纳米药物是白蛋白结合(型)的紫杉醇(在本发明也简称为“白蛋白紫杉醇”)。
27.优选地,本发明所提供的二次纳米化药物的粒径的范围是50-150nm;优选地,约100nm。
28.细胞
29.另一方面,本发明提供了包含前述制备方法制得的药物或前述二次纳米化药物的细胞。
30.优选地,所述细胞包括动物细胞;
31.优选地,所述细胞是人源细胞;
32.更优选地,所述细胞是中性粒细胞。
33.药物组合物
34.另一方面,本发明提供了包含前述制备方法制得的药物或前述二次纳米化药物的药物组合物。
35.优选地,所述药物组合物还包括能够作为多颗粒剂型、包含丸粒的片剂、微片剂、胶囊、囊剂、泡腾片剂或用于口服悬浮液的干粉剂的成分的任何活性药用物质;
36.本发明化合物的药物组合物可采用下面的任意方式施用:口服、喷雾吸入、直肠用药、鼻腔用药、颊部用药、局部用药、非肠道用药,如皮下、静脉、肌内、腹膜内、鞘内、心内室、胸骨内或静脉内给药方式。
37.优选地,所述药物组合物还包括药学上可接受的载体、稀释剂或赋形剂。
38.优选地,所述药学上可接受的载体、稀释剂或赋形剂包括但不限于已经由美国食品和药品管理局或中国食品药品监督管理局批准可用于人或家畜的任何佐剂、载体、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增味剂、表面活性剂、润湿剂、分散剂、悬浮剂、稳定剂、等渗剂、溶剂、表面活性剂或乳化剂。
39.优选地,所述药物组合物可以为片剂,丸剂,粉剂,颗粒剂,胶囊剂,锭剂,糖浆剂,液体,乳剂,混悬剂,控制释放制剂,气雾剂,膜剂,注射剂,静脉滴注剂,透皮吸收制剂,软膏剂,洗剂,粘附制剂,栓剂,小药丸,鼻制剂,肺制剂,眼睛滴剂等等,口服或胃肠外制剂。
40.系统
41.另一方面,本发明提供了一种放化疗结合的癌症治疗系统,所述系统至少包括以下两个模块:
42.1)进行放疗的放疗模块,具体地,所述放疗模块包括进行放射治疗的仪器或试剂;
43.2)向患者施用前述制备方法制得的药物或前述二次纳米化药物的化疗模块,优选地,所述化疗模块还可以包括施用药物所需要的其他仪器装置。
44.优选地,所述放疗模块和化疗模块反复交替施用;
45.优选地,所述化疗模块施用前1-3天施用放疗模块;一次放疗 一次化疗可以称为一个疗程,对于一位患者可以进行多个疗程的治疗;具体地,可以是:第一次使用放疗模块(简称“第一次放疗”)-第一次使用化疗模块(简称“第一次化疗”)-第二次使用放疗模块(简称“第二次放疗”)-第二次使用化疗模块(简称“第二次化疗”);
46.本发明所述“放疗”“放射治疗”是相同含义,可以互相替换。放射治疗是三种癌症核心疗法中的一种。研究人员发现靶向肿瘤的放射治疗能够作为“癌症疫苗”引起中性粒细胞介导的肿瘤细胞死亡,激发免疫系统对抗其他转移灶的癌细胞。
47.本发明所述“化疗”“化学药物治疗”是相同含义,可以互相替换。具体地,本发明所使用的化学药物是前述制备方法制得的药物或前述二次纳米化的药物。
48.应用
49.另一方面,本发明提供了前述制备方法制得的产品、二次纳米化的药物、细胞、药物组合物、在制备治疗癌症的药物中的用途。
50.优选地,所述治疗癌症的药物包括伴随放射治疗时使用的药物。
51.优选地,所述放射包括电离辐射、粒子束辐射。
52.优选地,所述粒子束包括电子、质子、中子、重离子例如碳离子或介子。
53.优选地,所述电离辐射包括x射线辐射、紫外线辐射、红外线辐射、γ射线辐射或微波辐射。
54.另一方面,本发明提供了前述癌症治疗系统在制备治疗癌症的产品中的应用。
55.优选地,所述癌症包括:宫颈癌、精原细胞瘤、睾丸淋巴瘤、前列腺癌、卵巢癌、肺癌、直肠癌、乳腺癌、皮肤鳞状细胞癌、结肠癌、肝癌、胰腺癌、胃癌、食管癌、甲状腺癌、膀胱移行上皮癌、白血病、脑瘤、胃癌、腹膜癌、头颈癌、子宫内膜癌、肾癌、雌性生殖道癌、原位癌、神经纤维瘤、骨癌、皮肤癌、胃肠道间质瘤、肥大细胞肿瘤、多发性骨髓瘤、黑色素瘤、胶质瘤和肉瘤。
56.优选地,所述癌症包括可以使用紫杉醇治疗的任何癌症。具体地,包括卵巢癌、乳腺癌、肺癌、食道癌、胃癌、非霍奇金氏淋巴瘤、大肠癌、黑色素瘤、头颈部癌、淋巴瘤、脑瘤也都有一定疗效。
57.优选地,所述癌症是肺癌。
58.优选地,所述治疗癌症是针对llc肺癌细胞构建的模式生物。
59.优选地,所述模式生物是小鼠。
60.治疗方法
61.另一方面,本发明提供了一种治疗癌症的方法,所述方法包括给患者施用前述二次纳米化药物、制备方法制得的产、细胞、药物组合物任意一种。
62.优选地,所述方法还包括对患者进行放射治疗。
附图说明
63.图1是二次纳米化白蛋白紫杉醇的粒径测量结果,图1a是检测结果图,图1b是数据统计图。
64.图2是二次纳米化白蛋白紫杉醇的电位测量结果,图2a是检测结果图,图2b是数据统计图。
65.图3是二次纳米化白蛋白紫杉醇的稳定性检测结果。
66.图4是二次纳米化白蛋白紫杉醇的粒径稳定性检测结果。
67.图5是二次纳米化白蛋白紫杉醇在电镜下的形态图。
68.图6是放疗刺激下中性粒细胞载药情况检测结果图。
69.图7是pma刺激下中性粒细胞载药情况检测结果图,图7a是流式细胞仪结果图,图1b是显微镜下结果图。
70.图8是趋化实验结果图,图8a是检测结果图,图8b是数据统计图。
71.图9是ros检测结果图,图9a是检测结果图,图9b是数据统计图。
72.图10是il-1β、il-6表达量的检测结果统计图,图10a是il-6β,图10b是il-6。
73.图11是小鼠实验的流程图。
74.图12是肿瘤实体图。
75.图13是肿瘤体积和肿瘤重量变化的统计图,图13a是体积,图13b是重量。
76.图14是小鼠体重变化的统计图。
77.图15是瘤内载药中性粒细胞细胞百分比,图15a是流式检测结果图,图15b是统计结果图。
78.图16是心肝脾肺肾he染色结果图,图16a:心,图16b:肺,图16c:肝,
79.图16d:脾,图16e:肾。
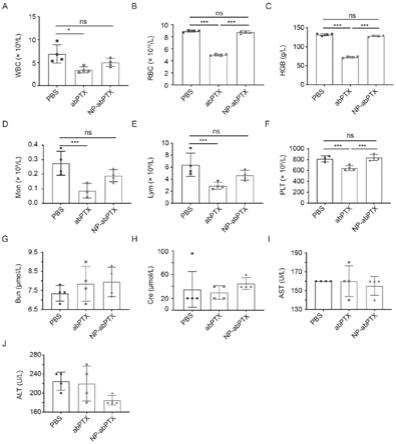
80.图17是血常规和肝肾功能检测结果图。
具体实施方式
81.下面结合实施例对本发明做进一步的说明,以下所述,仅是对本发明的较佳实施例而已,并非对本发明做其他形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更为同等变化的等效实施例。凡是未脱离本发明方案内容,依据本发明的技术实质对以下实施例所做的任何简单修改或等同变化,均落在本发明的保护范围内。
82.实施例1、制备二次纳米化白蛋白紫杉醇
83.制备方法:
84.1、取1ml浓度为20mg/ml的白蛋白结合型紫杉醇溶液(商品名:艾越;江苏恒瑞医药股份有限公司),置入含有搅拌转子的50ml锥形瓶,随后缓慢调大转速(1000rpm)进行搅拌;
85.2、向锥形瓶中缓慢滴加3.45ml无水乙醇,滴入速度为1ml/min,并采用保鲜膜封住锥形瓶口,室温搅拌10min;
86.3、最后加入20μl的8%戊二醛,搅拌均匀后将溶液转移至15ml离心管,室温(》25℃)孵育4小时;
87.4、取上述纳米溶液500μl,分装入1.5ml ep管中,12000rpm离心15min,弃上清,随后室温晾干;
88.5、加1ml灭菌水重悬沉淀,0.22nm滤过膜过滤后4℃避光保存。
89.特性验证
90.电镜下扫描制备得到的产品,并且测量产品的粒径、电位、稳定性、粒径稳定性。扫描图及检测结果如图1-5所示。
91.实施例2、二次纳米化白蛋白紫杉醇对中性粒细胞的影响
92.考虑到改造后纳米药物的疗效由中性粒细胞介导,因此判断改造后的纳米药物对中性粒细胞的影响。
93.如图6所示制备的纳米药物可在体内外被中性粒细胞正常吞噬(流式和电镜检测),炎症刺激状态下更为明显(图7),最高载药量可达到99.1%。
94.为明确改造后的纳米药物对其迁移特性、氧爆发和炎性细胞因子表达的影响,首先通过transwell实验评估了载药后的中性粒细胞的迁移特性;其次通过流式细胞术和荧光强度检测评估了载药后中性粒细胞胞内ros水平的变化;并且通过rt-qpcr评估了载药后中性粒细胞相关炎性细胞因子的表达,具体是il-1β、il-6。
95.趋化实验结果如图8所示(图中fmlp即fmlp,全称n-formyl-methionyl-leucyl-phenylalanine,中文名称:n-甲酰-l-甲硫氨酰-l-亮氨酰-l-苯丙氨酸三肽;是从细菌中发
现的一种白细胞趋化肽,具有很强的趋化和致炎活性,可迅速激活白细胞)。ros检测结果如图9所示(h2dcfda ,是常规用于检测细胞内活性氧(ros)的探针)。炎症细胞因子il-1β、il-6表达量的检测结果如图10。
96.以上结果说明载药并不影响中性粒细胞自身的迁移、ros生成和相关炎性细胞因子的表达。
97.实施例3、体内实验:肺癌模型
98.在小鼠右侧大腿部位构建小鼠llc肺癌皮下瘤模型;药物治疗前一天予以放疗;定期监测小鼠体重和肿瘤体积。具体流程如图11所示。
99.肿瘤实体图如图12所示,数据统计体积和重量的变化如图13所示。同时监测小鼠的体重变化,统计如图14所示。
100.对瘤内中性粒细胞是否载药进行检测,结果如图15所示,约89%的中性粒细胞载药。
101.实施例4、药物安全性的判断
102.在明确改造后纳米药物能明显抑制肿瘤后,通过对小鼠心肝脾肺肾的he染色明确改造后药物的毒副反应,结果如图16所示;同时通过小鼠生化仪和血常规分析仪分别检测小鼠的肝肾功能和外周血细胞的变化(图17)。
103.以上结果说明改造后纳米药物无明显毒副作用,且可明显减轻白蛋白结合型紫杉醇的骨髓抑制作用。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。