可结合cd4的纳米抗体4nb357及其应用
技术领域
1.本发明涉及生物医药领域。更特别地,涉及一种可结合cd4的纳米抗体,还涉及所述纳米抗体在制备hiv感染或cd4阳性的t细胞肿瘤的治疗药物和诊断剂中的应用。
背景技术:
2.cd4是t细胞表面上表达的重要受体分子,但同时也是病毒例如hiv等攻击t细胞的靶点。报道,hiv主要通过包膜表面的糖蛋白gp120与宿主细胞表面的特定受体(例如cd4)接触而影响病毒进入细胞的过程。抑制gp120和cd4的结合,可以有效地抑制hiv-1对宿主细胞的感染。另外,由于t细胞肿瘤也表达cd4。因此,可考虑以cd4为靶点,利用抗cd4抗体来治疗hiv感染或cd4阳性的t细胞肿瘤。
3.1993年,一种来源于骆驼科的新型天然抗体被发现。该抗体天然缺失轻链而只由重链组成,其重链包含两个恒定区(ch2和ch3)、一个铰链区和一个重链可变区(variable heavy chain domain,vhh,即抗原结合位点),该重链可变区的相对分子质量约为13kda,仅为常规抗体的1/10,且分子高度和直径均在纳米级别,是目前可获得的最小的功能性抗体片段,因此又被称为纳米单抗(nanobody,nb)。因纳米单抗稳定性高(90℃条件下仍不会降解)、亲和力高、与人源抗体同源性超过80%、毒性和免疫原性均较低等特点,最近纳米单抗被广泛用于免疫诊断试剂盒研发、影像学研发以及针对肿瘤、炎症、传染病和神经系统疾病等领域的抗体药物研发。
4.我们期望通过新的技术手段,筛选出获得能够结合cd4的抗体,为预防和治疗cd4相关疾病例如hiv感染或cd4阳性t细胞肿瘤等提供潜在新药。
技术实现要素:
5.本发明通过用抗原免疫骆驼,获取骆驼源纳米单抗及其vhh,用于治疗hiv感染的病人。基于这些研究,本发明提供了一种可结合cd4的纳米抗体,其特征在于,包括3个互补决定区cdr1-3,序列如seq id no:1-3所示。
6.在一个具体实施方案中,所述纳米抗体还包括4个框架区fr1-4,所述fr1-4与所述cdr1-3按顺序交错排列。例如,可将fr1-4序列设计为如seq id no:4-7所示(羊驼源),但本发明的范围不限于此。抗体的特异性识别和结合能力主要由cdr区序列决定,fr序列影响不大,可根据物种来设计,这是本领域公知的。可设计人源、鼠源或骆驼源的fr区序列来连接上述cdr,从而得到一个可结合cd4的纳米抗体。
7.在一个具体实施方案中,所述纳米抗体为骆驼源的vhh或人源化的vhh。
8.本发明还提供了上述纳米抗体在制备cd4检测剂中的应用。
9.本发明还提供了上述纳米抗体在制备hiv或cd4阳性的t细胞肿瘤的治疗药物中的应用。
10.本发明还提供了上述纳米抗体在制备针对hiv或cd4阳性的t细胞肿瘤的car-t治疗剂中的应用。
11.本发明还提供了编码上述纳米抗体的核酸。
12.本发明还提供了上述核酸在制备hiv感染或cd4阳性的t细胞肿瘤的治疗药物中的应用。
13.本发明针对hiv进行纳米抗体药物开发,通过制备cd4蛋白、免疫双峰骆驼、利用噬菌体库展示纳米单抗的平台技术等,筛选到特异性结合cd4的纳米抗体vhh,鉴定了其cdr序列,并构建了人源化的vhh-hufc1;同时利用假病毒中和实验评估4nb在治疗hiv感染的疗效。本发明利用cd4结合的纳米抗体为hiv感染的临床治疗以及cd4淋巴瘤的临床治疗提供潜在的纳米抗体新药,双靶向抗体新药,基因治疗新药以及car细胞治疗等。
附图说明
14.图1为cd4第3和4次免疫羊驼一周后的抗血清效价检测曲线;
15.图2为不同稀释度的第4次免疫骆驼一周后的抗血清抑制hiv假病毒体外感染ghost细胞的曲线,以免疫前的血清为对照;
16.图3为cd4-vhh噬菌体抗体文库为模板扩增的pcr产物的电泳图;
17.图4为cd4-vhh噬菌体抗体文库的淘选鉴定,其中,a为噬菌体文库针对cd4蛋白淘选后elisa检测统计图;b为从第二轮(2
nd
)和第三轮(3
rd
)淘选后的噬菌体抗体文库各挑选40个和46个克隆进行噬菌体elisa检测统计图;
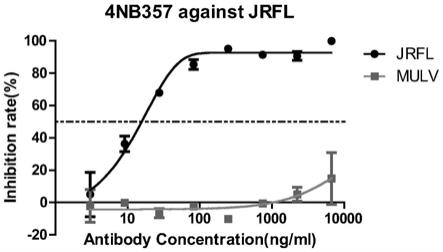
18.图5为抗体4nb357中和hiv假病毒感染实验统计图,jrfl为hiv假病毒,mulv为无关对照病毒,x轴为抗体浓度,y轴为病毒的相对抑制率。
具体实施方式
19.1.免疫原的制备
20.我们依据cd4蛋白序列和基因序列信息,分析并设计了可有效诱导骆驼产生针对cd4蛋白的特异性抗体的多肽cd4,在c端连接his-tag(cd4-his)或兔fc(cd4-rfc)用于后续纯化及检测。
21.2.羊驼免疫与抗血清的获得
22.用250μg cd4-rfc蛋白与250μl弗氏完全佐剂的乳化混合物对羊驼进行初免,在第14天、28天、42天用cd4-rfc蛋白与250μl弗氏不完全佐剂加强免疫3次,第2次和第3次免疫1周后,采血检测抗血清滴度;第4次免疫1周后,采血200ml用于噬菌体抗体库的构建。
23.抗血清效价通过elisa检测,用浓度为0.5μg/ml的cd4-his蛋白包被检测板,每孔加入梯度稀释的抗血清或者纯化的抗体100μl(对照为免疫前骆驼血清),37℃孵育1.5h,洗涤2次,每孔加入1:10000稀释的辣根过氧化物酶标记的goat anti-llamma igg(h l)二抗,37℃孵育1h,洗涤4-6次后,加100μl tmb底物,37℃孵育10min,50μl 0.2m的h2so4中止反应,测定od 450nm。elisa检测血清效价规定为在od450是空白对照的2.1倍以上并且大于0.2的最高稀释倍数。
24.结果如图1所示,3免和4免的抗血清效价分别为3.28
×
106和9.84
×
106。由此可见,该抗原可诱导骆驼产生特异性针对cd4蛋白的高滴度抗血清。
25.为了进一步验证该高滴度的骆驼抗血清是否能有效阻止hiv病毒感染,进行病毒感染的中和实验。将不同稀释浓度的抗血清和免疫前血清分别与hiv病毒共同孵育60min,
随后转移到ghost细胞,48h后通过glo max化学发光酶标仪(promega)检测病毒载量并计算中和效果。中和实验结果显示,cd4诱导的抗血清抑制90%hiv感染的id90为540倍稀释度以上(图2)。综上所述,cd4诱导了高滴度抗血清,同时该抗血清具有高效抑制hiv假病毒感染的能力。
26.3.vhh噬菌体库构建及淘选
27.收集200ml免疫后骆驼的外周血,利用淋巴细胞分离液(ge ficoll-paque plus)分离获得骆驼的pbmc,根据trizol操作手册,提取rna,并利用oligo(dt)反转为cdna,通过引物扩增,以及分子克隆等技术,将骆驼的vhh基因克隆至phagemid质粒,转化tg1细菌,得到vhh噬菌体库。
28.为了进一步鉴定cd4-vhh噬菌体库是否构建成功,通过pcr扩增免疫cd4骆驼的vhh目的基因,可以看出目的条带为500bp,大小符合预期(图3),说明该cd4-vhh噬菌体抗体文库里含有vhh基因。挑选50个克隆进行测序,测序结果显示,所测序列没有完全一致的重复序列;比对结果显示,差异序列大多在cdr结合区。经检测,该构建了一个cd4-vhh噬菌体抗体文库的库容为1.6
×
109,阳性率为100%,序列多样性(diversity)为100%,有效插入率(in frame rate)大于95%。
29.在m13ko7辅助噬菌体的帮助下,用vhh-phagemid转化的细菌,进行噬菌体抗体库的复苏,并用peg/nacl进行沉淀。将包被有50μg/ml的cd4-his蛋白进行三次富集噬菌体抗体库。将富集的噬菌体,洗脱、转化、涂板、挑取单克隆进行噬菌体与cd4蛋白elisa的结合鉴定,将结合读值》1.0的克隆进行测序,并克隆至表达载体phv3,转染293tt细胞表达生产纳米单抗。
30.淘选后的文库与cd4蛋白进行结合检测。噬菌体elisa结果显示,没有富集前的cd4-vhh噬菌体文库与cd4蛋白的结合读值为1.71,经过一轮、二轮、三轮富集后的噬菌体文库读值分别为2.5、3.1、3.1(图4a)。为了进一步验证富集后的文库中结合cd4-vhh蛋白的阳性噬菌体率,从第2轮和第3轮富集后的文库里各挑选了40、46个克隆进行单个噬菌体elisa检测。结果显示,第2轮文库里,57.5%的单个噬菌体克隆为阳性,第3轮文库里82.6%的噬菌体克隆克隆为阳性,而且结合的平均读值在3.0左右(图4b),通过cd4蛋白淘选成功的富集了高结合力的cd4-vhh噬菌体文库。其中,筛选出抗体4nb357,cdr1-3的序列如seq id no:1-3所示,fr1-4的序列如seq id no:4-7所示。
31.4.vhh-hufc真核表达
32.通过分子克隆技术,将文库筛选的阳性克隆vhh基因融合人的fc基因并插入在pcdna3.4真核表达载体,构建形成nb-hufc-pcdna3.4表达质粒。将构建好的nb-hufc-pcdna3.4,转染293tt细胞,表达生产nb-hufc(4nb)。收集细胞上清进行elisa测定。
33.对抗体4nb357与cd4蛋白的亲和力测定试验。应用fortebio生物分子相互作用平台检测亲和力。将抗体4nb357固化至anti-human igg fc capture biosensors(ahc)探头上,固化时间400s,再结合抗原cd4-his蛋白,结合时间180s,解离时间180s,观察抗体-抗原的结合解离情况,由仪器拟合曲线,导出数据。亲和力测定结果如表2所示,大部分的抗体的亲和力能达到10-8或10-9(nano mole级)。由此可见,我们获得了具有高亲和力的vhh-hufc1(c9nb)抗体,可用于检测cd4。
34.表1 4nb357的亲和力数据
35.clone idka(1/ms)kd(1/s)kd(m)response(nm)4nb3579.05e 04《1.0e-07《1.0e-120.35
36.5. 4nb357阻断hiv感染ghost细胞
37.将抗体4nb357稀释至1μg/ml作为起始浓度,3倍比梯度稀释,共设8个梯度,分别与jrfl病毒一起,于5%co
2 37℃下共孵育1个小时,添加1.0x104个ghost细胞,5%co237℃温箱培养48小时后,移除细胞上清,加入100μl/孔的glolysis buffer(提前恢复至室温),轻晃培养板使细胞充分裂解,接着转移50μl/孔细胞裂解物于96孔白色荧光酶标板中(costar),再加入50μl/孔brite-glo luciferase底物(提前恢复至室温),涡旋震荡混匀,立即放入glo max化学发光酶标仪(promega)进行检测。中和滴度(ic50)表述为50%抑制率时的抗体浓度。
38.结果如图5所示,抗体4nb357的ic50为14.7046ng/ml。
39.由以上实验结果可知,抗体4nb357及其人源化形式均可对特异性地识别、结合cd4,阻断cd4的配体与cd4的结合,从而抑制与cd4通路相关的疾病,例如hiv感染、cd4阳性的t细胞肿瘤等。因为抗体4nb357能够识别细胞表面的cd4分子,因此其序列也可以应用于car(chimeric antigen receptor,抗原嵌合受体,由vhh序列融合第三代或者第四代cd28-4-1bb-cd3zeta分子序列构成)细胞治疗肿瘤或hiv感染。
40.另外因为抗体4nb357能识别细胞表面的cd4分子,因此也可以通过偶联药物用于adc(antibody-drug conjugate,抗体偶联药物)治疗或者偶联同位素用于依赖抗体的分子影像诊断等。也可将编码抗体4nb357的核酸搭载在aav系统中,用于治疗作用。
41.以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
