树脂组合物,干膜,干膜、抗蚀剂膜、化合物、产酸剂及n-有机磺酰氧基化合物的制造方法
技术领域
1.本发明涉及化学放大型正型感光性树脂组合物、具备由该化学放大型正型感光性树脂组合物构成的感光性层的感光性干膜、该感光性干膜的制造方法、使用所述化学放大型正型感光性树脂组合物的图案化的抗蚀剂膜的制造方法、新型化合物、新型光产酸剂与n-有机磺酰氧基化合物的制造方法。
背景技术:
2.目前,光电加工(photofabrication)已经成为精密微细加工技术的主流。光电加工是指,将光致抗蚀剂组合物涂布在被加工物表面从而形成光致抗蚀剂层,利用光刻技术使光致抗蚀剂层图案化,并将图案化后的光致抗蚀剂层(光致抗蚀剂图案)作为掩模进行化学蚀刻、电解蚀刻,或者进行以电镀为主体的电铸等,来制造半导体封装等各种精密部件的技术的总称。
3.此外,近年来,随着电子设备的小型化,半导体封装的高密度安装技术不断推进,正在谋求基于封装的多引脚薄膜安装化、封装尺寸的小型化、倒装芯片方式的2维安装技术、3维安装技术的安装密度的提高。在这样的高密度安装技术中,例如封装上突出的凸块等突起电极(安装端子)、或将从晶圆上的外围端子延伸的再布线(rdl)与安装端子相连接的金属柱等作为连接端子而被高精度地配置在基板上。
4.在如上所述的光电加工中使用了光致抗蚀剂组合物,作为那样的光致抗蚀剂组合物,公知有包含产酸剂的化学放大型光致抗蚀剂组合物(参照专利文献1、2等)。化学放大型光致抗蚀剂组合物是指,通过照射放射线(曝光)而从产酸剂产生酸,通过加热处理促进酸的扩散,从而相对于组合物中的基体树脂等引起酸催化反应,使其碱溶解性发生变化。
5.这样的化学放大型正型光致抗蚀剂组合物被用于例如采用镀覆工序形成如凸块、金属柱及cu再布线那样的镀覆造型物等。具体而言,使用化学放大型光致抗蚀剂组合物,在如金属基板那样的支承体上形成所期望的膜厚的光致抗蚀剂层,经由规定的掩模图案进行曝光并显影,形成作为选择性地去除(剥离)了形成镀覆造型物的部分的铸模而使用的光致抗蚀剂图案。然后,通过镀覆将铜等导体埋入该被去除的部分(非抗蚀剂部)后,去除其周围的光致抗蚀剂图案,由此能够形成凸块、金属柱及cu再布线。
6.此外,化学放大型正型光致抗蚀剂组合物例如也被用于通过蚀刻加工基板时的蚀刻掩模的形成。具体而言,使用化学放大型光致抗蚀剂组合物在基板上形成所期望的膜厚的光致抗蚀剂层,接着,经由规定的掩模图案,仅对光致抗蚀剂层的与蚀刻对象部位相对应的部分进行曝光,之后将曝光后的光致抗蚀剂层显影,形成作为蚀刻掩模使用的光致抗蚀剂图案。
7.现有技术文献
8.专利文献
9.专利文献1:日本特开平9-176112号公报
10.专利文献2:日本特开平11-52562号公报
技术实现要素:
11.发明要解决的技术问题
12.为了实现期望的尺寸的抗蚀剂图案,能够使掩模图案忠实地再现于抗蚀剂图案的掩模保真度(掩模线性)良好至关重要。
13.但是,在如专利文献1、2等所公开的那样使用一直以来已知的化学放大型正型光致抗蚀剂组合物来形成抗蚀剂图案的情况下,常常无法使掩模图案忠实地再现于抗蚀剂图案。
14.此外,化学放大型光致抗蚀剂组合物大多是使产酸剂等成分溶解于丙二醇单甲醚乙酸酯等溶剂从而制作的。因此,从容易制备化学放大型光致抗蚀剂组合物、防止化学放大型光致抗蚀剂组合物在保管时析出产酸剂的观点出发,期望产酸剂的溶剂溶解性优异。
15.本发明鉴于上述技术问题而完成,其目的在于提供一种所含有的产酸剂的溶剂溶解性优异且容易形成掩模线性优异的抗蚀剂图案的化学放大型正型感光性树脂组合物、具备由该化学放大型正型感光性树脂组合物构成的感光性层的感光性干膜、该感光性干膜的制造方法、使用所述化学放大型正型感光性树脂组合物的图案化的抗蚀剂膜的制造方法、可优选地掺混于所述化学放大型正型感光性树脂组合物中的化合物及光产酸剂。
16.此外,本发明的目的在于提供能够应用于上述产酸剂的制造方法的、效率较高的n-有机磺酰氧基化合物的制造方法。
17.用于解决上述技术问题的方案
18.本发明人等为了达成上述目的而不断锐意研究,结果发现通过如下的化学放大型正型感光性树脂组合物,能够解决上述技术问题,从而完成了本发明,所述化学放大型正型感光性树脂组合物包含:产酸剂(a),通过活性光线或放射线的照射而产生酸;树脂(b),对碱的溶解性因酸的作用而增大,产酸剂(a)包含以下述式(a1)表示的化合物。
19.此外,本发明人等发现,对n-羟基化合物(a’),通过在利用硅烷化剂(c’)使n-羟基化合物(a’)所具有的氮原子上的羟基硅烷化的同时在碱性化合物(d’)的存在下使其与磺酰氟化合物(b’)反应,或者通过利用硅烷化剂(c’)使n-羟基化合物(a’)所具有的氮原子上的羟基硅烷化后,使生成的硅烷化物在碱性化合物(d’)的存在下与磺酰氟化合物(b’)反应,能够高效地得到n-有机磺酰氧基化合物。
20.具体而言,本发明提供以下方案。
21.本发明的第1方案为一种化学放大型正型感光性树脂组合物,包含:产酸剂(a),通过活性光线或者放射线的照射而产生酸;树脂(b),对碱的溶解性因酸的作用而增大,
22.产酸剂(a)包含以下述式(a1)表示的化合物,
23.【化1】
[0024][0025]
式(a1)中,r
b1
为碳原子数为1以上30以下的烃基,
[0026]
在作为r
b1
的烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-、-cr
b4rb5-及-nr
b6-构成的组中选择的基团取代,
[0027]
在作为r
b1
的烃基包含烃环的情况下,构成烃环的至少1个碳原子可以被从n、o、p、s及se构成的组中选择的杂原子或者包含该杂原子的原子团取代,
[0028]rb4
及r
b5
分别独立地为氢原子或者卤素原子,r
b4
及r
b5
中的至少一方为卤素原子,
[0029]rb6
为氢原子或者碳原子数为1以上6以下的烃基,
[0030]ra1
及r
a2
分别独立地为氢原子、可具有取代基的碳原子数为1以上20以下的脂肪族烃基、可具有取代基的环构成原子数为5以上20以下的芳香族基团或者以-r
a3-r
a4
表示的基团,
[0031]ra1
及r
a2
不同时为氢原子,
[0032]
在作为r
a1
或者r
a2
的脂肪族烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-及-nr
a5-构成的组中选择的基团取代,
[0033]ra5
为氢原子或者碳原子数为1以上6以下的烃基,
[0034]ra3
为亚甲基、-o-、-co-、-co-o-、-so-、-so
2-或者-nr
a6-,
[0035]ra6
为氢原子或者碳原子数为1以上6以下的烃基,
[0036]ra4
为可具有取代基的环构成原子数为5以上20以下的芳香族基团、碳原子数为1以上6以下的全氟烷基、可具有取代基的碳原子数为7以上20以下的芳烷基、或者包含可具有取代基的环构成原子数为5以上20以下的芳香族杂环基的杂芳基烷基,
[0037]
q1及q2分别独立地为氟原子或者碳原子数为1以上6以下的全氟烷基,
[0038]
l为酯键。
[0039]
本发明的第2方案为一种感光性干膜,具有基材薄膜与形成于基材薄膜的表面的感光性层,感光性层由第1方案的化学放大型正型感光性树脂组合物构成。
[0040]
本发明的第3方案为一种感光性干膜的制造方法,包括在基材薄膜上涂布第1方案的化学放大型正型感光性树脂组合物从而形成感光性层。
[0041]
本发明的第4方案为一种图案化的抗蚀剂膜的制造方法,包括:
[0042]
层叠工序,在基板上层叠由第1方案的化学放大型正型感光性树脂组合物构成的感光性层;
[0043]
曝光工序,对感光性层位置选择性地照射活性光线或放射线来进行曝光;
[0044]
显影工序,对曝光后的感光性层进行显影。
[0045]
本发明的第5方案为一种化合物,以下述式(a1)表示,
[0046]
【化2】
[0047][0048]
式(a1)中,r
b1
为碳原子数为1以上30以下的烃基,
[0049]
在作为r
b1
的烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-、-cr
b4rb5-及-nr
b6-构成的组中选择的基团取代,
[0050]
在作为r
b1
的烃基包含烃环的情况下,构成烃环的至少1个碳原子可以被从n、o、p、s及se构成的组中选择的杂原子或者包含该杂原子的原子团取代,
[0051]rb4
及r
b5
分别独立地为氢原子或者卤素原子,r
b4
及r
b5
中的至少一方为卤素原子,
[0052]rb6
为氢原子或者碳原子数为1以上6以下的烃基,
[0053]ra1
及r
a2
分别独立地为氢原子、可具有取代基的碳原子数为1以上20以下的脂肪族烃基、可具有取代基的环构成原子数为5以上20以下的芳香族基团或者以-r
a3-r
a4
表示的基团,
[0054]ra1
及r
a2
不同时为氢原子,
[0055]
在作为r
a1
或者r
a2
的脂肪族烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-及-nr
a5-构成的组中选择的基团取代,
[0056]ra5
为氢原子或者碳原子数为1以上6以下的烃基,
[0057]ra3
为亚甲基、-o-、-co-、-co-o-、-so-、-so
2-或者-nr
a6-,
[0058]ra6
为氢原子或者碳原子数为1以上6以下的烃基,
[0059]ra4
为可具有取代基的环构成原子数为5以上20以下的芳香族基团、碳原子数为1以上6以下的全氟烷基、可具有取代基的碳原子数为7以上20以下的芳烷基、或者包含可具有取代基的环构成原子数为5以上20以下的芳香族杂环基的杂芳基烷基,
[0060]
q1及q2分别独立地为氟原子或者碳原子数为1以上6以下的全氟烷基,
[0061]
l为酯键。
[0062]
本发明的第6方案为一种光产酸剂,包含第5方案的化合物。
[0063]
本发明的第7方案为n-有机磺酰氧基化合物的制造方法,包括使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下反应,
[0064]
其特征在于,在使n-羟基化合物(a’)与磺酰氟化合物(b’)反应时,在反应系统中存在硅烷化剂(c’),
[0065]
磺酰氟化合物(b’)以下述式(bi1)表示,
[0066]rbi1-so
2-f
···
(bi1)
[0067]
(式(bi1)中,r
bi1
为有机基团。)
[0068]
硅烷化剂(c’)可将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以下述式
(ac1)表示的甲硅烷氧基。
[0069]-o-si(r
c1
)3···
(ac1)
[0070]
(式(ac1)中,r
c1
分别独立地为碳原子数为1以上10以下的烃基。)
[0071]
本发明的第8方案为n-有机磺酰氧基化合物的制造方法,其包括:硅烷化工序,利用硅烷化剂(c’)使n-羟基化合物(a’)硅烷化;
[0072]
缩合工序,使在硅烷化工序中生成的n-羟基化合物(a’)的硅烷化物在碱性化合物(d’)的存在下,与磺酰氟化合物(b’)缩合,
[0073]
磺酰氟化合物(b’)以下述式(bi1)表示,
[0074]rbi1-so
2-f
···
(bi1)
[0075]
(式(bi1)中,r
bi1
为有机基团。)
[0076]
硅烷化剂可将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以下述式(ac1)表示的甲硅烷氧基。
[0077]-o-si(r
c1
)3···
(ac1)
[0078]
(式(ac1)中,r
c1
分别独立地为碳原子数为1以上10以下的烃基。)
[0079]
发明效果
[0080]
根据本发明,能够提供一种所含有的产酸剂的溶剂溶解性优异且容易形成掩模线性优异的抗蚀剂图案的化学放大型正型感光性树脂组合物、具备由该化学放大型正型感光性树脂组合物构成的感光性层的感光性干膜、该感光性干膜的制造方法、使用所述化学放大型正型感光性树脂组合物的图案化的抗蚀剂膜的制造方法、可优选地掺混于所述化学放大型正型感光性树脂组合物中的化合物及光产酸剂。
[0081]
此外,根据本发明,还提供能够适宜地用于上述产酸剂的制造方法的、效率较高的n-有机磺酰氧基化合物的制造方法。
具体实施方式
[0082]
《化学放大型正型感光性树脂组合物》
[0083]
化学放大型正型感光性树脂组合物(以下也记作感光性树脂组合物)含有:产酸剂(a),通过照射活性光线或者放射线而产生酸(以下也记作产酸剂(a));树脂(b),对碱的溶解性因酸的作用而增大(以下也记作树脂(b))。并且,在本发明中,产酸剂(a)包含以下述式(a1)表示的化合物。感光性树脂组合物也可以根据需要包含碱可溶性树脂(d)、含硫化合物(e)、酸扩散抑制剂(f)及有机溶剂(s)等成分。
[0084]
使用感光性树脂组合物所形成的抗蚀剂图案的膜厚没有特别地限定,厚膜及薄膜均可适用。感光性树脂组合物优选用于形成厚膜的抗蚀剂图案。具体而言,使用感光性树脂组合物而形成的抗蚀剂图案的膜厚优选为0.5μm以上,更优选为0.5μm以上300μm以下,进一步优选为0.5μm以上200μm以下,特别优选为0.5μm以上150μm以下。
[0085]
膜厚的上限值例如可以为100μm以下。膜厚的下限值例如可以为1μm以上,也可以为3μm以上。
[0086]
以下,对感光性树脂组合物所包含的必需或者任意的成分与感光性树脂组合物的制造方法进行说明。
[0087]
《产酸剂(a)》
[0088]
产酸剂(a)是通过活性光线或放射线的照射而产生酸的化合物,是通过光直接或者间接地产生酸的化合物。产酸剂(a)包含以下述式(a1)表示的化合物。
[0089]
【化3】
[0090][0091]
式(a1)中,r
b1
为碳原子数为1以上30以下的烃基。
[0092]
在作为r
b1
的烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-、-cr
b4rb5-及-nr
b6-构成的组中选择的基团取代。
[0093]
在作为r
b1
的烃基包含烃环的情况下,构成烃环的至少1个碳原子可以被从n、o、p、s及se构成的组中选择的杂原子或者包含该杂原子的原子团取代。
[0094]rb4
及r
b5
分别独立地为氢原子或者卤素原子,r
b4
及r
b5
中的至少一方为卤素原子。
[0095]rb6
为氢原子或者碳原子数为1以上6以下的烃基。
[0096]ra1
及r
a2
分别独立地为氢原子、可具有取代基的碳原子数为1以上20以下的脂肪族烃基、可具有取代基的环构成原子数为5以上20以下的芳香族基团或者以-r
a3-r
a4
表示的基团。
[0097]ra1
及r
a2
不同时为氢原子。
[0098]
在作为r
a1
或者r
a2
的脂肪族烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-及-nr
a5-构成的组中选择的基团取代。
[0099]ra5
为氢原子或者碳原子数为1以上6以下的烃基。
[0100]ra3
为亚甲基、-o-、-co-、-co-o-、-so-、-so
2-或者-nr
a6-。
[0101]ra6
为氢原子或者碳原子数为1以上6以下的烃基。
[0102]ra4
为可具有取代基的环构成原子数为5以上20以下的芳香族基团、碳原子数为1以上6以下的全氟烷基、可具有取代基的碳原子数为7以上20以下的芳烷基、或者包含可具有取代基的环构成原子数为5以上20以下的芳香族杂环基的杂芳基烷基。
[0103]
q1及q2分别独立地为氟原子或者碳原子数为1以上6以下的全氟烷基。
[0104]
l为酯键。
[0105]
式(a1)中,作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0106]
作为脂肪族烃基,优选为烷基。作为烷基的优选的具体例,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基及正癸基。
[0107]
作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可具有的取代基,可例举羟基、巯基、氨基、卤素原子、氧原子、硝基、氰基、羧基等。取代基的数量是任意的。作为r
a1
及ra2
的具有取代基的碳原子数为1以上20以下的脂肪族烃基,例如可例举碳原子数为1以上6以下的全氟烷基。作为其具体例,可例举cf
3-、cf3cf
2-、(cf3)2cf-、cf3cf2cf
2-、cf3cf2cf2cf
2-、(cf3)2cfcf
2-、cf3cf2(cf3)cf-、(cf3)3c-。
[0108]
式(a1)中,作为r
a1
及r
a2
的可具有取代基的环构成原子数为5以上20以下的芳香族基团,可以为芳香族烃基,也可以为芳香族杂环基。
[0109]
作为芳香族基团,可例举苯基、萘基等芳基或呋喃基、噻吩基等杂芳基。
[0110]
环构成原子数为5以上20以下的芳香族基团可具有的取代基与作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可具有的取代基相同。
[0111]
式(a1)中,作为r
a4
的可具有取代基的环构成原子数为5以上20以下的芳香族基团与对r
a1
及r
a2
说明的可具有取代基的环构成原子数为5以上20以下的芳香族基团相同。
[0112]
式(a1)中,作为r
a4
的碳原子数为1以上6以下的全氟烷基与作为r
a1
及r
a2
说明的碳原子数为1以上6以下的全氟烷基相同。
[0113]
式(a1)中,作为r
a4
的可具有取代基的碳原子数为7以上20以下的芳烷基的具体例,可例举苄基、苯乙基、α-萘基甲基、β-萘基甲基、2-α-萘基乙基及2-β-萘基乙基等。
[0114]
式(a1)中,杂芳基烷基是指芳基烷基中的构成芳香族烃环的一部分碳原子被n、o或s等杂原子取代而得的基团。作为r
a4
的包含可具有取代基的环构成原子数为5以上20以下的芳香族杂环基的杂芳基烷基的具体例,可例举吡啶-2-基甲基、吡啶-3-基甲基、吡啶-4-基甲基等。
[0115]
式(a1)中,作为r
a5
的碳原子数为1以上6以下的烃基可以为脂肪族烃基,也可以为芳香族烃基,还可以为脂肪族烃基与芳香族烃基的组合。脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0116]
作为脂肪族烃基,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基等烷基。
[0117]
作为芳香族烃基,可例举苯基。
[0118]
式(a1)中,作为r
a6
的碳原子数为1以上6以下的烃基与对r
a5
说明的碳原子数为1以上6以下的烃基相同。
[0119]
式(a1)中,作为r
b1
的碳原子数为1以上30以下的烃基可以为脂肪族烃基,也可以为芳香族烃基,还可以为脂肪族烃基与芳香族烃基的组合。脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0120]
作为脂肪族烃基,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基等链状的脂肪族烃基、环丙基、环丁基、环戊基、环己基、金刚烷基、降冰片基等环状的脂肪族烃基(烃环)。
[0121]
作为芳香族烃基,可例举苯基、萘基。
[0122]
作为将脂肪族烃基及芳香族烃基组合而得的基团,可例举苄基、苯乙基、呋喃基甲基。
[0123]
在作为r
b1
的烃基包含烃环的情况下,作为取代构成烃环的至少1个碳原子的包含杂原子的原子团,可例举-co-、-co-o-、-so-、-so
2-、-so
2-o-、-p(=o)-(or
b7
)3。r
b7
为碳原子数为1以上6以下的烃基,与对r
a5
说明的碳原子数为1以上6以下的烃基相同。
[0124]
式(a1)中,作为r
b4
及r
b5
的卤素原子的具体例,可例举氯原子、氟原子、溴原子及碘
原子。
[0125]
式(a1)中,作为r
b6
的碳原子数为1以上6以下的烃基,与式(a1)中作为r
a5
说明的碳原子数为1以上6以下的烃基相同。
[0126]
式(a1)中,作为q1及q2的碳原子数为1以上6以下的全氟烷基,与式(a1)中作为r
a1
及r
a2
说明的碳原子数为1以上6以下的全氟烷基相同。
[0127]
在以式(a1)表示的化合物中,作为l的酯键的方向没有特别限定,可以是-co-o-及-o-co-中的任一个。
[0128]
以式(a1)表示的化合物优选为以下述式(a1-1)表示的化合物。
[0129]
【化4】
[0130][0131]
(式(a1-1)中的r
b1
、r
a1
、q1及q2与式(a1)中的这些相同。)
[0132]
式(a1-1)中的r
a1
为可具有取代基的碳原子数为1以上20以下的脂肪族烃基,在作为r
a1
的脂肪族烃基包含1个以上的亚甲基的情况下,优选为至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-及-nr
a5-构成的组中选择的基团取代的、以式(a1-1)表示的化合物。
[0133]
这样的以式(a1)表示的化合物在丙二醇单甲醚乙酸酯等溶剂中的溶解性优异。因此,容易制备以期望的浓度包含作为产酸剂(a)的以式(a1)表示的化合物的感光性树脂组合物。此外,容易抑制所制备的感光性树脂组合物中的产酸剂(a)的析出。
[0134]
此外,若使用含有以式(a1)表示的化合物作为产酸剂(a)的感光性树脂组合物,则容易形成掩模线性优异的抗蚀剂图案。推测这是由于以式(a1)表示的化合物通过曝光产生的酸的扩散长度较短,酸难以向未曝光部扩散。另外,“掩模线性”是指能够将掩模图案忠实地再现到抗蚀剂图案的掩模保真度。因此,能够实现期望的尺寸的抗蚀剂图案。
[0135]
以式(a1)表示的化合物能够通过以下的n-有机磺酰氧基化合物的制造方法来制造。
[0136]
在能够制造以式(a1)表示的化合物的n-有机磺酰氧基化合物的制造方法中,包括使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应,其特征在于,在使n-羟基化合物(a’)与磺酰氟化合物(b’)反应时,系统中存在硅烷化剂(c’),磺酰氟化合物(b’)以下述式(b1-1)表示,硅烷化剂(c’)可以将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以下述式(ac1)表示的甲硅烷氧基。
[0137]-o-si(r
c1
)3···
(ac1)
[0138]
(式(ac1)中,r
c1
分别独立地为碳原子数为1以上10以下的烃基。)
[0139]rb1-l-cq1q
2-so
2-f
···
(b1-1)
[0140]
(式(b1-1)中,r
b1
、l、q1及q2分别与上述式(a1)中的这些相同。)
[0141]
此外,在能够制造以式(a1)表示的化合物的n-有机磺酰氧基化合物的制造方法中,包括:硅烷化工序,利用硅烷化剂(c’)使n-羟基化合物(a’)硅烷化;缩合工序,使在硅烷化工序中生成的n-羟基化合物(a’)的硅烷化物在碱性化合物(d’)的存在下,与磺酰氟化合物(b’)缩合,磺酰氟化合物(b’)以上述式(b1-1)表示,硅烷化剂可以将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以上述式(ac1)表示的甲硅烷氧基。
[0142]
n-羟基化合物(a’)是以下述式(a1-1)表示的化合物。
[0143]
【化5】
[0144][0145]
(式(a1-1)中的r
a1
及r
a2
与上述式(a1)中的这些相同。)
[0146]
n-羟基化合物(a’)能够通过例如国际公开第2014/084269号册子、日本特表2017-535595号公报、国际公开第2018/110399号册子中公开的那样的常规方法来合成。例如,以市售的溴化物为起始物质,通过以下述式所示的反应将萘二甲酸酐上的溴基转化为r
a1
之后,使羟胺盐酸盐等羟胺化合物作用于酸酐基来进行n-羟基酰亚胺化,由此能够合成以式(a1-1)表示的r
a2
为氢原子的化合物。此外,作为n-羟基化合物(a’),可以使用市售品。
[0147]
【化6】
[0148][0149]
此外,能够使对应的苊醌与过氧化物在有机溶剂中反应,得到对应的1,8-萘二甲酸酐,使羟胺化合物发挥作用,由此合成n-羟基化合物(a’)。
[0150]
此外,还能够通过使羟胺与如下得到的前体反应来合成,所述前体由3-羟基-1,8-萘二甲酸酐与下述式(i)的化合物,或者4-溴-羟基-1,8-萘二甲酸酐与下述式(ii)的化合物等反应得到。
[0151]
【化7】
[0152][0153]
(式(i)中,r
i1
表示氢原子或可具有羧酸基的碳原子数为1以上12以下的烷基,r
i2
表示氢原子或碳原子数为1以上12以下的烷基,xi表示氯原子、溴原子或碘原子。)
[0154]
【化8】
[0155][0156]
(式(ii)中,r
i1
表示氢原子或可具有羧酸基的碳原子数为1以上12以下的烷基,r
i2
表示氢原子或碳原子数为1以上12以下的烷基。sh表示硫醇基。)
[0157]
磺酰氟化合物(b’)能够通过常规方法合成。例如,在式(b1-1)中,q1及q2为氟原子的化合物能够通过以下述式表示的反应来合成。此外,作为磺酰氟化合物(b’),可以使用市售品。
[0158]
【化9】
[0159][0160]
式(ac1)中,作为r
c1
的碳原子数为1以上10以下的烃基可以为脂肪族烃基,也可以为芳香族烃基,还可以为脂肪族烃基与芳香族烃基的组合。脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0161]
作为脂肪族烃基,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基及正癸基等烷基。
[0162]
作为芳香族烃基,可例举苯基、萘基。
[0163]
作为硅烷化剂(c’),可例举以下述式(c1)表示的化合物。
[0164]
x-si(r
c1
)3···
(c1)
[0165]
(式(c1)中,r
c1
与式(ac1)中的r
c1
相同,x为卤素原子。)
[0166]
式(c1)中,作为x的卤素原子的具体例,可例举氯原子、氟原子、溴原子及碘原子。
[0167]
作为硅烷化剂(c’)的具体例,可例举三甲基氯硅烷、三甲基氟硅烷、三甲基溴硅烷、叔丁基二甲基氯硅烷、乙基二甲基氯硅烷、异丙基二甲基氯硅烷。
[0168]
碱性化合物(d’)可以是有机碱,也可以是无机碱。
[0169]
作为有机碱,例如可例举含氮碱性化合物,作为具体例,可例举甲胺、乙胺、正丙胺、异丙胺、正丁胺、二甲胺、二乙胺、二正丙胺、二异丙胺、二正丁胺、三甲胺、三乙胺、甲基二乙胺、n-乙基二异丙胺、三正丙胺、三异丙胺、单乙醇胺、二乙醇胺及三乙醇胺等胺类;吡咯、哌啶、1,8-二氮杂双环[5,4,0]-7-十一碳烯及1,5-二氮杂双环[4,3,0]-5-壬烷等环状碱性化合物;四甲基氢氧化铵(tmah)、四乙基氢氧化铵、四丙基氢氧化铵(tpah)、四丁基氢氧化铵、甲基三丙基氢氧化铵、甲基三丁基氢氧化铵、苄基三甲基氢氧化铵、苄基三乙基氢氧化铵及三甲基(2-羟乙基)氢氧化铵等季铵盐等。
[0170]
作为无机碱,例如可例举金属氢氧化物、金属碳酸氢盐及金属重碳酸盐。作为无机碱的具体例,可例举氢氧化锂、氢氧化钾、氢氧化钠、氢氧化铷、氢氧化铯、氢氧化镁、氢氧化钙、氢氧化锶及氢氧化钡等金属氢氧化物;碳酸锂、碳酸钾、碳酸钠、碳酸铷、碳酸铯、碳酸
镁、碳酸钙、碳酸锶及碳酸钡等金属碳酸盐;碳酸氢锂、碳酸氢钾、碳酸氢钠、碳酸氢铷及碳酸氢铯等金属重碳酸盐等。
[0171]
在n-有机磺酰氧基化合物的制造方法中,使这样的n-羟基化合物(a’)与磺酰氟化合物(b’)在硅烷化剂(c’)及碱性化合物(d’)的存在下进行反应。
[0172]
像这样,在使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应时,通过使硅烷化剂(c’)存在,能够如后述的实施例所示地高效地制造n-有机磺酰氧基化合物。例如,相对于原料的n-羟基化合物(a’)及磺酰氟化合物(b’),能够以65%以上得到n-有机磺酰氧基化合物。
[0173]
通过n-有机磺酰氧基化合物的制造方法,可得到具有n-羟基化合物(a’)的与氮原子键合的羟基的氢原子被去除的基团、和源自磺酰氟化合物(b’)的r
b1-so
2-键合而得的结构的n-有机磺酰氧基化合物。
[0174]
在n-有机磺酰氧基化合物的制造方法中,在使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应时,只要系统中存在硅烷化剂(c’)即可,可以同时混合n-羟基化合物(a’)、磺酰氟化合物(b’)、硅烷化剂(c’)及碱性化合物(d’),也可以在使n-羟基化合物(a’)与硅烷化剂(c’)部分反应后或者使n-羟基化合物(a’)与硅烷化剂(c’)完成反应后,再添加磺酰氟(b’)及碱性化合物(d’)。
[0175]
若使这样的n-羟基化合物(a’)与磺酰氟化合物(b’)在硅烷化剂(c’)及碱性化合物(d’)的存在下进行反应,则n-羟基化合物(a’)被硅烷化剂(c’)硅烷化,使氮原子上的羟基被转化为以上述式(ac1)表示的甲硅烷氧基(步骤1:硅烷化工序)。
[0176]
然后,使在硅烷化工序中生成的n-羟基化合物(a’)的硅烷化物与碱性化合物(d’)作用的磺酰氟化合物(b’)进行缩合(步骤2:缩合工序)。由此,可得到n-有机磺酰氧基化合物。
[0177]
作为n-有机磺酰氧基化合物的制造方法的一例,在以下示出使用以上述式(a1-1)表示的化合物作为n-羟基化合物(a’)、使用在上述式(b1-1)中q1及q2为氟原子的化合物作为磺酰氟化合物(b’)、使用三甲基氯硅烷作为硅烷化剂(c’)、使用三乙胺作为碱性化合物(d’)的情况下的反应式。另外,以下所示的不是分析确认的反应机理,而是根据原料与其反应中的行为推定的反应机理。
[0178]
【化10】
[0179]
step-1
[0180][0181]
【化11】
[0182]
step-2
[0183][0184]
作为能够在反应中采用的有机溶剂,例如可例举乙酸乙酯、乙酸丁酯、乙酸溶纤剂等酯类;丙酮、甲基乙基酮、异丁基酮、甲基异丁基酮等酮类;乙酸乙酯、乙酸丁酯、丙二酸二乙酯等酯类;n-甲基吡咯烷酮、n,n-二甲基甲酰胺等酰胺类;二乙醚、乙基环戊醚、四氢呋喃、二氧六环等醚类;甲苯、二甲苯等芳香族烃类;己烷、庚烷、辛烷、十氢化萘等脂肪族烃类;氯仿、二氯甲烷、甲叉二氯、二氯乙烷等卤代烃类;乙腈、丙腈等腈类溶剂;二甲亚砜、二甲磺酰胺等。所使用的有机溶剂可以使用1种溶剂,也可以将2种以上任意地组合来使用。
[0185]
作为能够采用的反应温度,例如在-10℃~200℃的范围内,优选在0℃~150℃的范围内,更优选在5℃~120℃的范围内。
[0186]
作为能够采用的反应时间,例如为5分钟以上20小时以下、10分钟以上15小时以下、30分钟以上12小时以下。
[0187]
相对于n-羟基化合物(a’),优选分别过量地使用磺酰氟化合物(b’)、硅烷化剂(c’)及碱性化合物(d’)。例如,相对于1.0摩尔n-羟基化合物(a’),优选以1.1摩尔以上2.5摩尔以下使用磺酰氟化合物(b’)、以1.1摩尔以上2.5摩尔以下使用硅烷化剂(c’)、以1.1摩尔以上2.5摩尔以下使用碱性化合物(d’)。
[0188]
产酸剂(a)也可以包含以上述式(a1)表示的化合物以外的其它产酸剂(以下也记作其它产酸剂)。该其它产酸剂是通过活性光线或者放射线的照射而产生酸的化合物,是通过光直接或者间接地产生酸的化合物。作为产酸剂(a)可以包含的其它产酸剂,优选为以下说明的第一到第五方案的产酸剂。
[0189]
作为产酸剂(a)中的其它产酸剂的第一方案,可例举以下述式(a101)表示的化合物。
[0190]
【化12】
[0191][0192]
在上述式(a101)中,x
101a
表示原子价g的硫原子或者碘原子,g是1或者2。h表示括号内的结构的重复单元数。r
101a
为与x
101a
键合的有机基团,表示碳原子数为6以上30以下的芳基、碳原子数为4以上30以下的杂环基、碳原子数为1以上30以下的烷基、碳原子数为2以上30以下的烯基或碳原子数为2以上30以下的炔基,r
101a
可以被从烷基、羟基、烷氧基、烷基羰基、芳基羰基、烷氧基羰基、芳氧基羰基、芳硫基羰基、酰氧基、芳硫基、烷硫基、芳基、杂环、芳氧基、烷基亚磺酰基、芳基亚磺酰基、烷基磺酰基、芳基磺酰基、亚烷基氧基、氨基、氰基、硝基的各基团及卤素构成的组中选择的至少1种取代。r
101a
的个数是g h(g-1) 1,r
101a
可以分别相互相同也可以不同。此外,2个以上的r
101a
可以相互直接键合或者经由-o-、-s-、-so-、-so
2-、-nh-、-nr
102a-、-co-、-coo-、-conh-、碳原子数为1以上3以下的亚烷基或亚苯基键合而形成包含x
101a
的环结构。r
102a
为碳原子数为1以上5以下的烷基或碳原子数为6以上10以下的芳基。
[0193]
x
102a
是以下述式(a102)表示的结构。
[0194]
【化13】
[0195][0196]
上述式(a102)中,x
104a
表示碳原子数为1以上8以下的亚烷基、碳原子数为6以上20以下的亚芳基、或碳原子数为8以上20以下的杂环化合物的2价基团,x
104a
可以被选自碳原子数为1以上8以下的烷基、碳原子数为1以上8以下的烷氧基、碳原子数为6以上10以下的芳基、羟基、氰基、硝基的各基团及卤素构成的组中的至少1种取代。x
105a
表示-o-、-s-、-so-、-so
2-、-nh-、-nr
102a-、-co-、-coo-、-conh-、碳原子数为1以上3以下的亚烷基或亚苯基。h表示括号内的结构的重复单元数。h 1个x
104a
及h个x
105a
可以分别相同也可以不同。r
102a
与上述的定义相同。
[0197]
x
103a-是鎓的抗衡离子,可例举以下述式(a117)表示的氟代烷基氟磷酸阴离子或者以下述式(a118)表示的硼酸根阴离子。
[0198]
【化14】
[0199]
[(r103a)jpf
6-j
|
‑ (a117)
[0200]
在上述式(a117)中,r
103a
表示80%以上的氢原子被氟原子取代而得的烷基。j表示r
103a
的个数,为1以上5以下的整数。j个r
103a
可以分别相同也可以不同。
[0201]
【化15】
[0202]
[0203]
在上述式(a118)中,r
104a
~r
107a
分别独立地表示氟原子或苯基,该苯基的氢原子的一部分或全部可以被选自氟原子及三氟甲基构成的组中的至少1种取代。
[0204]
作为以上述式(a101)表示的化合物中的鎓离子,可例举三苯基锍、三对甲苯基锍、4-(苯硫基)苯基二苯基锍、双[4-(二苯基锍基)苯基]硫醚、双〔4-{双[4-(2-羟基乙氧基)苯基]锍基}苯基〕硫醚、双{4-[双(4-氟苯基)锍基]苯基}硫醚、4-(4-苯甲酰基-2-氯苯硫基)苯基双(4-氟苯基)锍、7-异丙基-9-氧代-10-硫代-9,10-二氢蒽-2-基二对甲苯基锍、7-异丙基-9-氧代-10-硫代-9,10-二氢蒽-2-基二苯基锍、2-[(二苯基)锍基]噻吨酮、4-[4-(4-叔丁基苯甲酰基)苯硫基]苯基二对甲苯基锍、4-(4-苯甲酰基苯硫基)苯基二苯基锍、二苯基苯甲酰甲基锍、4-羟苯基甲基苄基锍、2-萘甲基(1-乙氧基羰基)乙基锍、4-羟苯基甲基苯甲酰甲基锍、苯基[4-(4-联苯硫基)苯基]4-联苯基锍、苯基[4-(4-联苯硫基)苯基]3-联苯基锍、[4-(4-乙酰苯硫基)苯基]二苯基锍、十八烷基甲基苯甲酰甲基锍、二苯基碘鎓、二对甲苯基碘鎓、双(4-十二烷基苯基)碘鎓、双(4-甲氧基苯基)碘鎓、(4-辛氧基苯基)苯基碘鎓、双(4-癸氧基)苯基碘鎓、4-(2-羟基十四烷氧基)苯基苯基碘鎓、4-异丙基苯基(对甲苯基)碘鎓或4-异丁基苯基(对甲苯基)碘鎓等。
[0205]
以上述式(a101)表示的化合物中的鎓离子中,作为优选的鎓离子,可例举以下述式(a119)表示的锍离子。
[0206]
【化16】
[0207][0208]
在上述式(a119)中,r
108a
分别独立地表示从氢原子、烷基、羟基、烷氧基、烷基羰基、烷基羰基氧基、烷基氧基羰基、卤素原子、可具有取代基的芳基、芳基羰基构成的组中选择的基团。x
102a
表示与上述式(a101)中的x
102a
相同的意思。
[0209]
作为以上述式(a119)表示的锍离子的具体例,可例举4-(苯硫基)苯基二苯基锍、4-(4-苯甲酰基-2-氯苯硫基)苯基双(4-氟苯基)锍、4-(4-苯甲酰基苯硫基)苯基二苯基锍、苯基[4-(4-联苯硫基)苯基]4-联苯基锍、苯基[4-(4-联苯硫基)苯基]3-联苯基锍、[4-(4-乙酰苯硫基)苯基]二苯基锍、二苯基[4-(对三联苯硫基)苯基]二苯基锍。
[0210]
在以上述式(a117)表示的氟代烷基氟磷酸阴离子中,r
103a
表示被氟原子取代而得的烷基,优选的碳原子数为1以上8以下,进一步优选的碳原子数为1以上4以下。作为烷基的具体例,可例举甲基、乙基、丙基、丁基、戊基、辛基等直链烷基;异丙基、异丁基、仲丁基、叔丁基等支链烷基,还可例举环丙基、环丁基、环戊基、环己基等环烷基等,烷基的氢原子被氟原子取代的比例通常为80%以上,优选为90%以上,进一步优选为100%。在氟原子的取代率小于80%的情况下,以上述式(a101)表示的氟代烷基氟磷酸鎓盐的酸强度降低。
[0211]
特别优选的r
103a
是碳原子数为1以上4以下且氟原子的取代率为100%的直链状或支链状的全氟烷基,作为具体例,可例举cf3、cf3cf2、(cf3)2cf、cf3cf2cf2、cf3cf2cf2cf2、
(cf3)2cfcf2、cf3cf2(cf3)cf、(cf3)3c。r
103a
的个数j为1以上5以下的整数,优选为2以上4以下,特别优选为2或3。
[0212]
作为优选的氟代烷基氟磷酸阴离子的具体例,可例举[(cf3cf2)2pf4]-、[(cf3cf2)3pf3]-、[((cf3)2cf)2pf4]-、[((cf3)2cf)3pf3]-、[(cf3cf2cf2)2pf4]-、[(cf3cf2cf2)3pf3]-、[((cf3)2cfcf2)2pf4]-、[((cf3)2cfcf2)3pf3]-、[(cf3cf2cf2cf2)2pf4]-、或者[(cf3cf2cf2)3pf3]-,其中,特别优选为[(cf3cf2)3pf3]-、[(cf3cf2cf2)3pf3]-、[((cf3)2cf)3pf3]-、[((cf3)2cf)2pf4]-、[((cf3)2cfcf2)3pf3]-、或[((cf3)2cfcf2)2pf4]-。
[0213]
作为以上述式(a118)表示的硼酸根阴离子的优选具体例,可例举四(五氟苯基)硼酸根([b(c6f5)4]-)、四[(三氟甲基)苯基]硼酸根([b(c6h4cf3)4]-)、二氟双(五氟苯基)硼酸根([(c6f5)2bf2]-)、三氟(五氟苯基)硼酸根([(c6f5)bf3]-)、四(二氟苯基)硼酸根([b(c6h3f2)4]-)等。其中,特别优选为四(五氟苯基)硼酸根([b(c6f5)4]-)。
[0214]
作为产酸剂(a)中其它产酸剂的第二方案,可例举2,4-双(三氯甲基)-6-胡椒基-1,3,5-三嗪、2,4-双(三氯甲基)-6-[2-(2-呋喃基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(5-甲基-2-呋喃基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(5-乙基-2-呋喃基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(5-丙基-2-呋喃基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3,5-二甲氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3,5-二乙氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3,5-二丙氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3-甲氧基-5-乙氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3-甲氧基-5-丙氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-[2-(3,4-亚甲基二氧基苯基)乙烯基]均三嗪、2,4-双(三氯甲基)-6-(3,4-亚甲基二氧基苯基)均三嗪、2,4-双-三氯甲基-6-(3-溴-4-甲氧基)苯基均三嗪、2,4-双-三氯甲基-6-(2-溴-4-甲氧基)苯基均三嗪、2,4-双-三氯甲基-6-(2-溴-4-甲氧基)苯乙烯基苯基均三嗪、2,4-双-三氯甲基-6-(3-溴-4-甲氧基)苯乙烯基苯基均三嗪、2-(4-甲氧基苯基)-4,6-双(三氯甲基)-1,3,5-三嗪、2-(4-甲氧基萘基)-4,6-双(三氯甲基)-1,3,5-三嗪、2-[2-(2-呋喃基)乙烯基]-4,6-双(三氯甲基)-1,3,5-三嗪、2-[2-(5-甲基-2-呋喃基)乙烯基]-4,6-双(三氯甲基)-1,3,5-三嗪、2-[2-(3,5-二甲氧基苯基)乙烯基]-4,6-双(三氯甲基)-1,3,5-三嗪、2-[2-(3,4-二甲氧基苯基)乙烯基]-4,6-双(三氯甲基)-1,3,5-三嗪、2-(3,4-亚甲基二氧基苯基)-4,6-双(三氯甲基)-1,3,5-三嗪、三(1,3-二溴丙基)-1,3,5-三嗪、三(2,3-二溴丙基)-1,3,5-三嗪等含卤素的三嗪化合物和三(2,3-二溴丙基)异氰脲酸酯等以下述式(a103)表示的含卤素的三嗪化合物。
[0215]
【化17】
[0216][0217]
上述式(a103)中,r
109a
、r
110a
、r
111a
分别独立地表示卤代烷基。
[0218]
此外,作为产酸剂(a)中其它产酸剂的第三方案,可例举α-(对甲苯磺酰氧基亚氨基)-苯基乙腈、α-(苯磺酰氧基亚氨基)-2,4-二氯苯基乙腈、α-(苯磺酰氧基亚氨基)-2,6-二氯苯基乙腈、α-(2-氯苯磺酰氧基亚氨基)-4-甲氧基苯基乙腈、α-(乙基磺酰氧基亚氨基)-1-环戊烯基乙腈和含有肟磺酸酯基的以下述式(a104)表示的化合物。
[0219]
【化18】
[0220][0221]
上述式(a104)中,r
112a
表示1价、2价或者3价的有机基团,r
113a
表示取代或未取代的饱和烃基、不饱和烃基或者芳香族基团,n表示括号内的结构的重复单元数。
[0222]
上述式(a104)中,作为芳香族基团,可例举例如苯基、萘基等芳基或者呋喃基、噻吩基等杂芳基。它们可以在环上具有1个以上的适当的取代基,例如卤素原子、烷基、烷氧基、硝基等。另外,r
113a
特别优选碳原子数为1以上6以下的烷基,可例举甲基、乙基、丙基、丁基。特别优选r
112a
为芳香族基团、r
113a
为碳原子数为1以上4以下的烷基的化合物。
[0223]
作为以上述式(a104)表示的产酸剂,在n=1时,可例举r
112a
为苯基、甲基苯基、甲氧基苯基中的任一个,且r
113a
为甲基的化合物,具体而言,可例举α-(甲基磺酰氧基亚氨基)-1-苯基乙腈、α-(甲基磺酰氧基亚氨基)-1-(对甲基苯基)乙腈、α-(甲基磺酰氧基亚氨基)-1-(对甲氧基苯基)乙腈、〔2-(丙基磺酰氧基亚氨基)-2,3-二羟基噻吩-3-亚基〕(邻甲苯基)乙腈等。在n=2时,作为以上述式(a104)表示的产酸剂,具体而言,可例举以下述式表示的产酸剂。
[0224]
【化19】
[0225][0226]
此外,作为产酸剂(a)中的其它产酸剂的第四方案,可例举在阳离子部具有萘环的鎓盐。该“具有萘环”是指具有源自萘的结构,是指至少具有2个环的结构,并且它们的芳香族性被维持。该萘环可以具有碳原子数为1以上6以下的直链状或支链状的烷基、羟基、碳原子数为1以上6以下的直链状或支链状的烷氧基等取代基。虽然源自萘环的结构可以是1价基团(游离原子价为1),也可以是2价基团(游离原子价为2)以上,但是期望是1价基团(其中,此时去除与上述取代基键合的部分来对游离原子价进行计数)。萘环的数量优选为1以上3以下。
[0227]
作为这样的在阳离子部具有萘环的鎓盐的阳离子部,优选是以下述式(a105)表示的结构。
[0228]
【化20】
[0229][0230]
上述式(a105)中,r
114a
、r
115a
、r
116a
中的至少1个表示以下述式(a106)表示的基团,其余表示碳原子数为1以上6以下的直链状或支链状的烷基、可具有取代基的苯基、羟基、或者碳原子数为1以上6以下的直链状或支链状的烷氧基。或者,r
114a
、r
115a
、r
116a
中的1个为以下述式(a106)表示的基团,其余的2个分别独立地为碳原子数为1以上6以下的直链状或支链状的亚烷基,它们的末端可以键合而成为环状。
[0231]
【化21】
[0232][0233]
在上述式(a106)中,r
117a
、r
118a
分别独立地表示羟基、碳原子数为1以上6以下的直链状或支链状的烷氧基、或者碳原子数为1以上6以下的直链状或支链状的烷基,r
119a
表示单键或可具有取代基的碳原子数为1以上6以下的直链状或支链状的亚烷基。l及m分别独立地表示0以上2以下的整数,l m为3以下。其中,在存在多个r
117a
的情况下,它们可以彼此相同也可以不同。此外,在存在多个r
118a
的情况下,它们可以彼此相同也可以不同。
[0234]
从化合物的稳定性的方面来看,上述r
114a
、r
115a
、r
116a
中的以上述式(a106)表示的基团的数量优选为1,其余为碳原子数为1以上6以下的直链状或支链状的亚烷基,它们的末端可以键合而成为环状。在该情况下,上述2个亚烷基包含硫原子而构成三~九元环。构成环的原子(包含硫原子)的数量优选为5以上6以下。
[0235]
此外,作为上述亚烷基可以具有的取代基,可例举氧原子(在该情况下,与构成亚烷基的碳原子一起形成羰基)、羟基等。
[0236]
此外,作为苯基可以具有的取代基,可例举羟基、碳原子数为1以上6以下的直链状或支链状的烷氧基、碳原子数为1以上6以下的直链状或支链状的烷基等。
[0237]
作为适宜为这些阳离子部的结构,能够例举以下述式(a107)、(a108)表示的结构等,特别优选为以下述式(a108)表示的结构。
[0238]
【化22】
[0239][0240]
作为这样的阳离子部,可以是碘鎓盐也可以是锍盐,从产酸效率等观点来看,期望是锍盐。
[0241]
因此,作为适宜为在阳离子部具有萘环的鎓盐的阴离子部的阴离子,期望是可形成锍盐的阴离子。
[0242]
作为这样的产酸剂的阴离子部,为氢原子的一部分或者全部被氟化的氟烷基磺酸离子或芳基磺酸离子。
[0243]
氟烷基磺酸离子中的烷基可以为碳原子数为1以上20以下的直链状、支链状或环状的烷基,从所产生的酸的体积大小和其扩散距离出发,优选为碳原子数为1以上10以下。尤其是支链状或环状的烷基的扩散距离短,故优选。此外,从可廉价地进行合成的方面出发,能够例举甲基、乙基、丙基、丁基、辛基等作为优选的基团。
[0244]
芳基磺酸离子中的芳基为碳原子数为6以上20以下的芳基,可例举可以被烷基、卤素原子取代或未被取代的苯基、萘基。尤其从可廉价地合成的方面来看,优选碳原子数为6以上10以下的芳基。作为优选的芳基的具体例,能够例举苯基、甲苯磺酰基、乙基苯基、萘基、甲基萘基等。
[0245]
在上述氟烷基磺酸离子或芳基磺酸离子中,氢原子的一部分或全部被氟化时的氟化率优选为10%以上100%以下,更优选为50%以上100%以下,特别是将氢原子全部用氟原子取代而得的物质因酸的强度变强而优选。作为这样的例子,具体而言,可例举三氟甲烷磺酸根、全氟丁烷磺酸根、全氟辛烷磺酸根、全氟苯磺酸根等。
[0246]
其中,作为优选的阴离子部,可例举以下述式(a109)表示的阴离子部。
[0247]
【化23】
[0248][0249]
在上述式(a109)中,r
120a
是以下述式(a110)、(a111)及(a112)表示的基团。
[0250]
【化24】
[0251][0252]
在上述式(a110)中,x表示1以上4以下的整数。此外,在上述式(a111)中,r
121a
表示氢原子、羟基、碳原子数为1以上6以下的直链状或支链状的烷基、或者碳原子数为1以上6以下的直链状或支链状的烷氧基,y表示1以上3以下的整数。其中,从安全性的观点出发,优选是三氟甲烷磺酸根、全氟丁烷磺酸根。
[0253]
此外,作为阴离子部,也能够使用以下述式(a113)、(a114)表示的含有氮的阴离子部。
[0254]
【化25】
[0255][0256]
上述式(a113)、(a114)中,xa表示至少1个氢原子被氟原子取代而得的直链状或支链状的亚烷基,该亚烷基的碳原子数为2以上6以下,优选为3以上5以下,最优选碳原子数为
3。此外,ya、za分别独立地表示至少1个氢原子被氟原子取代而得的直链状或支链状的烷基,该烷基的碳原子数为1以上10以下,优选为1以上7以下,更优选为1以上3以下。
[0257]
xa的亚烷基的碳原子数或者ya、za的烷基的碳原子数越小,在有机溶剂中的溶解性也越良好,故优选。
[0258]
此外,在xa的亚烷基或ya、za的烷基中,被氟原子取代的氢原子的数量越多,酸的强度越强,故优选。该亚烷基或烷基中氟原子的比例即氟化率优选为70%以上100%以下,更优选为90%以上100%以下,最优选为全部的氢原子被氟原子取代而得的全氟亚烷基或全氟烷基。
[0259]
作为这样的在阳离子部具有萘环的鎓盐而优选的化合物,可例举以下述式(a115)、(a116)表示的化合物。
[0260]
【化26】
[0261][0262]
此外,作为产酸剂(a)中的其它产酸剂的第五方案,可例举双(对甲苯磺酰基)重氮甲烷、双(1,1-二甲基乙基磺酰基)重氮甲烷、双(环己基磺酰基)重氮甲烷、双(2,4-二甲基苯基磺酰基)重氮甲烷等双磺酰基重氮甲烷类;对甲苯磺酸2-硝基苄酯、对甲苯磺酸2,6-二硝基苄酯、甲苯磺酸硝基苄酯、甲苯磺酸二硝基苄酯、磺酸硝基苄酯、碳酸硝基苄酯、碳酸二硝基苄酯等硝基苄基衍生物;邻苯三酚三甲磺酸酯、邻苯三酚三甲苯磺酸酯、甲苯磺酰苄酯、磺酸苄酯、n-甲基磺酰氧基琥珀酰亚胺、n-三氯甲基磺酰氧基琥珀酰亚胺、n-苯基磺酰氧基马来酰亚胺、n-甲基磺酰氧基邻苯二甲酰亚胺等磺酸酯类;n-(三氟甲基磺酰氧基)邻苯二甲酰亚胺、n-(三氟甲基磺酰氧基)-1,8-萘二甲酰亚胺、n-(三氟甲基磺酰氧基)-4-丁基-1,8-萘二甲酰亚胺等三氟甲磺酸酯类;二苯基碘鎓六氟磷酸盐、(4-甲氧基苯基)苯基碘鎓三氟甲磺酸盐、双(对叔丁基苯基)碘鎓三氟甲磺酸盐、三苯基锍六氟磷酸盐、(4-甲氧基苯基)二苯基锍三氟甲磺酸盐、(对叔丁基苯基)二苯基锍三氟甲磺酸盐等鎓盐类;苯偶姻甲苯磺酸酯、α-甲基苯偶姻甲苯磺酸酯等苯偶姻甲苯磺酸酯类;其他二苯基碘鎓盐、三苯基锍盐、苯基重氮鎓盐、碳酸苄酯等。
[0263]
产酸剂(a)整体的含量相对于感光性树脂组合物的总固体成分量优选为0.01质量%以上20质量%以下,更优选为0.03质量%以上10质量%以下,特别优选为0.05质量%以上8质量%以下。
[0264]
此外,以上述式(a1)表示的化合物相对于感光性树脂组合物的总固体成分量优选为0.01质量%以上20质量%以下,更优选为0.03质量%以上10质量%以下,特别优选为0.05质量%以上8质量%以下。
[0265]
通过使产酸剂(a)的使用量为上述范围内,容易制备具备更良好的灵敏度、为均匀的溶液、且保存稳定性优良的感光性树脂组合物。
[0266]
以式(a1)表示的化合物对有机溶剂(s)的溶解性优异。因此,容易制成以期望的浓度包含作为产酸剂(a)的以式(a1)表示的化合物的感光性树脂组合物。
[0267]
《树脂(b)》
[0268]
作为对碱的溶解性因酸的作用而增大的树脂(b),并没有特别地限定,能够使用任意的对碱的溶解性因酸的作用而增大的树脂。其中,优选含有选自酚醛清漆树脂(b1)、聚羟基苯乙烯树脂(b2)及丙烯酸树脂(b3)构成的组中的至少1种树脂。
[0269]
[酚醛清漆树脂(b1)]
[0270]
作为酚醛清漆树脂(b1),能够使用包含以下述式(b-11)表示的结构单元的树脂。
[0271]
【化27】
[0272][0273]
上述式(b-11)中,r
1b
表示酸解离性溶解抑制基团,r
2b
、r
3b
分别独立地表示氢原子或者碳原子数为1以上6以下的烷基。
[0274]
作为以上述r
1b
表示的酸解离性溶解抑制基团,优选以下述式(b-12)、(b-13)表示的基团、碳原子数为1以上6以下的直链状、支链状或环状的烷基、乙烯基氧基乙基、四氢吡喃基、四氢呋喃基或者三烷基甲硅烷基。
[0275]
【化28】
[0276][0277]
上述式(b-12)、(b-13)中,r
4b
、r
5b
分别独立地表示氢原子、或者碳原子数为1以上6以下的直链状或支链状的烷基,r
6b
表示碳原子数为1以上10以下的直链状、支链状或环状的烷基,r
7b
表示碳原子数为1以上6以下的直链状、支链状或环状的烷基,o表示0或者1。
[0278]
作为上述直链状或支链状的烷基,可例举甲基、乙基、丙基、异丙基、正丁基、异丁基、叔丁基、戊基、异戊基、新戊基等。另外,作为上述环状的烷基,可例举环戊基、环己基等。
[0279]
在此,作为以上述式(b-12)表示的酸解离性溶解抑制基团,具体来说,可例举甲氧基乙基、乙氧基乙基、正丙氧基乙基、异丙氧基乙基、正丁氧基乙基、异丁氧基乙基、叔丁氧基乙基、环己氧基乙基、甲氧基丙基、乙氧基丙基、1-甲氧基-1-甲基-乙基、1-乙氧基-1-甲基乙基等。此外,作为以上述式(b-13)表示的酸解离性溶解抑制基团,具体来说,可例举叔丁氧基羰基、叔丁氧基羰基甲基等。此外,作为上述三烷基甲硅烷基,可例举三甲基甲硅烷基、三叔丁基二甲基甲硅烷基等各烷基的碳原子数为1以上6以下的基团。
[0280]
[聚羟基苯乙烯树脂(b2)]
[0281]
作为聚羟基苯乙烯树脂(b2),能够使用包含以下述式(b4)表示的结构单元的树脂。
[0282]
【化29】
[0283][0284]
上述式(b4)中,r
8b
表示氢原子或者碳原子数为1以上6以下的烷基,r
9b
表示酸解离性溶解抑制基团。
[0285]
上述碳原子数为1以上6以下的烷基例如为碳原子数为1以上6以下的直链状、支链状或环状的烷基。作为直链状或支链状的烷基,可例举甲基、乙基、丙基、异丙基、正丁基、异丁基、叔丁基、戊基、异戊基、新戊基等,作为环状的烷基,可例举环戊基、环己基等。
[0286]
作为上述以r
9b
表示的酸解离性溶解抑制基团,能够使用与上述式(b-12)、(b-13)中例示的酸解离性溶解抑制基团同样的酸解离性溶解抑制基团。
[0287]
进而,出于适度地控制物理、化学特性的目的,聚羟基苯乙烯树脂(b2)能够包含其他的聚合性化合物作为结构单元。作为这样的聚合性化合物,可例举公知的自由基聚合性化合物、阴离子聚合性化合物。此外,作为这样的聚合性化合物,例如能够例举丙烯酸、甲基丙烯酸、巴豆酸等一元羧酸类;马来酸、富马酸、衣康酸等二元羧酸类;2-甲基丙烯酰氧基乙基琥珀酸、2-甲基丙烯酰氧基乙基马来酸、2-甲基丙烯酰氧基乙基邻苯二甲酸、2-甲基丙烯酰氧基乙基六氢邻苯二甲酸等具有羧基及酯键的甲基丙烯酸衍生物类;(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸丁酯等(甲基)丙烯酸烷基酯类;(甲基)丙烯酸2-羟基乙酯、(甲基)丙烯酸2-羟基丙酯等(甲基)丙烯酸羟基烷基酯类;(甲基)丙烯酸苯酯、(甲基)丙烯酸苄酯等(甲基)丙烯酸芳基酯类;马来酸二乙酯、富马酸二丁酯等二元羧酸二酯类;苯乙烯、α-甲基苯乙烯、氯苯乙烯、氯甲基苯乙烯、乙烯基甲苯、羟基苯乙烯、α-甲基羟基苯乙烯、α-乙基羟基苯乙烯等含乙烯基的芳香族化合物类;乙酸乙烯酯等含乙烯基的脂肪族化合物类;丁二烯、异戊二烯等共轭二烯烃类;丙烯腈、甲基丙烯腈等含腈基的聚合性化合物类;氯乙烯、偏氯乙烯等含氯的聚合性化合物;丙烯酰胺、甲基丙烯酰胺等含酰胺键的聚合性化合物类等。
[0288]
[丙烯酸树脂(b3)]
[0289]
作为丙烯酸树脂(b3),只要是对碱的溶解性因酸的作用而增大的丙烯酸树脂、且是一直以来掺混在各种感光性树脂组合物中的丙烯酸树脂,就没有特别地限定。
[0290]
丙烯酸树脂(b3)优选为含有从包含例如含-so
2-环式基或者含内酯环式基的丙烯酸酯衍生的结构单元(b-3)。在该情况下,在形成抗蚀剂图案时,容易形成具有优选的截面形状的抗蚀剂图案。
[0291]
(含-so
2-环式基)
[0292]
在此,“含-so
2-环式基”表示在其环骨架中含有包含-so
2-的环的环式基,具体而言,为-so
2-中的硫原子(s)形成环式基的环骨架的一部分的环式基。在该环骨架中将包含-so
2-的环计作第1个环,在只有该环的情况下称为单环式基,在还具有其他环结构的情况下不论其结构如何均称为多环式基。含-so
2-环式基可以是单环式的,也可以是多环式的。
[0293]
含-so
2-环式基特别优选为在其环骨架中包含-o-so
2-的环式基,即含有-o-so
2-中
的-o-s-形成为环骨架的一部分的磺酸内酯(sultone)环的环式基。
[0294]
含-so
2-环式基的碳原子数优选为3以上30以下,更优选为4以上20以下,进一步优选为4以上15以下,特别优选为4以上12以下。该碳原子数是构成环骨架的碳原子的数量,不包含取代基中的碳原子数。
[0295]
含-so
2-环式基可以为含-so
2-的脂肪族环式基,也可以为含-so
2-的芳香族环式基。优选为含-so
2-的脂肪族环式基。
[0296]
作为含-so
2-的脂肪族环式基,可例举从构成其环骨架的碳原子的一部分被-so
2-或者-o-so
2-取代而得的脂肪族烃环中去除至少1个氢原子而得的基团。更具体而言,可例举从构成其环骨架的-ch
2-被-so
2-取代而得的脂肪族烃环中去除至少1个氢原子而得的基团、从构成其环的-ch
2-ch
2-被-o-so
2-取代而得的脂肪族烃环中去除至少1个氢原子而得的基团等。
[0297]
该脂环式烃环的碳原子数优选为3以上20以下,更优选为3以上12以下。该脂环式烃环可以是多环式的,也可以是单环式的。作为单环式的脂环式烃基,优选为从碳原子数为3以上6以下的单环烷烃中去除2个氢原子而得的基团。作为该单环烷烃,能够例示环戊烷、环己烷等。作为多环式的脂环式烃环,优选为从碳原子数为7以上12以下的多环烷烃中去除2个氢原子而得的基团,作为该多环烷烃,具体而言,可例举金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等。
[0298]
含-so
2-环式基可以具有取代基。作为该取代基,可例举例如烷基、烷氧基、卤素原子、卤代烷基、羟基、氧原子(=o)、-coor”、-oc(=o)r”、羟基烷基、氰基等。
[0299]
作为该取代基的烷基,优选碳原子数为1以上6以下的烷基。该烷基优选为直链状或支链状。具体而言,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、正戊基、异戊基、新戊基、正己基等。这些之中,优选为甲基或者乙基,特别优选为甲基。
[0300]
作为该取代基的烷氧基,优选碳原子数为1以上6以下的烷氧基。该烷氧基优选为直链状或支链状。具体而言,可例举作为上述取代基的烷基所例举的烷基与氧原子(-o-)键合而得的基团。
[0301]
作为该取代基的卤素原子,可例举氟原子、氯原子、溴原子、碘原子等,优选氟原子。
[0302]
作为该取代基的卤代烷基,可例举上述烷基的一部分或全部的氢原子被上述卤素原子取代而得的基团。
[0303]
作为该取代基的卤代烷基,可例举作为上述取代基的烷基所例举的烷基的一部分或全部的氢原子被上述卤素原子取代而得的基团。作为该卤代烷基,优选为氟代烷基,特别优选为全氟烷基。
[0304]
上述的-coor”、-oc(=o)r”中的r”均为氢原子或者碳原子数为1以上15以下的直链状、支链状或环状的烷基。
[0305]
在r”为直链状或支链状的烷基的情况下,该链状的烷基的碳原子数优选为1以上10以下,更优选为1以上5以下,特别优选为1或者2。
[0306]
在r”为环状的烷基的情况下,该环状的烷基的碳原子数优选为3以上15以下,更优选为4以上12以下,特别优选为5以上10以下。具体而言,能够例示从可被氟原子或氟代烷基取代或者未被取代的单环烷烃中、或者从双环烷烃、三环烷烃、四环烷烃等多环烷烃中去除
1个以上氢原子而得的基团等。更具体而言,可例举从环戊烷、环己烷等单环烷烃中或者从金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等多环烷烃中去除1个以上氢原子而得的基团等。
[0307]
作为该取代基的羟基烷基,优选碳原子数为1以上6以下的羟基烷基。具体而言,可例举作为上述取代基的烷基所例举的烷基的至少1个氢原子被羟基取代而得的基团。
[0308]
作为含-so
2-环式基,更具体而言,可例举以下述式(3-1)~(3-4)表示的基团。
[0309]
【化30】
[0310][0311]
(式中,a’为可以含有氧原子或硫原子的碳原子数为1以上5以下的亚烷基、氧原子或者硫原子,z为0以上2以下的整数,r
10b
为烷基、烷氧基、卤代烷基、羟基、-coor”、-oc(=o)r”、羟基烷基或者氰基,r”为氢原子或者烷基。)
[0312]
在上述式(3-1)~(3-4)中,a’为可以含有氧原子(-o-)或硫原子(-s-)的碳原子数为1以上5以下的亚烷基、氧原子或者硫原子。作为a’中的碳原子数为1以上5以下的亚烷基,优选为直链状或支链状的亚烷基,可例举亚甲基、亚乙基、正亚丙基、异亚丙基等。
[0313]
在该亚烷基包含氧原子或硫原子的情况下,作为其具体例,可例举在所述亚烷基的末端或碳原子间介有-o-或-s-的基团,例如可例举-o-ch
2-、-ch
2-o-ch
2-、-s-ch
2-、-ch
2-s-ch
2-等。作为a’,优选碳原子数为1以上5以下的亚烷基或者-o-,更优选碳原子数为1以上5以下的亚烷基,最优选亚甲基。
[0314]
z可以是0、1及2中的任一个,最优选为0。在z是2的情况下,多个r
10b
可以分别相同也可以不同。
[0315]
作为r
10b
中的烷基、烷氧基、卤代烷基、-coor”、-oc(=o)r”、羟基烷基,可分别例举与上述说明的作为含-so
2-环式基可以具有的取代基而例举的烷基、烷氧基、卤代烷基、-coor”、-oc(=o)r”及羟基烷基同样的基团。
[0316]
以下,例示以上述式(3-1)~(3-4)表示的具体的环式基。另外,式中的“ac”表示乙酰基。
[0317]
【化31】
[0318][0319]
【化32】
[0320][0321]
作为含-so
2-环式基,优选为在上述中以所述式(3-1)表示的基团,更优选为从以所述化学式(3-1-1)、(3-1-18)、(3-3-1)及(3-4-1)中的任一个表示的基团构成的组中选择的至少1种,最优选为以所述化学式(3-1-1)表示的基团。
[0322]
(含内酯环式基)
[0323]“含内酯环式基”表示在其环骨架中含有含-o-c(=o)-的环(内酯环)的环式基。将内酯环记作第一个环,在仅有内酯环的情况下称为单环式基,在还具有其它环结构的情况下,无论其结构如何均称为多环式基。含内酯环式基可以为单环式基,也可以为多环式基。
[0324]
作为结构单元(b-3)中的含内酯环式基,没有特别限定,可使用任意的含内酯环式基。具体而言,作为含内酯单环式基,可例举从四~六元环内酯中去除1个氢原子而得的基团,例如从β-丙内酯中去除1个氢原子而得的基团、从γ-丁内酯中去除1个氢原子而得的基团、从δ-戊内酯中去除1个氢原子而得的基团等。此外,作为含内酯多环式基,可例举从具有内酯环的双环烷烃、三环烷烃、四环烷烃中去除1个氢原子而得的基团。
[0325]
作为结构单元(b-3),只要是具有含-so
2-环式基或含内酯环式基的结构单元,则其他部分的结构并无特别地限定,优选从作为从与α位的碳原子键合的氢原子可以被取代基取代的丙烯酸酯衍生的结构单元的、包含含-so
2-环式基的结构单元(b-3-s)及作为从与
α位的碳原子键合的氢原子可以被取代基取代的丙烯酸酯衍生的结构单元的、包含含内酯环式基的结构单元(b-3-l)构成的组中选择的至少1种结构单元。
[0326]
〔结构单元(b-3-s)〕
[0327]
作为结构单元(b-3-s)的例子,更具体而言,可例举以下述式(b-s1)表示的结构单元。
[0328]
【化33】
[0329][0330]
(式中,r为氢原子、碳原子数为1以上5以下的烷基或者碳原子数为1以上5以下的卤代烷基,r
11b
为含-so
2-环式基,r
12b
为单键或者2价的连接基团。)
[0331]
式(b-s1)中,r与上述相同。
[0332]r11b
与上述例举的含-so
2-环式基相同。
[0333]r12b
可以是单键、2价的连接基团中的任一种。从使本发明的效果优异的观点来看,优选为2价的连接基团。
[0334]
作为r
12b
中的2价的连接基团,没有特别地限定,作为优选的例子,可例举可具有取代基的2价烃基、含杂原子的2价的连接基团等。
[0335]
·
可具有取代基的2价烃基
[0336]
作为2价的连接基团的烃基,可以是脂肪族烃基,也可以是芳香族烃基。脂肪族烃基表示不具有芳香族性的烃基。该脂肪族烃基可以是饱和的,也可以是不饱和的。通常优选为饱和烃基。作为该脂肪族烃基,更具体而言,可例举直链状或支链状的脂肪族烃基、在结构中含环的脂肪族烃基等。
[0337]
上述直链状或支链状的脂肪族烃基的碳原子数优选为1以上10以下,更优选为1以上8以下,进一步优选为1以上5以下。
[0338]
作为直链状的脂肪族烃基,优选为直链状的亚烷基。具体而言,可例举亚甲基[-ch
2-]、亚乙基[-(ch2)
2-]、亚丙基[-(ch2)
3-]、亚丁基[-(ch2)
4-]、亚戊基[-(ch2)
5-]等。
[0339]
作为支链状的脂肪族烃基,优选为支链状的亚烷基。具体而言,可例举-ch(ch3)-、-ch(ch2ch3)-、-c(ch3)
2-、-c(ch3)(ch2ch3)-、-c(ch3)(ch2ch2ch3)-、-c(ch2ch3)
2-等烷基亚甲基;-ch(ch3)ch
2-、-ch(ch3)ch(ch3)-、-c(ch3)2ch
2-、-ch(ch2ch3)ch
2-、-c(ch2ch3)
2-ch
2-等烷基亚乙基;-ch(ch3)ch2ch
2-、-ch2ch(ch3)ch
2-等烷基亚丙基;-ch(ch3)ch2ch2ch
2-、-ch2ch(ch3)ch2ch
2-等烷基亚丁基等烷基亚烷基等。作为烷基亚烷基中的烷基,优选碳原子数为1以上5以下的直链状的烷基。
[0340]
上述的直链状或支链状的脂肪族烃基可以具有取代氢原子的取代基(氢原子以外的基团或者原子),也可以不具有取代基。作为该取代基,可例举氟原子、被氟原子取代而得的碳原子数为1以上5以下的氟代烷基、氧代基(=o)等。
[0341]
作为上述的在结构中含环的脂肪族烃基,可例举在环结构中含杂原子的可含取代
基的环状的脂肪族烃基(从脂肪族烃环中去除2个氢原子而得的基团)、该环状的脂肪族烃基与直链状或支链状的脂肪族烃基的末端键合而得的基团、该环状的脂肪族烃基介于直链状或支链状的脂肪族烃基之间的基团等。作为上述的直链状或支链状的脂肪族烃基,可例举与上述相同的基团。
[0342]
环状的脂肪族烃基的碳原子数优选为3以上20以下,更优选为3以上12以下。
[0343]
环状的脂肪族烃基可以是多环式的,也可以是单环式的。作为单环式的脂肪族烃基,优选从单环烷烃中去除2个氢原子而得的基团。该单环烷烃的碳原子数优选为3以上6以下。具体而言,可例举环戊烷、环己烷等。作为多环式的脂肪族烃基,优选从多环烷烃中去除2个氢原子而得的基团。该多环烷烃的碳原子数优选为7以上12以下。具体而言,可例举金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等。
[0344]
环状的脂肪族烃基可以具有取代氢原子的取代基(氢原子以外的基团或者原子),也可以不具有取代基。作为该取代基,可例举烷基、烷氧基、卤素原子、卤代烷基、羟基、氧代基(=o)等。
[0345]
作为上述取代基的烷基,优选碳原子数为1以上5以下的烷基,更优选甲基、乙基、丙基、正丁基及叔丁基。
[0346]
作为上述取代基的烷氧基,优选碳原子数为1以上5以下的烷氧基,更优选甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基及叔丁氧基,特别优选甲氧基及乙氧基。
[0347]
作为上述取代基的卤素原子,可例举氟原子、氯原子、溴原子及碘原子等,优选为氟原子。
[0348]
作为上述取代基的卤代烷基,可例举上述烷基的一部分或全部的氢原子被上述卤素原子取代而得的基团。
[0349]
环状的脂肪族烃基中,构成其环结构的碳原子的一部分可以被-o-或者-s-取代。作为该含杂原子的取代基,优选-o-、-c(=o)-o-、-s-、-s(=o)
2-、-s(=o)
2-o-。
[0350]
作为2价烃基的芳香族烃基,为具有至少1个芳香环的2价烃基,可以具有取代基。芳香环只要是具有4n 2个π电子的环状共轭体系则没有特别地限定,可以是单环式,也可以是多环式。芳香环的碳原子数优选为5以上30以下,更优选为5以上20以下,进一步优选为6以上15以下,特别优选为6以上12以下。其中,该碳原子数不包含取代基的碳原子数。
[0351]
作为芳香环,具体来说,可例举苯、萘、蒽及菲等芳香族烃环;构成所述芳香族烃环的碳原子的一部分被杂原子取代而得的芳香族杂环等。作为芳香族杂环中的杂原子,可例举氧原子、硫原子、氮原子等。作为芳香族杂环,具体来说,可例举吡啶环、噻吩环等。
[0352]
作为2价烃基的芳香族烃基,具体而言,可例举从上述芳香族烃环或芳香族杂环中去除2个氢原子而得的基团(亚芳基或者亚杂芳基);从包含2个以上的芳香环的芳香族化合物(例如联苯、芴等)中去除2个氢原子而得的基团;从上述芳香族烃环或芳香族杂环中去除1个氢原子而得的基团(芳基或者杂芳基)的1个氢原子被亚烷基取代而得的基团(例如从苄基、苯乙基、1-萘基甲基、2-萘基甲基、1-萘基乙基、2-萘基乙基等芳基烷基中的芳基中进一步去除1个氢原子而得的基团)等。
[0353]
与上述芳基或者杂芳基键合的亚烷基的碳原子数优选为1以上4以下,更优选为1以上2以下,特别优选为1。
[0354]
在上述的芳香族烃基中,该芳香族烃基所具有的氢原子可以被取代基取代。例如,
该芳香族烃基中与芳香环键合的氢原子可以被取代基取代。作为该取代基,例如可例举烷基、烷氧基、卤素原子、卤代烷基、羟基、氧代基(=o)等。
[0355]
作为上述取代基的烷基,优选碳原子数为1以上5以下的烷基,更优选甲基、乙基、正丙基、正丁基及叔丁基。
[0356]
作为上述取代基的烷氧基,优选碳原子数为1以上5以下的烷氧基,且优选甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基及叔丁氧基,更优选甲氧基及乙氧基。
[0357]
作为上述取代基的卤素原子可例举氟原子、氯原子、溴原子、碘原子等,优选氟原子。
[0358]
作为上述取代基的卤代烷基,可例举上述烷基的一部分或全部的氢原子被所述卤素原子取代而得的基团。
[0359]
·
含杂原子的2价的连接基团
[0360]
含杂原子的2价的连接基团中的杂原子是指碳原子及氢原子以外的原子,例如可例举氧原子、氮原子、硫原子及卤素原子等。
[0361]
作为含杂原子的2价的连接基团,具体而言,可例举-o-、-c(=o)-、-c(=o)-o-、-o-c(=o)-o-、-s-、-s(=o)
2-、-s(=o)
2-o-、-nh-、-nh-c(=o)-、-nh-c(=nh)-、=n-等非烃类连接基团、这些非烃类连接基团中的至少1种与2价烃基的组合等。作为该2价烃基,可例举与上述可具有取代基的2价烃基相同的基团,优选为直链状或支链状的脂肪族烃基。
[0362]
上述中,-c(=o)-nh-中的-nh-、-nh-、-nh-c(=nh)-中的h可以分别被烷基、酰基等取代基取代。该取代基的碳原子数优选为1以上10以下,更优选为1以上8以下,特别优选为1以上5以下。
[0363]
作为r
12b
中的2价的连接基团,特别优选为直链状或支链状的亚烷基、环状的脂肪族烃基或者含杂原子的2价的连接基团。
[0364]
在r
12b
中的2价的连接基团为直链状或支链状亚烷基的情况下,该亚烷基的碳原子数优选为1以上10以下,更优选为1以上6以下,特别优选为1以上4以下,最优选为1以上3以下。具体而言,可例举与在作为所述2价的连接基团的“可具有取代基的2价烃基”的说明中、作为直链状或支链状的脂肪族烃基而例举的直链状的亚烷基、支链状的亚烷基相同的基团。
[0365]
在r
12b
中的2价的连接基团为环状的脂肪族烃基的情况下,作为该环状的脂肪族烃基,可例举与在作为所述2价的连接基团的“可具有取代基的2价烃基”的说明中、作为“在结构中含环的脂肪族烃基”而例举的环状的脂肪族烃基相同的基团。
[0366]
作为该环状的脂肪族烃基,特别优选为从环戊烷、环己烷、降冰片烷、异冰片烷、金刚烷、三环癸烷或者四环十二烷中去除两个以上氢原子而得的基团。
[0367]
在r
12b
中的2价的连接基团为含杂原子的2价的连接基团的情况下,就作为该连接基团而优选的例子而言,可例举-o-、-c(=o)-o-、-c(=o)-、-o-c(=o)-o-、-c(=o)-nh-、-nh-(h可以被烷基、酰基等取代基取代)、-s-、-s(=o)
2-、-s(=o)
2-o-、以通式-y
1b-o-y
2b-、-[y
1b-c(=o)-o]m’-y
2b-或者-y
1b-o-c(=o)-y
2b-表示的基团[式中,y
1b
及y
2b
分别独立地为可具有取代基的2价烃基,o为氧原子,m’为0以上3以下的整数]等。
[0368]
在r
12b
中的2价的连接基团为-nh-的情况下,-nh-中的氢原子可被烷基、酰基等取代基取代。该取代基(烷基、酰基等)的碳原子数优选为1以上10以下,更优选为1以上8以下,
特别优选为1以上5以下。
[0369]
式-y
1b-o-y
2b-、-[y
1b-c(=o)-o]m’-y
2b-或者-y
1b-o-c(=o)-y
2b-中,y
1b
及y
2b
分别独立地为可具有取代基的2价烃基。作为该2价烃基,可例举与作为所述2价的连接基团的说明中所例举的“可具有取代基的2价烃基”相同的基团。
[0370]
作为y
1b
,优选直链状的脂肪族烃基,更优选直链状的亚烷基,更优选碳原子数为1以上5以下的直链状的亚烷基,特别优选亚甲基及亚乙基。
[0371]
作为y
2b
,优选直链状或支链状的脂肪族烃基,更优选亚甲基、亚乙基及烷基亚甲基。该烷基亚甲基中的烷基优选碳原子数为1以上5以下的直链状的烷基,更优选碳原子数为1以上3以下的直链状的烷基,特别优选甲基。
[0372]
在以式-[y
1b-c(=o)-o]m’-y
2b-表示的基团中,m’为0以上3以下的整数,优选为0以上2以下的整数,更优选为0或者1,特别优选为1。即,作为以式-[y
1b-c(=o)-o]m’-y
2b-表示的基团,特别优选以式-y
1b-c(=o)-o-y
2b-表示的基团。其中,优选以式-(ch2)a’-c(=o)-o-(ch2)b’-表示的基团。该式中,a’为1以上10以下的整数,优选为1以上8以下的整数,更优选为1以上5以下的整数,进一步优选为1或2,最优选为1。b’为1以上10以下的整数,优选为1以上8以下的整数,更优选为1以上5以下的整数,进一步优选为1或者2,最优选为1。
[0373]
对于r
12b
中的2价的连接基团,作为含杂原子的2价的连接基团,优选由至少1种非烃基与2价烃基的组合构成的有机基团。其中,优选具有氧原子作为杂原子的直链状的基团例如包含醚键或者酯键的基团,更优选以所述的式-y
1b-o-y
2b-、-[y
1b-c(=o)-o]m’-y
2b-或者-y
1b-o-c(=o)-y
2b-表示的基团,特别优选以所述的式-[y
1b-c(=o)-o]m’-y
2b-或者-y
1b-o-c(=o)-y
2b-表示的基团。
[0374]
作为r
12b
中的2价的连接基团,优选亚烷基或者包含酯键(-c(=o)-o-)的2价的连接基团。
[0375]
该亚烷基优选为直链状或支链状的亚烷基。作为该直链状的脂肪族烃基的优选例,可例举亚甲基[-ch
2-]、亚乙基[-(ch2)
2-]、亚丙基[-(ch2)
3-]、亚丁基[-(ch2)
4-]及亚戊基[-(ch2)
5-]等。作为该支链状的亚烷基的优选例,可例举-ch(ch3)-、-ch(ch2ch3)-、-c(ch3)
2-、-c(ch3)(ch2ch3)-、-c(ch3)(ch2ch2ch3)-、-c(ch2ch3)
2-等烷基亚甲基;-ch(ch3)ch
2-、-ch(ch3)ch(ch3)-、-c(ch3)2ch
2-、-ch(ch2ch3)ch
2-、-c(ch2ch3)
2-ch
2-等烷基亚乙基;-ch(ch3)ch2ch
2-、-ch2ch(ch3)ch
2-等烷基亚丙基;-ch(ch3)ch2ch2ch
2-、-ch2ch(ch3)ch2ch
2-等烷基亚丁基等烷基亚烷基等。
[0376]
作为包含酯键的2价的连接基团,特别优选以式:-r
13b-c(=o)-o-[式中,r
13b
为2价的连接基团]表示的基团。即,结构单元(b-3-s)优选为以下述式(b-s1-1)表示的结构单元。
[0377]
【化34】
[0378]
[0379]
(式中,r及r
11b
分别与上述相同,r
13b
是2价的连接基团。)
[0380]
作为r
13b
,并无特别地限定,例如可例举与所述的r
12b
中的2价的连接基团相同的基团。
[0381]
作为r
13b
的2价的连接基团,优选为直链状或支链状的亚烷基、在结构中含环的脂肪族烃基、或者含杂原子的2价的连接基团,更优选为直链状或支链状的亚烷基或者包含氧原子作为杂原子的2价的连接基团。
[0382]
作为直链状的亚烷基,优选为亚甲基或者亚乙基,特别优选为亚甲基。作为支链状的亚烷基,优选为烷基亚甲基或者烷基亚乙基,特别优选为-ch(ch3)-、-c(ch3)
2-或者-c(ch3)2ch
2-。
[0383]
作为包含氧原子的2价的连接基团,优选包含醚键或者酯键的2价的连接基团,更优选所述的-y
1b-o-y
2b-、-[y
1b-c(=o)-o]m’-y
2b-或者-y
1b-o-c(=o)-y
2b-。y
1b
及y
2b
分别独立地为可具有取代基的2价烃基,m’为0以上3以下的整数。其中,优选-y
1b-o-c(=o)-y
2b-,特别优选以-(ch2)
c-o-c(=o)-(ch2)
d-表示的基团。c为1以上5以下的整数,优选为1或2。d为1以上5以下的整数,优选为1或2。
[0384]
作为结构单元(b-3-s),特别地,优选为以下述式(b-s1-11)或者(b-s1-12)表示的结构单元,更优选为以式(b-s1-12)表示的结构单元。
[0385]
【化35】
[0386][0387]
(式中,r、a’、r
10b
、z及r
13b
分别与上述相同。)
[0388]
式(b-s1-11)中,a’优选为亚甲基、氧原子(-o-)或者硫原子(-s-)。
[0389]
作为r
13b
,优选为直链状或支链状的亚烷基或者包含氧原子的2价的连接基团。作为r
13b
中的直链状或支链状的亚烷基、包含氧原子的2价的连接基团,可分别例举与所述的直链状或支链状的亚烷基、包含氧原子的2价的连接基团相同的基团。
[0390]
作为以式(b-s1-12)表示的结构单元,特别地,优选为以下述式(b-s1-12a)或者(b-s1-12b)表示的结构单元。
[0391]
【化36】
[0392][0393]
(式中,r及a’分别与上述相同,c~e分别独立地为1以上3以下的整数。)
[0394]
〔结构单元(b-3-l)〕
[0395]
作为结构单元(b-3-l)的例子,例如可例举将所述的式(b-s1)中的r
11b
以含内酯环式基进行取代而得的结构单元,更具体而言,可例举以下述式(b-l1)~(b-l5)表示的结构单元。
[0396]
【化37】
[0397][0398]
(式中,r为氢原子、碳原子数为1以上5以下的烷基或者碳原子数为1以上5以下的卤代烷基;r’分别独立地为氢原子、烷基、烷氧基、卤代烷基、羟基、-coor”、-oc(=o)r”、羟基烷基或者氰基,r”为氢原子或者烷基;r
12b
为单键或者2价的连接基团,s”为0以上2以下的整数;a”为可以含有氧原子或硫原子的碳原子数为1以上5以下的亚烷基、氧原子或者硫原子;r为0或者1。)
[0399]
式(b-l1)~(b-l5)中的r与上述相同。
[0400]
作为r’中的烷基、烷氧基、卤代烷基、-coor”、-oc(=o)r”、羟基烷基,可分别例举与作为含-so
2-环式基可以具有的取代基所例举的有关烷基、烷氧基、卤代烷基、-coor”、-oc(=o)r”、羟基烷基的前述说明的基团相同的基团。
[0401]
若考虑工业上容易获得等,则r’优选为氢原子。
[0402]
r”中的烷基可以为直链状、支链状、环状的任一种。
[0403]
在r”为直链状或支链状的烷基的情况下,优选碳原子数为1以上10以下,进一步优
选碳原子数为1以上5以下。
[0404]
在r”为环状的烷基的情况下,优选碳原子数为3以上15以下,进一步优选碳原子数为4以上12以下,最优选碳原子数为5以上10以下。具体而言,能够例示从可被氟原子或氟代烷基取代或者未被取代的单环烷烃中、或者从双环烷烃、三环烷烃、四环烷烃等多环烷烃中去除1个以上的氢原子而得的基团等。具体而言,可例举从环戊烷、环己烷等单环烷烃中或者从金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等多环烷烃中去除1个以上的氢原子而得的基团等。
[0405]
作为a”,可例举与所述的式(3-1)中的a’相同的基团。a”优选碳原子数为1以上5以下的亚烷基、氧原子(-o-)或者硫原子(-s-),更优选碳原子数为1以上5以下的亚烷基或者-o-。作为碳原子数为1以上5以下的亚烷基,更优选为亚甲基或者二甲基亚甲基,最优选为亚甲基。
[0406]r12b
与所述式(b-s1)中的r
12b
相同。
[0407]
式(b-l1)中,s”优选为1或者2。
[0408]
以下,对以所述式(b-l1)~(b-l3)表示的结构单元的具体例进行例示。以下的各式中,r
α
表示氢原子、甲基或者三氟甲基。
[0409]
【化38】
[0410][0411]
【化39】
[0412][0413]
【化40】
[0414][0415]
作为结构单元(b-3-l),优选从以所述的式(b-l1)~(b-l5)表示的结构单元构成的组中选择的至少1种,更优选从以式(b-l1)~(b-l3)表示的结构单元构成的组中选择的至少1种,特别优选从以所述的式(b-l1)或者(b-l3)表示的结构单元构成的组中选择的至少1种。
[0416]
其中,优选从以所述的式(b-l1-1)、(b-l1-2)、(b-l2-1)、(b-l2-7)、(b-l2-12)、(b-l2-14)、(b-l3-1)及(b-l3-5)表示的结构单元构成的组中选择的至少1种。
[0417]
此外,作为结构单元(b-3-l),还优选为以下述式(b-l6)~(b-l7)表示的结构单元。
[0418]
【化41】
[0419][0420]
式(b-l6)及(b-l7)中,r及r
12b
与上述相同。
[0421]
此外,丙烯酸树脂(b3)中,作为因酸的作用使丙烯酸树脂(b3)对碱的溶解性提高的结构单元,包括具有酸解离性基团的以下述式(b5)~(b7)表示的结构单元。
[0422]
【化42】
[0423][0424]
上述式(b5)~(b7)中,r
14b
及r
18b
~r
23b
分别独立地表示氢原子、碳原子数为1以上6以下的直链状或支链状的烷基、氟原子、或者碳原子数为1以上6以下的直链状或支链状的氟代烷基,r
15b
~r
17b
分别独立地表示碳原子数为1以上6以下的直链状或支链状的烷基、碳原子数为1以上6以下的直链状或支链状的氟代烷基、或者碳原子数为5以上20以下的脂肪族环式基,分别独立地表示碳原子数为1以上6以下的直链状或支链状的烷基、或者碳原子数为1以上6以下的直链状或支链状的氟代烷基,r
16b
及r
17b
可以相互键合而与两者所键合的碳原子一起形成碳原子数为5以上20以下的烃环,yb表示可以具有取代基的脂肪族环式基或烷基,p表示0以上4以下的整数,q表示0或者1。
[0425]
另外,作为上述直链状或支链状的烷基,可例举甲基、乙基、丙基、异丙基、正丁基、异丁基、叔丁基、戊基、异戊基、新戊基等。此外,氟代烷基是指,上述烷基的一部分或全部的氢原子被氟原子取代而得的基团。
[0426]
作为脂肪族环式基的具体例,可例举从单环烷烃中或者从双环烷烃、三环烷烃、四环烷烃等多环烷烃中去除1个以上的氢原子而得的基团。具体而言,可例举从环戊烷、环己
烷、环庚烷、环辛烷等单环烷烃中或从金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等多环烷烃中去除1个氢原子而得的基团。特别地,优选从环己烷、金刚烷中去除1个氢原子而得的基团(可以进一步具有取代基)。
[0427]
在上述r
16b
及r
17b
未相互键合形成烃环的情况下,从高对比度、分辨率、焦深宽度等良好的观点来看,作为上述r
15b
、r
16b
及r
17b
,优选碳原子数为2以上4以下的直链状或支链状的烷基。作为上述r
19b
、r
20b
、r
22b
、r
23b
,优选为氢原子或者甲基。
[0428]
上述r
16b
及r
17b
也可以与两者所键合的碳原子一起形成碳原子数为5以上20以下的脂肪族环式基。作为这样的脂肪族环式基的具体例,可例举从单环烷烃中或者从双环烷烃、三环烷烃、四环烷烃等多环烷烃中去除1个以上的氢原子而得的基团。具体而言,可例举从环戊烷、环己烷、环庚烷、环辛烷等单环烷烃中或从金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等多环烷烃中去除1个以上的氢原子而得的基团。特别地,优选为从环己烷、金刚烷中去除1个以上的氢原子而得的基团(可以进一步具有取代基)。
[0429]
进而,在上述r
16b
及r
17b
形成的脂肪族环式基在其环骨架上具有取代基的情况下,作为该取代基的例子,可例举羟基、羧基、氰基、氧原子(=o)等极性基团或者碳原子数为1以上4以下的直链状或支链状的烷基。作为极性基团,特别优选为氧原子(=o)。
[0430]
上述yb为脂肪族环式基或者烷基,可例举从单环烷烃中或者从双环烷烃、三环烷烃、四环烷烃等多环烷烃中去除1个以上的氢原子而得的基团等。具体而言,可例举从环戊烷、环己烷、环庚烷、环辛烷等单环烷烃中或从金刚烷、降冰片烷、异冰片烷、三环癸烷、四环十二烷等多环烷烃中去除1个以上的氢原子而得的基团等。特别优选从金刚烷中去除1个以上的氢原子而得的基团(可以进一步具有取代基)。
[0431]
进而,在上述yb的脂肪族环式基在其环骨架上具有取代基的情况下,作为该取代基的例子,可例举羟基、羧基、氰基、氧原子(=o)等极性基团或者碳原子数为1以上4以下的直链状或支链状的烷基。作为极性基团,特别优选为氧原子(=o)。
[0432]
此外,在yb为烷基的情况下,优选碳原子数为1以上20以下、优选为6以上15以下的直链状或支链状的烷基。这样的烷基特别优选为烷氧基烷基,作为这样的烷氧基烷基,可例举1-甲氧基乙基、1-乙氧基乙基、1-正丙氧基乙基、1-异丙氧基乙基、1-正丁氧基乙基、1-异丁氧基乙基、1-叔丁氧基乙基、1-甲氧基丙基、1-乙氧基丙基、1-甲氧基-1-甲基-乙基、1-乙氧基-1-甲基乙基等。
[0433]
作为以上述式(b5)表示的结构单元的优选的具体例,能够例举以下述式(b5-1)~(b5-33)表示的结构单元。
[0434]
【化43】
[0435][0436]
上述式(b5-1)~(b5-33)中,r
24b
表示氢原子或者甲基。
[0437]
作为以上述式(b6)表示的结构单元的优选的具体例,能够例举以下述式(b6-1)~(b6-26)表示的结构单元。
[0438]
【化44】
[0439][0440]
上述式(b6-1)~(b6-26)中,r
24b
表示氢原子或者甲基。
[0441]
作为以上述式(b7)表示的结构单元的优选的具体例,能够例举以下述式(b7-1)~(b7-15)表示的结构单元。
[0442]
【化45】
[0443][0444]
上述式(b7-1)~(b7-15)中,r
24b
表示氢原子或者甲基。
[0445]
在以上说明的以式(b5)~(b7)表示的结构单元中,从容易合成且比较容易高灵敏度化的观点来看,优选为以式(b6)表示的结构单元。此外,在以式(b6)表示的结构单元中,优选yb是烷基的结构单元,且优选r
19b
及r
20b
中的一方或者双方是烷基的结构单元。
[0446]
进而,丙烯酸树脂(b3)优选为由包含以上述式(b5)~(b7)表示的结构单元并且包含从具有醚键的聚合性化合物衍生的结构单元的共聚物构成的树脂。
[0447]
作为上述的具有醚键的聚合性化合物,能够例示具有醚键及酯键的(甲基)丙烯酸衍生物等自由基聚合性化合物,作为具体例,可例举(甲基)丙烯酸2-甲氧基乙酯、(甲基)丙烯酸2-乙氧基乙酯、甲氧基三乙二醇(甲基)丙烯酸酯、(甲基)丙烯酸3-甲氧基丁酯、乙基卡必醇(甲基)丙烯酸酯、苯氧基聚乙二醇(甲基)丙烯酸酯、甲氧基聚乙二醇(甲基)丙烯酸酯、甲氧基聚丙二醇(甲基)丙烯酸酯、(甲基)丙烯酸四氢糠酯等。此外,上述具有醚键的聚合性化合物优选为(甲基)丙烯酸2-甲氧基乙酯、(甲基)丙烯酸2-乙氧基乙酯、甲氧基三乙二醇(甲基)丙烯酸酯。这些聚合性化合物可以单独使用,也可以将2种以上组合使用。
[0448]
进而,出于适度地控制物理、化学特性的目的,在丙烯酸树脂(b3)中,能够包含其他的聚合性化合物作为结构单元。作为这样的聚合性化合物,可例举公知的自由基聚合性化合物、阴离子聚合性化合物。
[0449]
作为这样的聚合性化合物,例如能够例举以下化合物等:丙烯酸、甲基丙烯酸、巴豆酸等一元羧酸类;马来酸、富马酸、衣康酸等二元羧酸类;2-甲基丙烯酰氧基乙基琥珀酸、2-甲基丙烯酰氧基乙基马来酸、2-甲基丙烯酰氧基乙基邻苯二甲酸、2-甲基丙烯酰氧基乙基六氢邻苯二甲酸等具有羧基及酯键的甲基丙烯酸衍生物类;(甲基)丙烯酸甲酯、(甲基)
丙烯酸乙酯、(甲基)丙烯酸丁酯、(甲基)丙烯酸环己酯等(甲基)丙烯酸烷基酯类;(甲基)丙烯酸2-羟基乙酯、(甲基)丙烯酸2-羟基丙酯等(甲基)丙烯酸羟基烷基酯类;(甲基)丙烯酸苯酯、(甲基)丙烯酸苄酯等(甲基)丙烯酸芳基酯类;马来酸二乙酯、富马酸二丁酯等二元羧酸二酯类;苯乙烯、α-甲基苯乙烯、氯苯乙烯、氯甲基苯乙烯、乙烯基甲苯、羟基苯乙烯、α-甲基羟基苯乙烯、α-乙基羟基苯乙烯等含乙烯基的芳香族化合物类;乙酸乙烯酯等含乙烯基的脂肪族化合物类;丁二烯、异戊二烯等共轭二烯烃类;丙烯腈、甲基丙烯腈等含腈基的聚合性化合物类;氯乙烯、偏氯乙烯等含氯的聚合性化合物;丙烯酰胺、甲基丙烯酰胺等含酰胺键的聚合性化合物类。
[0450]
如上所述,丙烯酸树脂(b3)也可以包含源自具有上述一元羧酸类或二元羧酸类这样的羧基的聚合性化合物的结构单元。然而,从容易形成包括截面形状为良好的矩形的非抗蚀剂部的抗蚀剂图案的观点来看,丙烯酸树脂(b3)优选为实质上不包含源自具有羧基的聚合性化合物的结构单元。具体而言,丙烯酸树脂(b3)中的源自具有羧基的聚合性化合物的结构单元的比率优选为20质量%以下,更优选为15质量%以下,特别优选为5质量%以下。
[0451]
在丙烯酸树脂(b3)中,优选为,包含较多量的源自具有羧基的聚合性化合物的结构单元的丙烯酸树脂与仅包含少量或者不包含源自具有羧基的聚合性化合物的结构单元的丙烯酸树脂并用。
[0452]
此外,作为聚合性化合物,能够例举具有酸非解离性的脂肪族多环式基的(甲基)丙烯酸酯类、含乙烯基的芳香族化合物类等。从工业上容易获得等观点来看,作为酸非解离性的脂肪族多环式基,特别优选为三环癸基、金刚烷基、四环十二烷基、异冰片基、降冰片基等。这些脂肪族多环式基可以具有碳原子数为1以上5以下的直链状或支链状的烷基作为取代基。
[0453]
作为具有酸非解离性的脂肪族多环式基的(甲基)丙烯酸酯类,具体而言,能够例示下述式(b8-1)~(b8-5)的结构的化合物。
[0454]
【化46】
[0455][0456]
上述式(b8-1)~(b8-5)中,r
25b
表示氢原子或者甲基。
[0457]
在丙烯酸树脂(b3)包含含有含-so
2-环式基或者含内酯环式基的结构单元(b-3)的情况下,丙烯酸树脂(b3)中的结构单元(b-3)的含量优选为5质量%以上,更优选为10质量%以上,特别优选为10质量%以上50质量%以下,最优选为10质量%以上30质量%以下。感光性树脂组合物在包含上述范围内的量的结构单元(b-3)的情况下,容易兼顾良好的显影性与良好的图案形状。
[0458]
此外,丙烯酸树脂(b3)优选包含5质量%以上、更优选包含10质量%以上、特别优选包含10质量%以上50质量%以下的以上述式(b5)~(b7)表示的结构单元。
[0459]
丙烯酸树脂(b3)优选包含源自上述的具有醚键的聚合性化合物的结构单元。丙烯酸树脂(b3)中,源自具有醚键的聚合性化合物的结构单元的含量优选为0质量%以上50质量%以下,更优选为5质量%以上30质量%以下。
[0460]
丙烯酸树脂(b3)优选包含源自上述的具有酸非解离性的脂肪族多环式基的(甲基)丙烯酸酯类的结构单元。丙烯酸树脂(b3)中,源自具有酸非解离性的脂肪族多环式基的(甲基)丙烯酸酯类的结构单元的含量优选为0质量%以上50质量%以下,更优选为5质量%以上30质量%以下。
[0461]
只要感光性树脂组合物含有规定量的丙烯酸树脂(b3),则也能够使用以上说明的丙烯酸树脂(b3)以外的丙烯酸树脂作为树脂(b)。作为这样的丙烯酸树脂(b3)以外的丙烯酸树脂,只要是包含以上述的式(b5)~(b7)表示的结构单元的树脂,就没有特别地限定。
[0462]
以上说明的树脂(b)的聚苯乙烯换算质均分子量优选为10000以上600000以下,更优选为20000以上400000以下,进一步优选为30000以上300000以下。通过设为这样的质均分子量,能够在使感光性层从基板的剥离性不降低的前提下保持感光性层的充分的强度,进而能够进一步防止镀覆时的外形(profile)的膨胀或者裂纹的产生。
[0463]
此外,树脂(b)的分子量分布系数优选为1.05以上。在此,分子量分布系数是指将质均分子量除以数均分子量而得的值。通过设为这样的分子量分布系数,能够得到所期望的相对于镀覆的应力抗性或者能够避免由镀覆处理得到的金属层变得容易膨胀的问题。
[0464]
树脂(b)的含量相对于感光性树脂组合物的总固体成分量优选为5质量%以上70质量%以下。
[0465]
《碱可溶性树脂(d)》
[0466]
为了提高碱可溶性,感光性树脂组合物优选还含有碱可溶性树脂(d)。在此,碱可溶性树脂是指:利用树脂浓度20质量%的树脂溶液(溶剂:丙二醇单甲醚乙酸酯)在基板上形成膜厚1μm的树脂膜,在2.38质量%的tmah(四甲基氢氧化铵)水溶液中浸渍1分钟时溶解0.01μm以上的树脂,且是指不属于上述(b)成分的树脂(典型地,是指即使通过酸的作用,碱可溶性实质上也不变动的树脂)。作为碱可溶性树脂(d),优选为从酚醛清漆树脂(d1)、聚羟基苯乙烯树脂(d2)及丙烯酸树脂(d3)构成的组中选择的至少1种树脂。
[0467]
[酚醛清漆树脂(d1)]
[0468]
酚醛清漆树脂例如通过使具有酚性羟基的芳香族化合物(以下,简称为“酚类”)与醛类在酸催化剂下加成缩合而得到。
[0469]
作为上述酚类,例如可例举苯酚、邻甲酚、间甲酚、对甲酚、邻乙基苯酚、间乙基苯酚、对乙基苯酚、邻丁基苯酚、间丁基苯酚、对丁基苯酚、2,3-二甲苯酚、2,4-二甲苯酚、2,5-二甲苯酚、2,6-二甲苯酚、3,4-二甲苯酚、3,5-二甲苯酚、2,3,5-三甲基苯酚、3,4,5-三甲基苯酚、对苯基苯酚、间苯二酚、对苯二酚、对苯二酚单甲醚、连苯三酚、间苯三酚、羟基联苯、双酚a、没食子酸、没食子酸酯、α-萘酚、β-萘酚等。
[0470]
作为上述醛类,例如可例举甲醛、糠醛、苯甲醛、硝基苯甲醛、乙醛等。
[0471]
加成缩合反应时的催化剂没有特别地限定,例如可使用酸催化剂中的盐酸、硝酸、硫酸、甲酸、草酸、乙酸等。
[0472]
另外,通过使用邻甲酚、将树脂中羟基的氢原子取代为其他的取代基、或者使用体积大的醛类,可进一步提高酚醛清漆树脂的柔软性。
[0473]
酚醛清漆树脂(d1)的质均分子量在不妨碍本发明的目的的范围内并无特别地限定,优选为1000以上50000以下。
[0474]
[聚羟基苯乙烯树脂(d2)]
[0475]
作为构成聚羟基苯乙烯树脂(d2)的羟基苯乙烯类化合物,可例举对羟基苯乙烯、α-甲基羟基苯乙烯、α-乙基羟基苯乙烯等。
[0476]
进而,聚羟基苯乙烯树脂(d2)优选是与苯乙烯树脂的共聚物。作为这样的构成苯乙烯树脂的苯乙烯类化合物,可例举苯乙烯、氯苯乙烯、氯甲基苯乙烯、乙烯基甲苯、α-甲基苯乙烯等。
[0477]
聚羟基苯乙烯树脂(d2)的质均分子量在不妨碍本发明的目的的范围内并无特别地限定,优选为1000以上50000以下。
[0478]
[丙烯酸树脂(d3)]
[0479]
作为丙烯酸树脂(d3),优选包括由具有醚键的聚合性化合物衍生的结构单元及由具有羧基的聚合性化合物衍生的结构单元。
[0480]
作为上述具有醚键的聚合性化合物,能够例示2-甲氧基乙基(甲基)丙烯酸酯、甲氧基三乙二醇(甲基)丙烯酸酯、3-甲氧基丁基(甲基)丙烯酸酯、乙基卡必醇(甲基)丙烯酸酯、苯氧基聚乙二醇(甲基)丙烯酸酯、甲氧基聚丙二醇(甲基)丙烯酸酯、四氢糠基(甲基)丙烯酸酯等具有醚键及酯键的(甲基)丙烯酸衍生物等。上述具有醚键的聚合性化合物优选是2-甲氧基乙基丙烯酸酯、甲氧基三乙二醇丙烯酸酯。这些聚合性化合物可以单独使用,也可以将2种以上组合使用。
[0481]
作为上述具有羧基的聚合性化合物,能够例示丙烯酸、甲基丙烯酸、巴豆酸等一元羧酸类;马来酸、富马酸、衣康酸等二元羧酸类;2-甲基丙烯酰氧基乙基琥珀酸、2-甲基丙烯酰氧基乙基马来酸、2-甲基丙烯酰氧基乙基邻苯二甲酸、2-甲基丙烯酰氧基乙基六氢邻苯二甲酸等具有羧基及酯键的化合物等。上述具有羧基的聚合性化合物优选是丙烯酸、甲基丙烯酸。这些聚合性化合物可以单独使用,也可以将2种以上组合使用。
[0482]
丙烯酸树脂(d3)的质均分子量在不妨碍本发明的目的的范围内并无特别地限定,优选为50000以上800000以下。
[0483]
在将感光性树脂组合物的总固体成分设为100质量份的情况下,碱可溶性树脂(d)的含量优选是3质量份以上70重量份以下,更优选是5质量份以上50质量份以下。通过将碱可溶性树脂(d)的含量设为上述的范围,容易提高碱可溶性。
[0484]
《含硫化合物(e)》
[0485]
在将感光性树脂组合物用于形成在金属基板上的图案的情况下,感光性树脂组合物优选包含含硫化合物(e)。含硫化合物(e)是包含可以与金属配位的硫原子的化合物。另外,关于可以产生2个以上的互变异构体的化合物,在至少1个互变异构体包含与构成金属基板的表面的金属进行配位的硫原子的情况下,该化合物属于含硫化合物。
[0486]
在由cu等金属构成的表面上形成作为镀覆用的铸模来使用的抗蚀剂图案的情况下,容易产生底脚等截面形状的不良情况。但是,在感光性树脂组合物包含含硫化合物(e)的情况下,即使在基板中的由金属构成的表面上形成抗蚀剂图案的情况下,也容易抑制底
脚等截面形状的不良情况的发生。另外,“底脚”是指由于抗蚀剂部在基板表面与抗蚀剂图案的接触面附近向非抗蚀剂部侧伸出,从而在非抗蚀剂部中底部的宽度相比于顶部的宽度变窄的现象。
[0487]
在将感光性树脂组合物用于形成在除金属基板以外的基板上的图案的情况下,感光性树脂组合物无需特别包含含硫化合物。在将感光性树脂组合物用于形成在除金属基板以外的基板上的图案的情况下,从因感光性树脂组合物的成分数的降低而容易制造感光性树脂组合物的方面、能够降低感光性树脂组合物的制造成本的方面等来看,感光性树脂组合物优选不包含含硫化合物(e)。
[0488]
另外,不会特别发生用于形成在除金属基板以外的基板上的图案的感光性树脂组合物因包含含硫化合物(e)而导致的不良情况。
[0489]
可以与金属配位的硫原子例如作为巯基(-sh)、硫代羧基(-co-sh)、二硫代羧基(-cs-sh)及硫代羰基(-cs-)等而包含于含硫化合物中。
[0490]
从容易与金属配位、使底脚的抑制效果优异的方面来看,含硫化合物优选具有巯基。
[0491]
作为具有巯基的含硫化合物的优选例,可例举以下述式(e1)表示的化合物。
[0492]
【化47】
[0493][0494]
(式中,r
e1
及r
e2
分别独立地表示氢原子或者烷基,r
e3
表示单键或者亚烷基,r
e4
表示可包含除碳以外的原子的u价的脂肪族基,u表示2以上4以下的整数。)
[0495]
在r
e1
及r
e2
为烷基的情况下,该烷基可以为直链状,也可以为支链状,优选为直链状。在r
e1
及r
e2
为烷基的情况下,该烷基的碳原子数在不妨碍本发明的目的的范围内没有特别地限定。作为该烷基的碳原子数,优选为1以上4以下,特别优选为1或者2,最优选为1。作为r
e1
与r
e2
的组合,优选的是一方为氢原子而另一方为烷基,特别优选的是一方为氢原子而另一方为甲基。
[0496]
在r
e3
为亚烷基的情况下,该亚烷基可以为直链状,也可以为支链状,优选为直链状。在r
e3
为亚烷基的情况下,该亚烷基的碳原子数在不妨碍本发明的目的的范围内没有特别地限定。作为该亚烷基的碳原子数,优选为1以上10以下,更优选为1以上5以下,特别优选为1或者2,最优选为1。
[0497]re4
为可包含除碳以外的原子的2价以上4价以下的脂肪族基。作为r
e4
可包含的除碳以外的原子,可例举氮原子、氧原子、硫原子、氟原子、氯原子、溴原子及碘原子等。作为r
e4
的脂肪族基的结构可以为直链状,也可以为支链状,也可以为环状,还可以为将这些结构组合而得的结构。
[0498]
在以式(e1)表示的化合物中,更优选以下述式(e2)表示的化合物。
[0499]
【化48】
[0500][0501]
(式(e2)中,r
e4
及u与式(e1)同义。)
[0502]
在以上述式(e2)表示的化合物中,优选下述的化合物。
[0503]
【化49】
[0504][0505]
以下述式(e3-l1)~(e3-l7)表示的化合物也被例举为具有巯基的含硫化合物的优选例。
[0506]
【化50】
[0507][0508]
(式(e3-l1)~(e3-l7)中,r’、s”、a”及r与对于丙烯酸树脂(b3)所述的式(b-l1)~(b-l7)相同。)
[0509]
作为以上述式(e3-l1)~(e3-l7)表示的巯基化合物的优选的具体例,可例举下述的化合物。
[0510]
【化51】
[0511][0512]
以下述式(e3-1)~(e3-4)表示的化合物也被例举为具有巯基的含硫化合物的优选例。
[0513]
【化52】
[0514][0515]
(对于式(e3-1)~(e3-4)中的简写符号的定义,与关于丙烯酸树脂(b3)所述的、对于式(3-1)~(3-4)所述的内容相同。)
[0516]
作为以上述式(e3-1)~(e3-4)表示的巯基化合物的优选的具体例,可例举下述的
化合物。
[0517]
【化53】
[0518][0519]
此外,作为具有巯基的化合物的优选例,可例举以下述式(e4)表示的化合物。
[0520]
【化54】
[0521][0522]
(在式(e4)中,r
e5
为从羟基、碳原子数为1以上4以下的烷基、碳原子数为1以上4以下的烷氧基、碳原子数为1以上4以下的烷硫基、碳原子数为1以上4以下的羟基烷基、碳原子数为1以上4以下的巯基烷基、碳原子数为1以上4以下的卤代烷基及卤素原子构成的组中选择的基团,n1为0以上3以下的整数,n0为0以上3以下的整数,在n1为2或3的情况下,r
e5
可以相同也可以不同。)
[0523]
作为r
e5
为碳原子数为1以上4以下的可具有羟基的烷基的情况下的具体例,可例举
甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基及叔丁基。在这些烷基中,优选为甲基、羟基甲基及乙基。
[0524]
作为r
e5
为碳原子数为1以上4以下的烷氧基的情况下的具体例,可例举甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基及叔丁氧基。在这些烷氧基中,优选为甲氧基及乙氧基,更优选为甲氧基。
[0525]
作为r
e5
为碳原子数为1以上4以下的烷硫基的情况下的具体例,可例举甲硫基、乙硫基、正丙硫基、异丙硫基、正丁硫基、异丁硫基、仲丁硫基及叔丁硫基。在这些烷硫基中,优选为甲硫基及乙硫基,更优选为甲硫基。
[0526]
作为r
e5
为碳原子数为1以上4以下的羟基烷基的情况下的具体例,可例举羟基甲基、2-羟基乙基、1-羟基乙基、3-羟基正丙基及4-羟基正丁基等。在这些羟基烷基中,优选为羟基甲基、2-羟基乙基及1-羟基乙基,更优选为羟基甲基。
[0527]
作为r
e5
为碳原子数为1以上4以下的巯基烷基的情况下的具体例,可例举巯基甲基、2-巯基乙基、1-巯基乙基、3-巯基正丙基及4-巯基正丁基等。在这些巯基烷基中,优选为巯基甲基、2-巯基乙基及1-巯基乙基,更优选为巯基甲基。
[0528]
在r
e5
为碳原子数为1以上4以下的卤代烷基的情况下,作为卤代烷基中所包含的卤素原子,可例举氟、氯、溴、碘等。作为r
e5
为碳原子数为1以上4以下的卤代烷基的情况下的具体例,可例举氯甲基、溴甲基、碘甲基、氟甲基、二氯甲基、二溴甲基、二氟甲基、三氯甲基、三溴甲基、三氟甲基、2-氯乙基、2-溴乙基、2-氟乙基、1,2-二氯乙基、2,2-二氟乙基、1-氯-2-氟乙基、3-氯正丙基、3-溴正丙基、3-氟正丙基及4-氯正丁基等。在这些卤代烷基中,优选为氯甲基、溴甲基、碘甲基、氟甲基、二氯甲基、二溴甲基、二氟甲基、三氯甲基、三溴甲基及三氟甲基,更优选为氯甲基、二氯甲基、三氯甲基及三氟甲基。
[0529]
作为r
e5
为卤素原子的情况下的具体例,可例举氟、氯、溴或者碘。
[0530]
在式(e4)中,n1为0以上3以下的整数,更优选为1。在n1为2或3的情况下,多个r
e5
可以相同也可以不同。
[0531]
在以式(e4)表示的化合物中,苯环上的r
e5
的取代位置并无特别限定。苯环上的r
e5
的取代位置优选相对于-(ch2)
n0-sh的键合位置为间位或者对位。
[0532]
作为以式(e4)表示的化合物,优选至少具有1个从烷基、羟基烷基及巯基烷基构成的组中选择的基团作为r
e5
的化合物,更优选具有1个从烷基、羟基烷基及巯基烷基构成的组中选择的基团作为r
e5
的化合物。在以式(e4)表示的化合物具有1个从烷基、羟基烷基及巯基烷基构成的组中选择的基团作为r
e5
的情况下,烷基、羟基烷基或者巯基烷基的苯环上的取代位置优选相对于-(ch2)
n0-sh的键合位置为间位或者对位,更优选为对位。
[0533]
在式(e4)中,n0为0以上3以下的整数。从化合物的制备、获得较为容易的方面来看,n0优选为0或者1,更优选为0。
[0534]
作为以式(e4)表示的化合物的具体例,可例举对巯基苯酚、对硫代甲酚、间硫代甲酚、4-(甲硫基)苯硫醇、4-甲氧基苯硫醇、3-甲氧基苯硫醇、4-乙氧基苯硫醇、4-异丙氧基苯硫醇、4-叔丁氧基苯硫醇、3,4-二甲氧基苯硫醇、3,4,5-三甲氧基苯硫醇、4-乙基苯硫醇、4-异丙基苯硫醇、4-正丁基苯硫醇、4-叔丁基苯硫醇、3-乙基苯硫醇、3-异丙基苯硫醇、3-正丁基苯硫醇、3-叔丁基苯硫醇、3,5-二甲基苯硫醇、3,4-二甲基苯硫醇、3-叔丁基-4-甲基苯硫醇、3-叔-4-甲基苯硫醇、3-叔丁基-5-甲基苯硫醇、4-叔丁基-3-甲基苯硫醇、4-巯基苄醇、
3-巯基苄醇、4-(巯基甲基)苯酚、3-(巯基甲基)苯酚、1,4-二(巯基甲基)苯酚、1,3-二(巯基甲基)苯酚、4-氟苯硫醇、3-氟苯硫醇、4-氯苯硫醇、3-氯苯硫醇、4-溴苯硫醇、4-碘苯硫醇、3-溴苯硫醇、3,4-二氯苯硫醇、3,5-二氯苯硫醇、3,4-二氟苯硫醇、3,5-二氟苯硫醇、4-巯基儿茶酚、2,6-二叔丁基-4-巯基苯酚、3,5-二叔丁基-4-甲氧基苯硫醇、4-溴-3-甲基苯硫醇、4-(三氟甲基)苯硫醇、3-(三氟甲基)苯硫醇、3,5-双(三氟甲基)苯硫醇、4-甲硫基苯硫醇、4-乙硫基苯硫醇、4-正丁硫基苯硫醇及4-叔丁硫基苯硫醇等。
[0535]
此外,作为具有巯基的含硫化合物,可例举包含被巯基取代而得的含氮芳香族杂环的化合物及包含被巯基取代而得的含氮芳香族杂环的化合物的互变异构体。
[0536]
作为含氮芳香族杂环的优选的具体例,可例举咪唑、吡唑、1,2,3-三唑、1,2,4-三唑、恶唑、噻唑、吡啶、嘧啶、哒嗪、吡嗪、1,2,3-三嗪、1,2,4-三嗪、1,3,5-三嗪、吲哚、吲唑、苯并咪唑、苯并恶唑、苯并噻唑、1h-苯并三唑、喹啉、异喹啉、噌啉、酞嗪、喹唑啉、喹喔啉及1,8-萘啶(naphthyridine)。
[0537]
作为适宜为含硫化合物的含氮杂环化合物及含氮杂环化合物的互变异构体的优选的具体例,可例举以下的化合物。
[0538]
【化55】
[0539][0540]
在感光性树脂组合物包含含硫化合物(e)的情况下,其使用量相对于上述树脂(b)及后述的碱可溶性树脂(d)的合计质量100质量份优选为0.01质量份以上5质量份以下,更优选为0.02质量份以上3质量份以下,特别优选为0.05质量份以上2质量份以下。
[0541]
《酸扩散控制剂(f)》
[0542]
为了提高作为铸模使用的抗蚀剂图案的形状、或感光性树脂膜的静置稳定性等,感光性树脂组合物优选还含有酸扩散控制剂(f)。作为酸扩散控制剂(f),优选含氮化合物(f1),能够根据需要进一步含有有机羧酸、或者磷的含氧酸或其衍生物(f2)。
[0543]
[含氮化合物(f1)]
[0544]
作为含氮化合物(f1),能够例举三甲胺、二乙胺、三乙胺、二正丙胺、三正丙胺、三正戊胺、三苄胺、二乙醇胺、三乙醇胺、正己胺、正庚胺、正辛胺、正壬胺、乙二胺、n,n,n’,n
’‑
四甲基乙二胺、四亚甲基二胺、己二胺、4,4
’‑
二氨基二苯基甲烷、4,4
’‑
二氨基二苯醚、4,4
’‑
二氨基二苯甲酮、4,4
’‑
二氨基二苯胺、甲酰胺、n-甲基甲酰胺、n,n-二甲基甲酰胺、乙酰胺、n-甲基乙酰胺、n,n-二甲基乙酰胺、丙酰胺、苯甲酰胺、吡咯烷酮、n-甲基吡咯烷酮、甲基脲、1,1-二甲基脲、1,3-二甲基脲、1,1,3,3-四甲基脲、1,3-二苯基脲、咪唑、苯并咪唑、4-甲基咪唑、8-羟基喹啉、吖啶、嘌呤、吡咯烷、哌啶、2,4,6-三(2-吡啶基)均三嗪、吗啉、4-甲基吗啉、哌嗪、1,4-二甲基哌嗪、1,4-二氮杂双环[2.2.2]辛烷、吡啶等。这些可以单独使用,也
可以将2种以上组合使用。
[0545]
此外,也能够将adk stab la-52、adk stab la-57、adk stab la-63p、adk stab la-68、adk stab la-72、adk stab la-77y、adk stab la-77g、adk stab la-81、adk stab la-82及adk stab la-87(均为adeka公司制)或4-羟基-1,2,2,6,6-五甲基哌啶衍生物等市售的受阻胺化合物或者2,6-二苯基吡啶及2,6-二叔丁基吡啶等2,6-位被烃基等取代基取代的吡啶作为含氮化合物(f1)使用。
[0546]
含氮化合物(f1)相对于上述树脂(b)及上述碱可溶性树脂(d)的合计质量100质量份,通常以0质量份以上5质量份以下的范围来使用,特别优选以0质量份以上3质量份以下的范围来使用。
[0547]
[有机羧酸、或者磷的含氧酸或其衍生物(f2)]
[0548]
在有机羧酸、或者磷的含氧酸或其衍生物(f2)中,作为有机羧酸,具体而言,优选为丙二酸、柠檬酸、苹果酸、琥珀酸、苯甲酸、水杨酸等,特别优选为水杨酸。
[0549]
作为磷的含氧酸或其衍生物,可例举磷酸、磷酸二正丁酯、磷酸二苯酯等磷酸及它们的酯这样的衍生物;膦酸、膦酸二甲酯、膦酸二正丁酯、苯基膦酸、膦酸二苯酯、膦酸二苄酯等膦酸及它们的酯这样的衍生物;次膦酸、苯基次膦酸等次膦酸及它们的酯这样的衍生物等。在这些之中,特别优选为膦酸。这些可以单独使用,也可以将2种以上组合使用。
[0550]
有机羧酸、或者磷的含氧酸或其衍生物(f2)相对于上述树脂(b)及上述碱可溶性树脂(d)的合计质量100质量份,通常以0质量份以上5质量份以下的范围来使用,特别优选以0质量份以上3质量份以下的范围来使用。
[0551]
此外,为了形成盐而使其稳定化,有机羧酸、或者磷的含氧酸或其衍生物(f2)优选使用与上述含氮化合物(f1)同等的量。
[0552]
《有机溶剂(s)》
[0553]
感光性树脂组合物优选含有有机溶剂(s)。在不妨碍本发明的目的的范围内,有机溶剂(s)的种类没有特别地限定,能够从以往的用于正型的感光性树脂组合物的有机溶剂中适当地选择并使用。
[0554]
作为有机溶剂(s)的具体例,能够例举丙酮、甲基乙基酮、环己酮、甲基异戊酮、2-庚酮等酮类;乙二醇、乙二醇单乙酸酯、二乙二醇、二乙二醇单乙酸酯、丙二醇、丙二醇单乙酸酯、丙二醇单甲醚乙酸酯、二丙二醇、二丙二醇单乙酸酯的单甲醚、单乙醚、单丙醚、单丁醚、单苯醚等多元醇类及其衍生物;二氧六环等环式醚类;甲酸乙酯、乳酸甲酯、乳酸乙酯、乙酸甲酯、乙酸乙酯、乙酸丁酯、丙酮酸甲酯、乙酰乙酸甲酯、乙酰乙酸乙酯、丙酮酸乙酯、乙氧基乙酸乙酯、甲氧基丙酸甲酯、乙氧基丙酸乙酯、2-羟基丙酸甲酯、2-羟基丙酸乙酯、2-羟基-2-甲基丙酸乙酯、2-羟基-3-甲基丁酸甲酯、3-甲氧基丁基乙酸酯、3-甲基-3-甲氧基丁基乙酸酯等酯类;甲苯、二甲苯等芳香族烃类等。这些可以单独使用,也可以将2种以上混合使用。
[0555]
在不妨碍本发明的目的的范围内,有机溶剂(s)的含量没有特别地限定。在将感光性树脂组合物用于如使利用旋涂法等得到的感光性层的膜厚达到5μm以上那样的厚膜用途的情况下,优选以使感光性树脂组合物的固体成分浓度达到30质量%以上70质量%以下的范围来使用有机溶剂(s)。
[0556]
《其他成分》
[0557]
为了提高可塑性,感光性树脂组合物也可以还含有聚乙烯树脂。作为聚乙烯树脂的具体例,可例举聚氯乙烯、聚苯乙烯、聚羟基苯乙烯、聚乙酸乙烯酯、聚乙烯基苯甲酸、聚乙烯基甲基醚、聚乙烯基乙基醚、聚乙烯醇、聚乙烯基吡咯烷酮、聚乙烯基苯酚及它们的共聚物等。从玻璃化转变点较低的观点来看,聚乙烯树脂优选为聚乙烯基甲基醚。
[0558]
此外,为了提高使用感光性树脂组合物形成的铸模等抗蚀剂图案与基板的粘接性,感光性树脂组合物可以还含有粘接助剂。
[0559]
此外,为了提高涂布性、消泡性、流平性等,感光性树脂组合物可以还含有表面活性剂。作为表面活性剂,例如优选地使用氟类表面活性剂或有机硅类表面活性剂。
[0560]
作为氟类表面活性剂的具体例,可例举bm-1000、bm-1100(均为bm化学公司制)、megafac f142d、megafac f172、megafac f173、megafac f183(均为大日本油墨化学工业公司制)、fluorad fc-135、fluorad fc-170c、fluorad fc-430、fluorad fc-431(均为住友3m公司制)、surflon s-112、surflon s-113、surflon s-131、surflon s-141、surflon s-145(均为旭硝子公司制)、sh-28pa、sh-190、sh-193、sz-6032、sf-8428(均为东丽有机硅公司制)等市售的氟类表面活性剂,但不限定于这些。
[0561]
作为有机硅类表面活性剂,能够优选地使用未改性有机硅类表面活性剂、聚醚改性有机硅类表面活性剂、聚酯改性有机硅类表面活性剂、烷基改性有机硅类表面活性剂、芳烷基改性有机硅类表面活性剂及反应性有机硅类表面活性剂等。
[0562]
作为有机硅类表面活性剂,能够使用市售的有机硅类表面活性剂。作为市售的有机硅类表面活性剂的具体例,可例举paintadd m(东丽
·
道康宁公司制)、特皮卡(日文为
トヒ°カ
)k1000、特皮卡k2000、特皮卡k5000(均为高千穗产业公司制)、xl-121(聚醚改性有机硅类表面活性剂,科莱恩公司制)、byk-310(聚酯改性有机硅类表面活性剂,毕克化学公司制)等。
[0563]
此外,为了进行对显影液的溶解性的微调整,感光性树脂组合物也可以还含有酸、酸酐或者高沸点溶剂。
[0564]
作为酸及酸酐的具体例,能够例举:乙酸、丙酸、正丁酸、异丁酸、正戊酸、异戊酸、苯甲酸、肉桂酸等一元羧酸类;乳酸、2-羟基丁酸、3-羟基丁酸、水杨酸、间羟基苯甲酸、对羟基苯甲酸、2-羟基肉桂酸、3-羟基肉桂酸、4-羟基肉桂酸、5-羟基间苯二甲酸、丁香酸等羟基一元羧酸类;草酸、琥珀酸、戊二酸、己二酸、马来酸、衣康酸、六氢邻苯二甲酸、邻苯二甲酸、间苯二甲酸、对苯二甲酸、1,2-环己烷二羧酸、1,2,4-环己烷三羧酸、丁烷四羧酸、偏苯三酸、均苯四酸、环戊烷四羧酸、丁烷四羧酸、1,2,5,8-萘四羧酸等多元羧酸类;衣康酸酐、琥珀酸酐、柠康酸酐、十二烯基琥珀酸酐、三羧酸酐、马来酸酐、六氢邻苯二甲酸酐、甲基四氢邻苯二甲酸酐、纳迪克酸酐、1,2,3,4-丁烷四羧酸酐、环戊烷四羧酸二酐、邻苯二甲酸酐、均苯四酸酐、偏苯三酸酐、二苯甲酮四羧酸酐、乙二醇双偏苯三酸酐、甘油三偏苯三酸酐等酸酐等。
[0565]
此外,作为高沸点溶剂的具体例,能够例举n-甲基甲酰胺、n,n-二甲基甲酰胺、n-甲基甲酰苯胺、n-甲基乙酰胺、n,n-二甲基乙酰胺、n-甲基吡咯烷酮、二甲基亚砜、苄基乙基醚、二己基醚、丙酮基丙酮、异佛尔酮、己酸、辛酸、1-辛醇、1-壬醇、苯甲醇、乙酸苄酯、苯甲酸乙酯、草酸二乙酯、马来酸二乙酯、γ-丁内酯、碳酸乙烯酯、碳酸丙烯酯、苯基溶纤剂乙酸酯等。
[0566]
此外,为了提高灵敏度,感光性树脂组合物可以还含有敏化剂。
[0567]
《化学放大型正型感光性树脂组合物的制备方法》
[0568]
以通常的方法将上述各成分混合、搅拌从而制备化学放大型正型感光性树脂组合物。作为能够在将上述各成分混合、搅拌时使用的装置,可例举溶解器、均化器、三辊研磨机等。在将上述各成分均匀地混合后,可以进一步使用筛网、膜滤器等对得到的混合物进行过滤。
[0569]
《感光性干膜》
[0570]
感光性干膜具有基材薄膜与形成于该基材薄膜的表面的感光性层,感光性层由前述的感光性树脂组合物构成。
[0571]
作为基材薄膜,优选具有透光性。具体而言,可例举聚对苯二甲酸乙二醇酯(pet)薄膜、聚丙烯(pp)薄膜、聚乙烯(pe)薄膜等,在使透光性及断裂强度的平衡优异的观点来看,优选聚对苯二甲酸乙二醇酯(pet)薄膜。
[0572]
在基材薄膜上涂布所述感光性树脂组合物,从而形成感光性层,由此制造感光性干膜。
[0573]
在基材薄膜上形成感光性层时,使用涂敷器、棒涂布器、线棒涂布器、辊涂布器、幕帘涂布器等来涂布感光性树脂组合物并使其干燥,从而使得在基材薄膜上干燥后的膜厚优选达到0.5μm以上300μm以下,更优选达到1μm以上300μm以下,特别优选达到3μm以上100μm以下。
[0574]
感光性干膜也可以在感光性层上还具有保护薄膜。作为该保护薄膜,可例举聚对苯二甲酸乙二醇酯(pet)薄膜、聚丙烯(pp)薄膜、聚乙烯(pe)薄膜等。
[0575]
《图案化的抗蚀剂膜的制造方法》
[0576]
使用上述说明的感光性树脂组合物而在基板上形成图案化的抗蚀剂膜的方法并无特别地限定。所述图案化的抗蚀剂膜优选用作用于形成镀覆造型物的铸模、利用蚀刻加工基板时的蚀刻掩模等。
[0577]
可例举包括以下工序的图案化的抗蚀剂膜的制造方法作为优选的方法:
[0578]
层叠工序,在基板上层叠由感光性树脂组合物构成的感光性层;
[0579]
曝光工序,对感光性层位置选择性地照射活性光线或放射线来进行曝光;
[0580]
显影工序,对曝光后的感光性层进行显影。
[0581]
具备用于形成镀覆造型物的铸模的带铸模基板的制造方法除了具有在具有金属表面的基板的金属表面上层叠感光性层的工序、并且在显影工序中利用显影制作用于形成镀覆造型物的铸模以外,与图案化的抗蚀剂膜的制造方法相同。
[0582]
作为对感光性层进行层叠的基板,没有特别地限定,能够使用以往公知的基板,例如能够例示电子部件用的基板或在其上形成了规定的布线图案的基板等。作为基板,也能够使用硅基板或玻璃基板等。
[0583]
在制造具备用于形成镀覆造型物的铸模的带铸模基板的情况下,作为基板,使用具有金属表面的基板。作为构成金属表面的金属种类,优选为铜、金、铝,更优选为铜。
[0584]
例如以如下的方式在基板上层叠感光性层。即,在基板上涂布液状的感光性树脂组合物,通过加热去除溶剂,由此形成期望的膜厚的感光性层。只要能够以期望的膜厚形成作为铸模的抗蚀剂图案,则对感光性层的厚度没有特别地限定。感光性层的膜厚没有特别
地限定,优选为0.5μm以上,更优选为0.5μm以上300μm以下,特别优选为1μm以上150μm以下,最优选为3μm以上100μm以下。
[0585]
作为向基板上涂布感光性树脂组合物的涂布方法,能够采用旋涂法、狭缝涂布法、辊涂法、筛网印刷法、涂敷器法等方法。优选对感光性层进行预烘烤。预烘烤的条件根据感光性树脂组合物中的各成分的种类、掺混比例、涂布膜厚等的不同而不同,但通常是以70℃以上200℃以下、优选以80℃以上150℃以下,进行2分钟以上120分钟以下左右。
[0586]
对如上述那样形成的感光性层,经由规定的图案的掩模,选择性地照射(曝光)活性光线或放射线,例如波长为300nm以上500nm以下的紫外线或可见光线。
[0587]
作为放射线的线源,能够使用低压汞灯、高压汞灯、超高压汞灯、金属卤化物灯、氩气激光等。此外,放射线中包括微波、红外线、可见光线、紫外线、x射线、γ射线、电子射线、质子射线、中子射线、离子射线等。放射线照射量根据感光性树脂组合物的组成、感光性层的膜厚等的不同而不同,例如在使用超高压汞灯的情况下,为100mj/cm2以上10000mj/cm2以下。此外,为了产生酸,放射线中包含使产酸剂(a)活化的光线。
[0588]
曝光后,使用公知的方法加热感光性层从而促进酸的扩散,在感光性树脂膜中被曝光的部分中,使感光性层的碱溶解性变化。
[0589]
接着,将被曝光后的感光性层按照以往已知的方法进行显影,溶解并去除不需要的部分,由此形成规定的抗蚀剂图案或者用于形成镀覆造型物的铸模。此时,作为显影液,可使用碱性水溶液。
[0590]
作为显影液,例如能够使用氢氧化钠、氢氧化钾、碳酸钠、硅酸钠、偏硅酸钠、氨水、乙胺、正丙胺、二乙胺、二正丙胺、三乙胺、甲基二乙胺、二甲基乙醇胺、三乙醇胺、四甲基氢氧化铵(羟化四甲铵)、四乙基氢氧化铵、吡咯、哌啶、1,8-二氮杂双环[5,4,0]-7-十一烯、1,5-二氮杂双环[4,3,0]-5-壬烷等碱类的水溶液。此外,也能够将在上述碱类的水溶液中添加有适当量的甲醇、乙醇等水溶性有机溶剂或表面活性剂的水溶液作为显影液使用。
[0591]
显影时间根据感光性树脂组合物的组成、感光性层的膜厚等的不同而不同,通常为1分钟以上30分钟以下之间。显影方法可以是盛液法、浸渍法、水坑显影法、喷雾显影法等中的任一种。
[0592]
在显影后,进行30秒以上90秒以下之间的流动水洗涤,使用空气枪、烤箱等进行干燥。像这样地,在基板的表面上,形成图案化为期望的形状的抗蚀剂图案。此外,像这样地,能够制造在具有金属表面的基板的金属表面上具备作为铸模的抗蚀剂图案的带铸模基板。
[0593]
由于感光性树脂组合物能够形成掩模线性优异的抗蚀剂图案,因此能够形成具有所期望的尺寸的抗蚀剂图案。
[0594]
在利用上述的方法形成的带铸模基板的铸模中的非抗蚀剂部(被显影液去除的部分)中,利用镀覆埋入金属等导体,由此能够形成例如凸块及金属柱等连接端子、或cu再布线那样的镀覆造型物。另外,镀覆处理方法没有特别地限制,能够采用以往公知的各种方法。作为镀覆液,特别优选使用焊接镀覆液、铜镀覆液、金镀覆液、镍镀覆液。剩下的铸模在最后根据常规方法使用剥离液等去除。
[0595]
在制造镀覆造型物时,有时优选对在成为镀覆造型物形成用的铸模的抗蚀剂图案的非图案部中所露出的金属表面进行灰化处理。
[0596]
具体而言,例如将使用包含含硫化合物(e)的感光性树脂组合物而形成的图案用
作铸模来形成镀覆造型物的情况。在该情况下,有时容易损害镀覆造型物对金属表面的密合性。该不良情况在使用以所述的式(e1)表示的含硫化合物(e)或以式(e4)表示的含硫化合物(e)的情况下较为显著。
[0597]
但是,若进行上述的灰化处理,则即使将使用包含含硫化合物(e)的感光性树脂组合物而形成的图案用作铸模,也容易形成与金属表面良好地密合的镀覆造型物。
[0598]
另外,对于将包含被巯基取代而得的含氮芳香族杂环的化合物用作含硫化合物(e)的情况,与镀覆造型物的密合性有关的上述的问题几乎不会发生或为轻度。因此,在使用包含被巯基取代而得的含氮芳香族杂环的化合物作为含硫化合物(e)的情况下,即使不进行灰化处理,也容易形成对金属表面的密合性良好的镀覆造型物。
[0599]
灰化处理只要是不会造成在成为镀覆造型物形成用的铸模的抗蚀剂图案上无法形成所期望的形状的镀覆造型物的程度的损害的方法,则并无特别地限定。
[0600]
作为优选的灰化处理方法,可例举使用氧等离子体的方法。为了使用氧等离子体对基板上的金属表面进行灰化,只要使用公知的氧等离子体产生装置来产生氧等离子体,并且对基板上的金属表面照射该氧等离子体即可。
[0601]
在用于产生氧等离子体的气体中,能够在不妨碍本发明的目的的范围内混合以往与氧气一起用于等离子体处理的各种气体。作为该气体,例如可例举氮气、氢气及cf4气体等。
[0602]
使用氧等离子体的灰化条件在不妨碍本发明的目的的范围内并无特别地限定,处理时间为例如10秒钟以上20分钟以下的范围,优选为20秒钟以上18分钟以下的范围,更优选为30秒钟以上15分钟以下的范围。
[0603]
通过将采用氧等离子体的处理时间设定为上述的范围,从而容易在不给抗蚀剂图案的形状带来变化的前提下发挥使镀覆造型物的密合性改良的效果。
[0604]
以式(a1)表示的化合物是新型化合物,如上所述,能够作为光产酸剂使用。
[0605]
《n-有机磺酰氧基化合物的制造方法》
[0606]
对能够适用于以上述式(a1)表示的化合物的制造的n-有机磺酰氧基化合物的制造方法进行说明。
[0607]
例如,作为可掺混于化学放大型感光性树脂组合物的光产酸剂,已知有肟的有机磺酸酯或n-羟基萘二甲酰亚胺等有机磺酸酯等、具有在含氮化合物的氮原子上键合有有机磺酰氧基的结构的n-有机磺酰氧基化合物(日本特开2010-159243号公报)。
[0608]
作为这样的n-有机磺酰氧基化合物的合成方法,例如已知有以下方法:使有机磺酰氟化合物在碱的存在下与具有在含氮化合物的氮原子上键合有羟基的结构的n-羟基化合物反应的方法(例如参照日本特开2010-159243号公报)。
[0609]
但是,在该方法中,反应难以推进,存在无法得到作为目标的n-有机磺酰氧基化合物,或者即使得到了n-有机磺酰氧基化合物其收率也较差的问题。
[0610]
因此,要求效率良好的n-有机磺酰氧基化合物的制造方法。
[0611]
能够通过下述n-有机磺酰氧基化合物的制造方法来解决这样的问题。并且,下述n-有机磺酰氧基化合物的制造方法能够应用于以上述式(a1)表示的化合物的制造。
[0612]
在该n-有机磺酰氧基化合物的制造方法中,包括使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应。并且,在n-有机磺酰氧基化合物的制造方
法中,其特征在于,在使n-羟基化合物(a’)与磺酰氟化合物(b’)反应时,系统中存在硅烷化剂(c’),磺酰氟化合物(b’)以下述式(bi1)表示,硅烷化剂(c’)是可以将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以下述式(ac1)表示的甲硅烷氧基的化合物。
[0613]
n-羟基化合物(a’)具有在含氮化合物的氮原子上键合有羟基的结构。n-羟基化合物在1个分子中包含多个氮原子的情况下,也可以在多个氮原子中的2个以上的氮原子上键合有羟基。
[0614]
在n-羟基化合物(a’)中,优选在与键合有羟基的氮原子相邻的位置存在1或2个羰基。
[0615]
作为在与键合有羟基的氮原子相邻的位置存在1个羰基的n-羟基化合物(a’),可例举以r
a0-noh-co-r
a0
表示的n-羟基酰胺化合物、以r
a0-noh-co-n(r
a0
)2表示的n-羟基脲化合物及以r
a0-noh-co-o-r
a0
表示的n-羟基氨基甲酸酯化合物等。在此,r
a0
分别独立地为氢原子或有机基团。作为r
a0
的有机基团优选为碳原子数为1以上20以下的烃基,更优选为碳原子数为1以上10以下的烃基,进一步优选为碳原子数为1以上6以下的烃基。作为r
a0
的烃基,可以是直链状,也可以是支链状,也可以是环状,也可以是将它们组合而成的结构。作为r
a0
的烃基的优选具体例,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基及苯基。作为在与键合有羟基的氮原子相邻的位置存在1个羰基的n-羟基化合物(a’)的优选的具体例,可例举n-羟基乙酰胺、n-羟基丙酸酰胺、n-羟基苯甲酰胺及氨基甲酰基羟胺(n-羟基脲)。
[0616]
作为在与键合有羟基的氮原子相邻的位置存在2个羰基的n-羟基化合物(a’),优选为以r
a0-co-noh-co-r
a0
表示的n-羟基酰亚胺化合物、在环上可具有1个以上的取代基的n-羟基琥珀酰亚胺化合物、以及在环上可具有1个以上的取代基的n-羟基马来酰亚胺化合物。此外,还优选在苯环上可具有1个以上的取代基的n-羟基邻苯二甲酰亚胺化合物及在萘环上可具有1个以上的取代基的n-羟基萘二甲酰亚胺化合物等、在芳香环上可具有取代基的n-羟基芳香族二羧酸酰亚胺化合物。关于r
a0
如上文所述。作为在与键合有羟基的氮原子相邻的位置存在2个羰基的n-羟基化合物(a’)的优选例,可例举在环上可具有1个以上的取代基的n-羟基琥珀酰亚胺、在环上可具有1个以上的取代基的n-羟基马来酰亚胺、在苯环上可具有1个以上的取代基的n-羟基邻苯二甲酰亚胺及在萘环上可具有1个以上的取代基的n-羟基萘二甲酰亚胺。
[0617]
在与键合有羟基的氮原子相邻的位置存在2个羰基的n-羟基化合物中,作为可以存在于苯环、萘环等环上的取代基,可例举卤素原子、硝基、氰基、有机基团。有机基团也可以含有n、o、p、s、se等杂原子。作为取代基的有机基团,可例举与后述的式(ai1-1)中的作为r
a1
及r
a2
的氢原子以外的基团相同的基团。
[0618]
在上述n-羟基化合物(a’)中,从生成的n-有机磺酰氧基化合物作为光产酸剂非常有用的观点来看,优选在萘环上可具有1个以上的取代基的n-羟基萘二甲酰亚胺化合物。作为在萘环上可具有1个以上的取代基的n-羟基萘二甲酰亚胺化合物的优选例,可例举以下述式(ai1-1)表示的化合物。
[0619]
【化56】
[0620][0621]
(式(ai1-1)中,r
a1
及r
a2
分别独立地为氢原子、可具有取代基的碳原子数为1以上20以下的脂肪族烃基、可具有取代基的环构成原子数为5以上20以下的芳香族基团或者以-r
a3-r
a4
表示的基团,
[0622]
在作为r
a1
及r
a2
的脂肪族烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-及-nr
a5-构成的组中选择的基团取代,
[0623]ra5
为氢原子或者碳原子数为1以上6以下的烃基,
[0624]ra3
为亚甲基、-o-、-co-、-co-o-、-so-、-so
2-或者-nr
a6-,
[0625]ra6
为氢原子或者碳原子数为1以上6以下的烃基,
[0626]ra4
为可具有取代基的环构成原子数为5以上20以下的芳香族基团、碳原子数为1以上6以下的全氟烷基、可具有取代基的碳原子数为7以上20以下的芳烷基、或者包含可具有取代基的环构成原子数为5以上20以下的芳香族杂环基的杂芳基烷基。)
[0627]
在以式(ai1-1)表示的化合物中,-co-o-的方向没有特别限定。
[0628]
式(ai1-1)中,作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0629]
作为脂肪族烃基,优选为烷基。作为烷基的优选的具体例,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基及正癸基。
[0630]
作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可具有的取代基,可例举羟基、巯基、氨基、卤素原子、氧原子、硝基、氰基等。取代基的数量是任意的。作为r
a1
及r
a2
的具有取代基的碳原子数为1以上20以下的脂肪族烃基,例如可例举碳原子数为1以上6以下的全氟烷基。作为其具体例,可例举cf
3-、cf3cf
2-、(cf3)2cf-、cf3cf2cf
2-、cf3cf2cf2cf
2-、(cf3)2cfcf
2-、cf3cf2(cf3)cf-、(cf3)3c-。
[0631]
式(ai1-1)中,作为r
a1
及r
a2
的可具有取代基的环构成原子数为5以上20以下的芳香族基团,可以为芳香族烃基,也可以为芳香族杂环基。
[0632]
作为芳香族基团,可例举苯基、萘基等芳基或呋喃基、噻吩基等杂芳基。
[0633]
环构成原子数为5以上20以下的芳香族基团可具有的取代基与作为r
a1
及r
a2
的碳原子数为1以上20以下的脂肪族烃基可具有的取代基相同。
[0634]
在式(ai1-1)中,r
a4
~r
a6
分别与式(a1)中的r
a4
~r
a6
相同。
[0635]
作为n-羟基化合物(a’),也可以使用肟。
[0636]
n-羟基化合物(a’)的合成方法等获得方法如上所述。
[0637]
在n-有机磺酰氧基化合物的制造方法中使用的磺酰氟化合物(b’)是以下述式(bi1)表示的化合物。
[0638]rbi1-so
2-f
···
(bi1)
[0639]
(式(bi1)中,r
bi1
为有机基团。)
[0640]
式(bi1)中,作为r
bi1
的有机基团没有特别限定,根据作为目标的n-有机磺酰氧基化合物进行选择即可。
[0641]
作为一例,作为r
bi1
的有机基团是与上述式(ai1-1)中的作为r
a1
及r
a2
的氢原子以外的基团相同的基团。
[0642]
作为以上述式(bi1)表示的化合物,可例举以下述式(bi1-1)表示的化合物。
[0643]rbi2-cq1q
2-so
2-f
···
(bi1-1)
[0644]
(式(bi1-1)中,q1及q2分别独立地为氟原子或者碳原子数为1以上6以下的全氟烷基,r
bi2
为有机基团。)
[0645]
式(bi1-1)中,作为q1及q2的碳原子数为1以上6以下的全氟烷基,与式(ai1-1)中作为r
a1
及r
a2
说明的碳原子数为1以上6以下的全氟烷基相同。
[0646]
式(bi1-1)中,作为r
bi2
的有机基团没有特别限定,根据作为目标的n-有机磺酰氧基化合物进行选择即可。
[0647]
作为一例,作为r
bi2
的有机基团是与上述式(ai1-1)中的作为r
a1
及r
a2
的氢原子以外的基团相同的基团。
[0648]
作为以上述式(bi1)表示的化合物,优选为以下述式(bi1-2)表示的化合物。
[0649]rbi3-l
i-cq1q
2-so
2-f
···
(bi1-2)
[0650]
(式(bi1-2)中,q1及q2分别与式(bi1-1)中的这些相同,
[0651]
li为-co-o-或者-o-,
[0652]rbi3
为碳原子数为1以上30以下的烃基,
[0653]
在作为r
bi3
的烃基包含1个以上的亚甲基的情况下,至少一部分亚甲基可以被从-o-、-s-、-co-、-co-o-、-so-、-so
2-、-cr
b4rb5-及-nr
b6-构成的组中选择的基团取代,
[0654]
在作为r
bi3
的烃基包含烃环的情况下,构成烃环的至少1个碳原子可以被从n、o、p、s及se构成的组中选择的杂原子或者包含该杂原子的原子团取代,
[0655]rb4
及r
b5
分别独立地为氢原子或者卤素原子,r
b4
及r
b5
中的至少一方为卤素原子,
[0656]rb6
为氢原子或者碳原子数为1以上6以下的烃基。)
[0657]
在以式(bi1-2)表示的化合物中,-co-o-的方向没有特别限定。
[0658]
式(bi1-2)中,作为r
bi3
的碳原子数为1以上30以下的烃基可以为脂肪族烃基,也可以为芳香族烃基,还可以为脂肪族烃基与芳香族烃基的组合。脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0659]
作为脂肪族烃基,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基等链状的脂肪族烃基、环丙基、环丁基、环戊基、环己基、金刚烷基、降冰片基等环状的脂肪族烃基(烃环)。
[0660]
作为芳香族烃基,可例举苯基、萘基。
[0661]
作为将脂肪族烃基及芳香族烃基组合而得的基团,可例举苄基、苯乙基、呋喃基甲基。
[0662]
在作为r
bi3
的烃基包含烃环的情况下,作为取代构成烃环的至少1个碳原子的包含杂原子的原子团,可例举-co-、-co-o-、-so-、-so
2-、-so
2-o-、-p(=o)-(or
b7
)3。r
b7
为碳原子数为1以上6以下的烃基,与对r
a5
说明的碳原子数为1以上6以下的烃基相同。
[0663]
式(bi1-2)中,作为r
b4
及r
b5
的卤素原子的具体例,可例举氯原子、氟原子、溴原子及碘原子。
[0664]
式(bi1-2)中,作为r
b6
的碳原子数为1以上6以下的烃基,与式(ai1-1)中作为r
a5
说明的碳原子数为1以上6以下的烃基相同。
[0665]
磺酰氟化合物(b’)能够通过常规方法合成。例如,在式(bi1-2)中,li为-co-o-、q1及q2为氟原子的化合物能够通过以下述式表示的反应来合成。此外,作为磺酰氟化合物(b’),可以使用市售品。
[0666]
【化57】
[0667][0668]
在n-有机磺酰氧基化合物的制造方法中使用的硅烷化剂(c’)是可将n-羟基化合物(a’)所具有的氮原子上的羟基转化为以下述式(ac1)表示的甲硅烷氧基的化合物。
[0669]-o-si(r
c1
)3···
(ac1)
[0670]
(式(ac1)中,r
c1
分别独立地为碳原子数为1以上10以下的烃基。)
[0671]
式(ac1)中,作为r
c1
的碳原子数为1以上10以下的烃基可以为脂肪族烃基,也可以为芳香族烃基,还可以为脂肪族烃基与芳香族烃基的组合。脂肪族烃基可以为直链状,也可以为支链状,也可以为环状,还可以为这些结构的组合。
[0672]
作为脂肪族烃基,可例举甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、2-乙基己基、正壬基及正癸基等烷基。
[0673]
作为芳香族烃基,可例举苯基、萘基。
[0674]
作为硅烷化剂(c’),可例举以下述式(c1)表示的化合物。
[0675]
x-si(r
c1
)3···
(c1)
[0676]
(式(c1)中,r
c1
与式(ac1)中的r
c1
相同,x为卤素原子。)
[0677]
式(c1)中,作为x的卤素原子的具体例,可例举氯原子、氟原子、溴原子及碘原子。
[0678]
硅烷化剂(c’)的具体例与上述的硅烷化剂(c’)的具体例相同。
[0679]
在n-有机磺酰氧基化合物的制造方法中使用的碱性化合物(d’)可以是有机碱,也可以是无机碱。
[0680]
作为有机碱,例如可例举含氮碱性化合物,具体例与上述碱性化合物(d’)的具体例相同。
[0681]
作为无机碱,例如可例举金属氢氧化物、金属碳酸氢盐及金属重碳酸盐。无机碱的具体例与上述的碱性化合物(d’)的具体例相同。
[0682]
在n-有机磺酰氧基化合物的制造方法中,使这样的n-羟基化合物(a’)与磺酰氟化合物(b’)在硅烷化剂(c’)及碱性化合物(d’)的存在下进行反应。
[0683]
像这样,在使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应时,通过使硅烷化剂(c’)存在,能够如后述的实施例所示地高效地制造n-有机磺酰氧基化合物。例如,相对于原料的n-羟基化合物(a’)及磺酰氟化合物(b’),能够以收率65%以上得到n-有机磺酰氧基化合物。
[0684]
通过n-有机磺酰氧基化合物的制造方法,可得到具有n-羟基化合物(a’)的与氮原子键合的羟基的氢原子被去除的基团、和源自磺酰氟化合物(b’)的r
bi1-so
2-键合而得的结构的n-有机磺酰氧基化合物。
[0685]
作为得到的n-有机磺酰氧基化合物,可例举以下述式表示的化合物。
[0686]
【化58】
[0687][0688]
(式中,r
a1
及r
a2
与式(ai1-1)中的r
a1
及r
a2
分别相同,q1、q2、li及r
bi3
与式(bi1-2)中的q1、q2、li及r
bi3
分别相同。)
[0689]
在n-有机磺酰氧基化合物的制造方法中,在使n-羟基化合物(a’)与磺酰氟化合物(b’)在碱性化合物(d’)的存在下进行反应时,只要系统中存在硅烷化剂(c’)即可,可以同时混合n-羟基化合物(a’)、磺酰氟化合物(b’)、硅烷化剂(c’)及碱性化合物(d’),也可以在使n-羟基化合物(a’)与硅烷化剂(c’)部分反应后或者使n-羟基化合物(a’)与硅烷化剂(c’)完成反应后,再添加磺酰氟化合物(b’)及碱性化合物(d’)。
[0690]
若使这样的n-羟基化合物(a’)与磺酰氟化合物(b’)在硅烷化剂(c’)及碱性化合物(d’)的存在下进行反应,则n-羟基化合物(a’)被硅烷化剂(c’)硅烷化,使氮原子上的羟基被转化为以上述式(ac1)表示的甲硅烷氧基(步骤1:硅烷化工序)。
[0691]
然后,使在硅烷化工序中生成的n-羟基化合物(a’)的硅烷化物与碱性化合物(d’)作用的磺酰氟化合物(b’)进行缩合(步骤2:缩合工序)。由此,可得到n-有机磺酰氧基化合物。
[0692]
作为n-有机磺酰氧基化合物的制造方法的一例,在以下示出使用以上述式(ai1-1)表示的化合物作为n-羟基化合物(a’)、使用在上述式(bi1-2)中li为-co-o-、q1及q1为氟原子的化合物作为磺酰氟化合物(b’)、使用三甲基氯硅烷作为硅烷化剂(c’)、使用三乙胺作为碱性化合物(d’)的情况下的反应式。另外,以下所示的不是分析确认的反应机理,而是根据原料与其反应中的行为推定的反应机理。
[0693]
【化59】
[0694]
step-1
[0695][0696]
【化60】
[0697]
step-2
[0698][0699]
作为能够在反应中采用的有机溶剂,例如可例举乙酸乙酯、乙酸丁酯、乙酸溶纤剂等酯类;丙酮、甲基乙基酮、异丁基酮、甲基异丁基酮等酮类;乙酸乙酯、乙酸丁酯、丙二酸二乙酯等酯类;n-甲基吡咯烷酮、n,n-二甲基甲酰胺等酰胺类;二乙醚、乙基环戊醚、四氢呋喃、二氧六环等醚类;甲苯、二甲苯等芳香族烃类;己烷、庚烷、辛烷、十氢化萘等脂肪族烃类;氯仿、二氯甲烷、甲叉二氯、二氯乙烷等卤代烃类;乙腈、丙腈等腈类溶剂;二甲亚砜、二甲磺酰胺等。所使用的有机溶剂可以使用1种溶剂,也可以将2种以上任意地组合来使用。
[0700]
作为能够采用的反应温度,例如在-10℃~200℃的范围内,优选在0℃~150℃的范围内,更优选在5℃~120℃的范围内。
[0701]
作为能够采用的反应时间,例如为5分钟以上20小时以下、10分钟以上15小时以下、30分钟以上12小时以下。
[0702]
相对于n-羟基化合物(a’),优选分别过量地使用磺酰氟化合物(b’)、硅烷化剂
(c’)及碱性化合物(d’)。例如,相对于1.0摩尔n-羟基化合物(a’),优选以1.1摩尔以上2.5摩尔以下使用磺酰氟化合物(b’)、以1.1摩尔以上2.5摩尔以下使用硅烷化剂(c’)、以1.1摩尔以上2.5摩尔以下使用碱性化合物(d’)。
[0703]
根据这样的制造方法,能够高效地得到n-有机磺酰氧基化合物,得到的n-有机磺酰氧基化合物能够作为化学放大型正型感光性树脂组合物的产酸剂、在医药品等各种领域中使用的化合物来使用。
[0704]
【实施例】
[0705]
以下,通过实施例对本发明更详细地进行说明,但是本发明并不限定于这些实施例。
[0706]
《n-羟基化合物(a’)》
[0707]
作为n-羟基化合物,使用了按照下述方法制备的a1、a3~a8及下述的a2。
[0708]
【化61】
[0709][0710]
【化62】
[0711][0712]
[a1的制备]
[0713]
在氮气气氛下,在对冷却至-70℃的534g四氢呋喃、0.24g1-丁基锂15%己烷溶液进行搅拌的同时,以反应系统不会上升至高于-60℃的速度滴加203g溴化锌与640g四氢呋喃的悬浮液。然后,使反应系统回到10℃,搅拌1小时,制备丁基锌试剂。
[0714]
在氮气气氛下,将上述丁基锌试剂滴加至100g 4-溴萘二甲酸酐、5.88g[1,1
’‑
双(二苯基膦)二茂铁]二氯化钯(ii)二氯甲烷加合物与534g四氢呋喃的混合液中,在室温下搅拌1小时。向其中加入1000g水,在将有机层分液、浓缩得到的固相中加入532g甲苯、100g硅胶,搅拌后滤出固相。在浓缩滤液而得到的固相中加入333g甲醇,对加热得到的溶液进行过滤并对得到的滤液进行冷却来进行晶析,用异丙醇洗涤,进行真空干燥,得到48.0g淡黄色固体(4-丁基萘二甲酸酐)。
[0715]
将通过上述得到的6.10g 4-丁基萘二甲酸酐悬浮于36.0g二甲基甲酰胺中,在室温下加入2.00g nh2oh-hcl,滴加2.30g 50%氢氧化钠水溶液,搅拌5小时。向其中加入24.0g水、0.63g 20%盐酸,进一步搅拌2小时。滤取析出物,用甲醇与水的混合物洗涤后,以50℃真空干燥,得到3.17g上述a1(收率49%)。
[0716]
[a3的制备]
[0717]
在3角烧瓶中将28g 4-溴-1,8-萘二甲酸酐(东京化成工业公司制)及11g三乙胺分散于400g乙腈后,投入22g巯基乙酸-2-乙基己酯(东京化成工业公司制),以75℃反应6小时。接着,滴加投入18g 50%羟胺水溶液(东京化成工业公司制),在室温下反应2小时。反应
结束后,向离子交换水中投入反应液后,投入盐酸直至ph达到5。搅拌片刻后,过滤回收析出物,以70℃进行减压干燥,得到11.4g淡黄色固体的上述a3(收率52%)。
[0718]
[a4的制备]
[0719]
除了将28g 4-溴-1,8-萘二甲酸酐变更为21g 3-羟基-1,8-萘二甲酸酐(东京化成工业公司制)、将11g三乙胺变更为27g碳酸钾、以及将22g巯基乙酸-2-乙基己酯变更为21g 2-溴己酸(东京化成工业公司制)以外,进行与[a3的制备]同样的操作,得到7.5g上述a4(收率45%)。
[0720]
[a5的制备]
[0721]
在3角烧瓶中,将40g 2-溴己酸、4g二甲基氨基吡啶及80g叔丁醇溶解于800g二氯甲烷中后,投入50g 1-(3-二甲基氨基丙基)-3-乙基碳二亚胺盐酸盐,在室温下反应3小时。接着,用1%盐酸水溶液洗涤后,通过减压去除溶剂,得到溴己酸叔丁酯。
[0722]
在3角烧瓶中将21g 3-羟基-1,8-萘二甲酸酐及27g碳酸钾分散于400g乙腈后,投入由上述得到的40g溴己酸叔丁酯,以75℃反应6小时。然后,将碳酸钾过滤去除后,滴加投入18g 50%羟胺水溶液,在室温下反应2小时。反应结束后,向离子交换水中投入反应液后,投入盐酸直至ph达到5。搅拌片刻后,过滤回收析出物,以70℃进行减压干燥,得到10g上述a5(收率51%)。
[0723]
[a6的制备]
[0724]
将5.5g 3-羟基-1,8-萘二甲酸酐、5.9g二碳酸二叔丁酯(东京化成工业公司制)分散在32g乙腈中,加入2.2g吡啶,以50℃搅拌2小时。冷却至室温后,投入水中,滤出析出物,得到白色固体。对该白色固体进行水洗并干燥,由此得到6.5g 3-异丁氧基羰基氧基-1,8-萘二甲酸酐。将得到的6.5g 3-异丁氧基羰基氧基-1,8-萘二甲酸酐溶解于137g乙腈中,加入2.0g 50%羟胺水溶液,在室温下搅拌2小时。将反应液投入水中,滤出析出物,得到白色固体。对该白色固体进行水洗并干燥,由此得到3.7g上述a6(收率55%)。
[0725]
[a7的制备]
[0726]
将43.4g碳酸钾分散在168g丙酮中,加入8.4g 1,6-二羟基萘(东京化成工业公司制)、38.8g 1-碘丁烷,在50℃下搅拌20小时。冷却至室温后,进行滤出并向滤液中加入15g甲基丁基醚,水洗并馏去溶剂,由此得到14.3g 1,6-二丁氧基萘。将得到的1,6-二丁氧基萘作为原料,在氮气气氛下向按照文献(helv.chem.acta,1921,342.)中记载的方法合成的2.0g 3,6-二丁氧基苊醌的29g甲醇分散液中一次性加入10g过氧单硫酸钾(复盐)。在强烈搅拌该分散液的同时回流一天。反应结束后,冷却至室温,投入大量的水中。过滤得到的固体,通过减压干燥得到1.6g化合物。将1.6g得到的化合物分散于20g乙腈中,加入2.0g 50%羟胺水溶液,以50℃搅拌一天。将反应液投入稀盐酸水溶液中,滤出析出物,进行水洗、干燥,由此得到1.0g上述a7(收率60%)。
[0727]
[a8的制备]
[0728]
除了将1,6-二丁氧基萘变更为2,6-二异丙基萘(东京化成工业公司制)、将2.0g 3,6-二丁氧基苊醌变更为2.0g 3,7-二异丙基苊醌以外,进行与[a7的制备]相同的操作,得到1.0g上述a8(收率57%)。
[0729]
《磺酰氟化合物(b’)》
[0730]
作为磺酰氟化合物(b’),使用了下述的b1与按照下述方法制备的b2~b4。
[0731]
【化63】
[0732][0733]
[b2的制备]
[0734]
将8.9g 2-环己基乙醇与14.8g下述羧酸在80.0g甲苯中,在7.5g硫酸的存在下且在回流下搅拌2小时。然后,用纯水对反应液进行洗涤,馏去溶剂,由此得到作为粘性液体的下述b2。
[0735]
【化64】
[0736][0737]
[b3的制备]
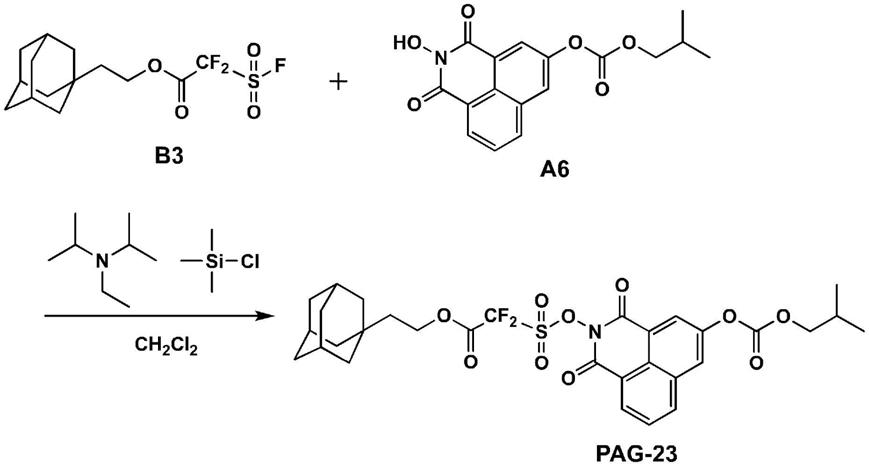
[0738]
除了将2-环己基乙醇变更为1-金刚烷乙醇以外,进行与[b2的制备]相同的操作,得到下述b3。
[0739]
【化65】
[0740][0741]
[b4的制备]
[0742]
除了将2-环己基乙醇变更为下述醇以外,进行与[b2的制备]相同的操作,得到b4。
[0743]
【化66】
[0744][0745]
【化67】
[0746][0747]
(产酸剂(a)的制备)
[0748]
(制备例1)
[0749]
在混合了1.94g作为n-羟基化合物(a’)的a1、42.4g二氯甲烷的混合物中,添加1.12g作为碱性化合物(d’)的n-乙基二异丙胺,添加1.02g作为硅烷化剂(c’)的三甲基氯硅
烷,接着添加1.54g作为磺酰氟化合物(b’)的b1,在室温下搅拌12小时。
[0750]
然后,用1%盐酸洗涤反应液,用纯水进行洗涤,馏去溶剂,由此得到2.71g的pag-1作为粘性液体(收率85%)。下述化合物pag-1的1h-nmr的测量结果如下所述。
[0751]1h-nmr(cdcl3):δ=8.41-8.80(m,3h),7.85(m,1h),7.64(d,1h),4.00(s,3h),3.31(t,2h),1.80(m,2h),1.49(m,2h),1.10(t,3h)
[0752]
【化68】
[0753][0754]
(制备例2)
[0755]
除了使用b2代替b1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-2。收率为83%。
[0756]
【化69】
[0757]
[0758]
(制备例3)
[0759]
除了使用b3代替b1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-3。收率为90%。
[0760]
【化70】
[0761][0762]
(制备例4)
[0763]
除了使用b4代替b1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-4。收率为85%。
[0764]
【化71】
[0765][0766]
(制备例5)
[0767]
除了使用a2代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-7。收率为80%。
[0768]
【化72】
[0769][0770]
(制备例6)
[0771]
除了使用b4代替b1、使用a2代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-8。收率为75%。
[0772]
【化73】
[0773][0774]
(制备例7)
[0775]
除了使用a3代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-9。收率为84%。
[0776]
【化74】
[0777][0778]
(制备例8)
[0779]
除了使用a3代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-10。收率为86%。
[0780]
【化75】
[0781][0782]
(制备例9)
[0783]
除了使用a3代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-11。收率为87%。
[0784]
【化76】
[0785][0786]
(制备例10)
[0787]
除了使用a3代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-12。收率为80%。
[0788]
【化77】
[0789][0790]
(制备例11)
[0791]
除了使用a4代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-13。收率为87%。
[0792]
【化78】
[0793][0794]
(制备例12)
[0795]
除了使用a4代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-14。收率为80%。
[0796]
【化79】
[0797][0798]
(制备例13)
[0799]
除了使用a4代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-15。收率为79%。
[0800]
【化80】
[0801][0802]
(制备例14)
[0803]
除了使用a4代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-16。收率为76%。
[0804]
【化81】
[0805][0806]
(制备例15)
[0807]
除了使用a5代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-17。收率为82%。
[0808]
【化82】
[0809][0810]
(制备例16)
[0811]
除了使用a5代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-18。收率为85%。
[0812]
【化83】
[0813][0814]
(制备例17)
[0815]
除了使用a5代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-19。收率为86%。
[0816]
【化84】
[0817][0818]
(制备例18)
[0819]
除了使用a5代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-20。收率为81%。
[0820]
【化85】
[0821][0822]
(制备例19)
[0823]
除了使用a6代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-21。收率为80%。
[0824]
【化86】
[0825][0826]
(制备例20)
[0827]
除了使用a6代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-22。收率为83%。
[0828]
【化87】
[0829][0830]
(制备例21)
[0831]
除了使用a6代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-23。收率为83%。
[0832]
【化88】
[0833][0834]
(制备例22)
[0835]
除了使用a6代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-24。收率为79%。
[0836]
【化89】
[0837][0838]
(制备例23)
[0839]
除了使用a7代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-25。收率为86%。
[0840]
【化90】
[0841][0842]
(制备例24)
[0843]
除了使用a7代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-26。收率为84%。
[0844]
【化91】
[0845][0846]
(制备例25)
[0847]
除了使用a7代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-27。收率为91%。
[0848]
【化92】
[0849][0850]
(制备例26)
[0851]
除了使用a7代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-28。收率为82%。
[0852]
【化93】
[0853][0854]
(制备例27)
[0855]
除了使用a8代替a1以外,进行与制备例1同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-29。收率为88%。
[0856]
【化94】
[0857][0858]
(制备例28)
[0859]
除了使用a8代替a1以外,进行与制备例2同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-30。收率为86%。
[0860]
【化95】
[0861][0862]
(制备例29)
[0863]
除了使用a8代替a1以外,进行与制备例3同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-31。收率为93%。
[0864]
【化96】
[0865][0866]
(制备例30)
[0867]
除了使用a8代替a1以外,进行与制备例4同样的操作。对得到的化合物进行与制备例1同样的分析,由此确认到其为下述化合物pag-32。收率为84%。
[0868]
【化97】
[0869][0870]
〔实施例1~28及比较例1~4〕
[0871]
在实施例1~28及比较例1~4中,使用上述pag-1~pag-4及pag-7~pag-32还有下述pag-5及pag-6作为产酸剂(a)。
[0872]
【化98】
[0873][0874]
在实施例1~28及比较例1~4中,使用以下的resin-a作为对碱的溶解性因酸的作用而增大的树脂(树脂(b))。下述结构式中的各结构单元中的括号的右下的数字表示树脂中的结构单元的含量(质量%)。树脂resin-a的质均分子量mw为42000。
[0875]
【化99】
[0876]
resina
[0877][0878]
作为碱可溶性树脂(d),使用以下的resin-b(聚羟基苯乙烯树脂)、resin-c(酚醛清漆树脂(间甲酚单独缩合物))。下述结构式中的各结构单元中的括号的右下的数字表示各树脂中的结构单元的含量(质量%)。树脂resin-b的质均分子量(mw)为2500,分子量分布系数(mw/mn)为2.4。树脂resin-c的质均分子量(mw)为8000。
[0879]
【化100】
[0880]
resin-b
[0881][0882]
【化101】
[0883]
resin-c
[0884][0885]
作为含硫化合物(e),使用以下的含硫化合物t1及t2。
[0886]
【化102】
[0887][0888]
使用二叔丁基吡啶(q1)作为酸扩散控制剂(f)。
[0889]
分别使表1及表2所记载的种类及量的、产酸剂(a)、树脂(b)、碱可溶性树脂(d)、含硫化合物(e)、酸扩散控制剂(f)与表面活性剂(byk310,毕克化学公司制)溶解于丙二醇单甲醚乙酸酯(pgmea),得到各实施例及比较例的感光性树脂组合物。另外,表面活性剂(byk310,毕克化学公司制)以相对于树脂(b)及碱可溶性树脂(d)的合计量为0.05质量份的方式进行添加。
[0890]
实施例1~28及比较例1~4的感光性树脂组合物以固体成分浓度为35质量%的方式进行制备。
[0891]
使用得到的感光性树脂组合物,按照以下的方法评价掩模线性。将结果示出在表1及表2。
[0892]
[掩模线性的评价]
[0893]
准备在直径500mm的玻璃基板的表面上设置有溅射而得的铜层的基板,将实施例及比较例的感光性树脂组合物涂布在该基板的铜层上,形成了膜厚为5μm的感光性层。接着,将感光性层以120℃预烘烤4分钟。预烘烤后,使用线宽2.0μm、间距宽2.0μm的布线间距图案(line and space pattern)的掩模与曝光装置canon fpa-5510iv(佳能公司制),通过波长365nm的紫外线进行图案曝光。接着,将基板载置在加热板上以90℃进行4分钟的曝光后加热(peb)。然后,重复进行共计2次以下操作:将四甲基氢氧化铵的2.38重量%水溶液(显影液,nmd-3,东京应化公司制)滴加到曝光后的感光性层之后,在23℃下静置30秒钟。之后,将抗蚀剂图案表面进行流动水洗涤(漂洗)后,吹送氮气,得到抗蚀剂图案。
[0894]
在上述抗蚀剂图案的形成中,以可形成布线间距(ls)图案的曝光量(j/m2),使焦点适当上下错开,从而与上述抗蚀剂图案的形成同样地形成ls图案。此时,求出该ls图案在目标尺寸
±
10%(即1.80~2.20μm)的尺寸变化率的范围内能够形成的焦深宽度(dof,单位:μm),作为掩模线性的评价基准。dof是指,在同一曝光量下,在使焦点上下错开而进行曝光时,能够以相对于目标尺寸的偏移在规定范围内的尺寸形成抗蚀剂图案的焦深的范围,即,是能够得到忠实于掩模图案的抗蚀剂图案的范围,其值越大越为优选。即,dof的值越大,掩模线性越好。将结果示出在表1及表2。
[0895]
[产酸剂的溶解性的评价]
[0896]
对在实施例1~28及比较例1~4中使用的各产酸剂测量溶解于丙二醇单甲醚乙酸酯(pgmea)的最大浓度。将结果示出在表1及表2。
[0897]
【表1】
[0898][0899]
【表2】
[0900][0901]
根据实施例1~28可知,包含以式(a1)表示的化合物作为通过活性光线或放射线的照射而产生酸的产酸剂(a)的正型感光性树脂组合物形成了掩模线性优异的抗蚀剂图案。此外,产酸剂(a)的溶剂溶解性也良好。
[0902]
另一方面,根据比较例1~4可知,在正型感光性树脂组合物所包含的产酸剂为式(a1)以外的化合物的情况下,与实施例1~28相比,所含产酸剂的溶剂溶解性较差,或者掩模线性较差。
[0903]
(比较制备例1)
[0904]
向混合了2.00g作为n-羟基化合物(a’)的a2和30.0g二氯甲烷的混合物中,添加1.45g作为碱性化合物(d’)的n-乙基二异丙胺,接着,添加1.98g作为磺酰氟化合物(b’)的b1,在室温下搅拌12小时。然后,用1%盐酸洗涤反应液,用纯水进行洗涤,馏去溶剂,由此得到0.17g固体。
[0905]
对得到的化合物进行根据nmr的结构鉴定,未能确认到为上述化合物pag-7。
[0906]
如上述制备例1~6、制备例7~30(实施例)所示,根据本发明的制备方法,能够高效地制造n-有机磺酰氧基化合物。
[0907]
另一方面,在未使用硅烷化剂(c’)的比较制备例1中,未能制造n-有机磺酰氧基化合物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
