1.本发明涉及生物检测技术及临床医学检测技术领域,尤其涉及一种荧光探针及其制备方法和应用。
背景技术:
2.过氧亚硝基阴离子是一种氧自由基,在生物体系中,过氧亚硝基阴离子的半衰期短,能自由的穿透生物膜,通过氧化和硝化蛋白质的氨基酸残基来调控细胞的功能和细胞凋亡,作为一种高活性的氧化剂,更与体内的氧化应激反应密切相关。研究认为,炎症和氧化应激反应是2型糖尿病发生的初始环节,氧自由基的过度产生可引发胰岛细胞的炎性损伤,自由基引起的氧化应激可以使细胞膜上的胰岛素受体受损,受体数量明显减少,与胰岛素结合作用降低,也就是说加速受体中胰岛素抵抗的发生。随着肿瘤细胞学的发展,氧化应激对机体细胞的影响逐渐明确,氧化应激也是近年来关于肿瘤形成及影响因素的研究热点,氧化应激产物可促进细胞的增殖分化,最终将导致细胞凋亡减少,甚至过度增殖从而引发肿瘤。
3.由于细胞粘度是生物系统中关键的微环境相关参数,细胞粘度的异常变化与多种疾病和功能障碍密切相关,多种疾病不可避免地会在细胞水平上引起粘度的异常变化,粘度增高会导致循环系统疾病如动脉硬化、糖尿病、肿瘤、脑血管疾病等。
4.近些年来,靶向过氧亚硝基阴离子和粘度的探针化合物
ⅴ
已经得到了相应的研究和开发,取得了巨大的经济效益,然而目前研究均局限在单独探测过氧亚硝基阴离子或细胞粘度,易出现检测假阳性、灵敏度低的问题。
5.因此,同时靶向过氧亚硝基阴离子和粘度的探针化合物开展研究具有重要意义。
技术实现要素:
6.针对现有技术所存在的技术问题,本发明提供一种荧光探针,用以解决现有技术中的探针不能同时靶向过氧亚硝基阴离子和细胞粘度的缺陷。
7.为达到上述目的,本发明采用如下技术方案:
8.一种荧光探针,所述荧光探针的结构式如式(
ⅴ
)所示:
9.10.本发明另一目的在于提供一种荧光探针的制备方法,用于制备如上述所述的荧光探针,包括如下步骤:
11.步骤s1、合成2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)
‑ꢀ
丙二腈,所述2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈的构型为e构型;
12.步骤s2、所述2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)
‑ꢀ
丙二腈和2-(4-(溴甲基)苯基)-4,4,5,5-四甲基-1,3,2-二氧硼杂环戊烷反应,合成所述荧光探针。
13.进一步,所述步骤s1中合成所述2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5
‑ꢀ
二甲基环己-2-烯基)-丙二腈采用如下方法:在惰性气体保护下,以2-(3,5,5
‑ꢀ
三甲基环己-2-烯基)-丙二腈和4-(二乙氨基)水杨醛为反应原料,二氯甲烷、乙腈或乙醇为溶剂,在哌啶催化下进行反应,得到所述2-(3-(4-二乙氨基-2
‑ꢀ
羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈。
14.进一步,所述2-(3,5,5-三甲基环己-2-烯基)-丙二腈和所述4-(二乙氨基) 水杨醛的摩尔比在1:1至1:3范围内。
15.进一步,所述反应的温度在100至130℃范围内,所述反应的时间在6 至12h范围内。
16.进一步,所述步骤s2中合成所述荧光探针采用如下方法:在惰性气体保护下,以n,n-二甲基甲酰胺为溶剂,碳酸钾为催化剂,所述2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈和所述2-(4-(溴甲基)苯基)-4,4,5,5-四甲基-1,3,2-二氧硼杂环戊烷在预设条件下进行反应,得到所述荧光探针。
17.进一步,所述2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)
‑ꢀ
丙二腈和所述2-(4-(溴甲基)苯基)-4,4,5,5-四甲基-1,3,2-二氧硼杂环戊烷的摩尔比在1:1至1:3范围内。
18.进一步,所述预设条件包括:反应温度在100至160℃范围内、反应时间在6至12h范围内。
19.本发明第三目的在于提供一种如上述所述的荧光探针的应用,所述荧光探针用于检测生物样本中的过氧亚硝基离子和的细胞粘度。
20.与现有技术相比,本发明的有益效果为:
21.(1)本发明所述的荧光探针,具有近红外荧光发射,组织穿透能力强,染料稳定性好,可同时靶向过氧亚硝基阴离子和细胞粘度,双靶检测的荧光探针化合物
ⅴ
相对于单靶检测的具有较大优势,可以降低单一靶标检测的假阳性,提高灵敏度。
22.(2)本发明所述的荧光探针的制备方法,合成工艺简单,分离纯化过程简便,反应条件温和,易于实现规模化生产。
附图说明
23.为了更清楚地说明本发明或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些
附图获得其他的附图。
24.图1是本发明实施例所述的荧光探针化合物
ⅴ
随甘油粘度变化的荧光强度变化图;
25.图2是本发明实施例所述的荧光探针化合物
ⅴ
对不同浓度的过氧亚硝基离子响应表征图,其中,图2(a)为荧光探针化合物
ⅴ
与过氧亚硝基离子浓度变化的荧光强度变化图,图2(b)为荧光强度与过氧亚硝基离子浓度在0至 20μm范围内的线性关系图;
26.图3为荧光探针化合物
ⅴ
对过氧亚硝基阴离子、甘油以及混合物的响应表征图,其中,图3(a)为荧光探针化合物
ⅴ
对20μm onoo-的荧光强度,图 3(b)为荧光探针化合物
ⅴ
在50%粘度的甘油的荧光强度,图3(c)为荧光探针化合物
ⅴ
在50%粘度甘油和20μm onoo-混合物下的荧光强度;
27.图4是本发明实施例所述荧光探针化合物
ⅴ
和不同分析物反应后的荧光强度的变化图;
28.图5是本发明实施例所述荧光探针化合物
ⅴ
在不同浓度粘度诱导条件下在正常肺细胞的荧光成像图,图5(a)为荧光成像图,图5(b)为细胞荧光强度的量化图;
29.图6是本发明实施例所述荧光探针化合物
ⅴ
在不同浓度过氧亚硝基条件下在正常肺细胞的荧光成像图,图6(a)为荧光成像图,图6(b)为细胞荧光强度的量化图;
30.图7是本发明实施例所述荧光探针化合物
ⅴ
在肺癌细胞的荧光成像图,图7(a)为荧光成像图,图7(b)为细胞荧光强度的量化图;
31.图8为本发明实施例所述荧光探针的检测机理图。
具体实施方式
32.为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明中的附图,对本发明中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
33.在本发明的描述中,应当说明的是,在本发明的实施例中所提到的术语“第一”、“第二”仅用于描述目的,并不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。
34.在本技术实施例的描述中,术语“一些具体实施方式”的描述意指结合该实施例或示例描述的具体特征、结构、材料或特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施或实例。而且,描述的具体特征、结构、材料或特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
35.荧光探针具有无损、易操作、可实现可视化检测等特点而受到普遍重视;相比于紫外可见方法,荧光探针具有更高的灵敏度以及高时空分辨率,被广泛应用于分子靶标的检测及示踪。
36.本发明的实施例提供了一种荧光探针,该荧光探针为同时靶向过氧亚硝基离子和细胞粘度的近红外荧光探针,该荧光探针的结构式如式(
ⅴ
)所示:
[0037][0038]
具体地,该荧光探针的分子式为c
36h44
bn3o3,分子量为577.3473。
[0039]
本实施例提供的结构式为式(
ⅴ
)的荧光探针,其具有近红外荧光发射,组织穿透力强,染料稳定性好,且该荧光探针可同时靶向过氧亚硝基阴离子和细胞粘度,双靶检测的荧光探针化合物
ⅴ
相对于单靶检测的具有较大优势,可以降低单一靶标检测所引起的假阳性,提高灵敏度,实现对临床样本的快速、准确初步的筛选。
[0040]
本发明的实施例还提供了该荧光探针的制备方法,包括如下步骤:
[0041]
步骤s1、合成2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)
‑ꢀ
丙二腈,2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈的构型为e构型;
[0042]
步骤s2、2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈和2-(4-(溴甲基)苯基)-4,4,5,5-四甲基-1,3,2-二氧硼杂环戊烷反应,合成荧光探针。
[0043]
本实施例提供的合成荧光探针的方法,合成工艺简单,分离纯化过程简便,反应条件温和,易于实现规模化生产。
[0044]
具体地,步骤s1中合成2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈(以下简称化合物ⅲ)采用如下方法:在惰性气体保护下,以2-(3,5,5-三甲基环己-2-烯基)-丙二腈(以下简称化合物ⅰ)和4-(二乙氨基) 水杨醛(以下简称化合物ⅱ)为反应原料,二氯甲烷、乙腈或乙醇为溶剂,在哌啶催化下进行反应,得到2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己
ꢀ‑
2-烯基)-丙二腈,合成路径如下:
[0045][0046]
其中,化合物ⅰ和化合物ⅱ的摩尔比在1:1至1:3范围内,反应的温度在在100℃至130℃范围内,反应的时间在6至12h范围内。
[0047]
反应结束后,将反应产物经过减压蒸馏,脱除反应溶剂后,得到粗产物,将粗产物用硅胶柱层析分离纯化,得到e构型的2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈。
[0048]
具体地,步骤s2中合成荧光探针采用如下方法:在惰性气体保护下,以n,n-二甲基甲酰胺为溶剂,碳酸钾为催化剂,2-(3-(4-二乙氨基-2-羟基苯乙烯)-5,5-二甲基环己-2-烯基)-丙二腈和2-(4-(溴甲基)苯基)-4,4,5,5-四甲基
ꢀ‑
1,3,2-二氧硼杂环戊烷(以下简称化合物ⅳ)在预设条件下进行反应,经过分离和纯化后,得到荧光探针,合成路径如下:
[0049][0050]
其中,化合物ⅲ和对化合物ⅳ的摩比在1:1至1:3范围内,预设条件包括:反应温度在100至160℃范围内、反应时间在6至12h范围内。
[0051]
反应结束后,将反应产物经过减压蒸馏脱除反应溶剂,再经过萃取和硅胶柱层析分离纯化后,得到荧光探针。
[0052]
本发明的实施例还提供了上述所述的荧光探针的应用,该荧光探针用于检测生物样本中的过氧亚硝基离子和的细胞粘度。
[0053]
本实施例中提供的荧光探针,结合图8所示,左边为荧光探针化合物v 的探针结构,解释了探针结构与过氧亚硝基和细胞粘度“双锁”的机制原理,右边是荧光探针化合物v的响应机制验证,图8(a)是荧光探针化合物v与过氧亚硝基单独反应,图8(b)是荧光探针化合物v与过氧亚硝基和细胞粘度同时反应,图8(c)是荧光探针化合物v与体系粘度单独反应,可见在细胞粘度或过氧亚硝基单独存在时,探针的响应较低,在过氧亚硝基与粘度同时存在时候,对这两种物质“双锁”的探针化合物v响应最高。
[0054]
由此可见,本发明制备的荧光探针对于细胞粘度及过氧亚硝基具有较高检测灵敏度,基于肿瘤和糖尿病病理进程中粘度和过氧亚硝基含量上升的特点,本发明提供的“双锁”检测探针化合物
ⅴ
在实现对两种重要病理指标同时检测的前提下,可有效减少单一指标检测所引起的假阳性,从而实现对临床样本的快速、准确初步的筛选。
[0055]
在上述实施例的基础上,本实施例还提供如下多个具体实施方式,对本实施例进行更进一步地说明。
[0056]
实施例1
[0057]
一种荧光探针的制备方法,具体包括以下步骤:
[0058]
步骤s1、合成化合物ⅲ:
[0059]
[0060]
将化合物ⅰ2-(3,5,5-三甲基环己-2-烯基)-丙二腈(1.86g,10mmol)和化合物ⅱ4-(二乙氨基)水杨醛(2.32g,12mmol)加入到含20ml乙醇的反应瓶中,再加入哌啶(0.085g,1mmol)作为催化剂,并在氮气保护下,在100℃下加热回流反应16h,反应结束后,将反应产物经过减压蒸馏,脱除反应溶剂,得到粗产物,将粗产物经柱层析分离纯化后,得到化合物ⅲ。
[0061]
本步骤中化合物ⅲ的收率为65%,其中,柱层析分离纯化中洗脱剂为石油醚和乙酸乙酯,且石油醚和乙酸乙酯的体积比为3:1。
[0062]
步骤s2、合成化合物v:
[0063][0064]
将化合物ⅲ(0.36g,1mmol)和化合物ⅳ2-(4-(溴甲基)苯基)-4,4,5,5-四甲基
ꢀ‑
1,3,2-二氧硼杂环戊烷(0.59g,2.0mmol)加入到含10毫升n,n-二甲基甲酰胺的反应瓶中,然后加入碳酸钾(0.28g,2.0mmol),在氮气保护下,于120℃回流反应12h,反应结束冷却至常温后,加入20ml水,采用萃取三次,合并有机相,并用无水硫酸钠干燥去除水分后,将有机相经柱层析分离纯化后,得到纯化后的化合物v。
[0065]
本步骤中化合物v的收率为55%,其中,柱层析分离纯化中洗脱剂为二氯甲烷和甲醇,且二氯甲烷和甲醇的体积比为30:1。
[0066]
通过核磁氢谱、碳谱和高分辨质谱表征对本发明实施例1中合成的荧光探针的结构进行分析,证明采用实施例1中的方法制备得到的物质确实为式 (
ⅴ
)所示的结构,具体结果如下:
[0067]1hnmr(400mhz,dmso)δ7.77
–
7.61(m,3h),7.52
–
7.41(m,3h), 6.35
–
6.19(m,2h),5.34
–
5.17(m,2h),3.34(d,j=11.4hz,4h),1.27(d,j= 17.9hz,18h),1.10
–
0.89(m,12h).
[0068]
13
c nmr(100mhz,cdcl3)δ166.74,159.77,154.83,145.61,144.25, 141.65,137.70,136.55,133.78,130.68,127.55,124.34,118.11,113.13,106.23, 99.46,87.72,71.56,67.98,46.42,42.05,38.75,32.52,28.74,24.62,12.99.
[0069]
hrms(esi):calcd.for[c
36h44
bn3o3 h]
578.3476;found 578.3473
[0070]
对实施例1中合成的荧光探针化合物(
ⅴ
)进行性能以及在靶向过氧亚硝基离子和细胞粘度上的应用进行分析,具体如下:
[0071]
1、荧光探针化合物
ⅴ
对甘油粘度的响应
[0072]
1.1荧光探针化合物
ⅴ
化合物的配制
[0073]
称取一定量实施例1制得的探针化合物
ⅴ
,用二甲亚砜溶液配置成 10mm母液备用。
[0074]
1.2不同粘度甘油的配制
[0075]
将100%的甘油用磷酸盐缓冲液(ph7.4)分别配置成粘度为10%、20%、 30%、40%、50%、60%、70%、80%、90%的甘油。
[0076]
1.3甘油性能测定实验
[0077]
将终浓度为探针化合物
ⅴ
(10μm)溶液与粘度为10%-90%的甘油等体积混合,用spectramax id5酶标仪测定混合液在690nm处的荧光发射强度。
[0078]
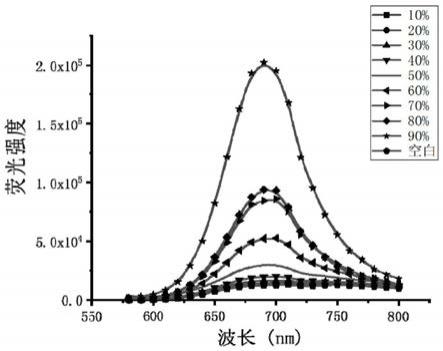
图1为37
°
下荧光探针化合物
ⅴ
和不同粘度甘油反应后的荧光发射光谱,从图1可以看出,荧光强度随粘度增高呈现明显上升趋势,可以证明,荧光探针化合物
ⅴ
可以实现粘度的实时检测。这是由于随着微环境粘度的增加,分子内旋转受到限制,导致分子内电荷转移被抑制,最终使探针的荧光增强。
[0079]
2、荧光探针化合物
ⅴ
对过氧亚硝基阴离子的响应
[0080]
2.1过氧亚硝基阴离子溶液的配制
[0081]
将5ml浓度0.6m的亚硝酸钠溶液加入到5ml浓度0.7m的过氧化氢溶液中,用磁力搅拌器高速搅拌混合,然后迅速加入1.5m的氢氧化钠溶液,测量302nm处的吸光度值为631.26nm(摩尔吸光系数为1670m-1
cm-1
),根据朗伯比尔定律c
过氧亚硝基阴离子
=abs302nm/1.67mmol/l,得到过氧亚硝基阴离子溶液浓度为378μm。
[0082]
2.2过氧亚硝基阴离子(onoo-)溶液的配制
[0083]
利用浓度50%的甘油将过氧亚硝基阴离子分别配置成浓度为2、5、10、 15、20μm的溶液,将探针化合物
ⅴ
(10μm)溶液分别与含浓度为2-20μm过氧亚硝基阴离子化合物溶液等体积混合,得到混合溶液,用spectramax id5 酶标仪测定混合溶液在690nm处的荧光发射强度。得到如图2所示的结果图,在几秒内,明显可见荧光强度随浓度增高上升,因此可以证明,荧光探针化合物可以实现过氧亚硝基阴离子活性的实时检测。图2为荧光探针化合物
ⅴ
对不同浓度的过氧亚硝基离子响应表征图。
[0084]
其中,图2(a)为荧光探针化合物
ⅴ
与过氧亚硝基离子浓度变化的荧光强度变化图,从图2(a)可以看出,荧光强度随浓度增高呈现明显上升趋势,比较增长前后的倍数差,可以选择过氧亚硝基阴离子溶液(20μm)为最适反应的过氧亚硝基阴离子浓度。
[0085]
图2(b)为荧光强度与过氧亚硝基离子浓度在0至20μm范围内的线性关系图,可以看出,反应体系的荧光强度与过氧亚硝基阴离子的含量成正比,表明化合物
ⅴ
可用于反应体系中过氧亚硝基阴离子的定量检测。线性曲线可以测定检出限,检出限越低可说明方法的灵敏度越高,根据检出限公式 lod=3*σ/s(其中σ为空白标准偏差,s为校正曲线斜率),计算,本检测试验的检出限为0.3。
[0086]
3、荧光探针化合物
ⅴ
对过氧亚硝基阴离子和甘油混合物的响应
[0087]
将荧光探针化合物
ⅴ
(10μm)分别与过氧亚硝基阴离子溶液(20μm)、50%粘度的甘油,以及过氧亚硝基阴离子溶液(20μm)和50%粘度的甘油混合物进行反应,用spectramax id5酶标仪进行荧光强度测试,得到如图3所示的结果图。
[0088]
图3为荧光探针化合物
ⅴ
对过氧亚硝基阴离子、甘油以及混合物的响应表征图,其中,图3(a)为荧光探针化合物
ⅴ
对20μm onoo-的荧光强度,图 3(b)为荧光探针化合物
ⅴ
在50%粘度的甘油的荧光强度,图3(c)为荧光探针化合物
ⅴ
在50%粘度甘油和20μm onoo-混合物下的荧光强度。
[0089]
从图3可以看出,比较增长前后的倍数差,50%粘度的甘油和过氧亚硝基阴离子
(20μm)混合后,与探针化合物
ⅴ
(10μm)的荧光响应最强。
[0090]
4、荧光探针化合物
ⅴ
的选择性进行测定
[0091]
对实施例1中合成的荧光探针化合物
ⅴ
的选择性进行测定,具体采用如下方法:
[0092]
用50%甘油溶液将次氯酸、过氧化氢、谷胱甘肽、同型半胱氨酸、溴化铜、硫酸亚铁、硝酸钠、硝酸钾、谷氨酸、色氨酸、苏氨酸、蛋氨酸、半胱氨酸分别配制为100μm、过氧亚硝基阴离子(20μm)的试样,配制完成后将各个试样与荧光探针化合物
ⅴ
(10μm)分别进行反应,并设置一空白对照-仅浓度为20μmol/l的荧光探针化合物
ⅴ
,用spectramax id5酶标仪测定各组在690nm处荧光强度值,得到如图4所示。
[0093]
从图4中我们可以看出,常见氨基酸、金属离子以及活性氧、巯基化合物和荧光探针化合物
ⅴ
反应后荧光强度的变化较小,显著弱于过氧亚硝基阴离子,也即说明了荧光探针化合物
ⅴ
对过氧亚硝基阴离子的选择性很好,荧光探针化合物
ⅴ
可以实现过氧亚硝基阴离子与细胞粘度混合物的选择性检测。
[0094]
5、荧光探针化合物
ⅴ
体内细胞性能测定
[0095]
5.1试剂配制
[0096]
用无血清培养基配制林西多明(体内过氧亚硝基阴离子供体,20μm、 60μm、100μm)、依托泊苷(体内粘度诱导剂20μm、60μm、100μm)各1ml。
[0097]
5.2荧光探针化合物
ⅴ
检测体内肺正常细胞
[0098]
对实施例1中合成的荧光探针化合物
ⅴ
在体内肺正常细胞中的荧光成像进行测定,具体采用如下方法:
[0099]
取贴壁24h生长的正常肺细胞置于6孔板生长过夜,实验前,用磷酸盐缓冲液(ph7.4)洗涤漂浮细胞1次,然后,在第一块板加入林西多明(20μm、 60μm、100μm)及空白对照,第二块板加入依托泊苷(20μm、60μm、100μm) 及空白对照,将细胞放入温箱孵育30分钟后,吸取液体丢弃,随后加入荧光探针化合物
ⅴ
(10μm)放置温箱孵育30分钟,取出后,将枪头深入液面下加入染核试剂dapi(5μm),避光静置5min,吸取丢弃液体,用磷酸盐缓冲液洗涤1次,加入1ml的磷酸盐缓冲液在显微镜下记录明场、染核场、荧光场图像,得到图5、图6结果。
[0100]
图5是荧光探针化合物
ⅴ
在不同浓度粘度诱导条件下在正常肺细胞的荧光成像图,图5(a)为荧光成像图,图5(b)为细胞荧光强度的量化图。从图5 可以看出,伴随粘度诱导剂的浓度增高,探针化合物
ⅴ
荧光强度也随之增加,且在20μm达到平台,说明体内粘度能与荧光探针化合物
ⅴ
产生反应。
[0101]
图6是荧光探针化合物
ⅴ
在不同浓度过氧亚硝基条件下在正常肺细胞的荧光成像图,图6(a)为荧光成像图,图6(b)为细胞荧光强度的量化图;从图 6可以看出,随过氧亚硝基的浓度增高,荧光探针化合物
ⅴ
的荧光强度也随之增高,说明体内过氧亚硝基能与荧光探针化合物
ⅴ
产生反应。
[0102]
5.3荧光探针化合物
ⅴ
检测体内肺癌细胞
[0103]
对实施例1中合成的荧光探针化合物
ⅴ
在体内肺癌细胞中的荧光成像进行测定,具体采用如下方法:
[0104]
取贴壁24h生长的肺癌置于6孔板生长过夜,实验前,用磷酸盐缓冲液 (ph7.4)洗涤漂浮细胞1次,然后,第一孔加入林西多明(100μm),第二孔加入依托泊苷(20μm),设置一
组空白对照,将细胞放入温箱孵育30分钟后,吸取液体丢弃,随后加入探针化合物
ⅴ
(10μm)放置温箱孵育30分钟,取出后,将枪头深入液面下加入染核试剂dapi(5μm),避光静置5min,吸取丢弃液体,用磷酸盐缓冲液洗涤1次,加入1ml的磷酸盐缓冲液在显微镜下记录明场、染核场、荧光场图像,得到图7结果。
[0105]
图7是荧光探针化合物
ⅴ
在肺癌细胞的荧光成像图,图7(a)为荧光成像图,图7(b)为细胞荧光强度的量化图;从图7可以看出,在粘度与过氧亚硝基同时存在的情况下,荧光探针化合物
ⅴ
的荧光强度比单独存在时更高。
[0106]
在此有必要指出的是,以上实施例仅限于对本发明的技术方案做进一步的阐述和说明,并不是对本发明的技术方案的进一步的限制,本发明的方法仅为较佳的实施方案,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。