1.本发明属于免疫医学领域,具体涉及一种人源包虫病抗原的重组蛋白及其应用。
背景技术:
2.包虫病又名棘球蚴病,是一种人畜共患病,在中国中西部地区(西藏、青海、四川、新疆等地)感染尤其严重。人源包虫病主要分为囊型包虫病和泡型包虫病。影像学检测是最直观最常用的包虫病诊断方法,但是由于包虫病的潜伏期较长,并且只有在包虫病形成的包囊大到一定程度时才能够通过影像学检测到,所以血清学检测是影像学诊断包虫病的重要辅助手段之一。目前,可以被用来诊断包虫病的血清学诊断抗原主要有抗原b(antigen b)和抗原5(antigen 5)以及与这两种抗原相关的一些重组抗原。
3.迄今为止,已经描述了几种用于包虫病实验室诊断的方法,包括抗体、抗原和细胞因子的检测。其中,抗体检测的发展主要依赖于包虫抗原种类的发展。但是不论天然纯化抗原还是重组纯化抗原,均在特异性和/或敏感性方面有一定的不足。更为重要的是人源包虫病因涉及到取样困难、分离包虫蛋白困难等因素,一直没有出现更多的可用于血清学检测的抗原。
4.现有技术中开发针对包虫抗原的抗体的困难如下:
5.1)从包虫病人术后分离的包虫囊中提取包虫蛋白并鉴定,本身是一个技术难点。如果鉴定到的包虫蛋白本身种类就很少,想从中选取可能作为包虫抗原的蛋白将更加困难。
6.2)单一抗原种类少。目前最广泛应用的包虫病诊断抗原是抗原b和抗原5,许多研究表明这两种抗原在血清学检测时会产生一定的假阳性或假阴性。
7.3)商品化包虫抗原是天然纯化抗原,分离纯化自细粒棘球蚴破碎后的可溶性抗原片段,是一种包含多种包虫蛋白的混合物。混合的蛋白越多越容易在血清学检测时产生更多假阴性或假阳性的结果。
8.因此,亟需一种能够高灵敏度、高特异性的同时还能高免疫反应率地检测包虫病的诊断抗原。
技术实现要素:
9.为了解决现有技术中缺少高灵敏度、高特异性和高免疫反应率检测包虫病的诊断抗原的技术问题,本发明提供了一种人源包虫病抗原的重组蛋白及其应用,尤其是在制备抗包虫病抗体或诊断细粒棘球蚴所致疾病的诊断剂中的应用,具有较高的免疫反应率、特异性和灵敏度。
10.本发明的第一方面提供一种重组蛋白或其突变,所述重组蛋白包含如seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9和seq id no:10所示的氨基酸序列的一种或多种;
11.所述突变的氨基酸序列与所述重组蛋白的氨基酸序列具有至少80%、85%、90%、
95%、98%、99%的同一性,并保持所述重组蛋白的功能。
12.优选地,所述重组蛋白包含如seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9和seq id no:10所示的氨基酸序列。
13.本发明的第二方面提供一种分离的核酸,所述分离的核酸编码如本发明第一方面所述的重组蛋白或其突变。
14.本发明的第三方面提供一种重组表达载体,所述重组表达载体包含如本发明第二方面所述的分离的核酸。
15.本发明的第四方面提供一种包含如本发明第二方面所述分离的核酸或如本发明第三方面所述的重组表达载体的转化体,其中,所述转化体为细菌或真核细胞。
16.优选地,所述细菌为e.coli bl21。
17.更优选地,所述转化体包含如seq id no:22所示的氨基酸序列。
18.本发明的第五方面提供一种检测包虫病的试剂盒,所述试剂盒包括如本发明第一方面所述的重组蛋白或其突变作为抗原检测包虫病。
19.优选地,所述试剂盒为间接elisa检测试剂盒,所述间接elisa检测试剂盒还包括第二抗体、包被液、洗液、显色液、终止液和稀释液。
20.本发明的第六方面提供一种抗包虫病的sirna或mrna疫苗,所述疫苗包含编码如本发明第一方面所述的重组蛋白或其突变的rna序列。
21.本发明的第七方面涉及如本发明第一方面所述的重组蛋白或其突变在制备抗包虫病抗体中的应用。
22.本发明的第八方面涉及如本发明第一方面所述的重组蛋白或其突变在制备诊断细粒棘球蚴所致疾病的诊断剂中的应用。
23.在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
24.本发明所用试剂和原料均市售可得。
25.本发明的积极进步效果在于:
26.1)构建了人源包虫病抗原的重组蛋白,对包虫病患者的免疫应答率达到100%,可以用来制作elisa试剂盒并用于临床检测人源包虫病。
27.2)扩充了包虫抗原数据库,所述重组蛋白可大量纯化,方便大规模筛选人源包虫病。
28.3)由于所述重组蛋白针对细粒棘球蚴具有较高的特异性和灵敏度,其单一使用或组合使用有可能提升实验室诊断包虫病的特异性和灵敏性。
附图说明
29.图1为七个囊液组分提取到的全蛋白的sds-page和western blotting结果示意图。
30.图2为mg2重组蛋白的纯化结果示意图。
31.图3为纯化后mg2重组蛋白的western blotting验证实验结果示意图。
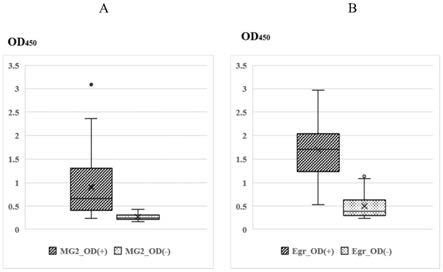
32.图4为elisa实验结果箱形图,其中a为mg2的elisa结果,b为egr的elisa结果。
具体实施方式
33.下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
34.实施例1
35.1、包虫病人术后分离的包虫囊鉴定包虫蛋白
36.1)首先将6个包虫病人(第一批)术后分离的包虫囊根据其组织结构分为四部分提取蛋白,由内向外分别是原头蚴、囊液、生发层和角皮层;又根据其囊液透明与否,将6个包虫囊分为囊液透明组和囊液非透明组。
37.2)对每个包虫囊的四个组分均进行了蛋白提取,并将提取的蛋白进行液态酶解,随后使用qe质谱仪进行lc-ms/ms鉴定;
38.3)qe下机的原始数据使用maxquant蛋白鉴定软件,使用人和包虫蛋白数据库合集,进行包虫蛋白质鉴定,统计鉴定结果并确定包虫蛋白含量多的包虫囊部分,结果如表1和表2所示;
39.4)由表1可知,有两点基本结论:一是鉴定的包虫蛋白更多的组织部分是囊液和原头蚴这两个部分;二是只有囊液透明组的囊液和原头蚴部分提取的蛋白中包含有更多的包虫蛋白。
40.5)根据上述第一点基本结论,为了鉴定到更多包虫蛋白,追加提取了另外10个包虫病人(第二批)术后包虫囊的囊液和原头蚴的蛋白,结果如表3和表4所示,仍然是囊液透明组的囊液和原头蚴部分提取的蛋白中包含更多包虫蛋白。
41.表1第一批6个包虫病人组中囊液透明组的蛋白质鉴定结果(_1表示原头蚴;_2表示囊液;_3表示生发层;_4表示角皮层)
[0042][0043]
表2第一批6个包虫病人组中囊液非透明组的蛋白质鉴定结果(_1表示原头蚴;_2表示囊液;_3表示生发层;_4表示角皮层)
[0044]
[0045][0046]
表3第二批10个包虫病人组中囊液透明组的蛋白质鉴定结果(_1表示原头蚴;_2表示囊液;_3表示生发层;_4表示角皮层)
[0047][0048]
表4第二批10个包虫病人组中囊液非透明组的蛋白质鉴定结果(_1表示原头蚴;_2表示囊液;_3表示生发层;_4表示角皮层)
[0049]
[0050][0051]
2、western blotting验证、切胶酶解并进行质谱鉴定(gelc-ms/ms)
[0052]
1)根据16个样本的囊液和原头蚴的qe鉴定结果,我们选取no.1、no.2、no.3、no.7、no.8、no.9、no.10七个囊液透明组样本的原头蚴和囊液组分分别与病人血浆进行western blotting实验,以验证包虫病人和正常西藏人的血浆与提取的全蛋白之间是否有免疫反应。
[0053]
2)因部分样本的原头蚴组分提取到的蛋白总量很少,故主要进行了囊液透明样本的囊液组分蛋白的western blotting实验,结果如图1所示,以no.1病人血浆为例,包虫病人和正常西藏人血浆与七个囊液透明组样本囊液组分蛋白的免疫反应图谱。其他病人血浆和正常西藏人血浆对七个样本蛋白的免疫反应图谱均与no.1病人相似。
[0054]
结果显示,七个囊液组分提取到的全蛋白对病人血浆存在强烈的免疫反应,而对正常西藏人血浆基本无反应。
[0055]
3)根据上述2)的sds-page图谱,我们对照western blotting的免疫条带对sds-page胶进行了切胶酶解,以期能够通过切胶分离鉴定到相应分子量区段里的更多包虫蛋白,增加找到与血浆发生免疫反应的包虫抗原的几率。另外,这样可以减少高丰度蛋白对鉴定的影响。
[0056]
4)为了减少损失和减轻工作量,统一将七个囊液透明组样本中的囊液组分蛋白根据western blotting免疫条带分成了10个组分,随后各组分分别进行了胶内酶解。
[0057]
5)经过qe-hf-x质谱仪的lc-ms/ms分析后,maxquant软件使用与鉴定蛋白中相同的数据库进行了蛋白搜库鉴定。结果如表5所示,括号中的数字表示总鉴定出的蛋白质,而括号外的数字表示每个组分中的包虫蛋白。
[0058]
6)通过数据分析可知,1_2、2_2和10_2这三个样本切胶分离所鉴定到的包虫蛋白包含了其余四个样本所鉴定到的包虫蛋白,所以,后续包虫抗原的候选从这三个样本各组分共同鉴定到的包虫蛋白中寻找。
[0059]
表5七个囊液透明样本中囊液组分蛋白切胶酶解的蛋白片段鉴定结果
[0060][0061]
3、筛选作为候选抗原的包虫蛋白
[0062]
1)将同一组分在三个样本中鉴定到的共同蛋白作为候选抗原库,最终10个组分一共产生了93个蛋白。
[0063]
2)这93个蛋白首先与人的蛋白数据库进行同源比对,删除同源性大于20%的蛋白或蛋白片段,以及已经被选为包虫抗原的那些蛋白后,对剩余的蛋白进行b细胞抗原表位的预测。
[0064]
4、抗原表位预测以及重组质粒构建
[0065]
1)使用在线预测工具http://tools.iedb.org/bcell/预测抗原表位,将蛋白质序列导入即可得到关于此蛋白可能成为抗原表位的序列列表,即抗原表位列表。
[0066]
2)根据每一个候选蛋白的抗原表位列表,选取包含一个或多个表位的序列片段组成重组蛋白的序列,并且将此序列导入比对工具中与人的蛋白质数据库进行比对,只有与人的同源蛋白相似度《=20%的序列片段才被选中构建重组蛋白。
[0067]
3)最终获得11个蛋白序列片段,并通过分子克隆技术插入到pet-30a( )质粒中构建重组质粒,并通过测序确认片段已被插入。
[0068]
5、重组蛋白的表达与纯化
[0069]
1)重组质粒转入bl21(de3)中进行小量试表达,确认重组蛋白可以表达且分子量正确后,再进行扩培。
[0070]
2)收集的菌液经过超声提取重组蛋白后,再通过质粒携带的his-tag进行镍柱纯化。
[0071]
6、重组质粒表达蛋白的western blotting验证
[0072]
纯化后的11个重组蛋白和商品化抗原(包虫纯化抗原echinococcusgranulosus,简称egr,杭州亿米诺生物科技有限公司,ym-vi08)分别与16个术后病人血浆样本进行western blotting实验,结果显示只有4个重组蛋白与16个术后病人血浆样本的免疫反应率大于或等于商品化抗原,故选择这4个重组蛋白作为候选包虫抗原进行更多血浆样本的
elisa验证试验。
[0073]
本实施例以murinoglobulin-2蛋白的截短蛋白(简称mg2重组蛋白)为例构建重组质粒。
[0074]
如表6所示,所述mg2重组蛋白包含10个抗原表位,所述抗原表位的氨基酸序列如seq id no:1-10所示,核苷酸序列如seq id no:11-20所示。
[0075]
所述重组质粒包含如seq id no:21所示的mg2重组蛋白核苷酸序列,对应的mg2重组蛋白氨基酸序列如seq id no:22所示。
[0076]
所述mg2重组蛋白的纯化结果如图2所示,图中所示为mg2重组蛋白的梯度洗脱结果,每个泳道上样量均为10μl。
[0077]
所述mg2重组蛋白的western blotting验证结果如图3所示,只统计43kd和34kd之间有明显条带的样本时,mg2重组蛋白的免疫反应率为100%,商品化抗原的免疫反应率为75%。
[0078]
在使用商品化抗原egr检测时,最主要依靠两种抗原antigen b和antigen 5,其中antigen b在诊断人源包虫病时发挥功能的最主要分子量大小在43kd和34kd之间,而且在16kd和24kd等处会出现因antigen b降解为蛋白亚基后与病人血浆作用而发生的免疫反应,如图3所示的western blotting结果也证明了这一点。
[0079]
与基于基因组学的顺向思维的直接利用包虫组织的dna进行pcr扩增得到与包虫抗原相关的序列的方法不同,本实施例中包虫抗原的获得基于蛋白组组学的逆向思维,通过切胶酶解并质谱检测,即gels-ms/ms技术,筛选出来的。本质上是通过蛋白质组学技术获得的目标物,有一定的实验验证基础。
[0080]
表6mg2重组蛋白的b细胞抗原表位、核苷酸序列和氨基酸序列
[0081][0082]
实施例2
[0083]
本实施例使用如实施例1所述的mg2重组蛋白,检测对象为60例b超阳性血浆(含疑似)样本和33例正常人血浆(确定为阴性)样本,按照间接elisa的标准操作步骤进行实施验证。
[0084]
1、elisa实验操作步骤
[0085]
1)抗原定量:每种抗原在包被前均使用移液枪吹匀,并使用微量紫外分光光度计给抗原定量,以确保蛋白未降解。在a280处无吸收峰,则说明抗原量很低,不宜用于包被;若蛋白析出或有不溶,则滴加8m尿素后吹匀,离心取上清并使用bradford方法重新定量蛋白浓度。
[0086]
2)包被:对比抗原管壁浓度及测量值,就低取值;包被量为2μg/ml、10ml/板,按照实际使用量配制包被抗原量;
[0087]
包被的elisa板上标记:抗原编号、名称、标签、包被日期及板子编号等,若包被浓度不是2μg/ml则需要标明包被浓度。标记完elisa板后,加入100μl/孔包被抗原,4℃包被过夜或37℃包被2h。
[0088]
3)洗板:包被完的板子,用洗板机洗板1次,于吸水纸上拍干。
[0089]
4)封闭:200μl/孔的2%脱脂奶粉作为封闭液进行封闭,4℃封闭过夜或37℃封闭2h。
[0090]
5)洗板:封闭完的板子,用洗板机洗板1次,于吸水纸上拍干。
[0091]
6)加一抗:加入血浆样本,使用pbs作为稀释液按照体积比1:500稀释血浆,37℃孵育1h。
[0092]
7)洗板:用洗板机洗板5次,于吸水纸上拍干。
[0093]
8)加第二抗体(二抗):因一抗来源为人的血浆,故使用山羊抗人二抗(碧云天,a0201)按体积比1:500加入,37℃孵育1h。
[0094]
9)洗板:用洗板机洗板5次,于吸水纸上拍干。洗板同时,配制好显色液tmb。
[0095]
10)显色:准备好终止液(2m硫酸)后,加入100μl/孔显色液,可以晃动板子加速显色过程并注意密切观察。
[0096]
11)tmb显色:显色4min时(一般不能让空白和阴性显色太高),加入100μl/孔的终止液,加入终止液后静置10min,使终止彻底、颜色均一(可以晃动板子加速终止过程),终止后读数。
[0097]
12)读数:酶标仪必须预热30min以上;tmb显色检测波长为450nm。打开相应的酶标仪测量软件进行读数;将数据存储到指定位置并完善数据。
[0098]
13)注意事项:
[0099]
96孔板用枪加样时,注意避免产生气泡,并且避免所加样品挂壁。
[0100]
加完样,整板观察,要求孔底无气泡;发现气泡时,震荡板子或用移液枪枪头去除气泡。
[0101]
洗板时需密切关注,确保洗板完全、彻底。
[0102]
显色时需密切关注,结合阴性、空白、阳性对照的显色情况,及时终止。
[0103]
14)各种试剂配方:
[0104]
所述包被使用包被液,包含:ph 9.6的碳酸钠-碳酸氢钠缓冲液、1.59gna2co3、2.93g nahco3;使用纯水定容至1000ml,用ph试纸检测ph值,4℃保存。
[0105]
所述洗板使用50x洗液,包含:154.4g tris、149.0g nacl、24.0ml tween-20和800ml纯水;使用约45ml浓盐酸调ph至7.2,纯水定容到1000ml,并于4℃保存。
[0106]
2、elisa结果分析
[0107]
1)阴性和阳性判断标准:选取阴性血浆样本的平均值(x)和标准差(sd),其置信区间上限cut-off值为x 2sd。待测样本在450nm处的od值大于等于x 2sd可判为阳性,小于x 2sd可判为阴性。
[0108]
2)通过计算,如图4所示,左侧的a图为mg2重组蛋白的elisa结果,右侧的b图为egr的elisa结果,其中mg2_od( )和egr_od( )指的是mg2或egr检测判定为阳性的血浆od值,mg2_od(-)和egr_od(-)指的是mg2或egr检测判定为阴性的血浆od值。使用本实施例的mg2重组蛋白作为包虫抗原免疫60例b超阳性血浆(含疑似)和33例正常人血浆(确定为阴性),其阳性检出率为80%,阴性检出率为100%;而用商品化抗原检测相同的血浆时阳性检出率为86%,阴性检出率为100%,因此本实施例中mg2重组蛋白的灵敏度达到80%,特异性为100%。
[0109]
3)虽然mg2重组蛋白的阳性检出率低于商品化抗原的阳性检出率,但是mg2重组蛋白对未被商品化抗原检测出阳性的样本均检测出阳性,因此可能作为使用商品化抗原临床检测人源包虫病的补充抗原。且根据westernblotting结果显示mg2重组蛋白对16例术后包虫病人血浆的免疫反应率为100%。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。