1.本发明涉及具有芴骨架的化合物及其制造方法,所述具有芴骨架的化合物适合作为形成构成以光学透镜、光学膜为代表的光学部件的热塑性树脂的单体,并适合作为高折射率、低双折射以及耐热性与成型性的平衡优异的热塑性树脂的原料。
背景技术:
2.近年来,将以9,9
‑
双(4
‑
(2
‑
羟基乙氧基)苯基)芴(bpef)为代表的具有芴骨架的醇作为原料的聚碳酸酯、聚酯、聚酯碳酸酯等热塑性树脂材料由于光学特性、耐热性、成型性等优异,因此作为光学透镜、光学片材等光学部件而受到关注。
3.例如,专利文献1中公开了一种以具有bpef骨架的醇为原料的聚碳酸酯树脂。然而,使用该醇的聚碳酸酯树脂的折射率虽然记载为1.64,但伴随着近年来的迅速的技术革新,不断要求上述特性的进一步提高。因此,为了实现进一步的高折射率化,专利文献2中开发了一种以9,9
‑
双[4
‑
(2
‑
羟基乙氧基)
‑3‑
苯基苯基]芴(bopbpef)为原料而得到的热塑性树脂,但该专利文献中记载的树脂在折射率上也仍存在改善的余地。另外,专利文献3中记载了一种以9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]芴(bnef)为原料的高折射率树脂,但是虽然折射率高却双折射也变高,所以在应用于光学透镜等透明材料时会存在很大问题。
[0004]
这样,高折射率与低双折射存在折衷关系,以往的聚碳酸酯、聚酯树脂难以兼具两特性。
[0005]
然而,作为9,9
‑
双(4
‑
(2
‑
羟基乙氧基)苯基)芴(bpef)的制造方法,已知有使用硫酸和硫醇类作为催化剂使9
‑
芴酮与2
‑
苯氧乙醇进行脱水缩合的方法。另外,作为9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]芴(bnef)的制造方法,公开了一种与bpef同样地使用硫酸和硫醇类作为催化剂使芴酮与2
‑
萘氧乙醇进行脱水缩合的方法(专利文献4)。进而,对于9,9
‑
双[4
‑
(2
‑
羟基乙氧基)
‑3‑
苯基苯基]芴(bopbpef),也公开了一种与bpef、bnef同样使用硫酸和硫醇类作为催化剂使芴酮与2
‑
(2
‑
联苯氧基)乙醇进行脱水缩合的方法(专利文献5)。另外,作为9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]芴(bnef)的制造方法,公开了如下方法:代替硫酸而将磷钨酸和正十二烷基硫醇作为酸催化剂使用,将9
‑
芴酮与2
‑
萘酚在甲苯和γ
‑
丁内酯中一边减压一边进行脱水缩合,然后在不进行纯化的情况下直接加成碳酸亚乙酯(专利文献6)。
[0006]
然而,上述任一方法都在酸催化剂中使用大量的硫酸、少量的正十二烷基硫醇这样的硫源,因此需要反应后的中和和纯化这样繁琐的纯化操作,且会产生大量的中和废水。另外,由于在产品中混入来自催化剂的硫成分,因此会产生产品的着色、稳定性的降低、纯度的降低等问题。进而,光学用树脂材料等为了得到高纯度的产品而需要反复进行用于除去硫成分的纯化操作,无法说是在工业上有利的方法。
[0007]
现有技术文献
[0008]
专利文献
[0009]
专利文献1:国际公开第2007/142149号小册子
[0010]
专利文献2:日本特开2015
‑
86265号公报
[0011]
专利文献3:日本特开2017
‑
171885号公报
[0012]
专利文献4:日本特开2016
‑
79405号公报
[0013]
专利文献5:日本特开2009
‑
256342号公报
[0014]
专利文献6:日本特开2019
‑
1780号公报
技术实现要素:
[0015]
本发明中,分子设计而成的下述式(1)的化合物的制造方法由2个工序构成,但本技术发明人即便使用上述专利文献中记载的方法也不完全反应,或者虽然进行了反应但反应速度慢,因而在工业上不利。另外,所使用的催化剂的量多,如果不进行活性碳处理或与其类似的金属的除去处理,则在下述式(1)表示的具有芴骨架的白色化合物中混入来自所使用的钯系催化剂的黑色粒子,该醇化合物的色调会恶化。另外,由于含有硫、溴的杂质多,因此有时该醇化合物的色调恶化,将该醇作为原料进行聚合时会导致反应不良。
[0016]
因此,本发明是为了解决上述以往技术的问题而进行了研究,结果达成,目的在于提供作为原料使用而得到的树脂的各种特性(光学特性、耐热性、成型性等)优异的新型的具有芴骨架的化合物及其制造方法。
[0017]
另外,本发明的目的在于提供优选钯含量等特定的金属含量少且树脂的原料、使用树脂的原料所得的树脂的色调优异的新型的具有芴骨架的化合物及其制造方法。
[0018]
进而,本发明的目的在于提供原料醇中的含有硫的杂质的含量少、更优选钯含量等特定的金属含量、含有溴的杂质的含量少、且树脂的原料、作为树脂的原料使用而得到的树脂的色调、各种特性(光学特性、耐热性、成型性等)优异的新型的具有芴骨架的化合物及其制造方法。
[0019]
本发明是为了解决上述以往技术的问题而进行了研究,结果达成,提供具有一定的品质、作为聚合物原料优异的具有芴骨架的化合物及其制造方法。具体而言,本发明涉及以下所示的具有芴骨架的化合物及其制造方法。
[0020]
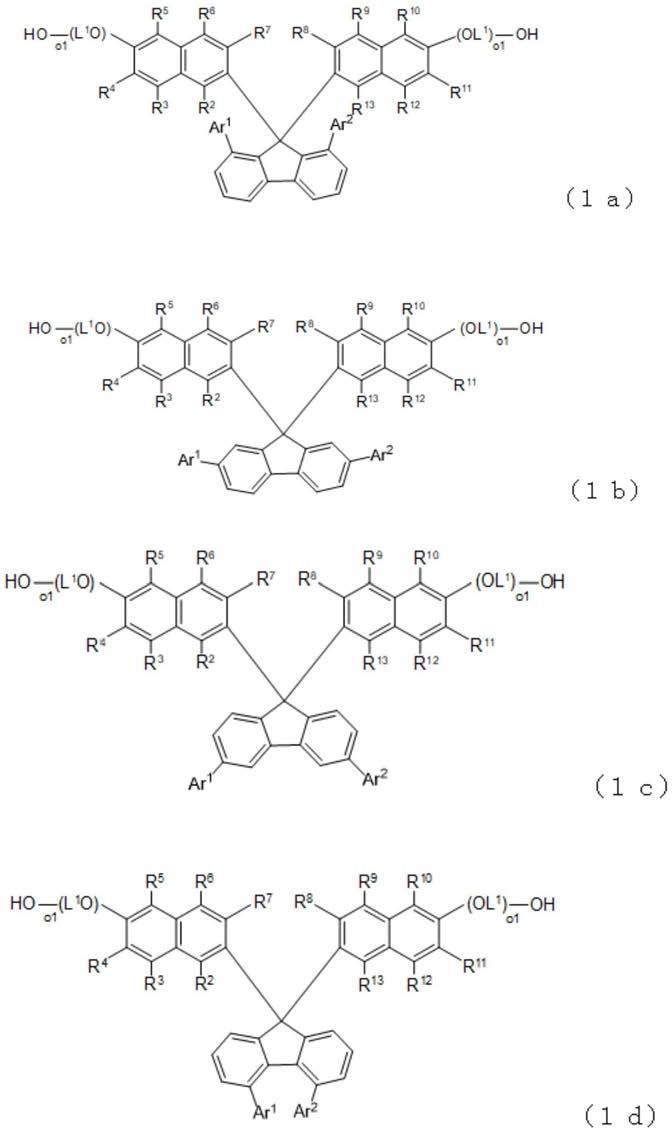
[1]下述式(1)表示的具有芴骨架的化合物。
[0021][0022]
(式中,r1表示氢原子、卤素原子或碳原子数1~12的可包含芳香族基团的烃基,ar1和ar2各自独立地表示碳原子数6~12的可具有取代基的芳香族基团,l1表示碳原子数1~12的亚烷基,m1和n1相同或不同且表示0~4的整数,m2和n2相同或不同且表示0~3的整数,m1 m2≥1。其中,m1 n1为4以下的整数,m2 n2为3以下的整数。о1和о2各自独立地表示0~5的整数。)
[0023]
[2]根据前项1所述的具有芴骨架的化合物,其中,上述式(1)表示的具有芴骨架的
化合物中的硫元素的含量为200ppm以下。
[0024]
[3]根据前项1或2所述的具有芴骨架的化合物,其中,上述式(1)表示的具有芴骨架的化合物中的钯元素的含量满足下述式(2)。
[0025]
0≤pd≤50ppm
ꢀꢀꢀꢀ
(2)
[0026]
[4]根据前项1或2所述的具有芴骨架的化合物,其中,使上述式(1)表示的化合物溶解于二甲基甲酰胺而得的5重量%溶液的apha为500以下。
[0027]
[5]根据前项1或2所述的具有芴骨架的化合物,其中,上述式(1)表示的化合物中的溴元素的含量为150ppm以下。
[0028]
[6]根据前项1或2所述的具有芴骨架的化合物,其中,上述式(1)为下述式(1a)~(1d)表示的化合物中的1个。
[0029]
[0030][0031]
(式中,r2~r
13
各自独立地表示氢原子、卤素原子或碳原子数1~12的可包含芳香族基团的烃基。ar1、ar2、l1和о1与上述式(1)相同。)
[0032]
[7]根据前项6所述的具有芴骨架的化合物,其中,上述式(1)为上述式(1b)。
[0033]
[8]根据前项1或2所述的具有芴骨架的化合物,其中,上述式(1)中的ar1和ar2表示苯基或萘基。
[0034]
[9]根据前项1或2所述的具有芴骨架的化合物,其中,上述式(1)为下述式(1
‑
b)表示的化合物。
[0035][0036]
[10]根据前项9所述的化合物,其中,式(1
‑
b)表示的化合物中的二苯芴酮的含量为0.2%以下。
[0037]
[11]根据前项9所述的化合物,其中,其晶体在差示扫描量热分析中在230~247℃处具有吸热峰。
[0038]
[12]根据前项9所述的化合物,其中,其晶体在基于cu
‑
kα射线的粉末x射线衍射图谱中的衍射角2θ为10.6
±
0.2
°
、10.8
±
0.2
°
、17.1
±
0.2
°
、17.6
±
0.2
°
和18.7
±
0.2
°
处具有峰。
[0039]
[13]一种具有芴骨架的化合物的制造方法,其特征在于,是上述式(1)表示的具有芴骨架的化合物的制造方法,至少包括下述的工序1和工序2。
[0040]
工序1:使下述式(3)表示的芴酮类与下述式(4)或(5)表示的有机硼酸类在反应溶剂中、在碱和钯系催化剂的存在下反应的工序,
[0041]
工序2:使工序1中制造的反应物(6)与下述式(7)表示的醇类在反应溶剂中、在酸催化剂的存在下、在减压下反应,不取出反应后进行中和之后所得到的下述式(8)表示的反应物而直接在碱的存在下与碳酸亚乙酯反应来制造目标物的工序。
[0042][0043]
(式中,x1为1位、2位、3位或4位的取代基,且表示卤素原子,x2为5位、6位、7位或8位的取代基,且表示卤素原子。)
[0044][0045]
(式中,y表示芳香族基团,r
14
表示氢原子、烷基、烯基、烷氧基、卤素原子。l为0、1或2,在l=2时,r
14
可以相同或不同。)
[0046][0047]
(式中,ar1和ar2与式(1)相同。)
[0048][0049]
(式中,p1和p2相同或不同且为0~4的整数,r1,n1和n2与上述式(1)相同。)
[0050][0051]
(式中,r1、ar1和ar2与式(1)相同。p1和p2与式(7)相同。n1和n2为0~3的整数。)
[0052]
[13
‑
1]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(3)表示的化合物为2,7
‑
二溴芴酮。
[0053]
[13
‑
2]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(4)表示的化合物为苯基硼酸。
[0054]
[13
‑
3]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(5)表示的化合物为苯基硼酸酐。
[0055]
[13
‑
4]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(6)表示的化合物为2,7
‑
二苯芴酮。
[0056]
[13
‑
5]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(7)表示的化合物为2
‑
萘酚。
[0057]
[13
‑
6]根据前项13所述的具有芴骨架的化合物的制造方法,其中,式(8)表示的化
合物为9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴。
[0058]
[13
‑
7]根据前项13所述的具有芴骨架的化合物的制造方法,其中,工序1中使用的钯系催化剂为四(三苯基膦)钯和/或pd/sio2表示的钯系催化剂。
[0059]
[13
‑
8]根据前项13所述的具有芴骨架的化合物的制造方法,其中,工序1中使用的碱为碳酸钾和/或碳酸钠。
[0060]
[13
‑
9]根据前项13所述的具有芴骨架的化合物的制造方法,其中,作为工序1中使用的反应溶剂,使用甲苯与乙醇的混合溶剂。
[0061]
[13
‑
10]根据前项13所述的具有芴骨架的化合物的制造方法,其中,工序2中使用的酸催化剂为由磷酸或硅酸和选自钒、钼和钨中的至少一种元素的含氧酸根离子构成的杂多酸。
[0062]
[13
‑
11]根据前项13所述的具有芴骨架的化合物的制造方法,其中,在工序2中与酸催化剂一起并用具有硫醇基的化合物。
[0063]
[13
‑
12]根据前项13所述的具有芴骨架的化合物的制造方法,其中,作为工序2中使用的反应溶剂,使用甲苯与γ
‑
丁内酯的混合溶剂。
[0064]
[13
‑
13]根据前项13所述的具有芴骨架的化合物的制造方法,作为工序2中使用的反应溶剂,使用甲苯与碳酸亚乙酯的混合溶剂。
[0065]
[14]一种具有芴骨架的化合物的制造方法,其特征在于,是上述式(1)表示的具有芴骨架的化合物的制造方法,至少包括下述的工序1~3。
[0066]
工序1:使下述式(13)表示的芴酮类与下述式(14)表示的醇类在反应溶剂中、在酸催化剂的存在下反应而得到下述式(15)表示的化合物的工序,
[0067]
工序2:使下述式(15)表示的化合物与碳酸亚乙酯在反应溶剂中、在碱的存在下反应而得到下述式(16)表示的化合物的工序,
[0068]
工序3:使下述式(16)表示的化合物与下述式(17)或(18)表示的有机硼酸类在反应溶剂中、在碱和钯系催化剂的存在下反应而得到上述式(1)表示的化合物的工序,
[0069][0070]
(式中,x1为1位、2位、3位或4位的取代基,且表示卤素原子,x2为5位、6位、7位或8位的取代基,且表示卤素原子。)
[0071][0072]
(式中,p1和p2相同或不同且为0~4的整数,r1、n1和n2与上述式(1)相同。)
[0073][0074]
(式中,x1和x2与上述式(13)相同。r1、p1和p2与式(14)相同。n1和n2为0~3的整数。)
[0075][0076]
(式中,x1和x2与上述式(13)相同。r1、l1、m1、m2、n1、n2、o1和o2与式(1)相同。
[0077][0078]
(式中,y表示芳香族基团,r
14
表示氢原子、烷基、烯基、烷氧基、卤素原子。l为0、1或2,在l=2时,r
14
可以相同或不同。)
[0079]
[14
‑
1]根据前项14所述的制造方法,其中,不取出上述式(15)表示的化合物而将上述工序1和工序2用一锅法进行。
[0080]
[14
‑
2]根据前项14所述的制造方法,其中,不取出上述式(15)和(16)表示的化合物而将上述工序1~3用一锅法进行。
[0081]
[14
‑
3]根据前项14所述的具有芴骨架的化合物的制造方法,其中,式(13)表示的化合物为2,7
‑
二溴芴酮。
[0082]
[14
‑
4]根据前项14所述的具有芴骨架的化合物的制造方法,其中,式(17)表示的化合物为苯基硼酸。
[0083]
[14
‑
5]根据前项14所述的具有芴骨架的化合物的制造方法,其中,式(18)表示的化合物为苯基硼酸酐。
[0084]
[14
‑
6]根据前项14所述的具有芴骨架的化合物的制造方法,其中,式(14)表示的化合物为2
‑
萘酚。
[0085]
[14
‑
7]根据前项14所述的具有芴骨架的化合物的制造方法,其中,式(15)表示的化合物为9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二溴芴。
[0086]
[14
‑
8]根据前项14所述的具有芴骨架的化合物的制造方法,其中,工序3中使用的钯系催化剂为四(三苯基膦)钯和/或pd/sio2表示的钯系催化剂。
[0087]
[14
‑
9]根据前项14所述的具有芴骨架的化合物的制造方法,其中,工序3中使用的碱为碳酸钾和/或碳酸钠。
[0088]
[14
‑
10]根据前项14所述的具有芴骨架的化合物的制造方法,其中,作为工序3中使用的反应溶剂,使用甲苯与乙醇的混合溶剂。
[0089]
[14
‑
11]根据前项14所述的具有芴骨架的化合物的制造方法,其中,工序1中使用的酸催化剂为由磷酸或硅酸与选自钒、钼和钨中至少一种元素的含氧酸根离子构成的杂多酸。
[0090]
[14
‑
12]根据前项14所述的具有芴骨架的化合物的制造方法,其中,在工序1中与酸催化剂一起并用具有硫醇基的化合物。
[0091]
[14
‑
13]根据前项14所述的具有芴骨架的化合物的制造方法,其中,作为工序1中使用的反应溶剂,使用甲苯与碳酸亚乙酯的混合溶剂。
[0092]
[15]一种前项1所述的具有芴骨架的化合物的使用方法,作为热塑性树脂的原料。
[0093]
本发明的芴化合物不仅在芴环的9位取代有环集合芳烃环,而且(优选在2、7位的位置还)具有二芳基,以该芴化合物为原料的热塑性树脂不仅光学特性优异,其它各种特性(耐热性、透明性、成型性等)也优异。另外,本发明的芴化合物优选含有硫的杂质的含量少,进而,钯等特定的金属的含量、含有溴的杂质的含量也少,色调也优异。另外,以该芴化合物为原料的热塑性树脂不仅光学特性优异,其它各种特性(耐热性、透明性、色调、成型性等)也优异。进而,本发明中,能够高效地制造这样特性优异的具有芴骨架的化合物。
附图说明
[0094]
图1是示出实施例i
‑
6中得到的9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴的差示扫描量热测定(dsc)曲线的图。
[0095]
图2是示出实施例i
‑
6中得到的9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴的粉末x射线测定图谱的图。
具体实施方式
[0096]
对本发明进行详细说明,以下记载的构成要件的说明为本发明的实施方式的代表例,并不限定于这些内容。
[0097]
<本发明的方式i>
[0098]
[具有芴骨架的化合物]
[0099]
本发明的方式i的具有芴骨架的化合物为下述式(1)表示的具有芴骨架的化合物,即,在芴类的9位取代或加成有2个具有至少1个羟基的芳香族烃的化合物。
[0100][0101]
(式中,r1表示氢原子、卤素原子、或碳原子数1~12的可包含芳香族基团的烃基,ar1和ar2各自独立地表示原子数6~12的可具有碳取代基的芳香族基团,l1表示碳原子数1~12的亚烷基,m1和n1相同或不同且表示0~4的整数,m2和n2相同或不同且表示0~3的整数,m1 m2≥1。其中,m1 n1为4以下的整数,m2 n2为3以下的整数。о1和о2各自独立地表示0~5的整数。)
[0102]
上述式(1)中,作为萘环的具体例,优选1,4
‑
萘二基或2,6
‑
萘二基,更优选2,6
‑
萘二基。
[0103]
应予说明,取代于芴环的9位的2个萘环可以彼此相同或不同,更优选为相同的环。应予说明,取代于芴骨架的9位的萘环的取代基没有特别限定。例如,为萘环时,与取代于芴环的9位的萘环对应的基团也可以为1
‑
萘基、2
‑
萘基等。
[0104]
上述式(1)中,r1表示氢原子、卤素原子、或碳原子数1~12的可包含芳香族基团的烃基,优选氢原子、甲基或苯基。
[0105]
上述式(1)中,作为r1表示的烃基,可以例示烷基、环烷基、芳基、萘基、芳烷基等。作为烷基的具体例,优选甲基、乙基、丙基、异丙基、丁基、叔丁基等c1‑6烷基、c1‑4烷基、c1‑3烷基,进一步优选c1‑3烷基,其中,更进一步优选甲基或乙基。
[0106]
另外,作为环烷基的具体例,优选环戊基、环己基等c5‑8环烷基、c5‑6环烷基等,更优选c5‑6环烷基。
[0107]
另外,作为芳基的具体例,优选苯基、烷基苯基(单或二甲基苯基、甲苯基、2
‑
甲基苯基、二甲苯基等)等,更优选苯基。
[0108]
另外,作为芳烷基的具体例,可以优选例示苄基、苯乙基等c6‑
10
芳基
‑
c1‑4烷基等。
[0109]
另外,作为卤素原子,优选氟原子、氯原子、溴原子等。
[0110]
上述式(1)中,作为取代基r1的取代数的n1和n2可以根据稠合烃的稠合环数等而适当地选择,没有特别限定,各自独立地优选为0以上,更优选为1以上的整数。应予说明,取代数n1和n2在萘环中可以相同或不同,通常,许多情况下是相同的。
[0111]
上述式(1)中,l1表示2价连接基团,优选为碳原子数1~12的亚烷基,更优选为亚乙基。通常,l1在同一萘环中可以为相同的亚烷基。另外,l1在不同的萘环中可以彼此相同或不同,通常,可以为相同的。
[0112]
作为氧化亚烷基(ol1)的数量(加成摩尔数)的о1和о2可以分别从0~5的范围选择,下限优选为0以上,上限优选为4以下,更优选为3以下,进一步优选为2以下。特别优选为0或1,最优选为1。应予说明,о1和о2可以为整数,也可以为平均值,在不同的萘环中,可以相同,也可以不同。另外,m1优选1,m2优选0。
[0113]
上述式(1)中,ar1和ar2各自独立地表示碳原子数6~10的芳香族基团,优选苯基或
萘基。基团ar1和ar2可以彼此不同或相同,通常为相同的。另外,ar1和ar2的各自的键合位置优选为芴骨架的1位和8位、2位和7位、3位和6位、或者4位和5位,更优选为2位和7位、3位和6位、或者4位和5位,进一步优选为2位和7位。
[0114]
以下,示出上述式(1)表示的二醇成分的代表例,但作为本发明的上述式(1)中使用的原料,并不受其限定。
[0115]
作为二苯基芴类型,可优选举出9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
1,8
‑
二苯基芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
3,6
‑
二苯基芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
4,5
‑
二苯基芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
1,8
‑
二苯基芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
3,6
‑
二苯基芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
4,5
‑
二苯基芴等。其中,更优选下述式(1
‑
a)~(1
‑
b)中示出的下述式(1
‑
a):9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴、下述式(1
‑
b):9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴,特别优选下述式(1
‑
b):9,9
‑
双(4
‑
(2
‑
羟基乙氧基)苯基)
‑
2,7
‑
二苯基芴。
[0116][0117]
作为二萘基芴类型,可优选举出9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
1,8
‑
二(1
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二(1
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
3,6
‑
二(1
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
4,5
‑
二(1
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
1,8
‑
二(1
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二(1
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
3,6
‑
二(1
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
4,5
‑
二(1
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
1,8
‑
二(2
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二(2
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
3,6
‑
二(2
‑
萘基)芴、9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
4,5
‑
二(2
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
1,8
‑
二(2
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二(2
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
3,6
‑
二(2
‑
萘基)芴、9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
4,5
‑
二(2
‑
萘基)芴等。其中,更优选下述式(2
‑
a)~(2
‑
b)示出的下述式(2
‑
a):9,9
‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二(2
‑
萘基)芴、下述式(2
‑
b):9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二(2
‑
萘基)芴,特别优选下述式(2
‑
b):9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二(2
‑
萘基)芴。
[0118][0119]
本发明的具有芴骨架的化合物的钯元素的含量优选满足下述式(2)。
[0120]
0≤pd≤50ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2)
[0121]
更优选满足下述式(2
‑
1)。
[0122]
0≤pd≤25ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
1)
[0123]
进一步优选满足下述式(2
‑
2)。
[0124]
0≤pd≤10ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
2)
[0125]
更进一步优选满足下述式(2
‑
3)。
[0126]
0≤pd≤5ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
3)
[0127]
特别优选满足下述式(2
‑
4)。
[0128]
0≤pd≤3ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
4)
[0129]
最优选满足下述式(2
‑
5)。
[0130]
0≤pd≤1ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
5)
[0131]
如果超过上述范围的上限,则有时对使用上述式(1)表示的原料醇的树脂的色调、使用该树脂的光学部件造成不良影响。钯元素的含量的下限可以为0.01ppm以上、0.05ppm以上或0.10ppm以上。
[0132]
本发明的具有芴骨架的化合物溶解于二甲基甲酰胺而得的5重量%溶液的apha优选为500以下,更优选为200以下,进一步优选为100以下。如果apha大于500,则有时对使用上述式(1)表示的原料醇的树脂的色调、使用该树脂的光学部件造成不良影响。
[0133]
对于本发明的具有芴骨架的化合物,上述式(1
‑
b)表示的化合物中的二苯芴酮的含量优选为0.2%以下,更优选为0.1%以下,更进一步优选为0.05%以下。如果二苯芴酮的含量大于0.2%,则有时对使用上述式(1)表示的原料醇的树脂的色调、使用该树脂的光学部件造成不良影响。
[0134]
[联萘化合物的多晶型]
[0135]
本发明的上述式(1
‑
b)表示的化合物的晶体优选在230~247℃的范围具有基于差示扫描量热分析的吸热峰。另外,在基于cu
‑
kα射线的粉末x射线衍射图谱中的衍射角2θ为10.6
±
0.2
°
、10.8
±
0.2
°
、17.1
±
0.2
°
、17.6
±
0.2
°
和18.7
±
0.2
°
处具有特征峰。另外,优选在衍射角2θ为10.8
±
0.2
°
处具有最大峰。本发明的上述式(1
‑
b)表示的化合物的晶体为处理性优异且色调、纯度都良好的晶体。
[0136]
[具有芴骨架的化合物的制造方法]
[0137]
本发明的方式i的具有芴骨架的化合物的制造方法大致由2个工序构成,可以通过第1工序1和第2工序2来制造,所述第1工序:使下述式(3)表示的芴酮类与下述式(4)或(5)表示的有机硼酸类在钯系催化剂和碱存在下反应;所述第2工序2:使工序1中制造的反应物(6)与下述式(7)表示的醇类的化合物在酸催化剂的存在下(优选在酸催化剂和硫醇系化合物的存在下)一边对反应体系内在减压下将副生成的水向体系外排出一边反应后,反应结束后直接进行中和,不取出产物(8)而加入碱性催化剂与碳酸亚乙酯反应。
[0138]
上述制造方法中,由于工序1中下述式(4)或(5)表示的有机硼酸类的反应性高、不发生副反应,工序2中通过并用硫醇系化合物而与不并用硫醇系化合物的情况相比反应速度快,且通过使体系内为减压下而能够高效地将副生成的水排出,因此反应快、副产物的生成得到抑制且可以不取出反应物(8)而用相同的反应釜进行制造,因而所使用的溶剂量也变少,能够以低成本而高效地制造本发明的具有芴骨架的化合物。
[0139]
工序1:
[0140][0141]
(式中,x1为1位、2位、3位或4位的取代基,且表示卤素原子,x2为5位、6位、7位或8位的取代基,且表示卤素原子。)
[0142][0143]
(式中,y表示芳香族基团,r
14
表示氢原子、烷基、烯基、烷氧基、卤素原子。l为0、1或2,在l=2时,r
14
可以相同或不同。)
[0144]
工序2:
[0145][0146]
(式中,ar1和ar2与式(1)相同。)
[0147][0148]
(式中,p1和p2相同或不同且为0~4的整数,r1、n1和n2与上述式(1)相同。)
[0149][0150]
(式中,r1、ar1和ar2与式(1)相同。p1和p2与式(7)相同。n1和n2为0~3的整数。)
[0151]
上述式(3)表示的化合物为与上述式(1)中芴骨架对应的芴酮化合物,x1为1位、2位、3位或4位的取代基,x2为5位、6位、7位或8位的取代基,x1和x2都表示卤素原子。
[0152]
以下,虽然示出上述式(3)表示的芴酮化合物的代表例,但作为本发明的上述式(1)中使用的原料,并不限定于此。
[0153]
作为具体例,可优选举出1,8
‑
二氟芴酮、2,7
‑
二氟芴酮、3,6
‑
二氟芴酮、4,5
‑
二氟芴酮、1,8
‑
二氯芴酮、2,7
‑
二氯芴酮、3,6
‑
二氯芴酮、4,5
‑
二氯芴酮、1,8
‑
二碘芴酮、2,7
‑
二碘芴酮、3,6
‑
二碘芴酮、4,5
‑
二碘芴酮、1,8
‑
二溴芴酮、2,7
‑
二溴芴酮、3,6
‑
二溴芴酮、4,5
‑
二溴芴酮等。其中,优选1,8
‑
二溴芴酮、2,7
‑
二溴芴酮、3,6
‑
二溴芴酮、4,5
‑
二溴芴酮,特别优选2,7
‑
二溴芴酮。
[0154]
这些可以单独使用,或者也可以混合2种以上,可以根据目的而任意选择。本发明中优选为2,7
‑
二溴芴酮。
[0155]
所使用的上述式(3)表示的芴酮类的纯度没有特别限定,通常,优选95%以上,更优选为99%以上。应予说明,芴酮类可以使用市售品,也可以使用合成所得的制品。例如,作为制造二溴芴酮类的方法,可举出非专利文献(journal of american chemical society,2017,vol.139,11073
‑
11080)中记载的方法、即使9
‑
芴酮与溴在水中下进行反应的方法等。
[0156]
上述式(4)或(5)表示的化合物的环y与上述式(1)中基团ar1和ar2对应。另外,上述式(4)和(5)中,基团r
14
的优选方式与上述r1的优选方式相同,l的优选方式与上述n1和n2的优选方式相同。
[0157]
所使用的有机硼酸类的纯度没有特别限定,通常,优选为95%以上,更优选为99%以上。应予说明,有机硼酸类可以使用市售品,也可以使用合成所得的制品。作为制造有机硼酸类的方法,例如可举出专利文献(日本特开2002
‑
47292号公报)中记载的方法、即使苯基格氏试剂与溶解于非醚系芳香族溶剂的硼酸酯类反应的方法等。
[0158]
本发明中使用的有机硼酸包括上述式(4)和(5)表示的烷基硼酸、烯基硼酸、芳基硼酸、杂芳基硼酸及其酐等,作为烷基硼酸,包括丁基硼酸、环己基硼酸、环戊基硼酸、2
‑
乙基硼酸、4
‑
乙基硼酸、己基硼酸、异丁基硼酸、异丙基硼酸、甲基硼酸、正辛基硼酸、丙基硼
酸、戊基硼酸、2
‑
苯基乙基硼酸、它们的酐,作为烯基硼酸,包括1
‑
环戊烯基硼酸、二茂铁硼酸、1,1
’‑
二茂铁二硼酸、它们的酐,作为芳基硼酸,包括2
‑
蒽硼酸、9
‑
蒽硼酸、苄基硼酸、2
‑
联苯硼酸、3
‑
联苯硼酸、4
‑
联苯硼酸、2,3
‑
二甲基苯基硼酸、2,4
‑
二甲基苯基硼酸、2,5
‑
二甲基苯基硼酸、2,6
‑
二甲基苯基硼酸、3,4
‑
二甲基苯基硼酸、3,5
‑
二甲基苯基硼酸、2
‑
乙氧基苯基硼酸、3
‑
乙氧基苯基硼酸、4
‑
乙氧基苯基硼酸、6
‑
甲氧基
‑2‑
萘硼酸、2
‑
甲基苯基硼酸、3
‑
甲基苯基硼酸、4
‑
甲基苯基硼酸、1
‑
萘硼酸、2
‑
萘硼酸、9
‑
菲硼酸、10
‑
苯基
‑9‑
蒽硼酸、苯基硼酸、苯基乙烷硼酸、4
‑
苯基(萘
‑1‑
基)硼酸、3
‑
丙氧基苯基硼酸、3
‑
异丙氧基苯基硼酸、4
‑
异丙氧基苯基硼酸、4
‑
丙基苯基硼酸、4
‑
异丙基苯基硼酸、10
‑
(萘
‑1‑
基)
‑9‑
蒽硼酸、10
‑
(萘
‑2‑
基)
‑9‑
蒽硼酸、它们的酐,作为杂芳基硼酸,包括苯并呋喃
‑2‑
硼酸、二苯并呋喃
‑4‑
硼酸、5
‑
甲酰基
‑2‑
呋喃硼酸、5
‑
甲酰基噻吩
‑2‑
硼酸、呋喃
‑2‑
硼酸、呋喃
‑3‑
硼酸、吡啶
‑3‑
硼酸、吡啶
‑4‑
硼酸、喹啉
‑2‑
硼酸、喹啉
‑3‑
硼酸、喹啉
‑4‑
硼酸、喹啉
‑5‑
硼酸、喹啉
‑6‑
硼酸、喹啉
‑8‑
硼酸、异喹啉
‑4‑
硼酸、2
‑
噻吩硼酸、3
‑
噻吩硼酸、5
‑
嘧啶硼酸、它们的酐。
[0159]
这些可以单独使用,或者混合2种以上,可以根据目的而任意选择。本发明中优选为苯基硼酸、2
‑
萘硼酸或其酐,特别优选为苯基硼酸或其酐。
[0160]
作为原料使用的上述式(4)表示的化合物的使用比率相对于上述式(3)表示的化合物(卤代芴酮化合物)1摩尔可以优选为2~5摩尔,更优选为2.05~3.0摩尔,进一步优选为2.1~2.5摩尔左右。该有机硼酸类小于2摩尔时,有时上述式(6)表示的产物的收率变低。另外,超过5摩尔时,虽然反应速度快,收率变高,但存在该具有芴骨架的化合物的制造成本上升的情况。
[0161]
另外,上述式(5)表示的化合物的使用比率相对于上述式(3)表示的化合物(卤代芴酮化合物)1摩尔可以优选为0.7~5摩尔,更优选为0.8~3摩尔,进一步优选为1~2摩尔左右。该有机硼酸类小于0.7摩尔时,有时上述式(6)表示的产物的收率变低。另外,超过5摩尔时,虽然反应速度快,收率变高,但存在该具有芴骨架的化合物的制造成本上升的情况。
[0162]
工序1的上述式(3)与上述式(4)和/或(5)表示的化合物的反应(脱卤反应)可以在反应溶剂中、碱和催化剂的存在下进行。
[0163]
作为工序1的反应中使用的碱,例如,可举出氢氧化钠、氢氧化钾等氢氧化物、碳酸钠(na2co3)、碳酸钾(k2co3)、碳酸铯(cs2co3)等碳酸盐、乙酸钠、乙酸钾等乙酸盐、磷酸钠(na3po4)、磷酸钾(k3po4)等磷酸盐等无机盐、三乙胺类、吡啶、吗啉、喹啉、哌啶、苯胺类、四正丁基乙酸铵等铵盐等有机盐等。其中,优选使用碳酸盐,优选碳酸钾和/或碳酸钠。这样的碱可以单独使用,另外也可以并用2种以上使用。
[0164]
另外,工序1的反应中,上述碱的使用量没有特别限定,相对于有机硼酸类1摩尔优选添加1~30当量,更优选添加1~10当量。
[0165]
作为工序1的反应中使用的钯系催化剂,优选铃木偶联反应中使用的钯化合物,例如,可举出四(三苯基膦)钯、双(三苯基膦)二氯化钯、乙酸钯、三(二亚苄基丙酮)二钯、双(二亚苄基丙酮)钯、双[4
‑
(n,n
‑
二甲基氨基)苯基]二叔丁基膦二氯化钯、双(二叔丁基异戊二烯基膦)二氯化钯、双(二叔巴豆基膦)二氯化钯、pd/sio2表示的钯系催化剂等。其中,优选四(三苯基膦)钯和/或pd/sio2表示的钯系催化剂。这样的钯系催化剂可以单独使用,另外,也可以并用2种以上使用。
[0166]
工序1的反应中,上述催化剂的使用量没有特别限定,相对于上述式(3)表示的芴
酮化合物1摩尔,以钯金属原子换算计优选为0.1~10mmol,更优选为0.5~5mmol。钯催化剂的使用量以钯金属原子换算计小于0.1mmol时,有时反应变得不易结束。另外,钯催化剂的使用量以钯金属原子换算计超过10mmol时,虽然反应结束,但难以使该具有芴骨架的化合物中的钯元素含量为式(2)的范围内,不仅有可能使利用该醇原料制造的热塑性树脂的色调恶化,而且有时该具有芴骨架的化合物的制造成本上升。
[0167]
作为工序1中使用的反应溶剂,没有特别限定,例如可以将甲苯、二甲苯等芳香族烃系溶剂与甲醇、乙醇、异丙醇、正丁醇等醇类单独或并用使用。芳香族烃系溶剂由于为高沸点溶剂,因此可以将反应温度设定得较高,另外,由于通过使用醇而与水的亲和性良好,反应性变得良好,因而优选使用。这样的溶剂可以单独使用,或者也可以并用2种以上使用。此外,也可以使用n,n
‑
二甲基甲酰胺或n,n
‑
二甲基乙酰胺等非质子性溶剂、邻二氯苯等卤代苯类。这样的溶剂也可以单独使用,另外,还可以并用2种以上使用。本发明中,更优选甲苯与乙醇的混合溶剂。
[0168]
上述反应溶剂(在本发明的情况下为甲苯与乙醇的混合溶剂)的使用量没有特别限定,相对于上述式(3)表示的芴酮类,甲苯优选为0.1重量倍以上,更优选为0.5~100重量倍,进一步优选为1~50重量倍。甲苯的使用量小于0.1重量倍时,有可能产物析出而使搅拌变得困难。另外,甲苯的使用量超过100重量倍时,没有与使用量匹配的效果,容积效率也恶化,存在该具有芴骨架的化合物的制造成本上升的情况。另外,乙醇的使用量也没有特别限定,相对于上述式(3)表示的芴酮类,优选为0.1~50重量倍,更优选为1~20重量倍。乙醇的使用量小于0.1重量倍时,反应速度慢,有可能收率下降。另外,乙醇的使用量超过50重量倍时,与甲苯同样地没有与使用量匹配的效果,容积效率也恶化,存在该具有芴骨架的化合物的制造成本上升的情况。
[0169]
反应温度根据所使用的原料、溶剂的种类而不同,优选为50~150℃,更优选为60~130℃,进一步优选为70~120℃。反应可以利用液相色谱法等分析手段进行追踪。
[0170]
反应结束后的反应混合物中,通常,除了生成的上述式(6)表示的化合物以外,还包含未反应的芴酮类、未反应的有机硼酸类、碱、催化剂、副反应产物等。因此,可以通过惯用方法例如过滤、浓缩、萃取、晶析、重结晶、再沉淀、活性碳处理或与其类似的金属的除去处理、柱层析等分离手段或将这些组合的分离手段而将上述式(6)表示的化合物进行分离纯化。例如,可以利用惯用方法(加入碱水溶液而形成水溶性的复合体的方法等)而除去有机硼酸类,进行活性碳处理或与其类似的金属的除去处理而除去钯化合物后,添加重结晶溶剂,进行冷却使其重结晶化,接着进行过滤分离来进行纯化。
[0171]
上述式(7)表示的醇类与在上述式(6)表示的二芳基芴衍生物中取代于9位的含有(多)羟基的芳烃环对应。即,上述式(7)中萘环与上述式(1)的萘环对应,r1、n1和n2与上述式(1)的r1、n1和n2对应。
[0172]
作为上述式(7)表示的化合物的具体例,可举出萘酚类(例如,萘酚(1
‑
萘酚、2
‑
萘酚)、具有烃基的萘酚(甲基萘酚、乙基萘酚、二甲基萘酚、丙基萘酚、丁基萘酚(c1‑4烷基萘酚)等烷基萘酚)、烷氧基萘酚(乙氧基萘酚等c1‑4烷氧基萘酚)、卤代萘酚(氯萘酚、溴萘酚))、与这些萘酚类(或单羟基萘类)对应的多羟基萘(例如,1,3
‑
二羟基萘、1,4
‑
二羟基萘、2,3
‑
二羟基萘、1,5
‑
羟基萘、1,7
‑
二羟基萘、1,8
‑
二羟基萘、2,6
‑
二羟基萘、2,7
‑
二羟基萘、1,2,4
‑
三羟基萘、1,3,8
‑
三羟基萘等二或三羟基萘类)等。其中,优选1
‑
萘酚、2
‑
萘酚,特别
优选2
‑
萘酚。
[0173]
这些醇类可以单独使用,或者也可以混合2种以上与芴酮类反应,可以根据目的而任意选择。本发明中优选为2
‑
萘酚。
[0174]
工序2的反应中,上述式(7)表示的醇类的使用量没有特别限定,从抑制副反应和经济性的方面考虑,相对于芴酮类1摩尔,优选为2~20摩尔,更优选为2.1~10摩尔,进一步优选为2.3~5摩尔。
[0175]
这些的上述式(7)表示的醇类可以使用市售品,也可以使用合成的制品。例如,作为制造萘酚类的方法,可举出专利文献(日本特开昭61
‑
115039号公报)中记载的方法、即将使萘磺化所得的2
‑
萘磺酸用碱中和而得到2
‑
萘磺酸钠后、将产物进行碱溶解而制成碱盐、然后进行水解来制造2
‑
萘酚的方法等。
[0176]
作为原料使用的上述式(7)表示的醇类(例如,萘酚类等)的纯度没有特别限定,通常,优选为95%以上,更优选为99%以上。
[0177]
工序2的反应通常可以在酸催化剂的存在下进行。作为酸催化剂,例如,可举出硫酸、巯基乙酸(
チオール
酸)、蒙脱石、杂多酸等,其中,由于来自酸催化剂的杂质的生成少,容易得到本发明的具有芴骨架的化合物,因此特别优选杂多酸。
[0178]
本发明中优选使用的杂多酸一般为2种以上的不同的无机含氧酸缩合而生成的化合物的通称,可以通过中心的含氧酸与在其周围缩合的其它种类的含氧酸的组合而形成各种杂多酸。将形成中心的含氧酸的数量较少的元素称为杂元素,将形成在其周围缩合的含氧酸的元素称为多元素。多元素可以为一种元素,也可以为多种元素。
[0179]
构成杂多酸的含氧酸的杂元素没有特别限定,例如,可举出铜、铍、硼、铝、碳、硅、锗、锡、钛、锆、铈、钍、氮、磷、砷、锑、钒、铌、钽、铬、钼、钨、铀、硒、碲、锰、碘、铁、钴、镍、铑、锇、铱、铂。优选为磷(磷酸)或硅(硅酸)。另外,构成杂多酸的含氧酸的多元素没有特别限定,例如,可举出钒、钼、钨、铌、钽。优选为选自钒、钼和钨中的至少1种元素。
[0180]
作为构成杂多酸骨架的杂多酸阴离子,可以使用各种组成的杂多酸阴离子。例如,可举出xm
12
o
40
、xm
12
o
42
、xm
18
o
62
、xm6o
24
等。优选的杂多酸阴离子的组成为xm
12
o
40
。各式中,x为杂元素,m为多元素。作为具有这些组成的杂多酸,具体而言,可例示磷钼酸、磷钨酸、硅钼酸、硅钨酸、磷钼钒酸等。
[0181]
杂多酸可以为游离的杂多酸,也可以将质子的一部分或全部用其它阳离子置换而作为杂多酸的盐使用。因此,本发明所说的杂多酸还包含这些杂多酸的盐。作为可与质子置换的阳离子,例如,可举出铵、碱金属、碱土金属等。
[0182]
杂多酸可以为酐,也可以为含有结晶水的物质,为酐时,反应更快,而且副产物的生成得到抑制,因而优选。为含有结晶水的物质时,可以通过预先进行减压干燥、与溶剂的共沸脱水等脱水处理而得到与酐同样的效果。杂多酸也可以以担载于活性碳、氧化铝、二氧化硅
‑
氧化铝、硅藻土等载体的形态使用。
[0183]
这些杂多酸可以单独使用,也可以组合2种以上使用。另外,也可以根据需要在不损害本发明的目的的范围并用除杂多酸以外的其它催化剂。
[0184]
杂多酸的使用量没有特别限定,为了得到足够的反应速度,相对于芴酮,优选为0.0001重量倍以上,更优选为0.001~30重量倍,进一步优选为0.01~5重量倍。
[0185]
实施本发明时,工序2的反应中,可以通过与上述杂多酸一起并用具有硫醇基(以
下有时简记为sh基)的化合物来提高反应速度且抑制杂质的生成。作为本发明中可并用的硫醇化合物,例如,可举出巯基羧酸、烷硫醇和它们的盐。
[0186]
作为巯基羧酸,可举出α
‑
巯基丙酸、β
‑
巯基丙酸、硫代乙酸、巯基乙酸、硫代草酸、巯基琥珀酸、巯基苯甲酸等。另外,作为烷硫醇,可举出甲烷硫醇、乙烷硫醇、1
‑
丙烷硫醇、2
‑
丙烷硫醇、1
‑
丁烷硫醇、2
‑
丁烷硫醇、1
‑
戊烷硫醇、2
‑
戊烷硫醇、1
‑
己烷硫醇、1
‑
庚烷硫醇、2
‑
庚烷硫醇、1
‑
辛烷硫醇、2
‑
辛烷硫醇、1
‑
壬烷硫醇、1
‑
癸烷硫醇、1
‑
十一烷硫醇、1
‑
十二烷硫醇等c1‑
16
烷基硫醇等。这样的具有sh基的化合物中,从能够廉价地得到看,优选β
‑
巯基丙酸和1
‑
十二烷硫醇,特别优选1
‑
十二烷硫醇。
[0187]
这样的具有sh基的化合物可以单独使用,另外,也可以并用2种以上使用。
[0188]
实施工序2的反应的方法没有特别限定,通常,可以通过将上述式(6)、上述式(7)表示的化合物以及杂多酸和/或硫醇化合物投入到反应装置中,在空气中或氮、氩等非活性气体气氛下,在甲苯、二甲苯等芳香族烃系和乙酸乙酯、γ
‑
丁内酯等酯类的非活性溶剂存在下进行加热搅拌来进行。此时,通过在除去催化剂所含有的水、反应生成水等反应体系内的水分的脱水条件下进行反应,从而与不脱水时相比反应进行得更快,副产物的生成得到抑制,能够以更高收率得到目标物。作为脱水的方法,没有特别限定,例如,可举出基于添加脱水剂的脱水、基于减压的脱水、基于常压或减压下与溶剂的共沸的脱水等。
[0189]
作为工序2中使用的反应溶剂,没有特别限定,例如,可举出甲苯、二甲苯等芳香族烃溶剂、氯苯、二氯苯等卤代芳香族烃溶剂、戊烷、己烷、庚烷等脂肪族烃溶剂、二氯甲烷、1,2
‑
二氯乙烷等卤代脂肪族烃溶剂、乙醚、二异丙基醚、甲基叔丁基醚、二苯基醚、四氢呋喃、二烷等脂肪族和环状醚溶剂、乙酸乙酯、乙酸丁酯、γ
‑
丁内酯、碳酸亚乙酯等酯溶剂、乙腈、丙腈、丁腈、苄腈等腈溶剂、n,n
‑
二甲基甲酰胺、n,n
‑
二甲基乙酰胺、1
‑
甲基
‑2‑
吡咯烷酮等酰胺溶剂等。优选为芳香族烃溶剂和酯溶剂,更优选为甲苯、二甲苯、氯苯或二氯苯与乙酸乙酯、乙酸丁酯、γ
‑
丁内酯或碳酸亚乙酯的混合溶剂,进一步优选为甲苯与γ
‑
丁内酯或碳酸亚乙酯的混合溶剂。这些反应溶剂可以单独使用,另外,也可以并用2种以上使用。
[0190]
另外,其使用量没有特别限定,从经济性的方面考虑,相对于上述式(6)表示的二苯芴酮,优选为0.1重量倍以上,更优选为0.5~100重量倍,进一步优选为1~20重量倍。
[0191]
工序2的反应温度根据所使用的原料、溶剂的种类而不同,优选为50~300℃,更优选为80~250℃,进一步优选为100~180℃。反应可以根据液相色谱法等分析手段进行追踪。
[0192]
工序2的反应时的内压优选为101.3kpa以下的压力,更优选为60.0kpa以下。副生成的水在该内压下一边从体系内排出一边进行反应时反应更高效地进行,且生成的副产物也变少,因而优选。
[0193]
工序2的反应后,可以根据需要将所使用的固体酸通过过滤而除去或中和。作为中和时使用的碱,例如,可举出氢氧化钠、氢氧化钾、氢氧化钙等碱金属或碱土金属的氢氧化物、碳酸钾、碳酸钙、碳酸钠、碳酸钠等碱金属或碱土金属的碳酸盐(碳酸氢)盐、胺类等。
[0194]
工序2的反应中,中和后的反应液可以在不除去因中和所生成的盐而用于与碳酸亚乙酯的反应。根据需要,也可以将因中和所生成的盐通过过滤进行分离,或者实施加入水进行搅拌并在静置后进行分液而除去水层的操作(也有时称为水洗工序)而将中和所生成的盐从反应体系内分离。该水洗工序可以根据需要而反复实施。
[0195]
工序2中,工序1中制造的反应物(6)与上述式(7)表示的醇类的反应后,可以在不取出上述式(8)表示的芴化合物而与碳酸亚乙酯反应。通过浓缩、晶析等方法而取出上述式(8)表示的芴化合物时,有可能收率降低,导致成本上升。
[0196]
工序2中,碳酸亚乙酯相对于工序1中使用的上述式(6)表示的二苯芴酮1摩尔,通常使用2~10摩尔,更优选使用2~5摩尔。
[0197]
工序2中,实施上述式(8)表示的芴化合物与碳酸亚乙酯的反应时,可以根据需要在碱性化合物存在下进行反应。在碱性化合物存在下进行反应时,优选工序1中使用的固体酸在实施工序2之前预先通过过滤而进行分离或者进行中和。
[0198]
作为工序2中可使用的碱性化合物,可例示碳酸盐类、碳酸氢盐类、氢氧化物类、有机碱类等。作为碳酸盐类,可举出碳酸钾、碳酸钠、碳酸铯、碳酸锂等。作为碳酸氢盐类,可举出碳酸氢钾、碳酸氢钠、碳酸氢锂、碳酸氢铯等。作为氢氧化物类,可举出氢氧化钠、氢氧化钾、氢氧化锂等。作为有机碱类,可举出三乙胺、二甲基氨基吡啶、三苯基膦、四甲基溴化铵、四甲基氯化铵等。
[0199]
上述的碱性化合物中,从处理性、安全性的观点考虑,优选使用碳酸钾、碳酸钠。这些碱性化合物可以单独使用,另外,也可以并用2种以上使用。
[0200]
在工序2中使用碱性化合物时,其使用量相对于工序1中使用的上述式(6)表示的二苯芴酮1摩尔,通常为0.01~1.0摩尔,优选为0.03~0.5摩尔。
[0201]
工序2的反应结束后,所得到的反应混合物可以添加稀释溶剂而使上述式(1)表示的化合物直接析出,也可以在实施清洗、浓缩、稀释、活性碳处理等后处理后,在小于50℃使上述式(1)表示的化合物析出。从根据需要实施上述后处理后的反应混合物中析出上述式(1)表示的化合物的操作根据需要通过使与溶剂混合的反应混合物达到50℃~溶剂的沸点(优选为70~110℃),再使其冷却到小于50℃来实施。上述式(1)表示的化合物的晶体在50℃以上从反应混合物中析出时,可以将在50℃以上晶体不析出的量的稀释溶剂与反应混合物混合后,使得到的混合物达到50℃~溶剂的沸点(优选为70~110℃),再将其冷却至小于50℃来实施。作为稀释溶剂,可举出作为上述反应中使用的溶剂所例示的溶剂、甲醇、乙醇、丙醇、异丙醇、丁醇、叔丁醇、异丁醇和戊醇等醇溶剂、碳酸二甲酯、碳酸二乙酯等碳酸溶剂、乙酸乙酯、乙酸丁酯、γ
‑
丁内酯、苯甲酸丁酯、苯甲酸甲酯、乙酸苯酯等酯溶剂、乙醚、二异丙基醚、甲基叔丁基醚、二苯基醚、四氢呋喃等醚溶剂、己烷、庚烷、辛烷、戊烷等脂肪族烃溶剂等,优选甲醇、乙醇或碳酸二甲酯,更优选甲醇和乙醇。
[0202]
这样的晶析操作可以进行一次,也可以反复进行多次。特别是,上述工序2的反应中,如果使用甲醇、乙醇等醇,则能够简便且高效地除去未反应的2
‑
萘酚、副生成的乙二醇单(2
‑
萘基)醚等杂质,因此即便进行一次晶析操作,也能够得到满足式(2)的上述式(1)表示的化合物。
[0203]
所析出的晶体通过过滤等进行回收。所得到的晶体可以使用上述反应中采用的溶剂等进行清洗,也可以进行干燥。这样得到的上述式(1)表示的化合物的纯化物的纯度优选为95%以上。
[0204]
由本发明的制造方法而得到的具有芴骨架的化合物的纯度可以从60~100%的较宽范围中选择,优选为70%以上,更优选为80%以上,进一步优选为90%以上。
[0205]
[具有芴骨架的化合物的特征和用途]
[0206]
本发明的具有芴骨架的化合物由于优选将二苯基芴骨架和二萘基芴骨架与芳烃环组合,因此不仅折射率、耐热性高,而且能够在制成聚合物时减轻双折射。到目前为止,为了提高折射率,已经使用了在芴骨架的9位取代有环集合芳烃环的芴化合物,但该情况下虽然折射率、耐热性高,但双折射降低。与此相对,本发明的具有芴骨架的化合物由于具有二苯基芴骨架和二萘基芴骨架,因此尽管折射率高,但双折射也小。此外,由于芳烃环上具有1个以上的羟基,芴化合物整体具有多个羟基,因此反应性高。因此,本发明的具有芴骨架的化合物可以作为各种树脂的原料(单体)利用。例如,可以作为热塑性树脂(例如,聚酯树脂、聚碳酸酯树脂、聚酯碳酸酯树脂、聚氨酯树脂等)、热固性树脂(例如,环氧树脂、酚醛树脂、热固化性聚氨酯树脂、(甲基)丙烯酸酯等)的多元醇成分使用。将本发明的具有芴骨架的化合物作为多元醇成分使用时,由于在芴骨架的9位取代有萘环且在芴骨架上具有二芳基,因此得到的树脂具备能够以高水平兼具高折射率和低双折射性的优点。
[0207]
另外,本发明的具有芴骨架的化合物可以在通用的溶剂中高效地制备衍生物。
[0208]
本发明的具有芴骨架的化合物的熔点可以从100~300℃的较宽范围中选择,优选为120~280℃,更优选为130~260℃,进一步优选为140~240℃,特别优选为150~230℃。
[0209]
<本发明的方式ii>
[0210]
[具有芴骨架的化合物]
[0211]
本发明的方式ii的具有芴骨架的化合物为上述<本发明的方式i>中说明的上述式(1)表示的具有芴骨架的化合物。
[0212]
本发明的方式ii的具有芴骨架的化合物的硫元素的含量为200ppm以下,优选为100ppm以下,更优选为50ppm以下,进一步优选为30ppm以下。硫元素的含量大于200ppm时,会对使用上述式(1)表示的原料醇所得的树脂的色调、使用该树脂所得的光学部件造成不良影响。另外,使用上述式(1)表示的原料醇而得到树脂时,会导致反应不良。
[0213]
本发明的具有芴骨架的化合物的溴元素的含量优选为150ppm以下,更优选为50ppm以下,更进一步优选为20ppm以下。溴元素的含量大于150ppm时,有时会对使用上述式(1)表示的原料醇所得的树脂的色调、使用该树脂所得的光学部件造成不良影响。另外,使用上述式(1)表示的原料醇而得到树脂时,有时会导致反应不良。
[0214]
本发明的具有芴骨架的化合物的钯元素的含量优选满足下述式(2)。
[0215]
0≤pd≤50ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2)
[0216]
更优选满足下述式(2
‑
1)。
[0217]
0≤pd≤25ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
1)
[0218]
进一步优选满足下述式(2
‑
2)。
[0219]
0≤pd≤10ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
2)
[0220]
更进一步优选满足下述式(2
‑
3)。
[0221]
0≤pd≤5ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
3)
[0222]
特别优选满足下述式(2
‑
4)。
[0223]
0≤pd≤3ppm
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2
‑
4)
[0224]
超过上述范围的上限时,有时会对使用上述式(1)表示的原料醇所得的树脂的色调、使用该树脂所得的光学部件造成不良影响。钯元素的含量的下限可以为0.01ppm以上、0.05ppm以上、或0.10ppm以上。
[0225]
本发明的具有芴骨架的化合物溶解于二甲基甲酰胺而得的5重量%溶液的apha优选为500以下,更优选为200以下,更进一步优选为100以下。apha大于500时,有时会对使用上述式(1)表示的原料醇所得的树脂的色调、使用该树脂所得的光学部件造成不良影响。
[0226]
对于本发明的具有芴骨架的化合物,上述式(1
‑
b)表示的化合物中的二苯芴酮的含量优选为0.2%以下,更优选为0.1%以下,更进一步优选为0.05%以下。二苯芴酮的含量大于0.2%时,有时会对使用上述式(1)表示的原料醇所得的树脂的色调、使用该树脂所得的光学部件造成不良影响。
[0227]
[具有芴骨架的化合物的制造方法]
[0228]
本发明的方式ii的具有芴骨架的化合物的制造方法可以通过下述工序1~3进行制造。
[0229]
工序1:使下述式(13)表示的芴酮类与下述式(14)表示的醇类在反应溶剂中、在酸催化剂的存在下反应而得到下述式(15)表示的化合物的工序
[0230]
工序2:使下述式(15)表示的化合物与碳酸亚乙酯在反应溶剂中、在碱的存在下反应而得到下述式(16)表示的化合物的工序
[0231]
工序3:使下述式(16)表示的化合物与下述式(17)或(18)表示的有机硼酸类在反应溶剂中、在碱和钯系催化剂的存在下反应而得到上述式(1)表示的化合物的工序
[0232][0233]
(式中,x1为1位、2位、3位或4位的取代基,且表示卤素原子,x2为5位、6位、7位或8位的取代基,且表示卤素原子。)
[0234][0235]
(式中,p1和p2相同或不同且为0~4的整数,r1、n1和n2与上述式(1)相同。)
[0236][0237]
(式中,x1和x2与上述式(13)相同。r1、p1和p2与式(14)相同。n1和n2为0~3的整数。)
[0238][0239]
(式中,x1和x2与上述式(13)相同。r1、l1、m1、m2、n1、n2、o1和o2与式(1)相同。
[0240][0241]
(式中,y表示芳香族基团,r
14
表示氢原子、烷基、烯基、烷氧基、卤素原子。l为0、1或2,在l=2时,r
14
可以相同或不同。)
[0242]
上述式(13)表示的化合物为与上述式(1)中芴骨架对应的芴酮化合物,x1为1位、2位、3位或4位的取代基,x2为5位、6位、7位或8位的取代基,x1和x2都表示卤素原子。
[0243]
以下,示出上述式(13)表示的芴酮化合物的代表例,作为本发明的上述式(1)中使用的原料,并不受它们限定。
[0244]
作为具体例,可优选举出1,8
‑
二氟芴酮、2,7
‑
二氟芴酮、3,6
‑
二氟芴酮、4,5
‑
二氟芴酮、1,8
‑
二氯芴酮、2,7
‑
二氯芴酮、3,6
‑
二氯芴酮、4,5
‑
二氯芴酮、1,8
‑
二碘芴酮、2,7
‑
二碘芴酮、3,6
‑
二碘芴酮、4,5
‑
二碘芴酮、1,8
‑
二溴芴酮、2,7
‑
二溴芴酮、3,6
‑
二溴芴酮、4,5
‑
二溴芴酮等。其中,优选1,8
‑
二溴芴酮、2,7
‑
二溴芴酮、3,6
‑
二溴芴酮、4,5
‑
二溴芴酮,特别优选2,7
‑
二溴芴酮。
[0245]
这些可以单独使用,或者混合2种以上,可以根据目的而任意选择。本发明中,优选为2,7
‑
二溴芴酮。
[0246]
所使用的上述式(13)表示的芴酮类的纯度没有特别限定,通常,优选95%以上,更优选为99%以上。应予说明,芴酮类可以使用市售品,也可以使用合成的制品。例如,作为制造二溴芴酮类的方法,可举出非专利文献(journal of american chemical society,2017,vol.139,11073
‑
11080)中记载的方法、即使9
‑
芴酮与溴在水中下反应的方法等。
[0247]
上述式(14)表示的醇类在上述式(13)表示的芴衍生物中与取代于9位的含有(多)羟基的芳烃环对应。即,上述式(14)中萘环与上述式(1)的萘环对应,r1、n1和n2与上述式(1)的r1、n1和n2对应。
[0248]
作为上述式(14)表示的化合物的具体例,可举出萘酚类(例如,萘酚(1
‑
萘酚、2
‑
萘酚)、具有烃基的萘酚(甲基萘酚、乙基萘酚、二甲基萘酚、丙基萘酚、丁基萘酚(c1‑4烷基萘酚)等烷基萘酚)、烷氧基萘酚(乙氧基萘酚等c1‑4烷氧基萘酚)、卤代萘酚(氯萘酚、溴萘
酚))、与这些萘酚类(或单羟基萘类)对应的多羟基萘(例如,1,3
‑
二羟基萘、1,4
‑
二羟基萘、2,3
‑
二羟基萘、1,5
‑
羟基萘、1,7
‑
二羟基萘、1,8
‑
二羟基萘、2,6
‑
二羟基萘、2,7
‑
二羟基萘、1,2,4
‑
三羟基萘、1,3,8
‑
三羟基萘等二或三羟基萘类)等。其中,优选1
‑
萘酚、2
‑
萘酚,特别优选2
‑
萘酚。这些醇类可以单独使用,或者也可以混合2种以上与芴酮类反应,可以根据目的而任意选择。本发明中优选为2
‑
萘酚。
[0249]
工序1的反应中,上述式(14)表示的醇类的使用量没有特别限定,从抑制副反应和经济性的方面考虑,相对于芴酮类1摩尔,优选为2~20摩尔,更优选为2.1~10摩尔,进一步优选为2.3~5摩尔。
[0250]
这些上述式(14)表示的醇类可以使用市售品,也可以使用合成的制品。例如,作为制造萘酚类的方法,可举出专利文献(日本特开昭61
‑
115039号公报)中记载的方法、即将使萘磺化所得的2
‑
萘磺酸用碱中和而得到2
‑
萘磺酸钠后、将产物进行碱溶解而制成碱盐、然后进行水解来制造2
‑
萘酚的方法等。
[0251]
作为原料使用的上述式(14)表示的醇类(例如,萘酚类等)的纯度没有特别限定,通常,优选为95%以上,更优选为99%以上。
[0252]
工序1的反应通常可以在酸催化剂的存在下进行。作为酸催化剂,例如,可举出硫酸、巯基乙酸、蒙脱石、杂多酸等,其中,特别是由于来自酸催化剂的杂质的生成少,容易得到本发明的具有芴骨架的化合物,因此特别优选杂多酸。
[0253]
本发明中优选使用的杂多酸一般为2种以上的不同的无机含氧酸缩合而生成的化合物的通称,可以通过中心的含氧酸与在其周围缩合的其它种类的含氧酸的组合而形成各种杂多酸。将形成中心的含氧酸的数量较少的元素称为杂元素,将形成在其周围缩合的含氧酸的元素称为多元素。多元素可以为一种元素,也可以为多种元素。
[0254]
构成杂多酸的含氧酸的杂元素没有特别限定,例如,可举出铜、铍、硼、铝、碳、硅、锗、锡、钛、锆、铈、钍、氮、磷、砷、锑、钒、铌、钽、铬、钼、钨、铀、硒、碲、锰、碘、铁、钴、镍、铑、锇、铱、铂。优选为磷(磷酸)或硅(硅酸)。另外,构成杂多酸的含氧酸的多元素没有特别限定,例如,可举出钒、钼、钨、铌、钽。优选为选自钒、钼和钨中的至少1种元素。
[0255]
作为构成杂多酸骨架的杂多酸阴离子,可以使用各种组成的杂多酸阴离子。例如,可举出xm
12
o
40
、xm
12
o
42
、xm
18
o
62
、xm6o
24
等。优选的杂多酸阴离子的组成为xm
12
o
40
。各式中,x为杂元素,m为多元素。作为具有这些组成的杂多酸,具体而言,可例示磷钼酸、磷钨酸、硅钼酸、硅钨酸、磷钼钒酸等。
[0256]
杂多酸可以为游离的杂多酸,也可以将质子的一部分或全部用其它阳离子置换而作为杂多酸的盐来使用。因此,本发明中所说的杂多酸还包含这些杂多酸的盐。作为可与质子置换的阳离子,例如,可举出铵、碱金属、碱土金属等。
[0257]
杂多酸可以为酐,也可以为含有结晶水的物质,为酐时,反应更快,而且副产物的生成得到抑制,因而优选。为含有结晶水的物质时,可以通过预先进行减压干燥、与溶剂的共沸脱水等脱水处理而得到与酐同样的效果。杂多酸也可以以担载于活性碳、氧化铝、二氧化硅
‑
氧化铝、硅藻土等载体的形态使用。
[0258]
这些杂多酸可以单独使用,也可以组合2种以上使用。另外,还可以根据需要在不损害本发明的目的的范围并用除杂多酸以外的其它催化剂。
[0259]
杂多酸的使用量没有特别限定,为了得到足够的反应速度,相对于芴酮类,优选为
0.0001重量倍以上,更优选为0.001~30重量倍,进一步优选为0.01~5重量倍。
[0260]
实施本发明时,工序1的反应中可以通过与上述杂多酸一起并用具有硫醇基(以下有时简记为sh基)的化合物来提高反应速度且抑制杂质的生成。作为本发明中可并用的硫醇化合物,例如,可举出巯基羧酸、烷硫醇和它们的盐。
[0261]
作为巯基羧酸,可举出α
‑
巯基丙酸、β
‑
巯基丙酸、硫代乙酸、巯基乙酸、硫代草酸、巯基琥珀酸、巯基苯甲酸等。另外,作为烷硫醇,可举出甲烷硫醇、乙烷硫醇、1
‑
丙烷硫醇、2
‑
丙烷硫醇、1
‑
丁烷硫醇、2
‑
丁烷硫醇、1
‑
戊烷硫醇、2
‑
戊烷硫醇、1
‑
己烷硫醇、1
‑
庚烷硫醇、2
‑
庚烷硫醇、1
‑
辛烷硫醇、2
‑
辛烷硫醇、1
‑
壬烷硫醇、1
‑
癸烷硫醇、1
‑
十一烷硫醇、1
‑
十二烷硫醇等c1‑
16
烷基硫醇等。这样的具有sh基的化合物中,从能够廉价地得到看,优选β
‑
巯基丙酸和1
‑
十二烷硫醇,特别优选1
‑
十二烷硫醇。
[0262]
这样的具有sh基的化合物可以单独使用,另外,也可以并用2种以上使用。
[0263]
实施工序1的反应的方法没有特别限定,通常,可以通过将上述式(13)、上述式(14)表示的化合物以及杂多酸和/或硫醇化合物投入到反应装置中,在空气中或氮、氩等非活性气体气氛下、在甲苯、二甲苯等芳香族烃系和乙酸乙酯、γ
‑
丁内酯、碳酸亚乙酯等酯类的非活性溶剂存在下加热搅拌来进行。此时,通过在除去催化剂所含有的水、反应生成水等反应体系内的水分的脱水条件下进行反应,能够与不脱水时相比反应进行得更快,副产物的生成得到抑制,能够以更高收率得到目标物。作为脱水的方法,没有特别限定,例如,可举出基于添加脱水剂的脱水、基于减压的脱水、基于常压或减压下与溶剂的共沸的脱水等。
[0264]
作为工序1中使用的反应溶剂,没有特别限定,例如可举出甲苯、二甲苯等芳香族烃溶剂、氯苯、二氯苯等卤代芳香族烃溶剂、戊烷、己烷、庚烷等脂肪族烃溶剂、二氯甲烷、1,2
‑
二氯乙烷等卤代脂肪族烃溶剂、乙醚、二异丙基醚、甲基叔丁基醚、二苯基醚、四氢呋喃、二烷等脂肪族和环状醚溶剂、乙酸乙酯、乙酸丁酯、γ
‑
丁内酯、碳酸亚乙酯等酯溶剂、乙腈、丙腈、丁腈、苄腈等腈溶剂、n,n
‑
二甲基甲酰胺、n,n
‑
二甲基乙酰胺、1
‑
甲基
‑2‑
吡咯烷酮等酰胺溶剂等。优选为芳香族烃溶剂和酯溶剂,更优选为甲苯、二甲苯、氯苯或二氯苯与乙酸乙酯、乙酸丁酯、γ
‑
丁内酯或碳酸亚乙酯的混合溶剂,进一步优选为甲苯与碳酸亚乙酯的混合溶剂。这些反应溶剂可以单独使用,另外,也可以并用2种以上使用。
[0265]
另外,其使用量没有特别限定,从经济性的方面考虑,相对于芴酮类,优选为0.1重量倍以上,更优选为0.5~100重量倍,进一步优选为1~20重量倍。
[0266]
工序1的反应温度根据所使用的原料、溶剂的种类而不同,优选为50~300℃,更优选为80~250℃,进一步优选为100~180℃。反应可以用液相色谱法等分析手段进行追踪。
[0267]
工序1的反应时的内压优选为101.3kpa以下的压力,更优选为60.0kpa以下。副生成的水在该内压下一边从体系内排出一边进行反应时反应更高效地进行,且生成的副产物也变少,因而优选。
[0268]
工序1的反应后,可以根据需要将所使用的固体酸通过过滤而除去或者进行中和。作为中和时使用的碱,例如,可举出氢氧化钠、氢氧化钾、氢氧化钙等碱金属或碱土金属的氢氧化物、碳酸钾、碳酸钙、碳酸钠、碳酸钠等碱金属或碱土金属的碳酸盐(碳酸氢)盐、胺类等。另外,还可以通过过滤、浓缩、萃取、晶析、重结晶、再沉淀、活性碳处理或与其类似的金属的除去处理、柱层析等分离手段或将这些组合的分离手段进行分离纯化。
[0269]
工序1的反应中,中和后的反应液可以不除去中和所生成的盐而用于与碳酸亚乙
酯的反应。根据需要,也可以将中和所生成的盐通过过滤进行分离,或者实施加入水进行搅拌并在静置后进行分液而除去水层的操作(也有时称为水洗工序)而将中和所生成的盐从反应体系内分离。该水洗工序可以根据需要而反复实施。
[0270]
工序1的反应后,可以不提取上述式(15)表示的芴化合物而与碳酸亚乙酯反应。即,可以将工序1和工序2用一锅法进行。利用浓缩、晶析等方法来提取上述式(15)表示的芴化合物时,有可能收率降低,导致成本上升。
[0271]
工序2中,碳酸亚乙酯相对于芴酮类1摩尔,通常使用2~10摩尔,优选使用2~8摩尔,更优选使用2~6摩尔。
[0272]
工序2中,实施上述式(15)表示的芴化合物与碳酸亚乙酯的反应时,可以根据需要在碱性化合物存在下进行反应。在碱性化合物存在下进行反应时,优选工序1中使用的固体酸在实施工序2之前通过过滤进行分离或者进行中和。
[0273]
作为工序2中可使用的碱性化合物,可例示碳酸盐类、碳酸氢盐类、氢氧化物类、有机碱类等。作为碳酸盐类,可举出碳酸钾、碳酸钠、碳酸铯、碳酸锂等。作为碳酸氢盐类,可举出碳酸氢钾、碳酸氢钠、碳酸氢锂、碳酸氢铯等。作为氢氧化物类,可举出氢氧化钠、氢氧化钾、氢氧化锂等。作为有机碱类,可举出三乙胺、二甲基氨基吡啶、三苯基膦、四甲基溴化铵、四甲基氯化铵等。上述的碱性化合物中,从处理性、安全性的观点考虑,优选使用碳酸钾、碳酸钠。这些碱性化合物可以单独使用,另外,也可以并用2种以上使用。
[0274]
工序2中使用碱性化合物时,其使用量相对于芴酮类1摩尔,通常为0.01~1.0摩尔,优选为0.03~0.5摩尔。
[0275]
工序2的反应结束后,优选进行在所得到的反应混合物中添加浓度3重量%以上的碱水溶液并在50℃以上的温度下加热搅拌的工序(以下,称为碱纯化工序)。添加到反应混合物溶液的碱水溶液的浓度优选为3重量%以上,更优选为6重量%,进一步优选为8重量%以上。通过添加浓度3重量%以上的碱水溶液并在50℃以上的温度进行加热搅拌,从而使式(15)表示的化合物1摩尔与碳酸亚乙酯3摩尔以上反应所得的副产物分解,成为式(16)表示的化合物。另外,由于能够将着色成分在碱水溶液中除去,因此能够得到高纯度且着色少的式(16)表示的化合物。碱水溶液的浓度低于3重量%时,不能高效地除去副产物、着色成分,因而不优选。碱浓度只要为3重量%以上,就没有特别限定,从碱的溶解度、操作容易性出发,优选为50重量%以下,更优选为30重量%以下,进一步优选为15重量%以下的浓度。
[0276]
加热搅拌碱水溶液的温度优选为50℃以上,更优选为60℃以上,进一步优选为80℃以上。另外,在所使用的溶剂的沸点以下的温度、更优选130℃以下进行。温度低于50℃时,无法除去副产物,或者无法高效地除去副产物,因而不优选。另外,温度高于130℃时,杂质增加,纯度降低,色调恶化,因而不优选。另外,搅拌时间没有特别限定,优选为0.5~10小时,更优选为1~9小时,进一步优选为2~8小时。
[0277]
本发明的碱水溶液中使用的碱没有特别限定,可举出氢氧化锂、氢氧化钠、氢氧化钾、四甲基氢氧化铵、四乙基氢氧化铵、氢氧化钙、氢氧化钡、碳酸钠、碳酸钾等。优选为氢氧化钠、氢氧化钾。碱的使用量没有特别限制,为了高效地进行副产物的除去、着色成分的除去,通常,相对于式(16)表示的化合物1摩尔,优选为0.1~20摩尔,更优选为0.2~10摩尔,更进一步优选为0.3~5摩尔。碱量少于0.1摩尔时,有时无法高效地除去副产物。另外,有时无法高效地除去着色成分,因而不优选。碱量多于20摩尔时,有时纯度降低、色调恶化,因而
不优选。
[0278]
本发明中,碱纯化工序可以在含有式(16)表示的化合物的反应混合物溶液中添加碱水溶液并进行加热搅拌,也可以将反应混合物溶液用有机溶剂稀释后添加碱水溶液并进行加热搅拌。通常,碱纯化工序在有机溶剂稀释后实施。稀释的有机溶剂没有特别限定,可举出苯、甲苯、二甲苯、均三甲苯等芳香族烃、戊烷、己烷、庚烷等脂肪族烃、氯苯、二氯苯等卤代芳香族烃、二甲基甲酰胺、二甲基亚砜等等。碱纯化操作后,可以将碱水溶液分液除去。
[0279]
工序2的反应结束后,所得到的反应混合物可以通过清洗、过滤、浓缩、萃取、晶析、重结晶、再沉淀、活性碳处理或与其类似的金属的除去处理、柱层析等分离手段或将这些组合的分离手段而进行分离纯化。根据需要从实施上述后处理的反应混合物中析出上述式(16)表示的化合物的操作通过使根据需要与溶剂混合的反应混合物达到50℃~溶剂的沸点(优选为70~110℃),并将其冷却到小于50℃来实施。上述式(16)表示的化合物的晶体在50℃以上从反应混合物中析出时,可以将在50℃以上时晶体不析出的量的稀释溶剂与反应混合物混合后,使所得到的混合物达到50℃~溶剂的沸点(优选为70~110℃),并将其冷却到小于50℃来实施。作为晶析溶剂,可举出作为上述反应中使用的溶剂所例示的溶剂、甲醇、乙醇、丙醇、异丙醇、丁醇、叔丁醇、异丁醇和戊醇等醇溶剂、碳酸二甲酯、碳酸二乙酯等碳酸溶剂、乙酸乙酯、乙酸丁酯、γ
‑
丁内酯、苯甲酸丁酯、苯甲酸甲酯、乙酸苯酯等酯溶剂、乙醚、二异丙基醚、甲基叔丁基醚、二苯基醚、四氢呋喃等醚溶剂、己烷、庚烷、辛烷、戊烷等脂肪族烃溶剂等,优选甲醇、乙醇、甲苯或碳酸二甲酯。
[0280]
这样的晶析操作可以进行一次,也可以反复进行多次。特别是,如果使用甲醇、乙醇等醇,则能够简便且高效地除去未反应的2
‑
萘酚、副生成的乙二醇单(2
‑
萘基)醚等杂质。
[0281]
析出的晶体通过过滤等进行回收。所得到的晶体可以使用上述反应中采用的溶剂等进行清洗,也可以进行干燥。这样得到的上述式(16)表示的化合物的纯化物的纯度优选为90%以上,更优选为95%以上。工序2的反应后,可以不提取上述式(16)表示的化合物而以一锅法进行工序3。此外,也可以将工序1~3全部用一锅法进行。能够通过用一锅法进行来提高收率、生产率。
[0282]
上述式(17)或(18)表示的化合物的环y与上述式(1)中基团ar1和ar2对应。另外,上述式(17)和(18)中,基团r
14
的优选的方式与上述r1的优选的方式相同,l的优选方式与上述n1和n2的优选方式相同。
[0283]
所使用的有机硼酸类的纯度没有特别限定,通常,优选为95%以上,更优选为99%以上。应予说明,有机硼酸类可以使用市售品,也可以使用合成的制品。作为制造有机硼酸类的方法,例如可举出专利文献(日本特开2002
‑
47292号公报)中记载的方法、即使苯基格氏试剂与溶解于非醚系芳香族溶剂的硼酸酯类反应的方法等。
[0284]
本发明中使用的有机硼酸包括上述式(14)和(15)表示的烷基硼酸、烯基硼酸、芳基硼酸、杂芳基硼酸及其酐等,作为烷基硼酸,包含丁基硼酸、环己基硼酸、环戊基硼酸、2
‑
乙基硼酸、4
‑
乙基硼酸、己基硼酸、异丁基硼酸、异丙基硼酸、甲基硼酸、正辛基硼酸、丙基硼酸、戊基硼酸、2
‑
苯基乙基硼酸、它们的酐,作为烯基硼酸,包含1
‑
环戊烯基硼酸、二茂铁硼酸、1,1
’‑
二茂铁二硼酸、它们的酐,作为芳基硼酸,包含2
‑
蒽硼酸、9
‑
蒽硼酸、苄基硼酸、2
‑
联苯硼酸、3
‑
联苯硼酸、4
‑
联苯硼酸、2,3
‑
二甲基苯基硼酸、2,4
‑
二甲基苯基硼酸、2,5
‑
二甲基苯基硼酸、2,6
‑
二甲基苯基硼酸、3,4
‑
二甲基苯基硼酸、3,5
‑
二甲基苯基硼酸、2
‑
乙氧基
苯基硼酸、3
‑
乙氧基苯基硼酸、4
‑
乙氧基苯基硼酸、6
‑
甲氧基
‑2‑
萘硼酸、2
‑
甲基苯基硼酸、3
‑
甲基苯基硼酸、4
‑
甲基苯基硼酸、1
‑
萘硼酸、2
‑
萘硼酸、9
‑
菲硼酸、10
‑
苯基
‑9‑
蒽硼酸、苯基硼酸、苯基乙烷硼酸、4
‑
苯基(萘
‑1‑
基)硼酸、3
‑
丙氧基苯基硼酸、3
‑
异丙氧基苯基硼酸、4
‑
异丙氧基苯基硼酸、4
‑
丙基苯基硼酸、4
‑
异丙基苯基硼酸、10
‑
(萘
‑1‑
基)
‑9‑
蒽硼酸、10
‑
(萘
‑2‑
基)
‑9‑
蒽硼酸、它们的酐,作为杂芳基硼酸,包含苯并呋喃
‑2‑
硼酸、二苯并呋喃
‑4‑
硼酸、5
‑
甲酰基
‑2‑
呋喃硼酸、5
‑
甲酰基噻吩
‑2‑
硼酸、呋喃
‑2‑
硼酸、呋喃
‑3‑
硼酸、吡啶
‑3‑
硼酸、吡啶
‑4‑
硼酸、喹啉
‑2‑
硼酸、喹啉
‑3‑
硼酸、喹啉
‑4‑
硼酸、喹啉
‑5‑
硼酸、喹啉
‑6‑
硼酸、喹啉
‑8‑
硼酸、异喹啉
‑4‑
硼酸、2
‑
噻吩硼酸、3
‑
噻吩硼酸、5
‑
嘧啶硼酸、它们的酐。
[0285]
这些可以单独使用,或者混合2种以上,可以根据目的而任意选择。本发明中,优选为苯基硼酸、2
‑
萘硼酸或其酐,特别优选为苯基硼酸或其酐。
[0286]
作为原料使用的上述式(17)表示的化合物的使用比率相对于上述式(16)表示的化合物1摩尔,可以优选为2~5摩尔,更优选为2.05~3.0摩尔,进一步优选为2.1~2.5摩尔左右。该有机硼酸类小于2摩尔时,有时上述式(1)表示的产物的收率变低。另外,超过5摩尔时,虽然反应速度变快,收率变高,但存在该具有芴骨架的化合物的制造成本上升的情况。
[0287]
另外,上述式(18)表示的化合物的使用比率相对于上述式(16)表示的化合物1摩尔,可以优选为0.7~5摩尔,更优选为0.8~3摩尔,进一步优选为1~2摩尔左右。该有机硼酸类小于0.7摩尔时,有时上述式(1)表示的产物的收率变低。另外,超过5摩尔时,虽然反应速度变速,收率变高,但存在该具有芴骨架的化合物的制造成本上升的情况。
[0288]
工序3的上述式(16)与上述式(17)和/或(18)表示的化合物的反应(脱卤反应)可以在反应溶剂中、在碱和催化剂的存在下进行。
[0289]
作为工序3的反应中使用的碱,例如,可举出氢氧化钠、氢氧化钾等氢氧化物、碳酸钠(na2co3)、碳酸钾(k2co3)、碳酸铯(cs2co3)等碳酸盐、乙酸钠、乙酸钾等乙酸盐、磷酸钠(na3po4)、磷酸钾(k3po4)等磷酸盐等无机盐、三乙胺类、吡啶、吗啉、喹啉、哌啶、苯胺类、四正丁基乙酸铵等铵盐等有机盐等。其中,优选使用碳酸盐,优选碳酸钾和/或碳酸钠。这样的碱可以单独使用,另外,也可以并用2种以上使用。
[0290]
另外,工序3的反应中,上述碱的使用量没有特别限定,相对于有机硼酸类1摩尔,优选添加1~30当量,更优选添加1~10当量。
[0291]
作为工序3的反应中使用的钯系催化剂,优选铃木偶联反应中使用的钯化合物,例如,可举出四(三苯基膦)钯、双(三苯基膦)二氯化钯、乙酸钯、三(二亚苄基丙酮)二钯、双(二亚苄基丙酮)钯、双[4
‑
(n,n
‑
二甲基氨基)苯基]二叔丁基膦二氯化钯、双(二叔丁基异戊二烯基膦)二氯化钯、双(二叔巴豆基膦)二氯化钯、pd/sio2表示的钯系催化剂等。其中,优选四(三苯基膦)钯和/或pd/sio2表示的钯系催化剂。这样的钯系催化剂可以单独使用,另外,也可以并用2种以上使用。
[0292]
工序3的反应中,上述催化剂的使用量没有特别限定,相对于上述式(16)表示的化合物1摩尔,以钯金属原子换算计优选为0.1~10mmol,更优选为0.5~5mmol。钯催化剂的使用量以钯金属原子换算计小于0.1mmol时,有时反应变得不易结束。另外,钯催化剂的使用量以钯金属原子换算计超过10mmol时,虽然反应结束,但难以使该具有芴骨架的化合物中的钯元素含量在式(2)的范围内,不仅有可能使使用该醇原料所制造的热塑性树脂的色调恶化,而且有时该具有芴骨架的化合物的制造成本上升。
[0293]
作为工序3中使用的反应溶剂,没有特别限定,例如可以将甲苯、二甲苯等芳香族烃系溶剂与甲醇、乙醇、异丙醇、正丁醇等醇类单独或并用使用。芳香族烃系溶剂由于为高沸点溶剂,因此可以将反应温度设定得较高,另外,通过使用醇而使与水的亲和性良好,反应性变得良好,因而优选使用。这样的溶剂可以单独使用,或者也可以并用2种以上使用。此外,也可以使用n,n
‑
二甲基甲酰胺或n,n
‑
二甲基乙酰胺等非质子性溶剂、邻二氯苯等卤代苯类。这样的溶剂可以单独使用,另外,也可以并用2种以上使用。本发明中,更优选甲苯与乙醇的混合溶剂。
[0294]
上述反应溶剂(在本发明的情况下为甲苯与乙醇的混合溶剂)的使用量没有特别限定,相对于上述式(16)表示的化合物1摩尔,甲苯优选为0.1重量倍以上,更优选为0.5~100重量倍,进一步优选为1~50重量倍。甲苯的使用量小于0.1重量倍时,有可能产物析出而难以搅拌。另外,甲苯的使用量超过100重量倍时,没有与使用量匹配的效果,容积效率也恶化,存在该具有芴骨架的化合物的制造成本上升的情况。另外,乙醇的使用量也没有特别限定,相对于上述式(16)表示的化合物1摩尔,优选为0.1~50重量倍,更优选为1~20重量倍。乙醇的使用量小于0.1重量倍时,有可能反应速度慢,收率下降。另外,乙醇的使用量超过50重量倍时,与甲苯同样,没有与使用量匹配的效果,容积效率也恶化,存在该具有芴骨架的化合物的制造成本上升的情况。
[0295]
反应温度根据所使用的原料、溶剂的种类而不同,优选为50~150℃,更优选为60~130℃,进一步优选为70~120℃。反应可以用液相色谱法等分析手段进行追踪。
[0296]
反应结束后的反应混合物中通常除了所生成的上述式(1)表示的化合物以外,还包含未反应的有机硼酸类、碱、催化剂、副反应产物等。因此,可以通过惯用方法例如过滤、浓缩、萃取、晶析、重结晶、再沉淀、活性碳处理或者与其类似的金属的除去处理、柱层析等分离手段或将这些组合的分离手段而进行分离纯化。例如,优选利用惯用方法(加入碱水溶液而形成水溶性的复合体的方法等)而除去有机硼酸类,进行活性碳处理或与其类似的金属的除去处理而除去钯化合物后,添加重结晶溶剂进行冷却使其重结晶化,接着,进行过滤分离而纯化。重结晶的方法与上述工序2中记载的方法相同。
[0297]
利用本发明的制造方法所得到的上述式(1)表示的化合物的纯度可以从60~100%的较宽范围中选择,优选为70%以上,更优选为80%以上,进一步优选为90%以上,更进一步优选为95%以上。
[0298]
[具有芴骨架的化合物的特征和用途]
[0299]
本发明的具有芴骨架的化合物由于优选将二苯基芴骨架和二萘基芴骨架与芳烃环组合,因此不仅折射率、耐热性高,而且能够在制成聚合物时减少双折射。到目前为止,为了提高折射率,已经使用了在芴骨架的9位取代有环集合芳烃环的芴化合物,但该芴化合物虽然折射率、耐热性高,但双折射会降低。与此相对,本发明的具有芴骨架的化合物可能是由于具有二苯基芴骨架和二萘基芴骨架,因此尽管折射率高,但双折射也变小。此外,由于芳烃环具有1个以上的羟基,芴化合物整体具有多个羟基,因此反应性高。因此,本发明的具有芴骨架的化合物可以作为各种树脂的原料(单体)利用。例如,可以作为热塑性树脂(例如,聚酯树脂、聚碳酸酯树脂、聚酯碳酸酯树脂、聚氨酯树脂等)、热固性树脂(例如,环氧树脂、酚醛树脂、热固化性聚氨酯树脂、(甲基)丙烯酸酯等)的多元醇成分使用。将本发明的具有芴骨架的化合物作为多元醇成分使用时,可能是由于在芴骨架的9位取代了萘环且在芴
骨架上具有二芳基,因此所得到的树脂具备能够以高水平兼具高折射率和低双折射性的优点。
[0300]
另外,本发明的具有芴骨架的化合物能够在通用的溶剂中高效地制备衍生物。
[0301]
本发明的具有芴骨架的化合物的熔点能够从100~300℃的较宽范围中选择,优选为120~280℃,更优选为130~260℃,进一步优选为140~240℃。
[0302]
实施例
[0303]
以下,根据实施例对本发明进行详细说明,本发明只要不超出其主旨,就不限定于以下的实施例。
[0304]
<本发明的方式i>
[0305]
实施例中,各种测定如下进行。
[0306]
(1)高效液相色谱(hplc)测定
[0307]
使用日立制高效液相色谱仪l
‑
2350对实施例中得到的化合物按照下表1的测定条件进行测定。实施例中,只要没有特别说明,%就为除去hplc中的溶剂进行校正所得的面积百分率值。
[0308]
表1
[0309][0310]
(2)nmr测定
[0311]
对实施例中得到的化合物、树脂利用下述装置、溶剂进行测定。
[0312]
装置:日本电子公司制jnm
‑
al400(400mhz)
[0313]
溶剂:cdcl3[0314]
(3)icp测定
[0315]
对实施例中得到的化合物利用下述装置进行测定。
[0316]
使用仪器:agilent technologies
[0317]
装置:agilent5100 icp
‑
oes
[0318]
(4)玻璃化转变温度(tg)测定,差示扫描量热测定(dsc)
[0319]
对实施例中得到的化合物、树脂利用下述装置、条件进行测定。
[0320]
装置:ta instruments制discovery dsc25
[0321]
条件:升温速度20℃/min
[0322]
(5)粒料b*值测定
[0323]
将实施例中得到的树脂用下述装置进行测定。
[0324]
装置:x
‑
rite公司制积分球分光光度计ce
‑
7000a
[0325]
(6)折射率(nd),阿贝数测定
[0326]
将实施例中得到的树脂利用下述装置、方法进行测定。
[0327]
装置:atago公司制dr
‑
m2阿贝折射计
[0328]
方法:使聚合结束后所得到的树脂粒料溶解于二氯甲烷,流延到玻璃皿上,进行干燥,对所制成的膜的25℃时的折射率(波长:589nm)和阿贝数(由波长486nm、589nm、656nm处的折射率利用下述式进行计算)进行测定。
[0329]
ν=(nd
‑
1)/(nf
‑
nc)
[0330]
应予说明,本发明中,
[0331]
nd表示波长589nm处的折射率,
[0332]
nc表示波长656nm处的折射率,
[0333]
nf表示波长486nm处的折射率。
[0334]
(7)粉末x射线衍射测定
[0335]
使用rigaku rint ttr iii按照下述测定条件进行测定。
[0336]
x射线源:cu
‑
kα,输出功率:50kv
‑
300ma(15kw)
[0337]
ds:1/2
°
,hs:10mm,ss:1/2
°
,rs:0.15
°
,
[0338]
step:0.01
°
,扫描速度:1.0
°
/min
[0339]
[实施例i
‑
1]
[0340]
<工序1>
[0341]
在具备搅拌机、冷却器以及温度计的烧瓶中使2,7
‑
二溴芴酮(以下,有时简记为dbfn)101.4g(0.30摩尔)、苯基硼酸76.8g(0.63mmol)溶解于甲苯1l和乙醇200ml的混合溶剂,进一步添加四(三苯基膦)钯1.7g(1.45mmol)、2m碳酸钾水溶液347ml后,以80℃搅拌6小时,由此进行反应。反应的进行程度利用hplc来确认,看到dbfn的残留量为0.1%以下而使反应结束。将得到的反应液减压浓缩而馏去甲苯和乙醇后,在残渣中加入1m氢氧化钠水溶液,用氯仿进行萃取。将氯仿层用活性碳进行脱钯催化剂处理,除去残留于体系内的钯催化剂后,将氯仿浓缩,在析出黄色晶体的时刻停止浓缩,直接进行重结晶。滤出所析出的黄色固体晶体,在85℃下干燥24小时,由此以收率81%得到作为目标物的2,7
‑
二苯芴酮(以下,有时简记为dpfn)的黄色晶体80.5g。利用hplc来测定所得到的黄色晶体的纯度,结果为99.8%。
[0342]
<工序2>
[0343]
向具备搅拌机、冷却器、水分离器以及温度计的烧瓶中加入工序1中制造的dpfn56.5g(0.17摩尔)、2
‑
萘酚58.8g(0.41摩尔)、十二钨(vi)磷酸n水合物(h3[pw
12
o
40
]
·
nh2o)0.8g(0.24mmol)、正十二烷硫醇1.8g(0.01摩尔)、甲苯53ml、γ
‑
丁内酯13ml后,减压
到55kpa后,升温到100℃,在同一温度下进行10小时搅拌。反应的进行程度利用hplc来确认,看到dpfn的残留量为0.3%以下使反应结束。
[0344]
反应后,加入25重量%氢氧化钠水溶液,中和十二钨(vi)磷酸n水合物(h3[pw
12
o
40
]
·
nh2o)后,在120℃馏去体系内的水(称为水洗工序)。水洗工序结束后,加入碳酸钾1.2g(8.87mmol)、碳酸亚乙酯37.4g(0.42摩尔),在110℃搅拌15小时进行反应。利用hplc来确认反应的进行程度,看到下述(8
‑
1)表示的9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴的残留量为0.2%以下使反应结束。
[0345][0346]
反应结束后,在所得到的反应液中加入水和25重量%氢氧化钠水溶液,在85℃搅拌5小时后,分离水层。将得到的反应液冷却至20℃,直接进行晶析,由此得到目标的9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴(以下,有时简记为bndp)的淡黄色固体。所得到的bndp进行活性碳处理和水洗后,减压加热干燥一晩,以收率78%、纯度98.8%得到淡黄色固体。利用icp来测定残留金属量,结果,pd为1ppm以下。dpfn为0.2%,apha为500。
[0347]
将由此合成的9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴25.91质量份、9,9
‑
双[4
‑
(2
‑
羟基乙氧基)苯基]芴16.44质量份、碳酸二苯酯16.23质量份和碳酸氢钠3.15
×
10
‑3质量份装入到带有搅拌机和馏出装置的反应釜中,进行3次氮置换后,将夹套加热到200℃,使原料熔融。完全熔解后,用5分钟减压到20kpa,同时以60℃/hr的速度将夹套升温到260℃,进行酯交换反应。其后,在将夹套保持在260℃的状态下,用50分钟减压至0.13kpa,在260℃、0.13kpa以下的条件下进行聚合反应直到达到规定的扭矩。反应结束后,将生成的树脂一边造粒一边拉出,得到聚碳酸酯树脂的粒料。将所得到的聚碳酸酯树脂利用1h nmr进行分析,确认了9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴成分相对于所有单体成分导入了50mol%。所得到的聚碳酸酯树脂的折射率为1.682,阿贝数为17.1,tg为177℃,粒料b*值为13.5。
[0348]
[实施例i
‑
2]
[0349]
将工序1中的苯基硼酸变更为苯基硼酸酐,除此以外,与实施例i
‑
1同样地得到目标的芴化合物(收率78%,纯度98.8%)。利用icp来测定残留金属量,结果,pd为1ppm以下。
[0350]
[实施例i
‑
3]
[0351]
将工序1中的碱变更为碳酸钠,除此以外,与实施例i
‑
1同样地得到芴化合物(收率78%,纯度98.8%)。利用icp来测定残留金属量,结果,pd为1ppm以下。
[0352]
[实施例i
‑
4]
[0353]
将工序1中的钯系催化剂变更为pd/sio2表示的pl催化剂,除此以外,与实施例i
‑
1同样地得到芴化合物(收率78%,纯度98.9%)。利用icp来测定残留金属量,结果,pd为1ppm以下。
[0354]
[实施例i
‑
5]
[0355]
将工序2中的酸催化剂变更为硅钨酸的n水合物(h4[siw
12
o
40
]
·
nh2o),除此以外,
与实施例i
‑
1同样地得到芴化合物(收率78%,纯度98.8%)。利用icp来测定残留金属量,结果,pd为1ppm以下。
[0356]
[实施例i
‑
6]
[0357]
向具备搅拌机、冷却器、水分离器以及温度计的烧瓶中加入实施例i
‑
1的工序1中制造的dpfn28.1g(0.08摩尔)、2
‑
萘酚29.3g(0.20摩尔)、十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)0.4g(0.12mmol)、正十二烷硫醇1.8g(0.01摩尔)、甲苯30ml、碳酸亚乙酯7.8g(0.09摩尔)后,减压到55kpa后,升温到100℃,在同一温度下进行3小时搅拌。反应的进行程度利用hplc来确认,看到dpfn的残留量为0.0%使反应结束。
[0358]
反应后,加入25重量%氢氧化钠水溶液中和十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)后,在120℃馏去体系内的水(称为水洗工序)。水洗工序结束后,加入碳酸钾0.6g(4.41mmol)、碳酸亚乙酯29.4g(0.33摩尔)、二甲基甲酰胺100ml,在110℃搅拌4小时进行反应。利用hplc来确认反应的进行程度,看到9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴的残留量为0.0%使反应结束。
[0359]
反应结束后,在所得到的反应液中加入水和25重量%氢氧化钠水溶液,在85℃搅拌1.5小时后,分离水层。将所得到的反应液冷却到20℃直接进行晶析,由此得到bndp。所得到的bndp进行活性碳处理和水洗后,减压加热干燥一晩,以收率78%、纯度98.8%得到白色晶体。另外,pd为1ppm以下,dpfn为0.0%,apha为80,dsc的吸热峰为237℃。将dsc图谱示于图1,将粉末x射线测定图谱示于图2,将粉末x射线测定的主要的峰示于表2。
[0360]
表2
[0361]
[0362]
[实施例i
‑
7]
[0363]
向具备搅拌机、冷却器、水分离器以及温度计的烧瓶中加入工序1中制造的dpfn28.1g(0.08摩尔)、2
‑
萘酚29.3g(0.20摩尔)、十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)0.8g(0.23mmol)、正十二烷硫醇1.8g(0.01摩尔)、甲苯45ml、碳酸亚乙酯37.20g(0.42摩尔)后,减压到55kpa后,升温到100℃,在同一温度下进行9小时搅拌。反应的进行程度利用hplc来确认,看到dpfn的残留量为0.0%使反应结束。
[0364]
反应后,加入25重量%氢氧化钠水溶液中和十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)后,在120℃馏去体系内的水(称为水洗工序)。水洗工序结束后,加入碳酸钾0.6g(4.41mmol)、二甲基甲酰胺100ml,在110℃搅拌4小时进行反应。利用hplc来确认反应的进行程度,看到9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴的残留量为0.0%以下使反应结束。
[0365]
反应结束后,在所得到的反应液中加入水和25重量%氢氧化钠水溶液,在85℃搅拌1.5小时后,分离水层。将得到的反应液冷却到20℃直接进行晶析,由此得到bndp。所得到的bndp进行活性碳处理和水洗后,减压加热干燥一晩,以收率78%、纯度98.8%得到白色晶体。另外,pd为1ppm以下,dpfn为0.0%,apha为90。
[0366]
[比较例i
‑
1]
[0367]
工序1中,将反应溶剂变更为甲苯,除此以外,与实施例i
‑
1同样地进行芴酮化合物的合成,反应不进行,无法得到目标的芴酮化合物。
[0368]
[比较例i
‑
2]
[0369]
将工序1中的四(三苯基膦)钯的使用量变更为0.56g(0.48mmol),除此以外,与实施例i
‑
1同样地进行芴化合物的合成,虽然反应进行,但二苯基体和单苯基体会以95:5(重量比)混合,无法以高纯度得到目标的芴酮化合物。
[0370]
[比较例i
‑
3]
[0371]
工序2中,将酸催化剂变更为硫酸和3
‑
巯基丙酸,除此以外,与实施例i
‑
1同样地进行芴化合物的合成,反应不进行,无法得到目标的芴化合物。
[0372]
[参考例i
‑
1]
[0373]
工序1和工序2中,不进行活性碳处理,除此以外,与实施例i
‑
1同样地得到芴化合物(bndp)的黄色固体(收率78%,纯度98.1%)。利用icp来测定残留金属量,结果,pd为70ppm。apha超过500。
[0374]
工序2中,使用上述方法中合成的9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴,除此以外,与实施例1同样地得到聚碳酸酯树脂的粒料。将得到的聚碳酸酯树脂利用1h nmr进行分析,确认9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴成分相对于所有单体成分导入了50摩尔%。所得到的聚碳酸酯树脂的折射率为1.682,阿贝数为17.1,tg为177℃,粒料b*值为32.3。
[0375]
[参考例i
‑
2]
[0376]
工序2中,使反应压力为101.3kpa(常压),除此以外,与实施例i
‑
1同样地进行芴化合物的合成,但反应未完成,dpfn残留了5重量%,导致bndp的纯度降低。此外,与实施例i
‑
1的工序2同样地使用该单体而得到的聚碳酸酯树脂的粒料b*值为105。
[0377]
[参考例i
‑
3]
[0378]
工序2中,将反应溶剂变更为甲苯,除此以外,与实施例i
‑
1同样地进行芴化合物的合成,但反应未完成,dpfn残留了10重量%,导致目标的bndp的纯度降低。所得到的黄色固体的收率为50%,纯度为88.7%。与实施例i
‑
1的工序2同样地使用该单体而得到的聚碳酸酯树脂的粒料b*值为200。
[0379]
<本发明的方式ii>
[0380]
实施例中,各种测定如下进行。
[0381]
(1)高效液相色谱(hplc)测定
[0382]
使用日立制高效液相色谱l
‑
2350,按照表3的测定条件进行测定。实施例中,只要没有特别说明,%就为除去hplc中的溶剂进行校正所得的面积百分率值。
[0383]
表3
[0384][0385]
(2)icp测定
[0386]
将实施例中得到的化合物利用下述装置进行测定。
[0387]
使用仪器:agilent technologies
[0388]
装置:agilent5100 icp
‑
oes
[0389]
(3)燃烧离子色谱测定
[0390]
使用三菱化学制自动试样燃烧装置aqf
‑
2100和thermo fisher制离子色谱系统dionex aquion,按照下述测定条件,进行硫元素的含量(s量)和溴元素的含量(br量)的测定。应予说明,标准曲线的制作是使用wako制溴化物离子标准液(br
‑
1000)和硫酸根离子标准液(so4(2
‑
):1000)而进行。
[0391]
测定温度:900℃
→
1000℃
[0392]
吸收液:加入过氧化氢的超纯水
[0393]
柱子:as
‑
17/ag
‑
17
[0394]
流速:1ml/min
[0395]
样品池温度:40℃,
[0396]
柱温:35℃
[0397]
(4)apha测定
[0398]
将使测定试样0.5g溶解于二甲基甲酰胺10ml而得的溶液装入φ25mm的试管中,使用日本电色制工业(株)制tz6000进行测定。
[0399]
[实施例ii
‑
1]
[0400]
<工序1和工序2>
[0401]
向具备搅拌机、冷却器以及温度计的烧瓶中加入2,7
‑
二溴芴酮(以下,有时简记为dbfn)28.1g(0.08摩尔)、2
‑
萘酚28.8g(0.20摩尔)、正十二烷硫醇1.8g(0.01摩尔)、十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)0.4g(0.12mmol)、甲苯30ml、碳酸亚乙酯7.7g后,减压到50kpa后,升温到100℃,在同一温度下搅拌5小时。反应的进行程度利用hplc来确认,看到dbfn的残留量为0.0%使反应结束。
[0402]
反应后,加入25重量%氢氧化钠水溶液中和十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)后,在120℃馏去体系内的水。其后,加入碳酸钾0.6g(4.16mmol)、碳酸亚乙酯28.9g(0.33摩尔)、二甲基甲酰胺100ml,在110℃下搅拌5小时进行反应。利用hplc来确认反应的进行程度,确认9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二溴芴的残留量为0.0%使反应结束。反应结束后,在得到的反应液中加入水和25重量%氢氧化钠水溶液,在85℃搅拌1.5小时后,分离水层。将所得到的反应液浓缩,加入甲苯使其溶解后,进行5次温水清洗。其后,用甲醇进行2次重结晶,减压加热干燥一晩,以收率77%、纯度97.4%得到9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二溴芴(以下,有时简记为bndb)的白色晶体。
[0403]
<工序3>
[0404]
向具备搅拌机、冷却器、水分离器以及温度计的烧瓶中加入工序1中制造的bndb44.7g(0.06摩尔)、苯基硼酸17.2g(0.14摩尔)、四(三苯基膦)钯0.7g(0.64mmol)、2m碳酸钾水溶液78ml、甲苯292ml、乙醇96ml后,在80℃搅拌3小时。反应的进行程度利用hplc来确认,看到bndb的残留量为0.0%使反应结束。反应后,将所析出的bndp过滤回收后,使其溶解于四氢呋喃进行活性碳处理后,用甲苯进行重结晶,将得到的晶体减压加热干燥一晩,以收率74%、纯度99.2%得到9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴(以下,有时简记为bndp)的白色晶体。另外,apha为60,s为20ppm,br为8ppm,pd为5ppm,二苯芴酮(以下,有时简写为dpfn)利用hplc进行测定,为0.0%。
[0405]
[实施例ii
‑
2]
[0406]
<工序1~3>
[0407]
向具备搅拌机、冷却器以及温度计的烧瓶中加入2,7
‑
二溴芴酮(以下,有时简记为dbfn)28.1g(0.08摩尔)、2
‑
萘酚28.8g(0.20摩尔)、正十二烷硫醇0.2g(0.83mmol)、十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)0.4g(0.12mmol)、甲苯30ml、碳酸亚乙酯7.7g后,减压到50kpa后,升温到100℃,在同一温度下搅拌3小时。反应的进行程度利用hplc来确认,看到dbfn的残留量为0.0%使反应结束。
[0408]
反应后,加入25重量%氢氧化钠水溶液中和十二钨(vi)磷酸n水合物(h3[pw12o40]
·
nh2o)后,在120℃下馏去体系内的水。其后,加入碳酸钾0.6g(4.16mmol)、碳酸
亚乙酯28.9g(0.33摩尔)、二甲基甲酰胺100ml,在110℃下搅拌4小时。利用hplc来确认反应的进行程度,看到9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二溴芴的残留量为0.0%使反应结束。
[0409]
反应后,加入苯基硼酸22.3g(0.18摩尔)、四(三苯基膦)钯0.5g(0.42mmol)、2m碳酸钾水溶液91ml、甲苯170ml、乙醇100ml后,在80℃搅拌3小时。反应的进行程度利用hplc来确认,看到bndb的残留量为0.0%使反应结束。反应后,将析出的bndp过滤回收后,使其溶解于四氢呋喃进行活性碳处理后,用甲苯进行重结晶,将得到的晶体减压加热干燥一晩,以收率75%、纯度99.0%得到9,9
‑
双[6
‑
(2
‑
羟基乙氧基)
‑2‑
萘基]
‑
2,7
‑
二苯基芴(以下,有时简记为bndp)的白色晶体。另外,apha为80,s为8ppm,br为15ppm,pd为3ppm,dpfn利用hplc进行测定,为0.0%。
[0410]
[比较例ii
‑
1]
[0411]
工序3中,将反应溶剂变更为甲苯,除此以外,与实施例ii
‑
1同样地进行芴酮化合物的合成,但反应不进行,无法得到目标的芴酮化合物。
[0412]
[比较例ii
‑
2]
[0413]
将工序3中的四(三苯基膦)钯的使用量变更为0.56g(0.48mmol),除此以外,与实施例ii
‑
1同样地进行芴化合物的合成,虽然反应进行,但二苯基体和单苯基体会以95:5(重量比)混合,无法以高纯度得到目标的芴酮化合物。
[0414]
[比较例ii
‑
3]
[0415]
工序1中,将酸催化剂变更为硫酸和3
‑
巯基丙酸,除此以外,与实施例ii
‑
1同样地进行芴化合物的合成,但反应不进行无法得到目标的芴化合物。
[0416]
[比较例ii
‑
4]
[0417]
在具备搅拌机、冷却器以及温度计的烧瓶中使2,7
‑
二溴芴酮(以下,有时简记为dbfn)101.4g(0.30摩尔)、苯基硼酸76.8g(0.63mmol)溶解于甲苯1l和乙醇200ml的混合溶剂,进一步添加四(三苯基膦)钯1.7g(1.45mmol)、2m碳酸钾水溶液347ml后,以80℃搅拌6小时,由此进行反应。反应的进行程度利用hplc来确认,看到dbfn的残留量为0.1%以下使反应结束。将得到的反应液减压浓缩馏去甲苯和乙醇后,在残渣中加入1m氢氧化钠水溶液用氯仿萃取。浓缩氯仿,在黄色晶体析出的时刻停止浓缩,直接进行重结晶。滤取所析出的黄色固体晶体,在85℃干燥24小时,由此以80.5g、收率81%得到作为目标物的2,7
‑
二苯芴酮(以下,有时简记为dpfn)的黄色晶体。利用hplc来测定所得到的黄色晶体的纯度,结果为99.8%。
[0418]
向具备搅拌机、冷却器、水分离器以及温度计的烧瓶中加入上述得到的dpfn56.5g(0.17摩尔)、2
‑
萘酚58.8g(0.41摩尔)、十二钨(vi)磷酸n水合物(h3[pw
12
o
40
]
·
nh2o)0.8g(0.24mmol)、正十二烷硫醇3.6g(0.02摩尔)、甲苯53ml、γ
‑
丁内酯13ml后,减压到55kpa后,升温到100℃,在同一温度下进行10小时搅拌。反应的进行程度利用hplc来确认,看到dpfn的残留量为0.3%以下使反应结束。
[0419]
反应后,加入25重量%氢氧化钠水溶液中和十二钨(vi)磷酸n水合物(h3[pw
12
o
40
]
·
nh2o)后,在120℃下馏去体系内的水(称为水洗工序)。水洗工序结束后,加入碳酸钾1.2g(8.87mmol)、碳酸亚乙酯37.4g(0.42摩尔),在110℃下搅拌15小时进行反应。利用hplc来确认反应的进行程度,看到9,9
’‑
双(6
‑
羟基
‑2‑
萘基)
‑
2,7
‑
二苯基芴的残留量为0.2重%以下使反应结束。
[0420]
反应结束后,向所得到的反应液中加入水和25重量%氢氧化钠水溶液在85℃搅拌5小时后,分离水层。将所得到的反应液冷却至20℃直接进行晶析,由此得到目标的bndp的淡黄色固体。将得到的bndp水洗后,减压加热干燥一晩,以收率78%、纯度98.8%得到淡黄色固体。另外,apha超过500,s为235ppm,br为170ppm,pd为70ppm,dpfn利用hplc进行测定,为0.2%。
[0421]
产业上的可利用性
[0422]
根据本发明的具有芴骨架的化合物及其制造方法,能够高效地制造具有高折射率、耐热性、低双折射等优异特性的树脂的原料(单体),因此能够优选用于树脂的原料(单体)、衍生物的反应成分等。
[0423]
因此,本发明的具有芴骨架的化合物或其衍生物、或者以新型的具有芴骨架的化合物为原料(单体)的树脂例如可以用于膜、透镜、棱镜、光盘、透明导电性基板、光卡、片材、光纤、光学膜、滤光片、硬涂膜等光学部件,特别是在透镜中是极其有用的。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。