1.本技术涉及生物医学技术领域,尤其涉及一种mir
‑
199a
‑
5p在制备用于预防或治疗1型糖尿病及其相关疾病药物中的应用。
背景技术:
2.1型糖尿病(t1dm)是一种自身免疫疾病,往往发病较急,常伴随酮症酸中毒等严重并发症。
3.t1dm的发病机制主要是体内反应性t细胞的异常增殖和活化,促炎细胞 th1、th17细胞大量扩增,而抑炎的调节性t细胞(treg)、th2细胞数量相对不足,造成th1/th2及th17/treg细胞比例失衡,形成胰岛周围炎,进而造成胰岛β细胞的破坏,胰岛素分泌减少,血糖升高。因此,有效抑制nod小鼠体内促炎的th1、th17细胞增殖,增加抑炎的treg细胞含量,是减轻胰岛炎,防止t1dm发病的核心问题,即纠正免疫失衡状态是预防及治疗t1dm 的关键。
4.nod小鼠是一种经典的自发1型糖尿病模型,该小鼠模型和人t1dm的发病机制及过程非常类似,可以很好的模拟t1dm的疾病过程,是目前公认的 t1dm疾病模型,被广泛用于相关研究。
5.mirna是一种高度保守的非编码小rna,是广泛存在于生物体中的基因表达调节剂。作为外分泌体的重要成分,mirna已成为多种疾病(包括免疫系统疾病)发病的关键调节因子。有证据表明mirna相比其他治疗药物具有靶向性强,微量高效的优势。
6.而现有技术中还未能够公开有关mirna可应用于预防或治疗1型糖尿病及其相关病症的相关报道。
技术实现要素:
7.为了解决上述问题,一方面本发明提供了mir
‑
199a
‑
5p在制备用于预防或治疗1型糖尿病及其相关疾病药物中的应用。
8.进一步的,所述用于预防或治疗1型糖尿病及其相关疾病药物包括降血糖制剂、胰岛功能损伤修复制剂和/或诱导t细胞分化制剂。
9.更进一步的,所述诱导t细胞分化制剂为抑制t细胞向th1细胞和th17细胞分化、促进其向th2细胞和treg细胞分化的制剂。
10.更进一步的,mir
‑
199a
‑
5p通过靶向下调缺氧诱导因子hif
‑
1α的表达诱导t细胞分化。
11.另一方面,将mir
‑
199a
‑
5p置于载体中应用。
12.进一步的,所述载体选自外泌体、病毒载体、高分子聚合物载体、脂质体中的一种或多种;优选的,所述载体为外泌体。
13.更进一步的,所述外泌体是来源于骨髓间充质干细胞的外泌体。
14.更进一步的,所述骨髓间充质干细胞外泌体采用以下方法提取获得:
15.将骨髓间充质干细胞培养至p5代后,收集细胞培养上清液,利用超速离心法和/或沉淀法提取上清液中的外泌体。
16.由于考虑到rna分子的不稳定性,在体内易被rna酶降解,实施例中采用bm
‑
msc外泌体作为mir199a
‑
5p的运载体进行实验,mir199a
‑
5p的运载体可选用和bm
‑
msc外泌体一样具有天然优势来源于其他组织细胞分泌的外泌体也可以选择具有同样优势的细胞外囊泡天然纳米颗粒、病毒载体、高分子聚合物载体、脂质体,在此不做限制。
17.另一方面,一种用于预防或治疗1型糖尿病及其相关疾病的药物制剂,其特征在于,所述药物制剂包括内部含有mir
‑
199a
‑
5p的骨髓间充质干细胞外泌体。
18.进一步的,所述药物制剂的剂型为注射制剂。
19.本发明具有如下有益效果:
20.本技术首次提出了mir
‑
199a
‑
5p,特别是含有mir
‑
199a
‑
5p的bm
‑
msc外泌体通过靶向下调hif
‑
1α表达,抑制t细胞向th1和th17细胞分化,促进其向th2和treg细胞分化,从而起到减轻胰岛炎,预防nod小鼠糖尿病发病的作用,进而能够使其具有制备1型糖尿病及其相关疾病药物中的新用途,以及在制备包括降血糖制剂、胰岛功能损伤修复制剂和诱导t细胞分化制剂的新用途;可有效降低1型糖尿病引起的血糖升高,在一定程度上改善胰岛炎病症,达到预防和治疗1型糖尿病的作用;采用mir
‑
199a
‑
5p作为有效成分,药物靶向性高,具有微量高效,安全可靠,毒性低的优势。
附图说明
21.此处所说明的附图用来提供对本技术的进一步理解,构成本技术的一部分,本技术的示意性实施例及其说明用于解释本技术,并不构成对本技术的不当限定。在附图中:
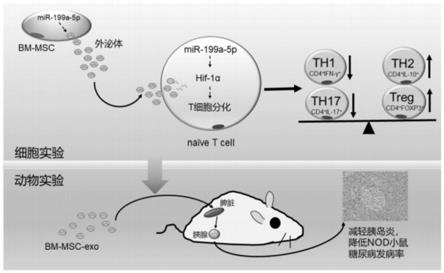
22.图1是含有mir
‑
199a
‑
5p的bm
‑
msc外泌体降低nod小鼠糖尿病发病率作用机制模式图;
23.图2是含有mir
‑
199a
‑
5p的bm
‑
msc外泌体降低nod小鼠糖尿病发病率实验流程图;
24.图3是bm
‑
msc细胞释放的外泌体囊泡(箭头)透射电镜图:图中标尺为100nm;
25.图4是外泌体粒径分析统计图;
26.图5是bm
‑
msc外泌体标志蛋白cd9和cd63 western blot鉴定结果图;
27.图6是nod小鼠生存曲线图;
28.图7是nod小鼠胰岛炎病症情况统计图;
29.图8是nod小鼠胰腺组织he染色图:图中标尺为50μm;
30.图9是nod小鼠脾脏淋巴细胞流式细胞术检测结果图;
31.图10是cck8法检测bm
‑
msc外泌体对cd3/cd28刺激的t细胞增殖的影响结果图,**p<0.01,***p<0.001;
32.图11是从c57bl/6小鼠脾脏分离提取t细胞结果图;
33.图12是bm
‑
msc外泌体中mirna定量结果图;
34.图13是t细胞与bm
‑
msc外泌体共孵育mirna定量结果图;
35.图14是t细胞中hif
‑
1α的表达量western blot鉴定结果图;
36.图15是t细胞中hif
‑
1α的表达量q
‑
pcr结果图,**p<0.01,#p <0.05。
具体实施方式
37.为了更清楚的阐释本技术的整体构思,下面结合说明书附图以实施例的方式进行详细说明。在下文的描述中,给出了大量具体的细节以便提供对本发明更为彻底的理解。然而,对于本领域技术人员来说显而易见的是,本发明可以无需一个或多个这些细节而得以实施。在其他的例子中,为了避免与本发明发生混淆,对于本领域公知的一些技术特征未进行描述。
38.实验仪器和试剂均为本领域已知技术,并且均可通过商业途径购得。其中, c57bl/6小鼠,nod/ltj小鼠由北京华阜康生物有限公司提供,超速离心机由 beckman coulter公司提供,t细胞磁珠分选试剂盒由美天旎公司提供。
39.实施例1小鼠bm
‑
msc的提取和鉴定
40.(1)股骨的分离:选取4周龄左右的c57bl/6小鼠,过量麻醉剂处死后用 75%乙醇浸泡5分钟,随后移入超净台,在无菌条件下分离小鼠的双侧股骨和胫骨。
41.(2)骨髓的获取:剪掉股骨两端,暴露骨髓腔,用5ml注射器吸取完全培养基(79%dmem/f12培养基 20%fbs 1%双抗)冲洗腔体,反复抽打2
‑
3次收获骨髓。
42.(3)种板:按照一条股骨所提骨髓液接种至六孔板中一个孔的原则进行种板,每孔约2.5ml。放至37℃、5%co2细胞培养箱中过夜培养,24小时后更换新的完全培养基。在随后的培养中使用10%fbs 1%双抗的dmem/f12 完全培养基进行培养。
43.(4)传代:细胞融合度达90%时可进行传代。用pbs清洗细胞表面,加入适当胰酶消化细胞,按照每孔细胞传至一个25cm2培养瓶的原则进行传代培养。选取第3
‑
4代细胞用于后续实验。
44.实施例2 bm
‑
msc外泌体的提取和鉴定
45.在bm
‑
msc培养p5代后,收集细胞培养上清(使用不含外泌体胎牛血清),超速离心法提取培养基中外泌体。
46.本实施例中具体操作为:取cm血培养上清液装入50ml离心管中,3000 g离心30min。取上清液装入高速离心管中,10000g离心30min,获得上清液。用0.22μm滤器过滤上清液。将滤过液装入38.5ml超速离心管中,110000 g离心70min。小心弃上清液后,得到bm
‑
msc外泌体,使用pbs、生理盐水或液体培养基重悬备用。
47.通过(1)电镜观察外泌体形态,观察结果如图3所示。(2)nta法进行外泌体粒径分析可知外泌体囊泡大小,分析结果如图4所示。(3)western blot 检测外泌体标志蛋白cd9、cd63和tsg101,检测结果如图5所示。
48.由图3
‑
图5所示结果可知,通过上述方法获得了高质量外泌体。
49.实施例3 bm
‑
msc外泌体对nod小鼠糖尿病发病的影响
50.将bm
‑
msc外泌体尾静脉注射入3周龄雌性nod小鼠(150μg/只)体内,且在小鼠第5周龄、7周龄和9周龄时各注射1次,剂量同前,分别进行以下实验:
51.(1)监测血糖:以连续2次随机血糖≥250mg/dl作为nod小鼠糖尿病发病标准,观察小鼠发病情况,小鼠发病统计结果如图6所示,由图可得在30 周时不加bm
‑
msc外泌体的对照组无血糖正常小鼠,而加入bm
‑
msc外泌体的实验组小鼠仍有80%保持血糖正常无发病现象,由此可得bm
‑
msc外泌体可明显减少nod小鼠发病。
52.(2)血清学指标:小鼠12周龄时行腹腔糖耐量实验(ipgtt)检测nod 小鼠胰岛功
能,小鼠胰岛炎统计结果如图7所示,由图可得,未加bm
‑
msc 外泌体的对照组小鼠胰岛炎发病数量和发病程度均比加入bm
‑
msc外泌体的实验组小鼠严重,由此可得bm
‑
msc外泌体可明显降低nod小鼠胰岛炎评分,缓解和治疗nod小鼠胰岛炎。
53.(3)胰岛组织学:小鼠12周龄时取胰腺组织,he染色观察胰腺组织形态学,免疫荧光检测cd3和胰岛素表达,评估各组小鼠胰岛中淋巴细胞浸润和胰岛素分泌情况,用以判断胰岛炎程度和胰岛功能,小鼠胰腺组织he染色结果如图8所示,由图可得nod小鼠胰腺组织he染色发现bm
‑
msc外泌体明显减轻胰岛炎性细胞浸润,bm
‑
msc外泌体可缓解和治疗nod小鼠胰岛炎。
54.实施例4 bm
‑
msc外泌体影响nod小鼠糖尿病发病机制探究
55.(1)cd63
‑
gfp
‑
msc稳转株构建:构建包装cd63
‑
gfp
‑
puro慢病毒,转染小鼠bm
‑
msc(moi=10),经嘌呤霉素(2μg/ml)抗性筛选之后,扩大培养,经western blot检测cd63和gfp表达,成功构建cd63
‑
gfp
‑
msc稳转株。
56.(2)超速离心法提取cd63
‑
gfp
‑
msc稳转株外泌体,将cd63
‑
gfp
‑
msc 稳转株外泌体(150μg/只)尾静脉注射入3周龄雌性nod小鼠体内,选取12 小时和24小时两个时间点取小鼠脾脏,冰冻切片后荧光显微镜观察脾脏中gfp 荧光分布,流式细胞术检测脾脏t细胞中gfp表达情况。
57.(3)将bm
‑
msc外泌体尾静脉注射入3周龄雌性nod小鼠(150μg/只)体内,且在小鼠第5周龄、7周龄和9周龄时各注射1次,剂量同前,小鼠12 周龄时获取小鼠脾脏细胞,流式细胞术检测其中th1(cd4 ifn
‑
γ )、th2 (cd4 il
‑
4 )、th17(cd4 il
‑
17 )和treg(cd4 cd25 foxp3 )细胞比例,检测结果如图9所示,由图可得bm
‑
msc外泌体明显降低nod小鼠脾脏中th1和th17细胞比例,增加th2和treg细胞比例。
58.实施例5t细胞对bm
‑
msc外泌体的摄取
59.(1)使用美天旎t细胞磁珠分选试剂盒从6周龄雄性c57bl/6小鼠脾脏单细胞悬液中分离提取t(cd3 cd4 cd25
‑
cd62l cd44low/
‑
)细胞。cd63
‑
gfp
‑
msc稳转株来源外泌体与t细胞共孵育12h和24h 后,4%多聚甲醛固定细胞,荧光显微镜观察t细胞中绿色荧光分布,检测t细胞摄取cd63
‑
gfp
‑
msc外泌体情况。cck8法检测bm
‑
msc外泌体对cd3/cd28刺激的t细胞增殖的影响,检测结果如图10所示,由图可得bm
‑
msc外泌体可剂量依赖性地抑制t细胞增殖。
60.(2)t细胞以0.25*10^6/孔的密度种板在96孔板中,分别在: th1(anti
‑
cd3:5μg/ml anti
‑
cd28:1μg/ml il
‑
2:20ng/ml il
‑
12:20ng/ml anti
‑
il
‑ꢀ
4:10μg/ml)、th2(anti
‑
cd3:5μg/ml anti
‑
cd28:1μg/ml il
‑
2:20ng/ml il
‑
4:100 ng/ml anti
‑
ifn
‑
γ:10μg/ml anti
‑
il
‑
12:10μg/ml)、th17(anti
‑
cd3:5μg/ml anti
‑ꢀ
cd28:1μg/ml il
‑
2:20ng/ml anti
‑
il
‑
4:10μg/ml anti
‑
ifn
‑
γ:10μg/ml)、treg(ant i
‑
cd3:5μg/ml anti
‑
cd28:1μg/ml il
‑
2:20ng/ml tgf
‑
β:5ng/ml)的细胞诱导分化培养体系下同外泌体共孵育5天,在该体系中分别加入0ug,5ug,10ug及 20ug的bm
‑
msc外泌体,使终体积为250ul/孔(96孔板),通过磁珠分选从c57bl/6小鼠脾脏分离提取t细胞(cd4 cd25
‑
),分离结果如图11所示,获得t细胞,并通过流式细胞术检测th1/th2/th17/treg细胞比例。
61.(3)western blot和q
‑
pcr检测t细胞分化过程中hif
‑
1α蛋白和mrna水平的
变化。
62.(4)设计合成包装hif
‑
1α过表达腺病毒,转染至t细胞中,qpcr 和western blot验证t细胞中过表达hif
‑
1α后,在th1/th2/th17/treg 诱导分化培养体系下,观察bm
‑
msc外泌体对t细胞向th1、th2、th17 和treg细胞分化的影响,可得bm
‑
msc外泌体降低nod小鼠脾脏中th1和 th17细胞比例,增加th2和treg细胞比例。
63.实施例6 bm
‑
msc外泌体中mirna的表达水平检测、mimics筛选验证
64.提取bm
‑
msc外泌体总rna,在illumina hiseq2500平台进行small rna 测序,qpcr法定量mirna表达丰度。
65.选择表达量前20位的mirna,结合hif
‑
1α基因进行生物信息学分析和文献分析,寻找bm
‑
msc外泌体中调控hif
‑
1α基因表达的mirna,与上述 mirnas(mir
‑
135a、mir
‑
138、mir
‑
1、mir
‑
210、mir
‑
199a
‑
5p、mir
‑
122、 mir
‑
433)对比分析,对入选的mirnas逐一使用mimics进行筛选验证,进一步明确并验证mir
‑
199a
‑
5p在bm
‑
msc外泌体的表达,结果如图12所示,由图可得mir
‑
199a
‑
5p、mir
‑
122、mir
‑
135a在bm
‑
msc外泌体中含量丰富,其中mir
‑
199a
‑
5p含量最高。
66.实施例7 mir
‑
199a
‑
5p对t细胞的作用
67.bm
‑
msc外泌体与t细胞共孵育24h后,qpcr检测细胞裂解液中的mir
‑
199a
‑
5p含量,如图13所示,t细胞与bm
‑
msc外泌体共孵育 24h后,细胞裂解液中的mir
‑
199a
‑
5p水平明显升高。
68.bm
‑
msc中加入20μm/l gw4869抑制细胞囊泡释放后,提取其外泌体,与t细胞共孵育24h后,qpcr检测t细胞裂解液中mirna
‑
199a
‑
5p 含量,此实验可明确t细胞中增加的mirna
‑
199a
‑
5p来源于bm
‑
msc 外泌体。
69.实施例8通过microrna靶基因预测软件targetscan获取mir
‑
199a
‑
5p与 hif
‑
1α基因3
′
utr潜在的互补结合位点
70.通过microrna靶基因预测软件targetscan(http://www.targetscan.org/)获取mir
‑
199a
‑
5p与hif
‑
1α基因3
′
utr潜在的互补结合位点;pcr扩增hif
‑
1α基因3
′
utr序列和3
′
utr的突变序列,将上述序列分别克隆至荧光素酶报告载体上(重组荧光素酶报告质粒),将上述两种质粒分别与mir
‑
199a
‑
5p mimics共同转染293
‑
t细胞,48h后收集细胞通过双荧光素酶报告系统检测细胞的荧光素酶活性,确定hif
‑
1α与mir
‑
199a
‑
5p的靶向调节关系。
71.实施例9 mir
‑
199
‑
5p mimics对t细胞分化的影响
72.设计并合成mir
‑
199
‑
5p mimics,在th1/th2/th17/treg细胞诱导分化培养体系下,流式细胞术检测mir
‑
199
‑
5p mimics对t细胞分化的影响。可得 mir
‑
199
‑
5p降低nod小鼠脾脏中th1和th17细胞比例,增加th2和treg细胞比例。
73.实施例10细胞水平研究mirna
‑
199a
‑
5p对t细胞hif
‑
1α表达和分化的影响
74.设计并合成mirna
‑
199a
‑
5p沉默寡核苷酸链(anti
‑
mirna
‑
199a
‑
5p oligonucleotide)和对照寡核苷酸(nc),fecttm cp转染试剂转染入bm
‑
msc 内,提取其外泌体,分别命名为bm
‑
msc
‑
exo
anti
‑
mir
‑
199a
‑
5p
和bm
‑
msc
‑
exo
nc
。 cck8实验检测bm
‑
msc
‑
exo
anti
‑
mir
‑
199a
‑
5p
对t细胞增殖的影响;在 th1/th2/th17/treg诱导分化培养体系下,流式细
胞术、western blot和qpcr 分别检测bm
‑
msc
‑
exoanti
‑
mir
‑
199a
‑
5p对t细胞分化、hif
‑
1α蛋白和 mrna表达的影响。
75.western blot检测bm
‑
msc
‑
exoanti
‑
mir
‑
199a
‑
5p对hif
‑
1α蛋白的影响,检测结果如图14所示,由图可得bm
‑
msc外泌体可显著下调t细胞hif
‑
1α的表达,且bm
‑
msc沉默mir
‑
199a
‑
5p后,其外泌体降低t细胞hif
‑
1α表达的作用被取消。
76.qpcr检测bm
‑
msc
‑
exoanti
‑
mir
‑
199a
‑
5p对mrna表达的影响,检测结果如图15所示,由图可得bm
‑
msc外泌体可显著下调t细胞hif
‑
1α的表达,且bm
‑
msc沉默mir
‑
199a
‑
5p后,其外泌体降低t细胞hif
‑
1α表达的作用被取消。
77.实施例11动物水平探究mirna
‑
199a
‑
5p对nod小鼠糖尿病发病的影响
78.bm
‑
msc
‑
exo
anti
‑
mir
‑
199a
‑
5p
和bm
‑
msc
‑
exo
nc
尾静脉注射入3周龄nod小鼠体内,剂量为150μg/只,且在小鼠第5周龄、7周龄、9周龄时再各注射1次,剂量同前,观察小鼠糖尿病发病情况,12周龄时观察小鼠胰岛炎情况、脾脏t 淋巴细胞亚群(th1、th2、th17、treg比例)和脾脏细胞hif
‑
1α表达。观察结果发现,注射bm
‑
msc
‑
exo
nc
可以起到减轻nod小鼠糖尿病发作的作用,而注射bm
‑
msc
‑
exo
anti
‑
mir
‑
199a
‑
5p
并不能减轻nod小鼠糖尿病发作情况,由此可见mirna
‑
199a
‑
5p在治疗和预防1型糖尿病中可以起到重要作用。
79.综上所述,本发明提出了mirna
‑
199a
‑
5p在制备1型糖尿病药物中的新用途,以及在制备胰岛炎药物中的新用途,mirna
‑
199a
‑
5p可有效抑制nod小鼠体内促炎的th1、th17细胞增殖,增加抑炎的treg细胞含量,纠正免疫失衡状态,降低血糖,达到治疗和预防1型糖尿病的目的。
80.以上所述仅为本技术的实施例而已,并不用于限制本技术。对于本领域技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原理之内所作的任何修改、等同替换、改进等,均应包含在本技术的权利要求范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。