1.本技术涉及核酸分子定量化分析技术领域,特别涉及一种使用微液滴进行核酸分子定量的方法及定量化系统
背景技术:
2.数字聚合酶链反应(dpcr)是对传统pcr方法的改进,可用于直接定量核酸序列的原始拷贝数,该思想发展最早来源于在微液滴内进行独立地扩增,进而检测扩增产物的思维,以微液滴为载体进行核酸分子链的扩增思想最早可见于英国医药研究委员会,之后转让给英国研究与创新基金会的系列化专利申请中,1999年12月16日提交的专利申请号us 09/464122美国申请,其主要保护了分割微液滴化思维的早期雏形方案;2002年10月03日提交的专利申请号us10/263984提出了在微液滴中增殖并筛选出特定的遗传核酸基因片段的方案等等;而真正将pcr用在基于微液滴的微流体芯片上的研究可见于pollack,m.g.等人在utas期刊上于2003年开展的基于通道的微流体芯片中,其采用的芯片见于kopp,m.等人,在science1998,280,1046
‑
1048期刊上所记载的技术,但是比较系统化明确化地提出利用荧光方案来实现定量化pcr的实现思维和实现系统,可见于2003年07月02日英国曼彻斯特大学递交的申请号为gb2003015438的英国申请,该方案基于电极驱动力在t型微通道中生成微液滴,适配kopp等人提出的pcr芯片,实现了(a)用于将水性反应混合物的微液滴引入载流体的装置(载流体然后可以流过芯片)使pcr反应在每个微液滴中发生;(b)用于检测每个微液滴中的pcr产物的系统。
3.在同时期,美国政府根据美国能源部和加利福尼亚大学之间关于劳伦斯
·
利弗莫尔国家实验室委托开发的数字类型pcr,在2003年03月14日递交了一篇申请号us10/389130的美国专利申请,其公开了利用微液滴结合荧光探测机理来实现绝对定量化的ddpcr基础原理,在块中扩增之前,将化学试剂和输入样品“分成”大量微液滴或其他形式的流体块结构,分块中至少部分包含了dna的溶液,也就是从技术层面公开了两种技术路径第一种为:利用微液滴实现分区;另一种利用微分区来实现流体的隔离。该方案为比较早的连续型微液滴方案,其利用循环泵在整个pcr扩增、解旋等等模块内进行循环,循环特定次数,检测产物以判定被检测样品是否呈阳性,后续比奥雷德公司,在该专利技术基础上布局了一系列专利,从不同角度进行专利保护,上述两种方案均为连续类型的液滴pcr方案,系统设计复杂,尤其是涉及微循环泵与微通道组件,这些部件的高要求也使得该技术成本和实现的复杂度非常高,另一方案由拜奥
‑
多特公司于2003年06月12日递交的申请号us60/477807美国申请所公开,其公开了一种间歇操作的芯片上非连续型dpcr工作机理,但是这种方案为注射类型的分布方案,其对于注射器要求比较高(如此才能获得更为均一且包含更精确的核酸分子链的微液滴),为了获得更精确的检测效果,对于整个系统的精度要求也特别高。
4.之后,几种芯片类型的实验室(loc)、微全分析(μtas)和生物微机电系统(biomems)已经被研究用于在表面上移动、合并/混合、分割和加热液滴,使得微液滴的行为变成可操控状态,例如电介质上电润湿(ewod)
5.[pollack,m.g.等,appl.phys.lett.(2000),77,1725
‑
1726]的方法、表面声波(saw)[wixforth,a.等,mstnews(2002),5,42
‑
43]的方案、双向电泳[cascoyne,p.r.c.等,lab
‑
on
‑
a
‑
chip(2004),4,299
‑
309]方法、以及局部不对称环境[daniel,s.等,langmuir(2005),21,4240
‑
4228]方法等等也尝试在芯片上可操纵地实现绝对定量化pcr检测等等微尺度检测。但是,这些方法不能很好地适合具有一系列步骤的方法,例如从粗的或复杂的混合物分离、纯化和离析起始材料和/或反应产物,其对于原始样液处理有很高的要求。这样的步骤可能,需要漂洗或清洗,然而这些目前只能在多孔板中使用例如自动化的标准实验室机器人或者微小控制器来进行。
[0006]
为了克服这些缺点,后续发展了具有微毛细管和微通道的elisa平台(song,jm.&vo
‑
dinh,t,analytica chimica acta(2004),507,115
‑
121;herrmann,m,等,lab
‑
on
‑
a
‑
chip(2006)6,555
‑
560)。但是,这样的平台更繁琐和昂贵,并且使用的灵活性和方便性较低,不利于系统在商业上的实现和大规模量产与之后的快速准确检测结果获得,之后伯乐公司在美国劳伦斯实验室研究的基础上对于微液滴pcr系统提出了新的实现方案,其在中国递交的2010年11月25日专利申请号为cn201080062146.9方案提出了一种非连续类型的微液滴类型pcr实现方案,其过程为利用液滴生成芯片生成非连续类型的液滴(液滴生成芯片结构复杂而且设计为一种两种流体相互作用而实现乳化的一体结构),在小液滴内进行pcr扩增循环,最后对于扩增完成后的微液滴进行统计输出原始拷贝数,在这一系统下国内很多厂商或者研究机构模仿了这一非连续类型的微液滴pcr技术,递交了大量基于此原理的非连续类型微液滴绝对定量化pcr专利申请,然而这一技术有其天然缺陷,由于其实现步骤为将液滴平铺之后在小液滴内进行pcr扩增(本身一体化结构的工艺复杂风险更大),而细小液滴体积又非常小几十至数百μm的量级,此时温度对于微液滴影响将是巨大的,这就要求设计出更合理的密封方案来保证在加热过程中微液滴不被蒸发掉,如此对于芯片的设计提出了非常高的要求,这也决定着系统输出的定量化结果是否准确可信可复现性是否更强。
[0007]
目前,市面上的微液滴类型数字pcr技术主要有三种,1)是通过在特定仪器中使用流动的油相切断水相的pcr溶液形成微液滴,然后在另外的两台仪器中完成pcr和检测;2)是通过将pcr溶液分布到挖空的硅片上,然后在特定仪器中进行pcr以及另外一台仪器中进行检测;3)是在一种仪器上将液体通过狭窄的沟道注入腔体形成微液滴,并完成pcr,然后在另一台仪器中完成检测。然而,当前三种方法的微液滴形成速度或者通量各有限制,此外,上述三种技术无一例外的依赖多台大型仪器,这些不但增加了仪器的购置的成本,限制了数字pcr的广泛使用;而且增加了实验操作的复杂度;为了解决上述已经提出的技术方案所存在技术缺陷和现有已经存在的微液滴类型pcr的复杂性和高成本以及结果可复现行较差等技术问题,亟待开发一种更为可靠的微液滴类型定量化方法和定量化系统来解决上述现有技术所存在的问题。
技术实现要素:
[0008]
本发明的目的在于,针对上述现有技术中的不足,本发明提出了一种使用微液滴进行核酸分子定量的方法及使用其的定量化系统,以解决现有的微液滴类型定量化方法和定量化系统具有的高复杂度,集成化较低功能单一可复现性较低等等一系列的问题。
[0009]
为实现上述目的,本发明的第一个发明目的在于,提出了一种使用微液滴进行核酸分子定量的方法,其包括以下步骤:
[0010]
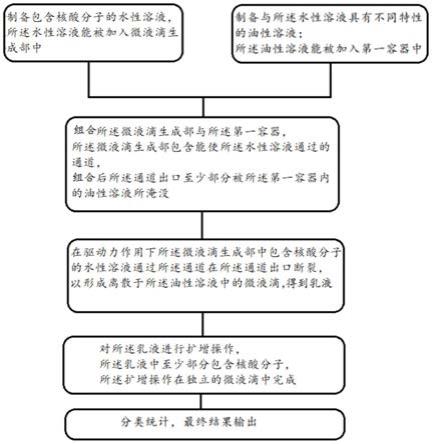
1)制备包含核酸分子的水性溶液,所述水性溶液能被加入微液滴生成部中;
[0011]
2)制备与所述水性溶液具有不同特性的油性溶液,所述油性溶液能被加入与所述微液滴生成部不同的第一容器中;
[0012]
3)组合所述微液滴生成部与所述第一容器,所述微液滴生成部包含能使所述水性溶液通过的通道,组合后所述通道的出口至少部分被所述第一容器内的油性溶液所淹没;
[0013]
4)在驱动力作用下,所述微液滴生成部中包含核酸分子的水性溶液通过所述通道在所述通道出口处断裂,以形成离散于所述油性溶液中的微液滴,并得到乳液;
[0014]
5)对所述乳液进行扩增操作,所述乳液中至少部分包含核酸分子,所述扩增操作在独立的微液滴中完成;
[0015]
6)包含靶核酸分子的微液滴经过扩增过程之后能产生荧光,通过统计能产生荧光的微液滴数量,最终获得原所述水性溶液中靶核酸分子的浓度。优选地,在步骤5)之后还包含微液滴平铺步骤7)将经过扩增之后的乳液转移至平面化的平铺芯片中,在所述平铺芯片中至少部分微液滴处于单层平铺状态,即微液滴之间不包含堆叠或者重叠的部分,对于所述平铺芯片中的微液滴执行步骤6)并获得所述靶核酸分子的浓度结果。
[0016]
优选地,所述水性溶液中包含核酸样本、扩增试剂和靶核酸识别因子,所述识别因子具有荧光特性。
[0017]
优选地,所述步骤6)中利用ccd或者cmos检测器识别所述乳液中微液滴是否具有荧光特性来判定所述微液滴是否含有所述靶核酸分子。
[0018]
优选地,所述微液滴生成部具有阻力特性,其保证所述微液滴生成部内包含的水性溶液在未施加驱动力的状态下不会通过所述通道流出。
[0019]
优选地,所述油性溶液的密度与所述水性溶液密度存在第一相差量,在所述第一相差量的作用下在所述通道出口生成的微液滴能够快速脱离。
[0020]
优选地,所述油性溶液的密度大于所述水性溶液密度,使得所述第一相差量为正值。
[0021]
优选地,组合后所述通道出口全部被所述第一容器内的油性溶液所淹没,并且所述通道出口的中心线没入所述油性溶液的预设深度中。
[0022]
优选地,所述通道接近所述通道出口的至少部分被设置为疏水特性。
[0023]
优选地,所述驱动力的来源于以下至少一种方式:
[0024]
通过至少部分可变形部变形产生驱动力;
[0025]
通过驱动丝杆产生驱动力;
[0026]
通过离心泵或/和涡旋泵等设备产生驱动力。
[0027]
优选地,所述步骤6)通过亮度差异对扩增后的微液滴进行分类统计。
[0028]
优选地,所述第一容器为扩增步骤中使用的核酸样本容器。
[0029]
优选地,所述微液滴生成部中包含能使所述水性溶液通过的多条通道,可记为m条通道,其中,m为大于等于2的整数;组合之后所述多条(m条)通道的至少部分没入所述第一容器中的油性溶液液面以下。
[0030]
优选地,所述多条(m条)通道的出口截面中心线基本处于同一水平面内。
[0031]
优选地,在完成所述水性溶液并在所述第一容器中生成乳液后,所述微液滴生成部能与所述第一容器分离。
[0032]
优选地,分离所述微液滴生成部和所述第一容器后,所述第一容器能被使用于扩增步骤中,并且在所述扩增步骤中其可自动实现密封。
[0033]
本发明的第二个发明目的在于,本发明还提出了一种实现使用微液滴进行核酸分子定量的方法的定量化系统,它包括:
[0034]
微液滴生成部,容纳包含核酸分子的水性溶液;
[0035]
第一容器,容纳与所述水性溶液具有不同特性的油性溶液;组合所述微液滴生成部与所述第一容器,所述微液滴生成部包含能使所述水性溶液通过的通道,组合后所述通道出口至少部分被所述第一容器内的油性溶液所淹没;
[0036]
驱动部,产生驱动力,并在驱动力作用下所述微液滴生成部中包含核酸分子的水性溶液通过所述通道在所述通道出口处断裂而形成离散于所述油性溶液中的微液滴,以得到乳液;
[0037]
扩增模块,对所述乳液进行扩增操作,所述乳液中至少部分包含核酸分子,所述扩增操作在独立的微液滴中完成;
[0038]
结果处理模块,经过扩增过程之后包含靶核酸分子的微液滴经过扩增过程之后能产生荧光,通过统计能产生荧光的微液滴数量,所述结果处理模块能最终获得原所述水性溶液中靶核酸分子的浓度。
[0039]
优选地,定量化系统还包含微液滴平铺模块,能容纳经过扩增之后的乳液,且在所述微液滴平铺模块中至少部分微液滴处于单层平铺状态,即不包含堆叠或者重叠的部分,所述结果处理模块依据所述微液滴平铺模块中的微液滴荧光信号获得所述靶核酸分子的浓度结果。
[0040]
优选地,所述驱动部的驱动力来源于以下至少一种方式:
[0041]
通过至少部分可变形部变形产生驱动力;
[0042]
通过驱动丝杆产生驱动力;
[0043]
通过离心泵或/和涡旋泵等设备产生驱动力。
[0044]
综上所述,由于采用了上述技术方案,本发明的有益效果是:本发明提供的一种使用微液滴进行核酸分子定量的方法,核酸分子的水溶液可以被独立地操作,油性溶液也不需要经过微小驱动元件驱动以分散水性微液滴,油性溶液只需被简单地充注进入第一容器内即可,只需要设计容纳水性溶液的微液滴生成部结构,之后组合两者,驱动力驱动水性溶液即可完成包含核酸片段的微液滴生成,同时对于第一容器内的乳液直接进行pcr扩增可以实现整个扩增过程依旧可在宏观尺度下进行的,因此为了保证蒸发量小而采取的措施很容易设计,第一容器内可以使用目前使用更多采用的热盖设计来减少乳液内的水性微液滴的蒸发,扩增完成之后再利用连续类型的微通道内或者通过非连续类型的平铺芯片结构实现利用荧光方案进行统计,最终获得原样品中目标核酸分子链的绝对定量化结果。
附图说明
[0045]
为了更清楚地说明本技术实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本技术的某些实施例,因此不应被看作是对
范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
[0046]
图1为本发明提供的一种基于微液滴绝对定量化实现方法示意图;
[0047]
图2为本发明提供的另一种基于微液滴绝对定量化实现方法示意图;
[0048]
图3a为本发明提供的一种液微滴生成部与第一容器组合生成微液滴工作原理示意图;
[0049]
图3b为本发明提供的一种微液滴生成部实现结构示意图;
[0050]
图4为本发明提供的一种实现定量化方法的定量化系统示意图;
[0051]
图5为本发明提供的一种移动模块与行架结构示意图;
[0052]
图6为本发明提供的一种移动模块内部包含移液器与转移机构结构示意图;
[0053]
图7为本发明提供的一种pcr扩增模块结构示意图;
[0054]
图8a为本发明提供的一种pcr扩增单元结构示意图;
[0055]
图8b为本发明提供的一种pcr扩增单元状态示意图;
[0056]
图9a为本发明提供的一种检测模块结构示意图;
[0057]
图9b为本发明提供的一种检测模块结构不同视角示意图;
[0058]
图10为本发明提供的一种平铺模块结构示意图。
具体实施方式
[0059]
为使本技术实施例的目的、技术方案和优点更加清楚,下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本技术一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本技术实施例的组件可以以各种不同的配置来布置和设计。
[0060]
因此,以下对在附图中提供的本技术的实施例的详细描述并非旨在限制要求保护的本技术的范围,而是仅仅表示本技术的选定实施例。基于本技术中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
[0061]
应注意到:相似的标号和字母在下面的附图中表示类似项,因此,一旦某一项在一个附图中被定义,则在随后的附图中不需要对其进行进一步定义和解释。
[0062]
目前的微液滴类型的pcr系统按照操作类型主要分为连续类型微液滴定量化pcr,主要原理为驱动油性溶液和包含核酸序列的水性溶液在集成的微流道内利用油性溶液对于水性溶液的剪切作用实现水性溶液的微液滴化,再利用微循环泵配合微阀门实现液滴在相对封闭的系统中循环于不同的温度区,通过特定次数的循环之后,配合微阀门的打开在后端设置微通道检测部,从而实现对于扩增循环完成之后的微液滴荧光特性进行检测,现有技术公开最多的为二元判定的阴阳性结果对于液滴进行统计,之后结合泊松分布算法计算出绝对定量化的原始拷贝结果;另一类型的微液滴定量化pcr为非连续类型,其基本原理为制备包含核酸序列的水性溶液与油性溶液,将两者驱动通过微液滴生成芯片,通常系统做成一体化,生成微液滴之后,在驱动力的作用下被转移至能够平铺液滴的芯片中,在此条件下通过对于平铺芯片进行热循环,进而实现原水性溶液内的核酸分子链循环扩增,经过预定次数的循环扩增之后对于平铺芯片内的液滴进行分类统计以获得原始溶液内的初始
拷贝数,然而现有技术中大多数芯片为一体化集成化设计,在微尺度条件下还需要考虑加热过程中的密封,如此整体设计实现将非常复杂,加工难度也很高,如此设计自动型的液滴定量化设备将存在极大的困难。
[0063]
图1为本发明提供的一种使用微液滴进行核酸分子定量的方法,包括制备包含核酸分子的水性溶液,其来源可以为待实验的标准核酸序列溶液,也可以为对于各种采集方案采集获得的样品提取到的核酸分子,例如采用咽拭子、全血采样、鼻拭子、肛拭子等等获得待检测样品,获得待检测样品之后经过例如磁珠提取方案对于样品中的核酸序列分离提取获得,同时为了实现荧光类型的探测,同时为了实现荧光类型的探测,所述水性溶液中还包含荧光染料或荧光探针。
[0064]
在本发明中,荧光染料包括荧光素类染料其包含异硫氰酸荧光素(fitc)、羟基荧光素(fam)等及其类似物;罗明类染料包含红色罗丹明(rbitc)、四甲基罗丹明(tamra)等及其类似物;alexa系列染料包含alexaflour350、405、430等等及其类似物;cy系列菁染料包含cy2、cy3等等及其类似物;蛋白类染料包含藻红蛋白(pe)、藻蓝蛋白(pc)等等及其类似物。进一步,荧光探针包括化学荧光探针包括有机小分子荧光探针,纳米荧光探针,基因荧光探针等等。荧光探针种类也比较多此处不再详细列举,荧光素与荧光探针的工作原理类似响应于一种波长的激发光之后会被激发从而发射出与激发光波长不相同的发射光,从而实现荧光探测的效果。
[0065]
进一步地,用于进行pcr反应的溶液和试剂还可包括缓冲液,所述缓冲液可包含大于约或小于约1、5、10、15、20、30、50、100或200mmol/l tris。在一些情况下,可以添加氯化钾其浓度可以是大约、大于约或小于约10、20、30、40、50、60、80、100、200mmol/l,由此缓冲溶液可由包含约15mmol/ltris和50mmol/l kcl组成的混合物。还包含核苷酸可为脱氧核苷酸三磷酸分子,包括datp、dctp、dgtp、dttp,各自的浓度是大约、大于约或小于约50、100、200、300、400、500、600或700μmol/l。在一些情况下,非标准核苷酸如dutp加入到扩增反应中达到大约、大于约或小于约50、100、200、300、400、500、600或700、800、900或1000μmol/l的浓度。在一些情况下,将氯化镁(mgcl2)以大约、大于约或小于约1.0、2.0、3.0、4.0或5.0mmol/l的浓度加入到扩增反应中形成激活剂,例如,激活剂mgcl2的浓度可为约3.2mmol/l。还包含引物,其可为催化延伸dna的各种类型的聚合酶(也可以称为不同类型的引物),包括但不限于大肠杆菌dna聚合酶、大肠杆菌dna聚合酶1的klenow片段、t7dna聚合酶、t4dna聚合酶、taq聚合酶、pfu dna聚合酶、pfx dna聚合酶、tth dna聚合酶、vent dna聚合酶、噬菌体29、redtaqtm、基因组dna聚合酶或测序酶。可使用热稳定的dna聚合酶,dna聚合酶可具有3’到5’外切核酸酶活性,dna聚合酶还可具有5’到3’外切核酸酶活性,当然dna聚合酶亦可同时具有3’到5’外切核酸酶活性和5’到3’外切核酸酶活性,所述水性溶液还可包含其他一些添加剂此处并不限定。油还可以具有高含量的氢、氟、硅、氧、或其任何组合等,油水混合物形成的任何乳液可以是油包水的(w/o)乳液(即在连续油相中的水滴),该油可以是或包括至少一种硅油、矿物油、氟烷油、植物油或其一种组合等。
[0066]
所述水性溶液能够被转移至微液滴生成部中,所述油性溶液能够被转移至第一容器内;两者可以通过相同的移液器进行操作,但是使用不同的移液头耗材,如此实现了系统与方法实现简便与高效的效果,也保障了制备两种不同性质的溶液在不同的容器中实现,两者互不干扰,完成制备之后,所述微液滴生成部与所述芯片组合,所述微液滴生成部包含
能使所述水性溶液通过的通道,组合后所述通道出口至少部分被所述第一容器内的油性溶液所淹没,此过程中所述第一容器内油性溶液已经不需要被操作,同时只需要对所述微液滴生成部的水性溶液施加驱动力即可生成微液滴,生成的微液滴体积可以为几十微升至数百微升此处并不限定,此时通过微液滴生成部的优化设计可以被设计为与移液器兼容的结构,如此对于微液滴类型pcr拆分实现了利用相同的驱动器同时实现移液与微液滴生成部驱动力产生部合一的功能,更进一步地简化了整个方法和系统,在驱动力作用下所述微液滴生成部中包含核酸分子的水性溶液通过所述通道在所述通道出口断裂而形成离散于所述油性溶液中的水性微液滴,形成乳液状态,如前所述本系统的驱动力可来源于移液器,其直接作用于微液滴生成部的水性溶液液面,或者作用于微液滴生成部的水性溶液液面上方的空气层进而间接地驱动水性溶液,通过所述通道所述水性溶液离散地分配进入所述油性溶液中,形成乳液状态,当然所述乳液状态中还可以包含表面活性剂,为了保证分散效果更好,所述液滴生成部的所有通道全部浸没于所述第一容器中的油性溶液液面以下,例如浸没液面以下的预设深度保证液滴生成的高效性,直接将微液滴生成在第一容器内也保证了液滴与空气的接触面小,在热盖保护的前提下就能很好地保证蒸发量较小,而不必担心分散之后微通道内表面张力与加热共同作用而导致的液滴蒸发量更大的现象,对所述乳液执行pcr扩增,所述乳液中至少部分包含核酸序列,所述核酸序列的扩增在独立的微液滴中完成,生成的乳液在第一容器中,直接对于第一容器进行pcr反应的热循环,乳液中的液滴至少部分包含1个、2个、3个等等的核酸分子原始拷贝数,在第一容器内,核酸分子在独立的液滴中进行pcr扩增,使得核酸片段呈现级数级增长,例如可以进行10次、15次、20次、25次、30次、35次等等的温度循环,完成温度循环中荧光染料或荧光探针与目标核酸片段的结合,之后在检测模块中可以容易地识别出单独微液滴是否包含目标核酸片段的信息,统计经过pcr扩增过程之后的微液滴中包含靶核酸序列的微液滴,最终获得原所述水性溶液中靶核酸序列的定量化结果,此处可以采用二元判定方案,只识别出微液滴是否包含目标核酸片段的信息,包含的微液滴标记为1,而不包含目标核酸片段信息的微液滴标记为0,当然也可以设置不同的分类依据,例如三种档位,不包含目标核酸片段的阴性微液滴,弱阳性微液滴,荧光特性在一定的强度范围内的微液滴,强阳性微液滴,荧光特性值高于某一阈值的微液滴,当然,也可以采用更多的档位对于微液滴表现出的荧光亮度差异进行分类,此处不限定。
[0067]
通过二元判定或者三档位分类等等的分类方案实现对于微液滴进行统计,当然统计方法可以采用连续类型的类似微通道连续流类型的检测方案,也就是在完成pcr扩增之后,第一容器内的乳液被驱动通过带有检测部的微通道,激发光探测器对于通过微通道内的乳液微液滴进行分类统计,或者可以利用非连续类型的平铺方案,之后利用泊松分布关系对于原始样品液的目标核酸序列的原始拷贝数给出较为准确的计算结果,从而实现绝对定量化的目标(也就是最终获得原所述水性溶液中靶核酸分子的浓度)。
[0068]
图2为本发明提供的另一种新类型的微液滴定量化方法,与图1相似步骤此处不再详细赘述,需要注意的是图2提供的定量化方法在乳液pcr扩增完成之后被执行平铺步骤,将经过扩增之后的乳液转移至平面化的平铺芯片中,使得至少部分微液滴处于单层平铺状态,即至少部分微液滴之间不包含堆叠或者重叠的部分,此方法中利用非连续类型微液滴pcr原理,将扩增之后的乳液转移至平铺芯片中,为了保证平铺芯片内转移之后的微液滴至
少部分不包含堆叠或者重叠的部分,平铺芯片内的通道截面高度具有预设的尺寸,例如适应于微液滴直径的尺寸特征,之后将包含乳液的平铺芯片转移至探测模块,实现利用激发光对于平铺芯片内所有微液滴的荧光分类识别,再利用泊松分布方案最终输出样品原始拷贝的目标核酸序列的绝对定量化结果,为了保证整个系统的可靠性和系统输出结果的可重复性更强,所述微液滴生成部内的水性溶液体积最优地为5μl~60μl,为了实现荧光探测的结果,探测系统的接收部可以为ccd或者cmos类型的二极管阵列型接收器,从而获得更高质量的探测结果,相比于连续类型的方案,该方案对于图像获取模块的要求更低,不需要具有特定化的图像获取速度,也不需要更大的内部存储空间,整个探测模块获得的结果处理时间更充足处理方法也更为简便。
[0069]
图3a为本发明提供的一种微液滴生成部与所述第一容器组合生成微液滴的示意图,其中第一容器为301,内部包含油性溶液,微液滴生成部为302,为了保证该方法能被使用于高自动化集成化的系统中,微液滴生成部302的顶部与移液器耗材的顶部设置为相同的结构,从而使得微液滴生成部的驱动力可以来源于移液器,所述微液滴生成部的内部包含水性溶液,所述微液滴生成部具有阻力特性,其保证所述微液滴生成部内包含的水性溶液在未施加驱动力的状态下不会通过所述通道303流出,例如可以在所述通道接近所述出口的至少部分被设置为疏水特性,从而保证微液滴生成部内的水性溶液不会在毛细现象的作用下泄露,在具体的操作中,当施加的所述驱动力小于阈值驱动力时所述芯片内的流体不能通过所述通道流出,进一步可以在所述微液滴生成部与所述第一容器组合前,所述驱动部施加不高于所述阈值驱动力的第一驱动压力,此时微液滴生成部中的水性溶液能够被第一驱动力驱动保证所述水性溶液还被包含在所述微液滴生成部通道303的出口范围内,此时可以保证在后续微液滴生成中生成平稳快速,也能保证微液滴生成部的空气残留较少以确保整个过程中的污染风险较小。为了保证生成的微液滴尺寸满足要求,本发明所使用的微液滴生成部中的通道尺寸需要进行合理化设计,微液滴直径与通道303的宽高比具有不同参数时进行测定,例如通道303的尺寸(宽
×
高)分别为26.6um
×
10.5um、47.4um
×
10.5um、56.0um
×
10.5um、69.4um
×
10.5um、42.8um
×
14.3um、62.4um
×
14.3um、77.7um
×
14.3um、100.7um
×
14.3um,通过上述8组尺寸的通道303可以制备出平均粒径在35um~70um范围内的微液滴。通过进一步调整通道303的尺寸,微液滴生成部302可以形成直径在5um至500um范围的单分散微液滴,体积范围为约65fl至65nl,满足不同应用场合的微液滴制备需求,当然此处也为示意性说明并不限定于此,当所述微液滴生成部302与所述第一容器301组合后,为了保证整个系统的可靠性组合后所述通道303出口至少部分被所述第一容器301内的油性溶液所淹没,并且所述通道303被所述油性溶液所淹没的出口中心线没入所述油性溶液的预设深度中。进一步,所有所述通道303均被所述第一容器301内的油性溶液所淹没,所述通道303的出口均被淹没于所述油性溶液液面以下的预设位置处,在实际的使用中预设位置可以为距离液面以下固定的距离范围内,例如可以是液面以下1mm
‑
4mm位置处,当然也可以为其他有效的淹没预设距离,此处并不限定具体的实现方案,当所述通道303出口被淹没于所述油性溶液液面以下预设位置处时,通过如下至少之一的方式,至少部分可变形部变形产生驱动力,通过驱动丝杆产生驱动力,通过离心泵涡旋泵等设备产生驱动力等等,产生直接或间接作用于所述水性溶液的驱动力,当然此处驱动元件也可以为压电陶瓷制备的微驱动元件,也可以为小电机带动的精密丝杆也就是与移液器相同的器件,所述微
液滴生成部302还具有临界值特性,所述驱动力小于所述微液滴生成部302临界特性对应的临界驱动力值,当驱动力更高时甚至超过所述临界驱动力值时液滴生成部302会产生不稳定的微液滴,液滴尺寸也会出现急剧的增大,甚至导致整个微液滴生成部302生成微液滴失败不可使用的现象,因此在所述微液滴生成部302与所述第一容器301组合的状态中,所述驱动部施加大于所述阈值驱动力但不高于所述临界驱动力的第二驱动力,使得微液滴生成部中的第一流体以微液滴形式离散地分布于所述第二流体中如图中310所示的乳液状态,此处的第二驱动力可以为固定值也可以为具有波动变化特性的驱动力,甚至在驱动所述水性溶液过程中,随着剩余水性溶液的量减少,所述第二驱动力也可以逐渐减小,所述油性溶液的密度与所述水性溶液密度有第一相差量,在所述第一相差量的作用下在所述通道出口生成的微液滴能够快速脱离,也就是两相密度差异所产生的浮力可以成为贡献水性溶液在所述通道303出口被切断成为微液滴的外力,当然切断微液滴的外力不限于浮力(所述微液滴生成部302与所述第一容器之间可以存在相对运动,例如旋转运动或者具有相对的移动,此时外力还包含粘度贡献的粘滞力等等)。
[0070]
图3a中所述油性溶液的密度大于所述水性溶液密度,所述使得所述第一相差量为正值,当然也可以采用所述油性溶液的密度小于所述水性溶液密度,使得所述第一相差量为负值,如此实现所述水性溶液通过所述通道303被分散成的微液滴能被分散于所述油性溶液的特定部位中(图中的上部位置所示的乳液310)方便后续的转移操作。
[0071]
图3b示意了微液滴生成部通道303实现的结构,所述微液滴生成部包含了中空的中间部,中空部可以容纳所述水性溶液,通道设置在中空部的底部,为了保证通道具有特定长度,例如需要保证其长度特征l与其当量直径特征满足l>3d,以使生成的微液滴具有更可靠稳定的直径,在之一实施方案中所述液滴生成部302的底部为平面结构320,所述通道303呈辐射状分布于所述底部的平面结构320上(当然通道303也可以以平行的结构布置在平面结构320上,此处并不限定),为了保证微液滴生成部的高效率特性所述通道303的数量大于2个,也就是所述微液滴生成部302中包含能使所述水性溶液通过的m条通道303(其中m为大于等于2的整数);组合之后所述m条通道303的至少部分没入所述第一容器301中的油性溶液液面以下,最优地所述通道303为等间距布置(包含等夹角分布),此处所述m条通道303的出口截面中心线基本处于同一水平面内,也就是上述描述的在相同平面内辐射状分布,当然微液滴生成部的底部也可以为非平面结构类型,例如微液滴生成部302底部设置为具有凸起结构以保证水性溶液最少残留的效果,通道303也可以设置为与所述中空部中心线夹角非90
°
的结构,可以设置为具有钝角夹角结构以保证通道303的出口低于其入口,从而实现微液滴生成部302内水性溶液的快速彻底转化为微液滴效果。
[0072]
利用图3a微液滴生成部302与所述第一容器301组合之后在驱动力作用下完成水性溶液的微液滴化处理,完成该乳化过程之后,所述微液滴生成部能与所述第一容器301分离,也就是在微液滴生成过程中第一容器301是否处于密封状态并不做特殊要求,这也保证了系统设计的简便性,分离所述微液滴生成部302和所述第一容器301后,所述第一容器301能被使用于pcr扩增步骤中,并且在所述扩增步骤中其可自动实现密封,在该系统设计中第一容器本身就是后续pcr反应容器,保证了整个方法和系统设计中耗材的简便化设计,同时在扩增步骤中可以使用与所述第一容器相配合的盖子,依靠设备自动地将两者扣合实现密封之后将所述第一容器转移至后续的pcr反应模块。
[0073]
图4为配合之前所述定量化方法实现定量化操作的系统,其包含移液器与转移机构组成的移动模块43,移液器可以包含1个、2个、3个等等的移液单元用于对于不同的样品进行处理,移液单元可以单独地被操作以实现对于不同液体的转移,转移机构用于转移系统中的各耗材部的耗材进行转移,其包含一种能够收缩的夹持头结构,整个移动模块43被设置于一个可移动的支架44上,从而实现移动模块43被前后或者左右地移动至预设位置(当然所述移动模块43也可以被设置为可以上下移动的结构)。本系统对于移液器与转移机构进行了归一化设计,两者组合成一个整体模块从而实现了系统高集成化的设计,并且整体的自动化程度也更高。
[0074]
耗材模块45包含了微液滴类型的绝对定量化方法所需要的不同耗材单元,其中451为平铺芯片单元,其能够放置完成扩增后转移进入的乳液,并且平铺芯片单元被放置在平铺芯片耗材区中,从而实现对于方法和系统所需的微液滴平铺芯片的供应,452为移液器耗材移液头单元,其包含了油性溶液移液头和水性溶液移液头两种类型移液头单元,两种类型的移液头可被阵列化地插设在不同的移液头存储区中,两种移液头之间不可混合插设,两种移液头的精度和容量可以不相同依据实际需求进行设计,453为微液滴生成部单元,大量的微液滴生成部被阵列型地布局在液滴生成部储存区域内,454为第一容器单元,所述第一容器以阵列化方式设置也可以堆叠设置,455为与所述第一容器相配合的密封盖存储单元,在利用pcr进行扩增过程中所述密封盖与所述第一容器相组合,从而实现对于第一容器内的乳液密封并且容易转移,456为油性溶液储存单元,其包含了形成乳液的油性溶液,为了保证供应量和设计的简便性其可以采用类似于全血样品耗材类似的试样管依据本发明的方法各个耗材模块是被分割的。如此,各个耗材单元之间即使存在加工缺陷也不会影响整个方法无法实现,相比于集成化的微小系统,该方法的可靠性更高,系统可实现性和整个系统的全自动化设计可能性也更高。
[0075]
46为样品冷藏模块,其包含核酸序列的水性溶液样品存储单元,当然所述水性溶液内还包含之前所描述的荧光染料或荧光探针等等,冷藏设置也保证了核酸序列等的可靠性,当然所述水性溶液可以是配合天隆科技的磁珠提取仪器genrotex、np968
‑
s、np968
‑
c等等,其从全血样品、鼻拭子、咽拭子、肛拭子等等获得的样品中提取完成获得的水性核酸样品,当然也可以是标准的核酸样本此处不限定其来源。
[0076]
47为液滴平铺模块,在该模块中第一容器与所述的平铺芯片密封性组合,当然不限定为严格的密封,通过加入第三类型液体实现对于完成扩增之后的第一容器内的乳液中的微液滴进行驱动转移,使得完成扩增之后的微液滴进入平铺芯片后平铺成至少部分微液滴不包含重叠或堆叠的部分。
[0077]
48为检测模块,其包含了多通道的荧光探测,完成微液滴平铺之后的平铺芯片被转移至检测模块48中,通过荧光检测识别出不同的目标核酸片段,从而实现对于多于一个的目标核酸片段的绝对定量化结果检测。
[0078]
49为pcr扩增循环模块,其包含了热盖设计,由于扩增过程在第一容器内进行,所以整个扩增模块设计可以与现有的荧光类pcr系统类似设计,保证了系统实现成本更低设计复杂度也更小,为了减小蒸发,扩增模块也可以包含配合于第一容器的热盖设计。
[0079]
40a为废弃耗材收集口,40b为废弃耗材转移部,用于打开废弃耗材部并使得工作人员或者机器可以处理掉相关的废弃耗材,40c为操作处理部,可以选择操作程序和输出显
示最终检测结果等等。
[0080]
系统的工作流程大致如下:
[0081]
包含核酸序列的水性溶液放置于冷藏模块46中,其可以按照需求设置,例如设置为48,96等等样品数量,油性溶液被存储于456的油槽或者油管中,移动模块43通过移动,使得移液器运动至油性溶液移液头的上部,此处以4移液头为示例进行说明,4个移液头可以同步或者分步地摄取四个油性溶液移液头,完成摄取后移动模块43将油槽或者油管内的油性溶液吸取转移至所述第一容器中,完成后所述移动模块43移动至废弃耗材收集口40a将使用过的油性溶液移液头遗弃,完成油性溶液转移后,所述移动模块43移动至水性溶液移液头耗材存储单元上方,并吸取4个所述冷藏模块46内四个不同容器内的水性溶液,之后所述移动模块43移动至所述微液滴生成部存储区,将所述四个不同的试样分配进四个不同的微液滴生成部中,之后在废弃耗材收集口40a遗弃所述水性溶液移液头,完成之后所述移动模块43移动至已包含水性溶液的微液滴生成部,所述移液器摄取包含水性溶液的四个所述微液滴生成部,移动所述移动模块43至已经包含油性溶液的第一容器上方,所述移液器竖直向下运动实现微液滴生成部与所述第一容器相组合,所述移液器施加驱动力,驱动所述水性溶液分散成液滴状态进入第一容器内形成乳液状态。之后在废弃耗材收集口40a遗弃所述微液滴生成部,完成微液滴生成后,所述移动模块43移动至所述第一容器存储单元上方,所述转移机构被竖直驱动夹取所述第一容器至所述扩增模块49内,之后所述移动模块43的转移机构夹取所述第一容器盖,并且配合所述第一容器与所述第一容器盖形成密封结构,所述扩增模块49上部的压合结构压合至所述盖体上,并包含热盖设计,热循环完成之后带盖的第一容器被所述移动模块43的转移机构转移至微液滴平铺模块47中,所述移动模块43的转移机构转移微液滴平铺芯片至所述微液滴平铺模块47中,所述微液滴平铺模块中通过注入第三油性液体,驱动所述乳液中的微液滴进入平铺芯片中,所述第三油性液体可以与所述第一容器内的油性溶液物理特性相同也就是两者成分相同。平铺完成之后所述移动模块43的转移机构转移平铺有微液滴的平铺芯片至检测模块48中,并在其中实现至少一种目标核酸检测,并可输出最终的定量化结果至40c的处理部(当然为了保证对于相同样本的更多检测项目适配性,冷藏模块46内对应的水性核酸样本液可以被液滴生成部添加至不同的第一容器子单元体内,此处不再详述)。
[0082]
图5为移动模块43和移动行架的示意图,其包含前后移动水平驱动部,通过电机的驱动实现前后方向的移动,在移动行架之上还包含驱动所述移动模块左右移动的驱动部,通过电机的驱动实现左右移动,通过行架装置的辅助移动模块可以实现四个自由度方向的移动,当然也可以在移动模块43上设置竖直方向驱动电机实现整个移动模块43在六个自由度上的移动。
[0083]
图6为移动模块43组成结构示意图,整体上其包含了移液器431和转移机构432,其中所述移液器431包含了四个子移液单元,四个子移液单元分别为4311、4312、4313和4314,当然实际的设计过程中也不限定于4个子移液单元,每个子移液单元包含控制器的独立电机43101、43102、43103和43104从而能够实现每个子移液单元独立控制,这在某些特殊情况下可以调整每个被操作对象具有不同的体积容量,当然对于一致性好的对象,也可以用单一电机实现不同子移液单元的同时竖直方向移动,此处不限定。转移机构432用于转移不同的耗材包含第一容器、平铺芯片、容器盖等等,为了保证不同容器均可实现兼容性转移,所
述转移机构432具有预设宽度特征的夹持头4320,用于夹持具有一定宽度范围的耗材,为了配合夹持头的宽度特征,所述被操作耗材需要满足预设的强度要求以防止操作过程中耗材被施加力而产生变形破坏,所述转移机构432具有驱动电机驱动器竖直移动以调整夹持位置,所述转移机构432还包含驱动夹持头宽度的驱动电机以保证所述转移机构432的兼容性。
[0084]
图7和图8a示意了pcr扩增模块的示意图,为了保证系统处理速度更快并且保证整个系统的操作连续性更流畅,pcr扩增模块可以包含四个子pcr扩增单元491、492、493和494,由于pcr扩增需要一定的时间,在完成一组pcr试样制备后对于下一组试样进行制备能保证在扩增过程中系统空闲模块更少,当然在结构布局紧凑的前提下可以不限定为4个子pcr扩增单元,此处也是示意一种保证系统高效性的示例,如图8a任一扩增单元包含竖直驱动电机4911,其可以驱动包含热盖的夹紧部4914,紧贴所述第一容器盖,并使所述第一容器与所述容器盖实现紧密扣合,底部还包含升降温单元,其可利用帕尔贴效应实现对于第一容器的升温降温功能,同时散热部4913可以配合风扇实现快速降温效果,pcr扩增单元的最底部还包含水平驱动电机4912,结合图8b,其可水平驱动第一容器装在单元露出或者配合所述夹紧部4914,以实现第一容器与第一容器盖取出或者放入。
[0085]
图9a和图9b为本发明实施例提供的一种检测模块示意图,其包含了被探测的平铺芯片接收台481,配合开合结构平铺芯片接收台481可被一维地移动出或者入探测模块,所述探测模块设置为封闭的壳体结构内也实现了探测模块受其他模块影响较小的效果,也能尽可能减少交叉污染的风险,还包含激发光产生部484,用于产生主动的探测激发光,接收单元483,接收经过被探测试样内反射激发的荧光,通过后续的处理模块处理输出原始样液的目标核酸序列的原始拷贝结果,检测偏振模块482用于对激发光的输出光波长进行限定,例如该探测系统中包含5个偏振单元4822,通过水平移动控制部4821的控制所述5个偏振单元4822的某一对准所述激发光源与所述探测接收单元,更优地,包含核酸序列的初始水性溶液中可以包含对应的5种不同的荧光染料或荧光探针,此处不限定于对于相同样品均进行5种不同的偏振单元进行检测,也不限定于系统检测的偏振单元4822数量为5个,在这种设计中,激发光产生部484与接收单元483固定于固定的壳体上,可以保证其检测焦点或者焦平面始终不变保证检测的准确性和可重复性更高的效果。
[0086]
图10为液滴平铺模块结构示意图,其包含了承载第一容器的容纳部471,在所述容纳部上放置第一容器之后所述平铺芯片能被放置于其上部,注入部472流体性连通所述微液滴平铺芯片与所述第一容器,从而实现注入第三油性液体的目标,当注入所述第三油性液体时,所述以微液滴类型分布的水性溶液被驱动进入平铺芯片中,而平铺芯片中之前存在的介质例如空气可以被排空部473排出,当然所述平铺芯片内还可以包含初始保护溶液,此处并不限定。
[0087]
下表1为利用本发明的方法和系统在实际测试中获得的定量化结果,由下表结果可以得到利用本发明方法与系统可以实现准确且重复性高的可靠化定量结果。
[0088]
表1.利用本发明方法和系统获得的定量化结果
[0089][0090][0091]
需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
[0092]
以上所述仅为本技术的优选实施例而已,并不用于限制本技术,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。应注意到:相似的标号和字母在下面的附图中表示类似项,因此,一旦某一项在一个附图中被定义,则在随后的附图中不需要对其进行进一步定义和解释。以上所述仅为本技术的优选实施例而已,并不用于限制本技术,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。