具有两个流体流动路径用于检测和区分两个或多个分析物的免疫分析测试设备
本技术是申请号为201680062821.5的专利申请的分案申请。相关专利申请的交叉引用
1.本技术要求于2015年8月27日提交的申请号为62/210,880的美国临时申请、于2015年12月16日提交的申请号为62/268,455的美国临时申请以及于2015年12月22日提交的申请号为62/271,101的美国临时申请的优先权,其全部内容通过引用并入本文。对序列清单、表或计算机程序的参考
2.序列清单以电子方式通过efs于2016年8月24日创建的文本文件的形式提交,并命名为“04189609438116wo00seqlist.txt”(9,252字节),其全部内容通过引用并入本文。
技术领域
3.本文所述的主题涉及横向流动免疫分析,其具有两个分开的流体流动路径以检测和区分液体样本中的两种感兴趣的物种。
背景技术:
4.快速横向流动免疫分析测试设备在临床和家庭环境中都有广泛的应用历史。这些设备用于测试各种分析物,诸如激素、蛋白质、尿液或血浆成分等。这些设备通常包括横向流动测试条,诸如硝化纤维素或滤纸、样本应用区域、测试结果区域和结合到某种可检测标签的特异性结合分析物的试剂,诸如有色颗粒、荧光或发光标签或酶检测系统。这些设备的简单性是维持其在市场上使用的一个因素,以及期望在单个样本中检测和区分多种分析物的附加测试。
技术实现要素:
5.以下各方面、以及以下描述和说明的实施例是示例性和说明性的,而不在于限制范围。
6.在一个方面,提供了一种用于确定由感染原导致的感染的存在或不存在的设备。该设备包括样本接收区域,该样本接收区域被配置为接收来自怀疑患有由感染原导致的感染的受试者的液体样本,该样本接收区域被定位成将该样本沿着第一流体流动路径分配到第一标签区域并且沿着第二流体流动路径分配到第二标签区域。该第一和第二标签区域中的每一个分别包括第一可活动可检测物种和第二可活动可检测物种,每种可活动可检测物种能够结合到该感染原或结合到抗该感染原的抗体。该设备还包括位于该第一标签区域下游的第一流体流动路径中的第一测试线,该第一测试线包括对该第一可活动可检测物种具有结合亲和力的固定物种。该设备还包括位于该第二标签区域下游的第二流体流动路径中的第二测试线,该第二测试线包括对该第二可活动可检测物种具有结合亲和力的固定物种。该设备还包括位于第一流体流动路径中的参考线,该参考线包括固定物种,该固定物种对沉积在参考线上游设备上的可检测部分具有结合亲和力。
7.在一个实施例中,所述第一流体流动路径和所述第二流体流动路径处于从直角(180
°
)、钝角和锐角中选择的角度。
8.在另一个实施例中,所述第一流体流动路径中的参考线在所述第一测试线的下游。
9.在另一个实施例中,该设备还包括在第二流体流动路径中的附加参考线。在另一个实施例中,所述附加参考线位于所述第二测试线的下游。
10.在其他实施例中,设备设计为使得所述第一测试线包括第一固定物种,所述第一固定物种直接结合抗存在于所述液体样本中的感染原的抗体,并且特异地结合由所述第一标签区域中的可活动可检测物种和抗所述样本中的感染原的抗体组成的缀合物(conjugate)。
11.在其他实施例中,所述第二测试线包括第二固定物种,所述第二固定物种直接结合抗存在于所述液体样本中存在的感染原的抗体,并且特异地结合包由所述第二标签区域中的可活动可检测物种和抗所述样本中的感染原的抗体组成的缀合物。
12.在一些实施例中,所述第一和第二固定物种是相同的。
13.在一个实施例中,所述第一标签区域中的可活动可检测物种是抗igm抗体。在另一个实施例中,所述抗igm抗体是非人类抗人igm抗体。
14.在另一个实施例中,所述第一测试线中的固定物种包括多种伯氏疏螺旋体(b.burgdorferi)的抗原,所述抗原对抗伯氏疏螺旋体的人igm抗体具有结合亲和力。
15.在另一个实施例中,可活动可检测物种第二标签区域是抗igg抗体。在另一个实施例中,抗igg抗体是非人类抗人类igg抗体。
16.在另一个实施例中,第一测试线中的固定物种包括多种抗伯氏疏螺旋体抗原,其对抗伯氏疏螺旋体的人igg抗体具有结合亲和力。
17.在一个实施例中,所述可活动可检测物种包括可光学检测的标记。示例包括但不限于荧光或化学发光标记或可检测颗粒,诸如铕珠。
18.在一个实施例中,所述样本接收区域位于所述第一标签区域和所述第二标签区域之间。
19.在另一个实施例中,所述基质包括所述第一标签区域和所述第二标签区域共有的单个样本接收区域。
20.在一个实施例中,所述第一和第二测试线位于光检测的单个光路径内以供仪器检查。在一个实施例中,单个光路径是沿着与所述第一和第二测试线相交的一个轴的路径。
21.在另一个实施例中,所述样本接收区域以基本相等的量和基本相等的速率将样本分配到所述第一标签区域和所述第二标签区域。
22.另一方面,提供了一种设备用于确定由感染原导致的感染的存在。该设备包括(i)样本接收区域,其被配置为接收来自怀疑患有由感染原导致的感染的受试者的液体样本,该样本接收区域被定位成将该样本沿着第一流体流动路径分配到第一标签区域并且沿着第二流体流动路径到第二标签区域,所述第一和第二标签区域中的每一个分别包括第一可活动可检测物种和第二可活动可检测物种,每种可活动可检测物种能够结合抗感染原的单独且不同的抗体;(ii)位于所述第一标签区域下游的所述第一流体流动路径中的第一测试线,所述第一测试线包括对所述第一可活动可检测物种具有结合亲和力的固定物种;(iii)
位于所述第二标签区域下游的所述第二流体流动路径中的第二测试线,所述第二测试线包括对所述第二可活动可检测物种具有结合亲和力的固定物种;(iv)位于所述第一流体流动路径中并且包括固定物种的参考线,所述固定物种对沉积在所述参考线上游的所述设备上的可检测部分具有结合亲和力。
23.在一个实施例中,所述第一可活动可检测物种是非人类抗人类igm抗体或莱姆(lyme)抗原。在另一个实施例中,所述第二可活动可检测物种是非人类抗人igg抗体或莱姆抗原。
24.在另一个实施例中,在所述第一测试线上对所述第一可活动可检测物种具有结合亲和力的所述固定物种是非人类抗人类igm抗体或莱姆抗原。
25.在另一个实施例中,在所述第二测试线上对所述第二可活动可检测物种具有结合亲和力的所述固定物种是非人类抗人igg抗体或莱姆抗原。
26.在另一个实施例中,所述参考线位于所述第一测试线的下游。
27.在另一个实施例中,所述参考线包括对非人类抗人igg抗体或非人类抗人igm抗体具有结合亲和力的固定物种。
28.在一个实施例中,所述参考线包括对不存在于液体样本中的物质具有结合亲和力的固定物种。
29.在另一个实施例中,抗感染原的两种或更多种单独且不同的抗体存在于所述液体样本中,并且能够结合所述第一测试线和所述第二测试线中的每一个上的固定物种,并且能够结合所述第一标签线或所述第二标签线上的所述可活动可检测物种。
30.在另一个实施例中,抗感染原的单独且不同的抗体存在于所述液体样本中,并且能够结合在所述第一标签线上的可活动可检测物种以形成第一缀合物并且能够结合在所述第二标记线上的可活动可检测物种以形成第二缀合物,并且在所述第一测试线上的固定物种对所述第一缀合物具有结合亲和力,而所述第二测试线上的固定物种对所述第二缀合物具有结合亲和力。
31.在一个实施例中,在所述第一测试线上的固定物种是非人类抗人类igm抗体。在另一个实施例中,在所述第一测试线上的固定物种是非人类抗人igg抗体。
32.另一方面,提供了用于分级致病性疏螺旋体(borrelia)物种,诸如伯氏疏螺旋体(b.burgdorferi)感染的方法。该方法包括将怀疑或有风险暴露于致病性疏螺旋体物种的人的液体样本沉积在本文所述的设备上;以及(使用仪器)检查第一测试线和第二测试线是否存在可活动可检测物种。
33.在一个实施例中,液体样本是血液、脑脊髓流体或尿液。
34.在另一个实施例中,液体样本是血液并以小于50μl的量沉积。
35.在另一个实施例中,在沉积液体样本之后约10分钟或更短时间内执行检查。
36.在其他实施例中,沉积和检查提供了敏感性以检测在暴露2周内超过70%的暴露受试者伯氏疏螺旋体暴露的igm抗体应答。在另一个实施例中,沉积和检查提供敏感性以检测暴露2周内对超过70%的暴露受试者对伯氏疏螺旋体暴露的igg抗体应答。
37.除了上面描述的示例性方面和实施例之外,通过参考附图和研究以下描述,其他方面和实施例将变得明显。
38.根据以下描述、附图、实施例和权利要求书、本方法和组合物等的其他实施例将变
得显而易见。从前述和以下描述可以理解,本文描述的每个特征以及两个或更多这些特征的每个和每个组合都包括在本公开的范围内,只要包括在这种组合中的特征是不相互矛盾。另外,可以从本发明的任何实施例中明确排除任何特征或特征的组合。在下面的描述和权利要求中阐述了本发明的其他方面和优点,特别是当结合所附示例和附图考虑时。
附图说明
39.图1a
‑
1b是具有第一和第二流体流动路径的测试设备的两个实施例的顶视图;
40.图2示出了具有双侧流体流动路径和用于检查测试和可选参考线的光学窗口的位置的测试设备的顶视图;
41.图3是具有用于区分样本中的两种分析物的双向流体流动路径的测试设备的立体图。序列简述
42.seq id no:1是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mkkndqivaaialrgva
43.seq id no:2是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:cmkkddqiaaamvlrgmakdgqfalk
44.seq id no:3是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mkkndqigaaialrgva
45.seq id no:4是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mkkddqiaaaialrgma
46.seq id no:5是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mkkddqiaaamvlrgmakdgqfalkd
47.seq id no:6是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mkkddqiaaaialrgmakdgkfavkd
48.seq id no:7是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:vqegvqqegaqqp
49.seq id no:8是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:pvvaespkkp
50.seq id no:9是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:cpvvaespkkp
51.seq id no:10是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:lcpvvaespkkp
52.seq id no:11是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:ygqnwtnpenmvtsgpfklkeripnekivfeknnk
53.seq id no:12是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:mtlflfiscnnsgkdgntsa
54.seq id no:13是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:kmtlflfiscnnsgkdgntsa
55.seq id no:14是对来自疏螺旋体致病性菌株的表位具有结合亲和力的肽抗原:
tilvnlliscgltga
56.seq id no:15是对来自疏螺旋体致病菌株的表位具有结合亲和力的肽抗原:kdlknkilkikkeatgkgvlfeaftglktg
57.seq id no:16是对来自疏螺旋体致病菌株的表位具有结合亲和力的融合肽抗原:vqegvqqegaqqpgggmtlflfiscnnsgkdgntsagggmkkndqivaaialrgva
58.seq id no:17是对来自疏螺旋体致病菌株的表位具有结合亲和力的融合肽抗原:vqegvqqegaqqpgggmkkndqivaaialrgva
59.seq id no:18是对来自疏螺旋体致病菌株的表位具有结合亲和力的融合肽抗原:vqegvqqegaqqpgggmkkddqiaaamvlrgmakdgqfalkd
60.seq id no:19是合成的接头肽:ggg
61.seq id no:20是伯氏疏螺旋体(genbank登录号wp_012686633.1)的外表面蛋白c的氨基酸序列。
62.seq id no:21是伯氏疏螺旋体的核心蛋白聚糖结合蛋白a(genbank登录号wp_010890380.1)的氨基酸序列。
具体实施方式
i.定义
63.现在将在下文中更全面地描述各个方面。然而,这些方面可以许多不同的形式来体现,并且不应该被解释为限于在此阐述的实施例;相反,提供这些实施例是为了使本公开内容彻底和完整,并将其范围充分传达给本领域技术人员。
64.在提供一定范围的值的情况下,意图是该范围的上限和下限之间的每个中间值以及该陈述范围中的任何其他陈述或中间值都包括在本公开内。例如,如果规定1μm到8μm的范围,则也明确地公开了2μm、3μm、4μm、5μm、6μm和7μm,以及数值范围大于或等于1μ米,数值范围小于或等于8μ米。
65.除非上下文另有明确规定,单数形式“一个(a)”、“一个(an)”和“该(the)”包括复数指示物。因此,例如,对“聚合物”的提及包括单个聚合物以及两种或更多种相同或不同的聚合物,提及“赋形剂”包括单个赋形剂以及两种或更多种相同或不同的赋形剂等等。
[0066]“样本”是针对感兴趣分析物的存在或量进行测试的任何材料。优选地,样本是流体样本,优选液体样本。可使用测试设备测试的液体样本的示例包括体液,体液包括血液、血清、血浆、唾液、尿液、眼液、精液、痰液,鼻腔排液和脊髓液。
[0067]“测试条”可以包括一种或多种吸水或非吸水材料。如果测试条包括多于一种材料,则一种或多种材料优选地流体连通。测试条的一种材料可以覆盖在测试条的另一种材料上,例如覆盖在硝化纤维上的滤纸。可替代地或另外地,测试条可以包括具有一种或多种材料的区域,接着是具有一种或多种不同材料的区域。在这种情况下,这些区域流体连通并且可能或可能不会彼此部分地重叠。测试条的合适材料包括但不限于由纤维素衍生的材料,诸如滤纸、色谱纸、硝化纤维和醋酸纤维素,以及由玻璃纤维、尼龙、涤纶、pvc、聚丙烯酰胺、交联葡聚糖、琼脂糖、聚丙烯酸酯、陶瓷材料等。测试条的一种或多种材料可以任选地被处理以改变它们的毛细管流动特性或所施加样本的特性。例如,测试条的样本应用区域可以用缓冲液处理以校正施用的尿液样本的ph或比重,以确保最佳的测试条件。
ii.设备
[0068]
在第一方面,提供了一种用于确定由感染原因导致感染的存在的设备。将参照某些附图来描述该设备的各种实施例。
[0069]
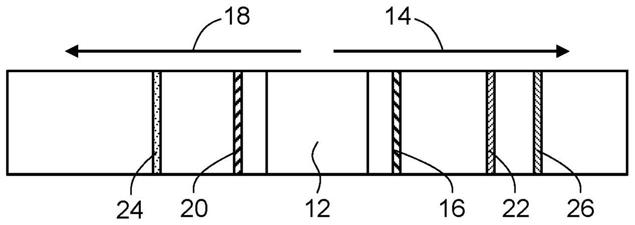
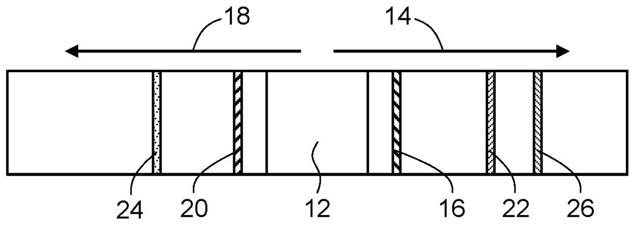
图1a中示出了设备的第一实施例。测试条10包括样本接收区域12,样本接收区域12被配置为接收液体样本。典型地,样本来自怀疑患有由感染原导致感染的受试者,并且下面描述了患者样本和感染原的类型的示例。样本接收区域12被定位成沿着图1a中箭头14所示的第一流体流动路径将样本分配到第一标签区域16并且沿着图1a中箭头18所示的第二流体流动路径分配到第二标签区域20。第一和第二标签区域中的每一个分别包括第一可活动可检测物种和第二可活动可检测物种,其中每种可活动可检测物种能够结合到感染原或抗感染原抗体,如将要描述的那样。
[0070]
如图1a所示的第一流体流动路径和第二流体流动路径处于180
°
的直角。在其他实施例中,第一流体流动路径和第二流体流动路径可以彼此成钝角或彼此成锐角。
[0071]
测试条10还包括位于第一流体流动路径中且位于第一标签区域(16)下游的第一测试线22。第一测试线包括对第一可活动可检测物种具有结合亲和力的固定物种。结合亲和力意味着两种物种之间的间接结合或直接结合,诸如抗原与抗体的直接结合或第二抗体与由第一抗体和抗原形成的缀合物的间接结合,其中第二抗体和第一抗体具有结合亲和力。例如,在一个实施例中,患者样本中的抗体指示由感染原感染的存在,并且患者样本中的抗体结合可活动可检测物种,该物种由对患者样本中的抗体具有结合亲和力的非人类抗体或指示疑似感染的感染原的抗原或来自感染物的抗原组成。
[0072]
测试条10还包括在第二流体流动路径(18)中并且位于第二标签区域(20)下游的第二测试线24。第二测试线包括对存在于第二标签区域中的第二可活动可检测物种具有结合亲和力的固定物种。如前一段所述,结合亲和力意味着两个物种之间的间接结合或直接结合。
[0073]
测试条10还包括位于第一流体流动路径(14)中的参考线26并且包括对于沉积在参考线上游或形成在设备上的可检测部分具有结合亲和力的固定物种。在一个实施例中,参考线26在第一测试线22的下游。可选地,并且如图1b所示,其中相同的元件由与图1a中相同的数字标识符表示,测试条包括第二流体流动路径(18)中的第二或附加参考线28。在一个实施例中,附加参考线位于第二测试线24的下游。
[0074]
如上所述,在一个实施例中,第一测试线包括直接结合存在于患者样本中的抗体的固定物种,抗体是由患者的免疫系统针对感兴趣的感染原引起并怀疑是患者感染原因的抗体。在另一个实施例中,第一测试线包括结合在测试设备上形成的缀合物的固定物种,缀合物由(i)第一标签区域中的可活动可检测物种和(ii)患者样本中存在的抗体组成,抗体是由患者的免疫系统针对感兴趣的感染原引起并怀疑是患者感染原因的抗体。
[0075]
在各种实施例中,第二测试线包括直接结合抗感染原的抗体的固定物种,抗体是由患者的免疫系统针对感兴趣的感染原引起并怀疑是患者感染原因的抗体。在另一个实施例中,第二测试线包括结合在测试设备上形成的缀合物的固定物种,缀合物由(i)第二标签区域中的可活动可检测物种和(ii)患者样本中存在的抗体组成,抗体是由患者的免疫系统针对感兴趣的感染原引起并怀疑是患者感染原因的抗体。
[0076]
现在描述继续参考图1a
‑
1b的说明性测试条。在该示例性测试条中,期望确定受试
者是否有莱姆病风险或具有莱姆病,或者期望确定是否感染疏螺旋体(borrelia)物种,例如但不限于伯氏疏螺旋体(borrelia burgdorferi)、阿氏疏螺旋体(borrelia afzelii)、伽氏疏螺旋体(borrelia garinii)、日本疏螺旋体(borellia japonica),处于感染的早期阶段或晚期阶段。为了实现这些愿望,提供了包括单个个人样本接收区域的测试条,并且患者样本被沉积在样本接收区域上或其中。样本接收区域对于测试条上的两个流体流动路径是共用的,其中第一流体流动路径在第一方向承载一部分沉积样本,并且第二流体流动路径在第二方向承载沉积样本的第二部分。在一个实施例中,两个流体流动路径和它们的流体流动方向彼此成180
°
,使得路径沿着共用的轴。两个流体流动路径中的每一个都包括标签区域,该标签区域包括可活动可检测物种。在示例性测试条中用于分级或检测由疏螺旋体属物种感染的可活动可检测物种在第一个实施例中是具有可检测标签或与可检测标签相关的非人类抗人类抗体。在一些实施例中,非人类抗人类抗体是带有可检测标签的非人类抗人类igg抗体,诸如荧光、化学发光或其他光学可检测标签,诸如珠子或化学部分。在一些实施例中,非人类抗人类抗体是带有可检测标签的非人类抗人igm抗体,诸如荧光、化学发光或其他光学可检测标签,诸如珠子或化学部分。在一个实施例中,光学可检测的意图是通过仪器可光学检测的,并且不能通过肉眼可视检测的。
[0077]
在该示例性测试条中,可检测非人类抗人类igm抗体被沉积在第一标签线上,并且可检测非人类抗人类igg抗体被沉积在第二标签线上。更具体地,将可检测的山羊抗人类igm抗体沉积在第一标签线上,并将可检测山羊抗人类igg抗体沉积在第二标签线上。非人类抗人类igg和igm抗体作为山羊抗人类抗体示例,然而抗体的非人类部分可以是任何哺乳动物,包括但不限于小鼠、兔、大鼠、绵羊等。
[0078]
用于检测或分级莱姆病的示例性测试条的第一测试线上沉积的是疏螺旋体属物种的抗原。例如,为了检测或分级由伯氏疏螺旋导致的莱姆病感染,将来自伯氏疏螺旋的一种或多种肽抗原沉积在测试条上每条流动路径的测试线上。在一个示例中,对伯氏疏螺旋的ospc、c6、c10、flab或bbk07区域具有结合亲和力的肽抗原以不可移动的方式沉积在测试线上。在另一个实施例中,将具有对伯氏疏螺旋或对伯氏疏螺旋抗体具有结合亲和力的重组蛋白质沉积在测试线上。例如,伯氏疏螺旋(genbank acc.no.wp_012686633.1;seq id no:20)的外表面蛋白质c(ospc)用于伯氏疏螺旋(genbank acc.no.wp_010890380.1;seq id no:21)的核心蛋白聚糖结合蛋白a(dbpa)的重组蛋白质,或考虑了来自蛋白质的12
‑
60个、12
‑
50个、12
‑
40个、10
‑
40个或10
‑
25个连续氨基酸残基的这些蛋白质的片段,如seq id no:12和seq id no:14所示。肽抗原的其他示例是本领域已知的,诸如在美国专利号8,338,556;6,716,574;6,719,983;8,071,109;8,354,240;6,475,492;6,660,274;7,887,815;5,643,733和美国专利公开号2015/0017666所示,其各自通过引用并入本文。
[0079]
在一个实施例中,沉积在一条或两条测试线上的肽抗原结合伯氏疏螺旋的c6区并且具有选自以下组的示例性序列:seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5或seq id no:6。在其他实施例中,沉积在一条或两条测试线上的肽抗原包括seq id no:1。seq id no:2。seq id no:3。seq id no:4。seq id no:5或seq id no 6(或者具有与其80%、85%、86%、87%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的肽)并且与生物素
‑
链霉抗生物素相互作用而附接在测试线上。在一个实施例中,沉积在第一测试线上和第二测试线上的肽抗原或多种肽抗原是相同的。在一个
实施例中,沉积在一条或两条测试线上的肽抗原具有与本文公开的肽或蛋白质序列之一80%、85%、86%、87%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的序列同一性。
[0080]
本文描述的测试条可以与包住测试条的壳体构件结合使用。壳体构件具有一个或多个孔,孔位于样本池和测试线以及参考线之上。用于壳体构件的材料在本领域中是已知的,用于测试条本身的材料也是已知的。图2示出了测试设备的俯视图,其中壳体构件中的光学窗口设置在测试线(22、24)和参考线(26、28)上方。光学窗口30和光学窗口32限定用户或光学读取器在用于审视测试线和参考线的仪器中可见的开口。
[0081]
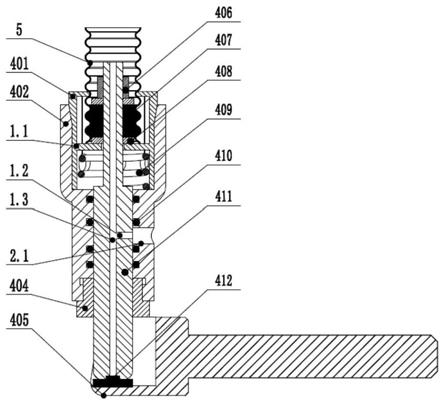
图3是具有用于区分样本中的两种分析物的双向流体流动路径的测试设备的透视图。在该实施例中,测试设备具有其上沉积测试线和对照线(诸如测试线42、44和对照线46、48)的基底硝化纤维素层40。样本垫50位于中央以通过标签垫(诸如标签垫52、54)将样本分配给每条测试线和对照线。标签垫具有适于接收可活动物种并且位于与硝化纤维素层和样本垫重叠以提供连续流体连通的材料。iii.使用方法
[0082]
本文所述的设备被设想用于检测任何致病原或感染原,现在描述几个示例。a.莱姆病的检测
[0083]
莱姆病通过携带病原体(致病性疏螺旋体属细菌(螺旋体))的各种硬蜱属咬伤传播。伯氏疏螺旋体sensu lato基团的生物体属于螺旋体科(spirochaetaceae),疏螺旋体属。伯氏疏螺旋体复合体中至少有11种物种,未知但大量的次基质。至少有3种borrelia burgdorferi sensu lato基团的基因组已被鉴定为病原体:b.burgdorferi sensu stricto、b.afzelli和b.garinii。在没有红斑迁徙的情况下诊断的当前基础是证明针对致病性疏螺旋体的抗体应答。本文所述的测试条提供了用于检测莱姆病的敏感和特异性诊断方法,例如,在感染后的早期阶段,并提供了一种手段来分级感染早期或晚期。
[0084]
在一个实施例中,提供了具有多个肽的测试条,多个肽固定在每个流体流动路径中的第一和第二测试线上,或者可在每个流体流动路径中的第一和第二标签线上移动。在每条测试线和/或标签线中,多个肽可以相同或不同。在一个实施例中,多种肽包括3种或更多种,或4种或更多种,或5种或更多种,或6种或更多种,或7种或更多种,或8种或更多种来自疏螺旋体物种,诸如b.burgdorferi sensu lato的不同肽序列。在另一个实施例中,多种肽包括多于2但少于10,或少于2但少于9,或多于2但少于8,或多于2但少于7,或多于2但少于6,或多于2但少于5,或多于2但少于4个的不同肽,肽特异性结合针对致病性疏螺旋体物种,诸如b.burgdorferi sensu lato的抗体。在一个实施例中,肽是与oppa、bbk32、ospc
‑
typek、reca、bmpa、dbpa、erpp、p35、ospf、crasp2、flilb、p66、ospc
‑
typea、flab或ddpb结合的肽的任何组合。在另一个实施例中,多种肽抗原包括含有来自borrelia flagellin p41的表位(例如,具有序列vqegvqqegaqqp(seq id no:7)的肽)和/或来自疏螺旋体ospc的表位(例如,具有序列pvvaespkkp(seq id no:8)的肽),包括活性(即,特异性结合的那些)变体。或者或另外,多种肽抗原包括含有来自vlse(区域ir6)疏螺旋体蛋白质(例如26个氨基酸的肽cmkkddqiaaa mvlrgmakdgqfalk(seq id no:2))的表位的肽或来自该区域的较短肽(诸如有来自seq id no:2的12
‑
18个连续残基的肽或来自seq id no:2的12
‑
18个非连续残基的肽,例如肽mkkndqigaaialrgva(seq id no:3))或其活性变体。
[0085]
锚定在测试条上的抗原还可以是一种、两种、三种、四种或更多种肽的融合肽,其与抗致病性疏螺旋体物种,诸如b.burgdorferi sensu lato的抗体结合。本领域技术人员可以理解接头肽的各种可能的组合和各种接头。本文提供了示例,其中例如flab肽(p41,seq id no:7)通过接头连接至c6肽(seq id no:1,seq id no:2,seq id no:3,seq seq id no:5或seq id no:6)以形成如seq id no:16,seq id no:17和seq id no:18所示出的融合肽。另一个示例在本文中阐述为seq id no:16,其由与来自与c6区域(seq id no:1)的肽连接的来自ospc1区域(seq id no:12)的肽连接的来自p41(flab)区域(seq id no:2),通过由三个氨基酸残基(ggg)组成的接头连接三个肽。在其他实施例中,接头肽包括1、2、3、4、5、6、7、8、9、10个或更多个氨基酸。在其他实施例中,接头包括1至2、1至5、2至5、2至4、1至10、5至10、3至6或2至10个氨基酸。在其他实施例中,接头是g、gg、ggg或gggg(seq id no:19)。
[0086]
用于连接本文公开的任何肽序列的合适接头可以容易地选择并且可以是任何合适的不同长度,诸如1个氨基酸(例如gly)至40个氨基酸、2个氨基酸至15个氨基酸、从3个氨基酸至12个氨基酸、包括4个氨基酸至10个氨基酸、5个氨基酸至9个氨基酸、6个氨基酸至8个氨基酸或7个氨基酸至8个氨基酸,并且可以是1、2、3、4、5、6或7个氨基酸。在一些实施例中,接头仅包括甘氨酸。在其他实施例中,1、2、3或4个甘氨酸被丝氨酸取代。
[0087]
非肽接头部分也可用于将载体部分连接或连接至线粒体融合调节肽。接头分子通常为长约6
‑
50个原子。接头分子还可以是,例如芳基乙炔,含有2
‑
10个单体单元的乙二醇低聚物、二胺、二酸、氨基酸或其组合。鉴于本公开,可以使用可以结合多肽的其他接头分子。
[0088]
应该理解,本文公开的和通过本文中的引入参考的肽仅仅是可以用于测定中的肽序列的示例。该测定的实施例考虑使用与两个序列沿其全长进行比较时与本文公开的任何序列具有80%、85%、86%、87%、89%、90%、91%、92%、93%、94%、95%、96%、97%序列同一性的肽序列。还应理解的是,任何序列都可以是生物素化的,包括在n
‑
末端,c
‑
末端生物素化或位于肽的第1、2、3、4、5个氨基酸(从n端氨基酸开始计算)内的氨基酸中的胺残基处。还应理解的是,任何序列可以在反应性部分或化学连接部分(例如羟基,羧基,胺或基团)的n端、c端或两者处被修饰。
[0089]
示例1
‑
4涉及用于检测针对致病性疏螺旋体物种的igg和igm抗体(示例1
‑
3)的测试条和用于由致病性疏螺旋体物种(实施例4)进行早期阶段或晚期阶段感染的阶段。设计测试条以检测由感染了致病性疏螺旋体物种的人受试者产生的免疫球蛋白。感染后,igm抗体在三至六周的时间内发展,并且这在本领域中被提及,并且在本文中被称为早期感染。igg抗体在感染后4
‑
12周内发展,并且指示后期感染,并且在本文中将其称为晚期感染。因此,在感染后3
‑
6周采集的血液样本中存在针对致病性疏螺旋体物种的igm抗体,表明感染或早期莱姆病的早期阶段,并且在感染后4
‑
12周采集的血液样本中存在针对致病性疏螺旋体物种的igg抗体,表明莱姆病的晚期阶段。在一个实施例中,莱姆病的晚期状态另外由样本中igg抗体的量大于样本中igm抗体的量来指示。示例1的测试条在第一和第二标签线上包括荧光标签和抗致病性疏螺旋体物种的igm或igg特异性的非人(例如,山羊)抗人类免疫球蛋白的缀合物。样本中的血液免疫球蛋白沿第一和第二流体流动路径行进至第一和第二标签线。在每条线上,对igg或igm的荧光缀合物山羊抗人类免疫球蛋白具有特异性的血液免疫球蛋白结合缀合物以形成特异性血液免疫球蛋白(igg或igm)和抗人类igg或igm的荧光缀合物的移动复合物。复合物向下游传播到它们各自的第一或第二测试线,其中复合物
的血液免疫球蛋白部分与沉积在每个测试线上的肽抗原结合,从而在一条测试线上检测致病性疏螺旋体物种的血液igg免疫球蛋白,并在其他测试线上检测致病性疏螺旋体属物种的血液igm免疫球蛋白。
[0090]
示例1的测试条旨在与具有光学读取器的仪器和用于操作光学读取器的软件相互作用,收集从测试条发出的信号并解释所收集的信号数据。测试条包括由仪器使用的参考线作为用于确定第一和第二测试线位置的位置对照。在示例1的测试条实施例中,参考线包括对igm特异性的固定非人类抗人类免疫球蛋白(尽管也可以使用对igg特异性的固定非人类抗人类免疫球蛋白)。固定非人类(例如兔)抗人类igm抗体结合沉积在标签线上的可活动非人类(例如,山羊)抗人类igm抗体可检测的缀合物并且结合标签线上形成的复合物,血液免疫球蛋白igm和非人类(例如山羊)抗人类igm抗体可检测缀合物的复合物。因此,在该实施例中,参考线捕获包括感兴趣分析物,针对感兴趣的病原体(在疏螺旋体物种的情况下)产生的血液免疫球蛋白的复合物。由于这个原因,参考线位于测试线的下游,因为如果存在少量待检测的感兴趣分析物,它将被捕获在参考线上,并且测试条将返回伪阴性。能够在测试条上捕获两个可检测部分的参考线
‑
在这种情况下,条上形成的复合物和标签线上的可检测标签物种
‑
增加了参考线上的可检测信号。
[0091]
示例2描述了用于确定针对致病性疏螺旋体物种的免疫球蛋白的存在并因此指示莱姆病的存在或不存在。在该测试条中,标签线包括一种或多种肽抗原的可活动可检测缀合物,缀合物对针对致病性疏螺旋体物种和可检测标签产生的血液中的免疫球蛋白igg或igm具有结合特异性可检测缀合物结合血液免疫球蛋白,形成行进到测试线下游的复合物。测试条上的一条测试线包括对igg免疫球蛋白具有结合亲和力的物种,而另一条测试线包括对igm免疫球蛋白具有结合亲和力的物种。以这种方式,igg和igm在测试线处的测试条上被区分。在示例1的实施例中,igg和igm在标签线处的测试条上被区分。在示例2的测试条中,在参考线上使用独立于与致病性borrelia物种相关的抗原
‑
抗体对的结合对。示例包括辣根过氧化物酶和抗辣根过氧化物酶以及葡萄糖氧化酶和抗葡萄糖氧化酶,其中一个结合对固定在参考线上,另一对结合构件沉积在参考线上游的测试条上。因此,考虑具有包括对液体样本中不存在的物质具有结合亲和力的固定物种的参考线的测试设备。
[0092]
示例3描述了用于确定针对致病性疏螺旋体物种的免疫球蛋白的存在并由此指示是否存在莱姆病的测试条的另一个实施例。测试条上的一条测试线包括对igg免疫球蛋白具有结合亲和力的物种,而另一条测试线包括对igm免疫球蛋白具有结合亲和力的物种。以这种方式,igg和igm在测试条上被区分。在样本池的一侧(例如,参见图1a)在下游至上游方向上沉积第一标签线,其包括附着于铕珠的可活动山羊抗人类igm抗体。该第一标签线的下游是第一测试线,其具有用于ospc区域的固定肽抗原(例如,鉴定为seq id no:12或seq id no:13的肽抗原)和用于伯氏疏螺旋体的dbpa区域(例如,鉴定为seq id no:14的肽抗原)。具有固定的兔子抗山羊igm抗体的参考线在第一标签线的下游。在样本池的相对侧(例如,参见图1a)在下游至上游方向上沉积第二标签线,其包括与铕珠结合的可活动小鼠抗人类igg抗体和具有用于伯氏疏螺旋体的c10(seq id no:8或seq id no:10),c6(seq id no:1,seq id no:2,seq id no:3,seq id no:4,seq id no:5或seq id no:6)和p41(flab;seq id no:7)的表位的固定肽抗原的第二测试线。修饰肽抗原以在n
‑
末端或n
‑
末端区域包括生物素部分,并通过与锚定的抗生蛋白链菌素分子结合而锚定在测试条上。
[0093]
从示例性测试条还可以理解,本文提供了区分针对相同感染原产生的单独的不同抗体的装置。测试条在第一测试线和第二测试线中的每一个上包括固定物种,固定物种结合针对相同感染原产生的单独的不同抗体中的每一种,并且通过使用对第一标签线和第二标签线上的单独的不同抗体之一具有特异性的可活动可检测物种来区分两种单独的不同抗体。
[0094]
如上所述,示例1
‑
3的测试条可以用来作为早期阶段或晚期阶段的致病性疏螺旋体物种的感染。如示例4中所述,方法包括将怀疑或有风险暴露于致病性疏螺旋体物种的人的液体样本沉积在本文所述的设备上,并检查第一测试线和第二测试线是否存在可活动可检测物种。在一个实施例中,沉积和检查提供敏感性,以检测暴露2周内超过70%的暴露受试者对伯氏疏螺旋体暴露的igm抗体的应答。在另一个实施例中,沉积和检查提供了敏感性,以检测暴露2周内超过70%的暴露受试者对伯氏疏螺旋体暴露的igg抗体的应答。
[0095]
在示例5中详述的另一项研究中,通过将常见的单个样本垫定位在硝化纤维条的中央,制备如图1a所示的测试条。在下游至上游方向的单个共用样本垫的一侧上沉积具有表面结合山羊抗人类igm抗体的多个可检测标记(例如铕珠)以形成第一标签线。在第一标签线的下游沉积了第一测试线,第一测试线由重组ospc(seq id no:20)和重组dbpa(seq id no:21)组成,各自在其n
‑
末端连接至生物素并通过抗生蛋白链菌素固定至硝化纤维。在第一测试线的下游沉积兔子抗山羊igg抗体以在硝化纤维上形成参考线。在共用单个样本垫的相对侧上,在下游至上游方向上沉积具有表面结合的小鼠抗人类igg抗体的多个可检测标记(例如,铕珠)以形成第二标签线。在第二标签线的下游沉积第二测试线,第二测试线构成针对伯氏疏螺旋体的c10(seq id no:8),c6(seq id no:6)和c6
‑
p41(seq id no:18)表位的固定肽抗原。修饰肽抗原以在n
‑
末端或n
‑
末端区域包括生物素部分并通过与锚定的抗生蛋白链菌素分子结合锚定至硝化纤维基质。c10肽抗原在其c
‑
末端用羟基基团修饰。测试条的每一端都放置吸水垫。
[0096]
获得来自患有急性红斑迁徙(莱姆病的早期指示)或莱姆关节炎(莱姆病晚期指示)的个体的血液样本,以及来自健康个体的血液样本作为阴性对照。用缓冲液稀释样本,并将已知体积放在测试条的样本垫上。孵育每个测试条,然后插入具有光学系统和软件的仪器中,询问测试线和参考线是否存在可检测标记。
[0097]
将仪器读取测试条的结果进行解释,并与酶免疫分析(eia),蛋白质印迹以及疾病控制和预防中心推荐的莱姆病的双层测试结果进行比较。在8例早期莱姆红斑迁徙样本中,用于igm检测的仪器读取测试条和蛋白质印迹igm检测到5/8(62.5%),并且通过eia检测igm检测的样本检测到4/8(50%),表明仪器读取测试条对于早期莱姆检测比eia更敏感。因此,在一个实施例中,如本文所述的测试条为检测igm提供了大于酶免疫测定法提供的敏感性,用于检测莱姆病或将莱姆病分级为早期阶段或晚期阶段。
[0098]
在所测试的4例晚期莱姆样本中,用于igg,蛋白质印迹igg和eia的仪器读取测试条检测到所有样本(100%),表明igg的仪器读取测试条具有相当于通过蛋白质印迹和eia检测igg的敏感性。因此,在一个实施例中,如本文所述的测试条为检测igg提供了敏感性,其与通过蛋白质印迹和/或酶免疫分析测定所提供的敏感性基本相同,用于检测莱姆病或作为分级莱姆病的早期阶段或晚期阶段。
[0099]
关于对照样本,igm和igg和蛋白质印迹igm和igg的仪器读取测试条对于所有测试
的20例阴性对照样本均为阴性(100%阴性一致)。eia报告了4例个阳性样本(80%阴性一致)。这表明用于igm和igg的仪器读取测试条比eia更具特异性并且与igm和igg蛋白质印迹特异性相当。因此,在一个实施例中,如本文所述的测试条为检测igm和/或igg提供了大于或高于通过酶免疫分析提供的igm和/或igg的特异性,用于检测莱姆病或将莱姆病分级为早期阶段或晚期阶段。b.用于检测和辨别两种或更多物种的其他示例性测试条
[0100]
除了上述用于检测和区分针对致病性疏螺旋体物种的igg和igm免疫球蛋白的测试条之外,还可以使用检测和区分或区分单纯疱疹病毒
‑
1和单纯疱疹病毒
‑
2(hsv
‑
1和hsv
‑
2),流感a和流感b(流感a和流感b),流感a b和呼吸道合胞体病毒(rsv)。还考虑了用于检测和区分与寨卡病毒相关的iga和igg的测试条。可以理解的是,双向测试条具有从共用样本池连通的两个单独的流体流动路径提供了从放置在共用样本池上的样本区分两种或更多种感兴趣的分析物的方法。
[0101]
关于用于hsv
‑
1和hsv
‑
2的检测和区分的测试设备,考虑了包括第一标签线和第二标签线的测试条,第一标签线和第二标签线各自包括可活动可检测抗人类igg抗体。测试条上的第一条测试线包括对hsv
‑
1具有结合亲和力的固定抗原,测试条上的第二测试线包括对hsv
‑
2具有结合亲和力的固定抗原。参考线位于第一测试线的下游并且包括独立于hsv感染性病原体的结合对的结合构件或包括结合沉积在标签线上的可活动可检测抗人类igg抗体的非人抗体。
[0102]
关于用于检测和区分流感a和流感b的测试设备,考虑了包括具有可活动可检测的抗流感a核蛋白抗体的第一标签线和具有可活动可检测抗流感b核蛋白抗体的第二标签线的测试条。第一测试线和第二测试线分别包括固定的抗流感a核蛋白抗体和固定的抗流感b核蛋白抗体。参考线位于第一测试线的下游,并且包括独立于流感a,流感b感染性病原体的结合对的结合构件或包括结合沉积在标签线上的可活动可检测的抗流感a(或流感b)核蛋白抗体的非人类抗体。
[0103]
关于用于检测和区分流感a/b和rsv的测试设备,考虑包括具有可活动可检测的抗流感a/b核蛋白抗体的第一标签线和可活动可检测的抗rsv抗体的第二标签线的测试条。第一测试线和第二测试线分别包括固定抗流感a/b核蛋白抗体和固定抗rsv抗体。参考线位于第一测试线的下游,并且包括独立于感染性病原体或感兴趣的结合对的结合构件或包括结合沉积在标签线上的可活动可检测抗体的非人类抗体。
[0104]
因此,本文的设备被设计成确定由感染原导致的感染的存在,并且能够检测和区分指示感染原的生物样本中的两种分析物(或两种或更多种分析物)。该设备包括样本接收区域,该样本接收区域被配置为从怀疑患有由感染原导致的感染的受试者接收液体样本,样本接收区域被定位成将样本沿着第一流体流动路径分配到第一标签区域并且沿着第二流体流动路径分配到第二标签区域。第一和第二标签区域中的每一个分别包括第一可活动可检测物种和第二可活动可检测物种,每个可活动可检测物种能够结合抗感染原的单独且不同的抗体。该设备还包括位于第一标记区域下游的第一流体流动路径中的第一测试线,第一测试线包括对第一可活动可检测物种具有结合亲和力的固定物种。该设备还包括位于第二标签区域下游的第二流体流动路径中的第二测试线,第二测试线包括对第二可活动可检测物种具有结合亲和力的固定物种。该设备还包括位于第一流体流动路径中的参考线,
该参考线包括对沉积在参考线上游设备上的可检测部分具有结合亲和力的固定物质。
[0105]
在一个实施例中,沉积在设备上的液体样本的体积小于约100μl、优选小于75μl、优选小于50μl、优选10
‑
75μl、优选10
‑
60μl、并且优选介于10
‑
50μl之间。
[0106]
测试在沉积液体样本之后约20分钟或更短时间内在第一和/或第二测试线处产生可检测信号,或者在沉积液体样本之后约15分钟或更少,或者在沉积液体样本之后约10分钟或更少,或者在沉积液体样本之后约10
‑
30分钟之间,或者在沉积液体样本之后约10
‑
45分钟之间。iv.示例
[0107]
以下示例本质上是说明性的,而不是限制性的。示例1用于检测抗伯氏疏螺旋体的抗体存在的测试条
[0108]
如下制备用于检测人血液中igg和igm抗体存在或不存在的横向流动免疫分析设备。测试条被构造成具有居中定位的样本垫,其用作测试条的共用样本池。在样本池的一侧(例如,参见图1a)在下游至上游方向上沉积第一标签线,其包括附着于铕珠的山羊抗人类igm抗体,第一测试线具有由以下列出的肽序列组成的固定肽抗原,以及具有固定兔子抗山羊igm抗体的参考线。在样本池的相对侧(例如,参见图1a)在下游至上游方向上沉积第二标签线,其包括与铕珠结合的山羊抗人类igg抗体和具有固定肽抗原的第二测试线,肽抗原由下面列出的肽序列组成。通过连接到测试条上的抗生蛋白链菌素部分固定的肽抗原和连接到每个肽并沉积在第一和第二测试线的每一个上的生物素是:mkkddqiaaaialrgma(seq id no:4)ygqnwtnpenmvtsgpfklkeripnekivfeknnk(seq id no:11)mtlflfiscnnsgkdgntsa(seq id no:12);以及vqegvqqegaqqpgggmtlflfiscnnsgkdgntsagggmkkndqivaaialrgva(seq id no:16)
[0109]
吸水垫定位在测试条的每个末端上。
[0110]
来自疑似患有由伯氏疏螺旋体引起的莱姆病的人的血液样本沉积在样品池上。15分钟后,将测试条插入具有光学系统和软件的仪器中,以确定第一测试线和第二测试线中是否存在铕。该仪器使用来自参考线的信号以确定第一和第二测试线的位置。示例2用于检测抗伯氏疏螺旋体抗体存在的测试条
[0111]
如下制备用于检测人血液中igg和igm抗体存在或不存在的横向流动免疫分析设备。测试条被构造成具有居中定位的样本垫,其用作测试条的共用样本池。在样本池的一侧(例如,参见图1a)在下游至上游方向上沉积第一标签线,其包括来自伯氏疏螺旋体的多种肽抗原,各自具有与针对伯氏疏螺旋体的抗体的特异性结合并附着于铕珠;具有固定山羊抗人类igg抗体的第一测试线;以及具有固定抗葡萄糖氧化酶抗体的参考线。第一条标签线包括葡萄糖氧化酶,其附着于与液体样本一起向下游行进的铕珠。在样本池(例如,参见图1a)的相对侧在下游到上游方向上沉积第二标签线,其包括来自伯氏疏螺旋体的多种肽抗原,其各自具有与伯氏疏螺旋体抗体的特异性结合并附着于铕珠;以及具有固定山羊抗人类igm抗体的第二测试线。沉积在第一和第二标签线上的肽抗原是:
mkkddqiaaaialrgma(seq id no:4)ygqnwtnpenmvtsgpfklkeripnekivfeknnk(seq id no:11)mtlflfiscnnsgkdgntsa(seq id no:12);以及vqegvqqegaqqpgggmtlflfiscnnsgkdgntsagggmkkndqivaaialrgva(seq id no:16)
[0112]
吸水垫定位在测试条的每个末端上。来自疑似患有由伯氏疏螺旋体引起的莱姆病的人的血液样本沉积在样品池上。15分钟后,将测试条插入具有光学系统和软件的仪器中,以确定第一测试线和第二测试线中是否存在铕。该仪器使用来自参考线的信号以确定第一和第二测试线的位置。示例3用于检测抗伯氏疏螺旋体抗体存在的测试条
[0113]
如下制备用于检测人血液中igg和igm抗体存在或不存在的横向流动免疫分析设备。测试条被构造成具有居中定位的样本垫,其用作测试条的共用样本池。在样本池的一侧(例如,参见图1a)在下游至上游方向上沉积第一标签线,其包括附着于铕珠的可活动山羊抗人类igm抗体,第一测试线具有用于ospc区域(seq id no:12)以及用于伯氏疏螺旋体的dbpa区域(seq id no:14)的固定肽抗原,以及具有固定兔子抗山羊igm抗体的参考线。在样本池的相对侧(例如参见图1a)在下游至上游方向上沉积第二标签线,其包括与铕珠结合的可活动小鼠抗人类igg抗体和具有用于伯氏疏螺旋体的c10(seq id no:8或seq id no:10),c6(seq id no:1,seq id no:2,seq id no:3,seq id no:4,seq id no:5或seq id no:6)以及p41(flab;seq id no:7)表位的固定肽抗原的第二测试线。修饰肽抗原以在n
‑
末端或n
‑
末端区域包含生物素部分,并通过与锚定的抗生蛋白链菌素分子结合锚定在测试条上。
[0114]
吸水垫定位在测试条的每个末端上。
[0115]
来自疑似患有由伯氏疏螺旋体引起的莱姆病的人的血液样本沉积在样本池上。15分钟后,将测试条插入具有光学系统和软件的仪器中,以确定第一测试线和第二测试线中是否存在铕。该仪器使用来自参考线的信号以确定第一和第二测试线的位置。示例4通过伯氏疏螺旋体对测试条进行分级感染
[0116]
制备如示例1中所述的测试条。从女性受试者采集血液样品,表现出肌痛,疲劳和红斑迁徙症状。血液样本沉积在测试条的样本垫上。20分钟后,将测试条插入具有光学系统和软件的仪器中以确定血液样本中针对伯氏疏螺旋体的igg和igm抗体的量或相对量。血液样本中针对伯氏疏螺旋体的igm抗体被捕获的测试线在被仪器探测时发出可检测信号。血液样本中针对伯氏疏螺旋体的igg抗体被捕获的测试线在被仪器探测时发出可检测信号。在igg抗体的测试线上发出的信号大于igm抗体在测试线上发出的信号,以指示晚期感染,因为igg抗体在感染后4
‑
12周升高(ed shapiro和p.auwaerter,传染病和抗微生物剂:伯氏疏螺旋体(莱姆病),2002年版)。示例5用于检测抗伯氏疏螺旋体抗体的测试条
[0117]
如下制备测试条。将样本垫置于硝化纤维条的中央。单个共用样本垫(例如,参见
图1a)的一侧在下游至上游方向沉积多个具有表面结合的山羊抗人类igm抗体的铕珠以形成第一标签线。在第一标签线的下游沉积了第一测试线,第一测试线由重组ospc(seq id no:20)和重组dbpa(seq id no:21)组成,各自在其n
‑
末端与生物素连接并通过抗生蛋白链菌素固定到硝化纤维上。在第一测试线的下游沉积兔子抗山羊igg抗体以在硝化纤维上形成参考线。在样本垫的相对侧上,在下游至上游方向上,沉积多个具有表面结合的小鼠抗人类igg抗体的铕珠以形成第二标签线。在第二标签线的下游沉积第二测试线,第二测试线由用于伯氏疏螺旋体的c10(seq id no:8),c6(seq id no:6)和c6
‑
p41(seq id no:18)表位的固定肽抗原组成。修饰肽抗原以在n
‑
末端或n
‑
末端区域包含生物素部分并通过与锚定的抗生蛋白链菌素分子结合锚定至硝化纤维基质。c10肽抗原在其c
‑
末端用羟基基团修饰。测试条的每一端都放置吸水垫。
[0118]
获得来自患有急性红斑迁徙(莱姆病早期指示)或莱姆关节炎(莱姆病晚期指示)的个体的血液样本,以及来自健康个体的血液样本作为阴性对照。使用校准的微量吸液管,将血液样本在缓冲液中1:10稀释(即在250μl缓冲液中的血液样本体积为25μl)。使用校准的微量吸液管,将100μl稀释的血液样本添加到测试设备的样本端口以与样本垫接触。将每个测试条培养10分钟,然后插入具有光学系统和软件的仪器中以询问测试线和参考线是否存在可检测的铕珠。来自每个测试设备运行的结果被解释为阳性(高于测定截止值)或阴性(低于测定截止值)。
[0119]
仪器读取测试条的结果被解释并与酶免疫分析(eia),蛋白质印迹和疾病控制和预防中心推荐的莱姆病的双层测试的结果进行比较。在8例早期莱姆红斑迁徙样本中,用于igm检测的仪器读取测试条和蛋白质印迹igm检测到5/8(62.5%),并且通过eia检测igm检测的样本检测到4/8(50%),表明仪器读取测试条对于早期莱姆检测比eia更敏感。因此,在一个实施例中,如本文所述的测试条为检测igm提供了大于酶免疫分析法提供的敏感性,用于检测莱姆病或将莱姆病分级为早期阶段或晚期阶段。
[0120]
在所测试的4个晚期莱姆样本中,用于igg,蛋白质印迹igg和eia的仪器读取测试条检测到所有样本(100%),这表明igg的仪器读取测试条具有相当于通过蛋白质印迹和eia检测igg的敏感性。因此,在一个实施例中,如本文所述的测试条为检测igg提供了敏感性,其基本上与通过蛋白质印迹和/或通过酶免疫分析法所提供的敏感性相同,用于检测莱姆病或将莱姆病分级为早期阶段或晚期阶段。
[0121]
关于对照样本,igm和igg和蛋白质印迹igm和igg的仪器读取测试条对于所有测试的20例阴性对照样本均为阴性(100%阴性一致)。eia报告了4例阳性样本(80%阴性一致)。这表明用于igm和igg的仪器读取测试条比eia更具特异性并且与igm和igg蛋白质印迹相当。因此,在一个实施例中,如本文所述的测试条为检测igm和/或igg提供了大于或高于通过酶免疫分析提供的igm和/或igg的特异性,用于检测莱姆病或将莱姆病分级为早期阶段或晚期阶段。
[0122]
在阳性和阴性样本中,仪器读取测试条的igm和蛋白质印迹igm结果之间有100%一致。仪器读取测试条的igg与蛋白质印迹igg结果之间有90.6%一致。仪器读取测试条的(igm igg)结果与2
‑
tier方法之间有96.8%的一致性。
[0123]
虽然以上已经讨论了多个示例性方面和实施例,但是本领域技术人员将认识到其某些修改,置换,添加以及其子组合是可行的。因此,以下所附权利要求和下文中引入的权
利要求旨在被解释为包括在其真实精神和范围内的所有这些修改,置换,添加和子组合。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。