一种用于诊断子宫腺肌病的mirna试剂盒
技术领域
1.本发明属于生物技术领域,具体涉及一种子宫腺肌病的分子诊断、疗效评估及与相关疾病鉴别诊断的生物标志物组合及其应用。本案是专利申请号为2018108552408,申请日为2018
‑
07
‑
31,发明名称为“一种与子宫腺肌病相关的血清mirna标志物及试剂盒”的分案申请。
背景技术:
2.子宫腺肌病(adenomyosis,am)是子宫内膜腺体和间质异位侵袭生长在子宫肌层,形成局部或弥漫性病灶的一种雌激素依赖性疾病,多数好发于35到50岁的育龄期女性,但也不乏发现在未有生育史的青少年女性人群(如20岁左右)中有诊断为子宫腺肌病的报道,常合并有子宫肌瘤、子宫内膜异位症及卵巢囊肿。子宫腺肌病的常见临床症状包括月经周期延长,月经量增多,进行性痛经和不孕。妇科检查可发现子宫均匀增大或局限性结节,质地较硬伴腹部压痛,甚至部分患者甚至无明显症状。子宫腺肌病已成为影响我国女性生活质量的重要疾病之一,是亟待解决的重大公共卫生问题。
3.子宫腺肌病的早期发生发展是一个非常缓慢的过程,发病早期无明显症临床状,即使伴有偶发性的月经周期延长,月经量增多或者痛经,临床影像学检查也很难发现微小病灶而造成漏诊或误诊。然而一旦患者出现典型的临床症状如月经周期延长,月经量增多,进行性痛经和不孕则暗示腺肌病病灶较为明显或数量众多,随后的药物治疗和手术治疗存在症状难以彻底缓解尤其是痛经、药物副作用明显、影响生育力保存及心理难以承受等一系列问题。但如果能很好地把握疾病进程,及时做出准确的临床诊断并采取相应的干预措施来阻止或减缓子宫腺肌病的发生,就可以极大地提高治疗效果和患者生活质量,因此,有效且准确的临床诊断手段显得尤为重要。
4.目前子宫腺肌病术后的组织病理学诊断仍是诊断子宫腺肌病的金标准,但病理诊断通常在子宫全切术后进行,不适用于临床的常规检查。经腹部超声具有检查方便快捷、价格低廉等特点,是目前影像学诊断子宫腺肌病的最主要手段。对于子宫腺肌病的诊断具有一定的临床价值。然而,经腹超声在临床运用过程中仍有一些不足,如分辨率较低,容易受到肥胖、腹腔脏器、气体以及腹壁疤痕的影响,对于区分子宫肌腺瘤与子宫肌瘤的微小病灶,其结构很难显示,存在较大的难度,在临床诊断时仍存在一定的误诊率和漏诊率。而其它的超声技术如经阴道超声、宫腔超声造影、弹性超声也存在类似的诊断学问题。除此之外,由于ct在软组织分辨率上有限,无法清晰呈现子宫体的形态、肌壁间回声情况、内膜厚度的图像,对于小的异位病灶成像效果不满意,因此在临床上应用于腺肌病的影像学检查相对比较少。鉴于 ct平扫诊断子宫腺肌病的价值不高,可作为诊断子宫腺肌病的补充手段。而mri对子宫腺肌症的诊断具有较好特异性和敏感性,且与阴道超声相比具有优越的空间分辨率和对比度,因此,mri可作为诊断子宫腺肌病的重要方法。然而,mri检查成本高、扫描检查时间长,这就局限了其作为筛选检查子宫腺肌病的常规作用。综上所述,我们仍需要进一步寻找一种非创伤性、特异性/敏感性高、方便可行且花费较低的诊断方法,而基于血
清/血浆、唾液及尿液等体液应用先进的分子生物学技术寻找敏感性、特异性高的蛋白质、脂类及核酸分子是为我们实现该设想提供了极大的可能性。
5.micrornas(即mirnas)是近年来肿瘤分子生物学研究领域的一个热点,它的成熟状态是一类进化上具有高度保守性且长约19
‑
244个核苷酸的小单链rna分子。它由dna转录产生,但不翻译成蛋白质,而是在蛋白质合成过程中调节其他靶基因的功能。mirnas参与了哺乳动物几乎所有的病理和生理活动,如个体发育、组织分化、细胞凋亡以及能量代谢等。近年来, mirna与肿瘤的关系已经成为研究的热点科学问题,研究证实mirna通过负调控基因的表达与多种肿瘤发病及进展密切相关。
6.研究已经证实血清中存在众多mirnas,这些小分子rnas性质稳定、含量丰富、易于定量检测,且存在疾病特异性。现有的成熟的技术,包括定性和定量mirna分子的技术,表明利用血清mirnas作为分子生物标志物的方法比传统的特异蛋白分子标记方法将更加有效,同时这也克服了分子标记在抗体制备和定量分析上发展所遇到的瓶颈。
7.然而,目前还没有关用于子宫腺肌病筛查或诊断较为稳定的生物标志物报道,若能筛选出子宫腺肌病血清中异常表达的mirnas作为生物标志物,并研制相应的疾病进展监测、辅助诊断试剂盒,将为子宫腺肌病的临床诊断行业现状带来一次有力的推动,同时也为对我国广大女性患者带来福音。
技术实现要素:
8.发明解决的技术问题
9.本发明的解决的第一个技术问题是找出一种与子宫腺肌病临床辅助诊断相关的血清mirna 标志物。
10.本发明解决的第二个技术问题是提供上述血清mirna标志物在制备子宫腺肌病筛查和诊断试剂盒中的应用。
11.本发明解决的第三个技术问题是提供用于子宫腺肌病分子筛查和诊断试剂盒。
12.发明采用的技术方案
13.一种与子宫腺肌病相关的血清mirna标志物,该标志物为hsa
‑
mir
‑
22
‑
3p、 hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p的任意组合。
14.所述的血清mirna标志物在制备子宫腺肌病辅助诊断试剂盒中的应用。
15.一种子宫腺肌病辅助诊断试剂盒,该试剂盒用于检测血清中hsa
‑
mir
‑
22
‑
3p、 hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p。
16.所述诊断试剂盒包括逆转录和探针法qpcr反应常用的生化试剂。用于逆转录的试剂包括如dntp mix(100mm),逆转录酶(50u/μl),10rt buffer,rnase抑制剂(20u/μl),nucleasefree water,mirna逆转录引物(具体包括hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及 hsa
‑
mir
‑
103a
‑
3p逆转录引物,购自applied bios
×
ystems)。用于探针法qpcr反应的试剂包括如universal master mixⅱwith ubg2
×
,assay 20
×
(具体包括 hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p的mgb probes和正反向pcr 引物),购自applied biosystems),nuclease free water。
17.所述诊断试剂盒还可以包括hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p的标准品(单链rna)。
18.发明的有益效果:
19.本发明提供的血清微小核糖核酸(micrornas/mirnas)标志物作为子宫腺肌病诊断的标志物的优越性在于:
20.(1)血清mirnas是一种新型生物标志物,区别于传统生物标志物,不仅稳定、微创、易于检测,且定量精确,将大大提高疾病诊断的敏感性和特异性,该类小分子rna生物标志物的成功开发有助于子宫腺肌病的辅助诊断,为其他疾病生物标志物的研制提供借鉴。
21.(2)血清mirnas试剂盒是一种系统、全面的诊断和监测试剂盒,可用于子宫腺肌病患者的辅助诊断,有助于反映子宫腺肌病患者的疾病状态,为临床医生快速准确掌握患者病情、及时采取更具个性化的防治方案提供支持。
22.(3)采用严密的设计和评价体系,本发明人初期采用solexa全基因组测术对混合子宫腺肌病患者血清样品和混合健康女性对照血清样品进行小rna测序,并应用qrt
‑
pcr的方法进行了多阶段验证(先训练集再验证集),以上方法和策略的应用加速和保证了血清mirnas 生物标志物和诊断试剂盒的应用,也为其他疾病生物标志物的研制提供方法和策略上的借鉴。
23.(4)本发明通过控制年龄等对疾病发展的影响因素,研究血清mirna在子宫腺肌病辅助诊断的应用前景,阐述异常表达的mirnas对于子宫腺肌病进展的影响,揭示其筛查和诊断价值。因此,本发明获得了子宫腺肌病发病相关血清mirnas表达数据库和特异性标志物;通过血清mirnas生物标志物和诊断试剂盒的研制和应用,可使得子宫腺肌病的诊断更加方便易行,为临床医生快速准确掌握患者病情,为临床治疗效果评价奠定基础,并为发现具有潜在治疗价值的新型小分子药物靶标提供帮助。
附图说明
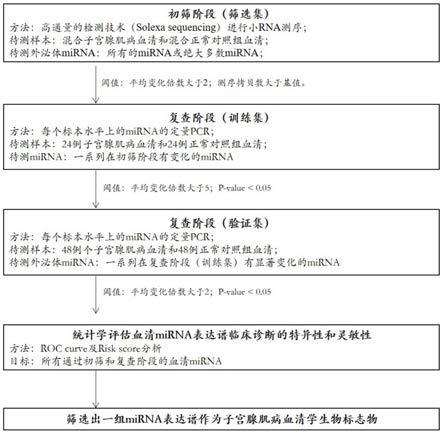
24.图1本发明的主要技术流程图。
25.图2训练集样本中qrt
‑
pcr检测候选mirna表达水平及统计分析。
26.图3验证集样本中qrt
‑
pcr进一步验证在训练集显著变化的mirna。
27.图4训练集样本使用3个mirna联合区分子宫腺肌病和健康女性roc曲线图。。
28.图5验证集样本使用3个mirna联合区分子宫腺肌病和健康女性roc曲线图。
29.图6全部样本(训练集 验证集)使用3个mirna联合区分子宫腺肌病和健康女性roc曲线图。
30.图7子宫腺肌病患者血清mirna表达水平与ca125水平相关性分析。
31.图8子宫腺肌病患者血清mirna表达水平与痛经评分相关性分析。
32.图9子宫腺肌病患者血清mirna表达水平与月经量评分相关性分析。
具体实施方式
33.本发明采用的思路(具体见图1):(1)以标准操作程序(sop)采集符合标准的血清样本,收集完整的人口学资料和临床资料。(2)选择子宫腺肌病病例、与子宫腺肌病年龄匹配的健康女性对照构成筛选集,solexa测序检测其血清mirna表达谱,筛选有显著差异表达mirnas (定义为初筛mirna)。(3)进一步选择子宫腺肌病病例、与子宫腺肌病年龄匹配的健康女性对照构成训练集,使用qrt
‑
pcr(taqman探针法)绝对定量法验证初筛mirna表达变
化,筛选显著差异表达mirnas(定义为训练集mirna)。(3)在(2)基础之上进一步选择子宫腺肌病病例、与子宫腺肌病年龄匹配的健康女性对照构成验证集,使用qrt
‑
pcr(taqman探针法) 绝对定量法验证训练集mirna表达变化,筛选仍有显著差异表达mirnas(定义为验证集 mirna)。(4)根据(1)、(2)、(3)分析单个mirna或多个mirna联合来用作子宫腺肌病血清生物标志物的敏感性及特异性,并开发子宫腺肌病mirnas诊断试剂盒。
34.发明人以标准操作程序(sop)采集符合标准的血清样本,收集完整的临床资料(年龄、生育史、月经史、痛经评分、月经量评分)等(这些资料可用于判断mirna表达水平与疾病进展的关系),并采用了solexa sequencing、rt
‑
pcr、real
‑
time pcr(taqman探针法)等检测技术。
35.具体来说本发明研究的实验方法主要包括以下几个部分:
36.1、研究样本的选择
37.(1)经病理学明确诊断的子宫腺肌病病例;
38.(2)手术前未经过激素或其它药物治疗;
39.(3)患者未合并有其它妇科生殖内分泌疾病及恶性肿瘤疾病;
40.(4)与病例年龄匹配的健康女性作为实验对照。
41.2、血清总rna提取及solexa测序样品质检
42.(1)取100ul血清样品加入到300ul水中,充分混匀后加入200ul(ph=4.7
‑
5.5)酸性酚,剧烈震荡混匀后加入200ul氯仿,再次充分震荡后16000g室温离心15分钟;
43.(2)小心吸取上清液(约400ul)加入到800ul异丙醇中,再加入ph=5.2,3m醋酸钠40ul, 充分混匀后
‑
20℃静置1h后,16000g,4度离心20分钟;
44.(3)充分弃上清后,加入75%乙醇1ml,轻柔颠倒数次,16000g,4度离心20分;
45.(4)充分弃上清,室温干燥后,加入20ul depc水溶解沉淀,
‑
80度保存。
46.(5)1%的琼脂糖电泳检测rna样品是否有降解以及杂质;凯奥k5500分光光度计检测样品纯度(凯奥,北京);安捷伦2100rna nano 6000assay kit(agilent technologies,ca,usa) 检测rna样品的完整性和浓度。
47.3、solexa测序
48.总rna样本检测合格后,首先对总rna进行片段选择,通过胶分离技术收集18
‑
30nt的 rna片段;在分离得到的rna片段的两端分别连接上接头,然后反转录成cdna,进行pcr扩增建立测序文库;最后,对检验合格的测序文库进行illumina hiseq高通量测序,采用se50 测序策略。
49.4、mirna反转录体系及反应条件
50.反应体系:dntps(100mm)0.15μl,multiscribe
tm rt 1.00μl,10
×
rt buffer 1.5 μl,rna inhibitor(20u/μl)0.19μl,nuclease h2o 7.16μl,血清总rna 2μl,共计15μl。反应条件:16℃,30min;42℃,30min;85℃,5min。
51.5.mirna绝对定量pcr反应体系及反应条件
52.反应体系:assay(20
×
)1.0μl,product from rt reaction 2.0μl,universal pcr master mixii(2
×
)10μl,h2o 7μl,cdna 2μl,共计20μl。反应条件:50℃,2min;95℃,10min;95℃,15s,60℃,60s,共40个循环。
53.6、标准曲线反应体系
54.人工合成mirna成熟体(上海吉玛制药技术有限公司)的不同浓度梯度(人工合成mirna 原液为10μmol/l,定义为起始浓度,然后用depc水分别稀释成10
‑3μmol/l、10
‑4μmol/l、 10
‑5μmol/l、10
‑6μmol/l、10
‑7μmol/l浓度梯度,上述浓度mirna的分别单独逆转,逆转录及qpcr反应体系和反应条件同上述4、5。样品浓度和对应ct值绘制标准曲线。
55.7、统计分析
56.根据solexa测序的拷贝数结果,对于无生物重复设计的样本,采用软件degseq进行差异分析,差异mirna(初筛mirna)的筛选条件为:padj<0.05并且|log2(fold_change)|≥1。
57.为了分析血清mirna对子宫腺肌病诊断特异性和灵敏性,评估其临床价值,对于单个 mirna,根据mirna浓度值和分组,利用spss19.0绘制roc曲线。
58.为了进一步研究这三种mirnas构成的综合指征用于子宫腺肌病诊断的效果,我们构建了一个数学公式,综合考虑每种mirna与子宫腺肌病发病的正、负关联情况和联系强度。具体来说,首先以训练集健康体检女性人群对照组hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p和hsa
‑
mir
‑
103a
‑
3p表达量的单侧95%参考值范围为标准,分别将这3种mirna的表达水平重新定义为0分和1分,然后通过训练集数据分析得出3种mirna的回归系数(即权重),综合考虑每种mirna的表达情况给每个人确定一个危险分值(risk score)。risk score计算方法如下:risk score=(3.091
×
hsa
‑
mir
‑
22
‑
3p的评分) (2.398
×
hsa
‑
mir
‑
182
‑
5p的评分) (2.231
×
hsa
‑
mir
‑
103a
‑
3p的评分),mirna表达水平界限值及mirna权重直接应用于验证集样本及总样本人群risk score计算。
59.运用x2检验(用于分类变量)或者student t检验(用于连续性变量)比较人口学特征、组织类型和mirna平均表达水平在研究对象组间分布的差异。统计学显著性水平p值设为0.05,所有统计学检验均为双侧检验。
60.以下是本发明进一步的说明:
61.在上述30例符合条件的子宫腺肌病病例及30例健康女性对照中,两组年龄按个体精确匹配。我们将这两组人群作为筛选集样本经solexa测序试验检测获得相关结果。
62.根据solexa测序方法,本发明人检测到在子宫腺肌病病例”组和“健康女性对照”组的血清中存在10个差异表达的微小核糖核酸(筛选标准:2组的拷贝数倍数差异大于5,统计水平pval<0.05、padj<0.05,测序raw count数值大于1000),具体包括:hsa
‑
mir
‑
192
‑
5p、 hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p、hsa
‑
mir
‑
122
‑
5p、hsa
‑
mir
‑
221
‑
3p、hsa
‑
mir
‑
142
‑
5p、 hsa
‑
mir
‑
223
‑
3p、hsa
‑
mir
‑
107、hsa
‑
mir
‑
103a
‑
3p、hsa
‑
mir
‑
15a
‑
5p(见表1、图1)。
63.表1.根据solexa测序结果初筛10个候选mirna作为子宫腺肌病生物标志物
64.mirna namefold change(fc)pvalpadjup/downsignificanthsa
‑
mir
‑
192
‑
5p13.4600upyeshsa
‑
mir
‑
22
‑
3p10.6100upyeshsa
‑
mir
‑
182
‑
5p8.4700upyeshsa
‑
mir
‑
122
‑
5p7.8100upyeshsa
‑
mir
‑
221
‑
3p7.4600upyeshsa
‑
mir
‑
142
‑
5p5.8200upyeshsa
‑
mir
‑
223
‑
3p5.2900upyes
hsa
‑
mir
‑
1075.2400upyeshsa
‑
mir
‑
103a
‑
3p5.0500upyeshsa
‑
mir
‑
15a
‑
5p5.0200upyes
65.根据初筛结果,进一步使用绝对定量qpcr(探针法)在训练集样本(24例乳腺癌病例和与其年龄匹配的24例健康女性对照)进行验证,结果发现共有3种mirnas(hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p)在“子宫腺肌病”组和“健康女性对照”组中表达情况存在显著性差异且差异倍数大于2倍(见表2、图2)。
66.表2.qrt
‑
pcr法检测训练集样本10个候选mirna表达水平及统计分析
67.mirna namefold change(fc)pup/downsignificanthsa
‑
mir
‑
192
‑
5p1.390.13upnohsa
‑
mir
‑
22
‑
3p3.30<0.0001upyeshsa
‑
mir
‑
182
‑
5p2.08<0.0001upyeshsa
‑
mir
‑
122
‑
5p0.940.52downnohsa
‑
mir
‑
221
‑
3p0.890.28downnohsa
‑
mir
‑
142
‑
5p0.760.23downnohsa
‑
mir
‑
223
‑
3p1.580.025upyeshsa
‑
mir
‑
1071.110.74upnohsa
‑
mir
‑
103a
‑
3p2.66<0.0001upyeshsa
‑
mir
‑
15a
‑
5p1.260.27upno
68.根据上述结果,将这3个与子宫腺肌病相关的mirnas在另外48例乳腺癌病例和与其年龄匹配的48例健康女性对照中进一步的验证。我们发现hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及 hsa
‑
mir
‑
103a
‑
3p)仍在病例组中呈高表达且差异表达倍数与在训练集样本差异倍数接近(见表3、图3)。
69.表3.qrt
‑
pcr法检测验证集样本10个候选mirna表达水平及统计分析
70.mirna namefold change(fc)pup/downsignificanthsa
‑
mir
‑
22
‑
3p3.26<0.0001upyeshsa
‑
mir
‑
182
‑
5p2.15<0.0001upyeshsa
‑
mir
‑
103a
‑
3p2.51<0.0001upyes
71.表4.训练集样本单因素逻辑回归分析结果(以对照组表达值95%参考值为界值)
[0072][0073]
多因素logistic回归分析结果表明(见表4),这3种mirnas的表达水平均与子宫腺ae 的发病存在着显著关联,我们使用spearman相关分析的方法分析血清中3种mirnas (hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p)表达水平与血清中ca125表达水平
之间的相关性,结果提示(见图4):血清中hsa
‑
mir
‑
22
‑
3p及hsa
‑
mir
‑
182
‑
5p表达水平与血清中ca125表达水平呈一定程度正相关(r2=0.181;r2=0.191)。进一步分析发现(见图5、6)hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p表达水平均与患者痛经评分和月经量评分成正相关。
[0074]
风险评分(risk score)及受试者工作特征曲线(roc)曲线分析分析这3种mirna的组合用于子宫腺肌病分子诊断的效果(见表5及图7、8及9),发现该组合(3panel mirna)对子宫腺肌病患者阳性预测值(ppv)分别达到0.82(基于训练集数据)、0.76(基于训练集数据)及0.78(基于训练集 验证集数据),子宫腺肌病患者分子诊断auc(area under the roc curve,即受试者工作特征曲线下面积)值分别达到0.915(基于训练集数据)、0.880(基于训练集数据)及0.891(基于训练集 验证集数据)。
[0075]
表5.mirna组合(hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p)用于区分不同集合子宫腺肌病和健康女性人群的风险评分(risk score)及受试者工作特征曲线(roc)曲线分析
[0076][0077]
根据上述实验结果,本发明人制备了一种能用于子宫腺肌病诊断的试剂盒,包含测定受试者血清中稳定存在且可检测的成熟hsa
‑
mir
‑
22
‑
3p、hsa
‑
mir
‑
182
‑
5p及hsa
‑
mir
‑
103a
‑
3p 的逆转录引物、探针及pcr引物和其他检测试剂。
[0078]
具体而言,这3种mirnas的组合构成的相关诊断试剂盒有助于子宫腺肌病的诊断,为临床医生快速准确掌握患者的疾病状态和病情严重程度,及时采取更具个性化的防治方案提供支持,从而最大限度提高子宫腺肌病患者的生活质量。
[0079]
发明人通过分离和研究子宫腺肌病者及与其年龄匹配的健康体检女性对照血清中的 mirnas,寻找一组与子宫腺肌病高度相关的高特异性和敏感性的mirnas可用于子宫腺肌病分子诊断,并研制出可便于临床应用的子宫腺肌病分子诊断试剂盒。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。