1.本发明涉及一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,属于富勒烯材料技术领域。
背景技术:
2.富勒烯具有完美的分子结构和丰富的物理化学性质,表面存在大量双键,具有强的清除自由基的性能,在化妆品、生物医药,以及超导、有机太阳能电池、非线性光学材料、人工光合成等领域具有十分广阔的应用前景。
3.作为一种非极性分子,富勒烯本身具有强烈的疏水性,在极性溶剂尤其是水中溶解度很低,限制了其实际应用,在化妆品和生物医药领域表现尤为明显。为提高富勒烯的水溶性,需对其进行化学修饰,获得富勒烯/水原液。一种常用的策略是使富勒烯表面羟基化,获得羟基化富勒烯,亦称富勒醇。
4.为使富勒醇获得足够的水溶性和胶体稳定性,需使表面羟基达到一定数目,从而不可避免地破坏富勒烯固有的π共轭体系。如何在保证水溶性和稳定性的前提下,最大限度地使富勒烯保持π共轭结构,是该领域一大难题。
5.富勒醇制备领域的另一个难题是制备工艺的繁琐和苛刻,且需用到强酸或强碱。当前主流工艺以强碱制备路线为主,制备过程中,需将原始富勒烯预先溶解于苯类溶剂中,继而与含强碱如氢氧化钠和双氧水的水溶液反应;为使反应顺利进行,还需加入相转移催化剂如四丁基氢氧化铵。此制备路线具有很多弊端,包括:苯类有机溶剂的残留易带来细胞毒性;强碱的使用易对设备和周围环境造成侵害;反应在两相界面处进行,效率低下且难以扩大生产;所得产品中易含有钠离子和四丁基铵离子,不利于后续应用。
6.因此,开发一种绿色环保、安全高效、能够最大限度地保持富勒烯的π共轭结构、具有优异水溶性和稳定性的富勒烯/水原液制备方法具有重要意义。
技术实现要素:
7.针对现有技术存在的不足,本发明提供一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法。本发明方法选用能够与富勒烯形成电子转移复合物的含氮极性有机溶剂,辅以羟基化反应、透析等流程,获得兼具高水溶性、稳定性和好的π共轭特性的水溶性富勒烯,突破以往富勒烯/水原液的两相制备工艺,避免强碱和苯系高毒性有机溶剂的使用,提高原液的生物相容性。本发明方法获得的富勒烯/水原液具有优良的抗氧化功效,可应用于化妆品、生物医药等领域。
8.本发明的技术方案如下:
9.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,包括步骤:
10.(1)将富勒烯充分溶于含氮极性有机溶剂或含氮极性有机溶剂与水的混合溶剂
中,得到富勒烯/有机溶剂母液;
11.(2)向步骤(1)制得的富勒烯/有机溶剂母液中加入氧化剂,使富勒烯发生羟基化反应;然后经透析处理,即得到电子转移复合物和表面羟基协同稳定的富勒烯/水原液。
12.根据本发明优选的,步骤(1)所述富勒烯为c
60
或c
70
中的一种或两种的混合物;优选为c
60
。
13.根据本发明优选的,步骤(1)所述含氮极性有机溶剂为吡啶、咪唑、嘧啶、吡唑或氮甲基吡咯烷酮中的一种或两种以上的混合物;优选为氮甲基吡咯烷酮。
14.根据本发明优选的,步骤(1)所述含氮极性有机溶剂与水的混合溶剂中,水所占的体积百分比为1
‑
30%,优选为10
‑
20%。
15.根据本发明优选的,步骤(1)所述富勒烯/有机溶剂母液中富勒烯的浓度为0.1~1.0毫克每毫升。
16.根据本发明优选的,步骤(2)所述氧化剂为双氧水水溶液,质量分数为10~30%。
17.根据本发明优选的,步骤(2)所述双氧水水溶液与富勒烯/有机溶剂母液的体积比为1:50~1:5,优选为1:20~1:5。
18.根据本发明优选的,步骤(2)所述羟基化反应是在搅拌条件下进行。
19.根据本发明优选的,步骤(2)所述羟基化反应的温度为10~60摄氏度,优选为25
‑
60摄氏度。
20.根据本发明优选的,步骤(2)所述羟基化反应的时间为24~168小时,优选为70
‑
150小时。
21.根据本发明优选的,步骤(2)所述透析处理过程中,透析膜的截留分子量为100~1000道尔顿,优选为100
‑
500道尔顿。采用透析处理以除去过量含氮极性有机溶剂。
22.根据本发明优选的,步骤(2)所述透析处理采用透析袋进行,透析袋外的去离子水与透析袋内液体的体积比为20:1~80:1;透析袋外的去离子水的置换间隔为12~48小时,去离子水的置换次数为3~8次。
23.根据本发明优选的,步骤(2)透析处理后还可包括稀释的步骤。
24.根据本发明优选的,步骤(2)所得富勒烯/水原液中,富勒烯的质量浓度为0.2
‑
1.5毫克/毫升。
25.本发明的技术特点及有益效果如下:
26.1、本发明方法制备过程未采用高毒性的苯类试剂溶解富勒烯,而是选取了毒性相对较低的含氮极性有机溶剂,制备过程较为绿色,且最终获得的富勒烯/水原液因不含苯类有机溶剂残存,细胞毒性低,生物相容性高。
27.2、本发明中羟基化反应为均相反应,克服了以往两相反应效率低下的弊端,便于扩大生产;制备过程无需加入相转移催化剂,避免了杂质离子的引入,提高了产品纯度,进一步简化了制备流程。
28.3、本发明方法制备过程避免了强碱的使用,绿色环保,最终产物不含金属离子,避免了过量金属离子给后续应用带来的制约。
29.4、本发明制备方法简单、绿色环保、安全高效、利于工业化生产。本发明方法所获得的富勒烯/水原液中,少量含氮极性有机溶剂与富勒烯间形成了电子转移复合物,同时富勒烯表面发生了羟基化反应;两种效应协同,使富勒烯表面接枝较少量的羟基即可具有很
高水溶性和分散稳定性,最大程度地保留了原有的π共轭结构,从而表现出强的自由基清除效果和抗氧化活性。本发明特定种类及用量的含氮极性有机溶剂结合适宜的氧化条件,共同作用实现本发明上述优异效果,即具有很高水溶性和分散稳定性的同时,相比现有富勒醇最大程度地保留了原有的π共轭结构,从而表现出强的自由基清除效果和抗氧化活性。
附图说明
30.图1为本发明实施例1中富勒烯c
60
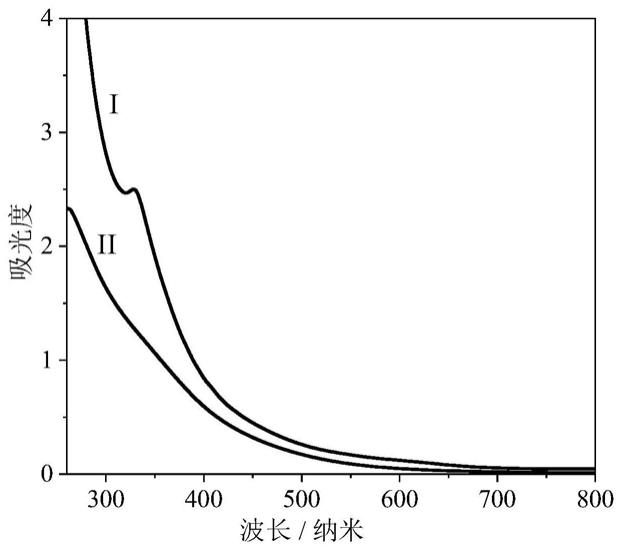
/氮甲基吡咯烷酮母液羟基化反应前(曲线i)、后(曲线ii)的紫外
‑
可见吸收光谱。
31.图2为本发明实施例1中所得到的富勒烯c
60
/水原液的照片。
32.图3为试验例中不同浓度富勒烯c
60
/水原液的清除羟基自由基的电子自旋共振测试结果图;其中,图b为图a中第二个峰的放大图;图c为根据图b绘制的羟基自由基清除率。
33.图4为本发明实施例1中所得到的富勒烯c
60
/水原液经冻干所得冻干粉的热重分析曲线。
34.图5为本发明实施例1中所得到的富勒烯c
60
/水原液经冻干所得冻干粉(曲线i)以及原始富勒烯c
60
的红外光谱(曲线ii)。
35.图6为本发明对比例1中透析过程袋内分散液外观与实施例1袋内溶液外观的对比图。
36.图7为本发明对比例1中所得富勒烯/水原液经冻干得到的冻干粉的红外光谱。
具体实施方式
37.下面结合具体实施例对本发明做进一步说明,但不限于此。
38.同时下述实施例中所述实验方法,如无特殊说明,均为常规方法;所述试剂、材料和设备,如无特殊说明,均可从商业途径获得。
39.实施例1
40.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,包括步骤:
41.称取500毫克富勒烯c
60
溶于500毫升氮甲基吡咯烷酮中,搅拌至c
60
完全溶解。取200毫升上述富勒烯/氮甲基吡咯烷酮母液,加入20毫升质量浓度为30%的双氧水,25摄氏度下搅拌反应6天。将产物转移至截留分子量为100道尔顿的透析袋中,透析袋外的去离子水的用量为8000ml,用去离子水透析一周,期间每24小时换一次水。透析结束后,将袋内溶液转出,用去离子水稀释至400毫升,得富勒烯c
60
/水原液。
42.富勒烯/氮甲基吡咯烷酮母液羟基化反应前(i)、后(ii)的紫外
‑
可见吸收光谱示于图1。为确保测试顺利,富勒烯/氮甲基吡咯烷酮母液或富勒烯c
60
/水原液经过了稀释,浓度为0.1毫克每毫升。从图中可以看出,富勒烯c
60
于328纳米附近的特征吸收峰反应后消失,表明富勒烯c
60
的π共轭结构被部分破坏,从而有力地证明了羟基化反应的成功进行。
43.所得到的富勒烯c
60
/水原液的照片示于图2;由图可知,可以看出原液底部无任何固体残渣,表明其具备良好的溶解性和稳定性。
44.将所得到的富勒烯c
60
/水原液冻干得到冻干粉,然后进行热重分析,其热重分析曲线如图4所示。从图中可以看出,粉末150度前只有微量的重量损失,表明粉末所含结晶水极
少。
45.将所得到的富勒烯c
60
/水原液冻干得到冻干粉,将上述冻干粉(i)和原始富勒烯c
60
(ii)进行红外光谱测试,测试结果如图5所示。其中来自富勒烯c
60
的特征峰,用星号标出。来自溶剂分子的特征峰,用三角形标出。来自羟基的特征吸收峰用圆圈标出,原始富勒烯c
60
此处的信号,来自于所含的微量水分。
46.将所得到的富勒烯c
60
/水原液冻干得到冻干粉,根据冻干粉x
‑
射线光电子能谱的测试结果,碳原子与氮原子的个数比为25.98,碳原子与氧原子的个数比为4.31。其中的氮元素,来源于少量与富勒烯c
60
形成电子转移复合物的含氮极性有机溶剂。
47.实施例2
48.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:将氮甲基吡咯烷酮替换为吡啶;其它步骤和条件与实施例1一致。
49.实施例3
50.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:将氮甲基吡咯烷酮替换为咪唑;其它步骤和条件与实施例1一致。
51.实施例4
52.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:将氮甲基吡咯烷酮替换为嘧啶;其它步骤和条件与实施例1一致。
53.实施例5
54.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:将氮甲基吡咯烷酮替换为吡唑;其它步骤和条件与实施例1一致。
55.实施例6
56.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:富勒烯c
60
的用量为375毫克,富勒烯/氮甲基吡咯烷酮母液中富勒烯的浓度为0.75毫克每毫升;其它步骤和条件与实施例1一致。
57.实施例7
58.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:富勒烯c
60
的用量为250毫克,富勒烯/氮甲基吡咯烷酮母液中富勒烯的浓度为0.5毫克每毫升;其它步骤和条件与实施例1一致。
59.实施例8
60.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:富勒烯c
60
的用量为125毫克,富勒烯/氮甲基吡咯烷酮母液中富勒烯的浓度为0.25毫克每毫升;其它步骤和条件与实施例1一致。
61.实施例9
62.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:溶剂氮甲基吡咯烷酮替换为氮甲基吡咯烷酮/水混合液(体积比为5:1);其它步骤和条件与实施例1一致。
63.实施例10
64.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:富勒烯c
60
替换为富勒烯c
70
;其它步骤和条件与实施例1一致。
65.实施例11
66.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:富勒烯c
60
替换为重量比为1:1的富勒烯c
60
/富勒烯c
70
混合物;其它步骤和条件与实施例1一致。
67.实施例12
68.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:质量浓度为30%的双氧水的用量为40毫升;其它步骤和条件与实施例1一致。
69.实施例13
70.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:质量浓度为30%的双氧水的用量为10毫升;其它步骤和条件与实施例1一致。
71.实施例14
72.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:反应温度为40摄氏度;其它步骤和条件与实施例1一致。
73.实施例15
74.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:反应温度为60摄氏度;其它步骤和条件与实施例1一致。
75.实施例16
76.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:反应时间为5天;其它步骤和条件与实施例1一致。
77.实施例17
78.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:反应时间为3天;其它步骤和条件与实施例1一致。
79.实施例18
80.一种电子转移复合物和表面羟基协同稳定的富勒烯/水原液的制备方法,如实施例1所述,所不同的是:透析袋的截留分子量为500道尔顿;其它步骤和条件与实施例1一致。
81.对比例1
82.一种富勒烯/水原液的制备方法,包括步骤:
83.称取500毫克富勒烯c
60
溶于500毫升氮甲基吡咯烷酮中,搅拌至c
60
完全溶解。取200毫升上述富勒烯/氮甲基吡咯烷酮母液,直接转移至截留分子量为100道尔顿的透析袋中,透析袋外的去离子水的用量为8000ml,用去离子水透析一周,期间每24小时换一次水。透析结束后,将袋内溶液转出,用去离子水稀释至400毫升即得。
84.与实施例1
‑
18相比,对比例中,富勒烯原液制备过程中未使用羟基化试剂双氧水。
85.透析过程中,袋内分散液外观与实施例1袋内溶液的对比图示于图6;从图中可以看出,对比例1所得分散液外观浑浊;透析结束后,分散液放置过程中出现了分层,稳定性差,表明羟基化试剂双氧水的使用有利于获得具有良好稳定性的富勒烯/水原液。
86.对比例1所得富勒烯/水原液经冻干得到的冻干粉的红外光谱示于图7。从图中可以看出,冻干粉仍然保留了原始富勒烯c
60
的特征吸收峰(星号标记),表明富勒烯c
60
未发生
明显的羟基化。
87.试验例
88.对实施例1制备的富勒烯c
60
/水原液进行稀释,分别得到富勒烯浓度为1.6ppm、8.0ppm、16ppm、80ppm的富勒烯c
60
/水原液,然后进行清除羟基自由基的电子自旋共振测试(电子自旋共振测试条件为:自由基捕获剂dmpo浓度为0.2摩尔每升,双氧水浓度为10毫摩尔每升,feso4·
7h2o浓度为0.25毫摩尔每升),同时设置不含富勒烯c
60
的空白试验,测试结果如图3所示。图b为图a中第二个峰的放大图,左侧峰自上而下,富勒烯c
60
的浓度(ppm)分别为:0、1.6、8.0、16、80。图c为根据图b绘制的羟基自由基清除率。从图中可以看出,富勒烯c
60
/水原液具有很强的羟基自由基清除能力,随浓度的升高,自由基清除率持续上升。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。