1.本发明属于分子诊断技术领域,具体涉及一种检测肺鳞癌抗氧化应激驱动通路相关基因突变的试剂、试剂盒和方法。
背景技术:
2.根据最新的2020年全球癌症统计报告,全球185个国家中肺癌的发病率和死亡率均居所有肿瘤的前列,肺癌的死亡人数占所有肿瘤死亡人数的近20%。作为肺癌中第二位的肺鳞癌,其对人群的危害也不容小觑,根据既往的流行病学资料显示,肺鳞癌发病率和死亡率均居首位。尽管多种突变位点以及针对各种突变的靶向药物层出不穷丰富了肺腺癌患者的治疗手段,使肺腺癌的治疗大步跨进了分子靶向的时代。然而关于肺鳞癌患者的驱动基因突变研究较少,治疗方式局限于手术和常规辅助治疗。随着全球肺癌分子研究的不断深入探索,由nfe2l2基因编码的nrf2蛋白主导的级联通路(即抗氧化应激通路)已经被证明是驱动肺癌发生发展的主要通路之一。抵抗氧化应激,本是正常人体对外界环境危险因素的正常生理功能,也是人体内细胞中对抗内外源性应激物质的重要手段,而且由于肺部器官的重要性,每一次呼吸都伴随着外界空气与肺上皮细胞的气体交换,而吸入气体中含有的对正常细胞有害的活性氧物质(ros)往往通过抗氧化应激通路的激活产生的下游基因来抵抗其影响。而一旦这条通路发生突变,对细胞的保护作用消失,从而导致细胞对外界环境因素的抵抗减弱,从而促进了肿瘤的发生和发展。对tcga数据库的突变数据分析表明,肺鳞癌病人中nfe2l2、keap1和cul3基因的突变率超过25%,上述基因的突变可使肿瘤细胞中的氧化应激状态得到过度激活,该通路下游基因的高表达往往引起细胞表达更多的氧化应激抵抗,对于肿瘤细胞来说,这种改变增强了肿瘤细胞的代谢变化和抗药性,从而导致肿瘤化疗耐药和免疫微环境的异质性形成,远期看导致了更差的生存预后。目前国际上针对keap1、nfe2l2和cul3抗氧化应激通路的靶向药物替拉格司他(cb
‑
839)的各项临床研究(尤其是针对肺癌的临床研究)正在如火如荼地开展。
3.目前肺鳞癌抗氧化应激驱动通路相关基因突变的检测并非临床常规项目,单独检测价格可达上万元,对于普通大众患者难以承受,有兼具准确性和应用价值的检测手段可以应用于临床,并且能够实现效益的更大化。关于检测肺鳞癌抗氧化应激驱动通路相关基因突变的试剂盒目前还未见报道。
技术实现要素:
4.针对现有技术中的不足,为了实现对肺鳞癌患者的精准治疗和个体治疗偏好,改善各类患者的预后,为肺鳞癌患者提供更多的治疗生存机会,本发明的目的之一是提供检测试剂在制备评估肺鳞癌抗氧化应激通路相关基因keap1、nfe2l2、cul3中任一基因突变的试剂盒中的应用,针对肺鳞癌中重要的驱动通路进行预测,以期推动肺鳞癌的分子靶向治疗进一步发展。
5.本发明的另一目的是提供评估肺鳞癌抗氧化应激通路相关基因keap1、nfe2l2、cul3中任一基因突变的试剂盒。
6.本发明的再一次目的是提供评估肺鳞癌抗氧化应激通路相关基因keap1、nfe2l2、cul3中任一基因突变的方法。
7.为达到上述目的之一,本发明的解决方案是:
8.检测试剂在制备评估肺鳞癌抗氧化应激通路相关基因(keap1、nfe2l2或cul3)突变的试剂盒中的应用,检测试剂由检测以下基因表达量的试剂组成:srxn1、trim16l、cyp4f3、diras2、c18orf65、nr0b1、lurap1、abcc2、fech、nqo1、bloc1s4、txnrd1;检测试剂作为试剂盒实现评估肺鳞癌抗氧化应激驱动通路相关基因突变的唯一关键成分。
9.作为本发明的优选实施例,试剂盒还包括说明书,说明书记载如下公式:riskscore=(0.2817
×
srxn1) (0.0219
×
trim16l) (0.0361
×
cyp4f3) (0.012
×
diras2) (0.0229
×
c18orf65) (0.0497
×
nr0b1) (
‑
0.2434
×
lurap1) (0.0434
×
abcc2) (0.106
×
fech) (0.0532
×
nqo1) (0.2071
×
bloc1s4) (0.432
×
txnrd1)。
10.作为本发明的优选实施例,肺鳞癌的截断值为5.014。
11.作为本发明的优选实施例,检测的样本为新鲜组织肿瘤样本。
12.作为本发明的优选实施例,当检测样本评分≥5.014时,代表该样本存在抗氧化应激通路相关基因突变的可能性较大;当检测样本评分<5.014时,代表该样本存在抗氧化应激通路相关基因突变的可能性较小。
13.为达到上述另一目的,本发明的解决方案是:
14.一种评估肺鳞癌抗氧化应激通路相关基因(keap1、nfe2l2或cul3)突变的试剂盒,其包括以下基因表达量的试剂:srxn1、trim16l、cyp4f3、diras2、c18orf65、nr0b1、lurap1、abcc2、fech、nqo1、bloc1s4、txnrd1。
15.为达到上述再一目的,本发明的解决方案是:
16.一种评估肺鳞癌抗氧化应激通路相关基因(keap1、nfe2l2或cul3)突变的方法,该方法用于非疾病的诊断和治疗目的,其包括如下步骤:
17.(1)检测样本以下基因表达量:srxn1、trim16l、cyp4f3、diras2、c18orf65、nr0b1、lurap1、abcc2、fech、nqo1、bloc1s4、txnrd1;
18.(2)计算:riskscore=(0.2817
×
srxn1) (0.0219
×
trim16l) (0.0361
×
cyp4f3) (0.012
×
diras2) (0.0229
×
c18orf65) (0.0497
×
nr0b1) (
‑
0.2434
×
lurap1) (0.0434
×
abcc2) (0.106
×
fech) (0.0532
×
nqo1) (0.2071
×
bloc1s4) (0.432
×
txnrd1);
19.(3)判断:当riskscore评分≥5.014时,代表该样本存在抗氧化应激通路相关基因突变的可能性较大;当riskscore评分<5.014时,代表该样本存在抗氧化应激通路相关基因突变的可能性较小。
20.由于采用上述方案,本发明的有益效果是:
21.第一、本发明首次提出了该基因组合物可用于评估肺鳞癌是否存在抗氧化应激通路相关基因(keap1、nfe2l2、cul3)的突变,可以有效指导肺鳞癌患者的个体化治疗,为精准治疗和个体化治疗添加更多重要的希冀,从而提高临床获益,同时避免不必要的医疗资源浪费。
22.第二、肺鳞癌抗氧化应激驱动通路相关基因突变目前在临床上属于非常规检测项
目,单独检测上述基因突变费用较高。该发明可通过临床上已广泛应用的rna测序技术判定肺鳞癌患者是否存在上述基因突变,具有经济实惠,准确性高、灵敏度和特异性好的优点。
附图说明
23.图1为本发明的实施例1中lasso回归中回归系数随着log(λ)的变化曲线图(纵坐标coefficients为系数)。
24.图2为本发明的实施例1中lasso回归中回归系数随着l1范数的变化曲线图(纵坐标coefficients为系数)。
25.图3为本发明的实施例1中lasso回归中均方差随着log(λ)的变化曲线图(纵坐标binomial deviance为二项式偏差)。
26.图4为本发明的实施例1中lasso回归筛选特征时,两种λ(min和1se)取值下的roc曲线比较图(横坐标false positive rate为误报率,纵坐标true positive rate为真实率)。
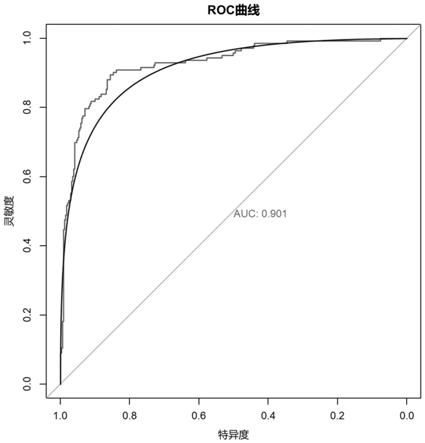
27.图5为本发明的实施例1中该预测模型在tcga(the cancer genome atlas)测试数据中的受试者工作特性曲线(roc)图。
具体实施方式
28.本发明提供了一种检测肺鳞癌抗氧化应激驱动通路相关基因突变的试剂、试剂盒和方法。
29.以下结合实施例对本发明基因集的筛选及效果验证做进一步的说明。
30.实施例1:
31.肺鳞癌抗氧化应激驱动通路相关基因突变的评分模型构建
32.方法:首先从tcga数据库中获得484个肺鳞癌样本数据,根据是否存在肺鳞癌抗氧化应激通路相关基因(keap1、nfe2l2、cul3)突变,将样本分为突变组(n=143)和野生组(n=341),通过对484个样本的编码蛋白的转录组rna表达谱基因的表达量数据以[log2(fpkm 1)形式]进行lasso回归分析,得到了与抗氧化应激通路相关基因突变状态显著相关的基因,最终挑选出12个基因为:srxn1、trim16l、cyp4f3、diras2、c18orf65、nr0b1、lurap1、abcc2、fech、nqo1、bloc1s4、txnrd1。
[0033]
此外,继续通过二分类logistic回归构建评分模型riskscore=(0.2817
×
srxn1) (0.0219
×
trim16l) (0.0361
×
cyp4f3) (0.012
×
diras2) (0.0229
×
c18orf65) (0.0497
×
nr0b1) (
‑
0.2434
×
lurap1) (0.0434
×
abcc2) (0.106
×
fech) (0.0532
×
nqo1) (0.2071
×
bloc1s4) (0.432
×
txnrd1)。
[0034]
最后,基于该评分模型计算每个样本的得分,通过roc曲线获取最佳阈值点,即截断值,截断值为5.014。根据截断值将tcga样本分为两组,评分高于该截断值归于突变组,评分低于该截断值归于野生组。
[0035]
实验结果表明:该预测模型灵敏度为0.852,特异度为0.913。
[0036]
图1显示了lasso回归通过收缩λ来限制不同回归特征的回归系数值。
[0037]
图2显示了lasso回归通过收缩l1范数来限制不同回归特征的回归系数值。
[0038]
图3显示了不同特征个数的纳入对整体的回归模型的均方差的影响。当均方差最
小时所得到的λ为λ(min),回归模型为min模型,在最小均方差的一个标准差时的所得到的λ为λ(1se),回归模型为1se模型。
[0039]
图4和图5从roc曲线结果选择使用min模型,对预测结果更加准确。
[0040]
实施例2:效果验证
[0041]
将复旦大学附属中山医院胸外科收集的30例肺鳞癌样本进行rna测序并检测了抗氧化应激通路相关基因(keap1、nfe2l2、cul3)突变,将rna表达数据带入该预测模型得到每个样本的riskscore评分,评分高于截断值5.014的为突变组,低于截断值5.014的为野生组。
[0042]
实验结果如表1所示:
[0043]
表1实验数据
[0044] 突变组野生组总计评分≥5.014729评分<5.01412021总计82230
[0045]
综上,该预测模型在中山医院病例队列中的效果验证的灵敏度为0.875,特异度为0.910。
[0046]
上述对实施例的描述是为了便于该技术领域的普通技术人员能理解和使用本发明。熟悉本领域技术人员显然可以容易的对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中,而不必经过创造性的劳动。因此,本发明不限于上述实施例。本领域技术人员根据本发明的原理,不脱离本发明的范畴所作出的改进和修改都应该在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。