一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测及鉴别系统
技术领域
1.本发明涉及生物医药检测技术领域,涉及poct快速核酸检测系统,具体涉及了一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测及鉴别系统。
背景技术:
2.乙型肝炎病毒(hepatitis b,hbv)是引起乙型肝炎(简称乙肝)的病原体,属嗜肝dna病毒科,hbv感染是全球性的公共卫生问题,给公共健康和社会经济带来了极大的负担。世界卫生组织统计数据表明,全球越有2.57亿人口患有慢性乙肝,约有15
‑
40%的慢性乙肝会转化成为肝硬化或者肝癌。因此,在hbv发生早期进行相关检测,对hbv的防治具有积极的意义。
3.中国专利cn112725531a公开了一种利用多交叉置换扩增(multiple cross displacement amplification,mcda)结合高分子纳米侧向流生物传感器(lateral flow biosensor,lfb)的手段,对于乙肝病毒进性核酸检测的技术方案。该检测系统包括用于扩增乙肝病毒的s基因的mcda单元和用于检测从mcda单元获得的mcda产物的检测单元;mcda单元包括置换引物对、交叉引物对和三对扩增引物对。该技术方案将mcda和lfb技术相结合,用于检测hbv病毒,其操作过程简单、扩增效率高且费用低廉,非常适合poct检测,以及在经济欠发达地区缺少检测设备的情况下进行快速检测。但是,上述技术方案仅仅能实现对乙肝病毒核酸的检测,并不能对待测样本进行乙肝病毒的分型,并且检测灵敏度有限。亟需研发一种能够检测乙肝病毒有无并同时能够获知乙肝病毒分型信息的快速检测方法,为临床诊断和治疗策略的制定提供有效参考。
技术实现要素:
4.本发明的目的在于一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测及鉴别系统,用以解决现有检测技术难以对乙肝病毒进行分型检测的技术问题。
5.为解决上述技术问题,采用的技术方案如下:
6.一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测鉴别系统,包括mcda扩增单元和crispr
‑
cas12b剪切检测单元;所述mcda扩增单元用于扩增b型和/或c型乙肝病毒的s基因并获得mcda扩增产物;所述crispr
‑
cas12b剪切检测单元用于处理mcda扩增产物并获得剪切产物;所述crispr
‑
cas12b剪切检测单元包括单链dna报告分子、grna和crispr
‑
cas12b蛋白;grna和crispr
‑
cas12b蛋白形成复合体,所述复合体用于识别mcda扩增产物并随后切割单链dna报告分子。
7.采用上述技术方案,技术原理为:
8.mcda扩增单元先对样本中的b型和/或c型乙肝病毒的s基因进行扩增,扩大目的片段的拷贝数,然后再将获得的mcda扩增产物加入crispr
‑
cas12b剪切检测单元中。grna和crispr
‑
cas12b蛋白形成复合体并识别mcda扩增产物,随后,该复合体对mcda扩增产物以及
单链dna报告分子进行切割,可对切割后的单链dna报告分子进行荧光检测或者免疫层析检测。如果样品中存在b型和/或c型乙肝病毒的s基因,则单链dna报告分子被上述过程剪切,显示出特定的阳性的检测信号。如果样品中不存在b型和/或c型乙肝病毒的s基因,则单链dna报告分子不会被剪切,则显示有别于阳性检测信号的信号。经过上述检测过程,推断样本中是否具有目的病原体,进而判断是否存在b型和/或c型乙肝病毒感染。
9.mcda的全称为多交叉置换扩增(multiple cross displacement amplification),是一种新型的快速的核酸扩增方法,采用本方对乙肝病毒的目的基因进行扩增,对设备的要求低且扩增效率高。较传统pcr技术而言,mcda技术不依赖于热循环扩增设备,反应速度快,敏感性好。mcda技术能够在恒温条件下实现靶序列扩增,具有扩增速度快、反应灵敏、特异性高等优点。现有技术中,已经有mcda结合免疫层析试纸条的检测技术,但是,上述检测过程并不能对不同类型的乙肝病毒形成区别和鉴定,并且检测灵敏度有限。采用本方案的mcda结合crispr的技术,通过适当的引物设计和反应条件的控制,可以实现对b型和/或c型乙肝病毒的检测和鉴别,并将获得理想的检测灵敏度。
10.进一步,所述mcda扩增产物上插入有pma序列。pam序列区是crispr
‑
cas12b系统行使切割功能的基本条件。如果靶序列没有pam序列,即使靶序列与sgrna序列完全匹配,crispr
‑
cas12b蛋白也不会切割该序列,也不会切割其周边的单链dna。
11.进一步,所述单链dna报告分子包括序列为5'
‑
fam
‑
tttttt
‑
bhq1
‑
3'的荧光报告分子;其中,fam表示羧基荧光素,bhq1表示猝灭基团。在荧光报告分子未被切割之前,fam和bhq1发生荧光淬灭。但在crispr
‑
cas12b剪切检测单元中,grna和crispr
‑
cas12b蛋白形成复合体,对荧光报告分子进行切割,fam和bhq1分离,发出荧光,可通过检测crispr
‑
cas12b剪切检测单元中的荧光强度来实现对样品是否为阳性的判断。如果样品中不含有b型和/或c型乙肝病毒的s基因,则荧光报告分子不会被切割,crispr
‑
cas12b剪切检测单元中不会检测出荧光信号。如果样品中含有b型和/或c型乙肝病毒的s基因,则荧光报告分子会被切割,crispr
‑
cas12b剪切检测单元中可以检测出荧光信号。
12.进一步,所述mcda扩增单元包括引物组合和bst dna聚合酶,所述引物组合包括用于扩增b型乙肝病毒的s基因的b型引物组合和用于扩增c型乙肝病毒的s基因的c型引物组合。bst dna聚合酶为可以高效介导mcda扩增反应等恒温扩增的酶,通过设置b型引物组合和c型引物组合两种引物组合,可以对b型乙肝病毒的s基因和c型乙肝病毒的s基因进行扩增,实现对两种类型的乙肝病毒的检测。
13.进一步,所述b型引物组合包括序列如seq id no:1所示的b
‑
f1;序列如seq id no:2所示的b
‑
f2;序列如seq id no:3所示的b
‑
p1;序列如seq id no:4所示的b
‑
p2;序列如seq id no:5所示的b
‑
c1;序列如seq id no:6所示的b
‑
c2;序列如seq id no:7所示的b
‑
d1;序列如seq id no:8所示的b
‑
d2;序列如seq id no:9所示的b
‑
r1;序列如seq id no:10所示的b
‑
r2。
14.进一步,所述c型引物组合包括序列如seq id no:12所示的c
‑
f1;序列如seq id no:13所示的c
‑
f2;序列如seq id no:14所示的c
‑
p1;序列如seq id no:15所示的c
‑
p2;序列如seq id no:16所示的c
‑
c1;序列如seq id no:17所示的c
‑
c2;序列如seq id no:18所示的c
‑
d1;序列如seq id no:19所示的c
‑
d2;序列如seq id no:20所示的c
‑
r1;序列如seq id no:21所示的c
‑
r2。
15.进一步,所述grna包括序列如seq id no:11所示的b
‑
grna和序列如seq id no:22所示的c
‑
grna。
16.采用上述引物组合可以实现对目的基因的高效扩增,并在扩增子上加入pam序列。针对mcda扩增,引物设计的难度非常大。有的引物组合虽然能够进行一定程度的扩增,但是扩增效率低,并不能实现检测目的。在本技术方案中,发明人对大量候选引物组合进行了测试,发现上述引物组合可以实现目的基因的高效扩增。
17.进一步,一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测鉴别系统还包括用于检测所述剪切产物的lfb单元;所述lfb单元包括储存有链霉亲和素修饰的纳米显色分子的结合垫、固定有羧基荧光素抗体质控线和固定有生物素偶联的牛血清蛋白的检测线;所述单链dna报告分子还包括序列为5'
‑
fam
‑
tttttt
‑
biotin
‑
3'的lfb报告分子;其中,fam表示羧基荧光素,biotin表示生物素。
18.lfb生物传感试纸条为现有技术中的常规结构,lfb依次包括样品垫、结合垫、质控线(cl)、检测线(tl)和吸收垫。本方案在结构的基础上,在结合垫中包埋了链霉亲和素修饰的纳米显色分子(sa
‑
gnps),在质控线上固定了羧基荧光素抗体(anti
‑
fam),在检测线上固定了生物素偶联的牛血清蛋白(biotin
‑
bsa)。将剪切产物加到样品垫上之后,在吸收垫的作用下,剪切产物向结合垫运功,剪切产物中的biotin(来自lfb报告分子,包括lfb报告分子被切割后的biotin端和未被切割的lfb报告分子)与sa
‑
gnps中的sa结合,形成biotin
‑
sa复合物;包含有biotin
‑
sa复合物的剪切产物继续向cl运动,剪切产物中的fam(来自lfb报告分子,包括lfb报告分子被切割后的fam端和未被切割的lfb报告分子)与cl上的anti
‑
fam结合,与anti
‑
fam结合的分子停留在cl处;剪切产物继续向tl运动,剪切产物中的biotin
‑
sa复合物(lfb报告分子被切割后的biotin端与sa
‑
gnps形成的复合结构)与biotin
‑
bsa中的biotin结合,与biotin
‑
bsa结合的分子固定在tl。通过观测质控线(cl)和检测线(tl)上是否形成猩红色的条带,来判断待测样品是否为阳性。
19.进一步,所述mcda扩增单元的工作温度为60
‑
70℃;所述crispr
‑
cas12b剪切检测单元的工作时长为1
‑
20min。经实验研究,mcda扩增单元的工作温度在60
‑
70℃之间,可以实现目的基因的高效扩增,并且以65℃为最优选择。使用crispr
‑
cas12b剪切检测单元剪切单链dna报告分子的剪切时间为1
‑
20min,可实现该分子的充分剪切,其中以2
‑
5min为最优选择。
20.进一步,一种基于crispr
‑
cas12b对乙肝病毒b型和c型的超灵敏快速检测鉴别系统的检测下限为10copies
21.综上所述,本方案将mcda、crispr
‑
cas12b和lfb技术相结合,用于检测同时检测b型和c型的hbv病毒,其操作过程简单、扩增效率高且费用低廉,非常适合床旁检测(poct),以及偏远地区缺少检测设备的情况下的快速检测。其中,检测前的dna模板准备需要约15min的时间,mcda扩增需要30min左右的时间,crispr
‑
cas12b剪切15min左右,lfb检测需要约2min的时间,完成整套检测仅需约70min的时间。除了节约时间,本方案的检测方法还可以提高检测灵敏度。中国专利cn112725531a将mcda和lfb结合使用lod可以达到5iu(每个反应),约25
‑
30copies(1iu为5
‑
6copies),在本技术方案中,对两种病毒的检测lod为10copies(每个反应)。所以本方案将检测灵敏度增加了2.5
‑
3倍,而检测时间只比现有技术增加了约5min左右,检测效率大大提升。
附图说明
22.图1为本发明实施例的b型hbv的s基因引物位点示意图。
23.图2为本发明实施例的c型hbv的s基因引物位点示意图。
24.图3为本发明实施例的mcda扩增的原理示意图。
25.图4为本发明实施例的基于crispr
‑
cas的反式剪切的原理示意图。
26.图5为本发明实施例的lfb检测的阴性和阳性的判断标准。
27.图6为本发明实施例的mcda
‑
crispr
‑
实时荧光检测的工作流程图。
28.图7为本发明实施例的mcda
‑
crispr
‑
lfb的工作流程图。
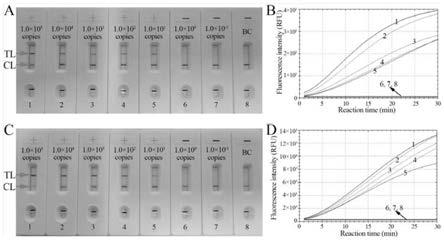
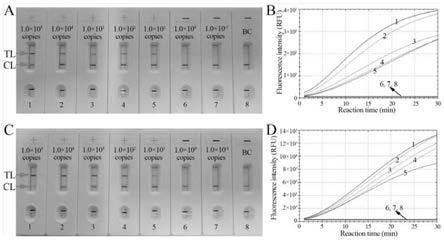
29.图8为本发明实验例1的灵敏度检测的实验结果图。
30.图9为本发明实验例2的最佳mcda反应温度的实验结果图(b型)。
31.图10为本发明实验例2的最佳mcda反应温度的实验结果图(c型)。
32.图11为本发明实验例2的crispr
‑
cas12b剪切时间的实验结果图。
33.图12为本发明实验例3的特异性检测结果(mcda
‑
crispr
‑
lfb)。
34.图13为本发明实验例3的特异性检测结果(mcda
‑
crispr
‑
实时荧光检测,b型)。
35.图14为本发明实验例3的特异性检测结果(mcda
‑
crispr
‑
实时荧光检测,c型)。
36.图15为本发明对比例1的mcda扩增的浊度随时间变化的曲线(b型,第一套引物)。
37.图16为本发明对比例1的mcda扩增的浊度随时间变化的曲线(b型,第二套引物)。
38.图17为本发明对比例1的mcda扩增的浊度随时间变化的曲线(b型,第三套引物)。
39.图18为本发明对比例1的mcda扩增的浊度随时间变化的曲线(b型,第四套引物)。
40.图19为本发明对比例1的mcda扩增的浊度随时间变化的曲线(b型,第五套引物)。
41.图20为本发明对比例1的mcda扩增的浊度随时间变化的曲线(c型,第一套引物)。
42.图21为本发明对比例1的mcda扩增的浊度随时间变化的曲线(c型,第二套引物)。
43.图22为本发明对比例1的mcda扩增的浊度随时间变化的曲线(c型,第三套引物)。
44.图23为本发明对比例1的mcda扩增的浊度随时间变化的曲线(c型,第四套引物)。
45.图24为本发明对比例1的mcda扩增的浊度随时间变化的曲线(c型,第五套引物)。
具体实施方式
46.下面结合实施例对本发明做进一步详细的说明,但本发明的实施方式不限于此。若未特别指明,下述实施例所用的技术手段为本领域技术人员所熟知的常规手段;所用的实验方法均为常规方法;所用的材料等,均可从商业途径得到。
47.实施例1:
48.1.目标dna和临床样本的制备
49.在本研究中合成了b型hbv的s基因的全长dna序列(b型的hbv的s基因的序列见genbank accession no.af100309),以及c型hbv的s基因的全长dna序列(c型的hbv的s基因的序列见genbank accession no.ab014381)。并将b型hbv的s基因和c型hbv的s基因使用现有技术的常规手段分别整合到puc57载体中,获得b型质粒和c型质粒(中国安徽general biol公司)。同时也获取了a型、d型、e型、f型、g型和h型hbv的s基因的全长dna序列(genbank accession no.分别为:af090842、x65259、ab032431、ab036910、af160501和ay090454),并使用puc57载体构建a型质粒、b型质粒、d型质粒、e型质粒、f型质粒、g型质粒和h型质粒。114
个疑似hbv感染的血清样本在2020年4月
‑
11月之间从医院采集。
50.2.mcda引物设计和grna的设计
51.b型hbv的s基因和c型hbv的s基因的mcda的引物设计如表1、表2、图1和图2所示。b型hbv的s基因和c型hbv的s基因的grna根据crispr
‑
cas12b原理设计。每个mcda引物和grna识别位点在基因上的位点参见图1和图2。为了满足crispr
‑
cas12b的要求,我们在mcda引物上添加了pma位点(attc),具体的是在在b
‑
d1和c
‑
d1的5’端修饰了pam位点(protospacer adjacent motif)。在图1和图2中,右箭头和左箭头分别表示同正义链一致的引物和同正义链反向互补的引物。b型hbv的s基因的mcda引物包括置换引物对、第一扩增引物对、第二扩增引物对、第三扩增引物对和交叉引物对。置换引物对包括b
‑
f1(正向置换引物)和b
‑
f2(反向置换引物);第一扩增引物对包括b
‑
d1(第一反向扩增引物)和b
‑
d2(第一正向扩增引物)、第二扩增引物对包括b
‑
c1(第二反向扩增引物)和b
‑
c2(第二正向扩增引物);第三扩增引物对包括b
‑
r1(第三反向扩增引物)和b
‑
r2(第三正向扩增引物);交叉引物对包括b
‑
p1(正向交叉引物)和b
‑
p2(反向交叉引物)。c型hbv的s基因的mcda引物的设置情况同b型hbv,在此不做赘述。所有寡聚核苷酸由genscript biotech co.,ltd.合成和纯化。图1和图2中的方框部分表示grna识别位点(grna与目的基因的扩增子形成互补配对)
52.表1:b型hbv的s基因mcda的引物设计
[0053][0054]
表2:c型hbv的s基因mcda的引物设计
[0055]
[0056]
3.基于纳米粒子的侧向流生物传感器的制备
[0057]
本方案的高分子纳米侧向流生物传感器(lateral flow biosensor,lfb,60mm
×
4mm)的制备采用现有技术中的方法,委托天津汇德鑫生物科技发展有限公司制备该高分子纳米侧向流生物传感器。lfb(又称免疫层析试纸条)包括四个部分,即在背板上依次设置的样品垫、结合垫、硝酸纤维素膜(nc膜)及吸水垫。在结合垫上包被有链霉亲和素修饰纳米金(streptavidin
‑
gold nanoparticles,sa
‑
gnps)。在硝酸纤维素膜上依次设置检测线及控制线,检测线和控制线之间间隔5mm。质控线(cl)上固定有羧基荧光素抗体anti
‑
fam,检测线(tl)上固定有生物素偶联的牛血清蛋白(biotin
‑
bsa)。sa
‑
gnps、anti
‑
fam和biotin
‑
bsa均可以通过商业化手段获得。
[0058]
4.mcda扩增
[0059]
mcda反应采用25μl反应体系,进行一步反应获得mcda扩增产物(使用的试剂盒为:isothermal amplification kit,huidexing biotech.co.,ltd.tianjing,china)。mcda反应体系包括:12.5μl of 2
×
反应缓冲液;(b
‑
或c
‑
)f1和(b
‑
或c
‑
)f2各0.4μm、(b
‑
或c
‑
)d1和(b
‑
或c
‑
)d2各0.8μm、(b
‑
或c
‑
)r1和(b
‑
或c
‑
)r2各0.8μm、(b
‑
或c
‑
)c1和(b
‑
或c
‑
)c2各0.8μm、(b
‑
或c
‑
)p1和(b
‑
或c
‑
)p2各1.6μm;1μl bst 2.0dna聚合酶(8u);核苷酸模板(使用标准质粒1μl,或者临床样本5μl);加双蒸水将整个体系调整至25μl。如果样品是rna,还需要在mcda反应体系中加入amv逆转录酶(10u)。上述扩增反应在恒温扩增设备中进行,并使用实时浊度仪(la
‑
500)监测反应进行过程,完成扩增之后获得mcda扩增产物。mcda扩增过程参见图3,由于d1修饰了pam位点,在完成mcda扩增之后,在目标扩增子上构建了crispr
‑
cas12b识别位点。
[0060]
5.crispr
‑
cas12b检测步骤
[0061]
在本方案中,cas12b(c2c1)被用来进行基于crispr
‑
cas的反式剪切检测(crispr
‑
cas
‑
based trans
‑
cleavage detection)。首先,合成crispr
‑
cas12b
‑
grna复合物(crispr
‑
cas12b
‑
grna complexes):将300nm crispr
‑
cas12b(c2c1)(cat no.ht100006)和100nm grna混合,在37℃和1
×
hdx缓冲液的环境中孵育10min,获得crispr
‑
cas12b
‑
grna复合物。形成的crispr
‑
cas12b
‑
grna复合物需要立即使用,如果不能立即使用,则需要将其储存在0
‑
4℃的环境中,储存时间不超过12h。
[0062]
crispr
‑
cas12b检测系统包括mcda扩增产物2μl、单链dna报告分子1μl(50μm或者100μm)、crispr
‑
cas12b
‑
grna复合物4μl、2
×
hdx缓冲液25μl,加水将crispr
‑
cas12b检测系统调整至50μl。然后,将crispr
‑
cas12b检测系统置于恒温37℃环境中孵育5min,获得剪切产物。剪切产物可以用于lfb检测,也可以在上述孵育过程中对crispr
‑
cas12b检测系统进行实时荧光检测。在使用实施荧光检测的时候,单链dna报告分子为5'
‑
fam
‑
tttttt
‑
bhq1
‑
3'(100μm,荧光报告分子);进行lfb检测时,单链dna报告分子为5'
‑
fam
‑
tttttt
‑
biotin
‑
3'(50μm,lfb报告分子)。crispr
‑
cas12b检测步骤的原理示意图参见图4,crispr
‑
cas12b
‑
grna复合物首先识别目标扩增子上的目标序列,然后crispr
‑
cas12b
‑
grna复合物将单链dna报告分子剪切。
[0063]
6.lfb检测
[0064]
按照样品在lfb上流动的顺序,lfb依次包括样品垫、结合垫、质控线(cl)、检测线(tl)和吸收垫,该结构为现有技术中常规的免疫层析试纸条的结构,只是在结合垫上固定
的是sa
‑
gnps,在质控线上固定的是anti
‑
fam,在检测线上固定的是biotin
‑
bsa。将1.5μl剪切产物加到试纸条的样品垫上,并同时在样品垫上加入50μl 100mm pbs,2min后可以在nc膜上观测tl和cl上是否显示出红色的线。层析过程如下:将剪切产物和pbs组成的样品加到样品垫上之后,在吸收垫的作用下,样品向结合垫运功,样品中的biotin(来自单链dna报告分子,包括单链dna报告分子被切割后的biotin端和未被切割的单链dna报告分子)与sa
‑
gnps中的sa结合,形成biotin
‑
sa复合物;包含有biotin
‑
sa复合物的样品继续向cl运动,样品中的fam(来自单链dna报告分子,包括单链dna报告分子被切割后的fam端和未被切割的单链dna报告分子)与cl上的anti
‑
fam结合,与anti
‑
fam结合的分子停留在cl处;样品继续向tl运动,样品中的biotin
‑
sa复合物(单链dna报告分子被切割后的biotin端与sa
‑
gnps形成的复合结构)与biotin
‑
bsa中的biotin结合,与biotin
‑
bsa结合的分子固定在tl。
[0065]
判定阴性和阳性的标准参见图5,左列表示lfb的示意图,右列表示lfb的对应的实物图;第一排是阳性的情形,第二排的阴性的情形。针对阳性检测结果,可以在tl上观测到猩红色条带,cl上的猩红色条带可能存在,也可能不存在。如果剪切产物中所有的单链dna报告分子均被完全切割消化,则cl上可不出现猩红色条带。在一些情况下,tl上的条带可以略微弱于cl上的条带。针对阴性检测结果,在cl上可以观测到猩红色条带,但是tl上不存在猩红色条带。tl上存在很微弱的信号也是可能的,但是tl上的信号会远远弱于cl的信号。tl上存在很微弱的信号的情况基本上发生在将加样后的lfb放置在室温中超过10min后。所以观测检测结果需要在10min内进行,最好在加样后2min左右进行结果观察。
[0066]
图6和图7分别展示了mcda
‑
crispr
‑
实时荧光检测和mcda
‑
crispr
‑
lfb的工作流程图。mcda
‑
crispr
‑
实时荧光检测包括:第一步:dna提取(本领域常规技术)、第二步:mcda扩增;第三步:crispr
‑
cas12b剪切以及实时荧光检测。mcda
‑
crispr
‑
lfb包括:第一步:dna提取(本领域常规技术)、第二步:mcda扩增;第三步:crispr
‑
cas12b剪切;第三步:lfb检测。
[0067]
实验例1:灵敏度的研究
[0068]
使用b型质粒和c型质粒作为模板,对mcda
‑
crispr
‑
实时荧光检测和mcda
‑
crispr
‑
lfb的灵敏度进行研究,b型质粒和c型质粒的用量分别为1
×
105,1
×
104,1
×
103,1
×
102,1
×
101,1
×
100,1
×
10
‑1copies每个反应,并同时设置空白对照(bc)。实验结果如图8所示,图8中a和b是使用b型质粒为模板,图8中c和d是使用c型质粒为模板,图8中a和c展示的是mcda
‑
crispr
‑
lfb,图8中b和d展示的是mcda
‑
crispr
‑
实时荧光检测,图8中“ ”表示阳性,
“‑”
表示阴性。由实验结果可知,mcda
‑
crispr
‑
实时荧光检测和mcda
‑
crispr
‑
lfb的lod(the limited of detection)均为10copies每个反应。在本实验例中,针对mcda
‑
crispr
‑
lfb,其他参数条件为:mcda扩增温度为65℃,扩增时间为30min,crispr
‑
cas12b剪切时间为5min,完成上述过程后,即开始进行lfb检测;针对mcda
‑
crispr
‑
实时荧光检测,mcda扩增温度为65℃,扩增时间为30min,在crispr
‑
cas12b剪切的同时检测实时荧光,检测时间至少持续20min。
[0069]
实验例2:最优反应条件的研究
[0070]
使用b型质粒和c型质粒作为模板(1.0
×
103copies每个反应),对mcda扩增的温度条件进行了研究(60
‑
67℃),使用浊度仪进行实时监测,实验结果参见图9和图10,结果显示65℃是最佳反应温度。
[0071]
对crispr
‑
cas12b剪切的时间进行了研究,反应时间分别选取1、5、10和20min进行
研究。实验结果参见图11,图11中a和c是使用b型质粒为模板,图11中b和d是使用c型质粒为模板,图11中a和b展示的是mcda
‑
crispr
‑
lfb,图11中c和d展示的是mcda
‑
crispr
‑
实时荧光检测。实验结果显示,针对mcda
‑
crispr
‑
lfb,crispr
‑
cas12b剪切为2min(b型)、5min(c型),即可观测到检测结果,针对mcda
‑
crispr
‑
实时荧光检测,crispr
‑
cas12b剪切为1min,即可观测到检测结果。在本实验例中,针对mcda
‑
crispr
‑
lfb,其他参数条件为:质粒浓度为1.0
×
103copies每个反应,mcda扩增温度为65℃,扩增时间为30min,完成上述过程后,即开始进行lfb检测;针对mcda
‑
crispr
‑
实时荧光检测,质粒浓度为1.0
×
103copies每个反应,mcda扩增温度为65℃,扩增时间为30min,在crispr
‑
cas12b剪切的同时检测实时荧光,检测时间至少持续20min。
[0072]
实验例3:特异性的研究
[0073]
研究了mcda
‑
crispr
‑
lfb和mcda
‑
crispr
‑
实时荧光检测两种方法的检测特异性,待检测的样本参见表3。本实验例采用最佳反应条件对多个样本进行了核酸检测。实验过程参见实施例1,结果参见图12
‑
14,只有b型或者c型hbv阳性样本才被成功检出,其他样本的检测结果均为阴性,说明本方案对目标物质b型或者c型的hbv的特异性强,符合应用要求。在图12a中,1的检测对象是表3中的1,2
‑
9的检测对象是表3中的3,10
‑
13的检测对象是表3中的5,14
‑
19的检测对象是表3中的6、2、7
‑
11,21
‑
29的检测对象是表3中的12
‑
20,30的检测对象是空白对照。在图12b中,1的检测对象是表3中的2,2
‑
9的检测对象是表3中的4,10
‑
13的检测对象是表3中的5,14
‑
20的检测对象是表3中的6、1、7
‑
11,21
‑
29的检测对象是表3中的12
‑
20,30的检测对象是空白对照。
[0074]
表3:实验用病原体信息(表中缩写含义为:atcc:美国典型培养物保藏中心;2
nd gzutcm:贵州中医大学第二附属医院;gzcdc:贵州省疾控中心;2
nd phgz:贵州省第二人民医院;p阳性,n阴性)
[0075][0076][0077]
实验例4:
[0078]
为进一步验证本方案的检测方法的准确性,发明人收集了114份临床疑似样本(疑似hbv感染的血清样本)。提取血清样本的dna后,参照实施例中的方法,采用最优条件进行检测。并同时对114份样本进行测序检测(委托dian medical laboratory center co.,ltd),以验证本方案的检测方法的准确性。实验结果参见表4,本方案的检测方法可准确反映出临床样本的被感染情况。
[0079]
表4:临床样本检测结果
[0080][0081]
对比例1:引物组合的选择
[0082]
为找到能够获得较好测试灵敏度和准确度的检测系统,发明人针对b型和c型的乙肝病毒的s基因的不同检测靶片段(用于mcda扩增的片段)设计了大量引物组合进行测试,现将部分实验过程中用到的引物组合的情况列举在表5(针对b型hbv)和表6(针对c型hbv)中。表5中第五套引物是表1中的引物组合,表6中的第三套引物是表2中的引物组合。使用表1和表2的引物组合分别进行mcda扩增实验,并采用实施例1的扩增方法(65℃),扩增同时进行实时的浊度检测,mcda扩增结果参见图15
‑
图19(针对b型hbv)、图20
‑
图24(针对c型hbv)。在图15
‑
图24中,浊度检测仪使用amplificatior模式,主要考察扩增效率。不同于图9和图10,在图9和图10中,浊度检测仪使用judgment模式,主要考察扩增时间。mcda扩增过程中会产生沉淀,例如,焦磷酸镁(dntp参与反应,失去焦磷酸根,焦磷酸根与扩增体系中的镁离子结合产生沉淀,而镁离子是dna聚合酶活性所必须的物质),故可以用浊度来表征mcda扩增进行的程度,此为本技术领域的惯用手段。针对图15
‑
24的实验结果,以及最大浊度值来判断引物组合的扩增效率,可见本方案的系统使用的引物组合的最大浊度值和出现最大浊度值的速度(扩增效率)均非常理想,其他引物组合均不能达到上述扩增效率。发明人尝试将扩增效果较好的表5中的第一套引物和表6中的第一套引物应用到实验例1的灵敏度检测中,发现使用两种引物的检测灵敏度分别为1
×
102copies每个反应,1
×
103copies每个反应。
[0083]
表5:针对b型hbv的引物设计
[0084][0085][0086]
表6:针对c型hbv的引物设计
[0087][0088]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。