1.本技术涉及一种吡柔比星的分离纯化方法,属于药物分离提纯技术领域。
背景技术:
2.吡柔比星,又名四氢吡喃阿霉素,为橙红色结晶性粉末,熔点188~192℃(分解),旋光度为 195
°
~ 215
°
(c=1mg/ml,氯仿),uv和可见光最大吸收(甲醇):234nm,252nm,290nm,498nm,531.5nm,580nm。易溶于氯仿、二氯甲烷、dmf,微溶于乙酸乙酯、乙醇或甲醇,难溶于水、正己烷或石油醚、乙醚。吡柔比星是半合成的蒽环类抗肿瘤抗生素,由多柔比星和二氢吡喃合成,能迅速进入癌细胞,通过抑制核酸合成阻止细胞分裂。给药后血中浓度迅速下降,很快分布至组织中,肺和脾中的浓度较多柔比星高,主要经胆汁排泄。对头颈部癌、乳腺癌、卵巢癌、子宫癌、白血病等有缓解作用。且对心脏、骨髓抑制的毒副作用较多柔比星小。其分子式为:c
32
h
37
no
12
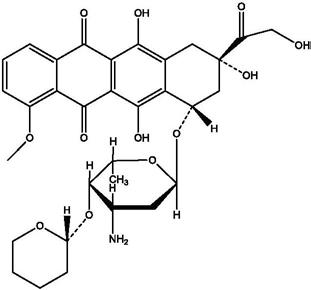
,分子量为:627.636,分子结构式:
[0003][0004]
吡柔比星的化学结构与多柔比星相近,是多柔比星氨基糖部分第4
′‑
oh与吡喃基发生加成反应的衍生物。多柔比星在吡喃化反应时,3,4
‑
二氢吡喃和4’位的羟基的反应会生成吡柔比星及其异构化产物,此异构化产物在总产物的比例约在30%左右,是吡柔比星合成反应中最大的杂质。同时此异构化产物与吡柔比星有非常相似的结构和理化性质,很难用常规方法去除。
[0005]
基于上述特性,研究吡柔比星的分离纯化技术具有重要价值。涉及针对吡柔比星的纯化技术及其专利及文献相对较少。其中专利cn101181280a提供了一种吡柔比星冻干制剂及其制备方法、专利cn101879144a提供了吡柔比星或盐酸吡柔比星脂质体冻干剂及其制备方法、专利cn101352418a提供了吡柔比星或盐酸吡柔比星脂质纳米粒及其制备方法,上述三篇专利所涉及的方法均为吡柔比星药物制剂的制备方法,并未提及吡柔比星的纯化方法。专利cn111675738a公开了一种吡柔比星的纯化方法,其采用的吡柔比星粗品要求质量含量65%以上,且涉及的粗品不含有异构体杂质,只含有多柔比星和多柔比星酮等杂质,通过萃取即可去除,没有借鉴意义。中国药科大学许建良等在西北药学杂志公开的《吡柔比星的分离与纯化》文献中提到了吡柔比星的纯化方法,该文献所提供的纯化工艺为硅胶层析柱纯化吡柔比星粗品,以二氯甲烷
‑
甲醇为洗脱液经过两次纯化,将含量35.7%的吡柔比星粗品纯化后得到纯度为99.6%的吡柔比星纯品。但采用硅胶分离纯化时,由于硅胶对吡柔
比星的氢键吸附力大,在洗脱过程中部分吡柔比星未能从硅胶上洗脱,导致吡柔比星的收率低,且需要进行两次的硅胶柱层析,溶剂消耗量大,同时由于硅胶吸附严重,无法重复利用,对环境污染比较严重。
[0006]
因此,如何进一步提高吡柔比星的纯度,是本领域技术人员所亟待解决的技术问题。
技术实现要素:
[0007]
根据本技术,提供了一种吡柔比星的分离纯化方法,通过采用二醇基键合硅胶作为分离纯化填料,明显提高了吡柔比星的纯度,异构体杂质含量在0.1%以下。
[0008]
本技术吡柔比星的分离纯化方法,至少包括以下步骤:
[0009]
步骤1、获得含有吡柔比星的样品的待处理溶液;
[0010]
步骤2、采用色谱分离纯化所述待处理溶液,得到吡柔比星纯品;
[0011]
所述色谱分离纯化中采用的色谱柱的填料为doil填料。
[0012]
可选地,所述待处理溶液的浓度为0.1mg/ml
‑
50mg/ml。
[0013]
优选地,所述待处理溶液的浓度为1mg/ml
‑
20mg/ml。
[0014]
具体地,所述待处理溶液的浓度下限可独立选自0.1mg/ml、2.5mg/ml、3mg/ml、3.5mg/ml、4mg/ml;所述待处理溶液的浓度上限可独立选自10mg/ml、20mg/ml、30mg/ml、40mg/ml、50mg/ml。
[0015]
可选地,所述待处理溶液采用含有吡柔比星的样品与溶剂i配制而成;
[0016]
所述溶剂i选自二氯甲烷、三氯甲烷、正己烷、正庚烷中的至少一种。
[0017]
可选地,所述含有吡柔比星的样品中,吡柔比星的质量含量为30%
‑
98%。
[0018]
具体地,所述含有吡柔比星的样品中,吡柔比星的质量含量下限可独立选自30%、38.1%、42.8%、45%、53.1%;吡柔比星的质量含量上限可独立选自60%、70%、80%、94.1%、98%。
[0019]
可选地,所述填料的粒径在5μm
‑
100μm。
[0020]
优选地,所述填料的粒径在25μm
‑
45μm。
[0021]
可选地,所述含有吡柔比星的样品的加入量为所述填料质量的0.1%
‑
15%。
[0022]
优选地,所述含有吡柔比星的样品的加入量为所述填料质量的1%
‑
10%。
[0023]
具体地,所述含有吡柔比星的样品的加入量下限可独立选自所述填料质量的0.1%、1%、5%、6%、7%、8%;所述含有吡柔比星的样品的加入量上限可独立选自所述填料质量的10%、11%、12%、13%、14%、15%。
[0024]
可选地,所述色谱分离纯化过程中,所采用的洗脱剂选自二氯甲烷、氯仿、正己烷、正庚烷、甲醇、乙醇、丙酮、乙酸乙酯中的至少一种。
[0025]
优选地,所述洗脱剂选自二氯甲烷和甲醇的混合溶液。
[0026]
可选地,所述色谱分离纯化过程中,洗脱速度为5ml/min
‑
500ml/min。
[0027]
优选地,所述洗脱速度为150ml/min
‑
300ml/min。
[0028]
具体地,所述洗脱速度的下限可独立选自5ml/min、10ml/min、50ml/min、100ml/min、150ml/min;所述洗脱速度的上限可独立选自200ml/min、250ml/min、300ml/min、400ml/min、500ml/min。
[0029]
可选地,所述步骤2中,采用tlc点板或hplc监测色谱分离纯化过程。
[0030]
具体地,在上样至色谱柱后,通过tlc点板或hplc监控有吡柔比星单点洗脱下来开始收集洗脱液;并在监测到有杂质洗脱下来时,停止收集。
[0031]
可选地,所述步骤2还包括:对所述色谱分离纯化得到的洗脱液进行浓缩、干燥。
[0032]
具体地,所述浓缩采用减压旋蒸浓缩。
[0033]
本技术对于浓缩、干燥的具体操作没有特殊要求,本领域技术人员可根据常规吡柔比星的操作要求选取合适的参数。具体地,本技术实施例中减压旋蒸浓缩操作的压力控制在
‑
0.01mpa以下,温度在25~35℃;干燥温度在25~35℃,干燥时间为2~6h。
[0034]
可选地,本技术吡柔比星的分离纯化方法,包括以下步骤:
[0035]
将含有吡柔比星的样品配制成上样液;
[0036]
将所述上样液上样至diol色谱柱中,进行分离纯化;
[0037]
采用tlc点板或hplc监控洗脱液,在有吡柔比星单点洗脱下来时,开始收集洗脱液;并在监测到有杂质洗脱下来时,停止洗脱液收集;
[0038]
对收集到的所述洗脱液进行浓缩,并对浓缩得到的固体进行(过滤、)干燥,得到所述吡柔比星的纯品。
[0039]
具体地,对收集到的所述洗脱液进行减压旋蒸浓缩,待有大量固体出现时停止操作;过滤浓缩产物,并对所得的固体进行干燥,得到所述吡柔比星的纯品。
[0040]
可选地,所述含有吡柔比星的样品选自市售吡柔比星或溶液固体、合成反应得到的含有吡柔比星的溶液或固体、合成反应后经萃取提纯得到的含有吡柔比星的溶液或固体中的至少一种。
[0041]
本技术中diol填料是指二醇基键合硅胶,又叫做二醇基化合物键合硅胶。
[0042]
本技术能产生的有益效果包括:
[0043]
1)本技术吡柔比星的分离纯化方法,填料中含有羟基官能团,相对于常规硅胶柱,分离纯化过程中填料对于吡柔比星的吸附性大大降低,容易被洗脱,提高了吡柔比星的收率,吡柔比星收率在75%以上。
[0044]
2)本技术吡柔比星的分离纯化方法,采用diol填料作为色谱分离纯化的填料,对样品的吸附小,用甲醇等适宜的溶剂即可使填料再生,可以实现多次重复再利用,相比于现有硅胶柱,更有利于环境。
附图说明
[0045]
图1是本技术实施例1洗脱液收集过程中的tlc点板图;
[0046]
图2是本技术实施例1吡柔比星样品纯化前的液相色谱图;
[0047]
图3是本技术实施例1得到吡柔比星纯品的液相色谱图;
[0048]
图4是本技术实施例2吡柔比星样品纯化前的液相色谱图;
[0049]
图5是本技术实施例2得到吡柔比星纯品的液相色谱图;
[0050]
图6是本技术实施例3吡柔比星样品纯化前的液相色谱图;
[0051]
图7是本技术实施例3得到吡柔比星纯品的液相色谱图;
[0052]
图8是本技术实施例3洗脱液收集过程中的tlc点板图。
具体实施方式
[0053]
下面结合实施例详述本技术,但本技术并不局限于这些实施例。
[0054]
如无特别说明,本技术的实施例中的原料均通过商业途径购买,吡柔比星原料为本技术人员所在单位自制。
[0055]
本技术采用岛津高效液相色谱仪(型号cbm
‑
20a)进行分析检测。
[0056][0057]
实施例1
[0058]
1、diol色谱柱装填:称取25μmdiol填料1kg,用1000ml二氯甲烷浸泡,搅拌均匀,湿法装进色谱柱中,通过降低筛板高度压实填料,制成diol色谱柱(φ95mm
×
250mm)。
[0059]
2、diol色谱柱平衡:用溶剂(二氯甲烷)5l,平衡色谱柱,平衡流速200ml/min。
[0060]
3、上样液制备:称取吡柔比星比星样品50g(质量含量42.8%,异构杂质38.2%),用溶剂(二氯甲烷)2l,搅拌溶解,得到吡柔比星上样液。
[0061]
4、样品上样:将吡柔比星上样液泵入diol色谱柱,上样流速为200ml/min。
[0062]
5、样品洗脱:用10l洗脱剂(二氯甲烷:甲醇900∶1)进行冲洗,洗脱流速200ml/min。如图1所示,采用tlc点板监控,有吡柔比星单点洗脱下来开始收集洗脱液;在tlc点板监控到有杂质洗脱下来时,停止收集。
[0063]
6、对收集到的洗脱液进行减压旋蒸浓缩,控制压力为
‑
0.06mpa,温度为35℃,当有大量固体出现时停止操作。过滤浓缩物,并对得到的固体在35℃下真空干燥4h,得到吡柔比星纯品。纯化前后的液相色谱图如图2、3所示,色谱图所对应的液相色谱数据如表1a、1b所示。
[0064]
表1a
[0065]
峰#保留时间面积高度面积%理论塔板#13.1295437389130.1815196.22524.319453371638326115.1333329.29836.084137723120900.4606403.43846.685325371124261.086165.71357.3201282750188340742.8176249.10168.0031144202769124438.1925520.147710.355199008128200.66410860.669827.8555883315100.19613256.312934.99714930719460.4986056.4901040.03823108225690.7715559.365总计 299589392010184100.000 [0066]
表1b
[0067]
峰#保留时间面积面积%高度理论塔板#13.657172840.08926876094.85724.04791830.04715109254.37934.60374890.03811239726.070
46.9751940366399.65412218544083.16958.14673600.03878115459.26869.39236450.01945922888.954712.69561300.03144217971.357815.655163650.0846688600.446总计 19471118100.0001229524 [0068]
吡柔比星回收率结果见表1c:
[0069]
表1c
[0070]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品50.0042.838.2
‑‑
纯化后样品17.0899.60.0479.5
[0071]
实施例2
[0072]
采用与实施例1相同的diol色谱柱和洗脱方法,区别在于:
[0073]
称取吡柔比星固体60g,质量含量53.1%,异构杂质质量含量39.8%,用溶剂(二氯甲烷)2l,搅拌溶解。diol色谱柱用溶剂(二氯甲烷)5l平衡,平衡流速200ml/min,后对色谱柱进行上样,上样流速200ml/min。上样完毕后,用洗脱剂(二氯甲烷:乙醇体积比为90∶1)冲洗diol色谱柱,洗脱流速200ml/min。hplc检测收集吡柔比星单点组分溶液(即洗脱液)。将洗脱液减压旋蒸浓缩,控制压力为
‑
0.07mpa,温度为32℃,当有大量固体出现时停止操作。过滤浓缩物,并对得到的固体在32℃下真空干燥4h,得到吡柔比星纯品。纯化前后的液相色谱图如图4、图5所示,色谱图所对应的液相色谱数据如表2a、2b所示。
[0074]
表2a
[0075]
峰#保留时间面积高度面积%理论塔板#11.488127393180.02325.42624.0502447148480.0451959.62434.16692917162250.1703248.48044.27187687173110.160609.55654.397224683293140.410869.70664.6461115837909322.0363463.48974.889274290344740.5002065.51585.08611059341100922.0185967.58296.385584035543131.0669509.756106.99529106116135533553.1032215.023118.11421840914102436139.8482946.875129.69320272087350.3705214.1531323.19613875822120.2533503.536总计 548111002748470100.000 [0076]
表2b
[0077]
峰#保留时间面积高度面积%理论塔板#
12.74927591640.047478.65523.34784180.00110431.98034.02927624140.0477959.18244.55150177670.0859677.22955.183982440.0173065.84865.61114081070.0249032.47177.096590680851573599.6418556.43688.21223602600.04017086.584912.93317301260.02919270.2431015.542811260.0140.0001115.82333831860.05715641.067总计 5928103517846100.000 [0078]
吡柔比星回收率结果见表2c:
[0079]
表2c
[0080]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品60.0053.139.8
‑‑
纯化后样品24.999.60.0477.8
[0081]
实施例3
[0082]
采用与实例1相同的diol色谱柱和洗脱方法,其区别在于:
[0083]
称取多柔比星80g,通过吡喃化反应得到含有吡柔比星的反应溶液,hplc检测吡柔比星含量38.1%,异构化杂质含量29.5%,多柔比星含量13.2%。反应液加水后,用二氯甲烷3l萃取,无水硫酸钠干燥,得到吡柔比星浓度为10mg/ml的上样液。diol色谱柱用溶剂(二氯甲烷)5l平衡,流速200ml/min;然后后对diol色谱柱进行上样,上样流速为200ml/min。上样完毕后,用洗脱剂(二氯甲烷乙醇体积比为90∶1)冲洗色谱柱,洗脱流速200ml/min。hplc检测收集吡柔比星单点组分溶液(即洗脱液)。将洗脱液减压旋蒸浓缩,控制压力为
‑
0.06mpa,温度为30℃,当有大量固体出现时停止操作。过滤浓缩物,并对得到的固体30℃下真空干燥4h,得到吡柔比星纯品。纯化前后的液相色谱图如图6、图7所示,色谱图所对应的液相色谱数据如表3a、3b所示。
[0084]
表3a
[0085]
峰#保留时间面积面积%高度理论塔板#13.7233834912.046284141776.30424.296248253513.2472829935778.24234.8762075711.108162463200.83045.192169230.090242710898.12256.0915766313.077598188880.21966.322547410.292666264.92677.009714193238.1105740856806.45287.449868420.4631042918835.03997.855553197329.5194273527383.713
109.637113230.0605734122.6071110.2322783691.485125907078.8591211.647337210.180226213014.0771314.1241246410.66552408451.5291425.3227950634.2434756787.2251533.8513503101.86948096193.3491639.4715205202.77859844636.8631747.4301437410.7679312105.427总计18740326100.0001445570
[0086]
表3b
[0087]
峰#保留时间面积高度面积%理论塔板#12.75218711370.0111077.29323.04121774830.0128256.63633.70112611770.0075754.732,44.07926663770.0157656.85254.6231431421620.0819510.99867.15217638700107763899.7394122.31878.04460306480.03416358.63988.42560666300.03415690.56198.96214841380.00815519.459109.74341724050.02419345.8781111.51418761290.01114006.4981213.35322001350.01216730.4941316.36920911170.01217313.398总计 176849091083177100.000 [0088]
吡柔比星回收率结果见表3c:
[0089]
表3c
[0090]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品80.0038.129.5
‑‑
纯化后样品23.4199.70.0376.5
[0091]
实施例4
[0092]
采用与实例1相同的diol色谱柱和洗脱方法,其区别在于:
[0093]
称取吡柔比星固体70g,含量94.1%,异构杂质质量含量2.3%,用溶剂(二氯甲烷)3l,搅拌溶解。diol色谱柱用溶剂(二氯甲烷)5l平衡,平衡流速200ml/min,后对diol色谱柱进行上样,流速200ml/min。上样完毕后,用洗脱剂(二氯甲烷:乙醇体积比为85∶1)冲洗色谱柱,洗脱流速200ml/min。tlc检测收集吡柔比星单点组分溶液(即洗脱液)。将洗脱料液减压旋蒸浓缩,控制压力为
‑
0.07mpa,温度为28℃,当有大量固体出现时停止操作。过滤浓缩物,并对得到的固体在28℃下真空干燥4h,得到吡柔比星纯品61.17g。hplc检测吡柔比星纯度99.6%,单杂小于0.1%,异构化杂质0.03%。
[0094]
吡柔比星回收率结果见表4:
[0095]
表4
[0096]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品70.0094.12.3
‑‑
纯化后样品61.1799.60.0392.5
[0097]
对比例1
[0098]
国药科大学的许建良等在西北药学杂志公开的《吡柔比星的分离与纯化》文献中提到了吡柔比星的纯化方法,该文献所提供的纯化工艺为硅胶层析柱纯化吡柔比星粗品,以二氯甲烷
‑
甲醇为洗脱液经过两次纯化。采用其公开的方法进行吡柔比星的纯化,具体操作步骤如下:
[0099]
称取200
‑
300目硅胶100g,用100ml二氯甲烷浸泡,湿法装入玻璃柱(φ3.5cm
×
20cm)中,备用。称取吡柔比星比星样品5g(质量含量42.8%,异构杂质含量38.2%),用200ml二氯甲烷溶解。对色谱柱进行上样,流速10ml/min。上样完毕,用洗脱剂(二氯甲烷:甲醇体积比为9:1)洗脱,洗脱流速10ml/min。tlc检测收集吡柔比星组分溶液。将洗脱料液减压旋蒸浓缩,控制压力为
‑
0.06mpa,温度为30℃,当有大量固体出现时停止操作。过滤浓缩物,滤饼在30℃下真空干燥4h,得到固体1.51g,纯度91.2%。
[0100]
对固体进一步分离纯化:称取200
‑
300目硅胶40g,用100ml二氯甲烷浸泡,湿法装入玻璃柱(φ2.5cm
×
20cm)中,备用。取上步得到的固体(质量含量91.2%),用100ml二氯甲烷溶解。对色谱柱进行上样,上样流速10ml/min。上样完毕,用洗脱剂(二氯甲烷:甲醇体积比为9∶1)洗脱,洗脱流速10ml/min。tlc检测收集吡柔比星组分溶液。将洗脱料液减压旋蒸浓缩,将洗脱料液减压旋蒸浓缩,控制压力为
‑
0.06mpa,温度为30℃,当有大量固体出现时停止操作。过滤浓缩物,滤饼在30℃下真空干燥4h,得到固体1.03g,纯度98.5%,异构化杂质0.23%。
[0101]
吡柔比星回收率结果见表5:
[0102]
表5
[0103]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品5.0042.838.2
‑‑
纯化后样品1.0398.50.23447.4
[0104]
对比例2
[0105]
称取25
‑
45μm diol填料50g,用100ml二氯甲烷浸泡,搅拌均匀,湿法装进色谱柱中,通过降低筛板高度压实填料,制成diol色谱柱(φ3.5cm
×
10cm)。
[0106]
用溶剂(二氯甲烷)100ml,平衡色谱柱,平衡流速10ml/min。
[0107]
称取吡柔比星比星样品5g(质量含量42.8%,异构杂质含量38.2%),用溶剂(二氯甲烷)200ml,搅拌溶解。
[0108]
对色谱柱进行上样,上样流速10ml/min。用1l洗脱剂(二氯甲烷:甲醇体积比为900∶1)溶剂进行冲洗,洗脱流速10ml/min。tlc点板检测收集吡柔比星单点。将洗脱料液减压旋蒸浓缩,将洗脱料液减压旋蒸浓缩,控制压力为
‑
0.06mpa,温度为30℃,当有大量固体出现时停止操作。过滤浓缩物,滤饼在30℃下真空干燥4h,得到吡柔比星纯品。
[0109]
吡柔比星回收率结果见表6:
[0110]
表6
[0111]
名称质量(g)纯度(%)异构化杂质(%)回收率(%)纯化前样品5.0042.838.2
‑‑
纯化后样品1.7299.70.0480.1
[0112]
以上所述,仅是本技术的几个实施例,并非对本技术做任何形式的限制,虽然本技术以较佳实施例揭示如上,然而并非用以限制本技术,任何熟悉本专业的技术人员,在不脱离本技术技术方案的范围内,利用上述揭示的技术内容做出些许的变动或修饰均等同于等效实施案例,均属于技术方案范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。