大鼠血浆中covid-19潜在治疗药物的检测方法
技术领域
1.本发明涉及药物分析领域,具体涉及大鼠血浆中covid-19潜在治疗药物的检测方法。
背景技术:
2.2019年末,由2019新型冠状病毒(2019-ncov)感染导致的新型冠状病毒肺炎(corona virus disease 2019,covid-19)疫情暴发。该病毒传播迅速,传染性强,人群普遍易感,疫情很快成为全球关注的焦点,而在全球范围内,尚无批准的针对covid-19的治疗方法,抗新冠病毒药物的研发迫在眉睫。
3.根据已上市药物以及相关的数据库进行了药物筛选,迅速发现了30种可能对covid-19有治疗作用的药物,其中包括瑞德西韦(remdesivir)、沙奎那韦(saquinavir)、洛匹那韦(lopinavir)、卡非佐米(carfilzomib)、利托那韦以及磷酸氯喹(chloroquine phosphate)等药物,此类药物大多可以阻止病毒rna合成以抑制病毒复制,相关细胞水平的试验表明此类药物可以有效的在细胞水平上抑制covid-19的感染,但其在人体上的作用还有待临床验证。根据国家食品药品监督管理总局规定,新药在临床验证前需相应的非临床试验数据支持。因此,有关针对covid-19潜在治疗药物的非临床安全评价工作尤为重要,其在不同动物模型中药物代谢以及毒理的方法准确性是其在进入临床试验中的重要安全保障。
4.目前,针对新冠病毒的相关潜在治疗药物主要是小分子药物,而小分子药物(分子量200~700)的代谢常用色谱法进行测定,方法开发过程中主要对所使用的溶剂和试剂、基质以及配制和处理步骤进行筛选,从而形成精确测定的方法。因此,covid-19潜在治疗药物临床前检测方法的开发至关重要。
技术实现要素:
5.本发明提供一种大鼠血浆中covid-19潜在治疗药物的检测方法。本发明的方法能够快速、简便地检测大鼠血浆中covid-19潜在治疗药物。
6.本发明是通过以下方案来解决技术问题的:
7.一种大鼠血浆中covid-19潜在治疗药物的检测方法,其包含以下步骤:
8.采用液相色谱-质谱联用法,对经处理的大鼠血浆进行分析检测,即可;
9.所述大鼠血浆的稳定剂为敌敌畏;
10.所述covid-19潜在治疗药物为(s)-2-(((s)-(((2r,3s,4r,5r)-5-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-5-氰基-3,4-二羟基四氢呋喃-2-基)甲氧基)(苯氧基)磷酰基)氨基)丙酸-2-乙基丁基酯。
[0011]
本发明中,所述大鼠血浆是指仅添加稳定剂的大鼠血浆;经过处理的大鼠血浆成为经处理的大鼠血浆。本发明中,所述大鼠血浆一般是指大鼠edta-k2血浆。
[0012]
本发明中,所述大鼠可为sd大鼠。
[0013]
本发明中,所述液相色谱-质谱联用法中的液相色谱的柱温较佳地为20~30℃,例如25℃。
[0014]
本发明中,所述液相色谱-质谱联用法中的液相色谱的进样量可为1~10μl,例如2μl。
[0015]
本发明中,较佳地,所述经处理的大鼠血浆采用蛋白沉淀法对所述大鼠血浆进行处理。所述蛋白沉淀法采用的蛋白沉淀剂较佳地为甲醇或乙腈。
[0016]
其中,所述处理可包括:将所述大鼠血浆、内标物和所述蛋白沉淀剂混合后,取上清液即可。
[0017]
所述内标物可为甲苯磺丁脲。
[0018]
本发明中,所述液相色谱-质谱联用法中的液相色谱的设备可为本领域常规。所述液相色谱-质谱联用法中的液相色谱的色谱柱固定相可为十八烷基键合硅胶;例如,poroshell 120sb-c18。所述色谱柱的规格可为本领域常规,例如2.1
×
50mm,2.7μm。
[0019]
本发明中,所述液相色谱-质谱联用法中的液相色谱采用的流动相可为极性有机溶剂和甲酸水溶液,所述甲酸水溶液中甲酸的体积百分含量为0.01%~0.5%,例如0.1%的甲酸水溶液,所述甲酸水溶液中甲酸体积百分含量的计算方法为甲酸的体积占水的体积的比例。
[0020]
其中,所述极性有机溶剂较佳地为甲醇或乙腈。
[0021]
其中,所述液相色谱-质谱联用法中的液相色谱可采用梯度洗脱,所述梯度洗脱时所述甲酸水溶液与所述极性有机溶剂的体积比可为95:5~5:95。
[0022]
其中,所述梯度洗脱中,所述流动相比例随时间的变化范围可如表1所示:
[0023]
表1
[0024]
时间(min)甲酸水溶液(%)(流动相a)极性有机溶剂(%)(流动相b)0~1.59551.5(不包括1.5)~2.55952.5(不包括2.5)~2.515
→
9595
→
52.5(不包括2.51)~3955
[0025]
其中,所述的梯度洗脱程序为:从初始状态到1.5min的时间段内,流动相a的体积百分比为95%,流动相b的体积百分比为5%,在1.5min到2.5min的时间段内,流动相a的体积百分比改变为5%,流动相b的体积百分比改变为95%;在2.5min到2.51min的时间段内,流动相a的体积百分比逐渐升高到95%,流动相b的体积百分比逐渐降低到5%;在2.51min到3.00min的时间段内,流动相a的体积百分比维持在95%,流动相b的体积百分比维持在5%。(上述流动相a和b的体积百分比以流动相a和b的总体积为基准)。
[0026]
其中,所述流动相的总流速为0.5ml/min。
[0027]
本发明中,所述液相色谱-质谱联用法中的质谱设备可为本领域常规,例如型号为ab sciex triple quad
tm 4500的质谱仪。
[0028]
本发明中,较佳地,对所述大鼠血浆中covid-19潜在治疗药物检测之前,还需分析所述检测方法的专属性,分析所述检测方法的专属性的步骤包括:
[0029]
步骤(1)、分别配制一定浓度梯度的所述covid-19潜在治疗药物的标准品工作液和质控工作液,再配制一定浓度的内标工作液;
[0030]
步骤(2)、将所述标准品工作液和所述质控工作液分别与大鼠空白血浆混合,即得标准品样品溶液和质控样品溶液;
[0031]
步骤(3)、样品溶液处理步骤:分别将所述标准品样品溶液和所述质控样品溶液,与所述内标工作液混合后,取上清液;
[0032]
步骤(4)、将所述上清液进样,进行液相色谱-质谱检测,测得所述covid-19潜在治疗药物与所述内标工作液中的内标物的峰面积比;
[0033]
步骤(5)、根据所述标准品工作液中的covid-19潜在治疗药物与所述内标工作液中的内标物的峰面积比和相应的所述标准品工作液的浓度,得到回归方程;
[0034]
步骤(6)、将步骤(4)中的峰面积比代入步骤(5)中得到的回归方程,计算得回算浓度;当至少67%的质控样品所述回算浓度(每个浓度水平至少50%的样品)与其相应的实际值的偏差在
±
15.0%之内时,所述检测方法的专属性良好。
[0035]
步骤(1)中,所述标准品工作液的配制方法可包括下列步骤:将所述covid-19潜在治疗药物代谢物与第一稀释液混合,即得标准品储备液;再将所述标准品储备液与第二稀释液混合,即得一定浓度梯度的所述标准品工作液。
[0036]
步骤(1)中,所述质控工作液的配制方法可包括下列步骤:将所述covid-19潜在治疗药物代谢物与所述第一稀释液混合,即得质控储备液;将所述质控储备液与所述第二稀释液混合,即得一定浓度梯度的所述质控工作液。
[0037]
步骤(1)中,所述内标工作液的配制方法可包括下列步骤:将所述甲苯磺丁脲与所述第一稀释液混合,即得内标储备液;将所述内标储备液与所述第二稀释液混合,即得一定浓度的所述内标工作液。
[0038]
其中,所述第一稀释液可为dmso。所述第二稀释液可为30%~70%甲醇水溶液。
[0039]
步骤(1)中,所述内标工作液的浓度可为1000ng/ml。
[0040]
步骤(1)中,所述标准品工作液的浓度梯度可依次为80ng/ml、200ng/ml、1000ng/ml、2000ng/ml、5000ng/ml、10000ng/ml、20000ng/ml和80000ng/ml。
[0041]
步骤(1)中,所述质控工作液的浓度梯度可依次为240ng/ml、3000ng/ml和60000ng/ml。
[0042]
步骤(2)中,所述标准品样品溶液的浓度可依次为4ng/ml、10ng/ml、50ng/ml、100ng/ml、250ng/ml、500ng/ml、1000ng/ml和4000ng/ml。
[0043]
步骤(2)中,所述质控样品溶液的浓度可依次为12ng/ml、150ng/ml和3000ng/ml。
[0044]
在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
[0045]
本发明所用试剂和原料均市售可得。
[0046]
本发明的积极进步效果在于:
[0047]
1)本发明中的covid-19潜在治疗药物在sd大鼠血浆样品中的检测方法,简单、用时短且易操作;从而分析covid-19潜在治疗药物代谢物在大鼠体中的药代/毒代动力学。
[0048]
2)本发明的方法所需的样本进样量小,所需的分析时间较短;本发明开发的处理方式使标准曲线线性精准,保证了检测的准确性和可靠性。
附图说明
[0049]
图1为标准曲线中covid-19潜在治疗药物的定量下限(即4ng/ml)图谱。
[0050]
图2为标准曲线中定量下限甲苯磺丁脲的(即50ng/ml)图谱。
[0051]
图3为标准曲线中covid-19潜在治疗药物的定量上限(也就是4000ng/ml)图谱。
[0052]
图4为标准曲线中定量上限甲苯磺丁脲的(即50ng/ml)图谱。
[0053]
图5为covid-19潜在治疗药物标准曲线图。
具体实施方式
[0054]
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
[0055]
以下实施例中的covid-19潜在治疗药物为(s)-2-(((s)-(((2r,3s,4r,5r)-5-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-5-氰基-3,4-二羟基四氢呋喃-2-基)甲氧基)(苯氧基)磷酰基)氨基)丙酸-2-乙基丁基酯。
[0056]
实施例大鼠血浆中covid-19潜在治疗药物检测方法的专属性验证
[0057]
1、试剂的配制
[0058]
流动相a(mpa),0.1%甲酸水溶液:取1000ml h2o中加入1ml甲酸(fa)于溶剂瓶中,混匀,室温保存有效期1个月。
[0059]
流动相b(mpb),甲醇(meoh):取1000ml meoh于溶剂瓶中,室温保存有效期3个月。
[0060]
强洗溶液(snw),meoh:(乙腈)acn:异丙醇(ipa):二甲基亚砜(dmso)=1:1:1:1,v/v/v/v:取500ml meoh,500ml acn,500ml ipa,500ml dmso,混匀。室温保存,有效期3个月。
[0061]
弱洗溶液(wnw),meoh:h2o=1:1,v/v:取1000ml meoh,1000ml h2o,混匀。室温保存,有效期3个月。
[0062]
沉淀剂&内标稀释液:meoh。
[0063]
取1000ml meoh。室温保存,有效期1个月。
[0064]
第二稀释液:meoh:h2o=1:1,v/v。
[0065]
取500ml meoh,500ml h2o,混匀。室温保存,有效期3个月。
[0066]
第一稀释液:dmso。
[0067]
取50ml dmso。室温保存,有效期3个月。
[0068]
2、标准品工作液和质控工作液的配制
[0069]
储备液和工作液均储存于超低温冰箱(-70~-90℃)中。
[0070]
2.1标准品储备液的配制
[0071]
精密称取适量covid-19潜在治疗药物标准品于透明样品瓶中,加入适量dmso溶解、摇匀,配制成浓度为1.000mg/ml的标准品储备液。(covid-19潜在治疗药物的质量折算因子为0.992(由于covid-19潜在治疗药物标准品本身纯度不是100%或带有水或盐,dmso的体积通过标准品储备液的浓度以及经折算的covid-19潜在治疗药物质量计算得到,其中,所述的经折算的covid-19潜在治疗药物的质量通过所称取的covid-19潜在治疗药物质量乘以covid-19潜在治疗药物的质量折算因子0.992计算得到)。
[0072]
2.2标准品工作液&sst(系统适应性样品)工作液的配制(稀释液:meoh:h2o=1:1,
v/v)
[0073]
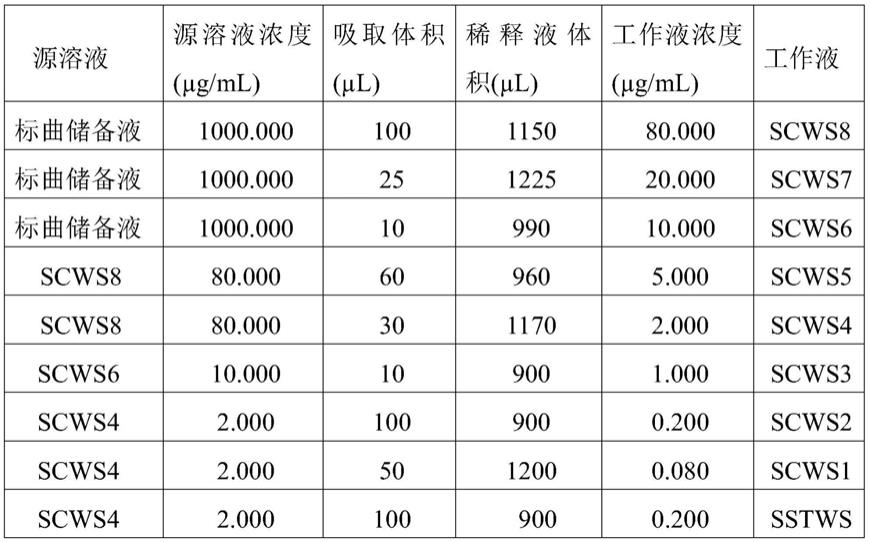
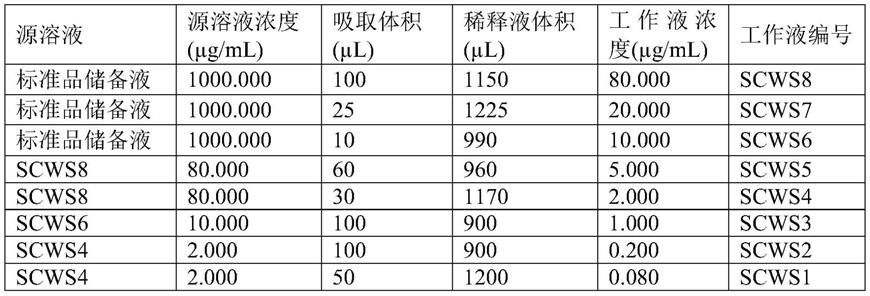
使用标准品储备液,依照下表2配制,得到标准品工作液&sst工作液:
[0074]
表2
[0075][0076][0077]
2.3标准品样品溶液的配制
[0078]
使用表2的工作液,依照下表3配制,得到标准品样品溶液,表中血浆为体积比按敌畏:空白血浆等于2:5的比例混合所地(例如40微升ddv:100微升空白血浆)
[0079]
表3
[0080][0081]
标准品样品溶液储存于超低温冰箱(-70~-90℃)中。
[0082]
2.4质控储备液的配制
[0083]
与标准品储备液相同。
[0084]
2.5质控工作液的配制(稀释液:meoh:h2o=1:1,v/v)
[0085]
使用质控储备液,依照下表4配制,得到质控工作液。
[0086]
表4
[0087][0088]
2.6质控样品溶液的配制
[0089]
使用质控工作液,依照下表5配制,得到质控样品溶液。表中血浆为体积比按敌畏:
空白血浆等于2:5的比例混合所得(例如40微升ddv:100微升空白血浆)。
[0090]
表5
[0091][0092][0093]
质控样品溶液储存于超低温冰箱(-70~-90℃)中。
[0094]
2.7内标储备液的配制
[0095]
精密称取适量甲苯磺丁脲于透明样品瓶中,加入适量dmso溶解、摇匀,配制成浓度为1.000mg/ml的内标储备液。(甲苯磺丁脲的质量折算因子为0.999,由于甲苯磺丁脲标准品本身纯度不是100%或带有水或盐,dmso的体积通过标准品储备液的浓度以及经折算的甲苯磺丁脲质量计算得到,其中,所述的经折算的甲苯磺丁脲的质量通过所称取的甲苯磺丁脲质量乘以甲苯磺丁脲的质量折算因子0.992计算得到)。
[0096]
2.8内标工作液的配制(稀释液:meoh:h2o=1:1)
[0097]
使用内标储备液,依照下表6配制,得到内标工作液:
[0098]
表6
[0099][0100]
3、进样样品前处理步骤
[0101]
1)样品涡旋(如果样品需要融化,在室温融化后再涡旋);
[0102]
2)吸取20μl样品(包括std、qc、db、carryover、blank)转移至96孔板或聚丙烯离心管中;其中,std对应表3样品;qc对应表5样品;db:不含待测物不含内标物;carryover:不含待测物;blank:不含待测物仅含内标物。
[0103]
3)向所有样品中加入20μl内标工作液(50%甲醇中有1000.000ng/ml甲苯磺丁脲);
[0104]
4)涡旋混匀后,向所有样品中加入160μlmeoh,作为蛋白沉淀剂;
[0105]
5)涡旋混匀,在4℃,4000rpm条件下离心10min;
[0106]
6)取离心后的上清液100μl至96孔板或聚丙烯离心管中,封膜,1000rpm下涡旋混匀10min;进样分析。
[0107]
图1和图2为std1样品进样分析所测;图3和图4为std8样品进样分析所测;图1~图4均表明在本发明标准曲线中的浓度均可通过色谱-质谱联用法进行检测。
[0108]
4、采用液相色谱串联质谱法(lc-ms/ms)检测大鼠血浆中的covid-19潜在治疗药物:
[0109]
其中液相色谱条件为:
[0110]
进样量:2μl;
[0111]
色谱柱:poroshell 120sb-c18,2.1
×
50mm,2.7μm,agilent;
[0112]
柱温:25℃;
[0113]
采用流动相a和流动相b进行梯度洗脱;
[0114]
运行时间:3.0min
[0115]
表7
[0116][0117]
其中,所述的梯度洗脱程序为:从初始状态到1.5min的时间段内,流动相a的体积百分比为95%,流动相b的体积百分比为5%,在1.5min到2.5min的时间段内,流动相a的体积百分比改变为5%,流动相b的体积百分比改变为95%;在2.5min到2.51min的时间段内,流动相a的体积百分比逐渐升高到95%,流动相b的体积百分比逐渐降低到5%;在2.51min到3.00min的时间段内,流动相a的体积百分比维持在95%,流动相b的体积百分比维持在5%。(上述流动相a和b的体积百分比以流动相a和b的总体积为基准)。
[0118]
洗针程序:冲洗类型:仅外部;
[0119]
冲洗模式:抽吸前后,浸入时间:2s;
[0120]
冲洗泵方式:冲洗泵,然后停止,时间:2s;
[0121]
冲洗设置:冲洗速度:35μl/s;
[0122]
冲洗体积:1000μl;
[0123]
测量管路吹扫量:100μl
[0124]
质谱条件为:
[0125]
仪器型号:ab sciex triple quadtm 4500
[0126]
离子源:esi
[0127]
离子化模式:正离子
[0128]
表8mrm离子对
[0129]
分析物q1质荷比q3质荷比扫描间隔(ms)covid-19潜在治疗药物603.300402.00150甲苯磺丁脲271.100154.800150
[0130]
表9质谱仪仪器参数
[0131]
参数covid-19潜在治疗药物甲苯磺丁脲离子化电压(v)55005500温度(℃)500500碰撞气(psi)99气帘气(psi)2020喷雾气(psi)5050辅助气(psi)4040去簇电压(v)9350入口电压(v)1010
碰撞能(v)2524碰撞室出口电压(v)1110
[0132]
5、分析批接收标准和标准曲线回归方法
[0133]
5.1回归方法
[0134]
提取mrm色谱图,拟合标准曲线,标准曲线以标准品工作液浓度为横坐标,以标准品工作液与内标峰面积比值为纵坐标,设置权重为1/x2,忽略原点,拟合线性标准曲线。以分析物峰面积与内标峰面积比对标准曲线中分析物的理论浓度进行线性最小二乘法回归计算,以所得回归方程计算样品中分析物的实测浓度。
[0135]
样品中分析物的实测浓度由以下回归方程计算:
[0136]
y=ax b
[0137]
其中,y=分析物与内标峰面积比
[0138]
a=标准曲线之斜率
[0139]
x=分析物浓度(单位ng/ml)
[0140]
b=标准曲线之截距(权重因子为1/x2)
[0141]
4.2分析批接收标准
[0142]
1)标准曲线各浓度点的回算值与标示值之间的偏差应在
±
15.0%范围内(定量下限处的偏差在
±
20.0%范围内)。
[0143]
2)至少75%的标准曲线样品,且每个浓度点至少50%的样品应符合接受标准。
[0144]
3)回归方程的相关系数(r2)必须大于等于0.98。
[0145]
4)当至少67%的质控样品结果(每个浓度至少50%)与它们相应标示值的偏差在
±
15.0%之内时,该分析批认为可接受。
[0146]
结果如图3所示(根据表3样品所测),标准曲线回归方程为:y=0.000958x 0.000926(r=0.9968,r2>0.98),标准曲线如图5所示。标准品样品溶液、质控样品溶液与标示值回算偏差结果如表10、表11所示,满足分析批接受标准。综上,本方法可以用于测定sd大鼠edta-k2血浆中的分析物(即为covid-19潜在治疗药物)的浓度。
[0147]
表10
[0148][0149]
表11
[0150]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。