1992326:581
‑
8)。
10.目前批准的ms疗法主要是免疫调节,并且通常对cns修复没有直接影响。虽然通常在较年轻患者中在ms病程的早期会发生一定程度的由少突胶质细胞所致的轴突髓鞘再生,但修复cns的能力最终会丧失,从而导致不可逆的组织损伤和疾病相关残疾的增加。因此,需要增强cns脱髓鞘疾病(例如ms和视神经炎)的髓鞘再生和神经轴突保护的额外疗法。
技术实现要素:
11.本公开部分涉及含有抗lingo
‑
1抗体或其lingo
‑
1结合片段的药物组合物及其在治疗cns脱髓鞘疾病(诸如多发性硬化症和视神经炎)中的用途。
12.在一个方面中,本公开的特征在于一种药物组合物,该药物组合物包含抗lingo
‑
1抗体或其lingo
‑
1结合片段、精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)和组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。
13.在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含免疫球蛋白重链可变结构域(vh)和免疫球蛋白轻链可变结构域(vl),该vh和该vl包含li81的cdr。在一些情况下,li81的六个cdr包含以下或由以下组成:seq id no:6(vh
‑
cdr1)所示的氨基酸序列;seq id no:7(vh
‑
cdr2)所示的氨基酸序列;seq id no:8(vh
‑
cdr3)所示的氨基酸序列;seq id no:14(vl
‑
cdr1)所示的氨基酸序列;seq id no:15(vl
‑
cdr2)所示的氨基酸序列;和seq id no:16(vl
‑
cdr3)所示的氨基酸序列。
14.在一些实施方案中,本发明提供一种药物组合物,该药物组合物包含抗lingo
‑
1抗体或其lingo
‑
1结合片段、组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合),和至少一种选自由脯氨酸(例如,游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合)和甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合)组成的组的额外赋形剂,其中抗lingo
‑
1抗体或lingo
‑
1结合片段包含免疫球蛋白重链可变结构域(vh)和免疫球蛋白轻链可变结构域(vl),该vh和该vl分别包含:(a)vh互补决定区(cdr),其中vh
‑
cdr1包含seq id no:6所示的氨基酸序列;vh
‑
cdr2包含seq id no:7所示的氨基酸序列;并且vh
‑
cdr3包含seq id no:8所示的氨基酸序列;以及(b)vl cdr,其中vl
‑
cdr1包含seq id no:14所示的氨基酸序列;vl
‑
cdr2包含seq id no:15所示的氨基酸序列;并且vl
‑
cdr3包含seq id no:16所示的氨基酸序列,并且其中该组合物的ph是约6.0至约7.0。在一些实施方案中,该组合物进一步包含精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐)。
15.在一些实施方案中,该组合物包含浓度为约50mg/ml至约300mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些实施方案中,该组合物包含浓度为约100mg/ml至250mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在其他实施方案中,该组合物包含浓度为约150mg/ml至225mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在其他实施方案中,该组合物包含浓度为175mg/ml至220mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在某些实施方
案中,该组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。
16.在一些实施方案中,该组合物进一步包含精氨酸(例如,arg hcl)。在一些实施方案中,该组合物进一步包含浓度为约50mm至约250mm的精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐)。在其他实施方案中,该组合物包含浓度为约70mm至约170mm的arg hcl。在其他实施方案中,该组合物包含浓度为约75mm至约175mm的arg hcl。在某些实施方案中,该组合物包含浓度为约80mm的arg hcl。在某些实施方案中,该组合物包含浓度为约100mm的arg hcl。在某些实施方案中,该组合物包含浓度为约120mm的arg hcl。在某些实施方案中,该组合物包含浓度为约140mm的arg hcl。在一些实施方案中,该组合物包含浓度为约160mm的arg hcl。
17.在一些实施方案中,该组合物进一步包含聚山梨醇酯
‑
80(ps80)。在一些实施方案中,该组合物包含浓度为约0.01%至约0.1%的ps80。在其他实施方案中,该组合物包含浓度为约0.03%至约0.08%的ps80。在某些实施方案中,该组合物包含浓度为约0.04%的ps80。在某些实施方案中,该组合物包含浓度为约0.05%的ps80。在某些实施方案中,该组合物包含浓度为约0.06%的ps80。
18.在一些实施方案中,该组合物进一步包含泊洛沙姆188。在一些实施方案中,该组合物包含浓度为约0.01%至约0.1%的泊洛沙姆188。在其他实施方案中,该组合物包含浓度为约0.03%至约0.08%的泊洛沙姆188。在某些实施方案中,该组合物包含浓度为约0.04%的泊洛沙姆188。在某些实施方案中,该组合物包含浓度为约0.05%的泊洛沙姆188。在某些实施方案中,该组合物包含浓度为约0.06%的泊洛沙姆188。
19.在一些实施方案中,该组合物包含组氨酸作为赋形剂。在某些实施方案中,该组合物包含浓度为约5mm至约30mm的组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。在某些实施方案中,该组合物包含浓度为约10mm至约30mm的组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。在某些实施方案中,该组合物包含浓度为约15mm至约25mm的组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。在某些实施方案中,该组合物包含浓度为约20mm的组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。
20.在一些实施方案中,该组合物进一步包含甲硫氨酸(如游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合)作为赋形剂。在一些实施方案中,甲硫氨酸(如游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合)的浓度为约5mm至约15mm。
21.在一些实施方案中,该组合物进一步包含脯氨酸(如游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合)作为赋形剂。在一些实施方案中,该组合物包含浓度为约140mm至约180mm的脯氨酸(如游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合)。
22.在一些实施方案中,该组合物的ph为约5.8至约7.0。在某些实施方案中,该组合物
的ph为约6.2至约6.8。在某些实施方案中,该组合物的ph为约6.2至约6.7。在一些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.4。在其他实施方案中,该组合物的ph为约6.5。
23.在各个实施方案中,该药物组合物不含柠檬酸盐。
24.在某些实施方案中,该药物组合物包含浓度为约150mg/ml至约300mg/ml的抗lingo
‑
1抗体或lingo
‑
1结合片段;浓度为约70mm至约180mm的精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合);浓度为约5mm至约30mm的组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合);浓度为约5mm至约15mm的甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合);以及浓度为约0.02%至约0.08%的聚山梨醇酯80。在一些情况下,该组合物的ph为约5.8至约7.0。在一些情况下,该组合物的ph为约6.2至约6.8。在某些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.5。
25.在某些实施方案中,该药物组合物包含浓度为约150mg/ml至约300mg/ml的抗lingo
‑
1抗体或lingo
‑
1结合片段;浓度为约70mm至约180mm的精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合);浓度为约5mm至约30mm的组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合);浓度为约140mm至约180mm的脯氨酸(例如,游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合);以及浓度为约0.01%至约0.1%(例如约0.04%至0.06%)的聚山梨醇酯80。在一些情况下,该组合物的ph为约5.8至约6.8。在一些情况下,该组合物的ph为约6.0至约6.8。在某些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.5。
26.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体或lingo
‑
1结合片段;浓度为约150mm至约175mm的精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合);浓度为约15mm至约25mm的组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合);浓度为约5mm至约15mm的甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合);以及浓度为约0.04%至约0.06%的聚山梨醇酯80。在一些情况下,该组合物的ph为约5.8至约6.8。在一些情况下,该组合物的ph为约6.0至约6.8。在某些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.5。
27.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体或lingo
‑
1结合片段;浓度为约150mm至约175mm的精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合);浓度为约15mm至约25mm的组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸,或游离碱形式的组氨酸和组氨酸盐酸盐的组
合);浓度为约5mm至约15mm的甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合);以及浓度为约0.04%至约0.06%的泊洛沙姆188。在一些情况下,该组合物的ph为约5.8至约6.8。在一些情况下,该组合物的ph为约6.0至约6.8。在某些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.5。
28.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体或lingo
‑
1结合片段;浓度为约70mm至约90mm的精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐);浓度为约15mm至约25mm的组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合);浓度为约140mm至约180mm的脯氨酸(例如,游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合);以及浓度为约0.04%至0.06%的聚山梨醇酯80。在一些情况下,该组合物的ph为约5.8至约6.8。在一些情况下,该组合物的ph为约6.0至约6.8。在某些实施方案中,该组合物的ph为约6.3至约6.7。在其他实施方案中,该组合物的ph为约6.5。
29.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为约150mm至约175mm的l
‑
精氨酸盐酸盐;浓度为约10mm至约30mm的l
‑
组氨酸;浓度为约5mm至约15mm的l
‑
甲硫氨酸;以及浓度为约0.01%至约0.1%的聚山梨醇酯80;并且该药物组合物的ph为约6.2至6.8。
30.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至225mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为150mm至175mm的l
‑
精氨酸盐酸盐;以及浓度为10mm至30mm的l
‑
组氨酸;浓度为5mm至15mm的l
‑
甲硫氨酸;以及浓度为0.01%至0.1%的ps聚山梨醇酯80;并且该药物组合物的ph为约6.2至6.8。
31.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,该轻链包含seq id no:17所示的氨基酸序列;浓度为约150mm至约175mm的l
‑
精氨酸盐酸盐;浓度为约10mm至约30mm的l
‑
组氨酸;浓度为约5mm至约15mm的l
‑
甲硫氨酸;以及浓度为约0.01%至约0.1%的聚山梨醇酯80;并且该药物组合物的ph为约6.2至6.8。
32.在某些实施方案中,该药物组合物包含浓度为175mg/ml至225mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为150mm至175mm的l
‑
精氨酸盐酸盐;浓度为10mm至30mm的l
‑
组氨酸;浓度为5mm至15mm的l
‑
甲硫氨酸;以及浓度为0.01%至0.1%的聚山梨醇酯80;并且该药物组合物的ph为约6.2至6.8。
33.在某些实施方案中,该药物组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为约160mm的l
‑
精氨酸盐酸盐;浓度为约20mm的l
‑
组氨酸;浓度为约10mm的l
‑
甲硫氨酸;以
及浓度为约0.05%的聚山梨醇酯80;并且该药物组合物的ph为约6.5。
34.在某些实施方案中,该药物组合物包含浓度为200mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为160mm的l
‑
精氨酸盐酸盐;浓度为20mm的l
‑
组氨酸;浓度为10mm的l
‑
甲硫氨酸;以及浓度为0.05%的聚山梨醇酯80;并且该药物组合物的ph为6.5。
35.在某些实施方案中,该药物组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为约160mm的l
‑
精氨酸盐酸盐;浓度为约20mm的l
‑
组氨酸;浓度为约10mm的l
‑
甲硫氨酸;以及浓度为约0.05%的聚山梨醇酯80;并且该药物组合物的ph为约6.5。
36.在某些实施方案中,该药物组合物包含浓度为200mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为160mm的l
‑
精氨酸盐酸盐;浓度为20mm的l
‑
组氨酸;浓度为10mm的l
‑
甲硫氨酸;以及浓度为0.05%的聚山梨醇酯80;并且该药物组合物的ph为6.5。
37.在某些实施方案中,该药物组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,该轻链包含seq id no:17所示的氨基酸序列;浓度为约150mm至约175mm的l
‑
精氨酸盐酸盐;浓度为约10mm至约30mm的l
‑
组氨酸;浓度为约5mm至约15mm的l
‑
甲硫氨酸;以及浓度为约0.01%至约0.1%的泊洛沙姆188;并且该药物组合物的ph为约6.2至6.8。
38.在某些实施方案中,该药物组合物包含浓度为175mg/ml至225mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为150mm至175mm的l
‑
精氨酸盐酸盐;浓度为10mm至30mm的l
‑
组氨酸;浓度为5mm至15mm的l
‑
甲硫氨酸;以及浓度为0.01%至0.1%的泊洛沙姆188;并且该药物组合物的ph为6.2至6.8。
39.在某些实施方案中,该药物组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为约160mm的l
‑
精氨酸盐酸盐;浓度为约20mm的l
‑
组氨酸;浓度为约10mm的l
‑
甲硫氨酸;以及浓度为约0.05%的泊洛沙姆188;并且该药物组合物的ph为约6.5。
40.在某些实施方案中,该药物组合物包含浓度为200mg/ml的抗lingo
‑
1抗体,其中vh包含seq id no:5所示的氨基酸序列,并且vl包含seq id no:13所示的氨基酸序列;浓度为160mm的l
‑
精氨酸盐酸盐;浓度为20mm的l
‑
组氨酸;浓度为10mm的l
‑
甲硫氨酸;以及浓度为0.05%的泊洛沙姆188;并且该药物组合物的ph为6.5。
41.在某些实施方案中,该药物组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为约160mm的l
‑
精氨酸盐酸盐;浓度为约20mm的l
‑
组氨酸;浓度为约10mm的l
‑
甲硫氨酸;以及浓度为约0.05%的泊洛沙姆188;并且该药物组合物的ph为约6.5。
42.在某些实施方案中,该药物组合物包含浓度为200mg/ml的抗lingo
‑
1抗体,其中该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链,其中该重链包含seq id no:9所示的氨基酸序列,并且该轻链包含seq id no:17所示的氨基酸序列;浓度为160mm的l
‑
精氨酸盐酸盐;浓度为20mm的l
‑
组氨酸;浓度为10mm的l
‑
甲硫氨酸;以及浓度为0.05%的泊洛沙姆188;并且该药物组合物的ph为6.5。
43.在一些实施方案中,该药物组合物包含抗lingo
‑
1抗体或lingo
‑
1结合片段,该抗lingo
‑
1抗体或lingo
‑
1结合片段包含vh和vl,其中该vh包含与seq id no:5至少80%同一的序列或由其组成,并且该vl包含与seq id no:13至少80%同一的序列或由其组成。在一些实施方案中,该vh包含与seq id no:5至少90%同一的序列或由其组成,并且该vl包含与seq id no:13至少90%同一的序列或由其组成。在一些实施方案中,vh包含seq id no:5的序列或由其组成并且vl包含seq id no:13的序列或由其组成。
44.在一些实施方案中,该抗lingo
‑
1抗体包含免疫球蛋白重链和免疫球蛋白轻链。在某些情况下,该重链包含与seq id no:9至少80%同一的序列或由其组成,并且该轻链包含与seq id no:17至少80%同一的序列或由其组成。在其他情况下,该重链包含与seq id no:9至少90%同一的序列或由其组成,并且该轻链包含与seq id no:17至少90%同一的序列或由其组成。在另一些其他情况下,该重链包含seq id no:9的序列或由其组成,并且该轻链包含seq id no:17的序列或由其组成。
45.在某些实施方案中,该药物组合物包含约210mg、约225mg、约250mg、约350mg、约375mg、约750mg、约1050mg、约1125mg、约1250mg、约3150mg、约3375mg、约3500mg、约6300mg或约6750mg固定剂量的抗lingo
‑
1抗体或lingo
‑
1结合片段。
46.在另一方面中,本公开的特征在于一种治疗有需要的人受试者的中枢神经系统(cns)脱髓鞘疾病的方法。cns脱髓鞘疾病的非限制性示例是多发性硬化症和视神经炎。该方法包括向人受试者施用本文所述的药物组合物。
47.在一些情况下,患者目前、先前和/或将来将用免疫调节剂进行治疗,该免疫调节剂包括但不限于二氢乳清酸脱氢酶抑制剂(例如,特立氟胺)、干扰素β1a、干扰素β1b、醋酸格拉替雷、芬戈莫德、阿仑单抗、克拉屈滨、奥美珠单抗、聚乙二醇干扰素β1a、富马酸酯(例如,富马酸二甲酯、富马酸地洛西美或富马酸单甲酯)、针对白细胞介素2受体α亚基的抗体,和/或那他珠单抗。
48.在上述方面的一些实施方案中,该药物组合物被皮下施用至人受试者。在这些方面的一些实施方案中,该药物组合物被静脉内施用至人受试者。在这些方面的一些实施方案中,该药物组合物被肌内施用至人受试者。
49.在上述方面中的某些情况下,抗lingo
‑
1抗体或lingo
‑
1结合片段的剂量为约3mg/kg人受试者的体重、约5mg/kg人受试者的体重、约10mg/kg人受试者的体重、约15mg/kg人受试者的体重、约30mg/kg人受试者的体重、约45mg/kg人受试者的体重、约90mg/kg人受试者的体重、约100mg/kg人受试者的体重或约120mg/kg人受试者的体重。
50.在上述方面中的其他情况下,该药物组合物包含约210mg、约225mg、约250mg、约350mg、约375mg、约750mg、约1125mg、约1250mg、约3150mg、约3375mg、约3500mg、约6300mg或约6750mg固定剂量的抗lingo
‑
1抗体或lingo
‑
1结合片段。
51.在又一方面中,本公开的特征在于包括本文所述的药物组合物的针筒。
52.在又另外的方面中,本发明提供一种包括针筒的试剂盒,该针筒包含本文所述的药物组合物和免疫调节剂(例如,干扰素β1a、干扰素β1b、醋酸格拉替雷、芬戈莫德、阿仑单抗、克拉屈滨、奥美珠单抗、聚乙二醇干扰素β1a、富马酸酯(例如,富马酸二甲酯、富马酸地洛西美或富马酸单甲酯)、那他珠单抗、针对白细胞介素2受体α亚基的抗体、二氢乳清酸脱氢酶抑制剂、类固醇和/或前述中的两者或更多者的组合)。
53.在一些实施方案中,本发明提供了一种试剂盒,该试剂盒包括一个或多个针筒,该一个或多个针筒包含本文所述的药物组合物,其中该一个或多个针筒适用于皮下施用。在一些实施方案中,该试剂盒进一步包括针对皮下施用所述组合物的说明书。
54.在一些实施方案中,本发明提供了一种试剂盒,该试剂盒包括一个或多个针筒,该一个或多个针筒包含本文所述的药物组合物,其中该一个或多个针筒适用于静脉内施用。在一些实施方案中,该试剂盒进一步包括针对静脉内施用所述组合物的说明书,包括例如针对在生理上可接受的液体(诸如0.9%nacl)中稀释该组合物的说明书。
55.在一些实施方案中,本发明提供一种试剂盒,该试剂盒包括一个或多个针筒,该一个或多个针筒包含本文所述的药物组合物,其中该一个或多个针筒适用于肌内施用。在一些实施方案中,该试剂盒进一步包括针对肌内施用所述组合物的说明书。
56.术语“约”是指规定值 /
‑
5%。例如,“约100mg/ml”是指95mg/ml至105mg/ml;并且“ph约6.0”是指ph为5.7至6.3。
57.术语“固定剂量”意指适合作为供一个或多个待治疗受试者用的单一剂量的物理离散单位。即,每个单位均含有经计算以在受试者中实现所需治疗浓度或效果的预定量的抗体。
58.除非另外定义,否则本文所用的所有技术和科学术语均具有与由本发明所属领域的普通技术人员通常所理解的相同的含义。虽然与本文中所述的方法和材料相似或等同的方法和材料可用于实践或测试本发明,但是下面描述了示例性方法和材料。本文提到的所有公布、专利申请、专利和其他参考文献以引用的方式整体并入。在出现矛盾的情况下,以包括定义的本技术为准。材料、方法和示例仅是说明性的而非旨在为限制性的。
59.从以下详细说明和权利要求书,本发明的其他特征和优点将显而易见。
附图说明
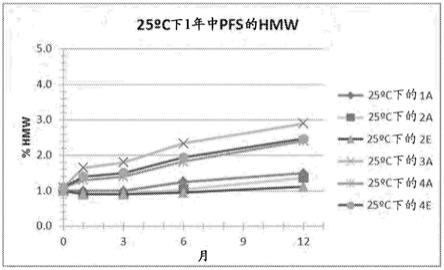
60.图1是示出在升高的蛋白质浓度下组氨酸缓冲剂的益处的折线图。高分子量(hmw)的百分比较低意味着稳定性升高。
61.图2是示出随着制剂ph升高,聚集减少的散点图。
62.图3是示出制剂中的精氨酸hcl浓度不会显著影响抗
‑
lingo
‑
1聚集的散点图。
63.图4是示出制剂ph对抗
‑
lingo
‑
1溶液粘度有显著影响的三维图。
64.图5是示出当制剂中包含不同赋形剂时,含有225mg/ml抗lingo
‑
1抗体的制剂中的聚集差异的柱形图。聚集较低意味着稳定性升高,低于3%的聚合是更为期望的。
65.图6是示出当制剂中包含不同赋形剂时,含有225mg/ml抗lingo
‑
1抗体的制剂的不同粘度的柱形图。
66.图7是示出根据长期发展稳定性评估在5℃下聚集体随时间的变化的线图。在24个月时,顶部线是制剂6,中间线是制剂5,底部线是制剂2。
67.图8是示出根据长期发展稳定性评估在25℃下聚集体随时间的变化的线图。在12个月时,顶部线是制剂1,下一根线是制剂5,下一根线是制剂3,下一根线是制剂6,底部线是制剂2。
68.图9是示出在2
‑
8℃下的长期聚集稳定性数据的线图,证实了200mg/ml抗lingo
‑
1抗体、20mm组氨酸、160mm精氨酸hcl、10mm甲硫氨酸、0.05%聚山梨醇酯80(ph 6.5)制剂的稳定性。
具体实施方式
69.本技术提供了含有抗lingo
‑
1抗体及其lingo
‑
1结合片段的药物组合物及其在治疗cns脱髓鞘疾病(诸如ms和视神经炎)中的用途。
70.lingo
‑171.含有富亮氨酸重复序列和免疫球蛋白结构域的nogo受体相互作用蛋白1(lingo
‑
1)(先前称为sp35)是在正常情况下在发育期间在成人cns中在神经元和少突胶质细胞、在中枢神经系统(cns)少突胶质细胞和神经元中选择性表达的细胞表面糖蛋白,并在cns疾病中上调。它含有具有12个富亮氨酸重复序列(lrr)基序(其侧接有n和c末端加帽模块)的大胞外结构域域,一个i1亚型的ig结构域,以及与跨膜区和短胞质尾区附接的茎区(mi等人,2004;mosyak等人,j biol chem 281:36378
–
36390,2006)。lingo
‑
1抑制少突胶质细胞分化,从而防止轴突髓鞘形成。在体外以及在脱髓鞘动物模型中,阻断它的功能会导致强健的髓鞘形成。
72.lingo
‑
1是包含以下3种其他旁系同源体的蛋白质家族的成员:lingo
‑
2(gi:12309630,61%蛋白质同一性)、lingo
‑
3(gi:23342615,56%同一性)和lingo
‑
4(gi:21211752,44%同一性)。lingo
‑
1在进化上是高度保守的,其中人和小鼠直向同源物共享99.5%同一性,并且人和大鼠lingo
‑
1共享99.5%同一性。通过northern印迹分析,发现lingo
‑
1在人脑中高度表达并且在非神经组织中不可检测(barrette等人(2007)mol cell neurosci,34:519
‑
38;carim
‑
todd等人(2003)eur journal neurosci,18:3167
‑
82;llorens等人(2008)dev neurobiol,68:521
‑
41;mi等人(2004)nat neurosci,7:221
‑
8;okafuji等人(2005)gene expr patterns,6:57
‑
62;park等人(2006)neurosci lett,404:61
‑
6;shao等人(2005)neuron,45:353
‑
9)。lingo
‑
1是受发育调节的,其中在新生大鼠中的表达在产后第1天达到峰值,然后在成年后下降(ji等人,mol cell neurosci.2006;33(3):311
‑
20;mi等人(2004)nat neurosci,7:221
‑
8;mi等人,cns drugs.2013;27(7):493
‑
503)。lingo
‑
1表达的下调与啮齿动物中正常cns髓鞘形成的发生相关。lingo
‑
1表达水平已被证明在神经病变中,诸如在脊髓损伤动物模型(ji等人,mol cell neurosci.2006;33(3):311
‑
20)和青光眼(fu等人,invest ophthalmol vis sci.2008;49(3):975
‑
85)中、在帕金森病(inoue proc natl acad sci u s a.2007;104(36):14430
‑
5)中以及在ms病变中上调。
73.lingo
‑
1还已经详细描述于2006年7月7日提交的国际申请p ct/us2006/026271、2004年3月17日提交的国际申请pct/us2004/008323、2005年6月24日提交的国际申请pct/us2005/022881、2008年1月9日提交的国际申请pct/us2008/000316、国际申请pct/us2017/041757;以及国际申请pct/us2016/012619中,该申请中的每一者以引用方式整体并入本
文。
74.lingo
‑
1在少突胶质前体细胞(opc)和神经元两者中选择性地表达。lingo
‑
1用作少突胶质细胞分化、髓鞘形成和髓鞘再生的负调节因子;防止由少突胶质细胞所致的轴突的髓鞘形成(lee等人(2007)j neurosci,27:220
‑
5;mi等人(2005)nat neurosci,8:745
‑
51;mi等人(2008)int journal biochem cell biol40(10):1971
‑
8;mi等人(2009)ann neurology,65:304
‑
15)。lingo
‑
1的轴突和神经元表达在损伤之后增加(ji等人(2006)mol cell neurosci,33:311
‑
20)。lingo
‑
1表达防止由少突胶质细胞所致的轴突的髓鞘形成。若干临床前研究已证实lingo
‑
1拮抗作用在以下的动物模型中有增强cns髓鞘再生和神经轴突保护方面的潜能:毒性(cuprizone)(mi等人(2009)ann neurology,65:304
‑
15)、化学性损伤(溶血磷脂酰胆碱[lpc])和炎性脱髓鞘(髓鞘少突胶质细胞糖蛋白
‑
实验性自身免疫性脑脊髓炎[mog
‑
eae])(mi等人(2007)nat med,13:1228
‑
33);以及毒性(1
‑
甲基
‑4‑
苯基
‑
1,2,3,6
‑
四氢吡啶[mptp])神经元损伤(inoue等人(2007)proc natl acad sci,104:14430
‑
5)、外伤性/高血压视神经损伤(fu等人(2008)invest opthalmol vis sci,49:975
‑
85)和脊髓损伤(ji等人(2006)mol cell neurosci,33:311
‑
20;ji等人(2008))mol cell neurosci,39:258
‑
67;lv等人(2010)neuroimmunomodulat,17:270
‑
8)。可通过由抑制轴突和少突胶质细胞中的lingo
‑
1引起的cns中的ngr1受体复合物上的髓鞘碎片和/或硫酸化蛋白多糖的信号传导阻断来提供髓鞘再生和神经轴突保护。这继而可经由使通常存在于ms患者的脑中的少突胶质细胞前体细胞(opc)的分化增强髓鞘再生。因此,lingo
‑
1的拮抗作用可增强例如,由少突胶质细胞所致的轴突的髓鞘形成或髓鞘再生,并且增强了cns中的神经轴突保护,以及例如cns脱髓鞘疾病(如多发性硬化症(ms)和急性视神经炎)中的神经轴突保护,从而导致改善的cns修复。
[0075]
lingo
‑
1在本领域中也可称为名称lrrn6、lrrn6a、flj14594、lern1、mgc17422和unq201。人全长野生型lingo
‑
1多肽含有由以下组成的lrr结构域:14个富亮氨酸重复序列(包括n和c末端帽)、ig结构域、跨膜区和胞质结构域。该胞质结构域含有典型的酪氨酸磷酸化位点。另外,天然存在的lingo
‑
1蛋白含有信号序列、介于lrr
‑
c末端结构域(lrrct)与ig结构域之间的短碱性区域,以及介于ig结构域与细胞质结构域之间的跨膜区。表1列出了基于在本文中示为seqid no:86的lingo
‑
1氨基酸序列,根据氨基酸残基数量的lingo
‑
1结构域及其他区。lingo
‑
1多肽在pct公布号wo2004/085648中被更详细地表征,该公布以引用的方式整体并入本文。
[0076]
表1
[0077][0078]
已在人和大鼠中研究了lingo
‑
1的组织分布和发育表达。已在实验动物(大鼠)模型中研究了lingo
‑
1生物学。大鼠lingo
‑
1的表达局限于神经元和少突胶质细胞,如通过northern印迹和免疫组织化学染色所确定的。大鼠lingo
‑
1mrna表达水平受发育调控,在出生后不久即大约产后一天达到峰值。在大鼠脊髓横切损伤模型中,lingo
‑
1在损伤部位是上调的,如通过rt
‑
pcr所确定。参见mi等人,nature neurosci.7:221
‑
228(2004)。
[0079]
在包含lingo
‑
1多肽的各种结构和功能结构域的氨基酸的情形下,术语“约”包括具体列举的值和多或少几个(例如,10、9、8、7、6、5、4、3、2或1个)氨基酸的值。由于如表1所列的这些结构域的位置已通过计算机图形学预测,因此本领域普通技术人员应理解构成结构域的氨基酸残基可根据用于定义结构阈的标准而稍改变(例如,约1个至15个残基)。
[0080]
全长的野生型lingo
‑
1与ngr1结合。参见pct公布号wo2004/085648。lingo
‑
1在少突胶质细胞中表达,并且lingo
‑
1蛋白参与了调控少突胶质细胞介导的轴突髓鞘形成。参见美国专利公布号2006/0009388a1,该美国专利公布以引用方式整体并入本文。
[0081]
全长lingo
‑
1分子的核苷酸序列如下:
[0082]
atgctggcggggggcgtgaggagcatgcccagccccctcctggcctgctg gcagcccatcctcctgctggtgctgggctcagtgctgtcaggctcggcca cgggctgcccgccccgctgcgagtgctccgcccaggaccgcgctgtgctg tgccaccgcaagcgctttgtggcagtccccgagggcatccccaccgagac gcgcctgctggacctaggcaagaaccgcatcaaaacgctcaaccaggacg agttcgccagcttcccgcacctggaggagctggagctcaac
nvsgnqlttl eesvfhsvgn letlildsnp lacdcrllwv frrrwrlnfn rqqptcatpe fvqgkefkdf pdvllpnyft crrarirdrk aqqvfvdegh tvqfvcradg dpppailwls prkhlvsaks ngrltvfpdg tlevryaqvq dngtylciaa naggndsmpa hlhvrsyspd wphqpnktfa fisnqpgege anstratvpf pfdiktliia ttmgfisflg vvlfclvllf lwsrgkgntk hnieieyvpr ksdagissad aprkfnmkm(seq id no:87)。参见例如,ncbi参考序列:np_001288115.1;uniprotkb/swiss
‑
prot登录号q96fe5。
[0087]
抗lingo
‑
1抗体
[0088]
用于本文描述的组合物和方法中的抗lingo
‑
1抗体或其lingo
‑
1结合片段与人lingo
‑
1结合。
[0089]
在一个实施方案中,将抗体分子分离、纯化或重组。“分离的”多肽或其片段、变体或衍生物旨在表示不在其天然环境中的多肽。不要求具体的纯化水平。例如,分离的多肽可从其天然或自然环境中移出。出于本发明的目,重组产生的多肽以及在宿主细胞中表达的蛋白质可被视为分离的,已通过任何合适的技术分离、分级,或者部分地或基本上纯化的天然或重组多肽也被视为分离的。
[0090]
如本文所用,术语“抗体分子”是指包含至少一个免疫球蛋白可变结构域序列的蛋白质。术语抗体分子包括,例如,全长抗体,成熟抗体,本文公开的抗体的片段(例如抗体的抗原结合片段)、衍生物、类似物或变体,以及它们的任何组合。
[0091]
当提及lingo
‑
1抗体分子或抗体多肽时,术语“片段”、“变体”、“衍生物”和“类似物”包括保留对应天然抗体或多肽的抗原结合性质中的至少一些抗原结合性质的任何多肽。除了本文别处论述的特定抗体片段之外,多肽的片段还包括蛋白水解片段以及缺失片段。lingo
‑
1抗体和抗体多肽的变体包含如上所述的片段以及具有由于氨基酸取代、缺失或插入而改变的氨基酸序列的多肽。变体可天然存在或非天然存在。可使用本领域已知的诱变技术来产生非天然存在的变体。变体多肽可包含保守或非保守的氨基酸取代、缺失或添加。lingo
‑
1抗体分子和抗体多肽的衍生物是已被改变成表现出在天然多肽上未发现的额外特征的多肽。示例包括融合蛋白。
[0092]
在一个实施方案中,抗lingo
‑
1抗体分子是全人抗lingo
‑
i单克隆抗体,该单克隆抗体被工程化为无糖基免疫球蛋白g亚类1(igg1)架构以降低效应子功能(在本文也称为li81)。已执行lingo
‑
1敲除小鼠的组织学和功能评估,并且已经在若干脱髓鞘动物模型中证实了li81的体内药理活性。已基于结合特性、生物活性和药理活性的评估,在体外和体内表征了li81。这些研究的结果表明,li81具有以下特征:(a)在人、猴、大鼠和小鼠中以类似的高表观亲和力结合至lingo
‑
1;(b)对lingo
‑
1有选择性并且不结合其他lingo家族成员,即lingo
‑
2、lingo
‑
3或lingo
‑
4;(c)增强原代大鼠、猴和人少突胶质细胞的体外分化;(d)增强体外大鼠背根神经节/opc共培养生物测定中的轴突髓鞘形成;(e)与野生型igg1相比,具有降低的fc(γ)和补体效应子功能;以及(f)在使用生化和功能读出的动物模型中是有效的(例如,当在干扰素β的存在下给予时在动物模型中是有效的,并且当在皮质类固醇的存在下给予时在动物模型中是有效的)。在以100mg/kg全身施用li81后,证实了大鼠lpc模型的髓鞘再生活性。在每周以3mg/kg和10mg/kg li81全身施用后,证实了大鼠mog
‑
eae模型的功能恢复。
[0093]
在一个实施方案中,抗lingo
‑
1抗体包含重链,该重链包含seq id no:9的氨基酸
序列,或与该氨基酸序列基本上同一的序列(例如,与该氨基酸序列至少80%、85%、90%或95%同一的氨基酸序列)。
[0094]
在其他实施方案中,抗lingo
‑
1抗体包含轻链,该轻链包含seq id no:17的氨基酸序列,或与该氨基酸序列基本上同一的序列(例如,与该氨基酸序列至少80%、85%、90%或95%同一的氨基酸序列)。
[0095]
在一些实施方案中,抗lingo
‑
1抗体结合至lingo
‑
1的lrr 4
‑
8内的富亮氨酸重复序列(lrr)结构域的凸表面。此外,抗lingo
‑
1抗体与lingo
‑
1的结合干扰了lingo
‑
1寡聚化的能力。
[0096]
在一些实施方案中,本文所述的组合物和方法中使用的抗lingo
‑
1抗体或其lingo
‑
1结合片段包含称为li81的抗体的三个重链可变结构域互补决定区(cdr)。
[0097]
因此,li81是可用于本文所述的组合物和方法中的示例性抗lingo
‑
1抗体。li81是一种全人igg1单克隆抗体,该全人igg1单克隆抗体以亚纳摩尔亲和力与人lingo
‑
1结合。发现li81对lingo
‑
1的胞外结构域的结合亲和力的k
d
值低于或等于20pm,并且发现li81的fab对lingo
‑
1的胞外结构域的kd值低于或等于50pm。重要的是,li81不与lingo家族的其他高度同源成员,例如,lingo
‑
2、lingo
‑
3和lingo
‑
4结合。
[0098]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含li81的三个轻链可变结构域cdr。在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含li81的三个重链可变结构域cdr。在又一些其他实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含li81的三个重链可变结构域cdr和三个轻链可变结构域cdr。cdr可以基于本领域中的任何cdr定义,例如kabat、chothia、来自abysis的chothia、增强型chothia/abm的定义,或基于接触定义。在下表2中提供了li81和其他抗lingo
‑
1抗体的vh序列(和该序列中的cdr序列)。
[0099]
表2:lingo
‑
1抗体vh序列
[0100]
[0101]
[0102]
[0103]
[0104]
[0105][0106]
在下表3中提供了li81和其他抗lingo
‑
1抗体的vl序列(和该序列中的cdr序列)。
[0107]
表3:lingo
‑
1抗体vl序列
[0108][0109]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含:vh cdr1,该vh cdr1包含seq id no:6所示的氨基酸序列或由其组成;vh cdr2,该vh cdr2包含seq id no:7所示的氨基酸序列或由其组成;以及vh cdr3,该vh cdr3包含seq id no:8所示的氨基酸序列或由其组成。在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含vl cdr1,该vl cdr1包含seq id no:14所示的氨基酸序列或由其组成;vl cdr2,该vl cdr2包含seq id no:15所示的氨基酸序列或由其组成;以及vl cdr3,该vl cdr3包含seq id no:16所示的氨基酸序列或由其组成。
[0110]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含:vh cdr1,该vh cdr1包含seq id no:6所示的氨基酸序列或由其组成;vh cdr2,该vh cdr2包含seq id no:7所示的氨基酸序列或由其组成;以及vh cdr3,该vh cdr3包含seq id no:8所示的氨基酸序列或由其组成;vl cdr1,该vl cdr1包含seq id no:14所示的氨基酸序列或由其组成;vl cdr2,该vl cdr2包含seq id no:15所示的氨基酸序列或由其组成;以及vl cdr3,该vl cdr3包含seq id no:16所示的氨基酸序列或由其组成。
[0111]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含li81的可变重链(vh)或由其组成。li81的vh具有以下氨基酸序列(带下划线的vh
‑
cdr):
[0112]
evqllesggglvqpggslrlscaasgftfsayemkwvrqapgkglewvsvigpsggftfyadsvkgrftisrdnskntlylqmnslraedtavyycategdndafdiwgqgttvtvss(seq id no:5)
[0113]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含li81的可变轻链(vl)或由其组成。li81的vl具有以下氨基酸序列(带下划线的vl
‑
cdr):
[0114]
diqmtqspatlslspgeratlscrasqsvssylawyqqkpgqaprlliydasnratgiparfsgsgsgtdftltisslepedfavyycqqrsnwpmytfgqgtkleik(seq id no:13)
[0115]
由下面列出的成熟重链(seq id no:9)和成熟轻链(seq id no:17)组成的抗体被称为如本文所用的“li81”。
[0116]
成熟li81重链(hc):
[0117]
evqllesggglvqpggslrlscaasgftfsayemkwvrqapgkglewvsvigpsggftfyadsvkgrftisrdnskntlylqmnslraedtavyycategdndafdiwgqgttvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynsayrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:9)。
[0118]
成熟li81轻链(lc):
[0119]
diqmtqspatlslspgeratlscrasqsvssylawyqqkpgqaprlliydasnratgiparfsgsgsgtdftltisslepedfavyycqqrsnwpmytfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:17)。
[0120]
在上面列出的vh、vl、hc和lc序列中,cdr 1、cdr2和cdr3基于kabat定义。
[0121]
在本文公开的方法和组合物的某些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:5所示的氨基酸序列的vh。在本文公开的方法和组合物的某些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:13所示的氨基酸序列的vl。在本文公开的方法和组合物的某些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:5所示的氨基酸序列的vh和具有seq id no:13所示的氨基酸序列的vl。在本文公开的方法和组合物的某些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:9所示的氨基酸序列的重链。在本文公开的方法和组合物的某些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:17所示的氨基酸序列的轻链。在本文公开的方法和组合物的其他实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段包含具有seq id no:9所示的氨基酸序列的重链和具有seq id no:17所示的氨基酸序列的轻链。
[0122]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段选择性地结合至lingo
‑
1,并且包含hc,该hc与seq id no:9的氨基酸序列至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多同一,或与seq id no:9相差至少1个至5个氨基酸残基,但少于40个、30个、20个、15个或10个残基。在一个实施方案中,六个cdr与li81的六个cdr同一,并且对架构区进行了任何取代。
[0123]
在一些实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段选择性地结合至lingo
‑
1,并且包含lc,该lc与seq id no:17的氨基酸序列至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多同一,或与seq id no:17相差至少1个至5个氨基酸残基,但少于40个、30个、20个、15个或10个残基。在一个实施方案中,六个cdr与li81的六个cdr同一,并且对架构区进行了任何取代。
[0124]
在某些实施方案中,抗lingo
‑
1抗体是igg抗体。在特定实施方案中,抗lingo
‑
1抗体具有选自例如igg1、igg2、igg3、igg4、igm、iga1、iga2、igd和ige的重链恒定区。在一个实施方案中,抗lingo
‑
1抗体是igg1同种型的。在另一个实施方案中,抗lingo
‑
1抗体是igg2同种型的。在又一个实施方案中,抗lingo
‑
1抗体是igg3同种型的。在进一步的实施方案中,抗lingo
‑
1抗体具有选自例如人κ或人λ轻链的轻链恒定区。在某个实施方案中,抗lingo
‑
1抗体是igg1/人λ抗体。
[0125]
在一些实施方案中,抗lingo
‑
1抗体是全长(整个)抗体或基本上全长的抗体。该蛋白质可包括至少一条,优选两条完整的重链,以及至少一条,优选两条完整的轻链。在一些实施方案中,抗lingo
‑
1抗体是lingo
‑
1结合片段。在一些情况下,lingo
‑
1结合片段是fab、fab'、f(ab')2、facb、fv、单链fv(scfv)、sc(fv)2或双抗体。
[0126]
本文公开的抗体的重链和轻链还可包含信号序列。该信号序列可选自本领域已知的那些信号序列,例如,mdmrvpaqllgllllwfpgsrc(seq id no:88)或mdmrvpaqllgllllwlpgarc(seq id no:89)。
[0127]
可以例如通过制备和表达编码所列举的氨基酸序列的合成基因,或者使人种系基因突变以提供编码所列举的氨基酸序列的基因来制备抗体(诸如li81)或其lingo
‑1‑
结合片段。此外,可以例如使用以下方法中的一种或多种方法来产生该抗体和其他抗lingo
‑
1抗体。
[0128]
抗lingo
‑
1抗体组合物
[0129]
本公开还提供了包含本文所述的抗lingo
‑
1抗体或其lingo
‑
1结合片段的组合物(例如,药物组合物)。请注意,组合物也可被称为制剂。例如,抗lingo
‑
1组合物包含抗lingo
‑
1抗体或其lingo
‑
1结合片段,该抗lingo
‑
1抗体或其lingo
‑
1结合片段包含免疫球蛋白重链可变结构域(vh)和免疫球蛋白轻链可变结构域(vl),其中该vh包括h
‑
cdr,并且该vl包括li81的l
‑
cdr。在某些情况下,重链cdr(h
‑
cdr)包含seq id no:6、seq id no:7和seq id no:8所示的氨基酸序列或由其组成;并且轻链cdr(l
‑
cdr)包含seq id no:14、seq id no:15和seq id no:16所示的氨基酸序列或由其组成。在一些实施方案中,抗lingo
‑
1组合物包含抗lingo
‑
1抗体或其lingo
‑
1结合片段,该抗lingo
‑
1抗体或其lingo
‑
1结合片段包含(i)vh,该vh包含与seq id no:5所示的氨基酸序列至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一的氨基酸序列或由其组成;和(ii)vl,该vl包含与seq id no:13所示的氨基酸序列至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一的氨基酸序列或由其组成。在一些实施方案中,抗lingo
‑
1组合物包含抗lingo
‑
1抗体,该抗lingo
‑
1抗体包含(i)重链,该重链包含与seq id no:9所示的氨基酸序列至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一的氨基酸序列或由其组成;和(ii)轻链,该轻链包含与seq id no:17所示的氨基酸序列至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一的氨基酸序列或由其组成。
[0130]
在某些实施方案中,这些组合物是高浓度抗lingo
‑
1抗体组合物。“高浓度抗lingo
‑
1抗体组合物”是指包含浓度大于约75mg/ml且小于约300mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段的组合物。在某些情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约100mg/ml至约275mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在某些情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约150mg/ml至约250mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在某些情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约175mg/ml至约225mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在其他情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约180mg/ml至约220mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约190mg/ml至约210mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在某些情况下,该高浓度抗lingo
‑
1抗体组合物包含浓度为约200mg/ml的抗lingo
‑
1抗体或其lingo
‑
1结合片段。
[0131]
包含本文所述的抗lingo
‑
1抗体或lingo
‑
1结合片段的组合物(例如,药物组合物)可以是多种形式中的任一种形式。这些形式包括,例如,液体溶液(例如,可注射和可输注的溶液)、分散体或悬浮液。优选形式可取决于意图施用模式和治疗应用。在一些实施方案中,包含本文所述的抗lingo
‑
1抗体或lingo
‑
1结合片段的组合物的施用途径是任何肠胃外途径,包括但不限于皮下(sc/sq)、腹腔内(ip)、静脉内(iv)、皮内(id)和肌内(im)。在某些实施方案中,本文所述的药物组合物呈无菌可注射或可输注溶液的形式。
[0132]
可通过将所需量的本文所述的抗体与一种成分或成分的组合掺在一起,然后进行过滤灭菌来制备无菌可注射溶液。一般地,通过将本文所述的抗体或抗体结合片段掺加到含有基础分散介质和所需其他成分的无菌媒介物中来制备分散体。在用于制备无菌可注射溶液的无菌粉末的情况下,示例性制备方法是真空干燥和冷冻干燥,该真空干燥和冷冻干燥从本文所述的抗体加任何额外期望成分的先前经无菌过滤的溶液得到本文所述的抗体和加任何额外期望成分的粉末。可例如通过使用诸如卵磷脂的包衣,在分散体的情况下通过维持所需粒度,以及通过使用表面活性剂来维持溶液的适当流动性。
[0133]
抗lingo
‑
1抗体组合物(例如,药物组合物)(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)可另外包含一种或多种赋形剂。在一些实施方案中,该赋形剂可以选自以下非限制性组分中的一种或多种组分:精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐)、组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、聚山梨醇酯80和脯氨酸(如游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合),或甲硫氨酸(如游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合)。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含柠檬酸盐(例如柠檬酸钠)。
[0134]
在一个实施方案中,与不含赋形剂的药物组合物中的抗体的稳定性、聚集和/或粘度相比,本文所述的抗lingo
‑
1抗体组合物(例如,药物组合物)(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)中的赋形剂缓冲药物组合物并且/或者增加药物组合物的稳定性并且/或者降低/减少该组合物中组分(例如,抗体或抗体片段)的聚集并且/或者降低/减少该组合物中的抗体(或抗体片段)的粘度。
[0135]
在某些实施方案中,本文所述的抗lingo
‑
1抗体组合物(例如,药物组合物)(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)中的赋形剂是精氨酸,诸如游离碱形式的精氨酸(例如,l
‑
精氨酸)、精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐),或游离碱形式的精氨酸(例如,l
‑
精氨酸)和精氨酸盐酸盐(例如,l
‑
精氨酸盐酸盐)的组合。在一些实施方案中,精氨酸是精氨酸盐酸盐(arg hcl,诸如l
‑
精氨酸盐酸盐)。在一些实施方案中,本文所述的含有抗lingo
‑
1抗体的组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)中的赋形剂是精氨酸盐酸盐(arg hcl),而不是游离碱形式的精氨酸,因为精氨酸盐酸盐(arg hcl)比游离碱形式的精氨酸提供了更大的稳定性和粘度益处。精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)可以以约50mm至约300mm、约60mm至约250mm、约65mm至约200mm、约70mm至约175mm、约75mm至约170mm、约80mm至约160mm、约150mm至约165mm,或约160mm的浓度包含在该组合物中。在某些实施方案中,精氨酸(例如精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)以约170mm的浓度存在于该组合物中。在某些实施方案中,精氨酸(例如精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)以约165mm的浓度存在于该组合物中。在特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约160mm的浓度包含在该组合物中。在某些实施方案中,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)以约155mm的浓度存在于该组合物中。在另一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约150mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约140mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约130mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约120mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约110mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约100mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约90mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约80mm的浓度包含在该组合物中。在又一特定情况下,精氨酸(例如,精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐)可以以约70mm的浓度包含在该组合物中。
[0136]
在某些实施方案中,本文所述的抗lingo
‑
1抗体组合物(例如,药物组合物)中的赋形剂是组氨酸,诸如游离碱形式的组氨酸(例如,l
‑
组氨酸)、组氨酸盐酸盐(例如,l
‑
组氨酸盐酸盐),或游离碱形式的组氨酸和组氨酸盐酸盐的组合。组氨酸(例如,游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐的组合)可以以约0.1mm至约100mm、约1.0mm至约80mm、约5.0mm至约60mm、约10mm至约45mm、约15mm至约30mm、约15mm至约25mm、约18mm至约22mm,或约20mm的浓度包含在该组合物中。在某些实施方案中,组氨酸(例如,游离碱形式的组氨酸和/或组氨酸盐酸盐的组合)可以以约20mm的浓度存在于该组合物中。在某些实施方案中,组氨酸(例如,游离碱形式诸如如l
‑
组氨酸)、组氨酸盐酸盐(例如,l
‑
组氨酸盐酸盐),或游离碱形式的组氨酸和组氨酸盐酸盐的组合以达到该组合物的目标ph的比率包含在该组合物中。在一些实施方案中,所述组合物的目标ph介于约ph 6.0与ph 7.0之间(例如,ph 6.5)。因此,当组合物被描述为含有20mm的组氨酸时,应理解该组合物含有
20mm的组氨酸(例如游离碱形式的组氨酸诸如l
‑
组氨酸)、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐(例如,l
‑
组氨酸盐酸盐)的组合,其中游离碱形式的组氨酸和组氨酸盐酸盐的量变化以达到所述组合的期望ph(例如,ph 6.5)。
[0137]
在某些实施方案中,本文所述的抗lingo
‑
1抗体组合物(例如,药物组合物)中的赋形剂是甲硫氨酸,诸如游离碱形式的甲硫氨酸(例如,l
‑
甲硫氨酸)、甲硫氨酸盐酸盐(例如,甲硫氨酸盐酸盐),或游离碱形式的甲硫氨酸和甲硫氨酸
‑
hcl的组合。在一些实施方案中,甲硫氨酸是游离碱形式的甲硫氨酸(例如,l
‑
甲硫氨酸)。甲硫氨酸(例如,游离碱形式的甲硫氨酸)可以以约0.1mm至约50mm、约1.0mm至约37.5mm、约5.0mm至约25mm、约7.5mm至约20mm、约8mm至约15mm、约9mm至约12mm或约10mm的浓度包含在该组合物中。在某些实施方案中,甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸)以约10mm的浓度存在于该组合物中。
[0138]
在某些实施方案中,本文所述的抗lingo
‑
1抗体组合物(例如,药物组合物)中的赋形剂是脯氨酸,诸如游离碱形式的脯氨酸(例如,l
‑
脯氨酸)、脯氨酸盐酸盐(例如,l
‑
脯氨酸盐酸盐),或游离碱形式的脯氨酸和脯氨酸
‑
hcl的组合。在一些实施方案中,脯氨酸是游离碱形式的脯氨酸。脯氨酸(例如,游离碱形式的脯氨酸诸如l
‑
脯氨酸)可以以约50mm至约300mm、约100mm至约200mm、约125mm至约175mm、约150mm至约165mm,或约160mm的浓度包含在该组合物中。在某些实施方案中,脯氨酸(例如,游离碱形式的脯氨酸诸如l
‑
脯氨酸)以约160mm的浓度存在于该组合物中。
[0139]
在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含柠檬酸盐。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含谷氨酸盐。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含海藻糖。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含蔗糖。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含氯化钙。在一些实施方案中,本文所述的抗lingo
‑
1抗体组合物(或包含抗lingo
‑
1抗体的lingo
‑
1结合片段的组合物)不包含赖氨酸。
[0140]
抗体产品制造是一个复杂的过程,该过程可能涉及多个步骤,诸如例如,原料药和物料配制(drug substance and bulk formulation)、过滤、运输、汇集、灌装、冻干、检查、包装和贮存。在这些步骤期间,可使抗体经受多种不同形式的胁迫(stress),例如搅动、温度、光暴露和氧化。这些类型的胁迫可导致抗体变性和聚集,这会损害产品质量,甚至可导致生产批次的损失。搅动是抗体治疗剂在制造工艺的过程期间经受的常见物理胁迫之一。搅动发生在例如混合、超滤/渗滤、泵送、运输和灌装期间。为了保护抗体组合物免受搅动引起的胁迫,该组合物可包含聚山梨醇酯。在某些实施方案中,该组合物包含浓度为约0.01%(w/v)至约0.5%(w/v)、约0.01%(w/v)至约0.1%(w/v)、约0.01%(w/v)至约0.09%(w/v)、约0.02%(w/v)至约0.08%(w/v)、约0.03%(w/v)至约0.07%(w/v)、约0.04%(w/v)至约0.07%(w/v)、约0.04%(w/v)至约0.06%(w/v)或约0.05%(w/v)的聚山梨醇酯
‑
80。在一些实施方案中,该组合物包含浓度为约0.01%(w/v)、约0.02%(w/v)、约0.03%(w/v)、约0.04%(w/v)、约0.05%(w/v)、约0.06%(w/v)、约0.07%(w/v)、约0.08%、约0.09%或约
0.1%(w/v)的聚山梨醇酯
‑
80。
[0141]
在一些实施方案中,该组合物包含大于0.03%(重量/体积)的聚山梨醇酯
‑
80。例如,在一些实施方案中,该组合物包含0.04%(w/v)的聚山梨醇酯
‑
80。在特定的实施方案中,该组合物包含浓度为0.05%(w/v)、ph 6.5的聚山梨醇酯
‑
80。
[0142]
在某些实施方案中,抗体组合物包含醋酸盐作为缓冲剂。在某些实施方案中,该组合物包含浓度为约5mm至约50mm、约5mm至约40mm、约5mm至约35mm、约5mm至约30mm、约5mm至约25mm、约10mm至约50mm、约10mm至约40mm、约10mm至约30mm、约10mm至约25mm、约15mm至约50mm、约15mm至约40mm、约15mm至约30mm,或约15mm至约25mm的醋酸盐。在某些实施方案中,该组合物包含浓度为约5mm至约35mm的醋酸盐。在某些实施方案中,该组合物包含浓度为约10mm至约30mm的醋酸盐。在一些实施方案中,该组合物包含浓度为约5mm、约10mm、约15mm、约20mm、约25mm、约30mm或约35mm的醋酸盐。在特定的实施方案中,该组合物包含浓度为约20mm的醋酸盐。
[0143]
在某些实施方案中,抗体组合物包含琥珀酸盐作为缓冲剂。在某些实施方案中,该组合物包含浓度为约5mm至约50mm、约5mm至约40mm、约5mm至约35mm、约5mm至约30mm、约5mm至约25mm、约10mm至约50mm、约10mm至约40mm、约10mm至约30mm、约10mm至约25mm、约15mm至约50mm、约15mm至约40mm、约15mm至约30mm,或约15mm至约25mm的琥珀酸盐。在某些实施方案中,该组合物包含浓度为约5mm至约35mm的琥珀酸盐。在某些实施方案中,该组合物包含浓度为约10mm至约30mm的琥珀酸盐。在一些实施方案中,该组合物包含浓度为约5mm、约10mm、约15mm、约20mm、约25mm、约30mm或约35mm的琥珀酸盐。在特定的实施方案中,该组合物包含浓度为约20mm的琥珀酸盐。
[0144]
抗lingo
‑
1抗体组合物的ph可为约5.8至约7.2。在某些情况下,抗体组合物的ph可为约6.0至约7.0。在某些情况下,抗体组合物的ph为约6.0、约6.1、约6.2、约6.3、约6.4、约6.5、约6.5、约6.7、约6.8、约6.9或约7.0。在特定实施方案中,抗体组合物的ph为约6.5。
[0145]
在某些情况下,抗lingo
‑
1抗体组合物包含精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)。在其他情况下,抗lingo
‑
1抗体组合物包含精氨酸(例如,游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)和组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)。在其他情况下,抗lingo
‑
1抗体组合物包含精氨酸(例如,游离碱形式精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)、组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)和甲硫氨酸(例如,游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合)以及聚山梨醇酯80。在另一些其他情况下,抗lingo
‑
1抗体组合物包含精氨酸(如游离碱形式的精氨酸诸如l
‑
精氨酸,或精氨酸盐酸盐诸如l
‑
精氨酸盐酸盐,或游离碱形式的精氨酸和精氨酸盐酸盐的组合)、组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、脯氨酸(如游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨
酸盐酸盐的组合)以及聚山梨醇酯80。
[0146]
在某些实施方案中,抗lingo
‑
1抗体组合物包含精氨酸盐酸盐(如l
‑
精氨酸盐酸盐,其为例如约160mm)、组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合,其为例如约20mm)、甲硫氨酸(如游离碱形式的甲硫氨酸诸如l
‑
甲硫氨酸,或甲硫氨酸盐酸盐诸如l
‑
甲硫氨酸盐酸盐,或游离碱形式的甲硫氨酸和甲硫氨酸盐酸盐的组合,其为例如约10mm)和聚山梨醇酯
‑
80(例如约0.05%w/v),并且具有约6.0至约6.8的ph(例如,约6.5的ph)。在一些实施方案中,抗lingo
‑
1抗体组合物包含精氨酸盐酸盐(如l
‑
精氨酸盐酸盐,其为例如约80mm)、组氨酸(如游离碱形式的组氨酸诸如l
‑
组氨酸,或组氨酸盐酸盐诸如l
‑
组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合,其为例如约20mm)、脯氨酸(如游离碱形式的脯氨酸诸如l
‑
脯氨酸,或脯氨酸盐酸盐诸如l
‑
脯氨酸盐酸盐,或游离碱形式的脯氨酸和脯氨酸盐酸盐的组合,其为例如约160mm)和聚山梨醇酯80(例如约0.05%w/v),并且具有约6.0至约6.8的ph(例如,约6.5的ph)。在所有这些实施方案中,抗lingo
‑
1抗体以约50mg/ml至约300mg/ml的浓度存在。在一种情况下,抗lingo
‑
1抗体以约175mg/ml的浓度存在。在一种情况下,抗lingo
‑
1抗体以约200mg/ml的浓度存在。在一种情况下,抗lingo
‑
1抗体以约220mg/ml的浓度存在。
[0147]
生产抗体的方法
[0148]
使用标准分子生物学技术来制备一种或多种重组表达载体、转染宿主细胞、选择转化体、培养宿主细胞并回收抗体。
[0149]
抗lingo
‑
1抗体或lingo
‑
1结合片段可在细菌或真核细胞中生产。一些抗体(例如,fab)可以在细菌细胞(例如,大肠杆菌细胞)中生产。抗体也可以在真核细胞,诸如转化的细胞系(例如,cho、293e、cos)中生产。此外,抗体(例如,scfv)可以在酵母细胞(诸如毕赤酵母(参见,例如,powers等人,j immunol methods.251:123
‑
35(2001))、汉逊酵母属或酵母属中表达。为了生产感兴趣的抗体,构建编码抗体的多核苷酸,将该多核苷酸引入到表达载体中,然后使该多核苷酸在合适的宿主细胞中表达。普通技术人员将容易设想编码包含本文所述的抗lingo
‑
1抗体的vh和/或vl、hc和/或lc的抗lingo
‑
1抗体的多核苷酸。使用标准分子生物学技术来制备重组表达载体、转染宿主细胞、选择转化体、培养宿主细胞并回收抗体。
[0150]
如果要使抗lingo
‑
1抗体或lingo
‑
1结合片段在细菌细胞(例如大肠杆菌)中表达,则表达载体应具有允许该载体在细菌细胞中扩增的特性。此外,当使用大肠杆菌(诸如jm109、dh5α、hb101,或xl1
‑
blue)作为宿主时,载体必须具有可允许在大肠杆菌中高效表达的启动子,例如lacz启动子(ward等人,341:544
‑
546(1989)、arab启动子(better等人,science,240:1041
‑
1043(1988))或t7启动子。此类载体的示例包括例如m13系列载体、puc系列载体、pbr322、pbluescript、pcr
‑
script、pgex
‑
5x
‑
1(pharmacia)、“qiaexpress system”(qiagen)、pegfp和pet(当使用该表达载体时,宿主优选是表达t7 rna聚合酶的bl21)。表达载体可含有用于抗体分泌的信号序列。为了生产到大肠杆菌的周质中,可以将pelb信号序列(lei等人,j.bacteriol.,169:4379(1987))用作用于抗体分泌的信号序列。对于细菌表达,可以使用氯化钙方法或电穿孔方法将表达载体引入到细菌细胞中。
[0151]
如果要使所述抗体在动物细胞(诸如cho、cos和nih3t3细胞)中表达,则表达载体
包含在这些细胞中表达所必需的启动子,例如sv40启动子(mulligan等人,nature,277:108(1979))、mmlv
‑
ltr启动子、ef1α启动子(mizushima等人,nucleic acids res.,18:5322(1990)),或cmv启动子。除了编码免疫球蛋白或其结构域的核酸序列之外,重组表达载体还可带有额外序列,诸如调控载体在宿主细胞中的复制的序列(例如,复制起点)和可选择标记基因。可选择标记基因有助于对已引入载体的宿主细胞进行选择(参见例如美国专利号4,399,216、4,634,665和5,179,017)。例如,通常可选择标记基因赋予已引入载体的宿主细胞对诸如g418、潮霉素或甲氨蝶呤的药物的抗性。具有可选择标记的载体的示例包括pmam、pdr2、pbk
‑
rsv、pbk
‑
cmv、poprsv和pop13。
[0152]
在一个实施方案中,抗体是在哺乳动物细胞中生产的。用于表达抗体的示例性哺乳动物宿主细胞包括中国仓鼠卵巢(cho细胞)(包括描述于urlaub和chasin(1980)proc.natl.acad.sci.usa 77:4216
‑
4220中的dhfr
–
cho细胞,其与例如如kaufman和sharp(1982)mol.biol.159:601
‑
621中描述的dhfr可选择标记一起使用)、人胚胎肾293细胞(例如,293、293e、293t)、cos细胞、nih3t3细胞、淋巴细胞系(例如,ns0骨髓瘤细胞和sp2细胞),以及来自转基因动物(例如转基因哺乳动物)的细胞。举例来说,该细胞可以是乳腺上皮细胞。在具体实施方案中,哺乳动物细胞是cho
‑
dg44i细胞。在另一示例中,哺乳动物细胞是cho
‑
k1细胞。
[0153]
在用于抗体表达的示例性系统中,通过磷酸钙介导的转染将编码抗lingo
‑
1抗体(例如li81)的抗体重链和抗体轻链的重组表达载体引入到dhfr
‑
cho细胞中。在重组表达载体内,抗体重链和轻链基因各自可操作地连接至增强子/启动子调控元件(例如,来源于sv40、cmv、腺病毒等,诸如cmv增强子/admlp启动子调控元件或sv40增强子/admlp启动子调控元件)以驱动所述基因的高水平转录。重组表达载体也带有dhfr基因,该dhfr基因允许使用甲氨蝶呤选择/扩增来选择已用载体转染的cho细胞。培养经选择的转化宿主细胞以允许抗体重链和轻链的表达,并且从培养基中回收该抗体。
[0154]
抗体还可由转基因动物产生。例如,美国专利号5,849,992描述了使抗体在转基因哺乳动物的乳腺中表达的方法。构建一种转基因,该转基因包括乳特异性启动子和编码感兴趣的抗体的核酸以及用于分泌的信号序列。由此类转基因哺乳动物的雌性产生的乳包括分泌于乳中的感兴趣的抗体。所述抗体可从乳中纯化,或对于一些应用来说,直接使用。还提供了包含本文所述的核酸中的一种或多种核酸的动物。
[0155]
可以从宿主细胞的内部或外部(诸如培养基)分离本公开的抗体,并将其纯化为基本上纯的且均质的抗体。通常用于抗体纯化的分离和纯化方法可以用于抗体的分离和纯化,并且不限于任何特定方法。可以通过适当地选择和组合例如柱色谱、过滤、超滤、盐析、溶剂沉淀、溶剂提取、蒸馏、免疫沉淀、sds
‑
聚丙烯酰胺凝胶电泳、等电聚焦、透析和重结晶来分离和纯化抗体。色谱包括例如亲和色谱、离子交换色谱、疏水色谱、凝胶过滤、反相色谱和吸附色谱(strategies for proteinpurification and characterization:a laboratory course manual.ed daniel r.marshak等人,cold spring harbor laboratory press,1996)。可以使用液相色谱法(诸如hplc和fplc)进行色谱。用于亲和色谱的柱包括蛋白a柱和蛋白g柱。使用蛋白a柱的柱的示例包括hyper d、poros和sepharose ff(ge healthcare biosciences)。本公开还包括使用这些纯化方法高度纯化的抗体。
[0156]
治疗方法
[0157]
本文所述的抗lingo
‑
1抗体组合物(例如,li81)可用于预防性和治疗性治疗有需要的受试者(例如人受试者)的cns脱髓鞘疾病。
[0158]
上述抗lingo
‑
1抗体(例如,li81)或其lingo
‑
1结合片段可以不同剂量施用于受试者,例如,人受试者。可以将抗lingo
‑
1抗体(例如,li81)或其lingo
‑
1结合片段作为固定剂量(即,独立于患者的体重)或以mg/kg剂量(即,基于受试者的体重而变化的剂量)施用。如本文所用的剂量单位形式或“固定剂量”是指适合于作为待治疗受试者的单位剂量的物理离散单位;每个单位均含有经计算可与需要的药物载体结合并且任选地与其他剂结合产生期望的治疗效果的预定量的活性化合物。可以给予单剂量或多剂量。治疗可以持续数天、数周、数月或甚至数年。
[0159]
在一个实施方案中,为了治疗本文所述的适应症,抗lingo
‑
1抗体(例如,li81)或其lingo
‑
1结合片段的剂量是750mg的固定剂量。
[0160]
上述固定剂量可各自在一段时间段内每天、每周、每2周、每4周、每6周、每8周、每月、每两周、每周或每天(视情况而定)施用,以涵盖至少2剂、3剂、4剂、5剂、6剂、7剂、8剂、9剂、10剂、12剂、14剂、16剂,18剂、20剂、22剂、24剂或更多剂。在一些实施方案中,每4周一次肠胃外施用750mg的固定剂量。
[0161]
在某些实施方案中,在由人受试者的医疗保健提供者确定对该受试者有益的时间段内,每4周向该人受试者施用750mg固定剂量的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些情况下,每4周向人受试者施用750mg固定剂量的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些实施方案中,向受试者施用至少4剂、至少5剂、至少6剂、至少7剂、至少8剂、至少9剂或至少10剂750mg固定剂量的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些实施方案中,向受试者施用4剂、5剂、6剂、7剂、8剂、9剂或10剂750mg固定剂量的抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些情况下,向受试者施用2剂至24剂、2剂至20剂、2剂至18剂、2剂至16剂、2剂至14剂、2剂至12剂、2剂至10剂或2剂至8剂50mg固定剂量的抗lingo
‑
1抗体或其lingo
‑
1结合片段。
[0162]
药物组合物可包含“治疗有效量”的本文所述的剂。此类有效量可以基于所施用剂的效果,或剂的组合效果(如果使用多于一种剂的话)来确定。剂的治疗有效量也可以根据诸如以下的因素变化:个体的疾病状态、年龄、性别和体重,以及所述化合物在个体中引发期望应答的能力。治疗有效量也是其中治疗上有益的作用超过所述组合物的任何毒性或有害作用的量。在一个实施方案中,抗lingo
‑
1抗体或其lingo
‑
1结合片段的治疗有效量为每4周一次地施用的750mg。
[0163]
抗lingo
‑
1抗体或其lingo
‑
1结合片段的施用途径和/或方式可以针对个体受试者进行定制。对于许多应用来说,施用途径是下面中的一种:皮下注射(sc)、静脉内注射或输注(iv)、腹腔内施用(ip),或肌内注射。在一个实施方案中,施用途径为皮下施用。在另一个实施方案中,施用途径为静脉内施用。
[0164]
应注意,本文所述的高浓度抗lingo
‑
1抗体组合物可直接施用,或可在施用前稀释(例如,在生理盐水中)。例如,如果要静脉内施用750mg剂量的抗lingo
‑
1抗体,并且高浓度抗lingo
‑
1抗体组合物含有200mg/ml的抗lingo
‑
1抗体(例如,本文所述的li81抗体),则可以简单地将3.75ml的200mg/ml溶液添加到100ml生理盐水溶液(例如,0.9%w/v nacl)袋中,并且可以静脉内施用该体积(即,103.75ml体积)。
[0165]
还应注意的是,如果要将750mg剂量的抗lingo
‑
1抗体与未稀释的高浓度抗lingo
‑
1抗体组合物一起施用(例如,皮下施用),则可将全剂量分为多次注射以达到全剂量。例如,对于皮下注射,特别是由患者自行施用的皮下注射,可能希望注射体积小于1.5ml以最小化注射部位的疼痛。如果抗lingo
‑
1抗体的全剂量为750mg,并且高浓度抗lingo
‑
1抗体组合物含有200mg/ml的抗lingo
‑
1抗体,则可以在三个注射部位施用全剂量,每个部位1.25ml(即每个注射部位施用250mg抗lingo
‑
1抗体)。当然,在一些实施方案中,如果患者可在单个注射部位耐受1.875ml的体积,则可通过在两个不同注射部位两次注射1.875ml 200mg/ml的抗lingo
‑
1抗体组合物来获得750mg的全剂量。
[0166]
可以用医疗装置施用包含单独的抗lingo
‑
1抗体或其lingo
‑
1结合片段,或抗lingo
‑
1抗体或其lingo
‑
1结合片段与一种或多种非lingo
‑
1抗体剂(例如,免疫调节剂诸如那他珠单抗或干扰素1β)的组合的药物组合物。该装置可以被设计为具有诸如便携性、室温贮存和易用性的特征,以便它可以在紧急情况下,例如,由未经培训的受试者或现场急救人员使用,并移至医疗设施和其他医疗设备中。该装置可包括例如用于贮存包含抗lingo
‑
1抗体或其lingo
‑
1结合片段的药物制品的一个或多个外壳,并且可被配置为递送一个或多个单位剂量的阻断剂。
[0167]
例如,药物组合物可用无针皮下注射装置,诸如us 5,399,163;5,383,851;5,312,335;5,064,413;4,941,880;4,790,824;或4,596,556中所公开的装置来施用。熟知的植入物和模块的示例包括:us4,487,603,其公开了用于以受控速率分配药物的可植入微输注泵;us4,486,194,其公开了用于经由皮肤施用药物的治疗装置;us 4,447,233,其公开了用于以精确输注速率递送药物的药物输注泵;us 4,447,224,其公开了用于连续药物递送的变速流可植入输注设备;us 4,439,196,其公开了具有多腔室隔室的渗透药物递送系统;以及us 4,475,196,其公开了渗透药物递送系统。许多其他装置、植入物、递送系统和模块也是已知的。
[0168]
在一个实施方案中,用针筒将抗lingo
‑
1抗体或其lingo
‑
1结合片段施用于人受试者。在另一个实施方案中,使用用于皮下递送的泵将抗lingo
‑
1抗体或其lingo
‑
1结合片段施用于人受试者。在一些实施方案中,用自动注射器将抗lingo
‑
1抗体或其lingo
‑
1结合片段施用于人受试者。在其他实施方案中,用皮下大容量注射器将抗lingo
‑
1抗体或其lingo
‑
1结合片段施用于人受试者。
[0169]
本公开还提供了一种针筒,该针筒包含药物组合物的无菌制品,该药物组合物包含如上所述的抗lingo
‑
1抗体(例如,li81)或其lingo
‑
1结合片段。如本文所用,术语“针筒”共同包括能够向受试者施用一定体积的组合物的泵、针筒和注射器(例如,自动注射器、皮下大容量注射器)。针筒可适用于皮下施用抗lingo
‑
1抗体或其lingo
‑
1结合片段。在一些情况下,针筒或泵递送固定剂量(例如,750mg)的抗lingo
‑
1抗体或其lingo
‑
1结合片段。
[0170]
因此,在一些实施方案中,本发明提供了包括至少两个针筒(例如,适于皮下施用)的试剂盒,该至少两个针筒包含包含如上所述的抗lingo
‑
1抗体(例如,li81)或其lingo
‑
1结合片段的药物组合物的无菌制品,其中包含在所述至少两个针筒内的抗lingo
‑
1抗体(或其lingo
‑
1结合片段)的全剂量是固定剂量,诸如750mg的lingo
‑
1抗体。在一些实施方案中,在所述组合物包含200mg/ml的抗lingo
‑
1抗体的情况下,该试剂盒提供三个针筒,该三个针筒中的每个针筒均包含1.25ml体积的所述组合物。在一些实施方案中,在所述组合物包含
200mg/ml的抗lingo
‑
1抗体的情况下,该试剂盒提供两个针筒,该两个针筒中的每个针筒包含1.875ml体积的组合物。
[0171]
在一些实施方案中,该试剂盒进一步包含免疫调节剂,诸如下述免疫调节剂之一,例如,含有适当剂量的免疫调节剂的针筒或口服可摄取制剂。该试剂盒可进一步包括,例如,针对施用包含抗lingo
‑
1抗体的组合物的说明书,以及任选地,针对施用免疫调节剂的说明书。
[0172]
免疫调节剂
[0173]
若干免疫调节剂目前被用于改变患者的多发性硬化症的过程,并且可以与包含抗lingo
‑
1抗体或其lingo
‑
1结合片段的组合物一起施用。此类剂包括但不限于ifn
‑
β1分子;谷氨酸、赖氨酸、丙氨酸和酪氨酸的聚合物,例如格拉替雷;抗α
‑
4整联蛋白的抗体或其片段,例如那他珠单抗;蒽二酮分子,例如米托蒽醌;芬戈莫德,例如,fty720;富马酸酯,例如富马酸二甲酯、富马酸地洛西美,或富马酸单甲酯,例如,口服富马酸酯,例如富马酸二甲酯、富马酸地洛西美,或富马酸单甲酯;针对t细胞的il
‑
2受体的α亚基(cd25)的抗体,例如达珠单抗;抗cd52的抗体,例如,阿仑单抗;二氢乳清酸脱氢酶抑制剂,例如特立氟胺;针对cd20的抗体,例如奥美珠单抗;和皮质类固醇。本文公开的修复剂可与这些剂中的任何一种剂组合使用。
[0174]
示例性免疫调节剂更详细地描述如下。
[0175]
ifnβ剂(β干扰素)
[0176]
用于ms的一种已知疗法包括用干扰素β治疗。干扰素(ifn)是由大多数动物的免疫系统细胞响应于外部剂诸如病毒、细菌、寄生虫和肿瘤细胞的攻击而产生的天然蛋白质。干扰素属于称为细胞因子的糖蛋白大类。干扰素β具有165个氨基酸。干扰素α和β是由许多细胞类型产生,该许多细胞类型包括t细胞和b细胞、巨噬细胞、成纤维细胞、内皮细胞、成骨细胞及其他细胞,并且刺激巨噬细胞和nk细胞两者。干扰素γ参与了免疫和炎性应答的调控。它是由活化的t细胞和th1细胞产生的。
[0177]
目前几种不同类型的干扰素已被批准用于人。干扰素α(包括以下形式:干扰素α
‑
2a、干扰素α
‑
2b、和干扰素alfacon
‑
1)被美国食品与药物管理局(fda)批准作为丙型肝炎的治疗。目前存在两种fda批准的干扰素β类型。干扰素β1a与在人中天然发现的干扰素β同一,并且干扰素β1b在某些方面与人中天然存在的干扰素β1a不同,包括其在17位处含有丝氨酸残基以代替半胱氨酸残基。干扰素β的其他用途包括治疗aids、皮肤t细胞淋巴瘤、急性丙型肝炎(非甲型、非乙型)、卡波济氏肉瘤、恶性黑色素瘤、毛细胞白血病和转移性肾细胞癌。
[0178]
ifnβ剂可通过本领域中已知的任何方法向受试者施用,包括全身地(例如,口服、肠胃外、皮下、静脉内、直肠、肌内、玻璃体内、腹膜内、鼻内、透皮或通过吸入或腔内安装)施用。通常,ifnβ剂是皮下或肌内施用的。
[0179]
ifnβ剂可用于治疗使用本文所述的方法确定为“响应者”的那些受试者。在一个实施方案中,ifnβ剂被用作单一疗法(即,用作单一“改变病情疗法”),但是治疗方案可进一步包括使用“症状管理疗法”,例如抗抑郁剂、镇痛剂、抗震颤剂等。在一个实施方案中,ifnβ剂是ifnβ
‑
1a剂(例如,)。在另一个实施方案中,infβ剂是infβ
‑
1b剂(例
如,)。
[0180]
(一种干扰素β
‑
1a)适用于治疗使用本文所述的方法被确定为响应者的患有复发型ms的患者,以减缓身体残疾的累积并降低临床恶化的频率。(干扰素β
‑
1a)是具有大约22,500道尔顿的预测分子量的166个氨基酸的糖蛋白。它是使用引入有人干扰素β基因的经遗传工程化的中国仓鼠卵巢细胞,通过重组dna技术而产生的。的氨基酸序列与天然人干扰素β的氨基酸序列同一。(干扰素β
‑
1a)的推荐剂量为每周一次肌内注射30mcg。可作为30mcg冻干粉末小瓶或30mcg预灌装的针筒商购获得。
[0181]
干扰素β1a与在人中天然发现的干扰素β(即干扰素β1a(swissprot登记号p01574和gi:50593016)同一。干扰素β的序列为:
[0182]
mtnkcllqialllcfsttalsmsynllgflqrssnfqcqkllwqlngrleyclkdrm nfdipeeikqlqqfqkedaaltiyemlqnifaifrqdssstgwnetivenllanvyhqin hlktvleeklekedftrgklmsslhlkryygrilhylkakeyshcawtivrveilrnfyfinrltgylrn(seq id no:90)。
[0183]
用于制备的方法是本领域已知的。
[0184]
对使用本文所述的方法鉴别的应答者的治疗进一步考虑了具有大体上类似于的生物活性的生物活性的组合物(例如,ifnβ1a分子)在以类似方式施用时将允许类似于用进行的治疗的成功治疗。此类其他组合物包括例如具有大体上类似的生物活性的其他干扰素及其片段、类似物、同源物、衍生物和天然变体。在一个实施方案中,infβ剂被修饰成增加一种或多种药代动力学性质。例如,infβ剂可为包括聚乙二醇化部分的修饰形式的干扰素1a。聚乙二醇化形式的干扰素β1a描述于例如baker,dp等人(2006)bioconjug chem 17(1):179
‑
88;arduini,rm等人(2004)protein expr purif 34(2):229
‑
42;pepinsky,rb等人(2001)j.pharmacol.exp.ther.297(3):1059
‑
66;baker,dp等人(2010)j interferon cytokine res30(10):777
‑
85中(所有这些文献都以引用方式整体并入本文,并且描述了在其n末端α氨基酸处被修饰成包括peg部分,例如,20kda的mpeg
‑
o
‑2‑
甲基丙醛部分的人干扰素β1a)。聚乙二醇化形式的ifnβ1a可通过例如可注射的施用途径(例如,皮下地)施用。
[0185]
也是干扰素β
‑
1a剂,而和是干扰素β
‑
1b剂。和都被调配用于通过皮下注射来施用。
[0186]
待施用的ifnβ剂的剂量可由本领域技术人员确定,并且包括待基于所用的特定干扰素
‑
β剂施用的临床上可接受的量。例如,通常每周一次经由肌内注射以30微克施用。例如每周三次以22微克或每周一次以44微克,经由皮下注射施用其他形式的干扰素β1a,特别是可例如以介于10μg与50μg之间的量肌内施用干扰素β
‑
1a。例如,可每五至十天,例如每周一次施用而可每周三次施用
[0187]
抗vla4抗体(例如,那他珠单抗)
[0188]
抗vla4抗体(例如,那他珠单抗)抑制白细胞从血液迁移到中枢神经系统。这些抗体结合至活化的t细胞及其他单核白细胞的表面上的vla
‑
4(也称为α4βl)。它们可破坏t细
胞与内皮细胞之间的粘附,并且由此防止单核白细胞迁移穿过内皮并进入到实质中。因此,促炎性细胞因子的水平也可降低。那他珠单抗可减少患有复发缓解型多发性硬化症和复发继发性进展性多发硬化症的患者中的脑病变的数目以及残疾的临床复发和累积。
[0189]
那他珠单抗和相关vla
‑
4结合抗体描述于例如美国专利号5,840,299中。单克隆抗体21.6和hp1/2是结合vla
‑
4的示例性鼠类单克隆抗体。那他珠单抗是人源化型式的鼠类单克隆抗体21.6(参见,例如美国专利号5,840,299)。还已描述了人源化型式的hp1/2(参见例如美国专利号6,602,503)。若干额外的vla
‑
4结合单克隆抗体诸如hp2/1、hp2/4、l25和p4c2描述于例如以下文献中:美国专利号6,602,503;sanchez
‑
madrid等人(1986)eur.j.immunol 16:1343
‑
1349;hemler等人(1987)j biol.chem.2:11478
‑
11485;issekutz等人(1991)j immunol 147:109(ta
‑
2mab);pulido等人(1991)j biol.chem.266:10241
‑
10245;以及美国专利号5,888,507)。上述出版物的内容(包括抗体组合物、剂量、施用和生产方法)以引用方式整体并入本文。
[0190]
富马酸二甲酯
[0191]
富马酸二甲酯,dmf是富马酸酯。dmf被认为减少了白细胞穿过血脑屏障,并且通过激活抗氧化途径,特别是经由激活nrf
‑
2途径发挥神经保护作用(lee等人(2008)int ms journal 15:12
‑
18)。研究还提示,具有降低炎性细胞对cns的活性和影响并诱导cns细胞中的直接细胞保护应答的潜能。这些效应可增强cns细胞减轻在ms病理生理中起作用的有毒的炎性和氧化应激的能力。
[0192]
醋酸格拉替雷
[0193]
(醋酸格拉替雷)由合成多肽,特别是四种天然存在的氨基酸:l
‑
谷氨酸、l
‑
丙氨酸、l
‑
酪氨酸和l
‑
赖氨酸的醋酸盐组成(bornstein等人(1987)n engl j med.317:408
‑
414)。表现出与髓鞘碱性蛋白的结构相似性并且被认为通过使t辅助细胞1型应答转变为t辅助细胞2型应答而起到免疫调节剂的作用(duda等人(2000)j clin invest 105:967
‑
976;nicholas等人(2011)drug design,development,and therapy 5:255
‑
274)。
[0194]
米托蒽醌(蒽二酮分子)
[0195]
米托蒽醌是蒽二酮分子(1,4
‑
二羟基
‑
5,8
‑
双[2
‑
(2
‑
羟乙基氨基)乙基胺基]
‑
蒽
‑
9,10
‑
二酮),并且是一种破坏dna合成和细胞修复的ii型拓扑异构酶抑制剂。其被用于治疗癌症和ms。米托蒽醌被用于治疗若干形式的晚期ms,包括继发进展型ms、进展复发型ms和晚期复发
‑
缓解型ms。
[0196]
例如,米托蒽醌可有效减缓继发进展型ms的进展并延长复发
‑
缓解型ms与进展复发型ms的复发之间的时间(fox e(2006)clin ther 28(4):461
‑
74)。
[0197]
芬戈莫德(鞘氨醇1
‑
磷酸酯受体调节剂)
[0198]
芬戈莫德是被批准用于治疗ms的免疫调节药物。它将复发缓解型多发性硬化症的复发率降低了一半以上,但可能会具有严重的副作用。芬戈莫德是鞘氨醇1
‑
磷酸酯受体调节剂,其隔离淋巴结中的淋巴细胞,从而防止它们移动到中枢神经系统中以进行ms的自身免疫应答。
[0199]
针对t细胞il
‑
2受体的α亚基(cd25)的抗体(例如,达珠单抗hyp;)
[0200]
针对t细胞的il
‑
2受体的α亚基(cd25)的抗体(例如,达珠单抗hyp)可在本文公开的方法和组合物中使用。达珠单抗hyp是针对t细胞il
‑
2受体α亚基(cd25)的治疗性人源化单克隆抗体。达珠单抗hyp在降低患有复发缓解型多发性硬化症的患者中的病变和年复发率方面显示出功效(kappos等人(2015).n.engl.j.med.373(15):1418
‑
28)。
[0201]
针对cd52的抗体,例如阿仑单抗
[0202]
针对cd52的抗体,例如,阿仑单抗(目前作为正在进一步开发中),结合至cd52,其为成熟淋巴细胞的表面上而不是干细胞上存在的蛋白质。iii期研究报告了在治疗患有复发缓解型ms(rrms)的患者中比较阿仑单抗与(高剂量皮下干扰素β
‑
1a)的阳性结果。阿仑单抗在欧洲已获得批准。
[0203]
针对cd20的抗体,例如奥美珠单抗
[0204]
针对cd20的抗体,例如,奥美珠单抗、利妥昔单抗,奥法木单抗靶向成熟的b淋巴细胞。对在复发缓解型ms中进行的利妥昔单抗和奥美珠单抗的2期临床研究已证实,通过脑病变所测量(例如,通过mri扫描所测量)的疾病活动性和复发率与安慰剂相比在统计学上显著降低。奥美珠单抗的3期研究显示与干扰素β
‑
1a(例如,)相比,复发率和残疾率都降低。
[0205]
二氢乳清酸脱氢酶抑制剂,例如特立氟胺
[0206]
二氢乳清酸脱氢酶抑制剂,例如特立氟胺,抑制嘧啶合成。特立氟胺(也称为a77 1726或)是来氟米特的活性代谢物。特立氟胺抑制被认为推动ms的疾病进程的包括活化的t细胞在内的快速分裂的细胞。特立氟胺作为用于治疗ms的药物在临床试验中进行了研究。(vollmerems news(2009年5月28日))。
[0207]
类固醇
[0208]
类固醇(例如皮质类固醇)和acth剂可用于治疗复发缓解型ms或继发性进展型ms的急性复发。此类剂包括但不限于此类剂包括但不限于和
[0209]
前述免疫调节剂中的一种或多种免疫调节剂可与本文所公开的抗lingo
‑
1抗体(或其lingo
‑
1结合片段)组合使用。
[0210]
以下是实践本发明的实施例。这些实施例不应被解读为以任何方式限制本发明的范围。
[0211]
实施例
[0212]
开发了含有抗lingo
‑
1抗体的制剂,以在广泛的临床剂量范围内实现广泛范围的肠胃外递送选项(皮下(sc、肌内(im)和静脉内(iv))。为了最大化药品呈现的灵活性,以高浓度制剂为目标。成功标准涉及在最小化产品粘度的同时获得稳定的产品质量特征。当不稀释地施用或在适当的静脉内媒介物(用于输注的0.9%盐水或5%葡萄糖)中稀释(例如,稀释成50ml或100ml)施用时,下文描述的制剂适用于肠胃外施用(包括皮下、肌内和静脉内施用)。
[0213]
实施例1:早期缓冲剂组分筛选
[0214]
进行制剂开发活动以研究高浓度稳定性。如下所示,这些活动表明与早期型式的
制剂中使用的柠檬酸盐缓冲剂相比,组氨酸是一种优越的缓冲体系。
[0215]
所测试的制剂如下:
[0216]
制剂1a:50mg/ml li81、10mm柠檬酸盐、160mm精氨酸盐酸盐和0.03%聚山梨醇酯80
[0217]
制剂2a:50mg/ml li81、10mm组氨酸(如游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸盐酸盐和0.03%聚山梨醇酯80
[0218]
制剂2e:50mg/ml li81、10mm组氨酸(如游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸盐酸盐、10mm甲硫氨酸和0.03%聚山梨醇酯80
[0219]
制剂3a:175mg/ml li81、10mm柠檬酸盐、160mm精氨酸盐酸盐,和0.03%聚山梨醇酯80
[0220]
制剂4a:175mg/ml li81、10mm组氨酸(如游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸盐酸盐,和0.03%聚山梨醇酯80
[0221]
制剂4e:175mg/ml li81、10mm组氨酸(如游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸盐酸盐、10mm甲硫氨酸和0.03%聚山梨醇酯80
[0222]
对于这些研究,使用连接到配备a280检测器的waters hplc仪器的tsk
‑
gel g3000swxl柱(7.8mm
×
30cm,5μm粒径)通过尺寸排除色谱法(sec)分析样品。使用来自waters corporation(milford,ma)的empower 2软件上的标准积分途径确定每个样品的所有二聚体和更高级可溶性聚集体种类(被称为总聚集体%)。
[0223]
图1示出了在保持其他制剂条件一致的同时,随着缓冲剂种类的改变抗
‑
lingo的制剂的长期稳定性数据。如图1所示,制剂4a(组氨酸,无柠檬酸盐)表现出比制剂3a(柠檬酸盐,无组氨酸)更好的长期稳定性。
[0224]
因此,基于这些结果,从制剂中去除柠檬酸盐并用组氨酸代替。
[0225]
实施例2:精氨酸hcl和ph水平的研究
[0226]
进行实验的制剂设计以研究选定的抗
‑
lingo制剂条件—蛋白质浓度、ph和精氨酸hcl浓度与它们对稳定性和粘度的影响之间的关系。
[0227]
对于这些研究,在介于480
‑
3900s
‑1之间的三种不同剪切速率下测量平均粘度。粘度特性被证实在剪切速率范围内是牛顿性的。粘度数据表示在介于480
‑
3900s
‑1之间的剪切速率下测量的三个读数的平均值。所有粘度测量均使用由rheosense inc.(san ramon,ca)供应的基于m
‑
vroc针筒的粘度计执行。
[0228]
使用连接到配备a280检测器的waters hplc仪器的tsk
‑
gel g3000swxl柱(7.8mm
×
30cm,5μm粒径)通过尺寸排除色谱法(sec)分析样品。使用来自waters corporation(milford,ma)的empower 2软件上的标准积分途径确定每个样品的所有二聚体和更高级可溶性聚集体种类(被称为总聚集体%)。
[0229]
将观察到的高分子量(hmw)百分比按照制剂的ph绘制成曲线。如图2所示,随着制剂ph的降低,聚集增加,其中浓度依赖性聚集在较低的ph下更加明显。例如,在ph 6.6
‑
6.8下,所有浓度具有几乎相同的低聚集量。然而,在介于约6.05与6.3之间的ph下,最高蛋白质
浓度(220mg/ml)具有最高量的聚集,而最低蛋白质浓度(170mg/ml)处于与在最高ph下观察到的相同的低水平。在最低的ph(例如,低于5.8)下,最高浓度(220mg/ml)具有最高量的聚集,而最低浓度(170mg/ml)具有最低量的聚集。
[0230]
这些结果表明,抗
‑
lingo的最佳制剂ph大于(>)6.2。
[0231]
接下来分析制剂中精氨酸的量。结果表明,将制剂中精氨酸hcl的浓度从160mm增加到高达300mm,对稳定性和溶液粘度的影响可忽略不计(参见图3)。换言之,制剂中的精氨酸hcl浓度不会显著影响抗lingo
‑
1聚集。
[0232]
然而,当查看多个变量(例如,ph、精氨酸浓度和粘度)时,很明显,制剂ph对含有抗lingo
‑
1制剂的粘度有显著影响(参见图4)。
[0233]
换言之,发现制剂ph对粘度有显著影响(图4),其中随着制剂ph增加,粘度降低。
[0234]
总之,这些结果表明含有抗lingo
‑
1的制剂的最佳制剂ph>6.2。基于这项工作,6.5的制剂ph适合于抗lingo
‑
1的稳定性和粘度。
[0235]
实施例3:高浓度制剂赋形剂筛选
[0236]
执行赋形剂筛选研究,以鉴定可有助于在保持所需质量属性的同时降低粘度的赋形剂。这项工作聚焦于鉴定可在高蛋白质浓度下保持稳定性(如通过按照尺寸排除色谱的聚集所指示的)和所需粘度水平两者的赋形剂。赋形剂水平被设计为等渗的,以确保与肠胃外注射施用途径的相容性。使用连接到配备a280检测器的waters hplc仪器的tsk
‑
gel g3000swxl柱(7.8mm
×
30cm,5μm粒径)通过尺寸排除色谱法(sec)分析样品。使用来自waters corporation(milford,ma)的empower 2软件上的标准积分途径确定每个样品的所有二聚体和更高级可溶性聚集体种类(被称为总聚集体%)。
[0237]
本实施例中的所有制剂均包含225mg/ml的抗lingo
‑
1抗体(例如,li81)、20mm组氨酸缓冲剂(游离碱形式的组氨酸和组氨酸盐酸盐的组合)和0.03%聚山梨醇酯80(ph 6.5)。表4示出了图5中使用的样品id号和额外赋形剂的量。
[0238]
表4:
[0239][0240]
对于用各种赋形剂配制的抗lingo,测量在40℃下贮存的3个月内高分子量物质(聚集)的变化。图5提供了上表2中列出的18种制剂的稳定性数据。需注意,图5中具有小于或等于3%的hmv(sec)的制剂(例如,来自表4的id 9)具有所需的稳定性特征,而图5中具有大于3%hmv(sec)的制剂(例如,来自表4的id 2)具有不太理想或非期望的稳定性特征。如图5所示,精氨酸hcl(来自表4中的id3和id 4)、脯氨酸(来自表4的id 15)和蔗糖(来自表4的id 13)稳定抗lingo
‑
1抗体的聚集。图5中的数据还证明精氨酸hcl和甲硫氨酸的组合(来自表4的id 9)以及精氨酸hcl和脯氨酸的组合(来自表4的id 8)稳定抗lingo聚集。来自表4和图5中的制剂id 3和id 4的比较表明,精氨酸hcl的稳定性益处存在于80mm下,并且使用增加浓度的精氨酸hcl未提供进一步的稳定性。
[0241]
将额外赋形剂添加到起始制剂(即,225mg/ml的抗lingo
‑
1抗体(例如,li81)、20mm组氨酸缓冲剂和0.03%聚山梨醇酯80(ph 6.5))中以创建新制剂来测试粘度。表5列出了这些新制剂,并且这些新制剂的结果在图6中给出。
[0242]
表5:
[0243][0244]
在480
‑
3900s
‑1之间的三种不同剪切速率下测量平均粘度粘度特性被证实在剪切速率范围内是牛顿性的。粘度数据表示在介于480
‑
3900s
‑1之间的剪切速率下测量的三个读数的平均值。所有粘度测量均使用由rheosense inc.(san ramon,ca)供应的基于m
‑
vroc针筒的粘度计执行。
[0245]
图6提供了上表5中列出的制剂的制剂粘度测量数据。应注意,图6中在20℃下小于或等于50cp的制剂(例如,来自表5的id 11)适合于自行施用,而图6中在20℃下大于50cp的制剂(例如,来自表5的id 18)不太适合或不适合于可自行施用。如图6所示,含有精氨酸hcl的制剂最有效地降低了粘度(来自表5的制剂id 3、id 4、id 5、id 9、id 10、id 11、id 12)。对含和不含精氨酸hcl的赋形剂组合的评估表明,精氨酸hcl是驱动制剂粘度降低的赋形剂。来自表5和图6的制剂id 3和id 9的比较表明,精氨酸hcl的粘度降低益处在80mm下是明显的,并且通过增加精氨酸hcl浓度(即增加到160mm)无法实现显著的额外粘度降低。
[0246]
对该实施例的稳定性和粘度数据的评估表明精氨酸hcl对稳定性是有益的并且可用于粘度管理。脯氨酸或甲硫氨酸在基于精氨酸hcl的制剂中的添加展现出稳定性益处。蔗糖在基于精氨酸hcl的制剂中的添加可提供稳定性益处。
[0247]
实施例4:稳定性评估
[0248]
选择下表6中列出的制剂进行长期稳定性评估。
[0249]
表6
[0250][0251][0252]
如上表6所示,所有制剂均含有20mm组氨酸/组氨酸hcl缓冲剂(游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)和0.05%聚山梨醇酯80,并且所有制剂均是基于精氨酸盐酸盐的。研究了精氨酸hcl与脯氨酸的组合以及精氨酸hcl与蔗糖的组合。还研究了略微升高的ph(7.0)和蛋白质浓度(230mg/ml)。
[0253]
图7和图8分别示出了在5℃和25℃下随着时间的推移,上表6中列出的制剂的高分子量物质(聚集体)的增加。如图7和图8所示,当基于精氨酸hcl的制剂中包含甲硫氨酸或脯氨酸时,观察到了稳定性益处。当制剂中包含蔗糖时,观察到了可接受的稳定性;然而,蔗糖的纳入导致粘度升高。与不含甲硫氨酸(已知的抗氧化剂)的制剂1相比,脯氨酸在制剂中的纳入导致抗lingo氧化减少。
[0254]
在本实施例4中检查的六种制剂中,200mg/ml抗lingo
‑
1、20mm组氨酸(游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸hcl、10mm甲硫氨酸、0.05%聚山梨醇酯80(ph 6.5)(来自上表6的制剂2)提供了最佳的稳定性和粘度特征。制剂5(200mg/ml抗lingo、20mm组氨酸(游离碱形式的组氨酸、组氨酸盐酸
盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、80mm精氨酸hcl、160mm脯氨酸、0.05%聚山梨醇酯80(ph 6.5))提供了可接受的替代的抗lingo的制剂。
[0255]
制剂2(来自表6)在至少50mg/ml至230mg/ml的广泛的抗lingo浓度范围内提供了稳定性。期望的稳定性和粘度特征所需的精氨酸hcl水平在80mm至160mm的范围内,超过80mm的量有助于形成适合于肠胃外注射的等渗溶液。甲硫氨酸水平范围可为5mm至25mm,并且聚山梨醇酯水平范围可为0.01%(w/v)至0.09%
[0256]
类似的范围适用于制剂5(表6),其中脯氨酸驱动高于80mm精氨酸hcl的张力。应注意,此制剂中不包含甲硫氨酸。
[0257]
实施例5:目标制剂的长期稳定性
[0258]
200mg/ml抗lingo
‑
1、20mm组氨酸(游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸hcl、10mm甲硫氨酸、0.05%聚山梨醇酯80(ph 6.5)的目标制剂是使用代表性的中试原料药工艺制造的,随后被灌装到玻璃小瓶中以实现长期药品稳定性。使用acquity uplc系统、acquity beh200 sec保护柱和分析柱以及uv检测,通过sec测量%高分子量(%hmw)。在每个时间点,在sec运行缓冲液中将样品稀释至75mg/ml。将0.3μl(25μg)的每种样品注入柱上,并使用以下运行缓冲剂进行洗脱:100mm磷酸钠、200mm nacl(ph 6.8),流速为0.35ml/min。每个样品的运行时间为10min。
[0259]
图9中提供的按照尺寸排除色谱数据的聚集体百分比表明,目标制剂中的200mg/ml抗lingo
‑
1在2
–
8℃的预期储存条件下可稳定至少4年。通过sec测定的聚集是稳定性的首要指标。
[0260]
200mg/ml抗lingo
‑
1抗体(例如,li81)、20mm组氨酸(游离碱形式的组氨酸、组氨酸盐酸盐,或游离碱形式的组氨酸和组氨酸盐酸盐的组合)、160mm精氨酸hcl、10mm甲硫氨酸、0.05%聚山梨醇酯80(ph 6.5)的制剂满足稳定性和粘度要求。此外,指定的制剂是等渗溶液,适用于肠胃外施用。当未稀释注射时,该制剂可适合于皮下和肌内注射。该制剂也适用于以未稀释或在0.9%生理盐水(nacl)或5%葡萄糖媒介物中稀释至低至1mg/ml的浓度的形式静脉内输注。
[0261]
实施例6:目标制剂的长期稳定性
[0262]
表7提供了制备本文所述的制剂中的一种制剂的非限制性配方:
[0263]
表7
[0264]
组分名称量li81抗体200mgl
‑
组氨酸2.2mgl
‑
精氨酸盐酸盐33.7mgl
‑
组氨酸盐酸盐一水合物1.2mgl
‑
甲硫氨酸1.5mg聚山梨醇酯800.5mg无菌水0mg
[0265]
其他实施方案
[0266]
虽然本发明已结合本发明的详细说明来描述,但是前述描述旨在说明而非限制本发明的范围,本发明的范围由所附权利要求书的范围所限定。其他方面、优势和修改在所附
权利要求书的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。