1.本发明涉及具有良好悬浮稳定性以及良好的免疫原性的羟基氧化铝佐剂材料的制备方法,具体说是纳米羟基氧化铝佐剂制备方法以及相关性质表征。
背景技术:
2.疫苗的发现可谓是人类发展史上一件具有里程碑意义的事件,控制传染性疾病最主要的手段就是预防,而接种疫苗被认为是最行之有效的措施。作为疫苗的重要组成部分,佐剂在指导和增强抗原的免疫反应中起着极其重要的作用。佐剂可以诱导人体产生长期,高效的特异性免疫反应,从而提高人体的保护能力。预防性疫苗中常见的铝佐剂包括羟基氧化铝和磷酸铝,羟基氧化铝占据重要的一部分。疫苗开发过程中的总体目标是配制和生产具有最佳免疫原性的安全稳定的产品,铝佐剂疫苗的效果受到多种因素影响,包括抗原,辅料等,其中铝佐剂是及其重要的一部分。其中配苗过程中需要重新均质后与抗原吸附,另外基于铝基疫苗制造的铝基疫苗是悬浮药物产品(dp),给药前也必须重新均质。基于需要解决铝佐剂疫苗制剂在储存后最终产品的再分散方面问题,在给药过程中均质性较差的疫苗会导致疫苗效果降低或者疫苗给药不足的现象,因此研究合成分散性,悬浮稳定性良好的,易于重悬的羟基氧化铝佐剂具有重要的意义。
技术实现要素:
3.本发明的目的是提供一种用廉价易得的反应原料以及简单的生产方法获得形貌均一,分散性悬浮稳定性良好的,易于重悬的,有优良免疫原性,可工业化生产的羟基氧化铝纳米佐剂的制备方法。
4.本发明的目的通过以下技术方案来实现:
5.一种悬浮稳定性良好的米粒状羟基氧化铝纳米佐剂的制备方法,包括以下步骤:
6.1)取无机铝盐与一定比例碱性固体完全溶解于去离子水形成透明澄清的前驱体混合溶液;
7.3)将上述混合均匀的澄清透明溶液转移至一定大小的反应釜中在一定温度下水热一定时间。
8.4)对上述产物冷却、离心、洗涤、干燥,得到羟基氧化铝粉末固体。
9.对于上文所述制备方法的技术方案中,优选的情况下,步骤1)所述的无机铝盐为九水合硝酸铝或六水合氯化铝,本发明中的前驱物材料是铝源。
10.对于上文所述制备方法的技术方案中,优选的情况下,步骤1)所述的碱性固体是氢氧化钾,氢氧化钠或尿素。
11.对于上文所述制备方法的技术方案中,优选的情况下,步骤1)所述的混合溶液中铝盐的浓度为0.03
‑
0.08m,碱性固体的浓度为0.03
‑
0.35m。
12.对于上文所述制备方法的技术方案中,优选的情况下,步骤1)所述的溶解过程在
搅拌条件下进行;所述的搅拌条件为:搅拌转速为400
‑
1000rpm,优选为400
‑
600rpm,搅拌时间为10
‑
20min,优选为15min;此处混合液反应总体积为50ml
‑
2l。
13.对于上文所述制备方法的技术方案中,优选的情况下,步骤2)所述的水热条件为:水热温度优选为160℃
‑
200℃,水热时间优选为20
‑
100min,更优选为20
‑
80min。
14.对于上文所述制备方法的技术方案中,优选的情况下,步骤3)中,所述冷却为将混合处理后的混合液空冷降温至室温即可;所述的离心转速为4000
‑
9000rpm,优选为8000rpm;离心时间为5
‑
40min,优选为5
‑
10min;所述的洗涤目的是除去所含杂质,洗涤次数为3
‑
5次,具体实施例中洗涤过程具体采用先乙醇后去离子水水洗两到三次除去所含杂质;干燥温度为50
‑
80℃,干燥时间为10
‑
24h。
15.对于上文所述制备方法的技术方案中,优选的情况下,步骤2)和3)之间还包括灭菌:对上述混合液在121℃条件下进行灭菌处理30min。
16.本发明的另一方面在于保护上文所述方法制备的悬浮稳定性良好的米粒状羟基氧化铝纳米佐剂。
17.本发明的有益效果:
18.本发明以水热法为基础合成悬浮稳定性良好,易于分散,免疫原性良好的米粒状羟基氧化铝纳米材料的制备方法,该方法利用无机铝盐和碱性固体(尿素)的混合溶液作为反应物,通过水热方法制备纳米尺寸的羟基氧化铝佐剂,所制备的羟基氧化铝佐剂纳米材料形貌均一,分散均匀,具有很好的均质性和免疫原性,对比现有的商业化羟基氧化铝佐剂突出优良的悬浮稳定性,在疫苗制备与生产及应用中具有良好的前景。
附图说明
19.图1是实施例1中不同浓度碱性固体条件下收集所得的羟基氧化铝纳米佐剂的透射电镜图。图1a
‑
d分别为铝盐与碱性固体摩尔比为1:2,1:4,1:6,1:13下反应所得的羟基氧化铝佐剂材料。其中,标尺为500nm。
20.图2是实施例1中不同碱性固体浓度下所得羟基氧化铝胶体的x射线衍射表征结果
21.图3是实施例1中不同碱性固体浓度下所得羟基氧化铝纳米佐剂和市场售卖的商业化羟基氧化铝,在盐溶液条件下的沉降结果。
22.图4是实施例1中不同碱性固体浓度下所得羟基氧化铝纳米佐剂和市场售卖的商业化羟基氧化铝吸附牛血清蛋白(bsa)抗原后在盐溶液条件下的沉降结果,采用invivogen购买的adjuvant,在盐溶液条件下的沉降结果。
23.图5是实施例1中不同碱性固体浓度下所得羟基氧化铝纳米佐剂吸附乙肝(hbv)抗原后进行的动物实验的总igg抗体滴度实验结果。
24.图6是实施例1中不同碱性固体浓度下所得羟基氧化铝纳米佐剂吸附乙肝(hbv)抗原后进行的动物实验的igg1抗体滴度实验结果。
具体实施方式
25.下述非限定性实施例可以使本领域的普通技术人员更全面地理解本发明,但不以任何方式限制本发明。
26.下述实施例中alhydrogel为市场售卖的商业化羟基氧化铝,采用invivogen购买
的adjuvant,cas号:21645
‑
51
‑
2。
27.实施例1
28.准确称取0.9375g九水合硝酸铝分别与0.3g(铝盐与碱性固体摩尔比为1:2),0.6g(铝盐与碱性固体摩尔比为1:4),0.9g(铝盐与碱性固体摩尔比为1:6),1.95g(铝盐与碱性固体摩尔比为1:13)的尿素在室温下溶解到50ml去离子水中,对溶液进行搅拌速率控制在500rpm搅拌至完全溶解于去离子水形成透明澄清的溶液。将澄清透明溶液转移至50ml的高压反应釜中,水热条件控制在水热温度为165℃,水热时间为70min。反应结束后放置冷却至室温,之后开始收集产物。待自然冷却至室温,采用先乙醇后去离子水水洗两到三次除去所含杂质,60℃下恒温干燥16h,得到白色粉末状固体,即为所得产物羟基氧化铝纳米佐剂(将铝盐与碱性固体摩尔比分别为1:2,1:4,1:6,1:13下反应所得的羟基氧化铝佐剂材料,依次命名为nanorice1,nanorice2,nanorice3,nanorice4)。
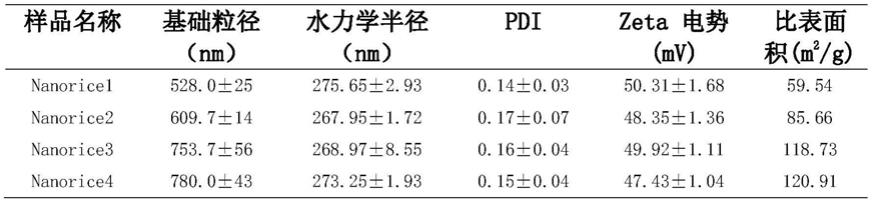
29.对上述合成的羟基氧化铝佐剂材料经过表征,透射电子显微镜法(tem)结果显示各浓度碱合成的羟基氧化铝佐剂均为米粒状结构(结果见图1),对透射电子显微镜法(tem)结果图进行纳米粒子进行分析,羟基氧化铝佐剂的平均粒径分布在500
‑
800nm之间(结果见表1)。用动态光散射仪(dls,pals)测定了羟基氧化铝纳米颗粒的流体力学尺寸和zeta电位。羟基氧化铝纳米颗粒的dls在200
‑
300nm纳米级尺寸,zeta电势50mv左右较高,pdi结果很小,材料分散性很好(结果见表1)。比表面积测试仪(bet)检测羟基氧化铝纳米颗粒的比表面积随着碱浓度的增大而逐渐增大(结果见表1)。检测羟基氧化铝纳米颗粒材料的悬浮稳定性以及吸附抗原后的悬浮稳定性良好,选择乙肝(hbv)、牛血清蛋白(bsa)作为抗原模型。定性使用生理盐水配置浓度均为1.1mg/ml的alhydrogel、nanorice1、nanorice2、nanorice3、nanorice4纳米佐剂溶液静置0h与12h进行拍照图像显示,定量采用紫外
‑
可见分光光度法在12h的时间间隔内,通过监测光吸光度(232nm)与时间的关系来测定悬浮液的稳定性指数(结果见图3)。吸附抗原后的悬浮稳定性通过使用生理盐水配置浓度均为1.1mg/ml的alhydrogel、nanorice1、nanorice2、nanorice3、nanorice4纳米佐剂混合液,其中添加49.5ug/ml的bsa,37℃下孵育30min后实现抗原的吸附,将吸附抗原后的纳米佐剂溶液静置0h与12h进行拍照图像显示,定量采用紫外
‑
可见分光光度法在12h的时间间隔内,通过监测光吸光度(232nm)与时间的关系来测定悬浮液的稳定性指数(结果见图4)。将生理盐水作为缓冲液,配置50ul缓冲液包含1111ug羟基氧化铝佐剂以及2ug的hbv的疫苗,将疫苗以每50ul的量于第0天和第21天肌内免疫于小鼠的胫骨前肌。生理盐水缓冲液组作为ctrl对照。hbv单独溶解在生理盐水缓冲液中作为hbv组。第42天采集血清,elisa检测乙肝抗原(hbv)总igg、igg1,结果该组佐剂的免疫原性结果很好(结果见图5和6)。
30.表1是实施例1中不同碱性固体浓度下所得羟基氧化铝纳米佐剂的水合粒径分布及zeta电势表征结果,以及比表面积,表面羟基量的表征结果
31.32.对于任何熟悉本领域的技术人员而言,在不脱离本发明技术方案范围情况下,都可利用上述揭示的技术内容对本发明技术方案做出许多可能的变动和修饰,或修改为等同变化的等效实施例。因此,凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同变化及修饰,均应仍属于本发明技术方案保护的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。