1.本发明涉及基因检测技术领域,具体涉及一种用于同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒。
背景技术:
2.近些年,在养猪生产中多种病原混合感染已成普遍现象。猪群发病,常常不是单一病原引起的,而是由两种或者多种病原共同作用造成的,延误了诊断和防治,导致猪群高发病率和高死亡率,造成极大的经济损失。在存在多病原混合感染的猪场,猪病临床症状复杂,病例变化不典型,病情严重,现场难以确诊,一般防治措施也难以奏效。对各病毒的检测可采用传统的诊断方法,比如病毒分离检测法或血清学检测方法。病毒分离检测方法存在操作方法繁琐,诊断时间长以及由于采样样本污染造成的结果不确定等问题,血清学诊断方法因病毒的变异株不断出现,导致该方法在实际应用中受到诸多限制,此外,这两种方法都存在检测灵敏度低的缺点。
3.目前市场上核酸检测试剂盒以荧光定量pcr检测试剂盒为主,此类试剂盒一般采用的方法都是taqman探针法,这也跟我们国内公布的各类病原的核酸检测标准所要求的方法一致。taqman探针法是在常规pcr基础上加入荧光标记探针来实现其定量功能的,与普通pcr相比,荧光定量pcr具有许多优点。它融汇pcr技术的核酸高效扩增、探针技术的高特异性、光谱技术个高敏感性和高精确定量的优点,直接探测pcr过程中荧光信号的变化以获得定量的结果。与传统pcr技术相比,它具有操作简便、快速、高效的优点。其次,它是在完全封闭的体系中完成扩增,实现实时监测,消除交叉污染。第三,无需凝胶电泳,只需通过特殊探头在反应管内直接检测。第四,定量结果准确,重现性好。因此,该项技术受到许多科研工作者的重视,并在很多领域得以应用。
4.商品化的pcr试剂盒多为单项pcr,1个试剂盒1次试验仅能检测1种病原,对于混合感染2种及以上的病原的同份猪病病料要确诊其病原就要2种及以上试剂盒并进行2次及以上的pcr试验,不仅费时费力,检测成本也较高。因此,开发一种可以同步检测2种及以上的病原且敏感性高的方法就非常有应用价值。
技术实现要素:
5.本发明为解决上述技术问题提供了一种用于同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒,以简单、快速、高效的检测非洲猪瘟病毒和猪伪狂犬病毒。
6.本发明解决上述技术问题的技术方案如下:一种用于同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒,所述试剂盒为多重荧光定量pcr试剂盒,包括用于分别扩增非洲猪瘟病毒cd2v基因、非洲猪瘟病毒p72基因和猪伪狂犬病毒epo基因的引物对以及对应的荧光探针,所述用于扩增cd2v基因的引物对为asfv
‑
cd2v
‑
f和asfv
‑
cd2v
‑
r,其对应的荧光探针为asfv
‑
cd2v
‑
p,所述用于扩增p72基因的引物对为asfv
‑
p72
‑
f和asfv
‑
p72
‑
r,其对应的荧光探针为asfv
‑
p72
‑
p,所述用于扩增epo的引物对为prv
‑
epo
‑
f和prv
‑
epo
‑
r,其对应的荧光探
针为prv
‑
epo
‑
p,所述asfv
‑
cd2v
‑
f、asfv
‑
cd2v
‑
r、asfv
‑
cd2v
‑
p、asfv
‑
p72
‑
f、asfv
‑
p72
‑
r、asfv
‑
p72
‑
p、prv
‑
epo
‑
f、prv
‑
epo
‑
r和prv
‑
epo
‑
p的核苷酸序列分别如seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8和seq id no:9所示。
7.本发明的有益效果是:该试剂盒利用不同荧光染料标记不同病原检测靶点的特异性探针,可以同时检测非洲猪瘟病毒和猪伪狂犬病病毒,提高了检测的效率,并且针对非洲猪瘟病毒设计了cd2v、p72两个检测靶点,提高了检测的可靠性。本发明的试剂盒具有灵敏度高、特异性强的特点,适用于科研及临床应用,具有良好的商业应用价值。
8.在上述技术方案的基础上,本发明还可以做如下改进。
9.进一步,所述荧光探针asfv
‑
cd2v
‑
p、asfv
‑
p72
‑
p和prv
‑
epo
‑
p的5’端均标记有荧光报告基团,3’端均标记有荧光淬灭基团。
10.进一步,所述荧光探针asfv
‑
cd2v
‑
p的5’端标记的荧光报告基团为fam,3’端标记的荧光猝灭基团为bhq1,所述荧光探针asfv
‑
p72
‑
p的5’端标记的荧光报告基团为rox,3’端标记的荧光猝灭基团为bhq2,所述荧光探针prv
‑
epo
‑
p的5’端标记的荧光探针为cy5,3’端标记的荧光猝灭基团为bhq3。
11.进一步,所述试剂盒还包括阳性对照,所述阳性对照包括含有非洲猪瘟病毒p72基因的重组质粒、含有非洲猪瘟病毒cd2v基因的重组质粒和含有猪伪狂犬病毒epo基因的重组质粒。
12.进一步,所述试剂盒还包括多重荧光定量pcr检测试剂和/或样本提取试剂。
附图说明
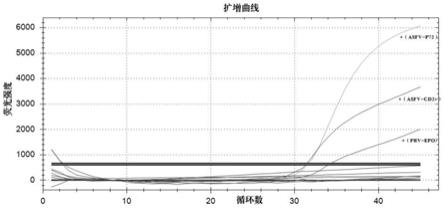
13.图1为本发明实施例2中多重荧光定量pcr的扩增曲线图;
14.图2为本发明实施例2中cd2v基因在不同tm值下的多重荧光定量pcr扩增曲线图;
15.图3为本发明实施例2中p72基因在不同tm值下的多重荧光定量pcr扩增曲线图;
16.图4为本发明实施例2中epo基因在不同tm值下的多重荧光定量pcr扩增曲线图;
17.图5为不同引物浓度下cd2v基因的多重荧光定量pcr扩增曲线图;
18.图6为不同引物浓度下p72基因的多重荧光定量pcr扩增曲线图;
19.图7为不同引物浓度下epo基因的多重荧光定量pcr扩增曲线图;
20.图8为不同荧光探针浓度下cd2v基因的多重荧光定量pcr扩增曲线图;
21.图9为不同荧光探针浓度下p72基因的多重荧光定量pcr扩增曲线图;
22.图10为不同荧光探针浓度下epo基因的多重荧光定量pcr扩增曲线图;
23.图11为实施例2中不同模板浓度下cd2v基因的多重荧光定量pcr扩增曲线图;
24.图12为实施例2中不同模板浓度下p72基因的多重荧光定量pcr扩增曲线图;
25.图13为实施例2中不同模板浓度下epo基因的多重荧光定量pcr扩增曲线图;
26.图14为实施例2中多重荧光定量pcr的特异性检测结果。
具体实施方式
27.以下结合附图及具体实施例对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
28.实施例1
29.为了对养猪生产中的多病原混合感染的病原菌进行检测,发明人设计了用于同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒,该试剂盒为多重荧光定量pcr试剂盒,对非洲猪瘟病毒cd2v基因、非洲猪瘟病毒p72基因和猪伪狂犬病毒epo基因进行检测。本试剂盒包括用于扩增非洲猪瘟病毒cd2v基因、非洲猪瘟病毒p72基因和猪伪狂犬病毒epo基因的引物对以及对应的荧光探针,根据genbank上公开的asfv cd2v、asfv
‑
p72和prv
‑
epo的基因序列,设计用于扩增cd2v基因的引物对asfv
‑
cd2v
‑
f和asfv
‑
cd2v
‑
r及其对应的荧光探针asfv
‑
cd2v
‑
p,用于扩增p72基因的引物对asfv
‑
p72
‑
f和asfv
‑
p72
‑
r及其对应的荧光探针asfv
‑
p72
‑
p,用于扩增epo的引物对为prv
‑
epo
‑
f和prv
‑
epo
‑
r及其对应的荧光探针prv
‑
epo
‑
p。
30.引物对及探针设计的具体方法为:将genbank上公开的对应的基因序列下载到本地进行引物及探针的设计,并利用primer 5.0进行分析,避免引物之间形成稳定的引物二聚体和发夹结构,并利用ncbi数据库对所有引物探针组进行特异性和覆盖度分析,保证它们的序列的特异性,同时可以覆盖目前已知的这两个病毒所有的基因型。
31.asfv
‑
cd2v
‑
f、asfv
‑
cd2v
‑
r、asfv
‑
cd2v
‑
p、asfv
‑
p72
‑
f、asfv
‑
p72
‑
r、asfv
‑
p72
‑
p、prv
‑
epo
‑
f、prv
‑
epo
‑
r和prv
‑
epo
‑
p的核苷酸序列分别如seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8和seq id no:9所示
32.asfv
‑
cd2v
‑
f:gaagaaatagaaagtccaycrcc(seq id no:1)
33.asfv
‑
cd2v
‑
r:gtaagggamatggkttgrgtg(seq id no:2)
34.asfv
‑
cd2v
‑
p:ttgtgttgagggacgcatgtartaaat(seq id no:3)
35.asfv
‑
p72
‑
f:ctgctcatggtatcaatcttatcga(seq id no:4)
36.asfv
‑
p72
‑
r:gataccacaagatcrgccgt(seq id no:5)
37.asfv
‑
p72
‑
p:ccacgggaggaataccaacccagtg(seq id no:6)
38.prv
‑
epo
‑
f:tcacctccatcctccaccac(seq id no:7)
39.prv
‑
epo
‑
r:ctgcccataragccagttgaag(seq id no:8)
40.prv
‑
epo
‑
p:ttcgtttgtggagacgcccgtgg(seq id no:9)
41.荧光探针asfv
‑
cd2v
‑
p、asfv
‑
p72
‑
p和prv
‑
epo
‑
p的5’端均标记有荧光报告基团,3’端均标记有荧光淬灭基团。荧光探针asfv
‑
cd2v
‑
p的5’端标记的荧光报告基团为fam,3’端标记的荧光猝灭基团为bhq1,荧光探针asfv
‑
p72
‑
p的5’端标记的荧光报告基团为rox,3’端标记的荧光猝灭基团为bhq2,荧光探针prv
‑
epo
‑
p的5’端标记的荧光探针为cy5,3’端标记的荧光猝灭基团为bhq3。
42.在一个优选的实施方案中,试剂盒还包括阳性对照,阳性对照包括含有非洲猪瘟病毒p72基因的重组质粒、含有非洲猪瘟病毒cd2v基因的重组质粒和含有猪伪狂犬病毒epo基因的重组质粒。
43.在一个优选的实施方案中,试剂盒还包括多重荧光pcr检测试剂和/或样本提取试剂。多重荧光pcr检测试剂包括qpcr buffer、dntp和taq dna聚合酶,样本提取试剂为核酸提取试剂。
44.实施例2一种同步检测非洲猪瘟病毒和猪伪狂犬病毒的方法
45.使用实施例1中的同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒进行非洲猪瘟病毒和猪伪狂犬病毒的检测。
46.根据genbank中公开的非洲猪瘟病毒(asfv)、猪伪狂犬病病毒(prv)的核酸序列分别合成含有cd2v、p72和epo部分序列的质粒,将上述3种质粒使用限制性内切酶进行线性化处理,经凝胶电泳后回收,利用分光光度计测量分别回收的这3种dna片段的浓度,按照通用的拷贝数换算公式获得这3种dna片段的拷贝数。按照拷贝数梯度稀释dna片段成1x106copies/ul、1x10
5 copies/ul、1x104copies/ul、1x103copies/ul、1x102copies/ul、1x101copies/ul、1x10
0 copies/ul共7个梯度,将每个浓度的梯度均作为模板进行多重荧光定量pcr
47.将合成的引物及荧光探针浓度均先稀释至50um的浓度。
48.多重荧光定量pcr的体系如下:
49.2x qpcr mix buffer 12.5ul,每个引物及荧光探针(50um)0.1ul;模板10ul,其余用depc
‑
h2o补充至25ul。
50.多重荧光定量pcr的扩增条件如下:
51.预变性95℃、1min;95℃、10s;59℃、40s、同步荧光信号收集,扩增45个循环。
52.图1为使用本发明实施例1的试剂盒在上述反应体系和反应条件下的多重荧光定量pcr的扩增曲线,证明该试剂盒在应用上述反应体系和扩增条件,可以很好的区分cd2v、p72和epo三个检测靶点。
53.引物及荧光探针浓度范围、退火温度范围通过试验确认,其中图2
‑
4分别为cd2v、p72和epo三个基因在不同tm值下的多重荧光定量pcr扩增曲线,证明退火温度在59℃就可以得到比较理想的ct值;图5
‑
7分别为不同引物浓度下cd2v、p72和epo三个基因的多重荧光定量pcr扩增曲线,证明引物浓度均在0.2um就可以得到理想的ct值;图8
‑
10为不同荧光探针浓度下cd2v、p72和epo三个基因的多重荧光定量pcr扩增曲线,证明荧光探针浓度均为0.2um就可以得到理想的ct值。
54.试剂盒灵敏度测试:
55.分别使用上述7个梯度稀释的dna片段为模板,按照上述体系和扩增条件进行多重荧光定量pcr,每个梯度设置3个复孔。结果如图11
‑
13所示,当反应体系中病毒核酸片段达到10个拷贝,即可获得有效的扩增信号。
56.试剂盒特异性测试:
57.以猪细小病毒基因组dna、猪圆环病毒
‑
i基因组dna、猪鼻支原体dna、大肠杆菌基因组dna和pk
‑
15细胞基因组dna为反应模板,以asfv
‑
p72、asfv
‑
cd2v和prv
‑
epo质粒混合物为阳性参照,depc
‑
h2o为空白对照,用本发明实施例1中的试剂盒进行检测,结果如图14所示,阳性对照有3条扩增曲线,而其他反应孔没有扩增曲线,说明使用该试剂盒进行非洲猪瘟病毒和猪伪狂犬病毒的检测具有良好的特异性。
58.本发明实施例1中的用于同步检测非洲猪瘟病毒和猪伪狂犬病毒的试剂盒利用不同荧光染料标记不同病原检测靶点的特异性探针,可以同时检测非洲猪瘟病毒和猪伪狂犬病病毒,提高了检测的效率,并且针对非洲猪瘟病毒设计了cd2v、p72两个检测靶点,提高了检测的可靠性。本发明的试剂盒具有灵敏度高、特异性强的特点,适用于科研及临床应用,具有良好的商业应用价值。
59.以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

