1.本发明涉及检验检测技术领域,特别涉及一种多糖浓度的检测方法。
背景技术:
2.现有的多糖浓度检测方法,主要有苯酚
‑
浓硫酸法、蒽酮
‑
浓硫酸法、硫酸
‑
咔唑法、碱性酒石酸钾钠铜滴定法等化学方法,气相色谱法(gc)、液相色谱法(lc)、高效阴离子交换色谱
‑
脉冲安培法、体积排除色谱法(vec)、薄层色谱(tlc)等色谱法,以及毛细管电泳法(ce),红外光谱法(ir)、毛细管电泳
‑
质谱联用技术(ce
‑
ms)、气相色谱
‑
质谱联用技术(gc
‑
ms)、液相色谱法(lc)
‑
质谱联用技术(lc
‑
ms)、糖谱法、速率比浊法等。
3.以上多糖浓度检测方法中,大多为损耗性检测,操作复杂,需要昂贵的仪器设备,耗时耗力。
技术实现要素:
4.本发明的主要目的是提出一种多糖浓度的检测方法及其应用,旨在提供一种简单、快捷的多糖浓度的检测方法。
5.为实现上述目的,本发明提出一种多糖浓度的检测方法,包括以下步骤:
6.s10、根据tds值与多糖浓度之间的数量关系,绘制多糖浓度标准曲线;
7.s20、获取待测液的tds值;
8.s30、根据所述tds值及所述多糖浓度标准曲线,确定待测液中的多糖浓度。
9.可选地,在步骤s10之前,所述多糖浓度的检测方法还包括:
10.s101、将多个不同量的多糖分别加入相同量的水中,充分搅拌溶解,得到多个多糖浓度不同的多糖标准溶液;
11.s102、分别测定每个所述多糖标准溶液的tds值。
12.可选地,所述多糖标准溶液的数量为n,n≥5。
13.可选地,所述多糖浓度的检测方法适用的多糖的浓度范围为0.1~200mg/l。
14.可选地,所述多糖浓度的检测方法的适用温度为20~25℃。
15.可选地,所述多糖包括水溶性淀粉、山药多糖、麦芽糊精多糖、阿拉伯胶、海藻酸钠、姜黄多糖、β
‑
葡聚糖、黄原胶中的一种。
16.本发明的技术方案中,提出一种多糖浓度的检测方法,建立多糖溶液的tds值与多糖溶液浓度之间的关系,如此,便可根据多糖溶液的tds值确定多糖溶液的浓度,而tds值的测定简单方便,仅需tds笔便可实现,因此,本发明提出的多糖浓度的测定方法,简单、方便、快捷,大大简化了多糖浓度检测的难度。
附图说明
17.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本
发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图示出的结构获得其他的附图。
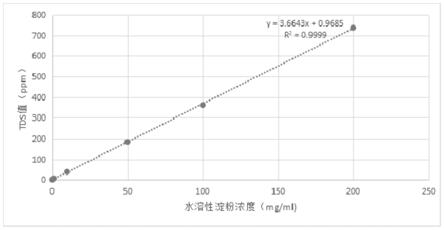
18.图1为本发明实施例1得到的水溶性淀粉浓度标准曲线;
19.图2为本法明实施例2中以本法明提出的多糖浓度的检测方法得到的山药多糖deae纤维素柱曲线;
20.图3为本发明实施例2中以苯酚
‑
浓硫酸法得到的山药多糖deae纤维素柱曲线;
21.图4为本发明实施例3得到的麦芽糊精浓度标准曲线;
22.图5为本发明实施例4得到的阿拉伯胶浓度标准曲线;
23.图6为本发明实施例5得到的海藻酸钠浓度标准曲线;
24.图7为本发明实施例6得到的姜黄多糖浓度标准曲线;
25.图8为本发明实施例7得到的β
‑
葡聚糖浓度标准曲线;
26.图9为本发明实施例8得到的黄原胶浓度标准曲线。
27.本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
28.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
29.需要说明,若本发明实施例中有涉及方向性指示(诸如上、下、左、右、前、后、外、内
……
),则该方向性指示仅用于解释在某一特定姿态(如附图所示)下各部件之间的相对位置关系、运动情况等,如果该特定姿态发生改变时,则该方向性指示也相应地随之改变。
30.另外,若本发明实施例中有涉及“第一”、“第二”等的描述,则该“第一”、“第二”等的描述仅用于描述目的,而不能理解为指示或暗示其相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。另外,全文中出现的“和/或”的含义,包括三个并列的方案,以“a和/或b”为例,包括a方案、或b方案、或a和b同时满足的方案。另外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本发明要求的保护范围之内。
31.现有的多糖浓度检测方法中,大多为损耗性检测,操作复杂,需要昂贵的仪器设备,耗时耗力。
32.鉴于此,本发明提出一种多糖浓度的检测方法及其应用,旨在提供一种简单、快捷的多糖浓度的检测方法。本发明附图中,图1为本发明实施例1得到的水溶性淀粉浓度标准曲线;图2为本法明实施例2中以本法明提出的多糖浓度的检测方法得到的山药多糖deae纤维素柱曲线;图3为本发明实施例2中以苯酚
‑
浓硫酸法得到的山药多糖deae纤维素柱曲线;图4为本发明实施例3得到的麦芽糊精浓度标准曲线;图5为本发明实施例4得到的阿拉伯胶浓度标准曲线;图6为本发明实施例5得到的海藻酸钠浓度标准曲线;图7为本发明实施例6得到的姜黄多糖浓度标准曲线;图8为本发明实施例7得到的β
‑
葡聚糖浓度标准曲线;图9为本发明实施例8得到的黄原胶浓度标准曲线。
33.本发明提出的多糖浓度的检测方法,包括以下步骤:
34.s10、根据tds值与多糖浓度之间的数量关系,绘制多糖浓度标准曲线;
35.s20、获取待测液的tds值;
36.s30、根据所述tds值及所述多糖浓度标准曲线,确定待测液中的多糖浓度。
37.本发明的技术方案中,提出一种多糖浓度的检测方法,建立多糖溶液的tds值与多糖溶液浓度之间的关系,如此,便可根据多糖溶液的tds值确定多糖溶液的浓度,而tds值的测定简单方便,仅需tds笔便可实现,因此,本发明提出的多糖浓度的测定方法,简单、方便、快捷,大大简化了多糖浓度检测的难度。
38.可以理解的是,tds为total dissolved solids的缩写,意思是溶解于水中的总固体含量,指水中全部溶质的总量。测量单位为ppm或毫克/升(mg/l),它表明1升水中溶有多少毫克溶解性固体。由于tds值是根据电导率计算得到的,和电导率存在一种相通的关系,tds也可以用来表示电导率,两者的关系:1ppm tds=2μs/cm,而在本发明实施例中,多糖溶液的导电性较差,因此,tds值在本发明实施例中并不严格是溶解于水中的总固体量,但tds值与溶液中多糖的浓度在一定范围内呈线性关系,如此,便可根据tds值确定溶液中多糖的浓度。
39.tds值可以用市面上常见的tds笔进行测量,tds笔使用方法一般是:打开tds笔探针盖,按下标有on/off按钮,待液晶屏显示后,将tds笔插入被测溶液中,待数值稳定后,读取数值,测试完毕后,自来水冲洗干净tds笔探针后盖上保护套,操作方便。
40.本发明提出的多糖浓度的检测方法,待测溶液测试完可以回收他用,不需要对待测溶液进行化学预处理,可直接对待测溶液进行检测快速得出结果,不需要特定的酶或抗体,对多糖的种类无特殊要求。
41.此外,由于tds值测定的限制性,为了保证tds值测量的准确性,本发明实施例的多糖浓度的测定方法不能用于流速过大的流体中,如流速高于4m/s。
42.优选地,在步骤s10之前,所述多糖浓度的检测方法还包括:
43.s101、将多个不同量的多糖分别加入相同量的水中,充分搅拌溶解,得到多个多糖浓度不同的多糖标准溶液;
44.s102、分别测定每个所述多糖标准溶液的tds值。
45.通过多糖标准溶液的配制以及其对应的tds值的测定,便于后续绘制标准曲线及拟合方程。
46.优选地,所述多糖标准溶液的数量为n,n≥5。可以理解,多糖标准溶液的数量越多,拟合得到的标准曲线越准确,为了保证准确性,优选地,多糖标准溶液的数量不少于5个。
47.优选地,所述多糖浓度的检测方法适用的多糖的浓度范围为0.1~200mg/l。在上述浓度范围内,多糖的浓度测量较为准确。浓度较大的溶液,可以稀释一定倍数后进行测量。
48.此外,多糖的溶解度会随温度的变化而变化,优选地,在本发明实施例中,所述多糖浓度的检测方法的适用温度为20~25℃。例如可以是20℃、21℃、22℃、23℃、24℃、25℃等,上述温度范围内,拟合得到的曲线线性度较高。
49.本发明实施例中的多糖为所有可溶性多糖,包括来源于植物、动物、微生物的水溶
性多糖。优选地,所述多糖包括水溶性淀粉、山药多糖、麦芽糊精多糖、阿拉伯胶、海藻酸钠、姜黄多糖、β
‑
葡聚糖、黄原胶中的一种。研究表明,上述多糖的线性度良好,测量较为准确。
50.本发明进一步提出一种如上所述的多糖浓度的检测方法的应用,在多糖的提纯过程中采用所述的多糖浓度的检测方法测定溶液中多糖的浓度。在多糖的提纯过程中,不可避免地需要监测溶液中多糖的浓度,采用本发明提出的多糖浓度的检测方法,具备了上述多糖浓度检测方法的全部有益效果,在此不再一一赘述。
51.优选地,所述多糖纯化方法为柱层析分离净化法。柱层析法又称色层法或色谱法,分离原理是根据物质在固定相上的吸附能力不同而进行分离,一般情况下极性大的物质易被固定相吸附,极性小的物质不易被固定相吸附,柱层析过程即是吸附、解吸、再吸附和再解吸的过程,与其它分离方法相比较具有能耗低、淋洗剂易于回收再利用和所得产品纯度高等优点。
52.以下结合具体实施例对本发明的技术方案作进一步详细说明,应当理解,以下实施例仅仅用以解释本发明,并不用于限定本发明。
53.实施例1
54.(1)将六个不同量的水溶性淀粉分别加入相同量的水中,充分搅拌溶解,得到六个多糖浓度分别为200mg/ml、100mg/ml、50mg/ml、10mg/ml、1mg/ml、0.1mg/ml的多糖标准溶液;
55.(2)分别测定每个所述多糖标准溶液的tds值;
56.(3)以水溶性淀粉多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制水溶性淀粉多糖浓度标准曲线,并进行线性回归分析,结果如图1所示,在0.1mg/ml~200mg/ml范围内,得标准曲线:y=3.6643x 0.9685,r2=0.9999,线性较好。
57.1、准确度测量
58.配制浓度分别为120mg/ml、100mg/ml、80mg/ml的水溶性淀粉供试液各3份,分别测定其tds值,通过标准曲线计算浓度,计算回收率,结果如表1。可以看出,水溶性淀粉供试液回收率在98%以上,rsd(标准偏差系数)在0.80%~1.82%间,<2%,准确度较高。
59.表1水溶性淀粉回收率试验结果
60.浓度(mg/ml)平均回收率(%)rsd(%)12099.010.8010099.070.558098.601.82
61.2、检出限测量
62.以纯水为空白对照,配制浓度分别为1mg/ml、0.1mg/ml、0.01mg/ml、0.001mg/ml的水溶性淀粉供试液,分别测定其tds值,结果如表2所示。由表2数据可知,扣除纯水的误差,能够准确定量测定被测物质的最低浓度是0.1mg/ml,因此本方法的检出限为0.1mg/ml。
63.表2水溶性淀粉检出限试验结果
[0064][0065]
[0066]
3、定量限测量
[0067]
配制6份浓度为0.1mg/ml的水溶性淀粉供试液,分别测定其tds值,结果如表3所示。由表3数据可得,定量限为0.1mg/ml。
[0068]
表3水溶性淀粉定量限试验结果
[0069] 123456平均值rsd(%)tds值(ppm)22222220
[0070]
4、重复性测量
[0071]
配制6份浓度为100mg/ml的水溶性淀粉供试液,分别测定其tds值,结果如表4所示。由表4数据可得,rsd=1.09%<2.0%,重复性较好。
[0072]
表4水溶性淀粉重复性试验结果
[0073] 123456平均值rsd(%)tds值(ppm)362366359358368361362.331.09
[0074]
5、稳定性测量
[0075]
配制3份浓度为100mg/ml的水溶性淀粉供试液,分别在0h、1h、2h、4h、8h、12h、24h、48h时间后,测定其tds值,结果如表5所示。由表5数据可得,rsd=1.59%<2.0%,稳定性较好。
[0076]
表5水溶性淀粉稳定性试验结果
[0077] 0h1h2h4h8h12h24h48h平均值rsd(%)tds值(ppm)362362362362368372374375367.131.59%
[0078]
实施例2
[0079]
50ml山药粗多糖上样,deae纤维素柱层析,柱体积为:3.5
×
14.5cm,纯水常压洗脱,流速为2.5ml/min,每4分钟收集一管。分别用本发明提出的多糖浓度的测定方法测定各管的tds值,得到图2,用苯酚
‑
浓硫酸法在480nm波长下测各管的吸光度a,得到图3,苯酚
‑
浓硫酸法测定多糖浓度是本领域常见的方法,在此不再赘述。
[0080]
比较图2和图3可见,两图的变化趋势是完全一致的,因此,用本发明提出的多糖浓度的测定方法,在进行山药多糖柱层析分离洗脱过程中,也可方便快捷无损耗地得到与苯酚
‑
浓硫酸法相同的结果。两种方法最后所得的结果都是合并13
‑
31管,32
‑
48管。
[0081]
实施例3
[0082]
(1)将六个不同量的麦芽糊精分别加入相同量的水中,充分搅拌溶解,得到六个多糖浓度分别为200mg/ml、100mg/ml、50mg/ml、10mg/ml、1mg/ml、0.1mg/ml的麦芽糊精多糖标准溶液;
[0083]
(2)分别测定每个所述多糖标准溶液的tds值;
[0084]
(3)以麦芽糊精多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制麦芽糊精多糖浓度标准曲线,并进行线性回归分析,结果如图4所示,在0.1mg/ml~200mg/ml范围内,得标准曲线:y=1.4262x 6.6676,r2=0.9991,线性较好。
[0085]
实施例4
[0086]
(1)将六个不同量的阿拉伯胶分别加入相同量的水中,充分搅拌溶解,得到六个多糖浓度分别为200mg/ml、100mg/ml、50mg/ml、10mg/ml、1mg/ml、0.1mg/ml的阿拉伯胶多糖标
准溶液;
[0087]
(2)分别测定每个所述多糖标准溶液的tds值;
[0088]
(3)以阿拉伯胶多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制阿拉伯胶多糖浓度标准曲线,并进行线性回归分析,结果如图5所示,在0.1mg/ml~200mg/ml范围内,得标准曲线:y=5.9232x
‑
4.8119,r2=0.9992,线性较好。
[0089]
实施例5
[0090]
(1)将八个不同量的海藻酸钠分别加入相同量的水中,充分搅拌溶解,得到八个多糖浓度分别为20mg/ml、10mg/ml、5mg/ml、2.5mg/ml、1.25mg/ml、0.63mg/ml、0.32mg/ml、0.16mg/ml的海藻酸钠多糖标准溶液;
[0091]
(2)分别测定每个所述多糖标准溶液的tds值;
[0092]
(3)以海藻酸钠多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制海藻酸钠多糖浓度标准曲线,并进行线性回归分析,结果如图6所示,在0.16mg/ml~20mg/ml范围内,得标准曲线:y=269.15x 31.195,r2=0.9998,线性较好。
[0093]
实施例6
[0094]
(1)将六个不同量的姜黄多糖分别加入相同量的水中,充分搅拌溶解,得到六个多糖浓度分别为200mg/ml、100mg/ml、50mg/ml、10mg/ml、1mg/ml、0.1mg/ml的姜黄多糖多糖标准溶液;
[0095]
(2)分别测定每个所述多糖标准溶液的tds值;
[0096]
(3)以姜黄多糖多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制姜黄多糖多糖浓度标准曲线,并进行线性回归分析,结果如图7所示,在0.1mg/ml~200mg/ml范围内,得标准曲线:y=46.244x
‑
33.136,r2=0.9965,线性较好。
[0097]
实施例7
[0098]
(1)将五个不同量的β
‑
葡聚糖分别加入相同量的水中,充分搅拌溶解,得到五个多糖浓度分别为100mg/ml、50mg/ml、25mg/ml、12.5mg/ml、6.3mg/ml的β
‑
葡聚糖多糖标准溶液;
[0099]
(2)分别测定每个所述多糖标准溶液的tds值;
[0100]
(3)以β
‑
葡聚糖多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制β
‑
葡聚糖多糖浓度标准曲线,并进行线性回归分析,结果如图8所示,在6.3mg/ml~100mg/ml范围内,得标准曲线:y=4.4951x
‑
4.4294,r2=0.9957,线性较好。
[0101]
实施例8
[0102]
(1)将五个不同量的黄原胶分别加入相同量的水中,充分搅拌溶解,得到五个多糖浓度分别为2.5mg/ml、1.25mg/ml、0.63mg/ml、0.32mg/ml、0.16mg/ml的黄原胶多糖标准溶液;
[0103]
(2)分别测定每个所述多糖标准溶液的tds值;
[0104]
(3)以黄原胶多糖标准溶液的多糖浓度为横坐标(x),多糖标准溶液的tds值(y)为纵坐标,绘制黄原胶多糖浓度标准曲线,并进行线性回归分析,结果如图9所示,在0.16mg/ml~2.5mg/ml范围内,得标准曲线:y=18.163x 3.1455,r2=0.9977,线性较好。
[0105]
综上,本发明提出的多糖浓度的测定方法,简单、方便、快捷,大大简化了多糖浓度检测的难度,且准确度、稳定性、重复性均较好。
[0106]
以上所述仅为本发明的优选实施例,并非因此限制本发明的专利范围,凡是在本发明的发明构思下,利用本发明说明书及附图内容所作的等效结构变换,或直接/间接运用在其他相关的技术领域均包括在本发明的专利保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。