一种双途径拮抗pcsk9的重组基因、载体、外泌体及制备方法和应用
技术领域
1.本发明涉及基因工程领域,特别是涉及一种双途径拮抗pcsk9的重组基因、载体、外泌体及制备方法和应用。
背景技术:
2.高脂血症系人体脂代谢失调所致,主要是指血清总胆固醇(tc),甘油三脂(tg)水平过高,血低密度脂蛋白胆固醇(ldl
‑
c)水平过高或血高密度脂蛋白胆固醇(hdl
‑
c)水平过低,是导致动脉粥样硬化的一个重要因素,是公认的高血压、冠心病和脑血管意外的主要危险因素。
3.防治高脂血症一直是医学领域的重要课题之一。降脂治疗可减轻或避免动脉粥样硬化的发生,从而降低冠心病和脑卒中的发病率。目前虽有较多降脂药物,但长期应用多有不良反应。现阶段,pcsk9已成为新式降脂作用靶点,但pcsk9拮抗剂多为单克隆抗体、rna干扰药物及模拟肽等,存在制备成本高,副作用未知,稳定性差,拮抗效率有限等一系列亟待解决的问题。因此,从高效拮抗pcsk9着手寻求一种有效治疗高脂血症和动脉粥样硬化且副作用小的方法是迫在眉睫的。
技术实现要素:
4.为了解决上述问题,本发明提供了一种双途径拮抗pcsk9的重组基因、载体、外泌体及制备方法和应用。本发明所述重组基因能够有效治疗高脂血症和动脉粥样硬化,而且具有副作用小、成本低、稳定性高、拮抗效率高的优势。
5.为了实现上述目的,本发明提供如下技术方案:
6.本发明提供了一种双途径拮抗pcsk9的重组基因,所述重组基因从3’端至5’端包括依次连接kozak片段、cd63第一片段、outer
‑
egf
‑
a片段、cd63第二片段、inner
‑
egf
‑
a片段和flag标签。
7.优选的,所述kozak片段的核苷酸序列如seq id no.3所示;所述cd63第一片段的核苷酸序列如seq id no.4所示;所述outer
‑
egf
‑
a基因的核苷酸序列如seq id no.5所示;所述cd63第二片段的核苷酸序列如seq id no.6所示;所述inner
‑
egf
‑
a片段的核苷酸序列如seq id no.7所示;所述flag标签的核苷酸序列如seq id no.8所示。
8.优选的,所述重组基因的核苷酸序列如seq id no.1所示。
9.优选的,在所述重组基因的3’端还包括酶切位点hindⅲ,5’端还包括酶切位点xhoⅰ。
10.优选的,所述重组基因的核苷酸序列如seq id no.2所示。
11.本发明提供了一种包括上述重组基因的重组表达载体,所述重组表达载体的基础质粒包括pcdna3.1( )。
12.本发明提供了一种双途径拮抗pcsk9的外泌体,外泌体携带跨膜蛋白的基因序列
包括上述重组基因或上述重组表达载体。
13.本发明提供了上述外泌体的制备方法,包括以下步骤:
14.将上述重组表达载体转染人间充质干细胞后,依次进行孵育、过滤和离心,得到外泌体。
15.优选的,所述转染包括将所述重组表达载体与转染试剂和msc混合,所述重组表达载体与转染试剂的质量体积比为(2.0~4.0)μg:(4.0~8.0)μl。
16.本发明提供了上述重组基因或上述重组表达载体或上述外泌体或利用上述制备方法制备得到的外泌体在制备治疗高脂血症和动脉粥样硬化药物中的应用。
17.有益效果:本发明提供了一种双途径拮抗pcsk9的重组基因,所述重组基因从3’端至5’端包括依次连接kozak片段、cd63第一片段(n
‑
cd63)、outer
‑
egf
‑
a基因(epidermal growth factor
‑
like repeat a(egf
‑
a)domain)、cd63第二片段(c
‑
cd63)、inner
‑
egf
‑
a基因和flag基因。本发明所述重组基因具有副作用小、成本低、稳定性高、拮抗效率高、免疫原性低,收率高等优点,而且能够利用egf
‑
a模序竞争性结合psck9以抑制ldlr
‑
pcsk9复合物的形成,使ldlr减少降解、增强循环,进而降低血脂,因此,本发明所述重组基因成为治疗高脂血症及动脉粥样硬化有效手段,具有良好的临床应用前景。
18.而且,本发明所述重组基因中,kozak片段能够增强该重组基因的翻译效率;将两组egf
‑
a片段中的组氨酸突变为酪氨酸以增强表达效率,即cac替换为tac;插入flag便于追踪。cd63第一片段和第二片段是嵌于外泌体膜上的四次跨膜蛋白。
19.另外,本发明所述外泌体内外均携带决定pcsk9和ldlr结合的关键蛋白egfa,内外均表达egf
‑
a的优势在于循环中的外泌体可以通过膜外egf
‑
a结合循环pcsk9让其随外泌体被吞噬降解,进而实现拮抗pcsk9的目的;而且本发明所述外泌体同时具备胞内胞外两条拮抗pcsk9的途径,既能高度特异结合循环pcsk9促进其降解,又能在肝细胞内体促进pcsk9
‑
ldlr复合物解离、加速ldlr再循环,同时具有平台稳定性高、靶向性强、副作用小的优势,更重要的是通过双途径拮抗pcsk9提高了其抑制效率,能够更大程度达到降低ldl
‑
c的效果。
附图说明
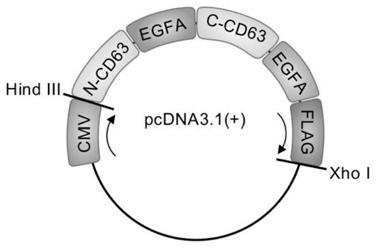
20.图1为重组表达载体构建示意图;
21.图2为外泌体westernblot,对细胞(cell)及外泌体(exo)进行检测,其中ctrl为对照组,ovegf
‑
a为质粒修饰组,flag为flag抗体,gapdh为内参;
22.图3为he染色图,其中pbs为pbs组,exo
ctrl
为对照外泌体组,exo
egf
‑
a
为egfa修饰外泌体组,alirocumab为alirocumab组。
具体实施方式
23.本发明提供了一种双途径拮抗pcsk9的重组基因,从3’端至5’端包括依次连接kozak片段、cd63第一片段、outer
‑
egf
‑
a片段、cd63第二片段、inner
‑
egf
‑
a片段和flag标签。在本发明中,所述kozak片段的核苷酸序列如seq id no.3所示:gccacc,添加kozak片段能够增强该重组基因的翻译效率;所述cd63第一片段(n
‑
cd63)的核苷酸序列如seq id no.4所示:atggcggtggaaggaggaatgaaatgtgtgaagttcttgctctacgtcctcctgctggccttttgcgcctgtgcagtgggactgattgccgtgggtgtcggggcacagcttgtcctgagtcagaccataatccagggggctac
ccctggctctctgttgccagtggtcatcatcgcagtgggtgtcttcctcttcctggtggcttttgtgggctgctgcggggcctgcaaggagaactattgtcttatgatcacgtttgccatctttctgtctcttatcatgttggtggaggtggccgcagccattgctggctatgtgtttagagataaggtgatgtcagagtttaataacaacttccggcagcagatggagaattacccgaaaaacaaccacactgct;所述outer
‑
egf
‑
a片段的核苷酸序列如seq id no.5所示:gggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggcttccagctggtggcccagcgaagatgcgaagatatc;所述cd63第二片段(c
‑
cd63)的核苷酸序列如seq id no.6所示:tcgatcctggacaggatgcaggcagattttaagtgctgtggggctgctaactacacagattgggagaaaatcccttccatgtcgaagaaccgagtccccgactcctgctgcattaatgttactgtgggctgtgggattaatttcaacgagaaggcgatccataaggagggctgtgtggagaagattgggggctggctgaggaaaaatgtgctggtggtagctgcagcagcccttggaattgcttttgtcgaggttttgggaattgtctttgcctgctgcctcgtgaagagtatcagaagtggctacgaggtgatg;所述inner
‑
egf
‑
a片段的核苷酸序列如seq id no.7所示:gggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggcttccagctggtggcccagcgaagatgcgaagatatc,本发明将两组egf
‑
a序列中的的组氨酸突变为酪氨酸以增强表达效率,即cac替换为tac,即下划线部分(序列表中seq id no.5和seq id no.7所示)为突变部分;所述flag标签的核苷酸序列如seq id no.8所示:gattacaaggatgacgacgataag,本发明插入flag便于追踪。
24.在本发明中,所述重组基因的核苷酸序列优选如seq id no.1所示:gccaccatggcggtggaaggaggaatgaaatgtgtgaagttcttgctctacgtcctcctgctggccttttgcgcctgtgcagtgggactgattgccgtgggtgtcggggcacagcttgtcctgagtcagaccataatccagggggctacccctggctctctgttgccagtggtcatcatcgcagtgggtgtcttcctcttcctggtggcttttgtgggctgctgcggggcctgcaaggagaactattgtcttatgatcacgtttgccatctttctgtctcttatcatgttggtggaggtggccgcagccattgctggctatgtgtttagagataaggtgatgtcagagtttaataacaacttccggcagcagatggagaattacccgaaaaacaaccacactgctgggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggcttccagctggtggcccagcgaagatgcgaagatatctcgatcctggacaggatgcaggcagattttaagtgctgtggggctgctaactacacagattgggagaaaatcccttccatgtcgaagaaccgagtccccgactcctgctgcattaatgttactgtgggctgtgggattaatttcaacgagaaggcgatccataaggagggctgtgtggagaagattgggggctggctgaggaaaaatgtgctggtggtagctgcagcagcccttggaattgcttttgtcgaggttttgggaattgtctttgcctgctgcctcgtgaagagtatcagaagtggctacgaggtgatggggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggcttccagctggtggcccagcgaagatgcgaagatatcgattacaaggatgacgacgataag;本发明优选在所述重组基因的3’端还包括酶切位点hindⅲ,5’端还包括酶切位点xhoⅰ;当所述重组基因的3’端包括酶切位点hindⅲ,5’端包括酶切位点xhoⅰ时,所述重组基因的核苷酸序列优选如seq id no.2所示:ggaagcttgccaccatggcggtggaaggaggaatgaaatgtgtgaagttcttgctctacgtcctcctgctggccttttgcgcctgtgcagtgggactgattgccgtgggtgtcggggcacagcttgtcctgagtcagaccataatccagggggctacccctggctctctgttgccagtggtcatcatcgcagtgggtgtcttcctcttcctggtggcttttgtgggctgctgcggggcctgcaaggagaactattgtcttatgatcacgtttgccatctttctgtctcttatcatgttggtggaggtggccgcagccattgctggctatgtgtttagagataaggtgatgtcagagtttaataacaacttccggcagcagatggagaattacccgaaaaacaaccacactgctgggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggct
tccagctggtggcccagcgaagatgcgaagatatctcgatcctggacaggatgcaggcagattttaagtgctgtggggctgctaactacacagattgggagaaaatcccttccatgtcgaagaaccgagtccccgactcctgctgcattaatgttactgtgggctgtgggattaatttcaacgagaaggcgatccataaggagggctgtgtggagaagattgggggctggctgaggaaaaatgtgctggtggtagctgcagcagcccttggaattgcttttgtcgaggttttgggaattgtctttgcctgctgcctcgtgaagagtatcagaagtggctacgaggtgatggggaccaacgaatgcttggacaacaacggcggctgttcctacgtctgcaatgaccttaagatcggctacgagtgcctgtgccccgacggcttccagctggtggcccagcgaagatgcgaagatatcgattacaaggatgacgacgataagtagctcgaggg。
25.本发明提供了一种包括上述重组基因的重组表达载体,所述重组表达载体的基础质粒包括pcdna3.1( )。
26.本发明对所述重组表达载体的构建方法并没有特殊限定,优选利用双酶切的方法将所述重组基因插入pcdna3.1( )载体的hindⅲ和xhoⅰ酶切位点之间。本发明实施例中,所述重组表达载体优选由南京金斯瑞生物科技公司完成。
27.本发明提供了一种双途径拮抗pcsk9的外泌体,外泌体携带跨膜蛋白的基因序列包括上述重组基因或上述重组表达载体。
28.本发明提供了上述外泌体的制备方法,包括以下步骤:
29.将上述重组表达载体转染人间充质干细胞(msc)后,进行孵育,得到外泌体,即为egfa修饰外泌体。
30.在本发明中,所述转染包括将所述重组表达载体与转染试剂和msc混合,所述重组表达载体与转染试剂的质量体积比优选为(2~4)μg:(4~8)μl,更优选为(2.5~3.5)μg:(5~7)μl。
31.在本发明中,所述孵育优选在细胞孵箱中进行;所述孵育的温度优选为37℃;孵育过程中,co2的体积百分含量优选为5%;所述孵育包括第一孵育和第二孵育;所述第一孵化优选在不含双抗培养基(dmem,gibco公司,美国;胎牛血清,gibco公司,美国)的msc培养基中进行;所述第一孵育的时间优选为4~6h,更优选为4.5~5.5h;所述第二孵化优选在无血清的完全培养基(dmem,gibco公司,美国)中进行,所述第二孵育的时间优选为48h。
32.本发明在所述混合后,优选还包括对混合所得混合物进行静置处理;所述静置的时间优选为20min;所述静置的温度优选为37℃。
33.本发明在所述孵育后,优选还包括对孵育所得孵育物进行过滤和离心;所述过滤优选采用0.22μm滤器过滤,能够去除多余的细胞碎片;所述离心的转速的离心力优选为100,000
×
g;所述过滤的时间优选为10h。
34.本发明所述外泌体的制备方法为大规模工程化外泌体的生产提供的新范式。
35.本发明所述外泌体具备胞内胞外两条拮抗pcsk9的途径,既能高度特异结合循环pcsk9促进其降解,又能在肝细胞内体促进pcsk9
‑
ldlr复合物解离、加速ldlr再循环,更重要的是通过双途径拮抗pcsk9提高了其抑制效率,能够更大程度达到降低ldl
‑
c的效果,因此本发明所述外泌体能够用于制备治疗高脂血症和动脉粥样硬化药物。
36.本发明提供了上述重组基因或上述重组表达载体或上述外泌体或利用上述制备方法制备得到的外泌体在制备治疗高脂血症和动脉粥样硬化药物中的应用。本发明所述重组基因、重组表达载体或外泌体膜内外均表达egfa,能够实现pcsk9与ldlr结合的胞内、胞外途径双覆盖,既能高度特异结合循环pcsk9促进其降解,还能在肝细胞内体促进pcsk9
‑
ldlr复合物解离,加速ldlr再循环,可见本发明所述重组基因、重组表达载体或外泌体能够通过双途径达到降低血脂和减缓动脉粥样硬化斑块形成的目的。
37.为了进一步说明本发明,下面结合实施例对本发明提供的一种双途径拮抗pcsk9的重组基因、载体、外泌体及制备方法和应用进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
38.实施例1
39.构建重组表达载体:所述重组表达载体由南京金斯瑞生物科技公司完成;
40.(1)酶切位点选用hindⅲ和xhoⅰ;
41.(2)3’端至5’端由依次连接kozak片段(如seq id no.3所示)、cd63第一片段(如seq id no.4所示)、outer
‑
egf
‑
a片段(如seq id no.5所示)、cd63基因第二片段(如seq id no.6所示)、inner
‑
egf
‑
a片段(如seq id no.7所示)和flag标签(如seq id no.8所示)组成,得到重组基因,核苷酸序列如序列表中seq id no.1所示;
42.(3)将上述重组基因装载pcdna3.1( )载体的hindⅲ和xhoⅰ酶切位点之间,成功将人源化cd63
‑2×
egf
‑
a模序装载到pcdna3.1( )载体上,得到重组表达载体,如图1所示。
43.(4)2~4μg重组表达载体与4~8μl转染试剂混合后,37℃静置20min后缓慢加入不含双抗培养基(dmem,gibco公司,美国;胎牛血清,gibco公司,美国)的msc培养皿中;
44.(5)放于37℃含5%co2的细胞孵箱,4~6h后换为无血清的完全培养基(dmem,gibco公司,美国),48h后收集细胞上清;
45.(6)用0.22μm滤器过滤细胞上清,去除细胞碎片;
46.(7)细胞上清采用100,000
×
g超速离心10h,所得沉淀即为egfa修饰外泌体。
47.(8)同步收集正常msc来源的外泌体,步骤同上,即对照外泌体。
48.实施例2
49.所得外泌体进行westernblot检测flag标签。
50.根据前述外泌体提取方法,对离心后沉淀的外泌体,真空泵吸除残余液体,加入50μl ripa裂解液(碧云天,中国),用移液器吹打至外泌体完全溶解,冰上放置30min,使外泌体蛋白充分裂解。通过倍比稀释法进行蛋白定量(thermo,美国)并进行蛋白样品制备。自行配制12%的凝胶(碧云天,中国),后加入外泌体蛋白样品进行电泳。设置电泳电压90v,30min,开始电泳。当蛋白样品进入下层分离胶后,调节电泳电压至120v,90min。观察蛋白样品位置,当到达预计位置后即可停止电泳,转而进行转膜,设置电流为200ma,时间120min。之后进行抗体孵育。根据抗体说明书,按比例稀释适量抗体,一抗选择flag抗体(sigma,美国),摇床上缓慢摇晃30min后,置于4℃冰箱,过夜孵育。二抗选择山羊抗兔igg hrp(bbi生工,中国),置于暗盒中,室温下在摇床上缓慢摇晃1h。最后进行发光(ecl发光液,ge,美国),以gapdh为内参。
51.结果如图2所示,msc来源外泌体携带人cd63
‑
egf
‑
a模序。
52.实施例3
53.将apoe
‑
/
‑
小鼠(集萃药康公司)随机分为4组进行尾静脉注射,分组情况为pbs组(pbs购自于凯基生物,kgb5001,作对照),对照外泌体组(实施例1提取的对照外泌体),egfa修饰外泌体组(实施例1提取的egfa修饰外泌体)及alirocumab组(pcsk9抑制剂购自于美伦生物,mb2787,作阳性对照)。
54.其中pbs组为:将pbs以每只150μg/200μl的剂量注射到apoe
‑
/
‑
小鼠体内,每周1次持续4周,之后对小鼠主动脉根部进行he染色;
55.对照外泌体组为:将对照外泌体以每只150μg/200μl的剂量注射到apoe
‑
/
‑
小鼠体内,每周1次持续4周,之后对小鼠主动脉根部进行he染色;
56.egfa修饰外泌体组为:将实施例1提取的egfa修饰外泌体以每只150μg/200μl的剂量注射到apoe
‑
/
‑
小鼠体内,每周1次持续4周,之后对小鼠主动脉根部进行he染色;
57.alirocumab组为:将pcsk9抑制剂以每只150μg/200μl的剂量注射到apoe
‑
/
‑
小鼠体内,每周1次持续4周,之后对小鼠主动脉根部进行he染色。
58.结果如图3所示,egfa修饰外泌体组apoe
‑
/
‑
小鼠血管斑块较pbs组及对照外泌体组明显减小,治疗效果与alirocumab组接近,表明该修饰外泌体能够有效抑制动脉粥样硬化斑块的形成。
59.虽然本发明已以较佳的实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可以做各种改动和修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。